Сущность метода. В основе метода определения общей щелочности воды лежит принцип образования нейтральных солей при взаимодействии кислоты с гидратами, гидрокарбонатами и карбонатами щелочных и щелочнозечельных металлов, а также свойство различных индикаторов изменять свой цвет в зависимости от величины рН.
Учитывая эти свойства, исследуемую пробу воды подвергают титрованию раствором соляной или серной кислоты требуемой концентрации в присутствии индикаторов фенолфталеина и метилоранжа.
Применяемые реактивы:
децинормальный (0,1 н.) раствор соляной или серной кислоты;
1%-ный спиртовый раствор фенолфталеина для определения гидратной и карбонатной щелочности;
0,1%-ный раствор метилоранжа, служащий индикатором при определении карбонатной и гидрокарбонатной щелочности.
Подготовка_пробы воды. При титровании воды кислота вступает во взаимодействие как со щелочами, так и с веществами, которые могут находиться в воде во взвешенном состоянии и которые не обусловливают щелочность воды. Чтобы уменьшить расход кислоты на ненужные реакции и обеспечить правильность определения щелочности, анализируемую пробу охлаждают до 20°С, если она была горячей, и пропускают через бумажный фильтр.
Порядок анализа. К 100 мл соответственно подготовленной для титрования пробы воды добавляют 2-3 капли фенолфталеина.
При окрашивании пробу титруют раствором соляной или серной кислоты соответствующей нормальности (0,1 н. или 0,01 н.) до исчезновения окраски. Титрование проводят медленно, тщательно перемешивая пробу воды.
Количество 0,1 н. или 0,01 н. раствора соляной или серной кислоты, пошедшее на титрование с фенолфталеином, записывают с пометкой «фф». Если в процессе прибавления фенолфталеина окрашивания не наступает, значит, в воде отсутствуют гидратная и карбонатная щелочности. В этом случае титровать пробы воды раствором кислоты не нужно, так как щелочность по фенолфталеину отсутствует.
После этого в эту же пробу добавляют 2-3 капли метилоранжа и титруют 0,1 н. или 0,01 н. раствором кислоты до перехода окраски пробы из желтой в оранжевую. Количество раствора кислоты, пошедшее на титрование с метилоранжем, записывают с пометкой «МО».
Для расчета общей щелочности воды берут суммарный расход кислоты, пошедшей на титрование с фенолфталеином и метилоранжем.
Расчет результатов анализа. Расчет результатов анализа основан на том, что каждый 1 мл нормального раствора соляной или серной кислоты оттитровывают 1 мг×экв щелочности. Соответственно этому 1 мл децинорнального (0,1 н.) раствора соляной кислоты оттитровывает 0,1 мг×экв. щелочности, а 1 мл сантинормального (0,01 н.) раствора оттитровывает 0,01 мг×экв щелочности.
Следовательно, общая щелочность воды
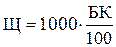
где Щ — общая щелочность воды, мг×экв/кг;
1000 — перерасчет результатов анализа на 1 л воды;
К — коэффициент нормальности раствора кислоты;
Б — суммарный расход кислоты на титрование, мл;
100 -объем пробы воды, взятой для анализа, мл.
При титровании 100 мл пробы воды децинормальным раствором кислоты (0,1 н.) формула упрощается:
При использовании саитинормального раствора кислоты (0,01 н.):
Для воды типа конденсата щелочность принято выражать в микро-грамм эквивалентах на литр (мкг×экв/кг). В этом случае
Щ =Б 0.01 × 1000 × 1000/100
СОСТАВЛЕНИЕ ОТЧЕТА
Для оформления отчета необходимо заполнить табл. 3.
Результаты расчетов
| № | Наименование параметра | По какой формуле определяется | Значение | Размерность |
| Карбонатная жесткость Некарбонатная жесткость Общая жесткость метод титрования метод комплексометрический Окисляемость Общая щелочность Сухой остаток Класс жесткости | табл.2 |
КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Чем обусловлена и в каких единицах измеряется карбонатная жесткость?
2. Чем обусловлена и в каких единицах измеряется некарбонатная жесткость?
3. Что такое общая жесткость?
4. Как определить класс жесткости воды?
5. Почему карбонатная жесткость устраняется при кипячении? Напишите, какие при этом протекают реакции.
6. Как устраняют жесткость воды в промышленных условиях?
7. Как определяют карбонатную жесткость?
8. Как определяют некарбонатную жесткость?
9. Как определяют общую жесткость?
10. Что такое окисляемоеть воды и чем она обусловлена, в каких единицах измеряется?
11. Как определяют окисляемоеть воды?
12. Что такое общая щелочность воды, в каких единицах измеряется?
13. Как определяют щелочность воды?
14. Что такое сухой остаток, в каких единицах измеряется и как определяется?
источник
Объемный (количественный) анализ.Объемный метод количественного анализа основан на точном измерении реагирующих веществ, концентрация одного из которых известна. Растворы с точно установленной концентрацией называются титрованными, т.к. они используются для определения концентрации исследуемых растворов, то их называют рабочими или стандартными. Процесс прибавления стандартного титрованного раствора к раствору исследуемого вещества называется титрованием. Титрование ведется до достижения точки эквивалентности, т.е. до того момента, когда количество прибавленного стандартного раствора будет эквивалентно количеству определяемого вещества согласно уравнению реакции. Необходимое условие объемного анализа – точная фиксация точки эквивалентности, поэтому используют реакции, конец которых характеризуется определенным внешним признаком (изменение окраски, выпадение осадка). Часто для фиксации точки эквивалентности употребляют специальные вещества, изменяющие цвет или другие свойства с изменением концентрации исследуемого иона. Такие вещества называются индикаторами.
Требования к реакциям, применяемым в объемном анализе:
— возможность тем или иным способом фиксировать точку эквивалентности;
— количественное течение реакции до равновесия, характеризующегося соответствующей величиной константы равновесия реакции;
— можно применять только те реакции, которые протекают с достаточной скоростью;
— при титровании не должны протекать побочные реакции, делающие точное вычисление результатов анализа невозможным.
В зависимости от типа реакции, которая протекает при титровании, выделяют методы объемного анализа:
1 Нейтрализация. В основе метода лежит реакция нейтрализации:
Этим методом определяют кислотность, щелочность, карбонатную жесткость воды.
2 Окислительно-восстановительные методы, в основе которых применяют окислительно-восстановительные реакции, в ходе которых исследуемое вещество количественно переводят в окисленную или восстановленную форму.
3 Осаждение. Объемные определения метода основаны на осаждении определенного иона в виде труднорастворимого соединения.
4 Комплексометрия. В методе исследуемый ион связывается водным реактивом в малодиссоциированный комплекс. Метод применяется при определении жесткости воды Mg 2+ , Ca 2+ , иона Fe 3+ .
Измерение объемов. Для точного измерения в объемном анализе используют бюретки, пипетки, мерные колбы.
1 Бюретки служат для титрования и представляют собой цилиндрические трубки с суженным концом, отсчет ведется сверху вниз.
2 Пипетки служат для точного отмеривания каких-либо определенных объемов исследуемого раствора.
3 Мерные колбы служат для разбавления исследуемого раствора до определенного объема.
Щелочность обусловлена присутствием в воде веществ, содержащих гидроксоанион, а также веществ, реагирующих с сильными кислотами (соляной, серной). К таким соединениям относятся:
1 сильные щелочи (KOH, NaOH) и летучие основания (например, NH3×H2O), а также анионы, обуславливающие высокую щелочность в результате гидролиза в водном растворе при рН > 8,4 (СО3 2– , S 2– , PO4 3– , SiO3 2– и др.);
2 слабые основания и анионы летучих и нелетучих слабых кислот (HCO3 – , H2PO4 – , HPO4 2– , CH3COO – , HS – , анионы гуминовых кислот и др.).
Щелочность пробы воды измеряется в моль-экв/л или моль-экв/л и определяется количеством сильной кислоты (обычно используют соляную кислоту с концентрацией 0,05 или 0,1 ммоль-экв/л), израсходованной на нейтрализацию раствора.
При нейтрализации до значений рН = 8,0 – 8,2 в качестве индикатора используют фенолфталеин. Определяемая таким образом величина называется свободной щелочностью. При нейтрализации до значений
рН = 4,2 – 4,5 в качестве индикатора используют метиловый оранжевый. Определяемая данным образом величина называется общей щелочностью. При рН = 4,5 проба воды имеет нулевую щелочность.
Соединения первой группы из приведенных выше определяются по фенолфталеину, второй – по метилоранжу.
Щелочность природных вод в силу их контакта с атмосферным воздухом и известняками обусловлена, главным образом, содержанием в них гидрокарбонатов и карбонатов, которые вносят значительный вклад в минерализацию воды. Соединения первой группы могут содержаться также в сточных и загрязненных поверхностных водах.
Экспериментальная часть
Определение свободной щелочности. В коническую колбу наливают 100 мл исследуемой воды, прибавляют 2 – 3 капли индикатора фенолфталеина и титруют раствором HCl до обесцвечивания раствора. Расчет производят по формуле:
где х – свободная щелочность воды, мг-экв/л;
СH(HCl) – молярная концентрация эквивалента раствора HCl, моль/л;
Определение общей щелочности. В ту же колбу, где проводили титрование, добавляют 2 – 3 капли индикатора метилового оранжевого и продолжают титрование до тех пор, пока окраска индикатора из желтой не перейдет в оранжевую.
Эксперимент повторяют три раза, результаты эксперимента записывают в таблицу 1. Из полученных результатов находят среднее арифметическое значение объема рабочего раствора.
Таблица 1 – Результаты титрования
| № | V (H2О), мл | V (HСl), мл | V (HCl) средн., мл |
| 100,0 |
Перед каждым титрованием заполняют бюретку раствором до нулевого деления шкалы.
Расчет производят по формуле:
где х – общая щелочность воды, мг-экв/л;
СH(HCl) – молярная концентрация эквивалента раствора HCl, моль/л;
V (H2О) – взятый объем воды, мл.
Аналогично щелочности при анализе сточных и технологических вод определяют кислотность воды.
Кислотность воды обусловлена содержанием в воде веществ, реагирующих с гидроксоанионами. К таким соединениям относятся:
1) сильные кислоты: соляная HCl, азотная HNO3, серная H2SO4;
2) слабые кислоты: уксусная CH3COOH; сернистая H2SO3; угольная H2CO3; сероводородная H2S и т.п.;
3) катионы слабых оснований: аммоний NH4 + ; катионы органических аммонийных соединений.
Кислотность пробы воды измеряется в моль-экв/л или моль-экв/л и определяется количеством сильной щелочи (обычно используют растворы КОН или NaOH с концентрацией 0,05 или 0,1 моль/л), израсходованной на нейтрализацию раствора.
Различают свободную и общую кислотность. Свободная кислотность определяется при титровании до значений рН = 4,3 – 4,5 в присутствии в качестве индикатора метилового оранжевого. В этом диапазоне оттитровываются HCl, HNO3, H2SO4, H3PO4.
Общая кислотность определяется при титровании до значений рН = 8,2 – 8,4 в присутствии фенолфталеина в качестве индикатора. В этом диапазоне оттитровываются слабые кислоты – органические, угольная, сероводородная, катионы слабых оснований.
Естественная кислотность обусловлена содержанием слабых органических кислот природного происхождения (например, гуминовых кислот). Загрязнения, придающие воде повышенную кислотность, возникают при кислотных дождях, при попадании в водоемы не прошедших нейтрализацию сточных вод промышленных предприятий и др.
Экспериментальная часть
Определение свободной кислотности. В коническую колбу наливают 100 мл исследуемой воды, прибавляют 2 – 3 капли индикатора метилового оранжевого и титруют раствором щелочи до перехода оранжевой окраски раствора в желтую.
Эксперимент повторяют три раза, результаты эксперимента записывают в таблицу 2. Из полученных результатов находят среднее арифметическое значение объема рабочего раствора.
Таблица 2 – Результаты титрования
| № | V (H2О), мл | V (NaOH), мл | V (NaOH) средн., мл |
| 100,0 |
Расчет проводят по формуле:
где х – свободная кислотность воды, мг-экв/л;
V (NaOH) – объем раствра щелочи, мл;
СH(NaOH) – молярная концентрация эквивалента раствора щелочи, моль/л;
Определение общей кислотности. В коническую колбу наливают 100мл исследуемой воды, прибавляют 2 – 3 капли индикатора фенолфталеина и титруют раствором щелочи появления малиновой окраски индикатора.
Эксперимент повторяют три раза, результаты эксперимента записывают в таблицу 3. Из полученных результатов находят среднее арифметическое значение объема рабочего раствора.
Таблица 3 – Результаты титрования
| № | V (H2О), мл | V (NaOH), мл | V (NaOH) средн., мл |
| 100,0 |
Расчет проводят по формуле:
где х – свободная кислотность воды, мг-экв/л;
V (NaOH) – объем раствора щелочи, мл;
СH(NaOHl) – молярная концентрация эквивалента раствора щелочи, моль/л;
Вопросы для самоконтроля
1 На титрование 100 мл исследуемой воды пошло 20 мл 0,1 н раствора соляной кислоты по метиловому оранжевому. Определите щелочность воды.
2 Вода содержит (мг/л): CaSO4 – 50, Ca(HCO3)2 – 100, Mg(HCO3)2 – 25. Какова величина щелочности.
3 Какова общая щелочность воды, содержащей СО3 2- – 50 мг/л, НСО3 — – 122 мг/л.
4 При определении щелочности воды было израсходовано 0,1 н кислоты на титрование 100 мл пробы с индикатором фенолфталеином 3 мл и дополнительно с индикатором метиловым оранжевым 5 мл. Рассчитайте общую и отдельные виды щелочности воды.
5 Вода имеет жесткость равную 9 мг-экв/л. Постоянная жесткость составляет 60 % от общей жесткости (соли натрия отсутствуют). Какова величина щелочности воды.
6 В 1 л воды содержится 210 мг NaHCO3 и 5,3 мг Na2CO3. Определите общую щелочность воды.
ЛАБОРАТОРНАЯ РАБОТА
Дата добавления: 2016-11-20 ; просмотров: 6912 | Нарушение авторских прав
источник
«Определение общей жесткости воды»
Используемая в паросиловых установкахвода содержит определенное количество растворенных минеральных веществ, суммарная концентрация которых определяет ведущий показатель качества воды общее солесодержание. От количества растворенньтх солей в значительной степени зависят происходящие в парогенераторе процессы накипеобразования и коррозии, избыточное содержание минеральных веществ может явиться и причиной загрязнения пара.
Общее солесодержание характеризуется наличием в воде солей, образованных катионами Са +2 , Мg +2 , Nа + и т д и анионами Сl — , НСО3 — и др. (см таблицу 1), из них соединения Са +2 , Мg +2 , Fе +2 обуславливают такой параметр качества воды, как жесткость. Под действием высокой температуры для солей кальция и магния достигается предел насыщения, что приводит к кристаллизации одних соединений (МgSiОз, Са10(Ро4)6(ОН)2 и др) в массе воды в виде шлама, других (СаSО4, СаSiОз , Мg(ОН)2) непосредственно на поверхности в виде накипи Образующаяся на внутренних поверхностях нагрева котла накипь, имея малый коэффициент теплопроводности, ведет к увеличению расхода топлива, снижает производительность котла и может стать, вследствие образования вздутий и трещин в кипятильных трубках, причиной аварии Следовательно, жесткость является основным критерием пригодности воды для питания паровых котлов.
В практике различают три вида жесткости карбонатную (гидрокарбонат), некарбонатную (хлориды, сульфаты и др), общую жесткость — как сумму карбонатной и некарбонатной (таблица 1)
Измеряют жесткость числом миллимолей эквивалентов жесткости (Са +2 и Мg +2 ) в 1 л воды (ммоль/л) Общую жесткость по анионному составу подразделяют на карбонатную Жк и некарбонатную Жнк. Таким образом, общая жесткость, с одной стороны, равна сумме кальциевой п магниевой жесткости, а с другой сумме карбонатной и некарбонатной, при этом концентрация ионов Са +2 и Мg +2 в воде, эквивалентная содержанию иона НСО — , определяет карбонатную жесткость воды (Жк), а концентрация ионов Са +2 и Мg +2 , эквивалентная анионам (Сl — , SО4 -2 и тд) — некарбонатную (Жнк) (Таблица 1)
Жо = Жнк + Жк
При длительном кипячении воды, обладающей карбонатной жесткостью, в ней появляется осадок СаСОз вследствие разложения гидрокарбоната кальция:
Поэтому карбонатную жесткость называют также временной жесткостью Количественно временную жесткость характеризуют содержанием гидрокарбонатов, удаляющихся из воды при ее кипячении в течение часа Жесткость, оставшаяся после такого кипячения, называется постоянной жесткостью Для снижения жесткости до определенной нормы используются различные методы умягчения воды (электродиализ, обратный осмос, ионный обмен и др) для судовых технологических вод с малым количеством солей (конденсат, дистиллят) жесткость может выражаться в градусах.
Например, французский градус соответствует 10 мг СаСОз в 1 л воды, английский — 1 гран СаСОз (64,79891 мг) в 1 галоне воды (4,54609 л), т е 14,24 мг СаСОз в 1 л воды
Соотношения между единицами солесодержания приведены в таблице №2.
Практически солесодержание определяют солемерами по электропроводности контролируемого потока воды, общую жесткость — с помощью судовых
лабораторий водоконтроля методом титрования воды раствором трилона — Б (комплексона Ш).
Определение общей жесткости основано на способности трилона—Б
НООС-Н2С СН2 -СООН
N-CН2-CН2-N
NаООС — Н2С СН2 – СООNа
— двунатриевой соли этилендиаминтетрауксусной кислоты образовывать с
катионами жесткости хорошо растворимые бесцветные соединения — комплексонаты, которые почти не диссоциируют в водном растворе Реакции комплексообразования могут быть выражены следующими схемами:
где Т- условное обозначение составной части комплекса (лиганды)
Наиболее устойчивые комплексы образуются в щелочной среде при РН = 7,5—10, поэтому при определении общей жесткости исследуемую воду подщелачивают буферной смесью. Титрование проводят в присутствии индикатора хромтемносинего (эриохрома черного), образующего с нонами кальция и магния растворимые комплексные соединения винно-красного цвета по схеме:
Н2R ↔ 2Н+R -2
темно-лиловый синий
Са +2 (Мg +2 ) + R — = Са(Мg)R
синий винно-красный
R- анионы индикатора.
При титровании трилоном — Б комплексы типа СаR. разлагаются, вследствие образования более прочных соединений вида Nа2[СаТ], при этом ноны индикатора переходят в раствор
СаR+ Nа2Н2Т =Nа2[СаТ] +R -2 + 2Н +
винно-красный бесцветный синий
В точке эквивалентности винно-красная окраска раствора изменяется на синюю, в результате появления в растворе анионов индикатора.
Жесткость рассчитывают по закону эквивалентов:
Массы участвующих в реакции веществ пропорциональны молярным массам их эквивалентов
Для реагирующих веществ находящихся в растворе, закон эквивалентов записывается следующим образом.
Сэк(1) * V1 = Сэк(2)*V2
где Сэк(1) и Сэк(2) — молярные концентрации эквивалентов растворов, моль экв/л; V1 и V2
— объемы реагирующих веществ, мл.
Молярная концентрация эквивалентов Сэк (нормальная концентрация) — это отношение количества вещества эквивалентов (моль) к объему раствора (л) Единица измерения нормальной концентрации моль/л (СИ) Раствор, в одном литре которого содержится 1 моль вещества эквивалентов, называют нормальным и обозначают 1 н. Соответственно могут быть 0,1 н, 0,01 н, и т. п. растворы.
Рассчитывают жесткость воды по закону эквивалентов (ммоль/л)
Где V1 — объем анализируемой воды, мл
V2— объем раствора Трилона Б, мл
Сэк(2) — молярная концентрация эквивалентов раствора Трилона Б, моль/л,
1000 — коэффициент перевода моль/л в ммоль/л
ПРАКТИЧЕСКАЯ ЧАСТЬ.
Опыт №1. «Определение жесткости котловой воды с помощью СКЛАВ-1.»
Оборудование и реактивы:
• Судовая лаборатория СКЛАВ,
• перечень необходимых для анализа реактивов, их состав и концентрация приведены в таблице № 10
Порядок выполнения работы:
Анализ проводят методом титрования 100 мл исследуемой котловой воды 0,ОIн раствором трилона-Б в присутствии индикатора хромтемносинего.
С этой целью мензуркой отбирают 100 мл анализируемой воды и переносят в коническую колбу. Туда же добавляют 5 мл аммиачно-буферного раствора и несколько крупинок сухого хромтемносинего. Установив стрелку трехходового крана «трилон», грушей накачивают в бюретку раствор и доводят уровень жидкости до нулевого деления. Анализируемый раствор титруют до перехода окраски в синий цвет, при интенсивном перемешивании. Ввиду скачкообразного изменения окраски раствора строго следят за процессом титрования, добавляя трилон-Б в конце титрования по каплям
Рассчитывают значения общей жесткости воды по формуле
Ж=1000*VТр*СЭКВ(Тр) / VH2O
где Ж — общая жесткость, ммоль/л
VТр -объем трилона-Б, пошедшего на титрование, мл,
СЭКВ(Тр) — молярная концентрация эквивалентов Трилона-Б, равная 0,01 н.
VH2O—объем исследуемой воды, взятой для анализа, мл
Анализ повторяют три раза.
ПРОТОКОЛ ЛАБОРАТОРНОЙ РАБОТЫ
«Определение общей жесткости воды»
1. Анализ проводят с помощью лаборатории_________
2. Исходные данные: а) для анализа взято исследуемой воды________ мл. б) СЭКВ(Тр) =0,01 н. 3. Ход анализа: 4 .В процессе определения получены следующие данные
| № определения | Объем раствора трилона-Б ( VТр , мл) | Общая жесткость ммоль/л | Среднее значение жесткости, ммоль/л |
Опыт 2. «Определениежесткости котловой воды с помощью экспресс лаборатории МАХIСRАD-T фирмы Аmeroid Магinе”
Оборудование и реактивы:
— Экспресс лаборатория МАХIСRАD-T,
— испытательные полоски для измерения жесткости,
— цветовая шкала для установления результатов опыта
Порядок выполнения работы:
Погрузите зеленый конец мягкой испытательной полоски в исследуемую воду, немедленно удалите, встряхните лишнюю воду. Через 15-20 сек. Сравните цвет полоски с цветовой шкалой Приблизительно оцените результат, если полученный цвет оказался между двумя цветовыми позициями.
ПРОТОКОЛ ЛАБОРАТОРНОЙ РАБОТЫ
“Определение жесткости котловой воды”
1. Анализ проводят с помощью лаборатории___
2. Исходные данные:
а) для анализа взято исследуемой воды _____мл.
б) бумага для определения жесткости
в) цветная шкала для снятия результатов.
З. Ход анализа.
4 . В процессе определения получены следующие данные.
5. Выводы по работе.
ЛАБОРАТОРНАЯ РАБОТА №2
«Определение щелочности котловой воды»
В котловой воде для предотвращения накипеобразования и подавлениякоррозионных процессов поддерживается некоторый избыток ионов гидроксила, обусловленный наличием растворенной щелочи и гидролизом солей
Nа2СО3 , Nа2РО4, и др.
Nа2СО3+Н2О ↔NaHСО3+NаОН
СО3 -2 +Н2O ↔HСО3 — +ОН —
Nа3РО4— Н2O↔Nа2НРО4+ NаОН
РO4 -3 +H2О ↔HРO4 -2 +ОН —
Суммарная концентрация находящихся в воде гидроксил , карбонат , фосфат
— ионов (табл 1), выраженная в ммоль/л определяет такой показатель качества воды, как общая щелочность (Що).
В переводе на эквивалентное количество NаОН по формуле ЩЧ = 40 Щ (мг/л), где 40 — значение ммоль/л NаОН, получают щелочное число (ЩЧ) (мг/л).
В зависимости от преимущественного содержания в воде ионов, обуславливающих щелочность, различают гидратную щелочность (Щг в ммоль/л), Щг = [ОН — ], карбонатную щелочность (Щк в ммоль/л), Щк = [СO3 -2 ], бикарбонатную (Щбк ммоль/л), Щбк = [НСО3 — ] .
По своему физическому смыслу бикарбонатная щелочность Щбк соответствует карбонатной жесткости Жк, Щбк = Жк.
При эксплуатации котельной установки щелочное число для котловой воды поддерживается в определенных для данного типа котлов пределах (табл 3). При заниженных значениях щелочности не обеспечивается безнакипный режим работы парогенератора, при завышенных возникает опасность щелочной коррозии, вызывающей интеркристаллитное разрушение металла. Корректируют щелочность по результатам анализа введением в котловую воду щелочей, карбонатов и фосфатов натрия, в зависимости от осуществляемого вводно-химического режима. Аналитическое определение щелочности проводят титрованием исследуемой пробы серной кислотой в присутствии индикаторов фенолфталеина и метилоранжа,
Щелочность по фенолфталеину (гидратная щелочность, РН выше 8,2-8,3) позволяет установить наличие ионов ОН — . Все оксиды, половина карбонатов, из фосфатов, все щелочеобразующие при гидролизе вещества (например, силикаты) включены в фенолфталеиновую (Р) щелочность.
В присутствии метилораижа определяется бикарбонатная щелочность (Щбк).
При условии, когда суммарная концентрация ионов Са2 и М8т2 превышает концентрацию нонов НСО3 — , бикарбонатная щелочность Щбк становится равной жесткости карбонатной Жк, а общая щелочность определяется по сумме щелочности гидратной и карбонатной.
Общая щелочность (РН выше 4,2-4,3). Все гидроксиды, все карбонаты, 2/3фосфатов включены в общую щелочность.
Правильный уровень щелочности гарантирует осаждение солей жесткости фосфатами; нейтрализацию кислого характера среды; пассивацию слоем магнетита; защиту от щелочной межкристаллической коррозии.
ПРАКТИЧЕСКАЯ ЧАСТЬ
Опыт 1 «Определение щелочности котловой воды с помощью лаборатории
СКЛАВ-1»
Оборудование к реактивы:
— Лаборатория СКЛАВ-1,
— серная кислота 0,Iн.
— фенолфталеин,
— метилоранж
Порядок выполнения работы:
Отбирают мензуркой 100 мл исследуемой котловой воды и переносят в коническую колбу, добавляя 2—З капли фенолфталеина, при наличии ионов ОН — вода окрасится в малиновый цвет. Установив стрелку трехходового крана на кислоту, грушей накачивают раствор в бюретку до нулевого деления. Затем осторожно, по каплям при перемешивании титруют анализируемый раствор серной кислотой до исчезновения окраски.
Отмечают объем кислоты, пошедшей на титрование V1. После этого вводят в исследуемый раствор 2—З капли метилоранжа, титруют кислотой до перехода окраски от желто-соломенного к оранжевой и фиксируют общий объем израсходованной серной кислоты V1. Анализ повторяют три раза.
Рассчитывают гидратную щелочность, карбонатную жесткость и общую щелочность на основании правила пропорциональности (см. расчет жесткости):
VH2O= 100 мл.
Щон = V1 ммоль/л
Жк = V2 — V1 ммоль/л
Щ= V2 ммоль/л
Щелочность котловой воды выражают также щелочным числом.
Щелочное число (мг/л) рассчитывают по общей щелочности в ммоль/л и умноженной на 40; для подсчета ЩЧ можно воспользоваться таблицей.
ПОДСЧЕТ ЩЕЛОЧНОГО ЧИСЛА ПО РЕЗУЛЬТАТАМ
ТИТРОВАНИЯ (ОБЪЕМ ПРОБЫ ТИТРУЕМОЙ ВОДЫ 1ОО мл)
| Целые числа мл титрованной кислоты | Десятичные доли миллиметров | ||||||||
| 0.0 | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 |
ПРОТОКОЛ ЛАБОРАТОРНОЙ РАБОТЫ
«Определение щелочности котловой воды»
1. Анализ проводят с помощью лаборатории______
2. Исходные данные
а) для анализа взято исследуемой воды _____мл
б) СЭКВ(H2SO4) =0.1 н.
З. Ход анализа:
4. В процессе определения получены следующие данные
| № определения | Объем кислоты мл, пошедшей на титрование в присутствии индикаторов | Значение щелочности в ммоль/л | Среднее значение общей щелочности | Среднее значение щелочного числа мг/л | |
| Фенол-фталеин | Метил-оранжа | Фенол-фталеин+Метил-оранж | Гидрат-ной | Карбон-атной | общей |
Опыт №2. «Определение щелочности котловой воды с помощью лаборатории SРЕСТRАРАС 311 фирмы UNITOR»
Оборудование и реактивы.
• Лаборатория SРЕСТRАРАС 311,
• таблетки для определения Ф Щелочности,
• таблетки для определения М Щелочности (Т —total общая щелочность)
Порядок выполнения работы:
С начало проводится испытание на Ф Щелочность.
Отбирают 200 мл исследуемой котловой воды в бутылку с красной притертой пробкой. Опускают одну таблетку для определения Ф Щелочности, взбалтывают до полного растворения, если щелочность присутствует, то проба станет голубого цвета. Затем добавляют таблетки по одной (давая время таблетке растворится) до тех пор пока голубой цвет не изменится на устойчивый желтый.
Подсчитывают количество используемых таблеток и делают следующий расчет Ф Щелочность ррm (СаСО3)= (количество таблеток * 20)- 10
Например: 12 таблеток израсходовано для получения устойчивого желтого цвета. Результаты (12*20)-10 = 230 ррm СаСО3
Далее продолжают испытание на М Щелочность.
К пробе с Ф Щелочностью добавляют одну таблетку для определения М Щелочности, взбалтывают до растворения. Продолжают добавлять таблетки по одной (давая время таблетке раствориться) до тех пор, пока образец не станет устойчиво красно-розового цвета.
Подсчитывают количество использованных таблеток и проводят следующий расчет М щелочность или Т щелочность ррm СаСО3 = (количество Ф и М таблеток *20) — 10 Например: Если использовано 12 Ф и 5 М таблеток, то
М(Т) щелочность ((12 + 5)*20) — 10 = 330 ррm СаСО3
ПРОТОКОЛ ЛАБОРАТОРНОЙ РАБОТЫ
«Определение щелочности котловой воды»
1. Анализ проводят с помощью лаборатории ___________________
2. Исходные данные
а) для анализа взято исследуемой котловой воды_________ мл
З. Ход работы:
4. В процессе определения получены следующие данные
| Количество Ф таблеток, используемых в ходе работы | Количество М таблеток, используемых в ходе работы | Значение Ф щелочности | Значение М щелочности |
5. Выводы по работе
Примечание: М щелочность по Метилоранжу равна Т щелочности — Total или общая Щелочность.
ЛАБОРАТОРНАЯ РАБОТА №3
«Определение содержания хлоридов»
Растворенные в воде хлориды натрия NаСI, кальция СаСI2 магния МgСl2 являются важнейшим параметром качества используемой в парогенераторе воды (таблица 3) Известно, что СГ — ионы, разрушают на внутренних поверхностях котлоагрегата коррозионно-устойчивую окисную пленку и активизируют коррозионных процессы. являясь деполяризаторами электрохимической коррозии. В этой связи установлены нормы на допустимое содержание хлоридов в конденсате, дистилляте и котловой воде (таблица 3). Источником увеличения хлоридов в котловой воде является добавочная вода, в конденсат хлориды поступают через неплотности в соединениях конденсатора, охлаждаемого забортной морской водой. Вследствие того, что соотношение между содержанием хлор-ионов и солей в морской воде является примерно постоянным, контроль по хлоридам позволяет оценить общее засоление конденсата морской водой при нарушении герметичности конденсатора В случае, если содержание хлоридов в котловой воде превышает допустимые нормы, производится продувание котла, при этом частично удаляемая вода компенсируется питательной. Количество хлоридов оценивается по содержанию в воде нона С1 — в мг/л, хлорида натрия NаСI в мг/л или в градусах Брандта.
Для пересчета одних единиц изменения в другие можно воспользоваться соотношением:
1 0 Бр= 10 мг/л NаСl=6.06 мг/л или таблицами. Контроль за содержанием хлоридов осуществляется методами титрования и калориметрирования.
ПРАКТИЧЕСКАЯ ЧАСТЬ
Опыт №1. “Определение содержания хлоридов в котловой воде с помощью
лаборатории СКЛАВ-1”
Оборудование и реактивы:
• Лаборатория СКЛАВ-1,
° азотнокислое серебро AgNО3
• фенолфталеин, серная кислота,
• хромовокислыи калий К2СгО4,
• дистиллят.
Порядок вьтолнення работы:
Определение основано на реакции хлоридов с азотнокислотным серебром в присутствии индикатора (10% раствор хромата калия К2СгО4):
NaCl + AgNО3= АgCl↓ +NaNО3
После полного осаждения хлор-иона в виде хлорида серебра, нитрат серебра вступает в реакцию с индикатором, в результате образуется осадок кирпично-красного цвета по реакции.
К2СгО4+ 2AgNО3 = Аg2СгО4— 2 КNО3
желтый кирпично-красный
Из отобранной пробы котловой воды берут 100 мл, прибавляют 2—З капли фенолфталеина, которым окрашивают воду. Вмалиновый цвет, затем по каплям добавляют 0,1 н. серную кислоту до обесцвечивания пробы (что указывает на нейтрализацию воды).После этого к этой же пробе добавляют 10 капель раствора хромовокислого калия, хорошо размешивают и из бюретки осторожно по каплям приливают в колбу для титрования раствор азотнокислого серебра, все время интенсивно помешивания воду. Добавку раствора азотнокислого серебра ведут до тех пор, пока в воде не появится бурый оттенок Содержание хлоридов в воде в мл/хлор—ионов на литр воды численно равно количеству мл раствора азотно-кислого серебра, пошедшего на титрование 100 мл пробы; умноженному на 10
Примечание: Содержание хлоридов в котловой воде можно проверить в нейтрализованной воде после определения щелочного числа.
б)для дизельных судов.
Из отобранной пробы котловой водымерной пробиркой берут 10 мл и переливают в колбу для титрования, в которую затем добавляют 40 мл конденсата или дистиллята (для облегчения титрования в большом объеме воды). Разбавленную пробу котловой воды нейтрализуют. для этого сначала к ней прибавляют 2—З капли фенолфталеина, которые окрашивают воду в малиновый цвет, затем по каплям добавляют 0,1 н. серную кислоту до обесцвечивания пробы (что указывает на нейтрализацию воды). После этого к этой же пробе воды добавляют 10 капель раствора хромовокислого калия, хорошо размешивают и из бюретки (осторожно, по каплям), приливают в колбу раствор азотнокислого серебра, все время аккуратно перемешивая. добавку раствора азотнокислого серебра ведут до тех пор, пока не появится бурый опенок.
Содержание хлоридов в воде (в миллиграммах хлориона в 1 л воды) численно равно количеству миллилитров раствора азотнокислого серебра, пошедшего на титрование 10 мл пробы; умноженному на 100).
ПРОТОКОЛ ЛАБОРАТОРНОЙ РАБОТЫ
«Определение содержания хлоридов методом титрования»
1. Анализ проводят с помощью лаборатории_________
2. Исходные данные:
а) для анализа взято исследуемой воды________ мл. (конденсата котловой воды)
б) нормальность раствора (AgNО3) ________
З. Ход анализа:
4. В процессе определения получены следующие данные:
| № определения | Объем AgNО3пошедший на титрование | Содержание в мг/л Cl — | Содержание в мг/ г NaCl | Количество хлоридов в градусах Брандта |
Опыт №2. «Определение содержания хлоридов в котловой воде с помощью лаборатории DREW Ameroid Marine Chloride ZMP.”
— Экспресс лаборатория DREW Ameroid Marine Chloride ZMP,
— индикатор фенолфталеин, серная кислота,
— индикатор хромовокислый
—нитрат серебра
Порядок выполнения работы:
В стеклянную трубку — пробирку наливают 2 мл исследуемой котловой воды, добавляют З капли фенолфталеина Окраска образца в розовый цвет говорит о присутствии щелочности Затем нейтрализуем анализируемую воду добавляя серную кислоту по каплям, пока не исчезнет розовая окраска. Вводят в раствор 6 капель. Хромокислого калия, образец пожелтеет. Добавляют нитрат серебра по каплям, пока образец не станет оранжевым (капли считают) Производят расчеты:
капли нитрат серебра x 50 = ppm хлорида
Например 4 капли серебряного нитрата израсходовалось для достижения оранжевой окраски4x 50= 200 ppm Хлоридов
ПРОТОКОЛ ЛАБОРАТОРНОЙ РАБОТЫ
“Определение содержания хлоридов”
1.Анализ проводится с помощью лаборатории _________
2. Исходные данные
а) для анализа взято исследуемой воды______ мл
3. Ход анализа:
4. В процессе определения получены следующие данные
| Число капель серебряного нитрата | Содержание хлоридов (ppm) |
Опыт №3 “Определение содержания хлоридов в котловой воде с помощью экспресс лаборатории HACH chloride 7p.”
Оборудование и реактивы:
• экспресс лаборатория HACH chloride 7p,
• пластиковые подушечки индикатора chloride 2,
• нитрат серебра,
• дистилированая вода
Порядок выполнения работы
Пластмассовую мензурку наполняют исследуемой котловой водой и переносят образец в специальную бутылочку Прибавляют дистилированую воду до объема 15 мл. С помощью ножниц вскрывают подушечку с индикатором, пересыпают в бутылочку о разбавленной котловой водой и тщательно перемешивают. Исследуемая вода желтеет. Затем по капле добавляют раствор нитрата серебра, бутылочку с пробой постоянно, считая капли, пока испытуемый раствор не изменит цвет с желтого на красно-коричневый (одна пипетка, заполненная до отметки, 1,0 мл равна 15 каплям)
Производят расчет каплих x 30 содержание хлоридов (ррm)
Например: для достижения красно-коричневой окраски, использовано 4 капли нитрат серебра 4 х 30=120 ррm Cl или 4 х 50=200 ррm NaСl
Содержание хлоридов равно 120 ррm Сl или 200 ррm NаСI.
ПРОТОКОЛ ЛАБОРАТОРИЙ РАБОТЫ
“Определение содержания хлоридов”
1. Анализ проводят с помощью лаборатории _______
2. Исходные данные
а) для анализа взято исследуемой котловой воды__________ мл
3. Ход работы
4. В процессе определения получены следующие данные
| Количество капель нитрата серебра | Содержание хлоридов |
| ррm Cl | ррm NаСI |
ЛАБОРАТОРНАЯ РАБОТА 4
«Определение фосфатного числа»
Основным реагентом внутрикотловой химической обработки воды — фосфатнонитратным, фосфатно-щелочным, фосфатно-коррекционным методами является Nа3Р04 тринатрий фосфат. Функциональное назначение фосфат-нона РО3заключается в связывании ионов жесткости и переводе их в малорастворимые соединения. Последние удаляются из котла периодическими продувками и, таким образом, поддерживается безнакипный режим работы котла. Не исключена для РО4 -3 нона и функция пассивирующего агента, что препятствует протеканию коррозии котлового оборудования.
Реакция взаимодействия кальциевых солей с тринатрийфосфатом идет следующим образом
б Nа3РO4+ 10Са СОз +2NаОН →Са10(Р04)6 (ОН) 2 + 10 NаСО3
где Са10(Р04)6 (ОН) 2 — гидроксилапатит, который представляет собой легкоподвижный шлам, практически нерастворимый в воде. Реакция идет только в сильной щелочной среде при РН>9,0. В нейтральной и кислой средах реакция идет в сторону образования фосфатной накипи
2 Nа3РO4 + 3 СаСО3 → Са3(РО4)2 + 3Nа2СО3
Таким образом, для обеспечения безнакипного режима в соответствии с нормами качества котловой воды (табл 1) следует поддерживать избыток фосфат-ионов и щелочности.
Но при высокой щелочности котловой воды (РН >10) магниевая жесткость выделяется из воды в виде гидроокисного шлама, образующего вторичные накипи
МgСО + 2NаОН→Мg(ОН)2 + Nа2СОз
Водные растворы тринатрийфосфата имеют щелочную реакцию
Nа3РO4+ Н2О →Nа2HРО4 +NаОН
Однако степень гидролиза Nа3РO4сильно зависит от температуры. При давлении в котле менее 1,6 МПа степень гидролиза невысока и в котловую воду следует вводить дополнительную щелочь в виде соды Nа2СОз
Nа2СО3 + Н2О →NаНСО3 + NаОН
При давлениях более 1,6 МПа гидролиз тринатрийфосфата обеспечивает щелочную среду, достаточную для перевода ионов Са +2 в пилам. Поэтому при давлениях более 1,6 МПа соду в котлы вводить не следует и при наличии солей жесткости в питательной воде требуется защита металла от щелочной коррозии.
На судах отечественной постройки для котлов всех типов с давлением от 1,6 МПа до 6,0 МПа рекомендуется фосфатно-нитратный режим.
При давлениях более 6,0 МПа обработку котловой воды следует вести без образования избыточной щелочности. Такой водный режим называется фосфатнокоррекционным и суть его заключается в том, что для предотвращения накипеобразования в котлы вместе с Nа3РO4вводят кислый Nа2HРО4.При этом нормированной щелочности котловой воды добиваются комбинацией относительных масс вышеназванных фосфатных солей
Nа3РO4+ Н2О ↔ Nа3HРО4 + NаОН
При осуществлении фофатно-коррекционного водного режима котлов фосфатное число котловой воды (Ф Ч) и щелочное число по индикатору фенолфталеину (Щ Ч) должны находиться в соотношении: Щ. Ч. = 0,42Ф. Ч.
Фосфатный режим, при котором соблюдается это соотношение, называется также режимом чистофосфатной щелочности.
0,42 — коэффициент, равный отношению молярных масс NаОН / РО4 -3 = 40/90=0,42.
Это соотношение исключает наличие свободной щелочи, т е предупреждает появление межкристаллической коррозии и обеспечивает безнакипный режим котлов.
Практически приемлемым для осуществления режима чистофосфатной щелочности является соотношение 9 6 (28.5 Ж П.В. +φ[РО4 -3 ] К.В. ) кг /сутки,
где Д— паропроизводительность котла, кг/час
С = 0,25— концентрация иона РО3в техническом тринатрийфосфате;
Ж П.В. — жесткость питательной воды, ммоль/л;
φ — коэффициент продувки котла,
[РО4 -3 ] К.В — нормированная концентрация фосфат-иона в котловой воде, мг/л,
которую определяют по формам качества котловой воды (таблица З).
Следует отметить, что значительный избыток фосфатов совместно с окислыми соединениями железа и меди вызывает появление железо—фосфатных накипей, способствующих развитию подшламовой коррозии.
Содержание фосфатов — фосфатное число (Ф Ч) оценивается либо количеством РО4 -3 иона в мг./л, либо оксидом Р2О5мг/л
Пересчет этих форм произведен в таблицах 8,9.
ПРАКТИЧЕСКАЯ ЧАСТЬ
Опыт№1. « Определениефосфатов в котловой воде с помощью экспресс-лаборатории
СКЛАВ-1”
Оборудование и реактивы:
• Лаборатория СКЛАВ-1.
• реактив на фосфаты,
• кювета;
• компаратор,
• сульфомолибденовый раствор, см .табл.
Порядок выполнения работы:
Определение содержания фосфатов в котловой воде основано на образовании растворимого соединения состава Р2О5 *V2О5* MоО3 * nН2О,окрашенного в интенсивно желтый цвет. Содержание фосфатов измеряется в компараторе путем сравнения окрасок испытуемой’ пробы и эталонных пленок. Набор эталонных пленок имеет окраску, соответствующую 10, 20 ЗО и 40 мг/л ионов фосфатов.
Отмерив в две градуированные пробирки по 10 мл котловой воды, добавляют по 2 мл реактива на фосфаты в каждую и содержимое пробирки тщательно перемешивают.
Через 10 минут раствор переливают поочередно в кювету 5, вставляют ее в паз компаратора 4, а в левом пазу последовательно поднимают стандартные пленки желтого цвета до тех пор, пока окраска их не сравняется с окраской испытуемой пробы. Если цвет пробы гуще цвета пленки, соответствующей содержанию РО? = 5Омг / л, пробу разбавляют в 2—4 раза, соответственно увеличив и результат анализаю Анализ повторяют три раза
ПРОТОКОЛ ЛАБОРАТОРНОЙ РАБОТЫ
«Определение фосфатногочисла”
1. Анализ проводят с помощью лаборатории _______
2. Исходные данные
а) для анализа взято исследуемой воды__________ мл
3. Ход анализа:
4. В процессе определения получены следующие данные
| № определения | Содержания фосфатов, мг/л | Среднее значение фосфатного числа |
| 1. |
Опыт № 2: “Определение фосфатов в котловой воде с помощью экспресс лаборатории Spectrapak 311 фирмы UNIOR”
Оборудование и реактивы:
· Экспресс лаборатория Spectrapak 311;
· таблетка для определения фосфатов,
· диск с цветными пленками для определения фосфатов;
· цилиндрические пробирки (10мл) с крышками.
Порядок выполнения работы:
Диск с цветными эталонными пленками для определения фосфатов вставляют в компаратор Набор пленок имеет окраску, соответствующую 10; 20; 30; 40 и т.д. 100 ppm фосфатов. Заполняют исследуемой котловой водой две пробирки до отметки 10 мл . Одну пробирку вставляют в левое отделение компаратора В другую опускают одну таблетку для определения фосфатов, взбалтывают и перемешивают до полного растворения Через 10 мин помещают пробирку в правое отделение компаратора Направляют компаратор на свет и вращают диск до совпадения цвета. Записывают результат.
ПРОТОКОЛ ЛАБОРАТОРНОЙ РАБОТЫ
«Определение фосфатов в котловой воде»
1. Анализ проводят с помощью лаборатории
2. Исходные данные
а) для анализа взято исследуемой воды мл
З. Ход анализа.
4. В процессе определения получены следующие данные
5. Выводы по работе
источник
Лекция №3. Показатели, необходимые для характеристики качества воды, определяются характером использования воды различными потребителями
Показатели, необходимые для характеристики качества воды, определяются характером использования воды различными потребителями. Например, качество воды хозяйственно-питьевого назначения характеризуют с помощью показателей, не применяемых во внимание при использовании воды на ТЭС и АЭС. Здесь рассмотрим основные показатели, используемые при анализе природных вод, применяемых в теплоэнергетике как исходное сырьё.
Минеральные примеси различных природных вод по количественному составу примерно постоянны и отличаются лишь концентрациями, установление которых и входит в задачу анализа природных вод. Важнейшие показатели качества воды, определяющие применимость для паротурбинных установок и метод её обработки – концентрация грубодисперсных примесей (взвешенные вещества), концентрация ионов Ca 2+ , Mg 2+ , Fe 2+ , , , , , , , , рН воды, удельная электропроводимость, технологические показатели (сухой прокаленный остаток, щелочность, жесткость, кремнесодержание, окисляемость), концентрация растворённых газов и .
Содержание грубодисперсных (взвешенных) веществ выражают в (мг/кг) и определяют фильтрованием 1 л пробы воды через бумажный фильтр, который затем высушивают при температуре 105-110 0 С до постоянной массы
Прозрачность воды определяют с помощью методов шрифта и креста. Для первого способа применяют градуированный на сантиметры стеклянный цилиндр высотой 30 см, под дно которого подложен определённый шрифт. Столб воды в сантиметрах, через который ещё можно прочесть текст, и определяет прозрачность воды. Прозрачность по кресту определяют по той же методике, используя трубку длиной 350 см, диаметром 3,0 см, на дно которой помещают бумажный круг с крестом, имеющим ширину линий в 1 мм.
Мутность воды пропорциональна содержанию в ней взвешенных частиц, определяют, сравнивая анализируемую пробу с определенным эталоном мутности.
Удельная электропроводность растворов χ, характеризуемая электро-проводностью 1 см 3 жидкости с размером граней 1 см и выражаемая в См/см, является важным показателем качества природной и обрабатываемой воды, указывающим на суммарную концентрацию ионгенных примесей. Удельная электропроводность воды, не содержащей примесей, при 25 0 С составляет 0,063 мкСм/см и определяется переносом в электрическом поле только ионов H + и . При постоянной температуре и данной степени диссоциации существует прямая зависимость между концентрацией электролита и его удельной электропроводностью. Так удельную электропроводность водных растворов различных солей концентрацией 500 мк/кг в условном пересчете на NaCl можно оценить из соотношения
1 мкСм/см↨≈ 0,5 мг NaCl/кг H2O.
Сухой остаток (СО) (мг/л) определяют путем выпаривания определенного объёма предварительно профильтрованной пробы и последующего просушивания остатка при температуре 110-120 0 С.
Сухой остаток выражает содержание растворенных в воде минеральных и органических примесей, нелетучих при указанной температуре. Содержащиеся в природной воде Ca(HCO3)2 и Mg(HCO3)2 при выпаривании разлагаются с выделением H2O и CO2 и в сухом остатке появляются CaCO3 и MgCO3; это надо иметь в виду, сравнивая сухой остаток с минеральным.
Минеральный остаток (мг/л) (общее солесодержание) подсчитывается путем суммирования концентраций катионов и анионов, определенных при проведении полного химического анализа воды.
Прокаленный остаток (мг/л) характеризует содержание в воде минеральных веществ; его определяют путем прокаливания при 800 0 С сухого остатка. При прокаливании сгорают органические вещества и частично разлагаются карбонаты.
Окисляемость воды – это показатель, имеющий условное значение и представляющий собой расход какого-либо сильного окислителя, необходимого для окисления в определённых условиях органических примесей, которые содержатся в 1 л воды. Обычно для этих целей применяют перманганат калия ( ) или бихромат калия ( ), различают соответственно перманганатную и бихроматную окисляемость. Окисляемость воды выражают в кислородных или перманганатных единицах (мгO2/кг, мг /кг), различающихся в 3,95 раза. Бихроматная окисляемость обычно превышает в 2-2,5 раза перманганатную, а разность между ними позволяет судить об устойчивости органических примесей к действию окислителей. При определении окисляемости обоих видов происходит окисление не только содержащихся в воде органических веществ, но и некоторых неорганических, например закисного железа, сероводорода, нитритов. Поэтому следует еще раз подчеркнуть, что окисляемость характеризует содержание в воде органических веществ лишь приближенно и условно.
Окисляемость чистых грунтовых вод составляет обычно 1-3 мгO2/л, в то время как в водах поверхностных источников окисляемость повышается до 10-12 мгO2/л. Реки болотного происхождения и поверхностные источники в период паводка отличаются очень высокой окисляемостью, превышающей, например, 30 мгO2/л. Сточные воды, содержащие органические вещества и сбрасываемые в водоемы, могут повышать окисляемость воды различных источников.
Для суммарной оценки органических загрязнений воды в последнее время начинают применять метод сорбции из воды органических веществ активированным углем с последующим его высушиванием и экстракцией из него этих веществ хлороформом (метод угольно-хлороформного экстракта). В массовых единицах (мг/кг) оценивают в ряде случаев содержание общего органического углерода в воде.
Жесткость воды – один из важнейших показателей её качества. Общей жесткостью называют суммарную концентрацию ионов кальция и магния, выраженную в единицах микрограмм-эквивалент (мг-экв/л) на 1 л воды.
= +
Общую жесткость воды подразделяют на кальцевую и магниевую. Кальциевая жесткость определяется катионами кальция Ca 2+ (мг-экв/л). Магнивая жесткость определяется катионами магния Mg 2+ (мг-экв/л). Часть (в предельном случае при Що > вся жесткость), эквивалентная содержанию бикарбонатов, называется карбонатной жесткостью; разность между общей и карбонатной жесткостями называется некарбонатной жесткостью.
Общая жесткость подразделяется на карбонатную Жк и некарбонатную Жн.к. Карбонатная жесткость обусловливается наличием в воде бикарбонатов и карбонатов кальция и магния, некарбонатная жесткость – присутствием в воде хлоридов, нитратов, сульфатов кальция и магния (мг-экв/л).
Процесс выделения из воды ионов Ca 2+ и Mg 2+ получил название умягчение воды. Воды с высокой жесткостью дают плотные отложения на теплопередающих поверхностях.
По значению общей жесткости природных вод установлена следующая класссификация: 12 мг-экв/кг – очень высокая жесткость.
Общая щелочность воды Що – суммарная концентрация в воде растворимых гидрооксидов и анионов слабых кислот за вычетом концентрации ионов водорода.
= + — , мг/экв/л,
= + + + + + +
+ .
Общую щелочность Що выражают в миллиграмм − эквивалентах на 1 л. Её определяют титрованием пробы воды кислотой в присутствии индикаторов: фенолфталеина и метилоранжа. Для вод, в которых может содержаться гидратная форм щелочности ( ), карбонатная ( ) или бикарбонатная ( ), вычисление отдельных форм (слагаемых) общей щелочности определяют по таблице в зависимости от результатов титрования пробы с фенолфталеином – и метилоранжем – .
Вычисление форм щелочности природной воды
| Соотношение Щфф | Гидраты Щг | Карбонаты Щк | Бикарбонаты Щб |
| Щфф = Щмо | Щфф; Щмо | Нет | Нет |
| Щфф > 0,5 Щмо | 2Щфф-Щмо | 2(Щмо-Щфф) | Нет |
| Щфф = 0,5 Щмо | Нет | Щмо; 2Щфф | Нет |
| Щфф 0 | Нет | Нет | Щмо |
Природные воды в своем большинстве характеризуются бикарбонатной формой щелочности, которая численно близка к величине общей щелочности (Що
В природных исходных водах соотношение между щелочностью и общей жесткостью могут быть различными, соответственно вычисляются значения карбонатной жесткости таблица:
| Щелочность исходной воды | Карбонатная жесткость исходной воды |
| Щи.в | Щи.в − Жк = ; Щи.в − = [NaHCO3] |
Ионный состав воды. Вода всегда электрически нейтральна, поэтому сумма концентраций содержащихся в ней катионов равна сумме концентраций анионов при условии, что они выражены в мг-экв/л: åск=åса.
Этой закономерностью, называемой уравнением электронейтральности раствора, пользуются при проверке правильности выполнения анализа воды. В водах энергетических объектов могут присутствовать ионы, приведенные в таблице
| Катионы | Анионы |
| Водород | Гидроксильный |
| Натрий | Бикарбонатный |
| Калий | Карбонатный |
| Аммоний | Нитритный |
| Кальций | Нитратный |
| Магний | Хлоридный |
| Железо двухвалентное | Фторидный |
| Железо трехвалентное | Сульфатный |
| Алюминий | Силикатный |
| Медь | Ортофосфатный |
| Гидросульфатный |
В природных водах обычно содержится катионы , , , и анионы , , , , реже , и , , .
Ионы натрия и калия с анионами природных вод не образуют труднорастворимых простых солей, практически не подвергаются гидролизу, поэтому их относят к группе устойчивых примесей. Концентрация ионов натрия и калия изменяется только в результате испарения или разбавления природной воды, при анализе воды ее часто выражают суммарно.
Ионы кальция и магния относятся к числу важнейших примесей воды и во многом определяют возможность ее использования для различных народнохозяйственных целей, так как эти ионы образуют труднорастворимые соединения с некоторыми находящимися в воде анионами. При использовании природной воды и связанном с этим изменении исходных концентраций катионов и анионов, например при упаривании или снижении растворимости с ростом температуры, происходит выделение труднорастворимых солей кальция и магния на теплопередающих поверхностях в виде твердой фазы.
Ионы железа характеризуются поливалентностью и могут находиться в различных формах: Fe 2+ и Fe 3+ . Во всех природных водах с высоким рН ионы Fe 3+ практически не могут содержаться и все соединения Fe 3+ находятся коллоидной или грубодисперсной форме. В подземных водах железо обычно находится в ионной форме в виде двухвалентного железа, стехиметрически отвечающего формуле соединения , которое при условии удаления растворенной углекислоты (выдерживание в открытом сосуде) легко гидролизуется, а при наличии в воде растворенного кислорода окисляется с образованием краснокоричневой твердой фазы гидроксида железа Fe(OH)3:
В водах поверхностных источников железо может входить также в состав органических соединений; присутствие в воде соединений железа в повышенных концентрациях создает условия для развития железобактерий, образующих бугристые колонии на стенках трубопроводов.
Концентрация железа в исходной воде может увеличиваться в процессе загрязнения продуктами коррозии.
Не нашли то, что искали? Воспользуйтесь поиском:
источник