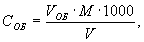Настоящий документ устанавливает методику выполнения измерений общей и свободной щелочности в пробах питьевой и природной воды титриметрическим методом в диапазоне измерений от 0,2 до 20 ммоль/дм 3 .
Методика выполнения измерений обеспечивает с вероятностью Р = 0,95 получение результатов анализа с погрешностью, не превышающей значения, приведенного в таблице 1.
Характеристика погрешности (границы интервала, в котором погрешность находится с доверительной вероятностью Р = 0,95), ± δ, %
Общая щелочность вод обусловлена присутствием в воде гидроксильных ионов и анионов слабых кислот (преимущественно гидрокарбонатов и карбонатов). Щелочность определяется количеством сильной кислоты, необходимой для замещения этих ионов.
В обычных природных водах щелочность зависит в основном от присутствия гидрокарбонатов щелочноземельных металлов, в меньшей степени щелочных. В этом случае значение рН воды не превышает 8,3. Растворимые карбонаты и гидроксиды повышают значение рН (более 8,3). Та часть общей щелочности, которая соответствует количеству кислоты, требуемому для понижения рН до 8,3, называется свободной щелочностью (или щелочностью по фенолфталеину). Титрованием пробы воды до рН 4,5 определяют в пробе общую щелочность. При рН воды меньше 4,5 ее щелочность равна нулю.
Конечную точку при титровании определяют визуально с использованием индикаторов или электрометрически. Электрометрическое определение предпочтительно при анализе загрязненных или окрашенных вод, а также вод, содержащих свободный хлор, обесцвечивающий индикатор.
4.1 Весы лабораторные общего назначения по ГОСТ 24104-88, 2 класса точности с наибольшим пределом взвешивания 200 г.
4.2 рН-метр по ГОСТ 27987-88, с погрешностью измерения ± 0,1 рН.
4.3 Стандарт-титры (фиксаналы) для приготовления образцовых буферных растворов 2-ого разряда по ГОСТ 8.135-74 или ГСО рН водных сред.
4.4 Колбы мерные по ГОСТ 1770-74, номинальной вместимостью 200, 250, 1000 см 3 .
4.5 Цилиндр мерный по ГОСТ 1770-74, номинальной вместимостью 100 см 3 .
4.6 Пипетки мерные по ГОСТ 29227-91, номинальной вместимостью 25 см 3 .
4.7 Бюретка по ГОСТ 29251-91, номинальной вместимостью 5 см 3 .
4.8 Колбы конические по ГОСТ 25336-82, вместимостью 250 см 3 .
4.9 Стаканчики для взвешивания по ГОСТ 25336-82, вместимостью 50 см 3 .
4.12 Мембранные фильтры с диаметром пор 0,45 мкм, например, по ТУ 6-55-221-903-88.
4.13 Фильтры обеззоленные «белая лента», например, по МРТУ 6-09-2411-65.
4.14 Кислота соляная, фиксанал, например, по ТУ 6-09-2540-87.
4.15 Метиловый оранжевый (индикатор), например, по ТУ 6-09-5171-84.
4.16 Ализариновый красный (индикатор), например, по ТУ 6-09-2105-77.
4.17 Фенолфталеин (индикатор), ч.д.а.
4.18 Вода дистиллированная по ГОСТ 6709-72.
Допускается применение других средств измерений, вспомогательных устройств и реактивов, в т.ч. импортных, с метрологическими и техническими характеристиками не хуже указанных.
При выполнении анализов необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007 и ГОСТ 12.4.021.
Требования по электробезопасности при работе с электроустановками должны соблюдаться по ГОСТ 12.1.019.
Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004 и иметь средства пожаротушения по ГОСТ 12.4.009.
Исполнители должны быть проинструктированы о мерах безопасности при работе с нагревательными приборами.
Организация обучения работающих безопасности труда производится по ГОСТ 12.0.004.
Измерения по методике может выполнять специалист-химик, прошедший соответствующую подготовку и имеющий навыки работы в химической лаборатории.
При подготовке к выполнению измерений и при их проведении необходимо соблюдать следующие условия:
температура окружающего воздуха, °С 20 ± 5,
атмосферное давление, кПа 101 ± 4 (760 мм рт.ст. ± 30 мм рт.ст.),
относительная влажность воздуха, % 65 ± 15,
напряжение питания сети, В 220 ± 22,
частота питающей сети Гц 50 ± 1
Общие требования к отбору проб по ГОСТ Р 51592-2000 «Вода. Общие требования к отбору проб», и ГОСТ Р 51593-2000 «Вода питьевая. Отбор проб», или другой нормативной документации, утвержденной в установленном порядке.
Объем пробы воды должен быть не менее 200 см 3 . При отборе бутыль следует заполнить водой доверху. Для отбора и хранения используют стеклянную или полиэтиленовую посуду. Щелочность необходимо определять не позднее, чем через 24 часа после отбора пробы. Мутные воды предварительно фильтруют через мембранные фильтры 0,45 мкм.
8.2 Приготовление реактивов
8.2.1 Приготовление раствора соляной кислоты молярной концентрации 0,1 моль/дм 3 (0,1 н). Раствор готовят из фиксанала разбавлением дистиллированной водой до 1000 см 3 .
8.2.2 Раствор индикатора метилового оранжевого с массовой долей 0,05 %. Растворяют 0,1 г метилового оранжевого в 200 см 3 дистиллированной воды.
8.2.3 Раствор индикатора ализаринового красного с массовой долей 0,05 %. Растворяют 0,1 г ализаринового красного в 200 см 3 дистиллированной воды.
8.2.4 Раствор индикатора фенолфталеина с массовой долей 0,5 %. Растворяют 1,0 г фенолфталеина в 200 см 3 дистиллированной воды.
8.3 Подготовка рН-метра к работе
рН-метр подготавливают к работе в соответствии с инструкцией по эксплуатации. Перед проведением измерений рН-метр прогревают в течение 30 минут и производят настройку его по двум стандартным образцам рН или буферным растворам с рН = 4,01 и рН = 6,86. Буферные растворы готовят в соответствии с указаниями в приложении к стандарт-титрам. Стандартные образцы используют в соответствии с инструкцией по применению ГСО рН.
9.1 Определение свободной щелочности
В коническую колбу мерным цилиндром помещают 100 см 3 исследуемой воды, добавляют 2 капли фенолфталеина и титруют на белом фоне раствором соляной кислоты до обесцвечивания. Фиксируют объем израсходованной кислоты ( V СВ ). Если розового окрашивания раствора не происходит, то щелочность по фенолфталеину равна 0.
При электрометрическом определении конечной точки титрования сосуд для титрования помещают на магнитную мешалку и при перемешивании измеряют рН пробы. Если рН пробы равно 8,3 или меньше, то щелочность по фенолфталеину равна 0. Если рН пробы больше 8,3, то пробу титруют до рН 8,3 и фиксируют объем израсходованной кислоты ( V СВ ).
9.2 Определение общей щелочности
В коническую колбу мерным цилиндром помещают 100 см 3 исследуемой воды (или используют раствор после определения свободной щелочности), добавляют 2 — 3 капли индикатора метилового оранжевого или ализаринового красного и титруют на белом фоне раствором соляной кислоты до начала перехода окраски индикатора. Фиксируют объем израсходованной кислоты ( V об ).
При электрометрическом определении конечной точки титрования сосуд для титрования помещают на магнитную мешалку и при перемешивании измеряют рН пробы. Пробу титруют до рН 4,5. Фиксируют объем израсходованной кислоты ( V об ).
Если для определения общей щелочности использовали раствор после определения свободной щелочности, то V об = V cb + V Р , где V Р — объем кислоты, израсходованный на титрование раствора после определения свободной щелочности.
10.1 Свободную щелочность анализируемой пробы вычисляют по формуле:
где ССВ — значение свободной щелочности, моль/дм 3 ;
V СВ — объем раствора соляной кислоты, см 3 , пошедший на титрование пробы до рН 8,3;
М — молярность раствора соляной кислоты, моль/дм 3 ;
1000 — коэффициент пересчета;
V — объем исследуемой пробы, см 3 .
10.2 Общую щелочность анализируемой пробы вычисляют по формуле:
где СОБ — значение общей щелочности, ммоль/дм 3 ;
V ОБ — объем раствора соляной кислоты, пошедший на титрование пробы, см 3 ;
М — молярность раствора соляной кислоты, моль/дм 3 ;
1000 — коэффициент пересчета;
V — объем исследуемой пробы воды, см 3 .
10.3 Результаты измерений общей и свободной щелочности анализируемой пробы представляют в виде:
где С — значение щелочности пробы, ммоль/дм 3 ,
Δ — абсолютная погрешность измерения щелочности при доверительной вероятности Р = 0,95, моль/дм 3 .
Значение Δ рассчитывают по формуле:
где δ — относительная погрешность измерения щелочности при Р = 0,95, %, таблица 1.
10.4 Результаты определения общей и свободной щелочности используются для вычисления содержания ионных форм углекислоты. Расчет основан на предположении, что щелочность вызывается только ионными формами углекислоты и, в отдельных случаях, гидроксильными ионами. Вследствие того, что эта предпосылка редко соответствует действительности, расчет почти всегда дает лишь приближенные результаты. Расчетом нельзя пользоваться при исследовании сильно загрязненных вод.
В зависимости от соотношения между свободной и общей щелочностью возможны 5 случаев расчета:
Отношение между свободной (ССВ) и общей (СОБ) щелочностью
Умножая содержание гидрокарбонат- и карбонат-ионов в ммоль/дм 3 , на 61,02 и 30 соответственно, получаем содержание этих ионов в мг/дм 3 .
Контроль стабильности результатов измерений в лаборатории осуществляют по ГОСТ Р ИСО 5725-6, раздел 6, используя методы контроля стабильности стандартного отклонения повторяемости или стандартного отклонения промежуточной прецизионности рутинного анализа.
Средством контроля являются пробы питьевых и природных вод, анализируемых в лаборатории.
11.1 При построении контрольных карт для контроля стандартного отклонения повторяемости используют приведенные к среднему значению результатов анализа значения расхождений ( w’ ) полученных результатов единичных измерений с1и с2, которые сравнивают с рассчитанными при построении контрольных карт пределами предупреждения и действия
где σ r — стандартное отклонение повторяемости результатов для значения у численно равного 1. Значение стандартного отклонения повторяемости приведено в таблице 2.
Пример. За три дня получены результаты параллельных определений 0,36 и 0,33 ммоль/дм 3 , 4,7 и 4,9 ммоль/дм 3 ; 6,5 и 6,7 ммоль/дм 3 .
Рассчитывают расхождения w 1 ‘ = |0,36 — 0,33| / 0,5 · (0,36 + 0,33) = 0,09
w 2 ‘ = |4,7 — 4,9| / 0,5 · (4,7 + 4,9) = 0,04
w 3 ‘ = |6,5 — 6,7| / 0,5 · (6,5 + 6,7) = 0,02
Значения расхождений наносят на контрольную карту.
Для расчета UCLn и UCL Диз таблицы 2 берут σ r = 5 %. Расчет UCLn = 2,834 · 0,05 = 0,14, UCL Д= 3,686 · 0,05 = 0,18, где 0,05 — абсолютное значение σ r = 5% для у = 1.
11.2 При построении контрольных карт для контроля стандартного отклонения промежуточной прецизионности используют приведенные к среднему значению расхождения ( w’ ) результатов, полученных в условиях промежуточной прецизионности (при различиях по факторам «время», «оператор», «оборудование») y 1 и у2, которые сравнивают с рассчитанными при построении контрольных карт пределами предупреждения и действия
где σI(T,O,E) — стандартное отклонение промежуточной прецизионности результатов для значения у численно равного 1. Значение стандартного отклонения промежуточной прецизионности приведено в таблице 2.
Пример. За три дня двумя операторами получены результаты измерений 0,31 и 0,26 ммоль/дм 3 , 5,2 и 5,6 ммоль/дм 3 , 6,3 и 6,6 ммоль/дм 3 .
Рассчитывают расхождения w 1 ‘ = |0,31 — 0,26 | / 0,5 · (0,31 + 0,26) = 0,18
Значения расхождений наносят на контрольную карту.
Диапазон измерений щелочности, ммоль/дм 3
Стандартное отклонение повторяемости, σr,.%
Стандартное отклонение промежуточной прецизионности при различиях по факторам «время», «оператор», «оборудование», σI(T,O,E), %
При неудовлетворительных результатах контроля, например, превышение предела действия или регулярное превышение предела предупреждения, выясняют причины этих отклонений, в том числе проверяют работу оператора.
Периодичность проведения контроля стабильности результатов измерений устанавливают индивидуально для каждой лаборатории в соответствии с документами по внутрилабораторному контролю качества результатов анализа.
После внедрения МВИ в практику работы лаборатории при необходимости проверки приемлемости результатов измерений, полученных в условиях воспроизводимости, проводят межлабораторные сравнительные испытания с использованием данной методики для оценки стандартного отклонения воспроизводимости. В случае невозможности организации межлабораторных сравнительных испытаний допускается, согласно МИ 2336-2002, оценить значение стандартного отклонения воспроизводимости, σ R , по формуле: σ R = 1,2 · σI(T,O,E). Проверку приемлемости результатов измерений в условиях воспроизводимости осуществляют по ГОСТ Р ИСО 5725-6-2002, пункт 5.3.
Оценки стандартных отклонений повторяемости и воспроизводимости
В таблице А.1 представлены данные по результатам межлабораторных сравнительных испытаний (МСИ) по определению общей щелочности в пробах питьевой воды, проведенных Органом по аккредитации ЦИКВ среди аккредитованных лабораторий и обработанных в соответствии с п. 7.4 ГОСТ Р 5725-2-2002. Представленные данные не применимы для обобщений.
р — количество лабораторий;
п — количество измерений, полученных в каждой лаборатории;
у — общее среднее значение щелочности в образце;
Sr — оценка стандартного отклонения повторяемости результатов измерений;
SR — оценка стандартного отклонения воспроизводимости результатов измерений.
Ионы СО3 2- и НСО3 при совместном присутствии определяют обычно путем титрования воды соляной кислотой. Это определение основано на реакциях:
При прибавлении соляной кислоты будет увеличиваться концентрация ионов водорода в воде, это повлечет за собой нарушение указанных выше равновесий, обе реакции пойдут слева направо. На основании того, что константы углекислоты различаются на 4 порядка, можно утверждать, что пока в воде остается заметное количество карбонат-ионов, в ней практически будет отсутствовать свободная углекислота.
Таким образом, вначале протекать практически будет только первая из указанных реакций, так как карбонат-ионы будут связывать ионы водорода, превращаясь в ионы НСО3 — . Сдвиг равновесия вправо для второй реакции не будет иметь практического значения. После окончания первой реакции рН воды будет равен 8,3. В этот момент вода не будет содержать практически ни ионов СО3 2- , ни свободной углекислоты.
При дальнейшем прибавлении соляной кислоты будет протекать уже вторая реакция. При значении рН около 4,5 в воде будет только свободная углекислота, ионы НСО3 — будут отсутствовать. При этом как в эквивалентной точке, соответствующей концу первой реакции, так и в эквивалентной точке, отвечающей концу второй реакции, будут отмечаться скачки в титровании, хотя и не очень большие.
Указанные обстоятельства позволяют определить конец первой и конец второй реакции при помощи двух различных индикаторов. Конец первой реакции устанавливается по фенолфталеину, конец второй — по метиловому оранжевому. При анализе загрязненных и окрашенных вод рекомендуется электрометрическое титрование.
Силикат-, фосфат-, борат-, сульфид-ионы, ионы гуминовых и других слабых кислот титруются вместе с карбонат- и гидрокарбонат-ионами. Обычно эти ионы присутствуют в природных водах в очень малых концентрациях.
«Унифицированные методы анализа вод» под общей редакцией Лурье Ю.Ю., М., 1971, издательство «Химия», с. 65 — 68, 165
«Методы определения вредных веществ в воде водоемов» под редакцией Щипковой А.П., М., издательство «Химия», 1981, с. 37 — 40
«Контроль химической, бактериальной и радиационной безопасности по международным стандартам» под редакцией Фомина Г.С., М., 1995, с. 118 — 120
Центр Исследования и Контроля Воды
аккредитован в Системе аккредитации аналитических лабораторий (центров) Госстандарта России, № Госреестра РОСС RU .0001.510045
Метрологическая служба аккредитована на право аттестации методик выполнения измерений и проведения метрологической экспертизы документов, в том числе применяемых в сферах распространения государственного метрологического контроля и надзора, № Госреестра 01.00031-97
199034, Санкт-Петербург, Университетская наб., 7/9
о метрологической аттестации методики выполнения измерений щелочности в пробах питьевой и природной воды титриметрическим методом (ЦВ 1.01.11-98 «А »)
Методика выполнения измерений щелочности в пробах питьевой и природной воды титриметрическим методом,
разработанная Центром исследования и контроля воды.
регламентированная в документе: «Методика выполнения измерений щелочности в пробах питьевой и природной воды титриметрическим методом» ЦВ 1.01.11-98 «А»,
аттестована в соответствии с ГОСТ Р 8.563-96.
Аттестация осуществлена по данным внутрилабораторного контроля воспроизводимости результатов измерений, полученным в 1997 — 1998 годах.
В результате аттестации установлено, что МВИ соответствует предъявляемым к ней метрологическим требованиям и обладает следующими основными метрологическими характеристиками:
Диапазон измерений щелочности, ммоль/дм 3
Характеристика погрешности (границы интервала, в котором погрешность находится с доверительной вероятностью Р = 0,95), ± σ, %
Свидетельство выдано 25 декабря 1998 г.
источник
| Классы МПК: | G01N33/18 воды | |||||
| Автор(ы): | Караван С.В. , Пинчук О.А. , Терентьев В.И. | |||||
| Патентообладатель(и): | Санкт-Петербургское государственное унитарное предприятие «Инженерный центр «Водоканал» | |||||
| Приоритеты: |
| Рейтинг: | 4.8 баллов / 2537 оценок |
| Формат: | Книга |
| Уже скачали: | 12783 раз |
Нам показалось, что Книги ниже Вас заинтересуют не меньше. Эти издания Вы так же можете скачивать и читать совершенно бесплатно на сайте!
Рождественская Т.Э. «Банковское право»В учебном пособии представлена система основных институтов банковского права: правовой статус Банка России, правовое положение кредитных организаций, банковские о . . .
Шаповаленко И.В. «Возрастная психология»Учебник «Возрастная психология» представляет собой развернутый курс по дисциплине «Психология развития и возрастная психология» разработанный в соответствии с Г . . .
Коржуков Н.Г. «Общая и неорганическая химия»Изложены основы энергетики химических реакций, химической термодинамики, химической кинетики, строения атома, химической связи и строения молекул, а также о . . .
Кусков В.В. «История древнерусской литературы»Книга замечательного ученого и педагога, почетного профессора МГУ им. М. В. Ломоносова В. В. Кускова давно и прочно вошла в учебный процесс филологических . . .
Грицанов А.А. «Всемирная энциклопедия: Философия»Издание включает в себя около 1700 аналитических статей, охватывающих как всю полноту классического философского канона (в его Западном, Восточном и во . . .
Стародубцев В.А. «Концепции современного естествознания»В учебнике рассмотрены вопросы становления современной парадигмы естествознания, его античные и классические предпосылки, концепции фундаменталь . . .
Солодовников Ю.А. «Мировая художественная культура. 8 класс»Учебник «Мировая художественная культура. Человек в мировой художественной культуре» для 8 класса продолжает знакомить с художественным насл . . .
Горкин А.П. «Биология. Современная иллюстрированная энциклопедия»Существенный объем тома занимают статьи о растениях и животных, в которых приводятся сведения об их систематическом положении, местах о . . .
Покидченко М.Г., Чаплыгина И.Г. «История экономических учений»В учебном пособии кратко изложен весь курс истории экономических учений: экономическая мысль Древнего Востока, античного мира, Средневеков . . .
Хомченко И.Г. «Решение задач по химии»Настоящее издание является дополнением к книге И. Г. Хомченко «Сборник задач и упражнений для средней школы» (М., 1996-2010). В нем даны решения типовых задач из . . .
Если вы хотите скачивать книги, журналы и аудиокниги бесплатно, без рекламы и без смс, оставлять комментарии и отзывы, учавствовать в различных интересных мероприятиях, получать скидки в книжных магазинах и многое другое, то Вам необходимо зарегистрироваться в нашей Электронной Библиотеке.
К сожалению, в нашей Бесплатной Библиотеке пока нет отзывов о Книге Унифицированные методы анализа вод. Помогите нам и другим читателям окунуться в сюжет Книги и узнать Ваше мнение. Оставьте свой отзыв или обзор сейчас, это займет у Вас всего-лишь несколько минут.
источник
Ответов в этой теме: 13
Страница: 1 2
«« назад || далее »»
| Автор | Тема: Определение органики в воде | |
| hamon Пользователь Ранг: 5 | 04.10.2006 // 10:43:46 Подскажите пожалуйста как можно определить количество органики суммарное в питьевой воде (на уровне 0 — 20 мг/л)? Необходимо проверить эффективность работы угольного фильтра. | |
| Реклама на ANCHEM.RU Администрация Ранг: 246 Размещение рекламы | ||
| woodpecker Пользователь Ранг: 399 | 04.10.2006 // 10:47:37 Есть специальные приборы для этой цели — анализатор общего органического углерода. Это для постоянного мониторинга и если есть деньги Для разового анализа, можете покипятить с марганцовкой | |
| Ed VIP Member Ранг: 3186 | 04.10.2006 // 11:39:24 Анализаторы общего органического углерода (ТОС-анализаторы) — это вещь действительно дорогая. Для ваших целей вполне подойдет определение ХПК (химического потребления кислорода), эта величина более-менее коррелирует с общим содержанием органики и анализ выполняется довольно просто, есть официальные методики, есть описание анализа, допустим, в Лурье. | |
| hamon Пользователь Ранг: 5 | 04.10.2006 // 12:30:38 А в какую стоимость можно уложиться при покупке прибора и какое доп оборудование необходимо? | |
| hamon Пользователь Ранг: 5 | 04.10.2006 // 12:33:26 Какая именно книга Лурье имеется в виду? И можно ли ее сейчас приобрести или только в библиотеке? | |
| woodpecker Пользователь Ранг: 399 | 04.10.2006 // 12:35:50
По всем производителям не скажу, но в районе 20 kEUR за полный комплект выйдет. | |
| Реклама на ANCHEM.RU Администрация Ранг: 246 Размещение рекламы |
| |
| Ed VIP Member Ранг: 3186 | 04.10.2006 // 13:28:21
Да, порядок цен примерно 20-25 kEUR, по крайней мере, Shimadzu TOC-V | |
| hamon Пользователь Ранг: 5 | 04.10.2006 // 14:31:38 Спасибо за информацию | |
| ernst Пользователь Ранг: 87 | 02.11.2006 // 18:19:01
Да, порядок цен примерно 20-25 kEUR, по крайней мере, Shimadzu TOC-V Эд! Я бы не стал рекомендовать Лурье. Слишком много ошибок Лучше всего посмотреть Алекин,Скопинцев, Семенов .Руководство по анализу природных вод.1973. или Семенов А.Д.(ред) Руководство по химическому анализу вод суши.1977. | |
| Ирекович Пользователь Ранг: 123 | 07.08.2007 // 8:45:07 Уважаемые Дамы и Господа — хроматографисты. Помогите пожалуйста. Нам необходимо определять содержание окиси этилена и ацетальдегида в воде. Может кто-нибудь подскажет хроматографическаую методику на данное определение. На каой фазе делать, при каких условиях, с каким детектором. И вообще существует ли такая метода в хроматографии. Дело горящее. | |
| Лидия VIP Member Ранг: 436 | 07.08.2007 // 9:01:52
Ответов в этой теме: 13 источник |