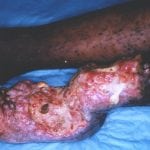
Саркома Капоши (Kaposi sarcoma, ангиосаркома Капоши, множественный геморрагический саркоматоз или просто СК) — онкодерматологическое заболевание, характеризующееся множественными злокачественными новообразованиями на поверхности дермы и в полости рта.
Поражения кожи образуются из-за разрастания внутренней оболочки лимфатических и кровеносных сосудов – эндотелия, они меняют свою структуру и истончаются.
Клетки сосудов становятся веретенообразными, что подтверждает диагноз Саркомы Капоши по гистологическому маркеру.
Обратить внимание на то, что это за болезнь Капоши саркома можно по наличию у пациентов синюшно-красноватых, ярко-красных, темно-красных или коричневатых пятен на кожных покровах (см. фото ниже), превращающихся потом в образования диаметром 5 мм.
Диагностика включает в себя анализ крови на ВИЧ, проведение биопсии для взятия образца на гистологию, исследование иммунной системы человека.
На начальной стадии образования безболезненные, но с прогрессированием процесса появляются боли.
Выделить ряд конкретных причин саркомы Капоши до сих пор невозможно. Но есть болезни и патологии, сопутствующие развитию множественного геморрагического саркоматоза:
Люди, подвергшиеся воздействию радиации, имеют предрасположенность к развитию саркомы кожи, так риск появления патологии увеличивается в 30-50 раз.
Множественная геморрагическая саркома может развиться при механическом повреждении тканей, быстром гормональном росте, наличии в организме инородных тел или онкогенных вирусов.
Трансплантация органов и, как следствие, полихимиотерапия и иммуносупрессивная терапия при этом повышает риск возникновения саркомы Капоши у мужчин на 10-15%, намного реже у женщин. По статистике в 75% случаев после проведенной операции у пациента диагностируется идиопатическая множественная геморрагическая саркома.
Ангиосаркома обнаруживается зачастую параллельно с ВИЧ-инфекцией в организме пациента.
Медики сходятся во мнении, что провоцирующим фактором саркомы Капоши является вирус герпеса 8 типа (Human Herpes Virus 8 type), который активизируется при понижении иммунитета.
Вирус выявляют у трети исследуемых пациентов, большая часть из которых бисексуалы и геи.
Предрасположенность к геморрагическому саркоматозу выявлена у пожилых мужчин, преимущественно из Средиземноморья и Центральной Африки, геев, бисексуалов и реципиентов, живущих с трансплантированными им органами.
Основные симптомы Саркомы Капоши:
- Образования на коже в виде пятен, бляшек, везикул, узелков размером до 5 мм (см. фото выше). Цвет опухолей синюшный темный, но может быть красноватого или фиолетового оттенков, коричневого, не меняет цвет при надавливании. Бляшки блестящие и гладкие на ощупь, в редких случаях могут шелушиться. Опухоли могут сливаться в одну, приобретая зеленый оттенок. Саркома кожи проявляется глубокими язвочками сине-багрового цвета с некротическим налетом и неприятным запахом выделяемого.
- Множественные опухоли образуют отек окружающих тканей, иногда возникает жжение, зуд. Пациента беспокоят боли, тяжесть в одной или обеих конечностях, может развиться слоновость.
- Поражение слизистых оболочек, при которых наблюдается болезненность при жевании, диарея и кровотечения в желудке и кишечнике. Сопровождается болезнь одышкой, кашлем, кровавой мокротой. Саркома Капоши во рту представляет собой фиолетово-красные узелки, увеличивающиеся постепенно в размере.
- Воспаление лимфоузлов в одиночном порядке или группами.
- Поражения печени, ЖКТ и нервной системы, костной ткани, которые легко спутать с другими патологиями. В данном случае без пятен и бляшек на коже багрового цвета Саркома Капоши у пациента может быть диагностирована не сразу.
Медленно прогрессирующая болезнь перерастает в кишечную и легочную форму патологии, что может угрожать жизни.
Ангиоэндотелиома кожи классифицируется на четыре типа:
1) Классический тип. Идеопатическая саркома поражает пожилых людей, локализуясь на ступнях и в виде пятен или бляшек синеватого, буро-коричневого оттенка.
Новообразования часто покрыты бородавками, участки вокруг них пигментированы (см. фото выше).
Постепенно поражаются другие области кожных покровов, в последнюю очередь могут быть затронуты половые и внутренние органы. Различают 3 стадии: 1. пятнистая 2. папулезная 3. опухолевая:
- Пятнистая. Саркома Капоши начальной стадии, когда дерма покрыта синюшными, фиолетовыми, багровыми пятнами. Диаметр пятен разрастается до 5 см, поверхность их гладкая. Прогрессирование болезни характерно слиянием множественных пятен в сплошную поверхность, которая чешется и жжет.
- Папулезная. При ней образуются узелковые образования, круглой или полукруглой формы, плотные. Одиночные папулы могут разрастаться до 10 мм, приобретают синюшный или коричнево-багровый окрас, а их поверхность напоминает апельсиновую корку. При слиянии нескольких образований появляется бляшка темно бурого оттенка или фиолетового.
- Опухолевая. Узлы и опухоли на данной стадии образуются в единичном порядке или группами. Образования имеют бурый или синюшный цвет и достигают 5 см в длину. При объединении нескольких образований в одно возникают язвы, которые кровоточат.
На каждой стадии опухолевидные образования могут провоцировать возникновение пурпуры или подкожных гематом.
2) Эндемическая ангиосаркома наиболее распространена в Центральной Африке. По статистике чаще всего заболеванию подвержены дети до года, где смертность наступает уже через пару лет.
3) Эпидемическая ангиосаркома, существующая параллельно со СПИДом, встречается у молодых людей до 30 лет.
Патологию легко узнать по пятнам на кончике носа или твердом небе, а также по ярким вкраплениям розового цвета по телу. Лимфатические узлы и внутренние органы быстро поражаются, а узлы становятся болезненными, кровоточащими.
4) Иммуносупрессивная саркома основана на лечении пациентов иммуносупрессивной терапией после трансплантации органов или при наличии онкозаболевания.
Тип болезни характерен для населения среднего возраста, преимущественно у мужчин. Патологию трудно диагностировать на ранней стадии, так как визуальных симптомов может почти не быть.
Первые признаки в виде пятен и бляшек синюшного и бурого цвета на коже, состояние иммунодефицита и наличие у пациента ВИЧ-инфекции дают практически всегда точный диагноз саркомы Капоши.
Сначала проводится лабораторная диагностика для определения наличия вируса герпеса 8 типа. Для этого происходит выделение возбудителя из пораженной опухолью ткани, и после обнаружения вируса находят к нему антитела.
Методы выявления поражения слизистых оболочек:
- Бронхоскопия.
- Рентгенография легких.
- Гастроскопия.
- Колоноскопия.
Диагностика пациента на наличие Саркомы Капоши включает этапы:
- осмотр слизистых оболочек, которые видны;
- проведение иммунограммы;
- анализ крови на наличие половых инфекций;
- УЗИ органов брюшной полости и рентген органов грудной клетки;
- эзофагогастродуоденоскопия;
- КТ почек и МРТ надпочечников.
Лечение саркомы Капоши начинается с терапии по повышению иммунитета, после чего уже назначается комплекс мер по устранению симптомов болезни.
Такое лечение как полихимиотерапия активно используется при саркоме Капоши, но при взаимодействии препаратов для лечения ВИЧ-инфекции, оказывается негативное воздействие на костный мозг.
Применение высокоактивной антиретровирусной терапии может полностью подавить жизнедеятельность одного из вирусов герпеса, который является возбудителем синдрома Капоши.
Такая химиотерапия длится год и способствует повышению иммунитета.
Терапия препаратами интерферона для поднятия иммунитета дает эффект, если проводить ее длительными курсами. Помимо этого, используется криотерапия, местная химиотерапия и радиационное облучение.
В настоящее время болезнь саркомы Капоши считается в большинстве случаев неизлечимой, а медикаменты могут только временно убрать симптомы и временно улучшить состояние больного.
Наиболее популярные препараты:
- Винкристин (применяется однократно раз в неделю по 1,4 мг/кг внутримышечно);
- Винбластин (схема применения сначала раз в неделю, затем перерыв, после чего еженедельная доза инъекции составляет 0,1 мг/кг);
- Доксорубицин (применяется раз в три недели по 60-70 мг/кг, но при необходимости дозу можно разделить на три приема раз в неделю);
- Проспидин (вводится раз в день внутривенно или внутримышечно, минимальная доза может составлять 0,05 мг/кг, максимальная 0,15 мг/кг);
- Блеомицин;
- Бендамустин;
- Циклофосфан.
На начальной стадии болезни сразу не назначаются противоопухолевые препараты, перед этим принимают общеукрепляющие средства.
Интерфероны применяются для усиления действия лекарств основной терапии.
Если саркома Капоши присутствует совместно с ВИЧ-инфекцией, назначается терапия сразу 3-4 препаратами.
Сильные побочные эффекты от противоопухолевых лекарств компенсируются проведением гормональной терапии.
Использовать хирургическое вмешательство при саркоме Капоши можно, при поверхностных поражениях, если они безболезненны. Но при заболевании более уместны коагуляция и облучение электронами.
При бездействии лучевой терапии используется хирургическое вмешательство, но при удалении одной опухоли возможно распространение пораженных клеток по организму с кровью.
В таких случаях иссечение очага болезни проводится совместно с химиотерапией или облучением, что дает шанс на длительную ремиссию у 30% пациентов.
К альтернативным методам лечения ангиосаркомы Капоши относятся:
- Питание и добавки к пище.
- Травяные настойки и бальзамы.
Рацион питания должен быть богат витаминами для повышения устойчивости иммунной системы, также следует употреблять легкоусвояемые белки для создания антител.
Клетчатка в продуктах питания будет способствовать опорожнению кишечника и выведению токсинов.
В борьбе с заболеванием в ежедневное меню можно добавить ягоды брусники и абрикосы с косточками.
Чтобы блокировать образование метастаз следует употреблять в пищу:
- чеснок;
- морскую рыбу, такую как сардина, форель, лосось;
- зеленые и желтые овощи.
Исключить из рациона при ангиосаркоме следует копчености, кислые ягоды и цитрусовые, алкогольные напитки, продукты, содержащие большое количество танина, который провоцирует тромбообразование.
Рецепты травяных настоек и бальзамов:
- Настойка на основе алоэ. Для этого необходимо измельчить четыре листа алоэ и залить их 0,5 литрами водки. После настаивания в течение двух недель, лекарство принимать по 1 столовой ложке трижды в сутки перед едой.
- Настойка на основе зверобоя и виноградной водки, которая настаивается две недели и принимается трижды в день по 30-40 капель.
- Бальзам из листьев подорожника. 100 грамм измельченных листьев подорожника следует смешать со 100 граммами сахарного песка, после чего бальзам будет давать сок в течение двух недель. Пить жидкий бальзам следует трижды в день перед едой.
Первые профилактические меры при саркоме Капоши заключаются в обнаружении людей, находящихся в группе риска.
Пациенты, использующие иммуносупрессивную терапию должны быть проверены одними из первых, на наличие больных с вирусом герпеса 8 типа.
Дальнейшая профилактика сводится за контролем над больными с целью преждевременного появления рецидива болезни.
К профилактическим мерам относят:
- предотвращение сексуальных контактов без презервативов;
- ежегодные медицинские осмотры стоматолога, хирурга, осмотра слизистых;
- исключение табачных изделий из повседневной жизни;
- запрет на использование кортикостероидов;
- укрепление иммунной системы;
- ограничение пребывания на солнце в летнее время;
- профилактика ВИЧ, СПИД.
Наличие ангиосаркомы у родственника – это повод задуматься и пройти обследование на наличие патологии, так как велика вероятность передачи заболевания по наследству.
Спрогнозировать жизнь пациента при ангиосаркоме можно в зависимости от остроты течения болезни. При прогрессирующем процессе заболевания и молниеносно распространяющихся симптомах пациент может прожить от двух месяцев до двух лет.
Подострая форма саркомы может в некоторых случаях дать возможность прожить пациенту еще три года. Если форма заболевания хроническая и прогрессирует медленно, то при соответствующей терапии жизнь пациента можно продлить на 5-10 лет.
Важным фактором является состояние иммунитета пациента, так при глубоком иммунодефиците в сочетании со СПИДом летальный исход может наступить в течении нескольких месяцев, о регрессировании болезни речи быть не может.
При диагностировании саркомы Капоши сначала проводится курс иммунотерапии, а после этого назначаются основные препараты для лечения. Болезнь в сочетании со СПИДом в большинстве случаев быстро заканчивается летальным исходом, так как процесс быстро прогрессирует. При появлении первых признаков патологии важно ежегодно контролировать наличие пятен и узелков на коже.
источник
Саркома Капоши (множественная геморрагическая идеопатическая саркома Капоши, ангиосаркома Капоши, ангиоэндотелиома кожи) — множественные злокачественные поражения дермы, развивающиеся из эндотелия проходящих в ней лимфатических и кровеносных сосудов. Зачастую заболевание сопровождается поражением слизистой рта и лимфатических узлов. Проявляется саркома Капоши множественными синюшно-красноватыми пятнами на коже, трансформирующимися в опухолевые узлы до 5 см в диаметре. Диагностика саркомы Капоши включает гистологию биопсийного образца из очага поражения, исследование иммунитета и анализ крови на ВИЧ. Лечение проводится путем системного и местного применения химиопрепаратов и интерферонов, лучевым воздействием на опухолевые узлы, криотерапией.
Саркома Капоши получила свое название по имени венгерского дерматолога, впервые описавшего заболевание в 1872 году. Распространенность саркомы Капоши не так велика, но среди больных ВИЧ она достигает 40-60%. У этих пациентов саркома Капоши является самой часто встречающейся злокачественной опухолью. По данным проводимых в дерматологии клинических исследований у мужчин саркома Капоши диагностируется примерно в 8 раз чаще, чем у женщин.
К группам риска, в которых развитие саркомы Капоши наиболее вероятно, относятся: инфицированные ВИЧ мужчины, мужчины средиземноморского происхождения в пожилом возрасте, народности Центральной Африки, реципиенты пересаженных органов или пациенты, длительно получающие иммуносупрессивную терапию.
Медицине пока неизвестны точные причины развития саркомы Капоши и ее патогенез. Заболевание нередко возникает на фоне других злокачественных процессов: грибовидного микоза, болезни Ходжкина, лимфосаркомы, миеломной болезни. Исследования последних лет подтверждают связь заболевания с присутствием в организме специфических антител, образующихся при инфицированности вирусом герпеса 8 типа. Заражение вирусом может произойти половым путем, через кровь или слюну.
На сегодняшний день ученым удалось выделить цитокины, оказывающие стимулирующее действие на клеточные структуры саркомы Капоши. К ним относят: 3FGF — фактор роста фибробластов, IL-6 — интерлейкин 6, TGFp — трансформирующий фактор роста. В возникновении опухоли у больных СПИДом большое значение отводят онкостатину.
Саркома Капоши является не совсем обычной злокачественной опухолью. Слабая митотическая активность, зависимость процесса от иммунного статуса пациента, мультицентрическое развитие, возможность обратного развития очагов опухоли, отсутствие клеточной атипии и гистологическое выявление признаков воспаления подтверждают предположение о том, что в начале своего возникновения саркома Капоши скорее представляет собой реактивный процесс, нежели истинную саркому.
Наиболее часто заболевание начинается с появления на коже фиолетово-синих пятен, которые инфильтрируются с образованием округлых дисков или узлов. В отдельных случаях саркома Капоши начинается с возникновения на коже папул, что имеет сходство с высыпаниями красного плоского лишая. Узлы постепенно растут, достигая величины лесного или грецкого ореха. Они имеют плотно-эластичную консистенцию и шелушащуюся поверхность, часто пронизанную сосудистыми звездочками. Узлы причиняют пациенту боль, усиливающуюся при давлении на них. Со временем при саркоме Капоши возможно самопроизвольное рассасывание узлов с образованием рубцов в виде вдавленных гиперпигментаций.
Выделяют 4 клинических варианта саркомы Капоши: классический, эпидемический, эндемический и иммунно-супрессивный.
Классическая саркома Капоши распространена в России, Украине, Белоруссии и странах Центральной Европы. Ее типичная локализация — кожа боковой поверхности голеней, стоп и кистей. Характерна четкая очерченность и симметричность опухолевых очагов, отсутствие субъективной симптоматики (лишь в некоторых случаях пациенты отмечают жжение или зуд). Данная форма саркомы крайне редко протекает с поражением слизистых. В течении классической саркомы Капоши выделяют 3 клинический стадии: пятнистую, папулезную и опухолевую.
Пятнистая стадия — самое начало заболевания. Представлена красно-синюшними или красно-бурыми пятнами неровной формы, размер которых не превышает 0,5 см. Пятна имеют гладкую поверхность.
Папулезная стадия саркомы Капоши имеет вид множественных элементов, выступающих над уровнем кожи в виде сфер или полусфер. Они плотные, эластичные, диаметр колеблется от 0,2 до 1 см. Сливаясь между собой, элементы могут образовывать полушаровидные или уплощенные бляшки с шероховатой или гладкой поверхностью. Но чаще отдельные элементы саркомы Капоши этой стадии остаются изолированными.
Опухолевая стадия характеризуется образованием опухолевых узлов диаметром от 1 до 5 см. Узлы, как и элементы пятнистой стадии, имеют синюшно-красный или красновато-бурый оттенок. Они сливаются друг с другом и изъязвляются.
Эпидемическая саркома Капоши ассоциирована со СПИДом и является одним из характерных симптомов этого заболевания. Типичен молодой возраст заболевших (до 37 лет), яркость высыпных элементов и необычное расположение опухолей: слизистые, кончик носа, верхние конечности и твердое небо. При этой форме саркомы Капоши происходит быстрое вовлечение в процесс лимфатических узлов и внутренних органов.
Эндемическая саркома Капоши встречается, как правило, в Центральной Африке. Заболевание развивается в детском возрасте, чаще на первом году жизни. Характеризуется поражением внутренних органов и лимфатических узлов, изменения кожи минимальны и редки.
Иммунно-супрессивная саркома Капоши протекает хронически и наиболее доброкачественно, как правило, без вовлечения внутренних органов. Возникает на фоне проводимого иммунносупрессивного лечения у пациентов, перенесших пересадку органов. При отмене подавляющих иммунитет препаратов часто происходит регресс симптомов заболевания.
Течение саркомы Капоши может быть острым, подострым и хроническим. При остром развитии заболевания происходит быстрая генерализация злокачественного процесса с развитием интоксикации и кахексии. Пациенты погибают в период от 2-х месяцев до 2-х лет от начала заболевания. Подострая форма без проведения лечения может длиться 2-3 года. Медленное развитие опухолевого процесса при хронической форме саркомы Капоши приводит к ее более длительному течению (8-10 и более лет).
К осложнениям саркомы Капоши относятся деформация и ограничение движений в пораженных конечностях, кровотечения из распадающихся опухолей, лимфостаз с развитием лимфедемы при сдавлении опухолью лимфатических сосудов и др. Изъязвление опухолевых узлов опасно возможностью инфицирования, что на фоне иммунодефицита приводит к быстрому развитию сепсиса и может явиться причиной летального исхода.
Диагностика саркомы Капоши основана на ее типичных клинических проявлениях и данных биопсии образований. Гистологическое исследование выявляет в дерме множественные новообразованные сосуды и пролиферацию веретенообразных клеток — молодых фибробластов. Наличие гемосидерина и экстравазатов (геморрагических экссудатов) позволяет отличить саркому Капоши от фибросаркомы.
Пациентам проводят иммуннологические исследования крови и анализ на ВИЧ. Для выявления поражений внутренних органов при саркоме Капоши применяют УЗИ брюшной полости и сердца, гастроскопию, рентгенографию легких, сцинтиграфию скелета, КТ почек, МРТ надпочечников и т. п.
Необходима дифференциальная диагностика саркомы Капоши с красным плоским лишаем, саркоидозом, гемосидерозом, грибовидным микозом, высокодифференцированной ангиосаркомой, микровенулярной гемангиомой и др.
Важным моментом в лечении саркомы Капоши является терапия основного заболевания для повышения иммунного статуса организма. Системное лечение саркомы Капоши обычно назначается пациентам с благоприятным иммунологическим фоном при бессимптомном течении болезни. Оно состоит в интенсивной полихимиотерапии. Риск применения подобной терапии у пациентов с иммуннодефицитом связан с токсическим воздействием препаратов на костный мозг, особенно в сочетании с медикаментами для лечения ВИЧ-инфекции. На 1 и 2 стадии саркомы Капоши наиболее оптимальной считается монотерапия проспидия хлоридом, который отличается отсутствием угнетающего действия на иммунную систему и кроветворение. В лечении классической и эпидемической формы саркомы Капоши успешно применяются интерфероны: α-2a, α-2b и β. Они препятствуют пролиферации фибробластов и способны инициировать апоптоз опухолевых клеток.
Местное лечение саркомы Капоши включает криотерапию, инъекции химиотерапевтических препаратов и интерферона в опухоль, аппликации динитрохлорбензола и мази проспидия хлорида, др. методы. При наличие болезненных и крупных очагов поражения, а также для лучшего косметического эффекта проводится локальное облучение.
Прогноз заболевания при саркоме Капоши зависит от характера его течения и тесно связан с состоянием иммунной системы пациента. При более высоких показателях иммунитета проявления заболевания могут носить обратимый характер, системное лечение дает хороший эффект и позволяет добиться ремиссии у 50-70% больных. Так у больных саркомой Капоши с показателем лимфоцитов CD4 больше 400 мкл-1 частота ремиссий на фоне проводимой иммунной терапии превышает 45%, а при CD4 меньше 200 мкл-1 добиться ремиссии удается лишь 7% пациентов.
источник
Версия: Клинические рекомендации РФ (Россия)
РОССИЙСКОЕ ОБЩЕСТВО ДЕРМАТОВЕНЕРОЛОГОВ И КОСМЕТОЛОГОВ
ФЕДЕРАЛЬНЫЕ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ВЕДЕНИЮ БОЛЬНЫХ САРКОМОЙ КАПОШИ
Шифр по Международной классификации болезней МКБ-10
С46.0, В21.0
ОПРЕДЕЛЕНИЕ
Саркома Капоши – это заболевание, ассоциированное с вирусом герпеса человека 8 типа (HHV-8) и характеризующееся множественными кожными и внекожными новообразованиями эндотелиальной природы.
Общепринятой классификации не существует.
Вирус герпеса человека 8 типа (HHV-8) относится к семейству g—herpesviridae, роду Rhadinovirus. Как и при других герпес-вирусах, экспрессия гена HHV-8 связана с вирусной латентностью или лизирующей вирусной репликацией.
Частота распространения классической формы саркомы Капоши (СК) значительно варьирует в различных географических областях от 0,14 на 1 млн. жителей (как мужчин, так и женщин) до 10,5 на 1 млн. мужчин и 2,7 на 1 млн. женщин. Мужчины болеют в 3 раза чаще. Начало заболевания СК регистрируется в возрасте 35-39 лет у мужчин и в возрасте 25-39 лет у женщин.
Большая частота встречаемости СК наблюдается в странах расположенных на побережье Средиземного моря и центральной Африки (эндемическая саркома Капоши). В развитых странах у пациентов, инфицированных вирусом иммунодефицита человека (ВИЧ) –1, частота встречаемости HHV-8 наиболее высока среди мужчин гомо- и бисексуальной ориентации. Саркома Капоши является самой распространенной СПИД-ассоциированной опухолью у мужчин, практикующих сексуальные отношения с мужчинами, и наблюдается у 20% больных СПИД.
Трансплантационная СК наблюдается преимущественно при пересадке почки. Возможно развитие СК у пациентов, получающих иммуносупрессивную терапию при лечении аутоиммунных заболеваний.
Одним из основных путей передачи HHV-8 является половой, риск инфицирования повышается с увеличением числа сексуальных партнеров и практикой нетрадиционных видов половых контактов.
Ротоглотка является местом наиболее выраженной репликации вируса; в слюне находится большое число копий вируса HHV-8. Неполовой механизм передачи вируса через слюну является общепризнанным и имеет важное значение в заражении детей в эндемических областях.
Вертикальный путь передачи HHV-8 от матери к плоду во время беременности и родов не имеет большого значения для распространения вируса.
Вирус HHV-8 также может передаваться через кровь, продукты крови, донорские органы после трансплантаций. Вирусный геном HHV-8 обнаруживается во всех элементах СК при всех стадиях заболевания независимо от клинического варианта.
Выделяют четыре типа СК:
— классический (идиопатический, спорадический, европейский);
— эндемический (африканский);
— эпидемический, связанный со СПИДом;
— иммунносупрессивный (ятрогенный, возникающий при проведении иммуносупрессивной терапии цитостатиками и иммунодепрессантами).
При классической (идиопатической) СК (С 46.0) на коже дистальных отделов нижних конечностей появляются одно- или двухсторонние синюшно-красные пятна диаметром 1-5 см с четкими границами, напоминающие гематому. Далее элементы медленно растут, трансформируясь в плотные узелки (при слиянии формируют бляшки) и узлы. Крупные узлы на нижних конечностях темнеют (из-за отложения гемосидерина) и изъязвляются, вызывая отторжение некротизированных тканей. По периферии узелков наблюдаются выраженные отеки с явлениями лимфостаза (в дальнейшем образуются участки фиброза).
Классическая СК обычно имеет доброкачественное течение, медленно распространяясь в проксимальном направлении; иногда пациенты могут жить с медленно прогрессирующей болезнью в течение десятков лет. Распространение высыпаний на другие участки тела, лимфатические узлы (С46.3), слизистую оболочку полости рта (С46.2) и гениталий, внутренние органы (часто с бессимптомным течением) (С46.7; С 46.8) происходит через 2-3 года. Летальный исход при классической СК чаще наступает от других причин, т.к. болезнь наблюдается у лиц пожилого возраста и заболевание развивается медленно.
Эндемическая (африканская) СК проявляется узловым, «цветистым», инфильтративным и лимфаденопатическим вариантами. «Цветистый», вегетирующий и инфильтративный варианты характеризуются более агрессивным течением с глубоким поражением дермы, подкожной клетчатки, мышц и костей. Лимфаденопатическая африканская СК преимущественно поражает детей и молодых людей и может иметь молниеносное течение с очень быстрым прогрессированием. Кожа и слизистые оболочки поражаются в меньшей степени.
Саркома Капоши, ассоциированная со СПИДом (эпидемический тип) (В21.0)
Для СК у больных СПИДом характерно быстрое течение с мультифокальным диссеминированием. Первичные проявления СК на лице отмечаются чаще на коже носа, век, ушных раковин, на туловище — вдоль линий наименьшего напряжения кожи. При отсутствии лечения диссеминированные элементы могут сливаться с образованием крупных бляшек, распространяющихся на кожу лица, туловища или конечностей, что нередко приводит к нарушениям функции органов.
Слизистая оболочка полости рта поражается у 10-15% больных. Наиболее типично расположение высыпаний в области твердого и мягкого неба и корня языка, где они быстро изъязвляются. Также часто наблюдается поражение глотки, которое может приводить к затруднению приема пищи, речи и дыхания. Кроме того, в воспалительный процесс вовлекаются лимфатические узлы, желудочно-кишечный тракт и легкие. Желудок и двенадцатиперстная кишка представляют собой места излюбленной локализации СК, и заболевание нередко сопровождается кровотечением и непроходимостью кишечника. При легочной форм СК могут наблюдаться респираторные симптомы: бронхоспазм, кашель и прогрессирующая дыхательная недостаточность.
Иммуносупрессивный тип СК чаще развивается после трансплантации внутренних органов и обусловлен ятрогенным воздействием иммуносупрессивных препаратов. Кожные проявления вначале имеют ограниченный характер, затем распространяются и напоминают высыпания при СПИД-ассоцированной СК. Снижение дозы или отмена иммуносупрессивных препаратов приводит к полному регрессу кожных и висцеральных проявлений СК у 24-80% больных, однако возобновление их применения ведет к рецидиву заболевания.
Диагностика СК основана на результатах физикального обследования (характерные клинические проявления на коже и слизистых оболочках).
Для верификации диагноза используют гистологическое исследование биоптатов кожи и идентификацию HHV-8 с помощью молекулярно-биологических методов исследования.
Учитывая высокую частоту ассоциации заболевания со СПИДом необходимо проведения серологического исследование на ВИЧ.
При морфологическом исследовании выделяют ангиоматозный, фибробластический и смешанный варианты СК. В пятнистых элементах определяется увеличение числа дермальных сосудов, окруженных эндотелиальными клетками, в прилегающих участках — отложения гемосидерина и экстравазальные эритроциты с умеренным периваскулярным инфильтратом. В бляшках при СК выявляется выраженная сосудистая пролиферация во всех структурах дермы, включая коллагеновые волокна. Характерным является наличие плотных тяжей и веретенообразных клеток между зазубренными сосудистыми клетками. В узлах больных СК определяются преимущественно веретеновидные клетки, участки ангиоматоза и плотные саркоматозные волокна. Воспалительный инфильтрат состоит из лимфоцитов, гистиоцитов и плазмоцитов.
В начальной стадии заболевания и при его локализованных формах необходимо проводить дифференциальную диагностику с гематомой, бактериальным ангиоматозом, пиогенной гранулемой, дифференцированной ангиосаркомой. В поздней стадии СК дифференциальная диагностика проводится с акроангиодерматитом (псевдосаркома Капоши типа Мали), бактериальным ангиоматозом. Поражения на слизистых оболочках полости рта и глотки дифференцируют с неходжкинской лимфомой, плоскоклеточным раком, бактериальным ангиоматозом.
Получить консультацию по медтуризму
— уменьшение выраженности симптомов и предотвращение прогрессирования заболевания;
— ремиссия опухоли;
— продление жизни и работоспособности больного;
— улучшение качества жизни пациента.
Общие замечания по терапии
Методы лечения саркомы Капоши зависят от клинической формы заболевания, размера поражений и вовлеченных в патологический процесс органов и/или систем.
Несмотря на огромное число данных в пользу того, что онкогенная герпес-вирусная инфекция, вызываемая HHV-8, играет в патогенезе саркомы Капоши центральную роль, применение специфических антигерпетических препаратов неэффективно!
Показания к госпитализации
Диссеминированные формы СК (в т.ч. с поражением внутренних органов)
Методы лечения
1. Локализованная форма СК
— хирургическое иссечение (А) [1];
— криодеструкция (А) [1];
— топические средства с 9-цис-ретиноевой кислотой (А) [1];
— лучевая терапия (А) [1].
2. Диссеминированные формы СК (в т.ч. с поражением внутренних органов)
Терапия классической СК
— липосомальный доксорубицин 20-40 мг/ м 2 каждые 2-4 недели, 6-8 введений на курс (А) [2]
— винбластин 6 мг внутривенно 1 раз в неделю. После достижения эффекта назначают поддерживающую дозу 0,15 мг/кг (каждые 7—14 дней до полного устранения симптомов). (В) [3]
— доксорубицин /блеомицин//винкристин 20-30 мг/м 2 // 1-2 мг каждые 2-4 недели до достижения эффекта (А) [1]
— интерферон -a 3-30 млн. ЕД. ежедневно внутривенно в течение 3 недель (В) [3].
Терапия СК, ассоциированной со СПИДом
начальная высокоактивная антиретровирусная терапия (А) [2]
При отсутствии эффекта – системная цитостатическая терапия (А) [2]Терапия СК у больных, получающих иммуносупрессивную терапию
— изменение схемы приема иммуносупрессивных препаратов (А) [2];
— липосомальный доксорубицин 20-40 мг/м 2 каждые 2-4 недели течение, 6-8 введений на курс (А) [2,4]
— паклитаксел 100мг/ м 2 каждые две недели течение до достижения эффекта под контролем лабораторных и функциональных показателей (А) [2,3,4]
Требования к результатам лечения
— предотвращение развития осложнений;
— клиническое выздоровление
ПРОФИЛАКТИКА
Особое внимание уделяется пациентам, получающим иммуносупрессивную терапию, с выявлением лиц, инфицированных HHV-8 и повышением их иммунного статуса.
Вторичная профилактика включает диспансерное наблюдение за больными в целях предотвращения рецидива заболевания, осложнений после лечения и их реабилитацию.
- Клинические рекомендации Российского общества дерматовенерологов и косметологов
- 1. Treatments for classic Kaposi sarcoma: A systematic review. Régnier-Rosencher E, Guillot B, Dupin N. J Am Acad Dermatol. 2013 Feb; 68(2):313-31. 2. Cianfrocca M, Lee S, Von Roenn J, Tulpule A, Dezube BJ, Aboulafia DM, et al. Randomized trial of paclitaxel versus pegylated liposomal doxorubicin for advanced human immunodeficiency virus-associated Kaposi sarcoma: evidence of symptom palliation from chemotherapy. Cancer. Aug 15 2010;116(16):3969-77. 3. Di Lorenzo G, Konstantinopoulos PA, Pantanowitz L, et al. Management of AIDS-related Kaposi’s sarcoma. Lancet Oncol. Feb 2008;8(2):167-76. 4. Brinkhof MW, Pujades-Rodriguez M, Egger M. Mortality of patients lost to follow-up in antiretroviral treatment programmes in resource-limited settings: systematic review and meta-analysis. PLoS One. 2009;13:e5790. doi: 10.1371.
Персональный состав рабочей группы по подготовке федеральных клинических рекомендаций по профилю «Дерматовенерология», раздел «Саркома Капоши»:
1. Дубенский Валерий Викторович – заведующий кафедрой дерматовенерологии ГБОУ ВПО «Тверская государственная медицинская академия» Минздрава России, доктор медицинских наук, профессор, г. Тверь
2. Дубенский Владислав Валерьевич — доцент кафедры дерматовенерологии ГБОУ ВПО «Тверская государственная медицинская академия» Минздрава России, кандидат медицинских наук, г. Тверь
МЕТОДОЛОГИЯ
Методы, использованные для сбора/селекции доказательств:
поиск в электронных базах данных.
Описание методов, использованных для сбора/селекции доказательств:
доказательной базой для рекомендаций являются публикации, вошедшие в Кокрановскую библиотеку, базы данных EMBASE и MEDLINE.
Методы, использованные для оценки качества и силы доказательств:
· Консенсус экспертов;
· Оценка значимости в соответствии с рейтинговой схемой (схема прилагается).
Рейтинговая схема для оценки силы рекомендаций:
| Уровни доказательств | Описание |
| 1++ | Мета-анализы высокого качества, систематические обзоры рандомизированных контролируемых исследований (РКИ) или РКИ с очень низким риском систематических ошибок |
| 1+ | Качественно проведенные мета-анализы, систематические, или РКИ с низким риском систематических ошибок |
| 1- | Мета-анализы, систематические, или РКИ с высоким риском систематических ошибок |
| 2++ | Высококачественные систематические обзоры исследований случай-контроль или когортных исследований. Высококачественные обзоры исследований случай-контроль или когортных исследований с очень низким риском эффектов смешивания или систематических ошибок и средней вероятностью причинной взаимосвязи |
| 2+ | Хорошо проведенные исследования случай-контроль или когортные исследования со средним риском эффектов смешивания или систематических ошибок и средней вероятностью причинной взаимосвязи |
| 2- | Исследования случай-контроль или когортные исследования с высоким риском эффектов смешивания или систематических ошибок и средней вероятностью причинной взаимосвязи |
| 3 | Неаналитические исследования (например: описания случаев, серий случаев) |
| 4 | Мнение экспертов |
Методы, использованные для анализа доказательств:
· Обзоры опубликованных мета-анализов;
· Систематические обзоры с таблицами доказательств.
Методы, использованные для формулирования рекомендаций:
Консенсус экспертов.
Рейтинговая схема для оценки силы рекомендаций:
| Сила | Описание |
| А | По меньшей мере один мета-анализ, систематический обзор или РКИ, оцененные как 1++ , напрямую применимые к целевой популяции и демонстрирующие устойчивость результатов или группа доказательств, включающая результаты исследований, оцененные как 1+, напрямую применимые к целевой популяции и демонстрирующие общую устойчивость результатов |
| В | Группа доказательств, включающая результаты исследований, оцененные как 2++, напрямую применимые к целевой популяции и демонстрирующие общую устойчивость результатов или экстраполированные доказательства из исследований, оцененных как 1++ или 1+ |
| С | Группа доказательств, включающая результаты исследований, оцененные как 2+, напрямую применимые к целевой популяции и демонстрирующие общую устойчивость результатов; или экстраполированные доказательства из исследований, оцененных как 2++ |
| D | Доказательства уровня 3 или 4; или экстраполированные доказательства из исследований, оцененных как 2+ |
Индикаторы доброкачественной практики (Good Practice Points – GPPs):
Рекомендуемая доброкачественная практика базируется на клиническом опыте членов рабочей группы по разработке рекомендаций.
Экономический анализ:
Анализ стоимости не проводился и публикации по фармакоэкономике не анализировались.
Метод валидизации рекомендаций:
· Внешняя экспертная оценка;
· Внутренняя экспертная оценка.
Описание метода валидизации рекомендаций:
Настоящие рекомендации в предварительной версии рецензированы независимыми экспертами.
Комментарии, полученные от экспертов, систематизированы и обсуждены членами рабочей группы. Вносимые в результате этого изменения в рекомендации регистрировались. Если же изменения не были внесены, то зарегистрированы причины отказа от внесения изменений.
Консультация и экспертная оценка:
Предварительная версия была выставлена для обсуждения на сайте ФГБУ «Государственный научный центр дерматовенерологии и косметологии» Минздрава России для того, чтобы лица, не участвующие в разработке рекомендаций, имели возможность принять участие в обсуждении и совершенствовании рекомендаций.
Рабочая группа:
Для окончательной редакции и контроля качества рекомендации повторно проанализированы членами рабочей группы.
Основные рекомендации:
Сила рекомендаций (A–D) приводится при изложении текста рекомендаций
источник
Саркома Капоши у ВИЧ-инфицированных пациентов развивается в 20 тысяч раз чаще всех остальных людей, даже при невирусном иммунном дефиците злокачественное поражение кожи встречается в 300 раз реже.
Вначале ВИЧ-эпидемии этот вариант ангиосаркомы поражал практически каждого третьего вирусоносителя, сегодня успехи противовирусной терапии втрое снизили заболеваемость и существенно изменили тяжесть злокачественного процесса.
Основное лечение саркомы — ВысокоАктивная АнтиретроВирусная Терапия или ВААРТ, при которой используется комбинация трёх-четырёх лекарственных средств. С противовирусных препаратов начинают лечение саркомы у ранее не подозревавших об инфекции и у регулярно проходивших специфическую терапию ВИЧ-инфицированных.
Появление саркомы Капоши у инфицированного манифестирует переход заболевания в терминальную стадию — СПИД, но оптимально подобранная ВААРТ способна существенно уменьшить саркоматозные очаги и привести к длительной ремиссии злокачественного процесса.
Изначально злокачественный процесс имеет распространённый характер, что проявляется образованием опухолевых очагов на обширных участках кожи и нередко во внутренних органах. Даже у не инфицированных ВИЧ этот вариант ангиосаркомы в редких случаях подлежит хирургическому лечению из-за почти 100% вероятности рецидива и многоочаговом поражении.
Тем не менее, при ограниченных очаговых поражениях кожи хирургическая операция может сочетаться с лучевой терапией операционного поля, и обязательно комбинируется с системным лекарственным воздействием — химиотерапией. Нередко хирургическое вмешательство дополняется локальной деструкцией остаточных очагов жидким азотом — криодеструкцией.
У большинства пациентов со СПИД технически невозможно радикальное хирургическое вмешательство.
Химиотерапия у больных СПИД чревата серьёзными осложнениями, поскольку на фоне значительного снижения иммунитета активизируются даже не патогенные для человека микроорганизмы. Как правило СПИД протекает с постоянным воспалением той или иной природы, чаще грибковым и пневмоцистным, генерализацией вирусов группы герпеса, что требует применения высоких доз антибиотиков и других противовоспалительных лекарственных препаратов.
- если у больного больше 25 опухолевых образований в коже;
- при выявлении злокачественного опухолевого поражения внутренних органов и сосудов;
- при наличии симптомов «раковой интоксикации» в виде повышения температуры тела, профузных ночных потов, за короткий период снижением более 10% веса;
- при отсутствии реакции на 3-месячную ВААРТ;
- при продолжающемся прогрессировании злокачественного процесса на фоне ВААРТ;
- при сочетании саркоматозных очагов с лимфатическим отёком тканей, что чаще всего развивается на конечностях.
На первом этапе применяют наиболее эффективные цитостатики с меньшей вероятностью тяжёлых осложнений — это заключённые в специальные микрокапсулы антрациклиновые антибитики доксорубицин или даунорубицин. При чувствительной к цитостатикам опухоли достаточно бывает 6 курсов с введениями через две-три недели.
Оба препарата агрессивно действуют на миокард и клетки крови, но за счёт липосомальной формы эти побочные реакции менее выражены, чем у обычных форм цитостатиков.
При неэффективности первой линии — продолжающемся росте саркоматозных элементов — пациента переводят на паклитаксел, имеющий схожий спектр токсичности, но с более интенсивными проявлениями. Препарат вводится по с предварительной подготовкой каждые 2-3 недели, число курсов определяется эффектом.
При отсутствии результата от второй линии химиотерапии остаётся альтернатива в виде курсов препаратами других групп, в том числе в сочетании с глюкокортикоидами, в отечественной практике часто используют избирательно накапливающийся в коже препарат из «советского прошлого» проспидин.
С больными злокачественными новообразованиями ВИЧ-инфицированными пациентами проведено очень мало клинических исследований, как правило, только наблюдательные, то есть без подбора сравниваемых групп. Анализ эффективности при наблюдательных исследованиях грешит невысокой достоверностью.
Научное онкологическое сообщество рекомендует проводить ВИЧ-инфицированным больным с раком стандартное лечение, не выделяя их в особую группу.
При всех иных, не ассоциированных с ВИЧ/СПИД, вариантах саркомы Капоши дополнительно к ВААРТ возможно проведение иммунной терапии интерферонами. С оптимальными дозами и стандартными режимами до настоящего времени не определились, но известно, что на результате лечения сказывается численность популяции СД4-лимфоцитов. При традиционном для СПИД содержании менее 200 клеток в миллилитре крови позитивный результат от применения пегилированного интерферона возможен только у каждого десятого пациента.
Клетки саркомы Капоши реагируют на лучевое воздействие, поэтому дистанционная лучевая терапия или рентгенотерапия активно используются, ограничивает их применение только большая площадь поражения.
Хороший результат достигается при введении внутрь опухолевого узла цитостатиков растительного происхождения — алкалоидов барвинка розового.
В литературе имеются указания на позитивный эффект при локальном использовании ретиноидов, а также ударно-волновой терапии на очаги поражения и даже компрессионного трикотажа при развитии опухоли на фоне лимфатического отёка конечности.
Прогноз зависит не только от обширности опухолевого поражения, но в первую очередь, от состояния иммунитета — от количества СД4-лимфоцитов. Нередко эффективная ВААРТ — быстро повышающая численность колонии иммунных клеток, способна контролировать течение саркомы Капоши и привести к ремиссии.
В обязательном порядке СПИД-больным проводится активная сопроводительная терапия, снижающая токсические проявления химиотерапии. После курса лечения необходима реабилитация для быстрейшего восстановления и предотвращения неблагоприятно сказывающегося на результате редуцирования доз и увеличения интервалов последующих курсов.
Течение СПИД сопровождается инфекционными и воспалительными процессами, для купирования которых разработаны стандартные лекарственные режимы, корректируемые в соответствии с особенностями пациента.
Главное для больного — найти не просто хорошего доктора, для лечения СПИД этого недостаточно. Для борьбы с саркомой Капоши, развивающейся на фоне ВИЧ, требуется команда специалистов, владеющих всем спектром оптимальных для пациента методик.
источник
Изобретение относится к области медицины и может быть использовано в дерматологии и онкологии. В способе диагностики саркомы Капоши, включающем микроскопическое исследование биоптата очага поражения, предложено исследовать биоптат в полимеразной цепной реакции (ПЦР) на наличие ДНК-последовательностей вируса герпеса человека 8-го типа. Дополнительно исследуют сыворотку крови методом непрямой иммунофлюоресценции (НИФ) при стандартных сериях разведения на наличие антител класса IgG к вирусу герпеса человека 8-го типа. При положительном значении ПЦР и любом показании НИФ, а также отрицательном значении ПЦР и положительном показании НИФ в разведении 1:120 и выше диагностируют саркому Капоши. Преимущество изобретения заключается в повышении точности диагностики на ранних стадиях заболевания.
Изобретение относится к области медицины и может быть использовано в дерматологии и онкологии.
Известен способ диагностики саркомы Капоши (СК), включающий микроскопическое исследование патоморфологического строения биоптата очага поражения (Казанцева И.А. Саркома Капоши: этиология, патогенез, гистогенез, патоморфологическая диагностика. Рос. Ж-л кожных и венерических болезней. №1, 1998 г., с.6-9, прототип). Для выявления характерных гистологических признаков размер биоптата обычно составляет в диаметре не менее 1 см, о результатах исследования судят по наличию веретенообразных клеток, диффузной сосудистой пролиферации и иммуноклеточного инфильтрата. При невыявлении типичных гистологических признаков проводят иммуногистохимическое исследование биоптата.
Недостатком этого способа является сложность установления диагноза на ранних стадиях заболевания, в случаях ангиоматозного варианта саркомы Капоши, в случаях инвалюцирующих элементов и при проведении дифференциального диагноза с группой сосудистых пролифераций (псевдосаркома Капоши, кавернозная гемангиома и т.д.). Способ травматичен, при иммуногистохимическом исследовании требует дорогостоящих реактивов.
Задачей настоящего изобретения является устранение указанных недостатков за счет выявления маркеров этиологического агента саркомы Капоши, которые позволяют более точно и в ранние сроки установить диагноз и проводить его при всех вариантах гистологического строения элементов заболевания.
Для этого в способе диагностики саркомы Капоши, включающем микроскопическое исследование биоптата очага поражения, предложено исследовать биоптат в полимеразной цепной реакции (ПНР) на наличие ДНК-последовательностей вируса герпеса человека 8-го типа и дополнительно исследовать сыворотку крови методом непрямой иммунофлюоресценции (НИФ) при стандартных сериях разведения на наличие антител класса IgG к вирусу герпеса человека 8-го типа и при положительном значении ПЦР и любом показании НИФ, а также отрицательном значении ПЦР и положительном показании НИФ в разведении 1:120 и выше диагностировать саркому Капоши.
Совокупность предлагаемых исследований позволяет значительно повысить точность диагностики как на ранних стадиях саркомы Капоши, так и в случаях, сложных для патоморфологической верификации диагноза.
Осуществление способа показано на конкретных клинических примерах.
Больной Ж., 68 лет, болен с 62-летнего возраста, когда на коже правой стопы заметил появление пятна красного цвета размером 0,3х0,5 см, не сопровождавшегося субъективными ощущениями. В течение года пятно увеличивалось в размере, появились новые очаги на левой голени, затем процесс распространился на стопы. Через три года после начала заболевания на коже левой голени стали появляться узелки полушаровидной формы красно-коричневого цвета. При поступлении: патологический процесс симметричный, представлен красно-синюшными пятнами и бляшками неправильной формы размером от 1

При гистологическом исследовании узелкового элемента: элемент опухоли представлен тонкостенными сосудистыми полостями, разделенными соединительно-тканными прослойками, располагающимися в ретикулярной дерме ассоциирующимися с придатками кожи и предсуществующими кровеносными сосудами. Сосудистые пространства заполнены эритроцитами.
Заключение: данные гистологического исследования не противоречат диагнозу саркомы Капоши, но подобные изменения могут наблюдаться и при кавернозной гемангиоме.
Для последующей верификации диагноза было проведено исследование биоптата очага поражения: выявление в образцах ДНК последовательностей вируса герпеса человека 8-го типа (предполагаемого этиологического агента саркомы Капоши) размером 233 п.н. проводили в ПЦР с использованием специфических праймеров KS 330233 (5′-AGCCGAAAGGANNCCACCAT-3′ и 5′-TCCGTGTGTCTACGTCCAG-3′). ПЦР ставили в термосайклере РТС-200 фирмы MJ Research, Inc. Кроме того, сыворотка крови больного была исследована в реакции непрямой иммунофлюоресценции (нИФ) на наличие антител класса IgG к вирусу герпеса человека 8-го типа с определением их титра. Для исследования использовали клетки линии BCBL, продуктивно инфицированные этим вирусом. Реакцию нИФ ставили по методу Henle и Henle. Для чтения реакции использовали люминесцентный микроскоп фирмы “Орton” (Германия). Присутствие антител в исследуемой сыворотке определяли по ярко-зеленому свечению клеток на фоне негативных клеток, окрашенных в красновато-коричневый цвет. Титром сыворотки считали последнее разведение, дававшее свечение не менее 0,5% слабо светящихся клеток в препарате.
В результате проведенных исследований биоптата был получен ПЦР-положительный сигнал, в сыворотке крови обнаружены вирус-специфические антитела в титре 1:320.
На основании проведенных исследований больному был установлен диагноз идиопатического типа СК и проведена специфическая противоопухолевая терапия, позволившая добиться ремиссии патологического процесса.
Больной Т., 72 лет, болен с 66-летнего возраста, когда отметил развитие плотного отека в области левой стопы и левого голеностопного сустава. В течение последующего года отек нарастал, появилось ограничение подвижности левого голеностопного сустава, в связи с чем обратился к хирургу по месту жительства. Получал местное лечение гелем троксевазина, компрессами с 30% ДМСО, но существенного эффекта не было. Через 3 года после начала заболевания отметил появление синюшных пятен неправильной формы размером от 0,3

При поступлении на фоне отеков стоп и нижней трети левой голени имеются множественные пятна и бляшки синюшно-буроватой окраски с четкими границами диаметром от 2 до 5 см. На поверхности бляшек выражен гиперкератоз. При ультразвуковом обследовании внутренних органов патологии не выявлено.
При гистологическом исследовании биоптата очага поражения была выявлена диффузная пролиферация капилляров вокруг предсуществующих сосудов. При иммуногистохимическом исследовании выраженная экспрессия CD31. Заключение: изменения могут соответствовать саркоме Капоши или псевдосаркоме Капоши.
При исследовании биоптата очага поражения в ПЦР получен ПЦР-отрицательный сигнал; при исследовании сыворотки крови в нИФ выявлены вирус-специфические антитела в титре 1:640.
На основании данных молекулярно-биологического исследования больному установлен диагноз саркомы Капоши и проведено специфическое лечение, позволившее добиться выраженного клинического эффекта.
Больной К., 63 лет, болен с 53-летнего возраста, когда на коже правой стопы заметил появление пятна красного цвета диаметром около 1,0 см, без субъективных ощущений. В течение последующих трех лет процесс медленно прогрессировал: пятно увеличивалось в размере, появились плотный отек правой стопы и новые пятна на левой стопе и в области голеностопных суставов. Через шесть лет после начала заболевания на коже левой стопы впервые заметил возвышающиеся над уровнем кожи бляшки. Через 8 лет после начала заболевания обратился в клинику дерматовенерологии и дерматоонкологии МОНИКИ.
При поступлении патологический процесс распространенный и симметричный, был представлен красно-фиолетовыми пятнами и бляшками неправильных очертаний размером от 1

При ультразвуковом обследовании внутренних органов патологии не выявлено.
Клинический диагноз: саркома Капоши, идиопатический тип, хроническая форма.
При гистологическом исследовании биоптата очага поражения была выявлена диффузная пролиферация капилляров, не позволяющая установить нозологический диагноз.
При исследовании биоптата очага поражения в ПЦР получен ПЦР-положительный сигнал; при исследовании сыворотки крови в нИФ вирус-специфические антитела не выявлены.
На основании данных молекулярно-биологического исследования больному установлен диагноз саркомы Капоши и проведено специфическое лечение, позволившее добиться выраженного клинического эффекта.
Больной X., 32 лет, обратился в клинику дерматовенерологии и дерматоонкологии МОНИКИ с жалобами на множественные высыпания в области нижних конечностей. Болен около 2 лет, со времени появления на своде стопы пятна красного цвета размером 0,7 см, субъективно не беспокоившего больного. В течение 3 последующих месяцев такие же пятна появились в области обеих стоп и голеней. К врачу не обращался, ни чем не лечился. В дальнейшем размер очагов медленно увеличивался.
При осмотре кожные покровы бледные. Патологический процесс распространенный с локализацией на стопах и голенях представлен пятнами размером от 2

При ультразвуковом обследовании внутренних органов патологии не выявлено. Клинический диагноз: саркома Капоши, идиопатический тип, хроническая форма.
При гистологическом исследовании биоптата очага поражения: разветвленная сеть капилляров в верхней части дермы с бледноокрашенным эндотелием обычного вида. Вокруг скоплений новообразованных капилляров незначительный инфильтрат из лимфоцитов. Заключение: процесс необходимо дифференцировать между саркомой Капоши и псевдосаркомой Капоши.
При исследовании биоптата очага поражения в ПНР получен ПЦР-отрицательный сигнал; при исследовании сыворотки крови в нИФ вирус-специфические антитела не выявлены.
На основании данных молекулярно-биологического исследования больному установлен диагноз псевдосаркомы Капоши. Дальнейшее лечение по поводу сопутствующей артериовенозной недостаточности привело к полному разрешению высыпаний.
Предлагаемый способ позволяет устанавливать диагноз на ранних стадиях заболевания, что повышает эффективность лечения и уменьшает время его проведения, снижает вероятность диагностических ошибок.
Способ диагностики саркомы Капоши, включающий микроскопическое исследование биоптата очага поражения, отличающийся тем, что исследуют биоптат в полимеразной цепной реакции (ПЦР) на наличие ДНК-последовательностей вируса герпеса человека 8-го типа и дополнительно исследуют сыворотку крови методом непрямой иммунофлюоресценции (нИФ) при стандартных сериях разведения на наличие антител класса IgG к вирусу герпеса человека 8-го типа и при положительном значении ПЦР и любом показании нИФ, а также при отрицательном значении ПЦР и положительном показании нИФ в разведении 1:120 и выше диагностируют саркому Капоши.
источник