Множественная миелома — это злокачественное заболевание плазматических клеток (плазмоцитов), являющихся конечным продуктом дифференцировки B-лимфоцита.
Плазмоциты — основные клетки в организме, которые отвечают за продукцию антител (иммуноглобулинов), защищающие его от инфекций.
Как осуществляется диагностика множественной миеломы? Какие лабораторные анализы и методы инструментального обследования назначают врачи при данной патологии?
Злокачественные клетки миеломы оккупируют костный мозг и вытесняют нормальные клетки.
Обычно плазмоциты продуцируются по мере необходимости. Когда организм сталкиваются с болезнетворными бактериями или вирусом, некоторые B-лимфоциты созревают до плазматических клеток, которые начинают вырабатывать антитела. Небольшое количество плазмоцитов содержится в костном мозге, лимфоидной ткани (например, в лимфоузлах) и дыхательных путях.
Когда плазматическая клетка перерождается в злокачественную, она начинает бесконтрольно делиться, создавая многочисленное число копий — клонов, которые формируют в костном мозге опухоли. Бесконтрольно размножаясь, злокачественные клетки вытесняют нормальные клетки костного мозга. Также эти новообразования разрушают кость, появляются литические поражения костной ткани — характерный клинический признак миеломы.
В зависимости от количества присутствующих опухолей, заболевание подразделяют на:
- солитарную плазмоцитому — одиночная опухоль образуется в кости или в другом органе,
- множественную миелому — в кости возникает более одной опухоли и в других органах.
Поскольку злокачественные плазмоциты при миеломе клонируются из одной и той же клетки, все они продуцируют одинаковые антитела, называемые аномальными моноклональными иммуноглобулинами (М-протеин), которые выявляются в крови, а иногда и в моче.
Выделяют 5 классов иммуноглобулинов: IgG, IgA, IgM, IgD и IgE. Каждый из них состоит из четырех белковых цепей — двух одинаковых тяжелых (длинных) и двух одинаковых легких (более коротких).
- Существует пять отдельных типов тяжелых цепей, различающихся аминокислотными последовательностями, которые соответствуют своему классу иммуноглобулина: гамма — IgG, мю — IgM, альфа — IgA, дельта — IgD и эпсилон — IgE.
- И два типа легких цепей, которые общие для всех классов иммуноглобулинов, называемые каппа и лямбда.
Внутри плазматической клетки две тяжелые цепи одного типа и две легкие цепи также одного типа формируют молекулу иммуноглобулина. Миеломная клетка синтезирует только один класс иммуноглобулина.
Y-образные синего цвета иммуноглобулины представляют собой M-протеин.
У пациентов с множественной миеломой злокачественные клетки продуцируют только один класс иммуноглобулина в больших количествах и / или продуцируют в избытке только одну из легких цепей или редко тяжелую цепь. Эти одинаковые иммуноглобулины или легкие цепи называются моноклональным белком (а также М-протеин, миеломным белком, парапротеином, или пиком протеина).
Выделяют несколько вариантов миелом, каждый из которых соответствует классу иммуноглобулина или легкой цепи.
- Иммуноглобулин-продуцирующие миеломы — чаще всего встречаются IgG и IgA-миеломы, вариант IgG встречается в 60% случаев, а на IgA-миелому приходится около 20%. Варианты IgE и IgD-миеломы встречаются редко.
- Продуцирующие легкие цепи миеломы — вариант, при котором производится чрезмерное количество только легких цепей. На него приходится до 20% случаев. М-протеин, который обнаруживается при данном варианте, называют протеин Бенс-Джонса. Этот белок в большом количестве попадает в кровоток. Из-за того, что это относительно небольшая молекула, белок свободно фильтруется почками. Поэтому в крови его выявляют в малых количествах, а в моче — много.
Мониторинг моноклональных антител — важный компонент эффективного лечения при меланоме.
Лабораторные исследования назначаются при меланоме для того, чтобы диагностировать заболевание, определить его тяжесть и распространение, выявлять осложнения по мере их возникновения и контролировать эффективность лечения.
Нет ни одного анализа, который мог бы “в одиночку установить” диагноз. При постановке диагноза врач руководствуется субъективными жалобами больного, анамнезом (история болезни), осмотром больного, результатами лабораторных анализов и / или методов медицинской визуализации (компьютерная томография, МРТ и др.).
Врач может заподозрить множественную миелому по характерным изменениям для данного заболевания в биохимическом и общем анализе крови.
- Увеличение общего белка.
- Повышение уровня кальция.
- Лейкопения (низкое содержание белый кровяных телец) или эритропения (низкое содержание эритроцитов).
- Умеренное или значительное повышение количества протеина в моче.
Такие результаты анализов позволяют заподозрить болезнь, но не являются диагностическими для миеломы, поскольку аналогичные изменения наблюдаются и при других заболеваниях. Они указывают на необходимость проведение дальнейшего диагностического поиска. Для этого врач назначает следующие лабораторные тесты:
- Электрофорез белков сыворотки и иммунофиксация. Анализ используется при постановке диагноза, а также для контроля течения болезни. Он позволяет выявить моноклональные парапротеины в сыворотке и других биологических жидкостях. С помощью электрофореза белки разделяют на фракции в зависимости от их электрического заряда и размера. У большинства людей (до 80%) с множественной миеломой большое количество аномального иммуноглобулина приводит к появлению М-градиента на протеинограмме, также известного как пик М. Также может значительно уменьшаться количество нормальных иммуноглобулинов. Электрофорез с иммунофиксацией проводится для идентификации конкретного типа белка, который вырабатывается злокачественными клетками. Количество этого белка может меняться в течении болезни, но его тип останется неизменным.
- Определение легкой цепи (протеина Бенс-Джонса) в моче. У некоторых людей с множественной миеломой определяется данным протеин в моче. Как правило, исследование предусматривает 24-часовой сбор мочи. Определение легкой цепи (каппа и лямбда) помогает при постановке диагноза, а также оценить эффективность проводимого лечения.
- Свободные легкие цепи иммуноглобулинов в сыворотке крови. Тест измеряет количество свободных легких цепей в крови. Даже у здорового человека (по неизвестным причинам) плазматические клетки вырабатывают избыток легких цепей по сравнению с тяжелыми, и это приводит к тому, что небольшое количество из них не участвует в формировании иммуноглобулинов. Они остаются свободными легкими цепями и попадают в кровоток. У людей с множественной миеломой наблюдается чрезмерное производство либо каппа, либо лямбда легких цепей. Определение отношения каппа и лямбда легких цепей является чувствительным индикатором этого заболевания. Анализ используется при постановки диагноза, а также для выявления прогрессирования заболевания и определения эффективности проводимого лечения.
- Количественное определение иммуноглобулинов. Анализ определяет количество разных классов иммуноглобулинов. Анализ на IgG, IgA и IgM назначают при постановки диагноза и с целью мониторинга болезни. Обратите внимание, что тест не определяет аномальный иммуноглобулин, вырабатываемый клетками миеломы.
- Аспирационная или трепан-биопсия костного мозга. Множественная миелома — болезнь костного мозга. Без проведения этого анализа невозможно определить, сколько злокачественных плазматических клеток присутствует в костном мозге, и оценить, как они влияют на развитие нормальных лейкоцитов, эритроцитов и тромбоцитов.
- Цитогенетический анализ. Исследование включает кариотипирование и флуоресцентную гибридизацию in situ (FISH), клетки оценивают под микроскопом с целью поиска аномальных хромосом. Аномалии, такие как транслокация хромосом (перенос участка хромосомы на негомологичную хромосому) или делеция (потеря участка хромосомы), наблюдаются при множественной миеломе. Обнаружение этих аномалий дает возможность спрогнозировать течение заболевания.
Как правило, следующие лабораторные анализы назначаются при постановки диагноза, а также для отслеживания течения заболевания и выявление осложнений:
Комплексная метаболическая панель, группа тестов, используемых для оценки функции почек и других органов, состояния электролитного баланса, определения уровня кальция, альбумина и общего белка.
- Развернутый анализ крови, с помощью его оценивают клеточный состав крови (лейкоциты, эритроциты и тромбоциты) и определяют степень тяжести анемии (измеряют гемоглобин).
- Содержания в крови мочевой кислоты. Повышение ее уровня указывает на неблагоприятное течение заболевания.
- Бета-2-микроглобулин, белок расположенный на поверхности плазматических клеток; повышение уровня может указывать на ухудшение прогноза; этот анализ используется при постановке диагноза.
- Вязкость сыворотки крови определяется по отношению к вязкости воды, и зависит от содержания белков в плазме крови; когда уровни аномального белка становятся очень высокими, вязкость сыворотки увеличиваться, появляется симптоматика «густой крови».
- Рентгенологическое исследование костей помогают оценить стадию процесса и проводить мониторинг течения заболевания. С помощью обычного рентгена выявляют очаги литического повреждения кости, определять их размеры, он помогает прогнозировать угрозу возникновения патологического перелома.
- МРТ (магнитно-резонансная томография) считается более информативной, чем обычные рентгеновские снимки при оценке разрушения кости.
- КТ (компьютерная томография) / ПЭТ (позитронно-эмиссионная томография) использоваться для поиска опухолей в случае, если в результате обычного рентгенологического исследования костных поражений не были выявлены при наличии болевого синдрома.
Стадирование помогает прогнозировать течение заболевания, разработать индивидуальный план мониторинга и лечения. Для этого используют следующие параметры:
- Количество аномального иммуноглобулина.
- Содержание кальция в крови.
- Степень и тяжесть повреждения костей.
- Степень тяжести анемии.
Существуют различные системы стадирование множественной миеломы, позволяющие оценить количество присутствующей опухолевой массы и дисфункцию органов. Анализ на бета-2 микроглобулина и содержание альбумина в крови, особенно важны при постановке диагноза миеломы.
Заметили ошибку? Выделите ее и нажмите Ctrl+Enter, чтобы сообщить нам.
источник
МИЕЛОМА, МНОЖЕСТВЕННАЯ МИЕЛОМА, МИЕЛОМНАЯ БОЛЕЗНЬ, СЕКРЕТИРУЮЩАЯ ЛИМФОМА, ПЛАЗМАЦИТОМА, БОЛЕЗНЬ РУСТИЦКОГО и т.д. – все это синонимы одного заболевания, которое обусловлено неконтролируемым ростом плазматических клеток, продуцируемым костным мозгом. Плазматические клетки, в свою очередь, являются конечной стадией дифференциации В-лимфоцитов – основного звена клеточно-гуморального иммунитета, основная функция которых – продукция иммунных белков – иммуноглобулинов IgG, IgA, IgM, IgE, IgD, участвующих в гуморальном иммунитете. Поэтому в норме костный мозг всегда содержит некоторое количество плазматических клеток. Однако, в случае их неконтролируемого роста увеличение количества плазматических клеток приводит к их сосредоточению в виде плазмацитомы в костном мозге, особенно в позвоночном столбе, тазовых костях, ребрах, плоских костях черепа, головках тазобедренных суставов, в результате чего нормальная костная ткань и костный мозг разрушаются. Очаги деструкции видны при рентгеновском исследовании, но, к сожалению, разрешающая способность рентгена позволяет выявить разрежение костной ткани, если порядка 30% ее уже разрушено. Миеломные клетки продуцируют иммуноглобулин одного вида (моноклональный), который при специфическом электрофоретическом исследовании сыворотки крови и мочи проявляется пиком, называемым М-градиентом, где М — означает моноклональный или миеломный. Отсюда происходит название болезни – миелома. Моноклональные белки (протеины), продуцируемые миеломными клетками, имеют измененную структуру, не выполняют функций иммунитета и называются «парапротеинами». Иногда они теряют какую-то свою часть и могут продуцироваться только моноклональные легкие цепи (белок Бенс-Джонса), или моноклональные тяжелые цепи.
(ДИАГНОСТИКУ МИЕЛОМНОЙ БОЛЕЗНИ СМ. ВНИЗУ СТРАНИЦЫ)
* — скидка 3% при оформлении заказа на сайте
Неконтролируемый рост плазматических клеток приводит к множеству тяжелых последствий, из которых наиболее характерные:
- Разрушение костной ткани скелета;
- Нарушения кроветворения в костном мозг;
- Увеличение вязкости крови из-за большого количества парапротеинов;
- Снижение иммунитета из-за подавления продукции нормальных иммуноглобулинов;
- Развитие почечной недостаточности из-за оседания нарушений в почечных клубочках и канальцах;
Миеломная болезнь может развиваться долгое время бессимптомно, но становится понятным, почему одними из первых характерных клинических симптомов Миеломы являются:
- Боли различной интенсивности в нижней части спины, ребрах или других участках скелета;
- Анемия, сопровождающаяся одышкой, слабостью, потерей зрения, болями в области сердца;
- В крови наблюдается повышенное СОЭ;
- Повышение содержания кальция в крови и моче из-за разрушения костной ткани;
- Появляется белок в моче, что приводит к серьезным нарушениям функции почек, особенно опасно появление белка Бенс-Джонса.
Понятно и то, что из-за незнания о существовании такого заболевания пациент идет к врачам другого профиля и часто теряет драгоценное время из-за отсутствия целенаправленного и компетентного обследования. Диагностика миеломной болезни зачастую проводится уже в последнюю очередь. Что еще хуже, с проблемами в костной ткани часто больные приходят к мануальным терапевтам, не зная, что миелома – это прямое противопоказание для мануальных процедур.
При наличии одного или нескольких из перечисленных выше симптомов абсолютно необходимо обследоваться в специализированной лаборатории для исключения миеломы, поскольку раннее выявление гарантирует успешное лечение. Следует помнить, что диагноз Миеломы не может быть установлен без результатов иммунохимической диагностики крови и мочи. Своевременная диагностика миеломной болезни – залог вашего выздоровления.
Если же диагностирована множественная миелома, то для пациентов с таким диагнозом нормальным поведением является систематическое рациональное обследование и определение прогностических факторов (бета2-микроглобулин в сыворотке крови и в моче, СРБ, белок Бенс-Джонса в моче, тип парапротеина), чтобы судить о развитии миеломы, ее агрессивности и контролировать эффективность выбранной схемы лечения. Такой контроль необходимо осуществлять не реже, чем 1 раз в 3 месяца во время лечения и 1 раз в 6-12 месяцев при стойкой ремиссии.
Пациенты должны также знать о том, что специализированная иммунохимическая диагностика Миеломы осуществляется только в трех медицинских учреждениях страны, одним из которых является «Иммунотест» — автор основных патентов и методик в этой области, постоянно обновляющий диагностическую базу современными методами, что создает оптимистичное будущее для больных Миеломой. Лечение миеломной болезни – это вполне реально, и шансы на выздоровление очень высоки, особенно на ранних стадиях. Успешное лечение миеломной болезни также во многом зависит от профессионализма лечащего врача, который, исходя из своих знаний и опыта, может прописать или порекомендовать действительно эффективное средство. Множественная миелома – это не приговор!
источник
Анализ периферической крови показывает, у большинства больных с множественной миеломой, наличие анемии. Эта анемия, обычно умеренная, гипохромного типа может быть иногда сильно выраженной (менее 1 миллиона гематий/мм3). На мазке наблюдаются аспекты анизоцитоза и пойкилоцитоза. Гематии проявляют часто тенденцию располагаться в виде «монетных столбиков»,—явление, связанное с наличием миеломатозных протеинов в сыворотке и с их скоплением на поверхности гематий. Количество Гб также понижено.
Число лейкоцитов, вариабильное, нормальное или повышенное. В развитых стадиях болезни можно наблюдать лейкопении, отягощаемые и применяемыми цитостатическими лечениями. Лейкоцитарная формула, обычно нехарактерная, может показывать иногда повышенное число плазмоцитарных элементов, подобных клеткам в костном мозге.
Число тромбоцитов нормальное или умеренно пониженное.
Исследование костного мозга при множественной миеломе имеет важнейшее значение для постановки диагноза. Костная пункция производится обычно в грудную кость или в подвздошный гребень, но ее можно производить и в другие затронутые кости: позвонки, пяточную кость, ключицу. Иногда проникание в кость происходит очень легко, костная ткань давая ощущение особой хрупкости.
Для миеломы характерен численный рост плазмоцитарной серии, которая может составлять 90% клеточного населения костного мозга. Вообще, при 20% плазмоцитарных элементов ставится вопрос о существовании миеломы. Аномалийные плазмоцитарные элементы или так называемые «миеломатозные клетки», это клетки диаметром в 15—30(л, круглые или овальные. Ядро, диаметром в 5—7у., круглое, расположенное эксцентрично, содержит 1—2 нуклеоли. Нуклеарный хроматин менее комковатый и уже не представляет тот регулярный порядок, который наблюдается в нормальном плазмоците. Цитоплазма этих клеток интенсивно базофильная, становится яркосиней при окрашивании May-Grunwald-Giemsa (цветная вклейка III).
В цитоплазме миеломатозных клеток можно встретить гиалиновые шарики (тела Russel), многочисленные вакуоли, придающие клетке вид ежевики (клетки Mott), или хрустальные азурофильные включения иногда подобные телам Auer при миелобластической лейкемии (протеиновые кристаллы) (цветная вклейка III).
Вариабильное число клеток может иметь 3 или более ядер. Другие имеют сильно выраженные черты незрелости: они более крупных размеров (20—35u) с болыпдм, круглым ядром, с очень тонким хроматином, а цитоплазма интенсивно базофильная. Встречаются также и несколько зрелых плазмоцитарных клеток, с ядром в виде «колесной спицы » и ясной перинуклеарной зоной. Иногда плазмоциты могут иметь ацидофильную цитоплазму, так называемые «пламенистые клетки » (flaming cells) (цветная вклейка III).
С цитохимической точки зрения, цитоплазма миеломатозных клеток является пероксидазо-отрицательной и окрашивается метахроматически с метиловой зеленью. Гиалиновые шарики (тела Russel) обычно PAS-положительные.
Миеломатозные клетки преставляют множество нуклеоцитоплазматических асинхронизмов созревания. Согласно Bernier и Graham, степень этих асинхронизмов пропорциональна клиническому распространению заболевания.
Исследования при помощи электронного микроскопа показали наличие определенных аномалий на уровне клеточных органитов, аномалии тем более явные, чем менее дифференцирована миеломатозная клетка. Митохондрии численно увеличены и имеют патологические аспекты: удлиненные, кольцевидные, иногда с чертами миелиновой дегенерации; аппарат Гольджи везикулярнио трансформирован, центриоли имеют гигантский удлиненный вид, а число рибозомов может возрастать (Bessis). Наиболее интересный аспект представляет эргастоплазмический аппарат. В большинстве случаев он расширен и имеет везикулярный вид.
Содержимое эргастоплазмических везикул состоит из протеина и имеет твердую консистенцию, принимая аспект тел Russel, либо в растворимой форме, flaming cells или тезауроцотив (Paraskevas и сотр.), либо в кристаллизованной форме.
Протеиновые кристаллы бирефрингентные с периодичностью около 110 A (Bessis). В других случаях эргатоплазмический аппарат менее развит и представлен несколькими пластинками, а редко бывает плохо развитым, подобным лимфоидной клетке. На уровне ядра появляются аномалийные, гипертрофированные нуклеоли, а также и множество интрануклеарных вакуолей (Smetena и сотр.). Некоторые авторы описали наличие в ядре вирусных телец, в 15% случаев (Sorensen), тельца, которые Bessis нашел лишь в одном из 12 изученных им случаев.
Иммунохимические и иммунофлюоресцентные исследования, с разными специфическими антисыворотками (IgG, IgA, IgM, IgD IgE, ламбда, каппа) показали наличие Ig в цитоплазме миеломатозных клеток. Они локализированы в особенности на уровне эргастоплазмического аппарата и рибозомов. Делались попытки установить связь между морфологическим аспектом клеток и типом секретированного Ig. Полученные до настоящего времени результаты неубедительны. Paraskevas и сотр. утверждают, что пламенистые клетки секретируют IgA.
Цитогенетическое исследование множественной миеломы показало существование разных форм анейплоидии, но которые наблюдаются не во всех случаях. Кроме этого кыло описано и присутствие различных хромозомов маркеров. Вследствие внедрения метода бандирования, Liang и Rowley нашли хромозом 14р+ у 3 больных с множественной миеломой и 1 больного с плазмоцитарной лейкемией, из 22 изученных больных. Этот хромозом 14q+ был найден и при других лимфомах типа Б, а также, изредка, и при лимфомах non-Б. Следует отметить, что Croce и сотрудники установили, что структуральные гены для тяжелых цепей Ig локализированы у человека на хромозоме 14.
Исследование протеинового обмена при множественной миеломе. Расстройства протеинового метаболизма составляют характерный аспект множественной миеломы. Злокачественно модифицированные плазмоциты сохраняют и усиливают способность синтетизировать цельные Ig или только определенные составные части глобулиновой молекулы.
Изменения протеинового метаболизма проявляются в трех формах:
1) появление сывороточной гипериротеинемии;
2) выведение протеинов через мочу и
3) отложение на уровне тканей аномалийных протеиновых веществ, известных под названием «амилоид» или «параамилоид».
В сыворотке большинства больных, общее количество протеинов повышено, достигая 23 г/100 мл. Среднее количество сывороточных протеинов у больных с миеломой равняется 9 г/100 мл. Этот рост происходит за счет глобулинов, точнее Ig. При электрофорезе на бумаге или в агаре наблюдается появление узкой и высокой полосы, с заметным сокращением остальных дуг. Это является изображением количественного роста гомогенного населения глобулинов. Пик находится обычно в зоне миграции у-глобулинов или b-глобулинов. Аномалийный протеин, находящийся в сыворотке больных с миеломой, получил название парапротеина, миеломатозного глобулина (М-глобулин) или компонента М.
В рамках множественной миеломы может происходить:
1) избыточный синтез, однако уравновешенный, цепей Н и L, с образованием цельных Ig;
2) неуравновешенный синтез, с избытком цепей L и образованием цельных Ig, параллельно с повышенным количеством свободных цепей L и
3) синтез лишь цепей L.
В настоящее время миеломы делятся по типу секретируемого Ig: миеломы IgG наиболее частые, встречающиеся в 60% случаев; миеломы IgA, в 20—25% случаев; IgD, в 2,1% случаев; и ограниченное число миелом IgE. Среди случаев множественной миеломы, 20% — с цепями L (миеломы Бенс-Джонса), причем некоторые без патологического протеина в сыворотке, так как он элиминируется через мочу. Очень малый процент заболеваний (1%) не представляет изменений протеинового метаболизма (несекретирующие миеломы).
В рамках миелом IgG, наблюдается следующее распределение на субклассы (Schur): yG1 60—82%; yG2 10—18%; yG3 6—15%; yG4 1—8%. Сравнивая эти цифры с относительными концентрациями в нормальной сыворотке (гл. 7) можно утверждать, что моноклональные Ig типа yGl и yG3 встречаются чаще по сравнению с yG2.
Характерной чертой миеломатозного Ig является его гомогенность: узкая зона электрофоретической миграции, индивидуальная антигенная специфичность и цепь L только одного типа (ламбда или каппа). При миеломах IgG и IgA преобладают случаи с цепями каппа (2/3 случаев) (Hobbs и Corbet); при миеломах IgD, цепи ламбда преобладают в 90% случаев, в то время как при миеломах Бенс-Джонса, цепи ламбда присутствуют приблизительно в 45% случаев (Jancelewicz и сотр.). До сих пор не удалось выявить физико-химические или иммунохимические различия между миеломатозными протеинами и соответствующими им нормальными Ig.
Было доказано, что миеломатозные Ig обладают способностью связываться с другими веществами, следовательно действовать как антитела. Такая антителовая деятельность отмечалась по отношению к бактериальным соединениям (стрептолизин 0 или спрептококковая гиалу-ронидаза), к гематиям, к некоторым сывороточным протеинам, а также и к гаптенам (динитрофенол, 5-ацетоурацил, пуриновые и пиримидиновые нуклеотиды) (Osterland и сотр.). Способность миеломатозного протеина связываться с гематиями или сывороточными протеинами порождает определенные симптомы, как например агглютинация гематий в виде монетных столбиков, явления повышенной кровоточивости и пр.
У больных с миеломой, количественный рост характерного миеломатозного Ig сопровождается сокращением производства других типов глобулинов.
Значительная диспротеинемия в крови больных с множественной миеломой оказывает влияние на все пробы коллоидальной лабильности.
Реакция оседания эритроцитов в большинстве случаев бывает очень ускоренной, достигая 100 мм в час. При миеломах Бенс-Джонса, РОЭ показывает более низкие цифры, иногда даже в нормальных пределах.
Реакции на формол-гелифицирование, сульфат кадмия, Вельтмана — положительные. Реакция Sia (помутнение сыворотки в дистилированной воде) — слабо или умеренно положительная.
В редких случаях отмечалось наличие сывороточных криоглобулинов с появлением синдрома Рейно на холоде и наблюдалось также наличие пироглобулинов.
Тесты на коагуляцию модифицированы у некоторых больных. Патологические протеины в сыворотке могут интерферировать с различными фазами коагуляции, как например в трансформация фибриногена в фибрин, во взаимодействии с факторами II, V и VII. Функции тромбоцитов могут быть также модифицированными.
Анализ мочи показывает наличие протеина Бенс-Джонса в 40—50% случаев, когда он детерминируется путем нагревания и в 61% случаев, когда он выявляется путем иммуноэлектрофореза. Он представлен выведением легких цепей. Протеин Бенс-Джонса преципитирует в моче нагретой до 50—60°, создавая беловатое облако, которое перерастворяется при кипячении. В случае ассоциированной альбуминурии, перерастворение является неполным и иногда оказывается неполным и без альбуминурии. В такой ситуации мочу можно сделать прозрачной путем добавления нескольких капель 5%-й уксусной кислоты. Физикохимическое исследование альбумина Бенс-Джонса показало, что он состоит из легких цепей, димеризованных дисульфидными связями. Постоянно легкая цепь в моче идентична с легкой цепью сывороточного миеломатозного протеина.
В мочевом осадке могут появляться цилиндры, гематии, а в случаях почечного калкулеза появляются кристаллы фосфатов, уратов, а также гематии и лейкоциты.
Гиперкальцемия встречается часто при множественной мизломе (20—53% случаев), достигая 12—16 мг/100 мл сыворотки. Этот рост связан в первую очередь с процессами костной деструкции, но и с гиперпаратиреоидизмом, как вторичное явление почечной недостаточности. Гиперкальцемия при множественной миеломе не сопровождается ростом фосфора в крови, а щелочные сывороточные фосфатазы находятся в нормальных пределах, что представляет ценные данные для дифференциальной диагностики по отношению к первичному гиперпаратиреоидизму.
Сывороточная мочевая кислота бывает часто повышена, а в случаях, осложняющихся почечной недостаточностью, наблюдается рост креатинина и непротеинового азота.
Патологоанатомическое исследование при множественной миеломе. Наиболее явные изменения встречаются на уровне скелета, особенно в черепных костях, позвонках, ключицах, ребрах, грудной кости, лопатке, тазовых костях. Длинные кости затронуты в меньшей мере. На срезе, кость оказывается мягкой, а нормальная ткань заменяется красноватой или серо-красноватой туморальной тканью. Иногда опухоль переходит за периост, инфильтрируя смежные участки.
Микроскопически, туморальная ткань состоит из пролиферации злокачественных плазмоцитоидных клеток, описанных при исследовании костного мозга. На срезе остеокласты и остеобласты немодифицированы.
В редких случаях внекостных миелом можно обнаруживать плазмоцитарные опухоли в различных органах, причем характерные особенности пролиферированных клеток подобны тем, которые наблюдаются при костных опухолях.
При множественной миеломе почка бывает часто затронута. Наиболее важные поражения встречаются на уровне канальцев. Дистальные канальцы расширены, с уплощенным эпителием и просветами заполненными эозинофильными и полихроматофильными цилиндрами. На периферии этих цилиндров встречаются многоядерные синцитин эпителиальных клеток. Цилиндры состоят из цельного миеломатозного Ig или из цепей L (протеин Бенс-Джонса). На электронном микроскопе, эти цилиндры имеют фибрилярную, амилоидную структуру (Abrahams и сотр.). Не удалось установить несомненную связь между наличием амилоида и протеинурией Бенс-Джонса. Несмотря на это, Glenner и сотр. показали in vitro образование амилоидных волокон путем протеолитической дигестии человеческого протеина Бенс-Джонса. Возможно, что подобный процесс происходит и на уровне почечных канальцев (Zlotnick).
В тубулярных эпителиальных клетках часто встречаются отложения кальция. Также на уровне почечных канальцев было отмечено наличие кристаллов, находящихся как в просвете, так и в эпителии. Их химическая структура не была установлена.
Почечные гломерулы бывают реже затронутыми при множественной миеломе. Отмечается утолщение базальной мембраны и мезангиомы, которое выступает с особенной ясностью на электронном микроскопе. Встречается также и гипертрофия эндотелиальных и эпителиальных клеток. В развитых фазах болезни появляются гиалиноз и склероз. Иногда в гломерулах можно найти отложения амилоида, что приводит к его гомогенизации.
Почечная интерстициальная ткань представляет инфильтрационные поражения, либо благодаря миеломатозным клеткам, либо благодаря клеткам хронического воспаления.
В общей сложности, эти поражения составляют аспект «миеломатозной клетки».
источник
Миеломная болезнь (плазмоцитома) — заболевание, относящееся к парапротеинемическим гемобластозам, специфическим маркером которых, в большинстве случаев, являются иммуноглобулины (парапротеины) сыворотки крови.
Иммунохимические варианты миеломы определяются по классу иммуноглобулинов и типу легких цепей (λ или κ):
1. иммуноглобулин G — миелома встречается в 55-65 %,
3. иммуноглобулин D — миелома — в 2-5%,
5. болезнь легких цепей (миелома Бенс-Джонса) — в 12 -20%.
Общий анализ крови — у большинства больных анемия нормохромного и нормоцитарного типа. Железодефицитная анемия может развиться при кровотечениях, нарушениях гемостаза и по другим причинам. При дефиците витамина В12 и фолиевой кислоты в костном мозге выявляются признаки мегалобластного кроветворения (В12-дефицитной анемии, фолиеводефицитной анемии). Количество ретикулоцитов понижено. СОЭ увеличена.
У больных миеломной болезнью отмечается лейкопения, реже лейкоцитоз (повышенное количества лейкоцитов в крови). В лейкоцитарной формуле нейтропения, моноцитоз. Плазматические клетки обычно выявляются в небольшом количестве (лучше в лейкоконцентратах). Содержание тромбоцитов снижено.
Биохимический анализ крови — в сыворотке отмечается увеличение общего белка до 90 — 100 г/л и выше (повышение уровня гамма-глобулинов), количество альбумина снижено. При миеломной болезни возрастает уровень кальция, мочевой кислоты. У большинства больных отмечается повышение уровня креатинина и азота мочевины, снижение содержания электролитов. Значительное повышение активности альфа-нафтилацетатэстеразы выявляется в плазматических клетках.
Определение бета-2-микроглобулина используется для наблюдения за динамикой заболевания и эффективностью лечения.
При миеломной болезни проводят электрофорез белков сыворотки крови в полиакриламидном геле. Анализ выявляет М-компонент, чаще всего за счет иммуноглобулинов G и М (иммунохимические варианты миеломы). При миеломе Бенс-Джонса М-компонент в крови обычно отсутствует и выявляется на электрофореграмме белков мочи.
В анализе костного мозга находят большое количество плазматических клеток, которые выявляются у 86 — 95 % больных.
В анализе мочи при миеломной болезни находят протеинурию, цилиндрурию, белок Бенс-Джонса (свыше 12 г/сут). Поражение почек наблюдается при миеломной болезни у большинства больных. С учетом этого обстоятельства проводятся пробы Зимницкого и Реберга-Тареева.
- функция почек ослаблена в менее 50% случаев, обычно это потеря почечной концентрационной способности и азотемия
- протеинурия встречается часто из-за наличия микроальбумина и глобулинов в моче
- протеинурия Бенс-Джонса может быть интермиттирующей
- белок Бенс-Джонса наблюдается в 50% случаев миеломы, но почти всегда формируется почечная недостаточность вследствие миеломы почки
- выраженная анемия непропорциональна азотемии
- непостоянные изменения вследствие поврежденной функции канальцев:
— снижение уровня мочевой кислоты в сыворотке
— потеря с мочой фосфатов со снижением сывороточного фосфора и увеличением уровня щелочной фосфатазы
— нефрогенный несахарный диабет
— олигурия или анурия с острой почечной недостаточностью из-за дегидратации.
- гиперхлоремия (повышение уровня хлора) или гипербикарбонатемия с нормой или снижением натрия в сыворотке снижает ионную проницаемость, и следует предположить миелому при конкретных клинических симптомах
- изменения вследствие ассоциированной гиперкальциемии
источник
Александр Борисович, здравствуйте. Обращаюсь к Вам опять за консультацией. Так как продолжаются неприятные ощущения, о которых я писала, сдала ОАК в поликлинике. Вот результат:
WBC-5.9 4.0-9.0
RBC-4.13 3.8-5.30
HGB-128 120-180
HCT-35.6 33.5-52.0
MCU-86.2 80.0-100
MCH-31.0 28.0-32.0
MCHC-360 310-350
PLT-174 120-330
LY -35.2 2.1 15.0-45.0
MO-2.7 0.2 0.0-10.0
GR-62.1 3.6 42.0-80.0
RDWCU-11.7 11.6-14.0
RDWSD-40.3 39.0-46.0
PCT-0.13 0.16-0.33
MPU-7.4 7.0-11.0
PDW-17.5 15.0-17.0
СОЭ-4
Объясните пожалуйста отклонения показателей PCT, PDW, MCHC. Могут ли эти отклонения говорить о заболевании крови. Еще я сдавала вот такой анализ:
Лямбда легкие цепи (сыворотка) — 88 110-240 мг/дл
Каппа легкие цепи (сыворотка) — 169. 200-440 мг/дл
Лямбда легкие цепи (моча) — 0 до 10 мг/л
Каппа легкие цепи(моча) — 0.1 до 10 мг/л
В этом анализе показатели сыворотки ниже нормы. Врач говорит, что это нормально. Очень хочу услышать Ваш ответ. Заранее Вам благодарна.
Александр Борисович, здравствуйте! Обращаюсь опять к Вам за консультацией. Появились покалывающие ощущения в разных местах тела, как от стекловаты, сильного зуда нет. Но когда колется хочется почесать. Сдала общий анализ крови в поликлинике и результат очень обеспокоил. Сдавала 6 октября 2017 г в этой же поликлинике и за месяц изменения.:
WBC-5.5 4.0-9.0 RBC-4.21 3.8-5.30 HGB-130 120-180 HCT-36.3 33.5-52.0 MCU-86.2 80.0-100 MCH-30.9 28.0-32.0 MCHC-358 310-350 PLT-149 120-330 LY -50.8 2.8 15.0-45.0 MO-3.3 0.2 0.0-10.0 GR-45.9 2.5 42.0-80.0 RDWCU-11.9 11.6-14.0 RDWSD-41.0 39.0-46.0 PCT-0.12 0.16-0.33 MPU-7.8 7.0-11.0 PDW-17.3 15.0-17.0 СОЭ-7
Ручной подсчет эоз-2, сег-46, мон-5, лимф-47 (если правильно поняла ручной подсчет очень непонятно).
О чем могут говорить эти изменения? ОАК за 6 октября выложен в переписке. МРТ органов брюшной полости делала 29 мая 2017. Отклонений не выявлено. Узи подчелюстных, и надключичных лимфоузлов не визуолизируются, преднешейные единичные справа до 4.4 х2.9 мм, слева до 4.6х2.3 мм, заднешейные единичные справа до 5.9 х2.8 мм, слева до 5.5 х2.8 мм. Эхогенность и эхоструктура не изменена. Как поступить далее, что проверять. Ответьте пожалуйста. Почему так за месяц изменились показатели? Почему то снижаются тромбоциты, растут лимфоциты.
Если вы не нашли нужной информации среди ответов на этот вопрос , или же ваша проблема немного отличается от представленной, попробуйте задать дополнительный вопрос врачу на этой же странице, если он будет по теме основного вопроса. Вы также можете задать новый вопрос , и через некоторое время наши врачи на него ответят. Это бесплатно. Также можете поискать нужную информацию в похожих вопросах на этой странице или через страницу поиска по сайту . Мы будем очень благодарны, если Вы порекомендуете нас своим друзьям в социальных сетях .
Медпортал 03online.com осуществляет медконсультации в режиме переписки с врачами на сайте. Здесь вы получаете ответы от реальных практикующих специалистов в своей области. В настоящий момент на сайте можно получить консультацию по 48 направлениям: аллерголога , анестезиолога-реаниматолога , венеролога , гастроэнтеролога , гематолога , генетика , гинеколога , гомеопата , дерматолога , детского гинеколога , детского невролога , детского уролога , детского хирурга , детского эндокринолога , диетолога , иммунолога , инфекциониста , кардиолога , косметолога , логопеда , лора , маммолога , медицинского юриста , нарколога , невропатолога , нейрохирурга , нефролога , онколога , онкоуролога , ортопеда-травматолога , офтальмолога , педиатра , пластического хирурга , проктолога , психиатра , психолога , пульмонолога , ревматолога , рентгенолога , сексолога-андролога , стоматолога , уролога , фармацевта , фитотерапевта , флеболога , хирурга , эндокринолога .
Мы отвечаем на 96.97% вопросов.
источник
Миелолейкозом называют злокачественное перерождение стволовых клеток костного мозга, который отвечает за производство форменных элементов крови-красных и белых кровяных телец и тромбоцитов. При миелолейкозе (белокровии, лейкозе крови) костный мозг производит бластные, недозревшие клетки, которые, постепенно, вытесняют из кровяного русла нормальные форменные элементы.
Заболевание носит преимущественно хронический характер и поражает в основном, взрослых. Для постановки диагноза необходимо провести анализ крови на миелолейкоз. Поскольку на разных стадиях заболевания, происходят значительные изменения в составе крови, требуется проводить анализы несколько раз. При подозрении на миелолейкоз, врачи рекомендуют проводить регулярные обследования.
Миелолейкоз — это результат мутирования лейкоцитов крови в костном мозге. Аномальная клетка теряет способность нормально функционировать и начинает стихийно делиться. Раковые клетки, размножаясь, постепенно вытесняют здоровые. В результате возникают тяжелые кровотечения и анемии и организм теряет защиту от инфекций. Лейкозные клетки проникают в лимфоузлы, кооперируются в опухоли и провоцируют патологические процессы.
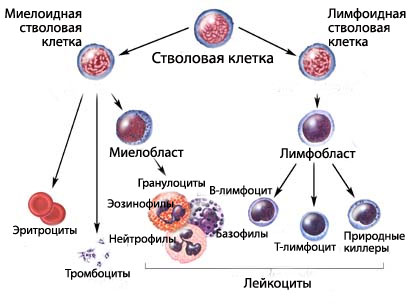
Причиной миеломной болезни может стать радиоактивное излучение или воздействие канцерогенов, среди которых имеются лекарственные препараты, растворители краски средства борьбы с грызунами и насекомыми.
Наследственные факторы при лейкозе, как и при других болезнях, имеют место. В семьях, где родственники заболевают миеломной болезнью, велика вероятность заболеваний среди потомков. Детям передаётся не сама болезнь, а предрасположенность к ней.
Существует гипотеза о инфекционной этиологии заболевания. В этом случае, имеет значение раса и место проживания человека.
Предварительный диагноз на миелолейкоз ставится на основании результатов общего анализа крови, стандартной диагностической процедуры при любом заболевании. Врача должно насторожить увеличение числа лейкоцитов.
Расшифровка анализа крови на миеломную болезнь , прежде всего, должна учитывать количество лейкоцитов и их соотношение с расчётом лейкоцитарной формулы. При подсчёте лейкоцитарной формулы наблюдается сдвиг влево, появление промиелоцитов. Растёт процент базофилов и эозинофилов, повышается СОЭ в крови. Число тромбоцитов в норме, или несколько повышено. Наблюдаются симптомы анемии в лёгкой форме.
Если миелолейкоз прогрессирует, результаты анализов крови меняются. Поэтому, необходимо повторять анализ крови на миелолейкоз через некоторое время. Результаты исследований выявляют сильную анемию, форменные элементы меняют размеры и деформируются, (анизоцитоз и пойкилоцитоз);число лейкоцитов многократно увеличивается в сравнении с прежними результатами. Количество бластных клеток достигает 15%. Содержание базофилов и эрзинофилов превышает норму. Блокируется действие щелочной фосфатазы в нейтрофилах.
Сопутствующими миелолейкозу симптомами являются проблемы с печенью, подтверждающиеся повышением активности сывороточных энзимов –аланинаминотрансферазы и щелочной фсфатазы.
Симптомы миелолейкоза являются:
- Боли в костях. Болят бедренные кости, позвоночник, таз, рёбра;
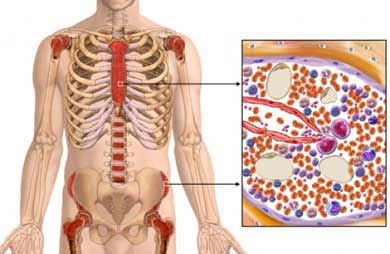
- Патологические переломы;
- Гиперкальциемия. Проявляется рвотой, тошнотой, запорами, полиурией. Могут возникнуть мозговые нарушения, человек впадает в летаргию или кому;
- Заболевания почек. Нефропатия проявляется в виде повышения содержания кальция и мочевой кислоты в крови, появления белка в моче;
- Анемия нормохромная. Цветовой показатель крови в норме, резко вырастает СОЭ;
- Остеопороз;
- Сдавливание спинного мозга опухолями позвоночника. Проявляется в виде болей в спине, усиливающихся при кашле, чихании. Нарушается работа мочевого пузыря и кишок.;
- Беззащитность перед бактериальными инфекциями. Связана с ослаблением иммунитета;
- Геморрагии. Кровотечения из носа, матки, дёсен, подкожные кровоизлияния.
Правила сдачи крови на общий анализ не предусматривают специфических правил подготовки. Как сдавать анализ крови на хронический миелолейкоз, известно. Кровь сдают натощак, утром, чтобы избежать «помех», искажающих результаты. В день, перед сдачей крови не рекомендуют тяжёлые физические нагрузки. Крайне нежелательно, в течение трёх суток перед процедурой, употребление жирных и жареных продуктов. Если эти условия соблюдены, то диагностический анализ крови на миелолейкоз будет чрезвычайно информативен.
Делают забор крови из вены или пальца. Венозная кровь более концентрирована, чем капиллярная, поэтому некоторые врачи требуют именно такого отбора проб на анализ.
Расшифровка результатов миелолейкоза, занимает два дня, с момента принятия результатов в обработку. Если лаборатория перегружена работой, то результат может быть получен позднее.
Современные диагностики крови предусматривают взятие образцов костного мозга на цитогенетический анализ из бедренной кости. Пробы отбирают методом биопсии или аспирации. Изучают хромосомы. Поражённые клетки содержат аномальную 22 хромосому. С целью обнаружения аномальной хромосомы используют цепную полимеразную реакцию.
Качество анализа является залогом успешной терапии. Выбор метода лечения и интенсивность рекомендуемых процедур зависят от фазы заболевания. У части больных миеломной болезнью наблюдают нарастающее прогрессирование процесса на протяжении многих лет, и не требующие противоопухолевого лечения.
У больных при наличии метастазов применяют локальную лучевую терапию. При медленном развитии миелолейкоза используют выжидательную тактику.
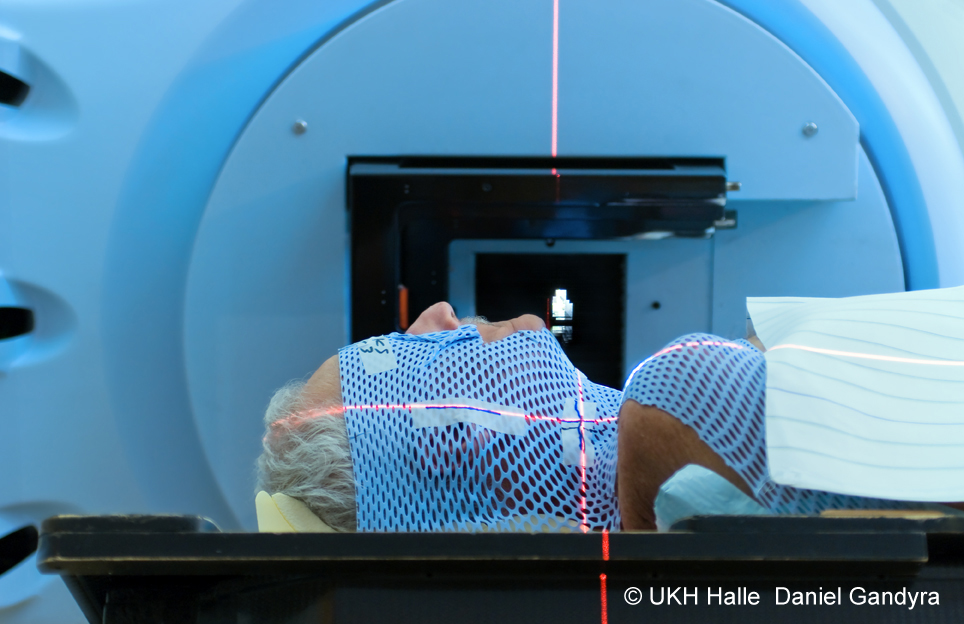
Если нарастают боли, что свидетельствует о разрастании опухоли, назначают цитостатики. Сроки лечения, при условии наличия позитивных результатов продолжаются до двух лет.
Проводят лечение, профилактирующие осложнения. Для купирования гиперкальциемии применяют кортикостероиды на фоне обильного питья. Применяют лекарства для лечения заболеваний почек и остеопороза.
Миеломное заболевание в вялотекущей фазе не является показанием для немедленного лечения. Необходимостью для начала терапии является появление в крови парапротеина, сгущение крови или понижение вязкости, наличие кровотечений, болей в костях, переломах, гиперкальциемия, поражение почек, компрессия спинного мозга, инфекционные осложнения.
Сдавливание спинного мозга требует хирургического лечения, а также, местного облучения. Переломы костей требуют ортопедического фиксирования.
В ряде случаев, если не показана радиационная терапия, используют цитотоксическое лечение. В этом случае надо иметь ввиду, что побочным эффектом может стать вторичная миелолейкемия.
При отсутствии лечения больные миеломной болезнью живут до двух лет. Полное излечение миеломы-это дело будущего.
Современные методы лечения способны затормозить разрушительное действие заболевания на организм и бороться с её конкретными симптомами.
источник
Миеломная болезнь (миелома, плазмоцитома, миеломатоз и болезнь Рустицкого-Калера) – это тяжёлое заболевание кроветворной системы, которое чаще всего определяется на поздних стадиях протекания и вследствие этого имеет неутешительные прогнозы. Своевременно начатое лечение позволяет продлить жизнь пациента и достигнуть относительно длительной ремиссии. Поэтому ранняя диагностика миеломной болезни – важный вопрос для всех людей, находящихся в группе риска.
Миеломатоз – самое распространённое заболевание в группе раковых опухолей плазматических клеток крови. Частота встречаемости миеломной болезни составляет до 1 % всех случаев онкологии и около 10 % случаев рака крови. Ежегодно среди 1 миллиона населения мира обнаруживается 30 новых случаев миеломы.
При данном виде онкологии происходит мутация одного из видов клеток крови – плазмоцитов. Плазмоциты или плазматические клетки – это конечная форма В-лимфоцитов. Их функция состоит в распознавании чужеродных агентов и выработке специфичных к ним антител (иммуноглобулинов).
При мутации происходит патологическое размножение (пролиферация) одного из клонов плазматических клеток. Изменённые плазмоциты вырабатывают патологический иммуноглобулин – парапротеин, который является основным маркером миеломатоза при дифференциальной диагностике.
Болезни подвержены в основном пожилые пациенты, организм которых не в состоянии переносить тяжёлые интенсивные курсы химиотерапии. Поэтому срок между появлением первых мутировавших плазмоцитов и диагностикой заболевания непосредственно влияет на прогнозы выживаемости. При этом рост числа патологических клеток и развитие миеломной болезни могут происходить чрезвычайно медленно. От появления первых плазмоцитов с мутациями до образования очагов миеломы может проходить 20-30 лет.
Переломный момент наступает после проявления клинических признаков заболевания. Миелома начинает быстро прогрессировать. Избыток парапротеина негативно влияет на висцеральные органы (в основном на выделительную систему) и кости организма.
Миеломы классифицируются в зависимости от особенностей расположения изменённых плазмоцитов в здоровых тканях костного мозга и специфики их состава. В зависимости от локализации патологических клеток в кроветворных тканях различают диффузную, диффузно-очаговую и множественную (множественно-очаговую) форму заболевания.
Состав клеток позволяет классифицировать миеломатозные опухоли на плазмобластные, плазмоцитарные, мелко- и полимфортноклеточные. Вид атипичных плазмоцитов определяется при тканевом (гистологическом) исследовании. Эта характеристика позволяет спрогнозировать скорость роста опухоли.
Одна из распространённых в медицинской практике классификаций учитывает также особенности локализации патологического очага (очагов) в костной системе и внутренних органах.
Солитарные или одиночные миеломатозные опухоли располагаются в кости, содержащей костномозговую ткань, либо в лимфоузле. Лимфоузлы непосредственно участвуют в реакции иммунитета на инфекционных агентов, поэтому нередко поражаются миеломной болезнью.
Множественные очаги миеломатоза занимают сразу несколько мест. Особенно уязвима для мутировавших плазмоцитов костномозговая ткань позвоночника, подвздошных и черепных костей, лопаток, ребёр. Нередко очаги опухоли образовываются в селезёнке, нескольких лимфоузлах и центральной части трубчатых костей ног и рук.
При подозрении на множественную миелому, а также рецидиве солитарной неоплазии плазматических клеток проводится полное исследование тела методами томографии.
На раннем этапе заболевание может протекать практически без симптомов. Когда количество патологически изменённых клеток достигает критического значения, и миелома образует солитарный или множественный очаг, проявляются клинические признаки плазмоцитарного рака.
Основные симптомы миеломной болезни:
- ноющие боли в костях конечностей, лопаток, черепа или позвоночника;
- тянущие боли в сердце и суставах (вызваны отложением амилоида – формы хранения парапротеинов во внутренних органах);
- частые бактериальные инфекции;
- патологические переломы костей конечностей, рёбер и позвонков;
- слабость, заторможенность когнитивных функций, нарушения работы ЖКТ (обусловлены гиперкальциемией – высвобождением кальция из растворённой костной ткани в кровь);
- анемия;
- учащённое сердцебиение (как результат компенсаторного механизма в ответ на недостаток эритроцитов);
- одышка, головная боль;
- деформация грудной клетки вследствие изменения костной ткани;
- нефропатия (нарушение функции почек вследствие образования кальциевых камней в их протоках);
- снижение свёртываемости крови (с образованием множественных кровоподтёков), нередко – на фоне роста вязкости плазмы (в результате при частых кровотечениях у пациента могут образовываться тромбы).
У каждого десятого больного патологические плазмоциты не продуцируют парапротеин. В результате даже на стадии обширного развития миеломы заболевание протекает бессимптомно.
Интенсивность проявления симптомов и их перечень зависит от стадии болезни, её типа (например, при множественном миеломатозе в первую очередь фиксируют переломы и гиперкальциемию) и сопутствующих хронических заболеваний.
Признаки миеломы на разных стадиях
| Диагностические признаки | 1-я стадия | 2-я стадия | 3-я стадия |
|---|---|---|---|
| Остеопороз (хрупкость, разрушение костей) | Признаки остеопороза отсутствуют или наблюдаются в зоне миеломатозного очага | Признаки разрушения присутствуют, но не столь явные, как при 3-й стадии болезни | Наблюдается интенсивный остеопороз |
| Количество костей с миеломатозным очагом | Одиночная миелома | 1-2 | 3 и более костей поражено опухолью |
| Гиперкальциемия | >2,55 ммоль/л | >3 ммоль/л | |
| Уровень гемоглобина | >100 г/л | Анемия 1-й или 2-й степени | |
| Концентрация белка Бенс-Джонса | от 4 до 12 г белка в суточной моче | >12 г/сутки | |
| Сывороточные парапротеины | Менее 5 г/дл (IgG) Менее 3 г/дл (IgА) | Промежуточные значения | Более 7 г/дл (IgG) Вторая стадия болезни определяется чаще методом исключения, если показатели не соответствуют критериям 1-й и 3-й.Белок Бенс-Джонса является соединением, которое выделяется плазматическими клетками. В силу небольшой молекулярной массы оно сразу выводится почками, что делает его наличие важным диагностическим признаком при обследовании пациентов. Для определения миеломной болезни диагностика должна включать визуальные, аппаратные и лабораторные методы исследования. При осмотре хирург или онколог расспрашивает пациента о жалобах и времени проявления неприятных симптомов, измеряют частоту пульса, пальпируют болезненные участки костей, фиксируя, усиливается ли боль при нажатии. Также оценивается цвет кожного покрова (бледность может говорить об анемии), наличие синяков и кровоподтёков, припухлостей в местах частой локализации опухоли. При подозрении на миеломатоз пациенту назначают ряд исследований. Перечень аппаратных методов диагностики, которые применяются для выявления миелом, включает:
Все три метода позволяют выявить участки сниженной плотности костной ткани и дифференцировать патологию от других заболеваний опорно-двигательного аппарата. При поражении множественной миеломой на рентгенограмме отчётливо заметно, что кости черепа, позвоночника, лопаток и конечностей испещрены тёмными пятнами остеолитических повреждений. При солитарной (одиночной) опухоли нарушение плотности наблюдается лишь в месте её локализации. Томография является более информативным и полным методом. Она позволяет отследить костные поражения всего опорно-двигательного аппарата за короткое время и без облучения отдельных частей тела. Инструментальная диагностика включает забор пробы (пункцию) костного мозга для составления миелограммы. Миелограмма – это результат анализа биоматериала (миелоидной ткани), в которой указаны качественный и количественный составы костного мозга. Это исследование даёт возможность дифференцировать заболевание с другими видами рака крови. Основным диагностическим симптомом миеломы является патологически повышенная доля плазматических клеток (более 10-30 % при норме до 1,5 %). Параллельно с плазмоцитами может повышаться содержание недифференцированных бластов (норма составляет до 1,1 %). Содержание эритробластов, лимфоцитов и других кроветворных клеток, напротив, значительно снижено. Ключевая роль в постановке диагноза «миелома» отводится не только анализу миелоидной ткани, но и лабораторной диагностике (пробам крови и мочи). Для диагностики миеломатоза используются такие методы исследования:
Результаты общего анализа крови при миеломе значительно отличаются от нормы. Уровень гемоглоибна, а также количество тромбоцитов, лейкоцитов, эритроцитов, ретикулоцитов (предшественников красных кровяных клеток), нейтрофилов снижается. Растут скорость оседания эритроцитов (что свидетельствует о патологии без указания на её генез) и доля моноцитов в лейкоцитарной формуле. В пробе могут обнаружиться 1-2 плазмоцита. В общем анализе мочи определяются цилиндры, эритроциты и лёгкие цепи парапротеина (белки Бенс-Джонса). Выделяемая жидкость имеет более высокую плотность, чем у здорового человека (в основном за счёт патологических белков). В биохимическом анализе наблюдаются признаки поражения почек (повышенный уровень концентрации мочевой кислоты, мочевины и креатинина) и гиперкальциемии. На фоне малого количества альбумина за счёт присутствия парапротеина фиксируется аномально высокая концентрация общего белка. Иммуноэлектрофорез проводится для определения парапротеинов в моче или плазме крови. В зависимости от типа патологических клеток во время анализа могут быть выявлены парапротеины классов IgА (IgD, IgE, IgG) или бета-2 микроглобулины (уровень последнего указывает на стадию болезни). В качестве дополнительных методов диагностики используются анализы на концентрацию L-лактата (маркера повреждения тканей), электролитов и С-реактивного белка (его концентрация влияет на уровень содержания фактора роста миелом – интерлейкина-6). После постановки диагноза специалист-онколог проводит анализ для определения перспектив и скорости роста опухоли (индекс мечения плазмацитов). Симптоматика миеломатоза нередко напоминает проявление более распространённых заболеваний онкологического и доброкачественного генеза. Наибольшую сложность представляет дифференцирование признаков плазмоцитомы и доброкачественной моноклональной гаммапатии. Доброкачественные гаммапатии также характеризуются образованием клонов иммуноглобулинпродуцирующих клеток, однако рост их количества не происходит или происходит очень медленно. Концентрация моноклональных иммуноглобулинов в сыворотке крови не превышает 3 г/дл, а доля плазмоцитов в костномозговой ткани составляет до 5 %. Поражения костей и гиперкальциемия не фиксируются. Гаммапатия является наиболее частой причиной парапротеинемии (повышенного количества патологического белка в крови). По статистике, она наблюдается у 1-1,5 % людей старше 50 лет и у 3-10 % людей старше 70 лет. Это состояние не требует срочного лечения, но обязательно наблюдается врачами, т. к. в 16 % случаев оно способно развиться в миеломную болезнь, а в 17 % и 33 % (в течение 10 и 20 лет соответственно) – в другие виды гемобластозов. В половине случаев повышенное количество патологического белка наблюдается в течение всей жизни пациента, но не становится причиной его смерти. Дифференциальная диагностика с другими причинами остеолитических повреждений (низкая секреция эстрогенов, болезнь Реклингаузена, старческий остеопороз, метастазы карциномы предстательной и щитовидной желёз) производится по анализу концентрации парапротеинов и миелограмме. Схожесть с симптомами миеломы имеют и признаки болезни Вальденстрёма. Наблюдаются характерное повышение моноклональных иммуноглобулинов (IgM), избыточная выработка парапротеинов и повышенное количество лимфоплазмоцитарных клеток. Отличие заключается лишь в отсутствии литических поражений костей, что определяется на томографии. Дифференциальная диагностика миеломатоза и других синдромов, связанных с парапротеинемией, проводится также при почечной недостаточности невыясненной этиологии. Ранняя диагностика миелом возможна только при регулярном проведении общих клинических анализов и почечных проб (биохимии крови). Если пациент бережно относится к своему здоровью и ежегодно отслеживает динамику результатов, то у него есть все шансы обратиться к врачу задолго до появления клинических признаков миеломатоза и с помощью интенсивной терапии достигнуть длительной ремиссии заболевания. Мы будем очень благодарны, если вы оцените ее и поделитесь в социальных сетях источник |



