Марганец является одним из самых распространенных элементов на планете, занимая по этому показателю четырнадцатое место. Неудивительно, что определенная концентрация марганца имеется и в воде.
Человеческий организм испытывает необходимость в данном веществе – учеными даже установлена дневная норма для человека – до 5 мг для взрослого и до 2 мг для подростка. Дефицит марганца может привести к замедлению роста и развития организма, нарушению работы кровеносной и центральной нервной системы. Таким образом можно заключить, что в небольших количествах марганец необходим для обеспечения стабильной работы организма.
Однако, повышенная концентрация элемента в воде может вызывать определенные проблемы. По данным СанПиН норма содержания марганца в системах централизованного водоснабжения не должна быть выше 0,1 ПДК, мг/л. Острое отравление наступает при единоразовом употреблении 40 мг. В случае превышения содержания марганца могут возникнуть следующие проблемы:
- нарушение репродуктивной функции;
- поражение центральной нервной системы;
- нарушение работу печени;
- развитие паркинсонизма.
Марганец в чистом виде встречается редко, являясь частью состава различных минералов. В воду элемент попадает двумя путями:
- Природный путь. Марганец удаляется водой из минералов, в которых содержится. Помимо этого, элемент может попадать в воду от разложившихся растений и животных, проживающих в водоемах.
- Техногенный путь. Марганец проникает в воду со сбрасываемыми в водоемы отходами предприятий. В некоторых сельскохозяйственных удобрениях также содержится данный элемент.
Уровень содержания марганца в воде может отличаться в зависимости от местности и типа воды – так в подземных водах содержание может достигать максимальных значений до 100 мг/л. Марганец опасен тем, что постоянное употребление питьевой воды с высоким содержанием элемента может привести к ухудшению общего состояния, снижению мышечного тонуса, появлению аллергии, а также оказать негативное влияние на почки, печень и тонкий кишечник.
При высокой концентрации марганца вода может стать мутной, обрести характерный запахом. При этом, если ее отстоять, на дне посуды появится черный осадок. Однако, опасность состоит в том, что марганец может негативно влиять на организм, будучи незаметным невооруженным взглядом. В связи с этим качественный и точный анализ воды на содержание марганца играет важную роль для обеспечения гарантий безопасного использования жидкости для питья или бытовых нужд.
Московская лаборатория «НОРТЕСТ» проводит исследование воды на марганец с применением современного оборудования и соблюдением требований нормативных документов. Профессиональный штат специалистов выполняет комплекс необходимых работ для получения точных данных в кратчайшие сроки.
Мы также поможем выбрать оптимальный метод очистки воды в случае повышенного содержания марганца. Решение зависит от результатов анализа и предусматривает лишение марганца способности растворяться.
- В частности, популярным вариантом очистки является применение ионообменных смол, которые отличаются высокой емкостью по отношению к разным элементам, в том числе железу и марганцу. Смолы способны поглощать в себя элемент, тем самым снижая уровень его концентрации в воде. Оптимальный режим работы фильтра и вид смолы подбирается в зависимости от установленной концентрации марганца.
- Еще один вариант – обратный осмос. Это универсальный фильтр, которые также справляется и с удалением марганца из воды. Наши специалисты помогут подобрать лучший вариант из имеющихся.
В лаборатории «НОРТЕСТ» клиенты всегда могут рассчитывать на квалифицированную помощь. После завершения работы мы выдаем подробный отчет с информацией об основных показателях, предположительным источником загрязнения, а также профессиональными рекомендациями по вопросу поиска оптимального решения для очистки.
источник
Настоящий документ устанавливает методику измерений массовой концентрации марганца в природных и сточных водах фотометрическим методом с персульфатом аммония.
Диапазон измерений от 0,005 до 10 мг/дм 3 .
Если массовая концентрация марганца в анализируемой пробе превышает 5 мг/дм 3 , пробу необходимо разбавлять.
Если массовая концентрация марганца в анализируемой пробе ниже 0,05 мг/дм 3 , то пробу концентрируют путем упаривания.
Мешающие влияния, обусловленные присутствием в пробе органических веществ, хлорид-ионов и железа, устраняются специальной подготовкой пробы к анализу (п. 9.1).
Значения показателя точности измерений 1 — расширенной относительной неопределенности измерений по настоящей методике при коэффициенте охвата 2 приведены в таблице 1. Бюджет неопределенности измерений приведен в Приложении А.
1 В соответствии с ГОСТ Р 8.563-2009 (п. 3.4) в качестве показателя точности измерений использованы показатели неопределенности измерений).
Диапазон измерений, мг/дм 3
Суммарная стандартная относительная неопределенность, u , %
Расширенная относительная неопределенность 2 , U при коэффициенте охвата k = 2, %
2 Соответствует характеристике погрешности при доверительной вероятности Р = 0,95.
Значения показателя точности методики используют при:
— оформлении результатов анализа, выдаваемых лабораторией;
— оценке деятельности лабораторий на качество проведения испытаний;
— оценке возможности использования результатов анализа при реализации методики в конкретной лаборатории.
При выполнении измерений применяют следующие средства измерений, вспомогательные устройства, реактивы и материалы.
— Спектрофотометр или фотоэлектроколориметр, позволяющий измерять оптическую плотность при длине волны λ = 540 нм.
— Кюветы с толщиной поглощающего слоя 50 мм.
— Весы лабораторные специального или высокого класса точности с ценой деления не более 0,1 мг, наибольшим пределом взвешивания не более 210 г по ГОСТ Р 53228-2008.
— Колбы мерные 2-(100,200,1000)-2 по ГОСТ 1770-74.
— Пипетки мерные градуированные с делениями 0,1 см 3 , 4(5)-2-1(2), 6(7)1-5(10), 3-1-50 по ГОСТ 29227-91.
— ГСО раствора с аттестованным содержанием ионов марганца и погрешностью аттестованного значения не более 1 % при Р = 0,95.
— Колбы конические Кн-1-250-14/23 ТС по ГОСТ 25336-82.
— Фарфоровые чашки для выпаривания по ГОСТ 9147-80.
— Фильтры обеззоленные «Синяя лента» по ТУ 6-09-1678-95.
— Бутыли из полимерного материала с притертыми или винтовыми пробками вместимостью 500 — 1000 см 3 для отбора и хранения проб.
1 Допускается использование других средств измерений утвержденных типов, обеспечивающих измерения с установленной точностью.
2 Допускается использование другого оборудования с метрологическими и техническими характеристиками, аналогичными указанным.
3 Средства измерений должны быть поверены в установленные сроки.
— Ртуть (II) азотнокислая 1-водная по ГОСТ 4520-78.
— Аммоний надсернокислый (персульфат) по ГОСТ 20478-75.
1 Все реактивы, используемые для анализа, должны быть квалификации ч.д.а. или х.ч.
2 Допускается использование реактивов, изготовленных по другой нормативно-технической документации, в том числе импортных.
Метод основан на окислении ионов марганца (II) до перманганат-ионов в азотнокислой среде под действием персульфата аммония в присутствии катализатора — ионов серебра с последующим измерением оптической плотности окрашенного раствора при длине волны 540 нм.
При выполнении измерений необходимо соблюдать следующие требования техники безопасности.
5.1 При выполнении измерений необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007-76.
5.2 Электробезопасность при работе с электроустановками по ГОСТ Р 12.1.019-2009.
5.3 Организация обучения работающих безопасности труда по ГОСТ 12.0.004-90.
5.4 Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004-91 и иметь средства пожаротушения по ГОСТ 12.4.009-83.
5.5 Содержание вредных веществ в воздухе не должно превышать установленных предельно допустимых концентраций в соответствии с ГОСТ 12.1.005-88.
Выполнение измерений может производить химик-аналитик, владеющий техникой экстракционно-фотометрического анализа, изучивший инструкцию по эксплуатации спектрофотометра или фотоэлектроколориметра и получивший удовлетворительные результаты при выполнении контроля процедуры измерений.
При выполнении измерений в лаборатории должны быть соблюдены следующие условия:
— температура окружающего воздуха (20 ± 5) °C;
— атмосферное давление (84,0 — 106,7) кПа;
— относительная влажность не более 80 % при температуре 25 °С;
— напряжение сети (220 ± 22) В.
При подготовке к выполнению измерений должны быть проведены следующие работы: подготовка прибора к работе, приготовление растворов, построение градуировочного графика, контроль стабильности градуировочной характеристики, отбор и хранение проб.
Подготовку спектрофотометра или фотоэлектроколориметра к работе проводят в соответствии с рабочей инструкцией по эксплуатации прибора.
8.2.1 Приготовление раствора нитрата ртути (II)
Растворяют 17,131 г Hg(NO3)2·H2O в дистиллированной воде, смочив сначала навеску 1 см 3 концентрированной азотной кислоты и доводят до метки дистиллированной водой в мерной колбе вместимостью 1 дм 3 .
1 см 3 полученного раствора эквивалентен 3,54 мг хлорид-ионов.
8.2.2 Приготовление раствора персульфата аммония
Растворяют 20 г персульфата аммония (NH4)2S2O8 в 80 см 3 дистиллированной воды.
8.2.3 Приготовление раствора нитрата серебра
Растворяют 16,9874 г AgNO3 в дистиллированной воде и разбавляют до 1 дм 3 .
8.2.4 Приготовление основного градуировочного раствора ионов марганца с массовой концентрацией 0,01 мг/см 3 из ГСО
Раствор готовят в соответствии с прилагаемой к образцу инструкцией. 1 см 3 раствора должен содержать 0,01 мг марганца.
Для построения градуировочного графика необходимо приготовить образцы для градуировки с массовой концентрацией ионов марганца от 0,05 до 5 мг/дм 3 . Условия анализа, его проведение должны соответствовать п.п. 7 и 9.
Состав и количество образцов для градуировки для построения градуировочного графика приведены в таблице 2. Погрешность, обусловленная процедурой приготовления образцов для градуировки, не превышает 2,5 %.
Массовая концентрация ионов марганца в градуировочных растворах, мг/дм 3
Аликвотная часть градуировочного раствора (см 3 ) с концентрацией 0,01 мг/см 3 помещаемого в мерную колбу вместимостью 100 см 3
Анализ образцов для градуировки проводят в порядке возрастания их концентрации. Для построения градуировочного графика каждую искусственную смесь необходимо фотометрировать 3 раза с целью исключения случайных результатов и усреднения данных. При построении градуировочного графика по оси ординат откладывают значения оптической плотности, а по оси абсцисс — величину массовой концентрации ионов марганца в мг/дм 3 .
Контроль стабильности градуировочной характеристики проводят не реже одного раза в квартал, а также при смене партий реактивов, после поверки или ремонта прибора. Средствами контроля являются вновь приготовленные образцы для градуировки (не менее 3 образцов из приведенных в таблице 2).
Градуировочную характеристику считают стабильной при выполнении для каждого образца для градуировки следующего условия:
где X — результат контрольного измерения массовой концентрации ионов марганца в образце для градуировки, мг/дм 3 ;
С — аттестованное значение массовой концентрации ионов марганца, мг/дм 3 ;
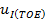
Значения 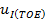
Если условие стабильности градуировочной характеристики не выполняется только для одного образца для градуировки, необходимо выполнить повторное измерение этого образца с целью исключения результата, содержащего грубую погрешность.
Если градуировочная характеристика нестабильна, выясняют причины и повторяют контроль с использованием других образцов для градуировки, предусмотренных методикой. При повторном обнаружении нестабильности градуировочной характеристики строят новый градуировочный график.
8.5.1 Отбор проб производится в соответствии с требованиями ГОСТ Р 51592-2000 «Вода. Общие требования к отбору проб».
Пробы воды отбирают в бутыли из полимерного материала, предварительно ополоснутые отбираемой водой. Объем отбираемой пробы должен быть не менее 200 см 3 .
8.5.2 Если пробы нельзя проанализировать в день отбора, их консервируют, подкисляя до pH менее 2 концентрированной азотной кислотой.
Законсервированные пробы хранят не более 1 месяца.
Если требуется определить марганец в растворенной форме, пробу фильтруют через обеззоленный фильтр «синяя лента» до консервации.
8.5.3 При отборе проб составляется сопроводительный документ по утвержденной форме, в котором указывается:
цель анализа, предполагаемые загрязнители:
должность, фамилия отбирающего пробу, дата.
9.1.1 Для устранения мешающего влияния хлорид-ионов, если концентрация их не превышает 300 мг/дм 3 , предлагается вводить раствор соли ртути (II), образующей с хлорид-ионами малодиссоциированное соединение. При более высоком содержании хлорид-ионов проводят предварительную обработку азотной и серной кислотами.
9.1.2 Мешают определению органические вещества при большой их концентрации (ХПК превышает 16 мг/дм 3 ). При высоком содержании органических веществ следует прибавить в пробу по 5 см 3 концентрированной азотной и концентрированной серной кислоты, выпарить в фарфоровой чашке до появления паров серной кислоты и после охлаждения растворить остаток в 5 см 3 , добавляя дистиллированную воду до 100 см 3 . При меньшем содержании органических веществ можно ограничиться кипячением пробы 5 — 10 мин с добавлением 10 см 3 концентрированной азотной кислоты на 100 см 3 .
9.1.3 Мешающее влияние железа устраняют добавлением 1 см 3 концентрированной ортофосфорной кислоты в пробу, до окисления персульфатом.
К 100 см 3 пробы, если необходимо, предварительно разбавленной или упаренной, приливают 3 см 3 концентрированной азотной кислоты и такой объем раствора нитрата ртути, чтобы он был эквивалентен содержанию хлорид-ионов во взятой пробе, и сверх того еще 2 см 3 . Добавляют, если надо, ортофосфорную кислоту (ρ = 1,7 г/см 3 ), нагревают до кипения, прибавляют 5 см 3 раствора персульфата аммония, 2 капли раствора нитрата серебра и кипятят 5 мин.
После охлаждения раствора, его переносят в мерную колбу вместимостью 200 см 3 , разбавляют дистиллированной водой до метки и перемешивают.
Оптическую плотность полученного раствора измеряют при λ = 540 нм по отношению к холостому опыту в кювете с толщиной поглощающего слоя 50 мм. Содержание марганца находят по градуировочному графику.
10.1 Массовую концентрацию ионов марганца X (мг/дм 3 ) рассчитывают по формуле:
С — массовая концентрация ионов марганца, найденная по градуировочному графику, мг/дм 3 ;
K — коэффициент разбавления или концентрирования.
10.2 За результат измерений принимают единичное значение или Хср — среднее арифметическое значение двух параллельных определений Х1 и Х2
для которых выполняется следующее условие:
где r — предел повторяемости, значения которого приведены в таблице 3.
Диапазон измерений, мг/дм 3
Предел повторяемости (относительное значение допускаемого расхождения между двумя результатами параллельных определений), r , %
Предел воспроизводимости (относительное значение допускаемого расхождения между двумя результатами измерений, полученными в разных лабораториях), R, %
При невыполнении условия (3) могут быть использованы методы проверки приемлемости результатов параллельных определений и установления окончательного результата согласно разделу 5 ГОСТ Р ИСО 5725-6-2002.
Расхождение между результатами анализа, полученными в двух лабораториях, не должно превышать предела воспроизводимости. При выполнении этого условия приемлемы оба результата анализа, и в качестве окончательного может быть использовано их среднее арифметическое значение. Значение предела воспроизводимости приведены в таблице 3.
При превышении предела воспроизводимости могут быть использованы методы оценки приемлемости результатов анализа согласно разделу 5 ГОСТ Р ИСО 5725-6-2002.
Результат измерений в документах, предусматривающих его использование, может быть представлен в виде: X ± U, мг/дм 3 ,
где X — результат измерений массовой концентрации марганца, мг/дм 3 ;
U — значение показателя точности измерений (расширенная неопределенность измерений с коэффициентом охвата k = 2), мг/дм 3 .
Значение Uотн. приведено в таблице 1.
Допускается результат измерений в документах, выдаваемых лабораторией, представлять в виде: X ± Uл, мг/дм 3 , Р = 0,95, при условии Uл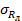
σI(TOE) — стандартное отклонение (СКО) промежуточной прецизионности, приведенное в бюджете неопределенности;
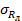
Оперативный контроль процедуры измерений проводят путем сравнения результата отдельно взятой контрольной процедуры Кк с нормативом контроля К.
Результат контрольной процедуры Кк рассчитывают по формуле
где Хср′ — результат измерений массовой концентрации марганца в пробе с известной добавкой — среднее арифметическое двух результатов параллельных определений, расхождение между которыми удовлетворяет условию (4), мг/дм 3 .
Хср — результат измерений массовой концентрации марганца в исходной пробе — среднее арифметическое двух результатов параллельных определений, расхождение между которыми удовлетворяет условию (4), мг/дм 3 .
Сд — величина добавки, мг/дм 3 .
Норматив контроля Кд рассчитывают по формуле:
где Uл,Х и Uл,Х′ показатели точности результатов измерений (расширенная неопределенность с коэффициентом охвата 2), установленные в лаборатории при реализации методики, соответствующие массовой концентрации марганца в рабочей пробе и в пробе с добавкой соответственно, мг/дм 3 .
Процедуру измерений признают удовлетворительной при выполнении условия:
При невыполнении условия (8) контрольную процедуру повторяют. При повторном невыполнении условия (8) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
Оперативный контроль процедуры измерений проводят путем сравнения результата отдельно взятой контрольной процедуры Кк с нормативом контроля К.
Результат контрольной процедуры Кк рассчитывают по формуле
где Сср — результат измерений массовой концентрации марганца в образце для контроля — среднее арифметическое двух результатов параллельных определений, расхождение между которыми удовлетворяет условию (4), мг/дм 3 ;
С — аттестованное значение образца для контроля.
Норматив контроля К рассчитывают по формуле
где Uл — значение показателя точности измерений (расширенной неопределенности с коэффициентом охвата k = 2), установленное при реализации методики в лаборатории и обеспечиваемое контролем стабильности результатов измерений.
Процедуру измерений признают удовлетворительной при выполнении условия:
При невыполнении условия (11) контрольную процедуру повторяют. При повторном невыполнении условия (11) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
Примечание — Допустимо показатели точности измерений при внедрении методики в лаборатории устанавливать на основе выражения: U л = 0,84·U(X) с последующим уточнением по мере накопления информации в процессе контроля стабильности результатов анализа.
Таблица А.1 — Бюджет неопределенности измерений
Стандартная относительная неопределенность 3 , %
Приготовление градуировочных растворов, u 1 , %
Степень чистоты реактивов и дистиллированной воды, u 2 , %
Подготовка проб к анализу, u 3 , %
Стандартное отклонение результатов измерений, полученных в условиях повторяемости 4 , ur (σ r ), %
Стандартное отклонение результатов измерений, полученных в условиях промежуточной прецизионности 4 , uI ( TOE ) (σ I (ТОЕ) ), %
Стандартное отклонение результатов измерений, полученных в условиях воспроизводимости, uR (σ R ), %
Суммарная стандартная относительная неопределенность, u с , %
Расширенная относительная неопределенность, (Uотн.) при k = 2, %
1 Оценка (неопределенности) типа А получена путем статистического анализа ряда наблюдений.
2 Оценка (неопределенности) типа В получена способами, отличными от статистического анализа ряда наблюдений.
3 Соответствует характеристике относительной погрешности при доверительной вероятности Р = 0,95.
4 Согласно ГОСТ Р ИСО 5725-3-2002 учтено при расчете стандартного отклонения результатов измерений, получаемых в условиях воспроизводимости.
источник
ПНД Ф 14.1;2.61-96 Количественный химический анализ вод. Методика выполнения измерений массовой концентрации марганца в природных и сточных водах
МИНИСТЕРСТВО ОХРАНЫ ОКРУЖАЮЩЕЙ СРЕДЫ И ПРИРОДНЫХ
РЕСУРСОВ РОССИЙСКОЙ ФЕДЕРАЦИИ
Утвердаю
заместитель Министра
________ В.Ф. Костин
»__» марта 1996 г.
КОЛИЧЕСТВЕННЫЙ ХИМИЧЕСКИЙ АНАЛИЗ ВОД
МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ МАССОВОЙ
КОНЦЕНТРАЦИИ МАРГАНЦА В ПРИРОДНЫХ И СТОЧНЫХ
ВОДАХ ФОТОМЕТРИЧЕСКИМ МЕТОДОМ С ПРИМЕНЕНИЕМ
ПЕРСУЛЬФАТА АММОНИЯ.
Методика допущена для целей государственного экологического контроля.
Москва 1996 г.
(издание 2004 г.)
Настоящий документ устанавливает методику количественного химического анализа проб природных и сточных вод для определения в них ионов марганца при массовой концентрации от 0,05 до 5,0 мг/дм 3 фотометрическим методом с применением персульфата аммония без разбавления и концентрирования пробы.
Если массовая концентрация ионов марганца в анализируемой пробе превышает верхнюю границу диапазона, то допускается разбавление пробы таким образом, чтобы концентрация ионов марганца соответствовала регламентированному диапазону.
Если массовая концентрация ионов марганца в анализируемой пробе ниже минимально определяемой по методике концентрации, то допускается концентрирование выпариванием.
Мешающие влияния, обусловленные присутствием в пробе органических веществ, хлорид-ионов и железа устраняются специальной подготовкой пробы к анализу (п. 9).
Фотометрический метод определения массовой концентрации ионов марганца основан на окислении ионов марганца ( 2+ ) до перманганат-ионов в азотнокислой среде действием персульфата аммония в присутствии катализатора — ионов серебра с последующим измерением оптической плотности раствора при ? = 540 нм.
2. ПРИПИСАННЫЕ ХАРАКТЕРИСТИКИ ПОГРЕШНОСТИ ИЗМЕРЕНИЙ И ЕЕ СОСТАВЛЯЮЩИХ
Настоящая методика обеспечивает получение результатов анализа с погрешностью, не превышающей значений, приведённых в таблице 1.
Значения показателей точности, повторяемости и воспроизводимости методики
Показатель точности (границы относительной погрешности при вероятности Р = 0,9) ± ?, %
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости), ?r, %
Показатель воспроизводимости (относительное среднеквадратическое отклонение воспроизводимости), ?R, %
Значения показателя точности методики используют при:
— оформлении результатов анализа, выдаваемых лабораторией;
— оценке деятельности лабораторий на качество проведения испытаний;
— оценке возможности использования результатов анализа при реализации методики в конкретной лаборатории.
3. СРЕДСТВА ИЗМЕРЕНИЙ. ВСПОМОГАТЕЛЬНОЕ ОБОРУДОВАНИЕ. МАТЕРИАЛЫ. РЕАКТИВЫ
При выполнении измерений должны быть применены следующие средства измерений, оборудование и материалы.
3.1. Средства измерений, вспомогательное оборудование
Спектрофотометр или фотоколориметр, позволяющий измерять оптическую плотность при длине волны ? = 540 нм.
*Кюветы с толщиной поглощающего слоя 50 мм.
Весы лабораторные, 2 класса точности, ГОСТ 24104.
*Внесены дополнения и изменения согласно протокола № 23 заседания НТК ФП’ «ЦЭКА » МПР России от 30 мая 2001 г.
Сушильный шкаф электрический, ОСТ 16.0.801.397.
Плитка электрическая, ГОСТ 14919.
ГСО водного раствора с аттестованным содержанием марганца.
Колбы мерные 2-(50, 200)-2, ГОСТ 1770.
Колбы конические Кн-1-250-14/23 ТС, ГОСТ 25336.
Пипетки мерные с делениями 0,1 см 3 , 4(5)-2-1(2);
*Внесены дополнения и изменения согласно протокола № 23 заседания НТК ФП’ «ЦЭКА » МПР России от 30 мая 2001 г.
Стаканы Н-1-150 ТСХ, ГОСТ 25336.
Цилиндры 3-25 (50, 100), ГОСТ 1770.
Фарфоровые чашки для выпаривания.
Бутыли из стекла или полиэтилена с притертыми или винтовыми пробками вместимостью 500 — 1000 см 3 для отбора и хранения проб и реактивов.
Дистиллированная вода, ГОСТ 6779.
Азотная кислота, ГОСТ 4461.
Ортофосфорная кислота, ГОСТ 6552.
Ртуть (II) азотнокислая 1-водная, ГОСТ 4520.
Серебро азотнокислое, ГОСТ 1277.
Аммоний надсернокислый, ГОСТ 20478.
Соляная кислота, ГОСТ 3118.
Все реактивы, используемые для анализа, должны быть квалификации чда или хч.
4. ТРЕБОВАНИЯ БЕЗОПАСНОСТИ
4.1. При выполнении анализов необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007.
4.2. Электробезопасность при работе с электроустановками по ГОСТ 12.1.019.
4.3. Организация обучения работающих безопасности труда по ГОСТ 12.0.004.
4.4. Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004 и иметь средства пожаротушения по ГОСТ 12.4.009
5. ТРЕБОВАНИЯ К КВАЛИФИКАЦИИ ОПЕРАТОРОВ
Выполнение измерений может производить химик-аналитик, владеющий техникой фотометрического анализа и изучивший инструкции по эксплуатации спектрофотометра или фотоколориметра.
Измерения проводятся в следующих условиях:
температура окружающего воздуха (20 ± 5) °С;
атмосферное давление (84,0 — 106,7) кПа (630 — 800 мм.рт.ст);
относительная влажность (80 ± 5) %;
напряжение сети (220 ± 10) В;
частота переменного тока (50 ± 1) Гц.
7. ОТБОР И ХРАНЕНИЕ ПРОБ ВОДЫ
Отбор проб производится в соответствии с требованиями ГОСТ Р 51592-2000 «Вода. Общие требования к отбору проб».*
*Внесены дополнения и изменения согласно протокола № 23 заседания НТК ФП’ «ЦЭКА » МПР России от 30 мая 2001 г.
7.1. Пробы воды отбирают в стеклянные или полиэтиленовые бутыли, предварительно ополоснутые отбираемой водой. Объем отбираемой пробы должен быть не менее 200 см 3 .
7.2. *Пробы анализируют не позднее, чем через два часа после отбора или консервируют добавлением 5 см 3 концентрированной азотной кислоты на 1 дм 3 воды.
*Если требуется определить марганец в растворенной форме, пробу фильтруют через бумажный фильтр «синяя лента» до консервирования.
7.3. При отборе проб составляется сопроводительный документ по утвержденной форме, в котором указывается:
цель анализа, предполагаемые загрязнители;
должность, фамилия отбирающего пробу, дата.
*Внесены дополнения и изменения согласно протокола № 23 заседания НТК ФП’ «ЦЭКА » МПР России от 30 мая 2001 г.
8. ПОДГОТОВКА К ВЫПОЛНЕНИЮ ИЗМЕРЕНИЙ
Подготовку спектрофотометра или фотоэлектроколориметра к работе проводят в соответствии с рабочей инструкцией по эксплуатации прибора.
8.2. Приготовление растворов
8.2.1. Приготовление раствора нитрата ртути (II).
Растворяют 17,131 г Hg(NO3)2•H2O в дистиллированной воде, смочив сначала 1 см 3 концентрированной азотной кислоты и разбавляют до 1 дм 3 .
1 см 3 полученного раствора эквивалентен 3,54 мг хлорид-ионов.
8.2.2.Приготовление раствора персульфата аммония.
Растворяют 20 г персульфата аммония (NH4)2S2O8 в 80 см 3 дистиллированной воды.
8.2.3. Приготовление раствора нитрата серебра.
Растворяют 16,9874 г AgNO3 в дистиллированной воде и разбавляют до 1 дм 3 .
8.2.4. Приготовление основного раствора марганца из ГСО с аттестованным содержанием марганца.
Раствор готовят в соответствии с прилагаемой к образцу инструкцией.
1 см 3 раствора должен содержать 0,01 мг марганца.
Раствор годен в течение месяца.
8.3. Построение градуировочного графика
Для построения градуировочного графика необходимо приготовить образцы для градуировки с массовой концентрацией ионов марганца от 0,05 до 0,5 мг/дм 3 . Условия анализа, его проведение должны соответствовать п. 6 и 10.
Состав и количество образцов для градуировки для построения градуировочного графика приведены в таблице 2. Погрешность, обусловленная процедурой приготовления образцов для градуировки, не превышает 2,5 %.
Состав и количество образцов для градуировки при анализе ионов марганца
Массовая концентрация марганца в градуировочных растворах, мг/дм 3
Аликвотная часть аттестованного раствора (см 3 ) с концентрацией 0,01 мг/см 3 помещенного в мерную колбу на 100 см 3
Анализ образцов для градуировки проводят в порядке возрастания их концентрации. Для построения градуировочного графика каждую искусственную смесь необходимо фотометрировать 3 раза с целью исключения случайных результатов и усреднения данных. При построении градуировочного графика по оси ординат откладывают значения оптической плотности, а по оси абсцисс — величину концентрации вещества в мг/дм 3 .
8.4. Контроль стабильности градуировочной характеристики
Контроль стабильности градуировочной характеристики проводят не реже одного раза в месяц или при смене партии реактивов. Средствами контроля являются вновь приготовленные образцы для градуировки (не менее 3 образцов из приведенных в таблице 2).
Градуировочную характеристику считают стабильной при выполнении для каждого образца для градуировки следующего условия:
где Х — результат контрольного измерения массовой концентрации ионов марганца в образце для градуировки;
С — аттестованное значение массовой концентрации ионов марганца в образце для градуировки;
— среднеквадратическое отклонение внутрилабораторной прецизионности, установленное при реализации методики в лаборатории.
Примечание. Допустимо среднеквадратическое отклонение внутрилабораторной прецизионности при внедрении методики в лаборатории устанавливать на основе выражения: с последующим уточнением по мере накопления информации в процессе контроля стабильности результатов анализа.
Значения приведены в таблице 1.
Если условие стабильности градуировочной характеристики не выполняется только для одного образца для градуировки, необходимо выполнить повторное измерение этого образца с целью исключения результата, содержащего грубую погрешность.
Если градуировочная характеристика нестабильна, выясняют причины и повторяют контроль с использованием других образцов для градуировки, предусмотренных методикой. При повторном обнаружении нестабильности градуировочной характеристики строят новый градуировочный график.
9. УСТРАНЕНИЕ МЕШАЮЩИХ ВЛИЯНИЙ
9.1. Для устранения мешающего влияния хлорид-ионов, если концентрация их не превышает 300 мг/дм 3 , предлагается вводить раствор соли ртути (II), образующей с хлорид-ионами малодиссоциированное соединение. При более высоком содержании хлорид-ионов проводят предварительную обработку азотной и серной кислотами.
9.2. Мешают определению органические вещества при большой их концентрации (ХПК превышает 16 мг/дм 3 ). При высоком содержании органических веществ следует прибавить в пробу по 5 см 3 концентрированной азотной и концентрированной серной кислоты, выпарить в фарфоровой чашке до появления паров серной кислоты и после охлаждения растворить остаток в 5 см 3 азотной кислоты, добавляя дистиллированную воду до 100 см 3 . При меньшем содержании органических веществ можно ограничиться кипячением пробы 5 — 10 минут с добавлением 10 см 3 концентрированной азотной кислоты на 100 см 3 .
9.3. Мешающее влияние железа устраняют добавлением 1 см 3 концентрированной фосфорной кислоты в пробу, до окисления персульфатом.
При выполнении измерений массовой концентрации ионов марганца в пробах природных и сточных вод выполняют следующие операции:
К 100 см 3 пробы, если надо предварительно разбавленной или упаренной, приливают 3 см 3 концентрированной азотной кислоты и такой объем раствора нитрата ртути (п. 8.2.1) чтобы он был эквивалентен содержанию хлорид-ионов во взятой пробе, и сверх того еще 2 см 3 . Добавляют, если надо фосфорную кислоту (d = 1,7 г/см 3 ), нагревают до кипения, прибавляют 5 см 3 раствора персульфата аммония (п. 8.2.2), 2 капли раствора нитрата серебра (п. 8.2.3) и кипятят 5 мин.
После охлаждения раствора, его переносят в мерную колбу вместимостью 200 см 3 , разбавляют дистиллированной водой до метки и перемешивают. Оптическую плотность измеряют при ? = 540 нм по отношению к холостому опыту в кювете с толщиной слоя 50 мм.
Содержание ионов марганца находят по градуировочному графику.
11. ОБРАБОТКА РЕЗУЛЬТАТОВ ИЗМЕРЕНИЙ
Содержание ионов марганца X (мг/дм 3 ) рассчитывают по формуле:
*
где С — концентрация ионов марганца, найденная по градуировочному графику, мг/дм 3 ;
К — коэффициент разбавления или концентрирования.*
*Внесены дополнения и изменения согласно протокола № 23 заседания НТК ФП’ «ЦЭКА » МПР России от 30 мая 2001 г.
За результат анализа Хср принимают среднее арифметическое значение двух параллельных определений X1 иХ2
для которых выполняется следующее условие:
(1)
где r — предел повторяемости, значения которого приведены в таблице 3.
Значения предела повторяемости вероятности Р = 0,95
Диапазон измерений, мг/дм 3
Предел повторяемости (относительное значение допускаемого расхождения между двумя результатами параллельных определений), r, %
При невыполнении условия (1) могут быть использованы методы проверки приемлемости результатов параллельных определений и установления окончательного результата согласно раздела 5 ГОСТ Р ИСО 5725-6.
Расхождение между результатами анализа, полученными в двух лабораториях, не должно превышать предела воспроизводимости. При выполнении этого условия приемлемы оба результата анализа, и в качестве окончательного может быть использовано их среднее арифметическое значение. Значения предела воспроизводимости приведены в таблице 4.
Значения предела воспроизводимости при вероятности Р = 0,95
Диапазон измерений, мг/дм 3
Предел воспроизводимости (относительное значение допускаемого расхождения между двумя результатами измерений, полученными в разных лабораториях), R, %
При превышении предела воспроизводимости могут быть использованы методы оценки приемлемости результатов анализа согласно раздела 5 ГОСТ Р ИСО 5725-6.
12. ОФОРМЛЕНИЕ РЕЗУЛЬТАТОВ АНАЛИЗА
12.1. Результат анализа Хcp в документах, предусматривающих его использование, может быть представлен в виде:
где ? — показатель точности методики.
Значение ? рассчитывают по формуле:
Значение ? приведено в таблице 1.
Допустимо результат анализа в документах, выдаваемых лабораторией, представлять в виде: при условии
где Хср — результат анализа, полученный в соответствии с прописью методики;
± ?R — значение характеристики погрешности результатов анализа, установленное при реализации методики в лаборатории и обеспечиваемое контролем стабильности результатов диализа.
Примечание. При представлении результата анализа в документах, выдаваемых лабораторией, указывают:
— количество результатов параллельных определений, использованных для расчета результата анализа;
— способ определения результата анализа (среднее арифметическое значение или медиана результатов параллельных определений).
12.2. В том случае, если массовая концентрация ионов марганца в анализируемой пробе превышает верхнюю границу диапазона, то допускается разбавление пробы таким образом, чтобы массовая концентрация ионов марганца соответствовала регламентированному диапазону.
Результат анализа Хср в документах, предусматривающих его использование, может быть представлен в виде:
где ±?’ — значение характеристики погрешности результатов анализа, откорректированное на величину погрешности взятия аликвоты.
12.3. Если массовая концентрация ионов марганца в анализируемой пробе ниже минимально определяемой по методике концентрации, то допускается концентрирование выпариванием. В этом случае одновременно с анализируемой пробой ведут контрольный анализ аттестованного раствора с содержанием ионов марганца или соответствующим содержанию их в исходной рабочей пробе.
Результат анализа исходной рабочей пробы признают удовлетворительным, если выполняется следующее условие:
где X — результат контрольного измерения массовой концентрации ионов марганца в образце для контроля (аттестованном растворе);
С — аттестованное значение массовой концентрации ионов марганца в образце для контроля (аттестованном растворе);
К — норматив оперативного контроля процедуры анализа.
— значение характеристики погрешности результатов анализа, откорректированное на величину концентрирования пробы.
13. КОНТРОЛЬ КАЧЕСТВА РЕЗУЛЬТАТОВ АНАЛИЗА ПРИ РЕАЛИЗАЦИИ МЕТОДИКИ В ЛАБОРАТОРИИ
Контроль качества результатов анализа при реализации методики в лаборатории предусматривает:
— оперативный контроль процедуры анализа (на основе оценки погрешности при реализации отдельно взятой контрольной процедуры);
— контроль стабильности результатов анализа (на основе контроля стабильности среднеквадратического отклонения повторяемости, среднеквадратического отклонения внутрилабораторной прецизионности, погрешности).
13.1 Алгоритм оперативного контроля процедуры анализа с использованием метода добавок
Оперативный контроль процедуры анализа проводят путем сравнения результата отдельно взятой контрольной процедуры Кк с нормативом контроля К.
Результат контрольной процедуры Кк рассчитывают по формуле
где X’cp — результат анализа массовой концентрации ионов марганца в пробе с известной добавкой — среднее арифметическое двух результатов параллельных определений, расхождение между которыми удовлетворяет условию (1) раздела 11.
Хcp — результат анализа массовой концентрации ионов марганца в исходной пробе — среднее арифметическое двух результатов параллельных определений, расхождение между которыми удовлетворяет условию (1) раздела 11.
Норматив контроля K рассчитывают по формуле
где — значения характеристики погрешности результатов анализа, установленные в лаборатории при реализации методики, соответствующие массовой концентрации ионов марганца в пробе с известной добавкой и в исходной пробе соответственно.
Примечание. Допустимо характеристику погрешности результатов анализа при внедрении методики в лаборатории устанавливать на основе выражения: с последующим уточнением по мере накопления информации в процессе контроля стабильности результатов анализа.
Процедуру анализа признают удовлетворительной, при выполнении условия:
(2)
При невыполнении условия (2) контрольную процедуру повторяют. При повторном невыполнении условия (2) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
13.2 Алгоритм оперативного контроля процедуры анализа с применением образцов для контроля
Оперативный контроль процедуры анализа проводят путем сравнения результата отдельно взятой контрольной процедуры Кк с нормативом контроля К.
Результат контрольной процедуры Кк рассчитывают по формуле
где Сcp — результат анализа массовой концентрации ионов марганца в образце для контроля — среднее арифметическое двух результатов параллельных определений, расхождение между которыми удовлетворяет условию (1) раздела 11;
С — аттестованное значение образца для контроля.
Норматив контроля К рассчитывают по формуле:
где ±?л — характеристика погрешности результатов анализа, соответствующая аттестованному значению образца для контроля.
Примечание. Допустимо характеристику погрешности результатов анализа при внедрении методики в лаборатории устанавливать на основе выражения: с последующим уточнением по мере накопления информации в процессе контроля стабильности результатов анализа.
Процедуру анализа признают удовлетворительной, при выполнении условия:
(3)
При невыполнении условия (3) контрольную процедуру повторяют. При повторном невыполнении условия (3) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
Периодичность оперативного контроля процедуры анализа, а также реализуемые процедуры контроля стабильности результатов анализа регламентируют в Руководстве по качеству лаборатории.
ГОСУДАРСТВЕННЫЙ КОМИТЕТ РОССИЙСКОЙ ФЕДЕРАЦИИ ПО СТАНДАРТИЗАЦИИ И МЕТРОЛОГИИ
ФГУП «УРАЛЬСКИЙ НАУЧНО-ИССЛЕДОВАТЕЛЬСКИЙ ИНСТИТУТ МЕТРОЛОГИИ» — ГОСУДАРСТВЕННЫЙ НАУЧНЫЙ МЕТРОЛОГИЧЕСКИЙ ЦЕНТР
«THE URALS RESEARCH INSTITUTE FOR METROLOGY» — STATE SCIENTIFIC METROLOGICAL CENTRE
620219, Екатеринбург,
ГСП-324,
ул. Красноармейская, 4, лаб. 224
факс (3432) 302-117
Телефон: (3432) 302-295
E-mail:
Dept. 224, 4,
Krasnoarmeyskaya, Str.,
620219, GBR-824,
Ekaterinburg, Russia
Fax: (3432) 302-117
Phone: (3432) 302-295
E-mail:
об аттестации методики выполнения измерений
Методика выполнения измерений массовой концентрации марганца в природных и сточных водах фотометрическим методом с применением персульфата аммония.
Разработанная ФГУ «Центр экологического контроля и анализа» МПР России (г.Москва).
аттестована в соответствии с ГОСТ Р 8.563-96.
Аттестация осуществлена по результатам метрологической экспертизы материалов по разработке методики выполнения измерений.
В результате аттестации установлено, что методика соответствует предъявляемым к ней метрологическим требованиям и обладает следующими основными метрологическими характеристиками:
1. Диапазон измерений, значения показателей точности, повторяемости, воспроизводимости
Диапазон измерений, мг/дм 3
Показатель точности (границы относительной погрешности при вероятности Р = 0,95),
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости),
Показатель воспроизводимости (относительное среднеквадратическое отклонение воспроизводимости),
источник
Провести в частный дом водопровод сейчас не составляет особого труда – было бы время и финансовые возможности. Многие в качестве источника воды используют скважины. Хорошо, если вам повезло, и вода в скважине соответствует санитарным и прочим нормам. А если нет, и в ней присутствуют вредные химические вещества? Тот же марганец встречается в воде не столь уж и редко. И если его концентрация слишком высокая, воду необходимо очищать. Сегодня мы поговорим о том, как это лучше сделать.
Из этой статьи вы узнаете:
- Как влияет на организм человека повышенный марганец в воде
- Чем опасен марганец в воде, и каковы нормы его содержания
- Как можно определить марганец в воде
- Какими методами осуществляется очистка воды от марганца
- Какие фильтры используются для очистки воды от марганца
Использовать в своих целях марганец люди научились очень давно. Еще естествоиспытатель из Древнего Рима Плиний Старший писал о разновидности магнитного железняка, с помощью которого можно осветлять стекло. Возможно, Плиний пошел бы в своих исследованиях и дальше, но он погиб во время извержения Везувия. В XVI веке знаменитый алхимик Альберт Великий назвал этот минерал магнезией. И только в конце восемнадцатого столетия шведский ученый Карл Шелле определил, что к магнитному железняку магнезия никакого отношения не имеет, а является соединением неизвестного еще металла. Первым металлический марганец в 1774 году получил друг Шелле – химик Юхан Готлиб Ганн.
Марганец – весьма распространенный элемент, занимающий четырнадцатое место по распространенности на планете. Он есть буквально везде: в земле, в воде, в растениях и животных. Свойства марганца таковы, что его можно использовать в самых разнообразных сферах жизни – от промышленности до медицины. Даже в быту применение марганца – не редкость.
В организме человека марганца совсем немного, микроскопическое количество, но значение его сложно переоценить. К примеру, без марганца мы бы не могли усваивать витамин В1, который отвечает за работу нервной и пищеварительной систем организма. Даже нормальная работа сердца зависит от В1, а значит, и от марганца. При недостаточном его количестве увеличивается риск развития диабета. Также этот микроэлемент помогает нормальному развитию костной системы.
Без определенной дозы марганца в организме нам не обойтись. И это количество давно уже подсчитано учеными-медиками:
- Норма в сутки для взрослого – до 5 мг;
- Для ребенка до 15 лет – 2 мг;
- Для ребенка до года – 1 мг.
Однако как сказал Гиппократ: «Все есть лекарство, и все есть яд – все дело в дозе». Так же и с марганцем. Большое количество этого микроэлемента в организме не принесет человеку ничего хорошего. Если содержание марганца превышено в восемь раз – нарушаются функции мозга. Наиболее опасно систематическое отравление марганцем.
Безопасных источников воды для питья в сегодняшнее время не так уж и много. Как правило, любую природную воду приходится очищать, чем и занимаются водоочистные станции. В некоторых районах нашей страны почва особенно богата солями марганца, и при использовании на этих территориях воды из подземных источников возникает соответствующая проблема. Излишки марганца из воды необходимо убирать, чтобы сохранить здоровье людей.
Марганец нечасто встречается в чистом виде, зато входит в состав большого числа минералов. Некоторые кислые и железистые руды также содержат марганец. Казалось бы, какое это имеет отношение к источникам воды, как марганец в них попадает? Есть два основных способа:
- Природный. Марганец вымывается водой из содержащих его минералов. Также в весьма значительных количествах он может поступать в воду от разложившихся водных животных и растительных организмов (особенно сине-зеленых).
- Техногенный. Это сбрасываемые в водоемы отходы химических предприятий и металлургических комбинатов. Некоторые сельскохозяйственные удобрения тоже содержат марганец, который затем попадает в воду.
Много ли в итоге марганца содержится в воде? Тут многое зависит от местности и от того, какая именно вода имеется в виду. Меньше всего его в морских водах – порядка двух микрограммов на кубический дециметр. В речных – от 1 до 160 мкг. Но абсолютный рекордсмен здесь – воды подземные. В них могут содержаться сотни и даже тысячи микрограммов на кубический дециметр. Довольно часто марганец содержится в воде вместе с железом, хотя концентрация его и меньше.
Количество марганца в воде – величина непостоянная, она изменяется в зависимости от сезона. Зимой и летом содержание тяжелых металлов в водоемах больше – из-за застоя воды. А вот весной и осенью дело обстоит с точностью до наоборот. Есть и другие факторы, от которых зависит уровень марганца в питьевой воде. Например:
- Температура;
- Количество кислорода;
- pH (водородный показатель);
- Насколько активно водные организмы поглощают или, наоборот, выделяют марганец;
- Связаны ли водохранилища с местными озерами или реками;
- Объем марганца, попавшего в стоки и т. п.
Согласно нормам Всемирной организации здравоохранения, количество марганца в воде не должно превышать 0,05 миллиграмма на литр. К сожалению, не везде они соблюдаются. В США, например, содержание марганца местами десятикратно превышает допустимый уровень. В России установленная норма для питьевой воды – не больше 0,1 миллиграмма на литр. Впрочем, эта же цифра актуальна и для воды хозяйственного назначения.
Когда марганца в воде слишком много, это плохо отражается не только на здоровье человека. Страдает и куда более устойчивая к химическим воздействиям бытовая техника и даже водопроводная система.
Влияние марганца на водопроводную систему и бытовую технику:
- Из-за отложений марганца ухудшается проходимость водопроводных труб, снижается продолжительность их службы.
- То же касается и системы отопления: налет марганца в трубах снижает теплоотдачу.
- Трубы могут полностью закупориться – «благодаря» марганцевым бактериям. Все происходит так же, как и в случае действия железобактерий.
- Большое количество марганца в воде плохо влияет на электроприборы. Накипь в чайнике или стиральной машине зачастую образуется как раз из-за этого вещества.
- Если на сантехнике или бытовых приборах появились черные пятна – это может быть свидетельством того, что в воде слишком высокое содержание марганца.
Человеческое здоровье куда более хрупко, чем бытовые приборы. Именно поэтому за водой, которой вы пользуетесь, нужно внимательно следить. Если вдруг у воды появился слегка желтоватый оттенок и она стала неприятной на вкус не только сама по себе, но даже в чае или кофе – верный признак того, что концентрация марганца в ней недопустимо высока.
Чем именно опасны излишки марганца в организме человека? Прежде всего, негативным влиянием на нервную систему. Для детей это особенно опасно. Согласно проведенным исследованиям, высокая концентрация марганца в организме ребенка может повлиять на его интеллектуальные способности.
Если концентрация металла в организме слишком велика, может возникнуть общее отравление. Главные симптомы его следующие:
- У человека снижается аппетит;
- Болит и кружится голова;
- Возникают судороги, боль в спине;
- Случаются смены настроения;
- У больного общий упадок сил и апатия.
Если постоянно пить воду с высокой концентрацией марганца, то:
- Может ухудшиться состояние скелета;
- Возможно снижение мышечного тонуса, даже развиться мышечная атрофия;
- Не исключено появление аллергии;
- Могут пострадать почки, печень, тонкий кишечник и даже головной мозг;
- Велик риск развития раковых заболеваний и болезни Паркинсона.
Марганец – это тяжелый металл, имеющий свойство постепенно накапливаться в организме. При постоянном употреблении воды с излишней концентрацией марганца рано или поздно пострадает нервная система человека. Тут можно выделить три стадии недуга :
При первой стадии нарушения нервной системы имеют функциональный характер. Человек быстрее утомляется, ему периодически или даже постоянно хочется спать. Руки и ноги ослабевают, появляются симптомы вегетативной дистонии. Присутствуют повышенная потливость и слюноотделение. Мускулы лица, наоборот, могут быть ослаблены, что неизбежно скажется на мимике. Также понижается мышечный тонус, в руках или ногах чувствуется онемение.
Психическая деятельность такого больного тоже меняется, хотя и не всегда это заметно для постороннего наблюдателя. Выражается это в следующих моментах:
- Область интересов такого больного становится более ограниченной;
- Активность также снижается;
- Способность к ассоциативному мышлению притупляется;
- Ослабляется память.
Показательно то, что больной не может адекватно оценивать свое состояние. А потому очаговые неврологические симптомы интоксикации у него довольно сложно диагностировать даже специалисту. В этом случае, если вовремя не выявить причину болезни (а именно: высокую концентрацию марганца в организме), то недуг можно запустить. Тогда повреждения могут стать необратимыми.
На второй стадии болезни симптомы токсической энцефалопатии нарастают. А именно:
- Человек становится все более апатичным;
- Его все чаще клонит в сон;
- Прогрессирует общая слабость, снижается работоспособность;
- Углубляется мнестико-интеллектуальный дефект;
- Появляются признаки экстрапирамидной недостаточности: замедленность движений, ослабление мимики лица, непроизвольное сокращение мышц и т. д.
Кроме этого, нарушается деятельность эндокринных желез, более явными становятся признаки онемения конечностей. Второй этап болезни очень опасен. Дело в том, что даже если причина недуга найдена и контакта с марганцем больше нет, процесс на этом не останавливается. Более того, в течение еще нескольких лет он будет только развиваться. Приостановить болезнь в конечном итоге получится, но окончательного выздоровления добиться, скорее всего, не удастся.
Последняя стадия отравления – марганцевый паркинсонизм – характеризуется тяжелыми расстройствами двигательных функций. У больного:
- Нарушается произношение;
- Речь становится монотонной, почерк – невнятным;
- Лицо маскообразное;
- Очень низкая двигательная активность;
- Спастико-паретическая походка (человек слишком широко расставляет ноги при ходьбе, его шатает из стороны в сторону);
- Парез стоп – когда во время ходьбы стопа может «волочится» по земле.
Кроме этого, происходят непроизвольные излишние движения мышц – в основном, в ногах. Иногда, напротив, тонус мышц значительно понижается. Психика больного также изменяется. Люди, подвергшиеся отравлению марганцем, испытывают апатию или же, наоборот, излишне благодушны и даже эйфоричны. Возможен беспричинный смех или плач. Зачастую человек не понимает, что он болен, или же считает, что его недуг несерьезен. Мнестико-интеллектуальный дефект прогрессирует. Больной плохо определяет время, у него ухудшается память, возникают проблемы как в профессиональной, так и в социальной деятельности.
Последствия, как видите, очень тяжелые. Именно поэтому так важно вовремя определить причину болезни. И если ею является высокая концентрация марганца в воде, нужно немедленно принять меры. Следует помнить: организм человека получает марганец не только употребляя пищу, приготовленную на «плохой» воде. В данном случае даже просто чистить зубы или умываться загрязненной водой весьма опасно.
Не случайно марганец называют вечным спутником железа. Если в воде, которой вы пользуетесь, есть железо – там обязательно присутствует и марганец. Но не наоборот. Даже когда в воде нет железа, там вполне может присутствовать марганец. О последствиях переизбытка этого элемента в организме человека мы уже говорили. Поэтому воду от марганца нужно обязательно очищать.
Как заметить, что в воде высокая концентрация марганца, не делая при этом специального химического анализа? Есть несколько признаков, на которые стоит обратить внимание:
- Вода становится мутной и темной, если в ней присутствуют соединения марганца;
- Обратите внимание на запах. Если он покажется вам необычным, это уже тревожный признак;
- Если воду отстоять, на дно посуды выпадет черный осадок;
- Когда в воде много марганца, то после долгого контакта с ней ваши руки и ногти обязательно окрасятся в черный цвет.
И это далеко не все признаки. Если такую воду вскипятить, то на посуде останется черный налет. У воды с высоким содержанием марганца не только странный запах, но и неприятный вяжущий вкус. Темные пятна на сантехнике, отложения в водопроводных трубах или даже их полная закупорка – тоже «вина» этого элемента. Вы почувствовали, что в квартире стало холоднее? Возможно, внутри системы отопления появился налет марганца, что затрудняет процесс теплообмена.
Наличие хотя бы одного из этих признаков – уже повод хорошо задуматься. В этом случае надо сразу ограничить потребление воды с возможным наличием в ней марганца. И обязательно сделать анализ, обратившись в санитарную станцию или частную лабораторию. Результаты вам предоставят примерно через 3–7 дней.
Для начала специалисты проводят анализ воды на концентрацию марганца, и только после этого выбирают наиболее подходящий способ ее очистки.
Марганец в земных породах чаще всего находится в виде соли, которая хорошо растворяется в воде. Следовательно, чтобы очистить воду от марганца, нужно сделать так, чтобы этот элемент перестал быть растворимым. Тут на помощь приходит химия. Двухвалентный марганец преобразуют в трех- или четырехвалентный с помощью окисления. Гидроксиды марганца с валентностью 2 и 3 в воде почти не растворяются.
Есть несколько методов окисления марганца:
- С помощью сильных окислителей, которые увеличивают окислительно-восстановительный потенциал среды. При этом значении рН воды не регулируется.
- Используют слабые окислители с одновременным повышением значения рН воды.
- Повышают значение рН воды, используя вместе с этим сильные окислители.
Двухвалентный марганец превращается в четырехвалентный гидроксид марганца и оседает на фильтрах. Кроме того, он сам превращается в катализатор, который ускоряет процесс окисления оставшегося в воде двухвалентного марганца при помощи растворенного кислорода.
Этот способ весьма доступный, а потому и наиболее распространенный. Проводится серьезная аэрация марганца, затем – фильтрация. Сначала из воды под вакуумом выделяют свободную углекислоту, что повышает степень показателя pH до 8,0–8,5 единиц. После этого наступает очередь работы фильтра. В качестве него используется зернистый наполнитель, например, кварцевый песок.
Однако данный метод подходит не для всех случаев. Его не применяют, если перманганатная окисляемость воды больше 9,5 мгО2/л. Для использования этого способа требуется наличие в воде двухвалентного железа, которое при окислении превращается в гидроксид железа. Он, в свою очередь, впитывает в себя двухвалентный марганец и окисляет его. Еще условие: соблюдение строгого соотношения между марганцем и двухвалентным железом – семь к одному. Впрочем, последний пункт можно искусственно подправить, добавив в воду железный купорос.
Гидроксид четырехвалентного марганца (образовавшийся на поверхности фильтра с помощью дозирующего насоса) окисляет двухвалентный оксид марганца. Полученный после этого трехвалентный оксид с помощью растворенного кислорода окисляется до нерастворимого в воде состояния.
Можно использовать для очистки и подземных, и наружных вод. Перманганат калия окисляет растворенный в воде марганец, превращая его в оксид, который растворяется в воде гораздо хуже. Оксид марганца, в свою очередь, хороший катализатор для растворения двухвалентного марганца. Чтобы избавиться от 1 мг последнего, нужно 1,92 мг перманганата калия. При таком соотношении 97 процентов двухвалентного марганца окислятся.
После этого воду надо профильтровать с помощью специального коагулянта, затем дополнительно используется песчаный наполнитель. Иногда задействуют и ультрафильтрующее оборудование.
Для окисления марганца в воде используют разные реагенты. Но в основном это хлор, его диоксид, гипохлорит натрия и озон. Здесь очень важно учитывать уровень рН воды. Если в воду с показателем pH не меньше 8,0–8,5 добавить хлор, то хорошего эффекта придется дожидаться примерно час-полтора. Такое же время действует и гипохлорит натрия. Часто обрабатываемую воду нужно подщелачивать. Это делается в тех случаях, когда в качестве окислителя выступает кислород и показатель pH воды не достигает 7 единиц.
Расчеты показывают, что для превращения двухвалентного марганца в четырехвалентный, на один мг марганца нужно брать 1,3 мг вещества-реагента. Но это в голой теории, на практике окислителя обычно требуется гораздо больше.
Диоксид хлора или озон при обработке ими воды действуют гораздо быстрее – всего около четверти часа. Правда, только в том случае, если показатель pH воды составляет 6,5–7,0 единиц. По расчетам стехиометрии, на 1 мг двухвалентного марганца уйдет 1,35 мг диоксида хлора или 1,45 мг озона. Но опять же озона потребуется больше, нежели в теоретических выкладках. Происходит так потому, что в процессе озонирования оксиды марганца озон разлагают.
Вообще, причин, по которым реагентов требуется больше, чем указано в расчетах, несколько. На процесс окисления марганца в воде влияет множество факторов. Например, это уровень pH воды, наличие в ней органики, время действия используемых реагентов. Очень многое зависит от оборудования, которое применяется для процесса. Практика показывает, что перманганата калия обычно нужно брать в 1–6 раз больше, озона – в 1,5–5 раз, а оксида хлора и вовсе может потребоваться в 1,5–10-кратном размере.
Ионный обмен подразумевает водород- или натрий-катионирование воды. Чтобы эффективно удалить растворенные в воде соли марганца, ее нужно обработать в двух слоях ионообменного материала. Для этого применяются две смолы: катионообменная с ионами водорода H+ и анионообменная с ионами гидроксила OH-. Используются они одновременно и последовательно. Такая смесь смол заменяет растворимые в воде соли на ионы гидроксида OH- и водорода H+. При объединении этих ионов получаются самые обычные молекулы воды без наличия в них соли.
На данный момент такой способ избавления воды от примесей марганца и железа является наиболее многообещающим. Главное в нем – правильно подобрать комбинацию ионообменных смол.
В основе этого способа – превращение воды в пар с последующей его концентрацией. Всем давно известно, что температура кипения воды – 100 °С. Но это не значит, что у других веществ она будет такой же. На разнице температур кипения и основан данный метод очистки воды от марганца. Чистая вода закипает первой и превращается в пар. Другие элементы испаряются только после выкипания большей части воды. Таким образом, получаем чистую, без примесей, воду. Технология несложная и всем понятная, но весьма энергозатратная.
Фильтры в данном случае подобрать не так уж и просто. Тут следует действовать по системе. Во-первых, определить состав воды, которую нужно очистить от марганца. Во-вторых, обозначить минимальные требования к качеству воды после ее фильтрации. В-третьих, при выборе системы очистки нужно обратить внимание на следующие моменты:
- Каково содержание железа и марганца в воде;
- На уровень pH воды;
- На количество в воде кислорода или углекислого газа;
- Есть ли в воде аммиак или сероводород;
- Также важны характеристики водопровода: его производительность и напор воды.
После этого можно приступать к выбору фильтрующего материала для очищения воды от марганца. Есть несколько из них, которые пользуются наибольшей популярностью.
Фильтрующий материал СУПЕРФЕРОКС – предназначенный для удаления растворенных в воде ионов железа и марганца, а также снижения мутности и цветности воды. Основой фильтрующей среды является прочный природный материал «розовый песок» с нанесенной на его поверхность каталитической пленкой, состоящей из высших оксидов марганца. Действие СУПЕРФЕРОКС основано на 2 принципах: сорбционного (за счет пористой структуры материала) и каталитического окисления. При фильтрации воды, находящиеся в каталитической пленке оксиды марганца, ускоряют процесс окисления двухвалентного железа до трехвалентного с образованием соответствующего гидроксида. За счет пористости структуры материала образование гидроксида трехвалентного железа происходит как на поверхности зерен СУПЕРФЕРОКС, так и внутри его пор, что приводит к увеличению грязеемкости и ускорению процесса обезжелезивания воды. Образовавшийся гидроксид железа способен каталитически окислять двухвалентный марганец с образованием практически нерастворимых гидроксидов Мn(ОН)3 и Мn(ОН)4. По исчерпанию ресурса фильтра, для восстановления свойств фильтрующей среды необходимо произвести регенерацию установки обратным потоком исходной или очищенной воды (эффективнее водо-воздушной смесью).
Многокомпонентная ионообменная загрузка FeroSoft создана для комплексного решения задач в системах водоподготовки. Данная загрузка состоит из нескольких ионообменных смол разного гранулометрического состава позволяющих эффективно удалять из исходной воды соли жесткости (Ca2+ и Mg2+), примеси железа (Fe3+ и Fe2+), марганец (Mn2+), органические соединения. Загрузка разработана для решения наиболее типичных проблем с питьевой водой, максимально подходит для использования в системах водоподготовки загородных домов и коттеджей.
Неподготовленному человеку трудно самостоятельно выбрать подходящий фильтр для очистки воды. К счастью, для этого есть специалисты.
В компании Biokit работают профессионалы, которые помогут вам с выбором наилучшего варианта. Причем нет принципиальной разницы, это уже существующая система водоподготовки, или она пока находится на стадии проектирования. Оптимальное решение будет основываться на предоставленных данных.
Компания Biokit предлагает также широкий выбор систем обратного осмоса, фильтры для воды и другое оборудование, способное вернуть воде из-под крана ее естественные характеристики.
Специалисты нашей компании готовы помочь вам:
- Подключить систему фильтрации самостоятельно;
- Разобраться с процессом выбора фильтров для воды;
- Подобрать сменные материалы;
- Устранить неполадки или решить проблемы с привлечением специалистов-монтажников;
- Найти ответы на интересующие вопросы в телефонном режиме.
Доверьте очистку воды системам от Biokit – пусть ваша семья будет здоровой!
Статья была вам полезна? Поставьте лайк , это поможет нам создавать больше новых, интересных материалов!
источник
