Цель работы : определение фосфат-ионов в пробах природных вод.
Фосфор является необходимым элементом для жизни. Являясь важнейшим биогенным элементом, именно фосфор чаще всего лимитирует развитие продуктивности водоемов. Поэтому поступление избытка соединений фосфора с водосбора в виде минеральных удобрений с поверхностным стоком полей (с гектара орошаемых земель может выносится 0,4–0,6 кг фосфора), со стоками ферм (0,01–0,05 кг/ сут . на одно животное), с недоочищенными или неочищенными бытовыми сточными водами (0,003–0,006 кг/ сут . на одного жителя), а также с некоторыми производственными расходами приводит к резкому неконтролируемому приросту растительной биомассы водного объекта. Особенно характерен данный процесс для малопроточных и непроточных водоемов. Происходит изменение трофического статуса водоема, сопровождающееся перестройкой всего водного сообщества и ведущее к преобладанию гнилостных процессов (и, соответственно, возрастанию мутности, солености, концентрации бактерий).
В природных и сточных водах фосфор может присутствовать в разных видах. В растворенном состоянии (иногда говорят — в жидкой фазе анализируемой воды) он может находиться в виде ортофосфорной кислоты (Н3РО4) и ее анионов в виде мет а- , пиро — и полифосфатов (эти вещества используют для предупреждения образования накипи, они входят также в состав моющих средств). Кроме того, существуют разнообразные фосфорорганические соединения — нуклеиновые кислоты, нуклеопротеиды, фосфолипиды и др., которые также могут присутствовать в воде, являясь продуктами жизнедеятельности или разложения организмов. К фосфорорганическим соединениям относятся также некоторые пестициды.
Минерализация приводит к превращению в ортофосфаты все, даже труднорастворимые , формы фосфатов в воде. Таким образом, определяется содержание общего фосфора в любой воде (этот показатель можно определять как для растворенных фосфатов, так и для нерастворимых соединений фосфора). Однако для природных вод, не содержащих или содержащих незначительное количество трудногидролизующихся фосфатов в твердой фазе, минерализации обычно не требуется, и полученный при анализе гидролизованной пробы результат с хорошим приближением может быть принят за содержание общего фосфора.
ПДК полифосфатов ( триполифосфат и гексаметафосфат ) в воде водоемов составляет 3,5 мг/л в пересчете на ортофосфат-анион РО4 3- , лимитирующий показатель вредности – органолептический.
Диапазон определяемых концентраций ортофосфатов в воде при визуально-колориметрическом определении – от 0,2 до 7,0 мг/л, при фотометрическом определении – 0,01–0,4 мг/л. Определение визуально-колориметрическим методом возможно и при концентрации ортофосфатов более 7,0 мг/л после соответствующего разбавления пробы чистой водой.
Метод основан на получении восстановленной фосфорномолибденовой гетерополикислоты – «молибденовой сини».
При взаимодействии фосфатов с молибдатом ( VI ) в кислой среде образуется фосфорно-молибденовая гетерополикислота Н7 Р( Мо2О7)6, которая восстанавливается аскорбиновой кислотой в присутствии сурьмяно-виннокислого калия до фосфорно-молибденового комплекса, окрашенного в голубой цвет.
Оптическую плотность образованного фосфорно-молибденового комплекса определяют на фотоэлектроколориметре при красном светофильтре. Содержание фосфора фосфатов в пробе определяют по показаниям прибора, пересчитанным по предварительно построенному градуировочному графику.
– колбы мерные вместимостью 50, 100 см 3 ;
– цилиндры мерные вместимостью 50, 100 см 3 ;
– колбы конические плоскодонные вместимостью 100 см 3 ;
– смесь аскорбиновой и серной кислот.
1. В коническую плоскодонную колбу вместимостью 100 см 3 отбирают 50,0 см 3 отфильтрованной исследуемой пробы воды. Объем отбирают пипеткой вместимостью 50 см 3 . К пробе добавляют 10,0 см 3 смешанного реактива, и раствор хорошо перемешивают.
2. Через 10 мин на фотоэлектроколориметре измеряют оптическую плотность раствора при красном светофильтре в кювете с толщиной оптического слоя 5 см , используя в качестве сравнения дистиллированную воду.
3. Если исследуемая проба воды окрашена или слегка мутная, отдельно измеряют ее оптическую плотность относительно дистиллированной воды при красном светофильтре в кювете с толщиной оптического слоя 5 см , добавив к пробе 10 см 3 смеси серной и аскорбиновой кислот вместо смешанного индикатора.
4. По градуировочной характеристике полученному значению оптической плотности ставят в соответствие значение концентрации фосфат-ионов в исходной пробе воды. Содержание фосфатов ( Сх ) в мг/дм 3 находят по формуле:
где С о – концентрация фосфат-ионов , найденная по градуировочной характеристике, мг/дм 3 ;
n – степень разбавления исходной пробы воды (в случае, если исследуемую пробу не разбавляли, n = 1).
Форма записи результатов определения фосфат иона в пробах природных вод представлена ниже.
Таблица. Форма записи результатов определения фосфат-иона в пробах природных вод
Содержание
фосфат-иона ,
найденного
по градуировочному
графику мг/дм3
источник
ПНД Ф 14.1:2.112-97 Количественный химический анализ вод. Методика выполнения измерений массовой концентрации фосфат-ионов в пробах природных и очищенных сточных вод фотометрическим методом восстановлением аскорбиновой кислотой
МИНИСТЕРСТВО ОХРАНЫ ОКРУЖАЮЩЕЙ СРЕДЫ И ПРИРОДНЫХ
РЕСУРСОВ РОССИЙСКОЙ ФЕДЕРАЦИИ
Государственного комитета РФ
по охране окружающей среды
______________ А.А. Соловьянов
КОЛИЧЕСТВЕННЫЙ ХИМИЧЕСКИЙ АНАЛИЗ ВОД
МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ
МАССОВОЙ КОНЦЕНТРАЦИИ
ФОСФАТ-ИОНОВ В ПРОБАХ ПРИРОДНЫХ
И ОЧИЩЕННЫХ СТОЧНЫХ ВОД
ФОТОМЕТРИЧЕСКИМ МЕТОДОМ ВОССТАНОВЛЕНИЕМ АСКОРБИНОВОЙ КИСЛОТОЙ
Методика допущена для целей государственного экологического контроля.
Методика рассмотрена и одобрена Главным управлением аналитического контроля и метрологического обеспечения природоохранной деятельности (ГУАК) и Главным метрологом Минприроды РФ.
В соответствии с требованиями ГОСТ Р ИСО 5725-1-2002 ÷ ГОСТ Р ИСО 5725-6-2002 и на основании свидетельства о метрологической аттестации № 224.01.03.035/2004 в МВИ внесены изменения (Протокол № 1 заседания НТС ФГУ «ФЦАМ» МПР России от 03.03.2004).
Настоящий документ устанавливает методику количественного химического анализа проб природных и очищенных сточных вод для определения фосфат-ионов при массовой концентрации от 0,05 до 1 мг/дм 3 РО4 3- фотометрическим методом.
Если массовая концентрация фосфат-ионов в анализируемой пробе превышает верхнюю границу, то допускается разбавление пробы таким образом, чтобы концентрация фосфат-ионов соответствовала регламентированному диапазону.
Мешающие влияния, обусловленные присутствием в пробе сульфидов, сероводорода, хроматов, арсенатов, нитритов и железа, устраняют специальной подготовкой пробы к анализу (п. 9).
Фотометрический метод определения массовой концентрации фосфат-ионов основан на взаимодействии фосфат-ионов в кислой среде с молибдатом аммония и образованием фосфорно-молибденовой гетерополикислоты, которая восстанавливается аскорбиновой кислотой в присутствии сурьмяно-виннокислого калия до фосфорно-молибденового комплекса, окрашенного в голубой цвет. Максимум светопоглощения соответствует длине волны λ = 690 нм.
Настоящая методика обеспечивает получение результатов анализа с погрешностью, не превышающей значений, приведенных в таблице 1.
Значения показателей точности, повторяемости и воспроизводимости методики
Показатель точности (границы относительной погрешности при вероятности Р = 0,95), ± δ, %
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости) σr, %
Показатель воспроизводимости (относительное среднеквадратическое отклонение воспроизводимости), σ r , %
Значения показателя точности методики используют при:
— оформлении результатов анализа, выдаваемых лабораторией,
— оценке деятельности лабораторий на качество проведения испытаний;
— оценке возможности использования результатов анализа при реализации методики в конкретной лаборатории.
3.1 . Средства намерений, вспомогательное оборудование
Спектрофотометр или фотоэлектроколориметр, позволяющий измерять оптическую плотность при длине волны λ = 690 нм.
Кюветы с толщиной поглощающего слоя 20 или 50 мм.
Весы лабораторные 2-го класса точности, ГОСТ 24104.
ГСО с аттестованным содержанием фосфат-ионов.
Колбы мерные 2-50 (100, 500, 1000)-2, ГОСТ 1770.
Колбы конические Кн-2-100-18 ТХС, ГОСТ 25336.
Стаканы для взвешивания СВ, ГОСТ 25336.
Бутыли из стекла или полиэтилена с притертыми или винтовыми пробками для отбора и хранения проб вместимостью 500 — 1000 см 3 .
Аскорбиновая кислота, ГОСТ 4815.
Антимонилтартрат калия, ТУ 6-09-803.
Сульфаминовая кислота, ТУ 6-09-2391.
Комплексен III, ТУ 6-09-2391.
Фильтры обеззоленные, ТУ 6-09-1181.
Бумага индикаторная универсальная, ТУ 6-09-1181.
Все реактивы, должны быть квалификации ч.д.а. или х.ч.
4.1 . При выполнении анализов необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007 .
4.2 . Электробезопасность при работе с электроустановками по ГОСТ 12.1.019 .
4.3 . Организация обучения работающих безопасности труда по ГОСТ 12.0.004 .
4.4 . Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004 и иметь средства пожаротушения по ГОСТ 12.4.009 .
Выполнение измерений может производить химик-аналитик, владеющий техникой фотометрического анализа и изучивший инструкцию по эксплуатации спектрофотометра или фотоколориметра.
Измерения проводятся в следующих условиях:
температура окружающего воздуха (20 ± 5) °С;
атмосферное давление (84,0 — 106,7) кПа (630 — 800 мм рт.ст);
относительная влажность (80 ± 5) %;
напряжение сети (220 ± 10) В;
частота переменного тока (50 ± 1) Гц.
Отбор проб производится в соответствии с требованиями ГОСТ Р 51592-2000 «Вода. Общие требования к отбору проб».
7.1 . Пробы воды отбирают в стеклянные или полиэтиленовые бутыли, предварительно ополоснутые отбираемой водой. Объем отобранной пробы должен быть не менее 100 см 3 .
7.2 . Пробу анализируют в день отбора или консервируют добавлением 2 — 4 см 3 хлороформа на 1 дм 3 воды и хранят при 3 — 5 °С не более 3 суток.
7.3 . При отборе проб составляется сопроводительный документ, в котором указывается.
цель анализа, предполагаемые загрязнители;
должность, фамилия отбирающего пробу, дата.
Подготовку спектрофотометра или фотоэлектроколориметра к работе проводят в соответствии с руководством по его эксплуатации.
8.2 . Приготовление вспомогательных растворов
8.2.1 . Приготовление раствора молибдата аммония.
3 г молибдата аммония помещают в стакан, растворяют в небольшом количестве дистиллированной воды, переносят в мерную колбу на 100 см 3 и доводят до метки дистиллированной водой. В случае появления мути раствор следует отфильтровать.
Раствор хранят в полиэтиленовой бутыли.
8.2.2 . Приготовление раствора аскорбиновой кислоты.
2 ,16 г аскорбиновой кислоты помещают в стакан, растворяют в небольшом количестве дистиллированной воды, переносят в мерную колбу на 100 см 3 и доводят до метки дистиллированной водой.
Раствор хранят в холодильнике в течение 3-х недель.
8.2.3 . Приготовление раствора антимонилтартрата калия.
0 ,34 г антимонилтартрата калия помещают в стакан, растворяют в небольшом количестве дистиллированной воды, переносят в мерную колбу на 500 см 3 и доводят до метки дистиллированной водой.
В мерную колбу на 500 см 3 наливают 400 см 3 дистиллированной воды и осторожно приливают 70 см 3 концентрированной серной кислоты. После охлаждения, раствор доводят до метки дистиллированной водой.
В колбе с притертой пробкой смешивают 125 см 3 раствора серной кислоты (п. 8.2.4), 50 см 3 раствора молибдата аммония (п. 8.2.1), 50 см 3 раствора аскорбиновой кислоты (п. 8.2.2) и 25 см 3 раствора антимонилтартрата калия (п. 8.2.3).
Смешанный реактив готовят непосредственно перед использованием.
8.2.6 . Приготовление 10 %-го раствора сульфаминовой кислоты.
10 г сульфаминовой кислоты растворяют в 90 см 3 дистиллированной воды.
8.3 . Приготовление градуировочных растворов фосфат-ионов
8.3.1 . Приготовление градуировочного раствора 1.
Раствор готовят из ГСО в соответствии с прилагаемой к образцу инструкцией. В 1 см 3 раствора должно содержаться 0,01 мг фосфат-ионов.
Раствор готовят в день проведения анализа.
8.3.2 . Приготовление градуировочного раствора 2.
Раствор готовят соответствующим разбавлением градуировочного раствора 1. В 1 см 3 раствора должно содержаться 0,001 мг фосфат-ионов
Раствор готовят в день проведения анализа.
8.4 . Построение градуировочных графиков
Для построения градуировочных графиков необходимо приготовить образцы для градуировки с массовой концентрацией фосфат-ионов 0,05 — 1,0 мг/дм 3 . Условия анализа, его проведение должны соответствовать п.п. 6 и 10.
Состав и количество образцов для градуировки приведены в таблице 2. Погрешность, обусловленная процедурой приготовления образцов для градуировки, не превышает 2,5 %.
Состав и количество образцов для градуировки при анализе фосфат-ионов.
Массовая концентрация фосфатов-ионов в градуировочных растворах, мг/дм
Аликвотная часть растворов (см 3 ), помещенных в мерную колбу на 50 см 3
Раствор 1 с концентрацией 0,01 мг/см 3
Раствор 2 с концентрацией 0,001 мг/см 3
Раствор из мерной колбы переносят в коническую колбу и добавляют реактивы по п. 10.
Анализ образцов для градуировки проводят в порядке возрастания их концентрации. Для построения градуировочного графика каждую искусственную смесь необходимо фотометрировать 3 раза с целью исключения случайных результатов и усреднения данных.
При построении градуировочного графика по оси ординат откладывают значения оптической плотности, а по оси абсцисс — величину концентрации вещества в мг/дм 3 .
8.5 . Контроль стабильности градуировочной характеристики
Контроль стабильности градуировочной характеристики проводят при смене партий реактивов, но не реже одного раза в месяц. Средствами контроля являются вновь приготовленные образцы для градуировки (не менее 3 образцов из приведенных в таблице 2).
Градуировочную характеристику считают стабильной при выполнении для каждого образца для градуировки следующего условия:
где X — результат контрольного измерения массовой концентрации фосфат-ионов в образце для градуировки;
С — аттестованное значение массовой концентрации фосфат-ионов в образце для градуировки,

Примечание. Допустимо среднеквадратическое отклонение внутрилабораторной прецизионности при внедрении методики в лаборатории устанавливать на основе выражения: 
Значения σ R приведены в таблице 1.
Если условие стабильности градуировочной характеристики не выполняется только для одного образца для градуировки, необходимо выполнить повторное измерение этого образца с целью исключения результата, содержащего грубую погрешность.
Если градуировочная характеристика нестабильна, выясняют причины и повторяют контроль с использованием других образцов для градуировки, предусмотренных методикой. При повторном обнаружении нестабильности градуировочной характеристики строят новый градуировочный график.
9.1 . Сильнокислые и сильнощелочные пробы предварительно нейтрализуют.
9.2 . Определению мешают сульфиды и сероводород в концентрациях, превышающих 3 мг/дм 3 S 2- . Мешающее влияние можно устранить, прибавляя несколько миллиграммов калия марганцевокислого на 100 см 3 пробы и встряхивая 1 — 2 мин, раствор должен оставаться розовым. После этого прибавление реактивов проводят в обратном порядке: сначала приливают раствор аскорбиновой кислоты, перемешивают, затем прибавляют смешанный реактив.
9.3 . Определению мешают хроматы в концентрациях, превышающих 2 мг/дм 3 CrO4 2- . Это мешающее влияние устраняется прибавлением реактивов в обратном порядке (по п. 9.2 ).
9.3 . Определению мешают арсенаты. Их содержание определяют отдельно и вычитают из найденного содержания фосфат-ионов.
9.4 . Для устранения мешающего влияния нитритов в смешанный реактив добавляют 10 см 3 10 %-го раствора сульфаминовой кислоты.
9.5 . Определению мешает железо (3+) в концентрации, превышающей 1 мг/дм 3 . Для устранения мешающего влияния железа вводят эквивалентное количество комплексона III .
К 50 см 3 пробы, профильтрованной на месте или в тот же день в лаборатории через плотный бумажный фильтр (синяя лента), или к меньшему объему, доведенному до 50 см 3 дистиллированной водой, прибавляют 5,0 см 3 смешанного реактива и через короткое время 0,5 см 3 раствора аскорбиновой кислоты (как указано в п. 9.2 в присутствии некоторых мешающих веществ реактивы приливают в обратном порядке). Смесь перемешивают. Через 15 мин измеряют оптическую плотность полученного раствора при длине волны 690 нм по отношению к холостому раствору, (холостой раствор готовится на дистиллированной воде с добавлением соответствующих реактивов).
Содержание фосфат-ионов в мг/дм 3 находят по градуировочному графику.
При анализе проб воды выполняют не менее двух параллельных определений.
Содержание фосфат-ионов (мг/дм 3 ) рассчитывают по формуле:
где С — концентрация фосфат-ионов, найденная по градуировочному графику, мг/дм 3 ;
50 — объем, до которого была разбавлена проба, в см 3 ;
V — объем, взятый для анализа, см 3 .
За результат анализа Хсрпринимают среднее арифметическое значение двух параллельных определений Х1 и Х2
для которых выполняется следующее условие:
где r — предел повторяемости, значения которого приведены в таблице 3.
Значения предела повторяемости при вероятности Р = 0,95
Предел повторяемости (относительное значение допускаемого расхождения между двумя результатами параллельных определений), r, %
При невыполнении условия (1) могут быть использованы методы проверки приемлемости результатов параллельных определений и установления окончательного результата согласно раздела 5 ГОСТ Р ИСО 5725-6.
Расхождение между результатами анализа, полученными в двух лабораториях, не должно превышать предела воспроизводимости. При выполнении этого условия приемлемы оба результата анализа, и в качестве окончательного может быть использовано их среднее арифметическое значение. Значения предела воспроизводимости приведены в таблице 4.
Значения предела воспроизводимости при вероятности Р = 0,95
Предел воспроизводимости (относительное значение допускаемого расхождения между двумя результатами измерений, полученными в разных лабораториях), R, %
При превышении предела воспроизводимости могут быть использованы методы оценки приемлемости результатов анализа согласно раздела 5 ГОСТ Р ИСО 5725-6.
12.1 . Результат анализа Хсрв документах, предусматривающих его использование, может быть представлен в виде: Хср ± Δ, Р = 0,95,
где Δ — показатель точности методики.
Значение Δ рассчитывают по формуле: Δ = 0,01 × δ × Хср.
Значение δ приведено в таблице 1.
Допустимо результат анализа в документах, выдаваемых лабораторией, представлять в виде: Хср ± Δл, Р = 0,95, при условии Δл
где Хср— результат анализа, полученный в соответствии с прописью методики;
± Δл — значение характеристики погрешности результатов анализа, установленное при реализации методики в лаборатории и обеспечиваемое контролем стабильности результатов анализа.
Примечание. При представлении результата анализа в документах, выдаваемых лабораторией, указывают:
— количество результатов параллельных определений, использованных для расчета результата анализа;
— способ определения результата анализа (среднее арифметическое значение или медиана результатов параллельных определений).
12.2 . В том случае, если массовая концентрация фосфат-ионов в анализируемой пробе превышает верхнюю границу диапазона, то допускается разбавление пробы таким образом, чтобы массовая концентрация фосфат-ионов соответствовала регламентированному диапазону.
Результат анализа Хсрв документах, предусматривающих его использование, может быть представлен в виде: Хср ± Δ′, Р = 0,95,
где ± Δ′ — значение характеристики погрешности результатов анализа, откорректированное на величину погрешности взятия аликвоты.
Контроль качества результатов анализа при реализации методики в лаборатории предусматривает:
— оперативный контроль процедуры анализа (на основе оценки погрешности при реализации отдельно взятой контрольной процедуры);
— контроль стабильности результатов анализа (на основе контроля стабильности среднеквадратического отклонения повторяемости, среднеквадратического отклонения внутрилабораторной прецизионности, погрешности)
13.1 . Алгоритм оперативного контроля процедуры анализа с использованием метода добавок
Оперативный контроль процедуры анализа проводят путем сравнения результата отдельно взятой контрольной процедуры Ккс нормативом контроля К.
Результат контрольной процедуры Кк рассчитывают по формуле:
где X ′ср — результат анализа массовой концентрации фосфат-ионов в пробе с известной добавкой — среднее арифметическое двух результатов параллельных определений, расхождение между которыми удовлетворяет условию (1) раздела 11.
X ср — результат анализа массовой концентрации фосфат-ионов в исходной пробе — среднее арифметическое двух результатов параллельных определений, расхождение между которыми удовлетворяет условию ( 1 ) раздела 11 .
Норматив контроля К рассчитывают по формуле:
где 

Примечание. Допустимо характеристику погрешности результатов анализа при внедрении методики в лаборатории устанавливать на основе выражения Δл = 0,84 × Δ, с последующим уточнением по мере накопления информации в процессе контроля стабильности результатов анализа.
Процедуру анализа признают удовлетворительной, при выполнении условия:
При невыполнении условия (2) контрольную процедуру повторяют. При повторном невыполнении условия (2) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
13.2 . Алгоритм оперативного контроля процедуры анализа с применением образцов для контроля
Оперативный контроль процедуры анализа проводят путем сравнения результата отдельно взятой контрольной процедуры Ккс нормативом контроля К.
Результат контрольной процедуры Кк рассчитывают по формуле:
где Сср— результат анализа массовой концентрации фосфат-ионов в образце для контроля — среднее арифметическое двух результатов параллельных определений, расхождение между которыми удовлетворяет условию (1) раздела 11;
С — аттестованное значение образца для контроля.
Норматив контроля К рассчитывают по формуле:
где ± Δл — характеристика погрешности результатов анализа, соответствующая аттестованному значению образца для контроля.
Примечание. Допустимо характеристику погрешности результатов анализа при внедрении методики в лаборатории устанавливать на основе выражения: Δл = 0,84 × Δ, с последующим уточнением по мере накопления информации в процессе контроля стабильности результатов анализа.
Процедуру анализа признают удовлетворительной, при выполнении условия:
При невыполнении условия (3) контрольную процедуру повторяют. При повторном невыполнении условия (3) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
Периодичность оперативного контроля процедуры анализа, а также реализуемые процедуры контроля стабильности результатов анализа регламентируют в Руководстве по качеству лаборатории.
источник
Фосфор относится к числу биогенных элементов, имеющих особое значение для развития жизни в водных объектах. Соединения фосфора встречаются во всех живых организмах, они регулируют энергетические процессы клеточного обмена. При отсутствии соединений фосфора в воде рост и развитие водной растительности прекращается, однако избыток их также приводит к негативным последствиям, вызывая процессы эвтрофирования водного объекта и ухудшение качества воды.
Соединения фосфора попадают в природные воды в результате процессов жизнедеятельности и посмертного распада водных организмов, выветривания и растворения пород, содержащих фосфаты, обмена с донными осадками, поступления с поверхности водосбора, а также с бытовыми и промышленными сточными водами. Загрязнению природных вод фосфором способствуют широкое применение фосфорных удобрений, полифосфатов, содержащихся в моющих средствах, флотореагентов и др.
Фосфаты в воде могут присутствовать в виде различных ионов в зависимости от величины рН. В водах соединения фосфора, как минеральные, так и органические могут присутствовать в растворенном, коллоидном и взвешенном состоянии. Переход соединений фосфора из одной формы в другую осуществляется довольно легко, что создает сложности при определении тех или иных его форм. Обычно идентификация их осуществляется по процедуре, с помощью которой проводят химический анализ сточных вод . В том случае, когда анализируют фильтрованную пробу воды, говорят о растворенных формах, в противном случае — о суммарном содержании. Содержание взвешенных соединений фосфора находят по разности. Определение растворенных фосфатов (ортофосфатов) при анализе сточных вод осуществляется по реакции с молибдатом аммония и аскорбиновой кислотой с образованием молибденовой сини в исходной водной пробе, в то время как для определения полифосфатов в сточной воде требуется предварительно перевести их в фосфаты путем кислого гидролиза.
Для получения сравнимых результатов определения соединений фосфора и однозначной их интерпретации важно строгое соблюдение условий предварительной обработки проб и процедуры анализа сточных вод , в частности при определении растворенных форм проба должна быть отфильтрована как можно быстрее после отбора через фильтр с размером пор 0,45 мкм.
Концентрация фосфатов в незагрязненных природных водах может составлять тысячные, редко сотые доли мг/дм 3 . Повышение их содержания свидетельствует о загрязнении водного объекта. Концентрация фосфатов в воде подвержена сезонным колебаниям, поскольку она зависит от интенсивности процессов фотосинтеза и биохимического разложения органических веществ Минимальные концентрации соединений фосфора наблюдаются весной и летом, максимальные — осенью и зимой
Уменьшение содержания фосфатов в воде связано с потреблением его водными организмами, а также переходом в донные отложения при образовании нерастворимых фосфатов
Предельно допустимая концентрация фосфатов (в пересчете на фосфор) в воде водных объектов рыбохозяйственного назначения составляет
— для олиготрофных водных объектов 0,05 мг/дм;
— для мезотрофных — 0,15 мг/дм;
Предельно допустимая концентрация фосфатов для водных объектов хозяйственно-питьевого и культурно-бытового назначения не установлена, в них нормируется только содержание полифосфатов Предельно допустимая концентрация полифосфатов составляет 3,5 мг/дм 3 в пересчете на фосфат-ион и 1,1 мг/дм 3 в пересчете на фосфор.
В лаборатории «Экологический мониторинг» вы можете заказать комплексный анализ питьевой воды, ливневых сточных вод и промышленных, хозбытовых стоков. Заказать анализ сточных вод, можно оставив заявку на sales@chemanalytica.ru , или воспользовавшись формой обратной связи.
Если у Вас возникли вопросы, направляйте их к нам на почту по адресу sales@chemanalytica.ru или звоните по телефонам
8-800-600-62-40; 8(495)969-35-06.
источник
ПНД Ф 14.1:4.248-07. Количественный химический анализ вод. Методика выполнения измерений массовых концентраций ортофосфатов, полифосфатов и фосфора общего в питьевых, природных и сточных водах фотометрическим методом
| Наименование документа: | ПНД Ф 14.1:4.248-07 |
| Тип документа: | ПНД Ф |
| Статус документа: | Действует |
| Название: | Количественный химический анализ вод. Методика выполнения измерений массовых концентраций ортофосфатов, полифосфатов и фосфора общего в питьевых, природных и сточных водах фотометрическим методом |
| Область применения: | Устанавливает методику фотометрического определения полифосфатов, фосфора общего и растворенных ортофосфатов (фосфат-ионов) в пробах питьевых, природных и сточных вод |
| Краткое содержание: | |
| Комментарий: | Методика допущена для целей государственного экологического контроля |
| Дата добавления в базу: | 01.09.2013 |
| Дата актуализации: | 01.12.2013 |
| Дата введение: | 11.07.2007 |
| Доступно сейчас для просмотра: | 100% текста. Полная версия документа. |
| Организации: |
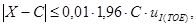 (1)
(1)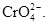 Это мешающее влияние устраняется прибавлением реактивов в обратном порядке (по п. 9.1.2).
Это мешающее влияние устраняется прибавлением реактивов в обратном порядке (по п. 9.1.2).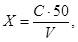 (2)
(2)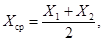 (3)
(3)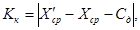 (5)
(5)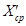 — результат анализа массовой концентрации фосфат-ионов в пробе с известной добавкой — среднее арифметическое двух результатов параллельных определений, расхождение между которыми удовлетворяет условию (4)
— результат анализа массовой концентрации фосфат-ионов в пробе с известной добавкой — среднее арифметическое двух результатов параллельных определений, расхождение между которыми удовлетворяет условию (4) (6)
(6)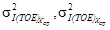 — стандартные отклонения промежуточной прецизионности, соответствующие массовой концентрации фосфат-ионов в пробе с известной добавкой и в исходной пробе соответственно, мг/дм 3 .
— стандартные отклонения промежуточной прецизионности, соответствующие массовой концентрации фосфат-ионов в пробе с известной добавкой и в исходной пробе соответственно, мг/дм 3 .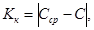 (8)
(8)