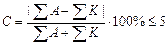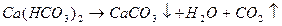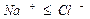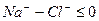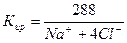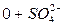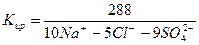Химический анализ подземных вод может служить качественным показателем использования воды для хозяйственно-питьевого водоснабжения, бальнеологических, промышленных и хозяйственных целей, а также диагностическим признаком при гидрохимических методах поисков и разведки месторождений полезных ископаемых.
Результаты химического анализа подземных вод могут быть выражены в табличной или сокращенной отчетной форме в виде формулы Курлова.
1). Табличная форма выражения химического анализа.
Количественно концентрация катионов и анионов выражается в г/дм 3 , мг/дм 3 , а эквивалентное содержание – миллимолях (ммоль) и процентах (%).
Пример расчета химического анализа воды в табличной форме приводится ниже.
| Ионы | Содержание, мг/дм 3 | Эквивалентное содержание | |
| ммоль | % | ||
| Na + Ca 2+ Mg 2+ | 88,04 22,75 15,62 | 69,9 17,6 12,5 | |
| Сумма катионов | — | 126,41 | |
| Cl — SO4 2 — HCO3 — | 98,40 17,43 3,51 | 82,5 14,5 3,0 | |
| Сумма анионов | — | 119,34 | |
| М (сухой остаток) | — | — | |
| СО2(свободный) | — | — | |
| рН водородный показатель | 5,3 | — | — |
| Т воды, градус С | — | — |
Эквивалентное (молярное) содержание определяется путем умножения каждого иона на пересчетный коэффициент, учитывающий его атомный вес и валентность и представляющий собой величины, обратные эквивалентным массам ионов (таблица 2).
| Катионы | Коэффициент | Анионы | Коэффициент |
| Na + Ca 2+ Mg 2+ | 0,0435 0,0499 0,08222 | Cl — SO4 2- HCO3 — | 0,0282 0,0208 0,0164 |
Для пересчета в %-эквивалентную форму суммы катионов и анионов в миллимолях принимаются за 100%, а затем определяется доля каждого катиона и аниона в % от соответствующей суммы катионов и анионов.
Химический анализ считается достоверным, если ошибка анализа не превышает 5%.
В нашем случае С = 2,88%. Анализ достоверен.
2) Сокращенная форма выражения химического анализа (формула М.Г. Курлова)
Формула Курлова представляет собой псевдодробь, в числителе которой в порядке убывания в %-эквивалентной форме располагаются анионы, а в знаменателе – катионы. Ионы, содержание которых менее 1%, в формулу не включаются. Проценты округляют до целых чисел.
Слева от дроби указывается содержание газов в мг/дм 3 и минерализация (М) в г/дм 3 , за которую принимается сухой остаток. Справа записывают значение (рН), температуру воды (Т) в градусах Цельсия, дебит источника в м 3 /сут и содержание микроэлементов, если такие имеются.
В нашем случае формула Курлова (таблица 1):
3) Наименование воды по химическому составу.
Наименование химического типа подземных вод должно состоять из двух частей, отражающих преобладающий анионный и катионный состав воды. Наименование химического типа воды начинается с ее анионного, а затем катионного состава в %-эквивалентной форме, превышающего 20% от суммы миллимолярной концентрации. Перечисление ионов производится в порядке возрастания концентрации – от меньшего значения к большему.
В сокращенном анализе анионы представлены хлоридами, сульфатами и гидрокарбонатами, а катионы – натрием, кальцием и магнием. В нашем случае вода хлоридно-натриевая.
4) Классификация воды по минерализации.
В зависимости от величины минерализации, за которую принимается сухой остаток, подземные воды классифицируются в соответствии с приведенной таблицей 3.
| Минерализация М, г/дм 3 | Подгруппа | Группа |
| £ 0,5 >0,5-1,0 | Весьма пресные Пресные | Пресные |
| >1,0-1,5 >1,5-3,0 >3,0-5,0 >5,0-10,0 >10,0-25,0 | Весьма слабосолоноватые Слабо солоноватые Умеренно солоноватые Солоноватые Сильно солоноватые | Солоноватые |
| >25,0-36,0 >36,0-50,0 | Слабосоленые Сильносоленые | Соленые |
| >50,0-150,0 >150,0-350,0 >350,0 | Рассолы слабые Рассолы крепкие Рассолы весьма крепкие (рапа) | Рассолы |
В нашем случае М = 6,9 г/дм 3 . Вода солоноватая.
Реакция воды обусловлена величиной концентрации водородных ионов рН, которая представляет собой обратный логарифм концентрации ионов водорода. Классификация воды по водородному показателю приведена в таблице 4.
| Водородный показатель рН при Т22 о С | Подгруппа | Группа |
| £ 3,5 >3,5-4,5 >4,5-5,5 >5,5-6,0 | Весьма кислая Кислая Умеренно кислая Слабокислая | Кислая |
| >6,0-8,0 | Нейтральная | Нейтральная |
| >8,0-8,5 >8,5-9,0 >9,0-9,5 >9,5 | Слабощелочная Умеренно щелочная Щелочная Весьма щелочная | Щелочная |
В нашем случае рН = 5,3. Вода умеренно кислая.
6) Классификация подземных вод по температуре воды.
Классификация воды по температуре приведена в таблице 5.
| Температура, Т о С | Наименование |
| 0-4 >4-20 >20-37 >37-50 >50-75 >75-100 >100-200 >200-374 | Переохлажденная Очень холодная Холодная Теплая Очень теплая Горячая Очень горячая Слабо перегретая Весьма перегретая |
Примечание: воды с температурой от 20 до 100 о С называются термальными.
В нашем случае Т15 о С. Вода холодная.
Жесткость воды имеет большое значение при использовании подземных вод для питьевого водоснабжения, промышленных и хозяйственных целей. Жесткость воды обусловливается содержанием в ней солей кальция и магния. Измеряется в миллимолях (мг-экв/дм 3 ).
Различают общую жесткость (ОЖ), устранимую или временную жесткость (УЖ) и постоянную жесткость (ПЖ).
Общая жесткость обусловлена присутствием в воде гидрокарбонатов, хлоридов и сульфатов кальция и магния и равняется сумме устранимой и постоянной жесткости.
Устранимая жесткость обусловлена присутствием в воде гидрокарбонатов кальция и магния. Такая жесткость получила название карбонатной (КЖ) и может быть устранена при кипячении
Карбонат кальция и магния выпадает в осадок, образуя накипь. При использовании такой воды для промышленных и коммунальных целей происходит отложение карбоната кальция и магния на стенках котлов и трубопроводов, что приводит к выводу их из эксплуатации.
При высоком содержании НСО3 — в воде, превышающем суммарную концентрацию кальция и магния, вся жесткость считается карбонатной.
Постоянная жесткость обусловлена наличием в воде сульфатов и хлоридов кальция и магния и равняется разности между общей и карбонатной жесткостью.
Классификация воды по общей жесткости приводится в таблице 6 (ГОСТ 6055-86).
| Содержание в ммоль | Группа жесткости |
| £ 1,5 >1,5-3,0 >3,0-6,0 >6,0-9,0 >9,0 | Очень мягкая Мягкая Умеренно жесткая Жесткая Очень жесткая |
Подземные воды, жесткость которых превышает 7 ммоль, не могут быть использованы для питьевого и промышленного водоснабжения.
В нашем случае общая жесткость составляет 38,37 ммоль, устранимая (карбонатная) – 3,50 ммоль, постоянная – 34,86 ммоль. Вода очень жесткая, непригодная для питьевого и промышленного водоснабжения.
8) Пригодность для питьевого водоснабжения.
Пригодность воды для питьевого водоснабжения нормируется ГОСТ 6055-86 «Вода питьевая». В рамках сокращенного гидрохимического анализа нормативными являются минерализация, общая жесткость, содержание Cl — и SO 2- 4 , а также величина рН с предельно допустимыми концентрациями, приведенными в таблице 7.
| Наименование показателей | ПДК | Содержание в нашем примере | Степень пригодности |
Минерализация М, мг/дм 3 Общая жесткость ОЖ, ммоль 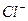 , мг/дм 3 , мг/дм 3 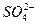 , мг/дм 3 рН , мг/дм 3 рН | 6,5-8,5 | 38,37 5,3 | Не пригодна Не пригодна Не пригодна Не пригодна Не пригодна |
В нашем случае вода по всем компонентам не пригодна для водоснабжения.
9) Пригодность для ирригационных целей.
Пригодность использования подземных вод, в том числе и шахтных, для ирригационных целей в сельском хозяйстве нормируется степенью минерализации воды и расчетным ирригационным коэффициентом. Классификация воды по минерализации, нормирующая степень пригодности для орошения сельскохозяйственных угодий, приведена в таблице 8.
| Минерализация, г/дм 3 | Степень пригодности для орошения |
| £1,7 >1,7-5,0 >5,0 | Пригодна Пригодна условно (возможно засоление) Не пригодна |
В нашем случае минерализация 6,9 г/дм 3 . Вода для орошения не пригодна.
Расчет ирригационного коэффициента выполняется в зависимости от соотношения ионов натрия, хлора и сульфатов в эквивалентной форме в миллимолях.


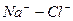
 |
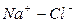

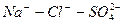
Во втором случае избыточное содержание катионов натрия может быть нейтрализовано содержащимся в воде сульфат-ионом. В третьем случае избыток натрия накапливается в почве в виде поглощенных катионов.
В первых двух случаях вода улучшению не подлежит, в третьем случае воду можно улучшить добавкой гипса. Классификация воды по ирригационному коэффициенту приведена в таблице 9.
| Ирригационный коэффициент | Характеристика воды | ||||||||||||||||||||||||||||||||||||||||||||||||||
| >18 >6-18 ³1,2-6,0 + — , Кир= 0,58. Вода очень плохая и улучшению не подлежит. 10) Агрессивность подземных вод. Подземные воды в зависимости от состава могут оказывать разрушающее действие на бетоны, цементы и металлы. Оценка агрессивности подземных вод по отношению к бетонам марки W4 и металлам производится на основании таблиц 5-7 и 26 СНиП 2.03.11-85 «Защита строительных конструкций от коррозии» (в скобках указаны номера таблиц согласно СНиП). Дата добавления: 2015-04-18 ; просмотров: 71 ; Нарушение авторских прав источник Обработку анализа выполнить в следующей последовательности: Перевести анализ воды из весовой в эквивалентную и процент-эквивалентную формы. Вычислить погрешность анализа по формуле: Определить минерализацию воды. Вычислить жесткость воды. Оценить пригодность воды для питья. Оценить агрессивность воды по отношению к бетонным и металлическим конструкциям. Результаты химического анализа природных вод, мг/дм 3 Предельно-допустимые концентрации на питьевую воду. (СанПиН 2.1.4.559-96) Анализ химического состава подземных вод открывает пути для изучения генезиса, пригодности для различных потребителей, определения уровня их агрессивности для бетонных и металлических конструкций. Результаты химических анализов воды могут быть выражены в весовой, эквивалентной и процент — эквивалентной форме. Перевести анализ воды из весовой в эквивалентную и процент — эквивалентную формы. Эквивалентная форма записи состава вод позволяет определить соотношение между ионами с точки зрения их способности участвовать в химических реакциях, оценить качество анализа, установить генезис вод. В расчетах используется форма записи: где Э-химический эквивалент иона. Процент — эквивалентная форма показывает относительную долю участие того или иного иона в формировании ионно — солевого состава воды. Анализ воды в эквивалентной и процент — эквивалентной форме. Вычисление погрешности анализа. На основе эквивалентной формы выражения состава можно определить погрешность анализа воды. Эта оценка основана на принципе электронейтральности раствора: сумма концентраций катионов (мг-экв/дм 3 ) равна сумме концентраций анионов. Анализ воды считается удовлетворительным, если погрешность определения менее 5%. Вывод: Анализ воды считается удовлетворительным, т.к. погрешность определения составляет Е = 2,37 % и это меньше 5%. Определение минерализации воды. Минерализация воды (М) — это сумма минеральных веществ, в граммах или миллиграммах, содержащихся в 1 дм 3 воды. М = К + + Nа + + Са 2+ + Мg 2+ + НСО3 — + SО4 2 — + СI — +Аs + Fе + Рb + Zn + Нg + Си + F — + NО3 — + Мn М=1+7+59+16+163+63+19,5+0,02+0,2+0,7+0,1+0,001+1,0+0,5+10,0+0,07=341,091 мг/дм 3 Вычисление жесткости воды. Жесткость воды — это совокупность свойств, обусловленных содержанием в воде катионов кальция Са 2+ и катионов магния Мg 2+ . Если концентрация этих катионов велика (Жо > 7 мг-экв/дм 3) , то воду называют жесткой, если мала (Жо 3 ) — мягкой. Различают: общую, карбонатную, временную (устранимую), некарбонатную, неустранимую (постоянную) жесткости. Общая жесткость определяется как сумма мг-экв ионов Са 2+ + Мg 2+ в 1дм 3 воды и слагается из Жк карбонатной и Жнк некарбонатной жесткости. Жо = 2,809524+1,311475=4,120999 мг-экв/дм 3 . Вывод: При расчете результата анализа жесткости грунтовых вод было выявлено, что данная вода является мягкой и дополнительного умягчения не требует. Оценка пригодности воды для питья. Согласно СанПиН 2.1.4.559-96 (Питьевая вода. Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения. Контроль качества.) данная грунтовая вода не пригодна для питья, т.к. не отвечает выше указанному документу и имеет превышение по 2 компонентам: ртуть, свинец. Оценка агрессивности воды по отношению к бетонным и металлическим конструкциям. Агрессивность воды связана с присутствием в ней ионов водорода, свободного диоксида углерода, сульфатов и магния. Агрессивные свойства воды проявляются по отношению к бетону и металлам. Агрессивность воды по отношению к бетону выражается в разрушительном воздействии подземных вод определенного состава. Оценка качества воды производится по нормам и техническим условиям. Эти нормы учитывают воздействие следующих видов агрессивности: выщелачивающую, углекислую, общекислотную, сульфатную и магнезиальную. 1) Выщелачивающую агрессивность связана с выщелачиванием карбонатов, главным образом кальция. Если вода, контактирующая с бетоном, содержит низкие концентрации Са 2+ , НСО3 — и СО3 2-, то карбонат кальция бетона переходит в раствор. Для бетона вода считается агрессивная при карбонатной жесткости меньше 0,54 — 2,14 мг-экв/дм 3 . Так как, данная грунтовая вода имеет карбонатную жесткость (НСО3 — 61мг-экв/дм 3 ), и низкую концентрацию катионов кальция (Са 2+ — 59 мг/дм 3) , то вода является не агрессивной для бетонных сооружений. 2) Углекислотная агрессивность обусловлена высокими концентрациями растворенной в воде углекислоты СО2. Эта агрессивность проявляется как в отношении металла (коррозия), так и бетона. Воды, обладающие карбонатной жесткостью менее 1,4 мг-экв/дм 3 , следует считать агрессивными. Так как, данная грунтовая вода имеет карбонатную жесткость (НСО3 — 61мг-экв/дм 3 ), то вода является не агрессивной для бетонных сооружений. 3) Общекислотная агрессивность воды связана с повышенной концентрацией ионов водорода Н + (пониженная величина рН). При этом бетон разрушается из-за растворения в кислой среде защитной карбонатной корки. Вода считается агрессивной для всех типов цементов: при рН 3 , при рН 3 . Грунтовая вода имеет кислую среду (рН — 7,7) и карбонатной жесткость (НСО3 — 61 мг-экв/дм 3 ), тем самым не разрушает бетонные конструкции и не является агрессивной средой. 4) Сульфатная агрессивность обусловлена присутствием в воде иона SО4 2- . Этот вид агрессии проявляется в кристаллизации в бетоне новых соединений и выщелачивании бетона. По сульфатной агрессии для обычных цементов воду относят к слабоагрессивной при содержании иона SО4 2 — от 250 — 800 мг/дм 3 и к агрессивной при содержании более 800 мг/дм 3 . Так как, данная грунтовая вода имеет слабую сульфатную агрессивность (SО4 2 — 63 мг/дм 3 ), то вода является не агрессивной для бетонных сооружений. 5) Магнезиальная агрессивность вызывает разрушение и вспучивание бетонных конструкций. Так как, данная грунтовая вода имеет слабую магнезиальную агрессивность (Мg 2+ 16 мг/дм 3 ), то вода является не агрессивной для бетонных сооружений. 6) Агрессивность воды по отношению к металлу связана с коррозирующей способностью вод. Агрессивные по отношению к металлу являются воды: углекислые; сероводородные кислые; обогащенные кислородом. Корродирующая способность воды определяется при помощи коэффициента коррозии: Кк= 1,311475 — 56,597500 = — 55,286025 мг-экв/дм 3 По величине коэффициента коррозии различают следующие группы вод (содержание Са 2+ в мг/дм 3 ): Кк + 0,05 Са 2+ 3 загрязненной воды. Данная грунтовая вода не пригодна для питья, так как имеет превышение по 2 компонентам: ртуть, свинец. Для нейтрализации ионов ртути применяют Na2S (двукратный избыток от стехиометрического соотношения). Ответ: Для удаления ионов ртути необходимо 0,0007 килограмм сульфида натрия. Для удаления ионов свинца применяют щелочные агенты (СаО, Са (ОН) 2, Nа2СО3, NаОН). Ответ: Для удаления ионов свинца необходимо 0,189 килограмм СаО. грунтовая вода очистка загрязненный Ответ: Для удаления ионов свинца необходимо 0,252 килограмм Са (ОН) 2. Ответ: Для удаления ионов свинца необходимо 0,357 килограмм Nа2СО3. Ответ: Для удаления ионов свинца необходимо 0,266 килограмм NаОН. Обработка результатов химического анализа сточной воды, взятой из скважин также показала, что данная сточная вода не имеет превышения по жесткости и кислотности. Поэтому по жесткости и кислотности расчетов не требуется. источник Основными задачами химического анализа подземных вод в практике гидрогеологических исследований являются:
Существует четыре типа химических анализов подземных вод: полевой, сокращенный, полный и специальный. Полевой анализ наиболее прост, он применяется для предварительной характеристики подземных вод района. Его проводят в полевых условиях в походных гидрохимических лабораториях, часто упрощенными методами. При полевом анализе определяют: физические свойства воды, ее pH, наличие Сl — , SO 2- 4 , NO — 3, HCO — 3, СО3 2- , общую жесткость, присутствие Са 2+ , Fe 2+ , Fe 3+ , NH + 4 , N0 — 2, С02своб; вычисляют: Na + + К + , карбонатную жесткость, Mg 2+ и общую минерализацию. Сокращенный анализ . Этот анализ производят более точными методами в стационарных лабораториях. При сокращенном анализе определяют: физические свойства воды, величину pH, содержание ионов и компонентов (Сl — , SO 2- 4 — , NO — 3, HCO — 3, СО3 2- , Na + , К + , Ca 2+ , Mg 2+ , Fe 2+ , Fe 3+ , NH + 4 , N0 — 2, свободную и агрессивную углекислоту С02, Si02, окисляемость, сухой остаток, жесткость общую, карбонатную и некарбонатную. Полный анализ применяется для подробной характеристики химического состава подземных вод. Он производится наиболее точными методами в стационарных лабораториях. Анализ позволяет произвести контроль определений как по сухому остатку, так и по суммам мг-экв катионов и анионов. При полном анализе определяют: физические свойства воды, ее pH, наличие Сl — , SO 2- 4 — , NO — 3, HCO — 3, СО3 2- , Na + , К + , Ca 2+ , Mg 2+ , Fe 2+ , Fe 3+ , NH + 4 , N0 — 2, С02 своб и C0 2arpec, Si 0 2, окисляемость, сухой остаток; вычисляют: жесткость общую, карбонатную и некарбонатную, С0 2агрес. Специальный анализ. Помимо характеристик, определяемых при перечисленных выше типах анализа, этот анализ включает установление специальных показателей (микрокомпонентов, органических веществ, газов, Eh и др.) по особому заданию в соответствии с целевым назначением исследований. Количество отбираемой для анализа воды зависит от точности и чувствительности анализа и минерализации воды. Чем выше требования к чувствительности и точности анализа, тем больше должен быть объем пробы; пресные и слабо минерализованные воды отбирают в ббльших объемах, чем сильно минерализованные. При полевом анализе обычно бывает достаточно 0,5 л воды, при сокращенном — от 0,5 до 1,0 л (в зависимости от минерализации), а при полном — от 1,0 до 2,0 л. Для определения неустойчивых (изменяющихся во времени) компонентов — С02, H 2 S, 02, Fe и др. — применяют специальные методы отбора и хранения проб. Результаты химического анализа воды выражают в массовых количествах веществ, растворенных в 1 л (или в 1 кг воды), в эквивалентных количествах или в процент-эквивалентных количествах (%-экв) воды. В гидрогеологической практике принято массовые количества компонентов выражать в миллиграммах на 1 л (мг/л), а эквивалентные количества ионов — в миллиграмм-эквивалентах (мг-экв) каждого иона в 1 л воды. Величину сухого (плотного) остатка получают взвешиванием пробы после выпаривания воды. Сумму ионов определяют суммированием массы всех ионов, содержащихся в исследуемой воде. Сумма минеральных веществ — более полное выражение, чем сумма ионов, так как она учитывает и недиссоциированные неорганические вещества Si0 2 и Fe 2 03. В настоящее время принята ионная форма выражения химических анализов воды. Данные лабораторных анализов подземных вод, выраженные в мг/л, подвергаются дальнейшей обработке (табл.ниже). источник Данная работа рассчитана на 2 часа академических занятий и на 4 часа самостоятельной работы студентов с преподавателем. Целью данной работы является ознакомление студентов с данными сокращенного химического анализа подземных вод, методикой их обработки и пересчета путем использования нормативов ГОСТа, систематизация и оценка пригодности их для питьевого водоснабжения или технического использования. 2.2.1 Свойства и характеристика подземных вод. Вопросы практического использования подземных и рудничных вод могут быть решены только после полного изучения их физико-химических свойств, химического и бактериального состава. Химический состав и физические свойства подземных вод изучают для различных целей: питьевого и технически-хозяйственного водоснабжения (питания паровых котлов, охлаждения машин, тушения пожаров и т.п.), орошения полей, лечебных целей, как поисковый критерий на различные полезные ископаемые, для оценки агрессивности подземных вод по отношению к бетону, коррозирующих свойств по отношению к металлам, для установления связи водоносных горизонтов между собой и с поверхностными водами и т.п. Подземные воды представляют собой сложные естественные растворы, находящиеся в многообразных связях и взаимодействии с окружающей природной средой. Естественная физико-географическая и геологическая обстановка определяют особенности генезиса и дальнейшего преобразования подземных вод. К физическим свойствам подземных вод относятся температура, цвет, запах, прозрачность, вкус, привкус, электропроводность и радиоактивность. Определение этих свойств частично проводится непосредственно в полевых условиях при отборе проб воды, а в основном – в химических лабораториях по специальной методике. Химические свойства подземных вод определяются количеством и соотношением содержащихся в них в растворенном виде солей, присутствующих в воде в виде ионов – анионов и катионов, а также некоторых недиссоциированных соединений, газов и органических соединений. Среди ионов наибольшее практическое значение имеют следующие: катионы – водород – H + , натрий – Na + , калий – K + , магний – Mg 2+ , кальций – Ca 2+ , железо – Fe 2+ ; анионы – хлор – Cl — , сульфат – SO4 2- , гидрокарбонат – HCO3 — . Из недиссоциированных соединений наиболее часто встречаются окислы железа – Fe2O3, кремния – Si2O3, алюминия – Al2O3, а из газов – углекислый газ – CO2, кислород – O2, азот – N2, метан – CH4, сероводород – H2S. В результате выполнения данной работы студенты, изучив химический состав подземных вод, должны иметь определенные навыки по их обработке и систематизации, а также определить область практического использования. Перечень необходимых определений веществ, содержащихся в подземных водах, устанавливается в соответствии с целевым назначением анализа, что и указывается в программе работ гидрогеологических исследований. 2.2.2 Способы выражения химического состава подземных вод. В природной воде молекулы солей почти полностью диссоциированы на ионы, поэтому основной формой выражения результатов химического анализа воды является ионная форма. При этом содержание любого иона в процессе исследования выражается в граммах или миллиграммах на кубический дециметр (что равнозначно литру) воды (г/дм 3 (г/л), мг/дм 3 (мг/л)). Поэтому результаты анализов в химических лабораториях даются в ионной форме, т.е. в г/дм 3 (г/л), мг/дм 3 (мг/л). Но, делать некоторые выводы о составе и свойствах воды можно, лишь имея анализы в миллиграмм — эквивалентной и эквивалент — процентной формах. Поэтому данные химического анализа должны быть пересчитаны (табл. 3). Для этого вначале необходимо определить эквивалент каждого аниона и катиона. Дело в том, что ионы взаимодействуют между собой в строго определенных эквивалентных весовых соотношениях. Например, один эквивалент одного иона хлора Cl — может взаимодействовать только с одним эквивалентом иона натрия Na + или кальция Ca 2+ . Следовательно, эквивалент – это число, показывающее, в каком весовом соотношении данный ион вступает в соединение с другим ионом. Для пересчета анализа из ионной формы в миллиграмм – эквивалентную следует число миллиграммов каждого иона разделить на его эквивалентный вес, который представляет собой отношение атомного (или ионного) веса данного элемента к его валентности. Например, кальция Ca 2+ в воде содержится 420 мг/дм 3 . Эквивалентный вес одного иона кальция Ca 2+ равен: 40,08 : 2 = 20,04 мг/экв. Чтобы определить его миллиграмм – эквивалентное содержание надо 420 : 20,04 = 20,96 мг/экв. Также для пересчета анализов воды в миллиграмм-эквиваленты содержание ионов умножают на специальные пересчетные коэффициенты, которые представляют частное от деления единицы на эквивалентный вес. Для выше приведенного примера пересчетный коэффициент кальция Ca 2+ равен 1 : 20,04 = 0,0499. Если 420 • 0,0499 = 20,96 мг/экв – миллиграмм-эквивалентная форма. Ниже приведены пересчетные коэффициенты для некоторых ионов: гидрокарбонат HCO3 — – 0,0164 Если сумму всех катионов и анионов в миллиграмм-эквивалентной форме принять за 100%, можно получить соответствующие выражения для анионов и катионов в эквивалент-процентной форме. Количества катионов и анионов, выраженные в эквивалент-процентной форме, должны быть равны между собой, т.е. сумма всех катионов должна составлять 50% и сумма всех анионов тоже 50%, что является удобным контролем анализа. В последнее время очень часто принимают за 100% сумму миллиграмм-эквивалентов анионов и также за 100% — сумму миллиграмм-эквивалентов катионов. Расчет от этого не изменяется, но величины эквивалент-процентов становятся в два раза больше. Если результаты анализа воды выражены в миллиграмм-эквивалентной форме, то перед символом иона ставят букву r, например rCl — и т.д. При анализе могут быть неточности. Допустимая неточность анализа определяется из выражения: Таблица 3 — Исходные данные
В итоге пересчетов должна быть составлена таблица следующей формы (табл. 4): Таблица 4 — Порядок пересчета ионной формы в другие формы
При химическом анализе воды определяют величину сухого остатка после выпаривания и количества веществ, содержащихся в воде (минерализацию). Количества веществ показывают в ионной форме, при которой содержание отдельных ионов определяют в миллиграммах на 1 л воды. При выборе и оценке воды источника централизованного хозяйственно-питьевого водоснабжения пользуются государственными стандартами (ГОСТ – 2874 – 82 и др.). Сумма растворенных в воде веществ – сухой остаток – при t = 105 – 110 0 C не должна превышать 1000 мг/л. 2.2.3 Минерализация. Это экспериментально определенный сухой остаток или подсчитанная сумма минеральных веществ. Единой классификации по степени минерализации нет, их достаточно много применительно к требованиям отдельных ведомств. В таблице 5 приводится выражение общей минерализации подземных вод по В.М. Вернадскому, согласующееся с требованиями их практического использования. Таблица 5 — Классификация подземных вод по общей минерализации
2.2.4 Жесткость воды. Особое ее качество, обусловленное присутствием углекислых и сернокислых солей Ca 2+ и Mg 2+ . Жесткость поземных вод имеет большое значение при их оценке для практического использования. Жесткая вода плохо взмыливается, дает накипь в паровых котлах (что уменьшает их теплопроводность, приводит к перерасходу топлива и может вызвать аварию) и в посуде, вспенивается, в жесткой воде медленнее развариваются овощи, мясо, крупы и другие продукты. Различают общую, временную (карбонатную или устранимую) и постоянную жесткость воды. Общей называют жесткость, соответствующую пробе свежей воды. При кипячении воды растворенные в ней бикарбонаты (двууглекислые соли) переходят в углекислые и выпадают в виде осадка или накипи. Жесткость, соответствующая кипяченной воде, называется постоянной. Разность между общей и постоянной жесткостью воды называют временной жесткостью. Жесткость выражают в градусах жесткости. Существует три системы градусов жесткости: немецкая, французская, английская. За один немецкий градус жесткости принимается содержание в 1 л 10 мг CaO или 7,2 мг MgO. За один французский градус – содержание в 1 л воды 10 мг CaCO3 или 17,5 мг MgCO3. В английской системе одному градусу жесткости соответствует содержание в 1 л воды14 мг CaCO3 (точнее, в английских мерах, — 1 гран (64,79892 мг) CaCO3 на 1 галлон (4,546 л) воды). Для перевода из одной системы градусов в другую можно воспользоваться такими соотношениями: 1,0 0 жестк. нем. = 1,79 0 жестк. франц. = 1,25 0 жестк. англ. 0,56 0 жестк. нем. = 1,0 0 жестк. франц. = 0,7 0 жестк. англ. 0,8 0 жестк. нем. = 1,43 0 жестк. франц. = 1,0 0 жестк. англ. Количество солей, мг/л, из которых каждая в отдельности обусловливает 1 0 жесткости, представлены ниже: 1,0 0 жестк. нем. 10,0 7,2 17,9 8,0 19,7 17,0 25,0 21,5 1,0 0 жестк. франц. 5,6 4,0 10,0 4,4 11,0 9,5 14,0 12,0 1,0 0 жестк. англ. 8,0 5,8 14,0 6,4 15,8 13,6 20,1 17,2 В настоящее время в нашем государстве вместо жесткости в градусах введено понятие жесткости в миллиграмм-эквивалентах на литр. За единицу жесткости принимают 1 мг-экв Ca, т.е.20,04 мг Ca на 1 л воды. Вместо кальция может быть принят 1 мг-экв магния, т.е. 12,16 мг Mg на 1 л воды. Для перевода из системы градусов жесткости (немецких) в миллиграмм-эквиваленты и обратно можно воспользоваться такими соотношениями: 1 мг-экв/л соответствует 2,8 0 жест. (нем.); 0,357 мг-экв/л соответствует 1,0 0 жест. (нем.). Жесткость природных вод колеблется в пределах от нескольких до десятков и сотен мг-экв/л; в одном и том же водоисточнике жесткость неодинаковая в разные времена года. В случае необходимости использования жестких вод для тех или иных целей их приходится обрабатывать специальными способами для снижения жесткости до требуемых норм. Природные воды по общей жесткости О.А. Алекин подразделяет на пять групп (табл. 6): Таблица 6 — Классификация природных вод по общей жескости
2.2.5 Оценка воды по активной реакции. Как уже отмечалось, в воде часть молекул всегда находится в диссоциированном состоянии, в виде ионов H + и OH — . Концентрация недиссоциированной воды считается постоянной, поэтому произведение ионов водорода и ионов гидроксила при данной температуре тоже будет величиной постоянной. При температуре 22 0 C эта величина равна 10 -14 . Так как чистая вода имеет нейтральную реакцию, количества ионов водорода и ионов гидроксила должны быть равны. Следовательно, Это выражение означает, что в 1 л чистой воды при 22 0 C содержится 10 -7 грамм-молекул воды в ионизированном виде, т.е. 10 -7 грамм-ионов водорода и 10 -7 грамм-ионов гидроксила. Если [H + ] = 10 -7 , то lg[H + ] = -7 и — lg[H + ] = 7. Выражение — lg[H + ] означает pH. Следовательно, если pH 7 – щелочная. По величине активной реакции или водородного показателя pH природные воды классифицируются следующим образом (табл. 7): Таблица 7 — Классификация природных вод по активной реакции
Подземные воды в большинстве своем имеют слабощелочную реакцию. Воды сульфидных и особенно колчеданных и каменноугольных месторождений обычно кислые и часто весьма кислые. Определять концентрацию водородных ионов необходимо на месте взятия пробы; наиболее употребительный способ определения – колориметрический, основанный на свойстве индикаторов менять окраску в зависимости от концентрации водородных ионов. 2.2.6 Агрессивные свойства подземных вод. Отрицательное воздействие подземных вод на металл и бетон называется агрессивностью воды. Это свойство обусловлено присутствием в воде ионов бикарбоната, водорода, агрессивной углекислоты, сульфатов и магния. В связи с этим различают агрессивность выщелачивания, общекислотную, углекислую, сульфатную и магнезиальную. Оценку различных видов агрессивности проводят по справочнику «Нормы и технические условия. Бетон гидротехнический. Признаки и нормы агрессивности воды-среды». Наличие натриевых и калиевых солей вызывает образование накипи. Свободный ион H + вызывает разъедание стенок котлов и труб. Временная (устранимая) жесткость воды является с этой точки зрения положительным фактором, так как ионы HCO3 — связывают свободные ионы H + . Кроме ионов водорода разъедающее действие на металл оказывают ионы кислорода, углекислоты, сероводорода. Поэтому вода, применяемая для технических целей, нуждается в предварительной обработке. После обработки вода по большей части становится непригодной для питья. Агрессивность выщелачивания возникает при малом содержании в воде HCO3 — (менее 1,5 мг-экв/л). В этих условиях происходит растворение и вымывание из бетона содержащейся в нем извести. Общекислотная агрессивность обусловлена низким значением водородного показателя pH (менее 5), из-за чего усиливается растворение извести бетона. Углекислая агрессивность возникает в результате действия агрессивной углекислоты CO2. В процессе взаимодействия с водой из цемента выделяется свободная известь CaCO3, которая реагирует со свободной углекислотой CO2. Реакция идет по схеме CaCO3 + CO2 + H2O = Ca(HCO3)2. Образующийся при этом бигидрокарбонат кальция является растворимым и легко выносится из бетона. Вода для большинства марок цемента становится агрессивной, если содержание в ней свободной углекислоты больше величины, определяемой по формуле a∙Ca + b. Содержание Ca 2+ выражается в мг/л, а коэффициенты a и b определяются в зависимости от карбонатной жесткости HCO3 — (мг-экв/л) и суммарного содержания ионов Cl — + SO4 2- в мг/л по специальной таблице 14. Сульфатная агрессивность возникает при наличии в воде повышенного количества сульфата SO4 2- ; в бетоне происходит кристаллизация новых соединений, образование которых сопровождается увеличением объема, вследствие чего происходит разрушение бетона. Такими новыми соединениями являются гипс CaSO4 ∙ 2H2O и сульфоаллюминат кальция 3CaO ∙ Al2O3 ∙ 3CaSO4 ∙ 31H2O (цементная бацилла). При образовании гипса объем бетона увеличится в два раза, а при образовании цементной бациллы – в 2,5 раза. При содержании в воде SO4 2- менее 250 мг/л сульфатная агрессивность отсутствует независимо от содержания хлора Cl — . Вода становится агрессивной по отношению к обычным портландцементам, если содержание ионов SO4 2- будет больше приведенных ниже показателей с учетом содержания в воде ионов хлора Cl — (мг/л): Cl — — менее 1000 SO4 2- — 250 Магнезиальная агрессивность, подобно сульфатной, ведет к разрушению бетона при соприкосновении его с водой, содержащей повышенное количество Mg 2+ . При этом, если содержание ионов магния Mg 2+ будет меньше 1000 мг/л, вода считается магнезиально – неагрессивной независимо от содержания иона SO4 2- (мг/л). При содержании ионов магния Mg 2+ более 1000 мг/л и больше величины, определяемой по формуле К- SO4 2- , вода считается агрессивной. Величина К для обычного портланд — цемента равна 7000. 2.2.7 Классификация подземных вод по химическому составу. Единой общепринятой классификации подземных вод в зависимости от их химического состава нет, что объясняется чрезвычайно разнообразным качественным и количественным химическим составом природных вод. Наиболее удобны те классификации, которые построены на принципе деления вод по преобладающим ионам (катионам и анионам) и по соотношению между ними. Именно на этом принципе построена классификация О.А. Алекина, широко используемая в геолого–разведочной, горной промышленности, гидротехнике и коммунальном хозяйстве. В соответствии с этой классификацией все природные воды по преобладающему в них аниону делятся на три больших класса – гидрокарбонатные, хлоридные и сульфатные. Каждый класс, в свою очередь, по преобладающему катиону делится на три группы – натриевые, кальциевые и магниевые. Группы по соотношению между ионами подразделяются на четыре типа: I тип: HCO3 — > Ca 2+ + Mg 2+ — воды маломинерализованные; II тип: HCO3 — 2+ + Mg 2+ — + SO4 2- — воды умеренной минерализации; III тип: HCO3 — + SO4 2- 2+ + Mg 2+ или, что то же самое, Cl — > Na + — воды высокоминерализованные; IV тип — HCO3 — = 0 – воды кислые, имеются только в сульфатном и хлоридном классе. Для удобства сопоставления анализов воды используют различные способы сокращенного изображения состава. Наиболее часто применяются формула М.Г. Курлова, графические – прямоугольник солевого состава Н.И. Толстихина и треугольники Фере ионного состава. Формула М.Г. Курлова представляет собой псевдодробь, где в числителе располагаются по убывающей анионы с индексом, равным содержанию данного иона в экв/%, в знаменателе — в такой же последовательности катионы. Ионы, содержание которых не превышает 10 экв/%, в формулу не включаются. Количество анионов и катионов округляется до целого числа. Перед дробью даются значение минерализации (М) с индексом, равным количеству сухого остатка в г/л, а также содержание элементов и газов с индексами, равными их содержанию в мг/л. После дроби указываются температура воды в градусах (t 0 C) и активная реакция воды (pH). В наименовании состава воды рекомендуется называть первыми анионы, затем катионы, а также элементы и газы. Ионы, содержание которых в воде менее 25%, не называются. Прямоугольник солевого состава Н.И. Толстихина (рис. 13) состоит из трех вертикальных граф. Левая и правая графы делятся на 10 равных частей, каждая часть приравнивается 10%. Нумерация производится снизу вверх. В левой графе изображаются катионы, в правой – анионы в экв/%. В средней графе показывают состав и процентное содержание солей, которые образуются в результате реакции катионов и анионов. Катионы и анионы на графике располагаются снизу вверх в последовательности, определяемой относительной реактивной силой: K + , Na + , Mg 2+ , Ca 2+ , Fe 2+ , NO3 — , Cl — , Br — , I — , SO4 2- , HCO3 — , CO3 2- .
Рисунок 13 – Прямоугольник солевого состава Треугольники Фере ионного состава (рис. 14) составляются отдельно для катионов и анионов, содержание которых дается в экв/%. В произвольном масштабе вычерчиваются два равносторонних треугольника, в вершинах которых располагаются катионы и анионы. Считается, что в вершине количество каждого катиона и аниона равно 100%. Далее, каждая сторона треугольника делится на 10 равных отрезков, соответствующих 10-ти процентам. Содержание катиона или аниона откладывается в виде точек на двух прилежащих к этой вершине сторонах треугольника. Эти точки затем соединяются прямой линией, параллельной третьей стороне. В итоге в каждом треугольнике получится по три прямые линии, точка пересечения которых графически изображает химический состав воды. 2.2.8 Оценка воды для питьевого водоснабжения. Вода, используемаядля хозяйственно-питьевого водоснабжения, должна удовлетворять требованиям ГОСТ — 2874-82 «Вода питьевая, технические требования к качеству». Согласно этого стандарта ниже приведены предельно-допустимые концентрации (ПДК) для некоторых показателей (табл. 8): Таблица 8 — Нормативы ГОСТ 2874-82
При отсутствии источника с пресной водой разрешается использовать воду с сухим остатком до 1500 мг/л, при общей жесткости до 10 мг-экв/л. В каждом случае возможность использования таких вод должна быть согласована с органами санитарно-эпидемиологической службы. Питьевая вода должна быть прозрачна, бесцветна, не иметь запаха, быть приятной на вкус. Золотисто-желтая или бурая окраска воды свидетельствует о наличии в ней растворенных органических веществ. Соленый вкус обуславливается значительным количеством NaCl, а горький – присутствием MgSO4. Наличие в воде солей азотной и азотистой кислот, а также аммиака указывает на связь этой воды с участками, где происходит разложение органических веществ, следовательно, на возможность наличия болезнетворных бактерий. Кроме того, пригодность воды для питья определяется по наличию кишечной палочки Coli. Сама по себе кишечная палочка безвредна, но ее наличие также свидетельствует о возможном присутствии болезнетворных бактерий. Количественные показатели определяются коли-тиром, т,е. наименьшим количеством кубических сантиметров воды, содержащим одну кишечную палочку (300 см 3 ), или коли-тестом, т.е. наибольшим количеством кишечных палочек, содержащихся в 1 л воды ( 0 C | Второ-степен. компо-ненты, мг/л | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Na + + K + | Ca 2+ | Mg 2+ | HCO3 — | SO4 2- | Cl — | ||||||||||||||||||||||||||||||||||||||||||||||
| 25,0 | 6,5 | 33,0 | CO2=18 Br2=0,6 |
Выполнить следующие виды работ:
а) Пересчитать результаты анализа из ионной формы в миллиграмм-эквивалентную и эквивалент-процентную формы и составить таблицу.
б) Оценить воду по степени минерализации.
в) Определить и оценить воду по всем видам жесткости.
д) Определить и оценить воду по всем видам агрессивности.
е) Произвести классификацию подземных вод по химическому составу.
ж) Выразить химический состав подземных вод в виде:
2) прямоугольника солевого состава
з) Оценить пригодность воды для питьевого водоснабжения.
Порядок выполнения работы
а) Для перерасчета результатов анализа согласно заданию составляется таблица 10.
В природной воде содержание K + составляет всего 4 – 10% от содержания Na + , поэтому все расчеты производятся по Na + .
Таблица 10 — Порядок пересчета из ионной формы в другие
| Основные ионы | мг/л | мг∙экв/л | экв./проц. | пересчетные коэффициен-ты | прочие определения, мг/л |
| Катионы: Na + K + Ca 2+ Mg 2+ | 482,85 20,96 106,86 | 79,07 3,43 17,50 | 0,0435 0,0256 0,0499 0,0822 | CO2=18,0 Br2=0,6 | |
| ∑ ∑r + Анионы HCO3 — Cl — SO4 2- ∑ ∑r — Всего | 610,67 1,15 545,67 56,16 602,98 | 0,19 90,50 9,31 | 0,0164 0,0282 0,0208 |
б) Определяем степень минерализации
Таблица 11 — Классификация подземных вод по общей минерализации
| Оценка воды (раствора) | Минерализация г/л |
| Пресная Солоноватая Соленая Горько-соленая Слабые рассолы Крепкие рассолы | До 1 1 – 3 3 – 10 10 – 50 50 – 100 >100 |
Согласно классификации данная вода горько-соленая (М = 34,940 г/л).
в) Определяем все виды жесткости
Общая жесткость равна 20,96 + 106,86 = 127,82 мг-экв/л
Карбонатная жесткость равна 1,15 мг-экв/л
Постоянная жесткость равна 127,82 – 1.15 = 126,67 мг-экв/л
Таблица 12 — Классификация природных вод по общей жесткости
| Оценка воды | Жесткость, мг-экв/л |
| Очень мягкая Мягкая Умеренно-жесткая Жесткая Очень жесткая | До 1,5 1,5 – 3,0 3,0 – 6,0 6,0 – 9,0 >9,0 |
Согласно таблицы 12 данная вода относится к очень жестким.
г) По значению активной реакции определяем pH среду
Таблица 13 — Классификация природных вод по активной реакции
| Признак | Значение pH |
| Весьма кислые Кислые Нейтральные Слабощелочные Высокощелочные | 9 |
Так как в нашем анализе pH = 6,5, данная среда – кислая.
д) Определяем агрессивные свойства данной воды
— так как значение HCO3 — равно 1,15 мг-экв/л, т.е меньше 1,5 мг-экв/л, агрессивность выщелачивания присутствует;
— так как pH = 6,5, больше 5,0, общекислотная агрессивность отсутствует;
— в нашем анализе содержание свободной углекислоты составляет 18,0 мг/л. Из таблицы 14 берем значения коэффициентов a = 0,00 и b = 17. Вычисляем по формуле: a∙Ca + b = 17. Так как содержание свободной углекислоты составляет 18,0 мг/л, т.е. больше, чем определенное по формуле, углекислая агрессивность присутствует.
— Так как в данном анализе содержание SO4 2- составляет 2700 мг/л при содержании Cl — = 19350 мг/л, сульфатная агрессивность присутствует.
— Содержание Mg 2+ составляет 1300 мг/л (>1000), применяем формулу К — SO4 2- , т.е. 7000 – 2700 = 4300, 1300 0 C pH6,5 ( 5 )
По химическому составу вода хлоридно-натриевая, бромисто-углекислая.
Рисунок 15—Прямоугольник солевого состава.
з) Оценка воды для питьевого водоснабжения
Таблица 15 — Нормативы ГОСТ 2874-82
| № | Показатель | ПДК, не более | Данные анализа |
| Активная реакция, pH Сухой остаток, мг/л Общая жесткость, мг∙экв/л Хлориды Cl — , мг/л Сульфаты SO4 2 , мг/л | 6,0 – 9,0 | 6,5 127,82 |
Вывод: Данная вода по сухому остатку, общей жесткости, содержанию хлоридов и сульфатов не подходит для практического применения.
Таблица 14 — Значения коэффициентов «a» и «b» для определения углекислой агрессивности водной среды.
| Карбонат. жестк. мг-экв/л | Суммарное содержание Cl — + SO4 2- | ||||||||||
| 0 — 200 | 201 -400 | 401 — 600 | 601 — 800 | 801 — 1000 | >1000 | ||||||
| a | b | a | b | a | b | a | b | a | b | b | b |
| 1,4 1,8 2,1 2,5 2,9 3,2 3,6 4,0 4,3 4,7 5,0 5,4 5,7 6,1 6,4 6,8 7,1 7,5 7,8 8,2 8,6 9,0 | 0,01 0,04 0,07 0,10 0,13 0,16 0,20 0,24 0,28 0,32 0,36 0,40 0,44 0,48 0,54 0,61 0,67 0,74 0,81 0,88 0,96 1,04 | 0,01 0,04 0,06 0,08 0,11 0,14 0,17 0,20 0,24 0,28 0,32 0,36 0,40 0,44 0,47 0,51 0,55 0,60 0,65 0,70 0,76 0,81 | 0,01 0,03 0,05 0,07 0,09 0,11 0,14 0,16 0,19 0,22 0,25 0,29 0,32 0,36 0,40 0,44 0,48 0,53 0,58 0,63 0,68 0,73 | 0,00 0,02 0,04 0,06 0,08 0,10 0,12 0,15 0,17 0,20 0,23 0,26 0,29 0,33 0,36 0,40 0,44 0,48 0,53 0,58 0,63 0,67 | 0,00 0,02 0,04 0,06 0,07 0,09 0,11 0,13 0,16 0,19 0,22 0,24 0,27 0,30 0,33 0,37 0,41 0,45 0,49 0,53 0,57 0,61 | 0,00 0,02 0,04 0,05 0,07 0,08 0,10 0,12 0,14 0,17 0,19 0,22 0,25 0,28 0,31 0,34 0,38 0,41 0,44 0,48 0,52 0,56 |
Вопросы для контроля знаний студентов
1. Перечислите основные физические свойства подземных вод и показатели, которыми они характеризуются.
2. Что входит в понятие «состав подземных вод»?
3. Каковы источники минерализации подземных вод? Что входит в понятие общей минерализации воды?
4. Что называется агрессивной углекислотой? Перечислите все виды агрессивности воды по отношению к бетону.
5. Каковы свойства жесткой воды и в каких единицах выражается жесткость?
6. Почему при кипячении жесткость уменьшается?
7. Какой показатель pH должна иметь вода, чтобы ее можно было отнести к кислотной, активной по отношению к металлам?
8. Как оценивается пригодность воды для питьевых целей? При каком коли-титре вода считается допустимой к употреблению без кипячения?
9. Как проводится пересчет результатов анализа воды из весовой формы в эквивалент-процентную?
10. Чем отличаются минеральные воды от минерализованных?
Список использованных источников
1. Ларионов А.К. Занимательная гидрогеология. – М.: Недра, 1979. – 155 с.
2. Николадзе Г.И. Улучшение качества подземных вод. – М.: Стройиздат, 1988. – 366 с.
3. Пешковский Л.М., Перескокова Т.М. Инженерная геология. – М: Высшая школа, 1982. – 344 с.
4. Седенко М.В. Основы гидрогеологии и инженерной геологии. – М: Недра, 1979. – 216 с.
5. Ташенов К.М. Подготовка технической воды. – А: КазГАСА, 1977. – 173 с.
6. Толстой М.П., Малыгин В.А. Геология и гидрогеологи. – М: Недра, 1988. – 274 с.
источник
Формула Курлова, название воды. Графические изображения химического состава подземных вод.
1. Пересчет результатов химических анализов.Для выяснения количественных соотношений между ионами данные химических анализов, выполненные химической лабораторией, должны быть представлены в миллиграмм-эквивалентной форме, т.к. ионы в растворе реагируют между собой в эквивалентных количествах.
Пересчет из ионной формы, выраженной в мг/л в моль-экв, осуществляется делением числа кг каждого иона на его эквивалентный вес (ионный вес, деленный на валентность) или умножением на пересчетный коэффициент. Наиболее просто находить моль-экв.. пользуясь пересчетной таблицей.
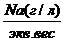
Na(мг/л)* К=Na моль- экв,.
где Кпересчетный коэффициент.
2.Пересчет результатов анализов. Пересчет результатов анализов заканчивается выражением его в процентах моль-эквивалентов. Для этого принимают каждую из вычисленных сумм мг/экв. катионов и анионов за 100% и по формулам

x = 
определяют процентное содержание каждого из катионов и анионов в отдельности. Все данные записывают в соответствующую ведомость химических анализов.
Ведомость химических анализов.
Содержание воды.
1. Вычисление видов жесткости. Жесткость воды обуславливается присутствием в воде ионов кальция,железа, алюминия, марганца, бария, стронция. Для вод , используемых в хозяйственных и технических целях, жесткость воды не учитывать нельзя. Жесткая вода требует больше мыла для получения пены, в ней медленнее развариваются овощи, мясо, образуется накипь на стенках труб и паровых котлов, что уменьшает теплоотдачу и требует большего потребления тепла. Различают жесткость воды общую, временную (устранимую, карбонатную) и постоянную (неустранимую, остаточную).
Общая жесткость определяется суммарным содержанием в воде иона Ca** и Mg**, так как содержание других элементов в воде ничтожно мало. Величина карбонатной жесткости соответствует количеству иона НСО 
Эта величина является расчетной и определяется по количеству ионов Са** Мg**, связанных с ионами НСО 



Временную жесткость определяют ионы Са** и Мg**, осаживающиеся при кипячении воды в виде карбонатов вследствие разрушения гидрокарбонат – иона.
Постоянную жесткость определяют ионы Са** и Мg**, остающиеся в воде после кипячения. Это есть разность между общей карбонатной жесткостью (в моль-экв).
Жесткость воды О.А.Алекин рекомендует следующее подразделение подземных вод по степени жесткости.
Классификация подземных вод по величине жесткости.
Для питьевых целей большей частью используются подземные воды с общей жесткостью до 7 моль-экв/л (около 20 нем. град.), но в некоторых местностях для питья потребляются и более жесткие воды.
2. Для наглядного изображения химического состава можно применять запись в виде формулы Курлова. Эта запись имеет структуру в виде дроби. В числителе в убывающем порядке (по абсолютному содержанию в % экв) записываются анионы, а в знаменателе в таком же порядке – катионы. Слева от дроби в кг/л становится газовый состав (СО 





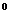

[CO 





В наименование состава воды включаются анионы и катионы, содержание которых превышает 25%-экв, название включает и специфические элементы, а также газовый состав.
Основные ионы Курлов М.Г. предлагает назвать в убывающем порядке, причем, первыми называются анионы, а вторыми , в таком же порядке – катионы. В приведенном примере название состава воды, выраженной формулой Курлова, будет борная, углекислая, железистая, фтористая, хлоридно- сульфатная натриево-магниевое.
Как видно из указанного примера, основные ионы определяют химический состав воды, а газовый и специфические элементы – специфическое содержание. При составлении химического названия воды необходимо соблюдать элементарные правила русского языка, согласно которым основное прилагательное пишется полностью а прилагательное, указывающее на второстепенное свойство предмета, пишется сокращенно. Если в химическом составе воды преобладают анионы хлоридный и сульфатный, причем сульфатного больше, чем хлоридного, то воду следует называть хлоридно-сульфатной, а не сульфатно-хлоридной.
Приведем два примера. Химический состав вод изображен в виде формул Курлова, причем скобками второстепенные ионы отделены от главных.
Здесь мы имеем пресную, гидрокарбонатную магниево-кальциевую воду с повышенным содержанием сульфатов. По классификации О. А. Алекина, данная вода принадлежит к гидрокарбонатному классу, группе кальция и магния и второму типу (CII Ca , Mg 0.4).
Вода солоноватая, сульфатно-хлоридная магниево-натриевая.
Как установлено, ионная форма свойственна в полной мере лишь водам низкой минерализации. При увеличении концентрации растворенных солей между ионами усиливается взаимодействие, причем развивается процесс, обратный диссоциации, т. е. ассоциация. В растворе образуются ассоциированные пары: нейтральные ( СаSО4 0 , МgSО4 0 , СаСО3 0 ) или несущие заряд (Mg(HCO3)2 Са(НСО3)2 + ).Ввиду сложности химического состава природных растворов во многих случаях нельзя предугадать, какие соли в каком порядке будут выпадать из данного раствора, так как на ход кристаллизации влияет температура и другие факторы. Поэтому наши пересчеты из ионной в солевую форму принято называть гипотетическими. При оценке питьевых, лечебных, технических и других качеств воды полезно принимать во внимание не только абсолютное содержание отдельных ионов, но
и предполагаемые ассоциации анионов с катионами (соли). Изображение химического состава вод в виде солей следует рассматривать как очень удобную рабочую гипотезу, позволяющую лучше разобраться в химических свойствах и происхождении природных вод.Пересчет из ионной формы в солевую производится в соответствии с растворимостью солей. В первую очередь комбинируются малорастворимые, а затем все более и более растворимые.
Простейшим для изображения единичных анализов является график-прямоугольник химического состава воды. График строится в виде двух прямоугольников, на одном из которых в масштабе нанесены %-эквиваленты анионов, на другом %-эквивалента катионов в последовательности, определяемой правилом Фрезениуса, т.е. в порядке их химической активности: К*, Na*, Mg**, Fe, Mg, H, NO , Cl, Br, I, SO, НCO, CO, OH. .
Графически изображать единичные анализы можно также с помощью круглой диаграммой Н.И.Толстихина.
Горизонтальной линией круг делится на две части. В верхней части по секторам откладываются в масштабе катионы слева направо в обратном порядке , чем на прямоугольной диаграмме, а в нижней — в таком же порядке анионы. Диаметр круга в масштабе отвечает минерализации воды, точно также и ширина прямоугольной диаграммы в масштабе соответствует величине минерализации воды.
Классификация Алекина О.А. сочетает принцип преобладающего иона и соотношение между ионами. За основу взято шесть главных иона (3 катиона, 3 аниона), содержание которых выражено в моль- эквивалентах:
По преобладающему аниону воды подразделяются на три класса: гидрокарбонатные и карбонатные (НСО 

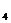
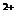
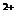


Каждая группа по соотношению между ионами подразделяются на три типа. Всего выделено четыре типа:
I) НСО 

II) НСО
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Студент — человек, постоянно откладывающий неизбежность. 10436 — 

195.133.146.119 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
источник