Настоящий документ устанавливает методику выполнения измерений (МВИ) массовой концентрации сульфат-ионов турбидиметрическим методом природной, а также неопалесцирующих, неокрашенных или слабоокрашенных проб сточной воды, содержащей не более 5 мг/дм 3 железа.
Диапазон измеряемых концентраций от 10 до 1000 мг/дм 3 сульфат-ионов. При более высокой концентрации сульфат-ионов (до 10000 мг/дм 3 ) допускается разбавление проб дистиллированной водой.
Мешающее влияние карбонатов и гидрокарбонатов устраняют соляной кислотой (в составе осадительной смеси).
Настоящая методика обеспечивает получение результатов анализа с погрешностью, не превышающей значений, приведенных в Таблице 1.
Диапазон измерений, значения показателей точности, повторяемости и воспроизводимости методики
Показатель точности (границы относительной погрешности при вероятности Р = 0,95), ± d , %
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости), s r
Показатель воспроизводимости (относительное среднеквадратическое отклонение воспроизводимости), s R, %
Значения показателя точности методики используют при:
— оформлении результатов измерений, выдаваемых лабораторией;
— оценке деятельности лабораторий на качество проведения испытаний;
— оценке возможности использования результатов измерений при реализации методики в конкретной лаборатории.
При выполнении измерений массовой концентрации сульфат-ионов применяют следующие средства измерения, реактивы, вспомогательные устройства, материалы и растворы.
3.1 Средства измерений и стандартные образцы
— Прибор для фотометрического анализа (фотометр, фотоэлектроколориметр или спектрофотометр, позволяющий измерять оптическую плотность в диапазоне 600 — 670 нм в кюветах с толщиной поглощающего слоя 30 и 50 мм.
— Весы лабораторные общего назначения (например, ВЛР-200, ВЛА-200) по ГОСТ 24104-2001.
— Колбы мерные вместимостью 100, 50, 25 см 3 2-го класса точности по ГОСТ 1770-74.
— Пипетки с одной отметкой 2-го класса точности вместимостью 5, 10, 25, 50 см 3 по ГОСТ 29169-91.
— Пипетки градуированные 2-го класса точности вместимостью 1, 2, 5, 10 см 3 по ГОСТ 29227-91.
— Государственный стандартный образец состава раствора сульфат-иона (1 мг/см 3 ) ГСО 7253-96.
Примечание. Допускается использование средств измерения и стандартных образцов с аналогичными или лучшими метрологическими характеристиками. Средства измерения должны быть поверены в установленные сроки.
3.3 Вспомогательные устройства в материалы
— Фильтры обеззоленные «синяя лента» по ТУ 609-1678-86.
— Колбы конические вместимостью 25, 100, 500, 1000 см 3 по ГОСТ 25336-82. Воронки лабораторные по ГОСТ 25336-82.
— Бутыли стеклянные и полиэтиленовые для хранения вспомогательных растворов, а также для хранения и транспортировки проб.
3.4 Приготовление растворов для анализа
60 г хлорида бария и 30 г борной кислоты растворяют при нагревании в 500 — 600 см 3 дистиллированной воды и охлаждают. Приливают 200 см 3 глицерина, 50 см 3 концентрированной соляной кислоты, разбавляют дистиллированной водой до 1000 см 3 , перемешивают и оставляют на 2 — 3 дня. Затем приготовленный раствор декантируют с осадка.
3.4.2 . Рабочий раствор сульфат-иона, массовая концентрация 100 мг/дм 3
В мерную колбу вместимостью 50 см 3 помещают 5 см 3 ГСО состава раствора сульфат-иона (массовая концентрация 1 мг/см 3 ), разбавляют до метки дистиллированной водой и тщательно перемешивают. Срок хранения полученного раствора — 3 месяца.
Примечание. При использовании ГСО с концентрацией сульфат-иона 10 мг/см 3 необходимо приготовить промежуточный раствор с концентрацией 1 мг/см 3 , разбавляя в мерной колбе 5 см 3 раствора ГСО до 50 см 3 дистиллированной водой.
Метод измерения массовой концентрации сульфат-иона основан на образовании стабилизированной суспензии сульфата бария в солянокислой среде с последующим измерением светорассеяния в направлении падающего луча (в единицах оптической плотности).
При выполнении измерений массовой концентрации сульфат-ионов необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007-76, требования электробезопасности при работе с электроустановками по ГОСТ 12.1.019-79.
Помещение должно соответствовать требованиям пожаробезопасности по ГОСТ 12.1.004-91 и иметь средства пожаротушения по ГОСТ 12.4.009-83. Содержание вредных веществ в воздухе не должно превышать допустимых значений по ГОСТ 12.1.005-88. Организация обучения работающих безопасности труда по ГОСТ 12.0.004-90.
К выполнению измерений и обработке результатов допускают специалиста, имеющего высшее или среднее специальное химическое образование или опыт работы в химической лаборатории, прошедшего соответствующий инструктаж, освоившего метод в процессе тренировки и уложившегося в нормативы оперативного контроля при выполнении процедур контроля погрешности.
При выполнении измерений в лаборатории должны быть соблюдены следующие условия:
температура воздуха 20 ± 5 °С;
атмосферное давление 84,0 — 106,7 кПа (630 — 800 мм рт.ст.);
влажность воздуха не более 80 % при температуре 25 °С;
напряжение в сети 220 ± 22 В;
частота переменного тока 50 ± 1 Гц.
Отбор проб производится в соответствии с требованиями ГОСТ Р 51592-2000 «Вода. Общие требования к отбору проб».
Объем отбираемой пробы составляет не менее 100 см 3 . Пробу можно не консервировать, однако при наличии соединений серы иных форм (сульфиты, сульфиды, тиосульфаты) проба должна быть проанализирована в течение 2 час.
При подготовке к выполнению измерений должны быть проведены следующие работы: приготовление вспомогательных (п. 3.4) и градуировочных растворов (п. 9.1) и градуировка фотометра (спектрофотометра).
9.1 Приготовление градуировочных растворов
В шесть мерных колб вместимостью 50 см 3 помещают по 20 см 3 осадительного раствора по п. 3.4.1 и затем в пять из них приливают по каплям 2,0; 4,0; 6,0; 8,0; 10,0 см 3 рабочего раствора сульфат-иона с концентрацией 100 мг/дм 3 , что соответствует его содержанию 0,2; 0,4; 0,6; 0,8; 1,0 мг в 50 см 3 , и затем содержимое всех колб (включая колбу, в которую сульфат-ион не добавляли) разбавляют до метки дистиллированной водой.
Растворы перемешивают в течение 30 сек и через 5 — 10 мин измеряют оптическую плотность каждого раствора относительно раствора, приготовленного без сульфат-ионов.
Примечание. Измерения для каждого раствора должны производиться строго в одно и то же время после добавления раствора сульфат-ионов.
9.2 Построение градуировочного графика
Через 5 — 10 мин после приготовления растворов по п. 9.1 измеряют оптическую плотность (не менее пяти отсчетов) полученных растворов при длине волны 600 — 670 нм в зависимости от спектральных характеристик светофильтра, входящего в комплект прибора. При использовании спектрофотометров измерения производят при длине волны 650 нм. Толщина поглощающего слоя — 30 или 50 мм, раствор сравнения — первый градуировочный раствор (без сульфат-иона).
Вычисляют среднее арифметическое полученных значений оптической плотности и строят градуировочный график в координатах оптическая плотность — содержание сульфат-ионов в растворах градуировочной серии, мг.
Рекомендуется для хранения и обработки градуировочного графика использовать возможности микропроцессора прибора и программы для ПЭВМ.
9.3 Контроль стабильности градуировочной характеристики
Контроль стабильности градуировочной характеристики проводят при смене партий реактивов, но не реже одного раза в месяц. Средствами контроля являются вновь приготовленные образцы для градуировки (не менее 3 образцов из приведенных в п. 9.1). Измеряют оптическую плотность (не менее 5 измерений) и находят среднее арифметическое полученных значений.
Градуировочную характеристику считают стабильной при выполнении для каждого образца для градуировки следующего условия:
где X — результат контрольного измерения массовой концентрации сульфат-ионов в образце для градуировки;
С — аттестованное значение массовой концентрации сульфат-ионов в образце для градуировки;
s Rл — среднеквадратическое отклонение внутрилабораторной прецизионности, установленное при реализации методики в лаборатории.
Примечание. Допустимо среднеквадратическое отклонение внутрилабораторной прецизионности при внедрении методики в лаборатории устанавливать на основе выражения: s Rл= 0,84 s R, с последующим уточнением по мере накопления информации в процессе контроля стабильности результатов анализа.
Значения s R приведены в Таблице 1.
Если условие стабильности градуировочной характеристики не выполняется только для одного образца для градуировки, необходимо выполнить повторное измерение этого образца с целью исключения результата, содержащего грубую погрешность.
Если градуировочная характеристика нестабильна, выясняют причины и повторяют контроль с использованием других образцов для градуировки, предусмотренных методикой. При повторном обнаружении нестабильности градуировочной характеристики строят новый градуировочный график.
Пробу сточной воды фильтруют через фильтр «синяя лента», отбрасывая первые порции фильтрата. Затем анализируют две аликвотные порции воды. Содержание сульфат-ионов в аликвотной порции должно составлять 0,2 — 1,5 мг, желательно 0,5 — 1,5 мг.
В три мерные колбы вместимостью 50 см 3 помещают по 20 см 3 осадительной смеси по п. 3.4.1, затем в две из них по каплям вносят 1 — 20 см 3 анализируемой пробы. Содержимое всех колб быстро доводят до метки дистиллированной водой, перемешивают в течение 30 сек и через 5 — 10 мин (точное значение времени выдержки должно быть таким же, как и при приготовлении градуировочных растворов) измеряют оптическую плотность растворов проб относительно раствора, приготовленного без введения пробы. Условия измерения оптической плотности те же, что и при построении градуировочной зависимости.
Вычисляют среднее арифметическое полученных значений оптической плотности для каждого из двух растворов проб и находят при помощи градуировочной зависимости содержание сульфат-ионов в отобранной аликвотной порции анализируемой пробы воды, мг.
Примечание. Если содержание сульфат-ионов в аликвотной порции пробы оказывается менее 0,2 мг или более 1,5 мг, то анализ повторяют, изменив аликвотную порцию.
Массовую концентрацию сульфата вычисляют по формуле:
где X — массовая концентрация сульфат-ионов в пробе, мг/дм 3 ;
Q — содержание сульфат-ионов в аликвотной порции пробы, найденное по градуировочному графику, мг;
V — объем аликвотной порции пробы, см 3 .
За результат измерения Хсрпринимают среднее арифметическое значение двух параллельных определений Х1и Х2
для которых выполняется следующее условие:
где r — предел повторяемости, значения которого приведены в Таблице 2.
Значения предела повторяемости при вероятности Р = 0,95
Предел повторяемости (относительное значение допускаемого расхождения между двумя результатами параллельных определений), r, %
При невыполнении условия (1) могут быть использованы методы проверки приемлемости результатов параллельных определений и установления окончательного результата согласно раздела 5 ГОСТ Р ИСО 5725-6.
Расхождение между результатами измерений, полученными в двух лабораториях, не должно превышать предела воспроизводимости. При выполнении этого условия приемлемы оба результата измерений, и в качестве окончательного может быть использовано их среднее арифметическое значение. Значения предела воспроизводимости приведены в Таблице 3.
Значения предела воспроизводимости при вероятности Р = 0,95
Предел воспроизводимости (относительное значение допускаемого расхождения между двумя результатами измерений, полученными в разных лабораториях), R, %
При превышения предела воспроизводимости могут быть использованы методы оценки приемлемости результатов анализа согласно раздела 5 ГОСТ Р ИСО 5725-6.
Результат измерения Хсрв документах, предусматривающих его использование, может быть представлен в виде: Хср± D , Р = 0,95,
где D — показатель точности методики.
Значение D рассчитывают по формуле: D = 0,01 ×d × Хср. Значение d приведено в таблице 1.
Допустимо результат измерения в документах, выдаваемых лабораторией, представлять в виде: Хср± D л , Р = 0,95, при условии D л D , где
Хср — результат измерения, полученный в соответствии с прописью методики;
± D л — значение характеристики погрешности результатов измерений, установленное при реализации методики в лаборатории, и обеспечиваемое контролем стабильности результатов измерений.
Примечание. При представлении результата измерения в документах, выдаваемых лабораторией, указывают:
— количество результатов параллельных определений, использованных для расчета результата измерения;
— способ определения результата измерения (среднее арифметическое значение или медиана результатов параллельных определений).
Контроль качества результатов измерений при реализации методики в лаборатории предусматривает:
— оперативный контроль процедуры измерений (на основе оценки погрешности при реализации отдельно взятой контрольной процедуры);
— контроль стабильности результатов измерений (на основе контроля стабильности среднеквадратического отклонения повторяемости, среднеквадратического отклонения внутрилабораторной прецизионности, погрешности).
13.1 Алгоритм оперативного контроля процедуры измерений с использованием метода добавок
Оперативный контроль процедуры измерений проводят путем сравнения результата отдельно взятой контрольной процедуры Ккс нормативом контроля К.
Результат контрольной процедуры Кк рассчитывают по формуле
где Х ¢ ср — результат измерения массовой концентрации сульфат-ионов в пробе с известной добавкой — среднее арифметическое двух результатов параллельных определений, расхождение между которыми удовлетворяет условию (1) раздела 11.
X ср — результат измерения массовой концентрации сульфат-ионов в исходной пробе — среднее арифметическое двух результатов параллельных определений, расхождение между которыми удовлетворяет условию ( 1 ) раздела 11 .
Норматив контроля К рассчитывают по формуле
где 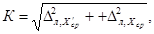
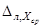
Примечание. Допустимо характеристику погрешности результатов измерений при внедрении методики в лаборатории устанавливать на основе выражения: D л = 0,84 × D , с последующим уточнением по мере накопления информации в процессе контроля стабильности результатов измерений.
Процедуру измерений признают удовлетворительной, при выполнении условия:
При невыполнении условия (2) контрольную процедуру повторяют. При повторном невыполнении условия (2) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
13.2 Алгоритм оперативного контроля процедуры измерений с применением образцов для контроля
Оперативный контроль процедуры анализа проводят путем сравнения результата отдельно взятой контрольной процедуры Ккс нормативом контроля К.
Результат контрольной процедуры Кк рассчитывают по формуле
где Сср — результат измерения массовой концентрации сульфат-ионов в образце для контроля — среднее арифметическое двух результатов параллельных определений, расхождение между которыми удовлетворяет условию (1) раздела 11;
С — аттестованное значение образца для контроля.
Норматив контроля К рассчитывают по формуле
где ± D л — характеристика погрешности результатов измерений, соответствующая аттестованному значению образца для контроля.
Примечание. Допустимо характеристику погрешности результатов измерений при внедрении методики в лаборатории устанавливать на основе выражения: D л = 0,84 × D , с последующим уточнением по мере накопления информации в процессе контроля стабильности результатов измерений.
Процедуру измерений признают удовлетворительной, при выполнении условия:
При невыполнении условия (3) контрольную процедуру повторяют. При повторном невыполнении условия (3) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
Периодичность оперативного контроля процедуры измерений, а также реализуемые процедуры контроля стабильности результатов измерений регламентируют в Руководстве по качеству лаборатории.
источник
Цель работы.Научиться определять содержание сульфатов в воде и осуществлять первичную обработку результатов.
Реактивы и растворы.
1. Хромат бария (ВаСгО4), химически чистый.
2. 2,5 N раствор соляной кислоты. Берут 2,08 мл концентрированной соляной кислоты и доводят объем до 10 мл дистиллированной водой.
3. 10%-ный раствор иодида калия.
4. 5%-ный раствор аммиака. Берут 20 мл 25%-ного раствора аммиака и доводят объем 100 мл дистиллированной водой.
5. 0,05 N раствор тиосульфата натрия. Берут 12,40 г NаS2O3×5H2O и доводят объем до метки дистиллированной водой в мерной колбе на 1 л.
7. Реактивы для определения поправки к титру раствора Na2S2O3.
1 Мерные цилиндры вместимостью 200 и 100 мл.
2 Конические колбы вместимостью 300 мл — по числу проб плюс одна.
3 Пипетки: на 1 мл 3 шт. (для раствора НСl, аммиака и крахмала); на 10 мл 3 шт. (для раствора НСl, KJ, KJO3).
4 Бюретка вместимостью 25 мл.
5 Мерные колбы вместимостью 250 и 100 мл.
7 Фильтровальная бумага с синей полосой.
Общие сведения.Соли серной кислоты (сульфаты) присутствуют в большинстве пресных водоемов в количествах до 20-30 мг/л. Больше всего сульфатов обнаруживается в водоемах расположенных на грунтах, содержащих СаSO4, и засолоненных, в частности в некоторых южных районах Украины и европейской части России.
Существенного влияния на существование живых организмов сульфаты сами по себе не оказывают, но большое их содержание при обилии в воде органических веществ может привести к образованию сероводорода.
Повышенное количество сульфатов (более 20—30 мг/л) свидетельствует о постороннем загрязнении водоема. Для этого изучают сульфаты в водоемах, подлежащих рыбохозяйственному использованию. Кроме того, определение количества сульфатов необходимо для полного представления о составе воды, для получения величины ее минерализации.
Содержание в воде сульфат-иона определяют несколькими методами. Самым точным из них является весовой метод, но он трудоемок, поэтому большое распространение имеет объемный иодометрический.
Принцип объемного метода заключается в осаждении сульфат-ионов хроматом бария ВаСгO4:
Количество выделившихся хромат-ионов, эквивалентное осажденному количеству сульфатов, определяют йодометрически, предварительно добавив в пробу КJ и НСl. Количество выделившегося йода будет эквивалентно количеству анионов СгO4 2 ¯ в растворе:
Выделившийся йод оттитровывают раствором тиосульфата натрия:
По количеству тиосульфата натрия, пошедшему на титрование, судят о содержании в воде сульфат-ионов.
Ход определения.Необходимое количество испытуемой воды обычно
200 мл, но при очень большом содержании сульфатов берут меньший объем и разбавляют пробу дистиллированной водой до 200 мл, помещают в коническую колбу, добавляют 1 мл 2,5 N раствора НСl и нагревают до кипения.
В кипящую пробу осторожно (иначе возможно выбрасывание пара и жидкости) всыпают 500 мг ВаСгO4, продолжают кипятить еще несколько минут, пока раствор из лимонно-желтого не станет светло-оранжевым.
Затем нейтрализуют 5%-ным раствором аммиака, добавляя его по каплям до перехода оранжеватой окраски в лимонно-желтую, и охлаждают до комнатной температуры. Охлажденную пробу с осадком переносят в мерную колбу на 250 мл и доводят общий дистиллированной водой до метки, многократно споласкивая дистиллированной водой колбу с пробой и вливая эту воду в мерную колбу.
Содержимое мерной колбы перемешивают и фильтруют через плотный беззольный фильтр (с синей полосой) в мерную колбочку на 100 мл, отбрасывая первые порции фильтрата 100 мл фильтровальной жидкости переносят в коническую колбу, приливают 10 мл 10%-ного раствора KJ и 10 мл 2,5 N раствора НСl и спустя 5 мин титруют выделившийся йод 0,05 N раствором тиосульфата, определяя конец титрования с помощью крахмала.
Определение поправочного коэффициента к титру раствора тиосульфата натрия.
Поправочный коэффициент определяют по 0,01 N раствору КJOз следующим образом. В коническую колбу для титрования пипеткой вносят 10 мл 0,01 N раствора КJO3, добавляют 0,5 г кристаллического KJ (взвешенного на технохимических весах) и 1 мл раствора H2SO4 или 2 мл 25%-ной Н2SО4 или концентрированной НСl. Содержимое колбы перемешивают, затем титруют выделившийся йод, раствором тиосульфата натрия, непрерывно перемешивая, до слабо-соломенного цвета. Чтобы точнее уловить конец титрования, вводят в колбу 1 мл свежеприготовленного раствора крахмала: крахмал в присутствии свободного йода окрашивает раствор в синий цвет. Дотитровывают пробу до обесцвечивания от одной капли раствора тиосульфата.
Титрование при определении поправочного коэффициента к концентрации раствора Nа2S2О3 проводят дважды. Расхождение в показаниях бюретки при параллельном титровании не должно превышать 0,03-0,05 мл. Поправочный коэффициент Копределяют по формуле (*), где n — количество мл раствора Nа2S2О3, пошедшее на титрование 10 мл раствора КJO3.
В формулу (*) подставляют среднее арифметическое значение n из двух параллельных титрований.
Вычисление результатов.Записи в процессе определения ведут форме по образцу табл.1(прилож.). Содержание в воде сульфатов выражают в мг/л и ммоль(экв.)/л. Расчетная формула имеет вид:
С (SО4 2 ¯) = (2,5×А×К×1,6×1000)/V мг/л (36)
где А — количество 0,05 N раствора тиосульфата натрия, пошедшее на титрование 100 мл фильтрата, К — поправочный коэффициент к нормальности раствора тиосульфата натрия; 1,6 — количество мг SО4 2 ¯, эквивалентное 1 мл 0,05 N раствора тиосульфата натрия, см. уравнения реакций (33), (34), (35); 2,5 — коэффициент пересчета, необходимый, поскольку из общего объема пробы (250 мл) после осаждения сульфатов для титрования было взято только 100 мл; V-объем пробы, взятый для анализа.
Для перехода количества мг/л сульфатов в ммоль(экв)/л полученную по формуле (36) величину делят на 48,03 , что соответствует 1 ммоль(экв) аниона SО4 2– .
Результаты определения сульфатов следует округлить до 0,001 ммоль(экв)/л и 0,1 мг/л.
Отчет.Отчет по данной лабораторной работе состоит в устном собеседовании с преподавателем. Результаты измерений представляются по установленной форме.
КОНТРОЛЬНЫЕ ВОПРОСЫ
1.О чем свидетельствует большое количество сульфатов, содержащихся в природной воде?
2.Какие существуют методы определения в воде количества SО4 2 ¯?
3.Изложите принцип определения сульфатов объемным методом.
4.Какая существует зависимость между количеством раствора Na2S2О3, пошедшим на титрование пробы, и содержанием в ней SО4 2 ¯?
5. В каких единицах выражают содержание в воде сульфатов?
ЛАБОРАТОРНАЯ РАБОТА №11.
ОПРЕДЕЛЕНИЕ ВОДОРОДНОГО ПОКАЗАТЕЛЯ (рН)
ПРИРОДНОЙ ВОДЫ
Цель работы.Научиться определять водородный показатель (рН) природной воды.
Приборы и реактивы.
2. Фосфатная смесь (КН2РО4 и Na2НРО4×2Н2О) для приготовления растворов со значениями рН от 5 до 8.
3. Борноборатная и боратнощелочная смесь (Na2B4O7×10H3BO3; Na2B4O×10H2O и NaOH) для приготовления буферных растворов со значениями рН более 8.
4. В качестве индикаторов по интервалам значений рН применяют следующие органические красители: метиловый красный при рН 4,4-6,0; бромтимоловый синий при рН 6,0-7,6; крезоловый красный при рН 7,6-8,2; тимоловый синий при рН 8,2-9,0.
5. Буферные растворы обычно готовят в пробирках, которые запаивают после приготовления шкалы. Точное значение рН в пробирках шкалы определяют электрометрическим методом. В продаже имеются готовые шкалы буферных растворов для определения рН.
6. рН-метр, электролитическая ячейка со стеклянными и хлорсеребряным электродами.
Общие сведения.Водородный показатель воды (рН) — величина, характеризующая активность или концентрацию ионов водорода и численно равная отрицательному десятичному логарифму этой активности или концентрации, выраженной в моль/дм 3 : рН = — lg aH + = — lg CH + , где aH + — активность ионов водорода, Сн + — концентрация ионов водорода.
В воде концентрация ионов водорода определяется электролитической диссоциацией по уравнению: Н2О 
где Сн + и Сон¯ — соответственно концентрации ионов водорода и гидроксильной группы, моль/дм 3 . Поскольку степень диссоциации воды очень мала, то, не внося значительной погрешности, можно считать концентрацию недиссоцииированых молекул воды постоянной величиной и объединить ее с Кд в одну постоянную:
В этом случае уравнение примет вид; Кw = Сн + Сон¯. Величина Кw, называется ионным произведением воды и является постоянной для данной температуры, так для 25°С Kw= 10 -14 .
Водородный показатель играет важную роль в определении качества воды, в речных водах его значение обычно колеблется от 6,5 до 8,5, в атмосферных осадках — от 4,6 до 6,1, в болотных водах — от 5,5 до 6,0, в воде океана от 7,9 до 8,3, в шахтных и рудных водах иногда достигает 1 ,0, а в воде содовых озер и термальных источников — 10,0. Концентрация ионов водорода подвержена сезонным колебаниям — зимой водородный показатель для большинства речных вод составляет 6,8-7,4, летом 7,4-8,2.
Концентрация ионов водорода имеет большое значение для химических и биологических процессов, протекающих в природных водах: от величины водородного показателя зависит развитие и жизнедеятельность водных растений, устойчивость различных форм миграции элементов, степень агрессивности воды по отношению к металлам и бетону и др.
Для определения водородного показателя (рН) применяют электрометрический или колориметрический метод. Электрометрический метод дает более точные результаты.
Определение рН воды.Потенциометрический (электрометрический) метод определения рН воды со стеклянным электродом наиболее универсален и точен. Приборы, измеряющие рН этим методом, называются рН-метрами. Большинство серийных рН-метров позволяет производить измерения с точностью 0,05-0,02 единицы рН в водах с широким диапазоном минерализации и содержащих окрашенные и взвешенные вещества.
Принцип действиярН-метра основан на измерении разности потенциалов, возникающих на границах между внешней поверхностью стеклянной мембраны электрода и исследуемым раствором с одной стороны и внутренней поверхностью мембраны и стандартным раствором кислоты с другой, поскольку внутренний стандартный раствор стеклянного электрода имеет постоянную активность ионов водорода, потенциал на другой поверхности мембраны не изменяется и измеряемая разность потенциалов определяется потенциалом, возникающим на границе внешней поверхности электрода и исследуемого раствора.
Измерения проводят относительно потенциала другого электрода, называемого электродом сравнения, В качестве последнего выбирают такой электрод, потенциал которого практически не зависит от активности ионов водорода, например каломельный, хлорсеребряный.
Наиболее распространенными типами рН-метров при измерении рН поверхностных вод являются «рН-121» и «рН-47М».
Общая схема измерения рН состоит из следующих операций. Проверяют и устанавливают так называемый «механический нуль» прибора перед его включением. Включают рН-метр, и после прогрева и установки «электрического нуля» проверяют и корректируют шкалу по двум-трем буферным растворам. Для этого в стакан с буферным раствором помещают стеклянный и каломельный (хлорсеребряный) электроды.
В стакан помещают термометр с ценой деления 0,1-0,5°С. К измерению приступают, убедившись, что на поверхности шарика стеклянного электрода нет пузырьков воздуха. Измерив рН буферного раствора, записывают его значение и спустя 2-3 мин. Повторяют измерение. Если значения рН совпадают, потенциал электрода считают установившемся и по инструкции к прибору проводят коррекцию шкалы. Затем аналогичные операции проводят со вторым и третьим буферными растворами.
После проверки и коррекции шкалы прибора стакан, электроды и термометр тщательно ополаскивают дистиллированной, а затем исследуемой водой. Последнюю наливают в стакан и измеряют рН таким же способом, как и в случае буферных растворов. Измерения повторяют 2-3 раза или больше с интервалами 2-3 мин. Последние два показания прибора должны быть одинаковыми.
Отчет.Отчет по данной лабораторной работе состоит в устном собеседовании с преподавателем. Результаты измерений представляются по установленной форме.
КОНТРОЛЬНЫЕ ВОПРОСЫ
1 Что такое водородный показатель рН?
2. Как можно рассчитать водородный показатель?
3. Какая реакция будет у воды при рН 10 и 5? Почему?
4. Каково значение рН природных вод?
5. Какие существуют методы для определения рН? Их точность?
6. Что такое рН-метр? Опишите принцип его действия.
7. Как определить рН воды электрометрическим методом?
источник
Сульфаты – это природные компоненты, представляющие собой соли серной кислоты. Большинство сульфатов светлого окраса, небольшой твердости и растворимы в воде.
Содержание сульфатов в воде обусловлено природным и антропогенным факторами.
К природным факторам относятся сульфаты:
- Осадочного происхождения – возникают в результате химических и озерных осадков;
- Представляющие из себя минералы зоны окисления;
- Возникшие в результате вулканической деятельности;
- Возникшие в результате растворения минералов, таких как гипс;
- Возникшие из воздуха (в результате окисления оксида серы (IV)).
К антропогенным факторам относятся сульфаты, возникшие в результате технологических процессов (большое количество содержится в сточных водах предприятий).
Следует отметить, что некоторые воды, насыщенные сульфатами, используются в санаториях для лечения еще с древних времен.
Они обладают следующими полезными свойствами:
- Налаживают перистальтику кишечника;
- Выводят токсичные вещества из организма;
- Снимают воспаления;
- Предотвращают образование холестериновых бляшек.
Сами по себе сульфаты в питьевой воде не оказывают токсического влияние на здоровье человека, но создают ряд неприятных особенностей в виде расстройства ЖКТ, возникновения аллергических реакций и зуда слизистых покровов. Кроме того, вода с данной примесью имеет неприятный соленый вкус.
Обильное содержание сульфатов в воде оказывает негативное влияние и на коммуникации. В случаях, когда содержание превышает значение 200 мг на литр, размываются свинцовые трубы и в воде появляются токсичные примеси.
Вступая в реакцию с кальцием, сульфаты образуют прочную накипь.
ПДК сульфатов в воде строго регламентируется санитарными нормами. В России данной примеси не должно быть более 500 мг на литр, в европейских странах – не более 250 мг на литр.
Повышенное присутствие сульфатов в воде служит поводом для отказа от ее использования как в питьевых, так и в хозяйственных целях.
Определить сульфат ионы в воде можно несколькими способами:
- На вкус – вода с большим содержанием примеси солоноватая;
- Опытным путем в лаборатории (рекомендуем).
Для того чтобы лабораторный анализ показал точные данные о сульфатах в воде, необходимо правильно собрать материал:
- Слить воду сильным напором в течении 5-10 минут (при отборе пробы из крана);
- Промыть чистую пластиковую тару (для питьевой воды) несколько раз в исходной воде без моющего средства;
- Уменьшить напор и отобрать 1,5-2 литра тонкой струей по стенке сосуда
- Закрыть емкость крышкой и незамедлительно доставить в пункт приема проб
Чтобы избавиться от избытка сульфатов в воде рекомендуется установить мембранный фильтр.
В лаборатории «ИОН» вы сможете провести подробный анализ вашей воды и узнать и методах ее улучшения. Мы работаем более 20 лет и исследуем любые виды вод:
- Водопроводную;
- Из скважин и колодцев;
- Бутилированную
- Из водоемов и родников;
- Из мест общего пользования;
- Технологическую.
Сотрудники нашей лаборатории – лучшие специалисты в стране, постоянно занимающиеся поиском новых методов диагностики веществ и материалов. Мы располагаем современным парком оборудования и тесно сотрудничаем с крупнейшими разработчиками аналитического оборудования. Гарантируем качественное проведение работы в строго установленные сроки.
Повышенное содержание данной примеси чаще всего встречается в колодцах, неглубоких скважинах, реках и озерах. Перед использованием такой воды в хозяйственных нуждах убедитесь в том, что содержание нитратов не превышает норму.
Главная причина жесткой воды – наличие солей кальция и магния. Источники жесткости имеют исключительно природный характер, это единственная экологическая проблема, которой не присущ антропогенный фактор.
* Бесплатный выезд для физических лиц в пределах МКАД при заказе на сумму более 5 000 ₽. Подробнее в разделе Доставка и оплата
© 1997-2019 — Лаборатория ИОН. Все права защищены.
Для химического анализа необходимо заполнить водой чистую пластиковую тару (оптимально 1,5 л). Использовать бутылки из-под сладких, газированных или ароматизированных напитков, а также солёной или минеральной воды недопустимо.
Если выбранный Вами анализ включает определение содержания нефтепродуктов, необходимо заполнить дополнительную стеклянную тару объемом 0,2 л.
Если выбранный Вами анализ включает определение содержания сероводорода, необходимо заполнить дополнительную стеклянную тару объемом 0,5 л (необходимо использовать консервант).
При отборе воды из проточного источника, непосредственно перед отбором необходимо пролить воду сильной струёй в течение 3-5 минут. Перед отбором проб ёмкости и крышки необходимо 3 раза промыть изнутри водой, подлежащей анализу. Использование моющих средств недопустимо. Наполнять тару необходимо тонкой струёй по стенке сосуда «под горлышко». Это снижает насыщение воды кислородом и предотвращает протекание реакций.
Для микробиологического анализа необходимо использовать стерильный контейнер для биоматериалов объемом 150-200 мл.
Перед взятием пробы необходимо протереть водопроводный кран спиртовой салфеткой, уделив особое внимание месту выхода воды.
При отборе воды из водопровода, скважины или колонки необходимо пролить воду сильной струёй в течение 3–5 минут.
При отборе воды из колодца с помощью ведра необходимо обдать ведро кипятком для дезинфекции. Отбор пробы через поливочные шланги и предметы, контактирующие с почвой, не допускается.
Для отбора пробы необходимо надеть перчатки и вскрыть упаковку стерильного контейнера. Не касаясь внутренней поверхности ёмкости, отобрать образец воды (2/3 объема контейнера) и закрыть крышкой.
Рекомендуем доставлять пробу сразу после отбора.
Если сразу после отбора нет возможности доставить пробу в лабораторию, допускается хранение образцов при температуре 2–10 °C в течение 1 суток.
Съезд на ул. Руставели, на первом светофоре поворот налево на ул. Яблочкова.
Через 300 м поворот направо на ул. Гончарова, через 500 м поворот налево (напротив дома №6), через 200 метров вы на месте — ул. Добролюбова, 21А, корпус А, 3-й подъезд (серая дверь, белый козырек из поликарбоната), помещение 14.
Поворот на ул. Руставели, на светофоре поворот направо на ул. Добролюбова, через 300м на светофоре поворот налево на ул. Гончарова, напротив дома №6 поворот направо, через 200 метров вы на месте — ул. Добролюбова, 21А, корпус А, 3-й подъезд (серая дверь, белый козырек из поликарбоната), помещение 14.
Двигаясь по ул. Милошенкова, поворачиваем на ул. Добролюбова
Через 150 метров поворот направо, за домом 21АкБ поворот налево, через 100-120 метров вы на месте — ул. Добролюбова, 21А, корпус А, 3-й подъезд (серая дверь, белый козырек из поликарбоната), помещение 14.
Ближайшее станция метро – Фонвизинская (600 м)
Последний вагон из центра. Выход в сторону улицы Фонвизина. Из стеклянный дверей направо. Перейти через пешеходный переход и идти через дворы в соответствии со схемой. Пункт назначения — ул. Добролюбова, 21А, корпус А, 3-й подъезд (серая дверь, белый козырек из поликарбоната), помещение 14.
Анализ «Минимальный» содержит минимальный и обязательный перечень загрязнителей, часто встречающихся в питьевой воде, и включает 16 показателей:
- органолептические: мутность, цветность, запах, привкус;
- общехимические: рН, жесткость, окисляемость перманганатная, минерализация, электропроводность, щелочность общая, щелочность свободная;
- катионы: железо, аммоний;
- анионы: нитраты, карбонат, гидрокарбонат.
Данный набор рекомендуется для исследования воды хозяйственно-бытового назначения. Анализ «Минимальный» не обладает достаточной информативностью для подбора системы водоочистки, так как не позволяет получить полную картину о безопасности воды. Если Вы планируете использовать воду в питьевых целях, рекомендуем обратить внимание на наборы, содержащие большее число параметров.
- Точность определения
- Подходит для воды, применяемой в хоз-бытовом назначении
- Срок выполнения — 3-4 рабочих дня
- Не подходит для воды, применяемой в питьевых целях
- Не подходит для корректного подбора/оценки работы фильтров
- Не включает определение тяжелых металлов
- Не включает определение органических загрязнителей
Анализ «Начальный» предназначен для выявления наиболее часто встречающихся вредных веществ в питьевой воде и включает 23 параметра:
- органолептические: мутность, цветность, запах, привкус;
- общехимические: рН, жесткость, окисляемость перманганатная, минерализация, электропроводность, щелочность общая, щелочность свободная;
- катионы: железо, аммоний, марганец, калий, магний, кальций;
- анионы: фториды, хлориды, нитраты, сульфаты, карбонаты, гидрокарбонаты.
Данный анализ рекомендуется для воды централизованных систем водоснабжения. По протоколу анализа «Начальный» также можно сделать вывод о корректности работы системы водоочистки. В перечень определяемых параметров входят органолептические показатели, общие химические показатели, а также содержание катионов и анионов.
- Точность определений
- Подходит для водопроводной воды
- Позволяет оценить эффективность работы системы водоочистки
- Позволяет корректно настроить водоочистное оборудование
- Срок выполнения — 5 рабочих дней
- Не включает определение тяжелых металлов
- Не включает определение органических загрязнителей
- Не подходит для полной проверки воды из колодца или скважины
Анализ «Расширенный» содержит перечень наиболее часто встречающихся загрязнителей воды, вне зависимости от источника, и включает 31 показатель:
- органолептические: мутность, цветность, запах, привкус;
- общехимические: рН, жесткость, окисляемость перманганатная, минерализация, электропроводность, щелочность общая, щелочность свободная;
- катионы: железо, аммоний, марганец, калий, магний, кальций, алюминий, натрий;
- анионы: фториды, хлориды, нитраты, сульфаты, карбонаты, гидрокарбонаты;
- тяжелые металлы и металлоиды: медь, мышьяк, свинец, кадмий, цинк, стронций.
Данный набор рекомендуется, в первую очередь, владельцам колодцев и скважин. Помимо катионов и анионов, органолептических и общих химических параметров содержит перечень основных тяжелых металлов и метталоидов. Перед покупкой системы водоподготовки рекомендуем провести исследование воды с данным перечнем загрязнителей. Ориентируясь на полученную информацию, Вы сможете подобрать оборудование водоочистки с эффективностью до 98%, а так же корректно его настроить. Если вода из Вашего источника имеет выраженный запах сероводорода (запах тухлых яиц), рекомендуем дополнительно проверить воду на содержание сероводорода.
- Точность определений
- Подходит для подбора водоочистного оборудования
- Подходит для колодцев и скважин
- Содержит перечень тяжелых металлов
- Позволяет оценить эффективность фильтрующей загрузки в фильтре и всей системы в целом
- Позволяет корректно и экономично настроить водоочистное оборудование
- Срок выполнения — 5-6 рабочих дней
Анализ «СанПиН» предназначен для исследования воды по максимальному перечню загрязнителей, вне зависимости от источника, и включает 61 параметр:
- органолептические: мутность, цветность, запах, привкус;
- общехимические: рН, жесткость, окисляемость перманганатная, минерализация, электропроводность, щелочность общая, щелочность свободная, сероводород, хлор общий, хлор остаточный свободный, нефтепродукты;
- катионы: железо, аммоний, марганец, калий, магний, кальций, алюминий, натрий, литий;
- анионы: фториды, хлориды, нитраты, нитриты, фосфаты, сульфаты, сульфиды, гидросульфиды, карбонаты, гидрокарбонаты;
- тяжелые металлы и металлоиды: барий, бериллий, бор, ванадий, молибден, кобальт, цинк, никель, хром, стронций, кадмий, мышьяк, медь, свинец, кремний, серебро, титан, ртуть;
- органические компаненты: АПАВ, фенол, формальдегид, бензол, толуол, о-ксилол, п-ксилол, м-ксилол, стирол.
Данное исследование рекомендуется тем, кто серьезно относится к выбору питьевой воды. Протокол анализа «Максимальный» позволяет со 100% уверенностью сделать вывод о пригодности воды для питья и приготовления пищи. Результаты исследования позволяют выбрать схему водоочиски, а также оценить эффективность уже установленного оборудования.
- Точность определений
- Подходит для подбора водоочистного оборудования
- Подходит для любых источников воды
- Позволяет оценить эффективность фильтрующей загрузки в фильтре и всей системы в целом
- Включает полный перечень тяжелых металлов
- Позволяет корректно и экономично настроить водоочистное оборудование
- Содержит полный перечень опасных органических веществ
- Срок выполнения — 5-6 рабочих дней
Помимо хичиеского анализа мы настоятельно рекомендуем провести микробиологическое исследование Вашей воды. Микробиологический анализ включает определение общего микробного числа (ОМЧ), общих колиформных и колиформных термотолерантных бактерий.
Важен правильный отбор проб и оперативная доставка образцов в лабораторию или пункт приема проб. Подробная информация здесь
Если у Вас есть точный перечень параметров, Вы можете заказать анализ по Индивидуальному перечню показателей. Минимальный чек на индивидуальный анализ — 1 500 руб! Для расчета стоимости позвоните нам по номеру +7 (495) 149-23-57 или напишите на почту info@ion-lab.ru.
Анализ «Водоем / Аквариум» включает в себя перечень параметров, превышения по которым чаще всего встречаются в водоемах. Анализ включает определение основных химических параметров.
Химические параметры:
- общехимические : рН, нефтепродукты, аммоний, ХПК, БПК5, АПАВ, фенол;
- анионы : нитраты, сульфаты, хлориды, нитриты, фосфаты, фториды;
- тяжелые металлы и металлоиды : марганец, железо общее, ртуть, цинк, никель, кадмий, мышьяк, медь, свинец, хром.
Нормирование осуществляется по №552 Минсельхоза РФ от 13.12.2016 г «Об утверждении нормативов качества воды водных объектов рыбохозяйственного значения, в том числе нормативов предельно допустимых концентраций вредных веществ в водах водных объектов рыбохозяйственного значения.»
источник
РД 52.24.405-2005 Массовая концентрация сульфатов в водах. Методика выполнения измерений турбидиметрическим методом
Федеральная служба по гидрометеорологии и мониторингу окружающей среды
МАССОВАЯ КОНЦЕНТРАЦИЯ СУЛЬФАТОВ В ВОДАХ.
МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ
ТУРБИДИМЕТРИЧЕСКИМ МЕТОДОМ
1. РАЗРАБОТАН ГУ «Гидрохимический институт»
2. РАЗРАБОТЧИКИ Л.В. Боева, канд. хим. наук, А.А. Назарова, канд. хим. наук, Т.С. Евдокимова
3. УТВЕРЖДЕН Заместителем Руководителя Росгидромета.
4. СВИДЕТЕЛЬСТВО ОБ АТТЕСТАЦИИ МВИ Выдано ГУ «Гидрохимический институт» 30.12.2004 г № 57.24-2004
5. ЗАРЕГИСТРИРОВАН ГУ ЦКБ ГМП за номером РД 52.24.405—2005 от 30.06.2005 г.
6. ВЗАМЕН РД 52.24.405-95 «Методические указания. Методика выполнения измерений массовой концентрации сульфатов в водах турбидиметрическим методом»
Сульфат-ионы являются важнейшим компонентом химического состава поверхностных вод. В маломинерализованных водах сульфаты находятся преимущественно в ионной форме. При увеличении минерализации они склонны к образованию ассоциированных нейтральных ионных пар типа CaSO 4 , MgSO 4 .
В поверхностные воды сульфаты поступают главным образом за счет процессов химического выветривания и растворения серосодержащих минералов, в основном гипса и ангидрита, а также окисления сульфидных минералов и серы. Значительные количества сульфатов поступают в водные объекты в процессе отмирания организмов и окисления веществ растительного и животного происхождения, а также с промышленными и бытовыми сточными водами.
Содержание сульфатов в незагрязненных речных водах и водах пресных озер зависит от их географического расположения и обычно находится в пределах от 5 до 500 мг/дм 3 , в дождевых водах — от 1 до 10 мг/дм 3 . В подземных водах содержание сульфатов нередко достигает значительно более высоких величин. В целом же оно ограничивается сравнительно малой растворимостью сульфата кальция (произведение растворимости 6,1 · 10 -5 ). Внутригодовые изменения концентрации сульфатов в поверхностных водах суши связаны, в основном, с особенностями гидрологического режима водного объекта.
Повышенное содержание сульфатов ухудшает органолептические свойства воды. Жесткие требования в отношении концентрации сульфатов предъявляются и к воде, питающей паросиловые установки, поскольку в присутствии кальция сульфаты образуют прочную накипь.
ПДК сульфатов для водных объектов хозяйственно-питьевого и культурно-бытового водопользования составляет 500 мг/дм 3 , рыбохозяйственного назначения — 100 мг/дм 3 .
МАССОВАЯ КОНЦЕНТРАЦИЯ СУЛЬФАТОВ В ВОДАХ. МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ ТУРБИДИМЕТРИЧЕСКИМ МЕТОДОМ
Настоящий руководящий документ устанавливает методику выполнения измерений (далее — методика) массовой концентрации сульфатов в пробах поверхностных вод суши и очищенных сточных вод в диапазоне от 2 до 40 мг/дм 3 турбидиметрическим методом. При анализе проб воды с массовой концентрацией сульфатов, превышающей 40 мг/дм 3 допускается выполнение измерений после соответствующего разбавления пробы бидистиллированной водой.
2.1. При соблюдении всех регламентируемых методикой условий проведения измерений характеристики погрешности результата измерения с вероятностью 0,95 не должны превышать значений, приведенных в таблице 1.
При выполнении измерений в пробах с массовой концентрацией сульфатов свыше 40 мг/дм 3 после соответствующего разбавления погрешность измерений не превышает величины Δ · n , где Δ — погрешность измерения концентрации сульфатов в разбавленной пробе; η — степень разбавления.
Предел обнаружения сульфатов турбидиметрическим методом равен 1 мг/дм 3 .
2.2. Значения показателя точности методики используют при:
— оформлении результатов измерений, выдаваемых лабораторией;
Таблица 1 — Диапазон измерений, значения характеристик погрешности и ее составляющих
Показатель повторяемости (среднеквадратическое отклонение повторяемости) s r, мг/дм 3
Показатель воспроизводимости (среднеквадратическое отклонение воспроизводимости) s R, мг/дм 3
Показатель правильности (границы систематической погрешности при вероятности Р = 0,95) ± D c, мг/дм 3
Показатель точности (границы погрешности при вероятности Р = 0,95) ± D , мг/дм 3
— оценке деятельности лабораторий на качество проведения измерений;
— оценке возможности использования результатов измерений при реализации методики в конкретной лаборатории.
3.1.1. Фотометр или спектрофотометр любого типа (КФК-3, КФК-2, СФ-46, СФ-56 и др.)
3.1.2. Весы аналитические 2 класса точности по ГОСТ 24104-2001.
3.1.3. Весы технические лабораторные 4 класса точности по ГОСТ 24104-2001 с пределом взвешивания 200 г.
3.1.4. Государственный стандартный образец состава водных растворов сульфат-ионов ГСО 7480-98.
3.1.5. Колбы мерные не ниже 2 класса точности по ГОСТ 1770-74 вместимостью:
3.1.6. Пипетки градуированные не ниже 2 класса точности по ГОСТ 29227-91 вместимостью: 1 см — 1 шт.
3.1.7. Пипетки с одной отметкой не ниже 2 класса точности по ГОСТ 29169-91 вместимостью: 5 см 3 — 1 шт.
3.1.8. Цилиндры мерные по ГОСТ 1770-74 вместимостью:
3.1.9. Колбы конические по ГОСТ 25336-82 вместимостью
3.1.10. Колба коническая термостойкая по ГОСТ 25336-82 вместимостью
3.1.11. Стакан химический по ГОСТ 25336-82 вместимостью 500 см 3 — 1 шт.
3.1.12. Стаканчик для взвешивания (бюкс) по ГОСТ 25336-82 — 1 шт.
3.1.13. Капельница с колпачком по ГОСТ 25336-82 — 1 шт.
3.1.14. Воронка лабораторная по ГОСТ 25336-82 диаметром
3.1.15. Колонка хроматографическая диаметром 1,5 — 2,0 и длиной 25 — 30 см
3.1.16. Часовое стекло диаметром 6 — 7 см — 1 шт.
3.1.17. Палочка стеклянная — 1 шт.
3.1.19. Шкаф сушильный общелабораторного назначения
3.1.20. Плитка электрическая по ГОСТ 14919-83.
3.1.21. Устройство для фильтрования проб с использованием мембранных или бумажных фильтров.
Допускается использование других типов средств измерений, посуды и вспомогательного оборудования, в том числе импортных, с характеристиками не хуже, чем у приведенных в 3.1.
3.2.1. Калий сернокислый (сульфат калия) по ГОСТ 4145-74, х. ч.
3.2.2. Барий хлорид 2-водный (хлорид бария) по ГОСТ 4108-72, ч. д. а.
3.2.3. Кислота соляная по ГОСТ 3118-77, ч. д. а.
3.2.4. Натрия гидроокись (натрия гидроксид) по ГОСТ 4328-77, ч. д. а.
3.2.5. Этиленгликоль по ГОСТ 10164-75, ч. д. а. (допускается ч.) или глицерин по ГОСТ 6259-75, ч. д. а.
3.2.7. Вода дистиллированная по ГОСТ 6709-72, вода бидистиллированная.
3.2.8. Универсальная индикаторная бумага (рН 1 — 10) по ТУ 6-09-1181-76.
3.2.10. Хлорид кальция безводный гранулированный по ТУ 6-09-4711-81, ч. (для эксикатора).
3.2.11. Фильтры мембранные «Владипор МФАС-ОС-2», 0,45 мкм, по ТУ 6-55-221-1-29-89 или другого типа, равноценные по характеристикам, или фильтры бумажные обеззоленные «синяя лента» по ТУ 6-09-1678-86.
Допускается использование реактивов, изготовленных по другой нормативно-технической документации, в том числе импортных, с квалификацией не ниже указанной в 3.2.
Определение сульфатов турбидиметрическим методом основано на измерении интенсивности помутнения растворов, содержащих сульфаты, при добавлении хлорида бария в кислой среде. Для стабилизации суспензии BaS О4 в реакционную смесь вводят этиленгликоль или глицерин, а для понижения растворимости сульфата бария — этиловый спирт.
Оптическую плотность растворов измеряют при 315 нм.
5.1. При выполнении измерений массовой концентрации сульфатов в пробах природных и очищенных сточных вод соблюдают требования безопасности, установленные в государственных стандартах и соответствующих нормативных документах.
5.2. По степени воздействия на организм вредные вещества, используемые при выполнении измерений, относятся ко 2, 3 классам опасности по ГОСТ 12.1.007-76.
5.3. Содержание используемых вредных веществ в воздухе рабочей зоны не должно превышать установленных предельно допустимых концентраций в соответствии с ГОСТ 12.1.005-88.
5.4. Вредно действующие вещества подлежат сбору и утилизации в соответствии с установленными правилами.
5.5. Дополнительных требований по экологической безопасности не предъявляется.
К выполнению измерений и обработке их результатов допускаются лица со средним профессиональным образованием или без профессионального образования, но имеющие стаж работы в лаборатории нe менее года, освоившие методику.
При выполнении измерений в лаборатории должны быть соблюдены следующие условия:
температура воздуха (22 ± 5) ° C ;
атмосферное давление от 84,0 до 106,7 кПа (от 630 до 800 мм рт. ст.);
влажность воздуха не более 80 % при 25 °C ;
напряжение в сети (220 ± 10) В;
частота переменного тока (50 ± 1) Гц.
Отбор и хранение проб производят в соответствии с ГОСТ 17.1.5.05-85 и ГОСТ Р 51592-2000. Оборудование для отбора проб должно соответствовать ГОСТ 17.1.5.04-81 и ГОСТ Р 51592-2000. Пробы фильтруют через мембранный фильтр 0,45 мкм, промытый дистиллированной водой. Допустимо использование промытых дистиллированной водой бумажных фильтров «синяя лента». При фильтровании через любой фильтр первые порции фильтрата следует отбросить.
Пробы хранят в полипропиленовой (полиэтиленовой) или стеклянной посуде при температуре 3 — 4 °C. Анализ проб сточных и загрязненных природных вод рекомендуется выполнять в течение 7 дней после отбора. Если в воде присутствуют заметные количества других соединений минеральной или органической серы, определение необходимо выполнять не позднее суток после отбора проб.
9.1. Приготовление растворов и реактивов
9.1.1. Раствор соляной кислоты (1:1)
50 см 3 концентрированной соляной кислоты смешивают с 50 см 3 бидистиллированной воды. Раствор устойчив.
9.1.2. Раствор хлорида бария, 5 %
6,2 г хлорида бария (ВаСl 2 · 2H 2 О) растворяют в 100 см 3 бидистиллированной воды.
Смешивают 50 см 3 5 %-ного раствора хлорида бария с 150 см 3 этиленгликоля или глицерина и 150 см 3 этилового спирта (или другие объемы, кратные указанным) в конической колбе вместимостью 500 см 3 . Доводят величину pH раствора приблизительно до 3 по универсальной индикаторной бумаге раствором соляной кислоты 1:1 и оставляют на 2 — 3 сут. в темном месте, накрыв колбу часовым стеклом. После отстаивания раствор осадителя переносят в темную склянку с притертой стеклянной или полипропиленовой пробкой. Если при отстаивании на дне колбы образовался осадок, перенос осадителя в склянку следует проводить осторожно, так чтобы осадок остался в колбе. Раствор осадителя пригоден в течение 1 — 1,5 месяца. Показателем непригодности осадителя являются неудовлетворительные результаты контроля стабильности градуировочной зависимости с использованием градуировочного образца с концентрацией 40 мг/дм 3 (9.4).
9.1.4. Раствор соляной кислоты 4 моль/дм 3
170 см 3 концентрированной соляной кислоты растворяют в 330 см 3 дистиллированной воды.
9.1.5. Раствора гидроксида натрия 1 моль/дм 3
20 г гидроксида натрия растворяют в 500 см 3 дистиллированной воды. Хранят в полиэтиленовой посуде.
9.1.6. Раствор гидроксида натрия, 0,4 %
2 г гидроксида натрия растворяют в 500 см 3 дистиллированной воды. Хранят в полиэтиленовой посуде.
Способ подготовки активного угля приведен в приложении А.
9.2. Приготовление градуировочного раствора
9.2.1. Градуировочный раствор готовят из стандартного образца (ГСО) с содержанием сульфатов 10 мг/см 3 .
Вскрывают ампулу и ее содержимое переносят в сухую чистую коническую пробирку. Отбирают 5 см 3 образца с помощью чистой сухой пипетки с одной отметкой и переносят в мерную колбу вместимостью 200 см 3 . Доводят объем в колбе до метки дистиллированной водой и перемешивают. Массовая концентрация сульфатов в градуировочном растворе составляет 0,250 мг/см 3 .
9.2.2. При отсутствии ГСО допускается использовать аттестованный раствор сульфата, приготовленный из соли сульфата калия. Методика приготовления аттестованного раствора приведена в приложении Б.
Для приготовления образцов для градуировки в мерные колбы вместимостью 50 см 3 с помощью градуированных пипеток вместимостью 1, 2, 5 и 10 см 3 вносят 0; 0,4; 0,8; 1,2; 1,6; 2,0; 3,0; 4,0; 5,0; 6,0 и 8,0 см 3 градуировочного раствора с массовой концентрацией сульфат-ионов 0,250 мг/см 3 .
Объемы растворов доводят до меток на колбах бидистиллированной водой и перемешивают. Массовая концентрация сульфатов в полученных образцах составит соответственно 0; 2,0; 4,0; 6,0; 8,0; 10,0; 15,0; 20,0; 25,0; 30,0; 40,0 мг/дм 3 .
По 5 см 3 каждого из приготовленных образцов вносят в две сухие конические колбы вместимостью 50 см 3 и добавляют по 1 капле раствора соляной кислоты 1:1. При непрерывном перемешивании приливают в каждую колбу 5 см 3 раствора осадителя и продолжают перемешивание содержимого еще 10 — 15 с. Через (40 ± 5) мин 2 — 3 раза измеряют оптическую плотность каждого из полученных растворов при длине волны 315 нм в кювете длиной 2 см. Среднее значение оптической плотности холостого опыта вычитают из усредненной оптической плотности растворов, содержащих сульфаты.
Градуировочные зависимости оптической плотности от концентрации сульфатов рассчитывают методом наименьших квадратов для диапазонов от 2 до 10 мг/дм 3 и от 10 до 40 мг/дм 3 . Градуировочные зависимости устанавливают при приготовлении нового раствора осадителя, а также при замене измерительного прибора.
9.4.1. Контроль стабильности градуировочной характеристики проводят каждый раз перед анализом серии проб. Средствами контроля являются образцы, используемые для установления градуировочной зависимости по 9.3 (не менее 3 для каждой градуировочной зависимости). Допускается проводить контроль стабильности одной градуировочной зависимости, если вторая зависимость не будет использована для расчета результатов анализа в данной серии проб. Градуировочная характеристика считается стабильной при выполнении следующих условий:
где X — результат контрольного измерения массовой концентрации сульфатов в образце, мг/дм 3 ;
С — приписанное значение массовой концентрации сульфатов в образце, мг/дм 3 ;
s R — показатель воспроизводимости для концентрации С, мг/дм 3 (таблица 1).
Если условие стабильности не выполняется для одного образца для градуировки, необходимо выполнить повторное измерение этого образца для исключения результата, содержащего грубую погрешность. При повторном невыполнении условия, выясняют причины нестабильности, устраняют их и повторяют измерение с использованием других образцов, предусмотренных методикой. Если градуировочная характеристика вновь не будет удовлетворять условию (1), устанавливают новую градуировочную зависимость.
9.4.2. При выполнении условия (1) учитывают знак разности между измеренными и приписанными значениями массовой концентрации сульфатов в образцах. Эта разность должна иметь как положительное, так и отрицательное значение, если же все значения имеют один знак, это говорит о наличии систематического отклонения. В таком случае требуется установить новую градуировочную зависимость.
10.1. Отбирают по 5,0 см 3 анализируемой воды в две сухие конические колбы вместимостью 50 см 3 , добавляют 1 каплю раствора соляной кислоты 1:1 и перемешивают. Через 1 — 2 мин при непрерывном перемешивании приливают в колбы по 5 см 3 раствора осадителя и продолжают перемешивание содержимого еще 10 — 15 с. Через (40 ± 5) мин измеряют оптическую плотность полученных растворов при длине волны 315 нм в кювете длиной 2 см относительно дистиллированной воды.
Если измеренное значение оптической плотности пробы превышает таковое для последней точки градуировочной зависимости, проводят повторное измерение после разбавления пробы. Для разбавления отбирают аликвоту от 5 до 25 см 3 исходной воды пипеткой с одной отметкой, помещают аликвоту в мерную колбу вместимостью 50 см 3 , доводят до метки бидистиллированной водой и перемешивают. Отбираемую для разбавления аликвоту следует выбирать таким образом, чтобы массовая концентрация сульфатов в пробе после разбавления находилась в пределах от 20 до 40 мг/дм 3 .
Одновременно выполняют два параллельных определения сульфатов в холостой пробе, используя 5 см 3 бидистиллированной воды.
10.2. Мешающее влияние взвешенных и коллоидных веществ устраняют предварительным фильтрованием пробы через мембранный фильтр с диаметром пор 0,45 мкм или бумажный фильтр «синяя лента».
10.3. Если анализируемая вода окрашена или опалесцирует (опалесценция или слабая муть может появиться при подкислении пробы), проводят измерение ее собственной оптической плотности, прибавив к 5 см 3 пробы 1 каплю раствора соляной кислоты 1:1 и 5 см 3 бидистиллированной воды.
Если оптическая плотность пробы, обусловленная ее окраской, превышает величину 0,2, для устранения влияния цветности воду пропускают через колонку с активным углем. Первую порцию воды, прошедшую через колонку (40 — 50 см 3 ), отбрасывают.
11.1. Вычисляют значение оптической плотности Ах, соответствующее концентрации сульфатов в пробе воды, по формуле
где А — значение оптической плотности анализируемой пробы воды с осадителем;
А1 — значение собственной оптической плотности проб;
А2 — среднее арифметическое значение оптической плотности холостой пробы.
11.2. По соответствующей градуировочной зависимости находят массовую концентрацию сульфатов в анализируемой пробе воды X согласно полученному значению оптической плотности Ах. Если измерение проводилось после разбавления пробы, то в полученный результат вводят соответствующую поправку.
11.3. Результат измерений в документах, предусматривающих его использование, представляют в виде:

где 
± D — границы характеристик погрешности результатов измерений для данной массовой концентрации сульфатов (таблица 1), мг/дм 3 .
Численные значения результата измерений должны оканчиваться цифрой того же разряда, что и значения характеристики погрешности.
11.4. Допустимо представлять результат в виде:

где ± D л — границы характеристик погрешности результатов измерений, установленные при реализации методики в лаборатории и обеспечиваемое контролем стабильности результатов измерений, мг/дм 3 .
Примечание — Допустимо характеристику погрешности результатов измерений при внедрении методики в лаборатории устанавливать на основе выражения D л = 0,84 · D с последующим уточнением по мере накопления информации в процессе контроля стабильности результатов измерений.
12.1. Контроль качества результатов измерений при реализации методики в лаборатории предусматривает:
— оперативный контроль исполнителем процедуры выполнения измерений (на основе оценки повторяемости, погрешности при реализации отдельно взятой контрольной процедуры);
— контроль стабильности результатов измерений (на основе контроля стабильности среднеквадратического отклонения повторяемости, среднеквадратического отклонения внутрилабораторной прецизионности, погрешности).
12.2.1. Контроль повторяемости осуществляют для каждого из результатов контрольных измерений, полученных в соответствии с методикой анализа. Для этого отобранную пробу воды делят на две части, и выполняют анализ в соответствии с разделом 10.
12.2.2. Результат контрольной процедуры r к , мг/дм 3 рассчитывают по формуле
где X 1 , X 2 — результаты контрольных измерений массовой концентрации определяемого компонента, мг/дм 3 .
12.2.3. Предел повторяемости r п , мг/дм 3 рассчитывают по формуле
где s r — показатель повторяемости методики, мг/дм 3 (таблица 1).
12.2.4. Результат контрольной процедуры должен удовлетворять условию
12.2.5. При несоблюдении условия (7) выполняют еще два измерения и сравнивают разницу между максимальным и минимальным результатами с нормативом контроля равным 3,6 s r . В случае повторного превышения предела повторяемости, поступают в соответствии с разделом 5 ГОСТ Р ИСО 5725-6-2002.
12.3. Алгоритм оперативного контроля процедуры выполнения измерений с использованием метода добавок
12.3.1. Контроль исполнителем процедуры выполнения измерений проводят путем сравнения результатов отдельно взятой контрольной процедуры Кк с нормативом контроля К.
12.3.2. Результат контрольной процедуры Кк рассчитывают по формуле

где 

С — величина добавки, мг/дм 3 .
12.3.3 Норматив контроля погрешности К рассчитывают по формуле

где 
D X — значение погрешности методики анализа соответствующее массовой концентрации сульфатов в рабочей пробе, мг/дм 3 .
12.3.4. Если результат контрольной процедуры удовлетворяет условию
процедуру анализа признают удовлетворительной.
При невыполнении условия (10) контрольную процедуру повторяют. При повторном невыполнении условия (10), выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
12.4. Периодичность оперативного контроля и процедуры контроля стабильности результатов выполнения измерений регламентируют в Руководстве по качеству лаборатории.
Расхождение между результатами измерений, полученными в двух лабораториях, не должно превышать предела воспроизводимости. При выполнении этого условия приемлемы оба результата измерений и в качестве окончательного может быть использовано их общее среднее значение. Значение предела воспроизводимости рассчитывают по формуле
При превышении предела воспроизводимости могут быть использованы методы оценки приемлемости результатов измерений согласно разделу 5 ГОСТ Р ИСО 5725-6-2002.
Примечание — Оценка приемлемости проводится при необходимости сравнения результатов измерений, полученных двумя лабораториями.
Порцию активного угля, достаточную для заполнения колонки, помещают в термостойкую коническую колбу, добавляют 100 — 150 см 3 раствора соляной кислоты 4 моль/дм 3 и кипятят 2 — 3 ч, накрыв колбу часовым стеклом. Если раствор кислоты окрашивается, повторяют операцию до т ex пор, пока он не останется бесцветным. Уголь отмывают дистиллированной водой до значения рН, соответствующего рН дистиллированной воды по универсальной индикаторной бумаге, добавляют 100 — 150 см 3 раствора гидроксида натрия 1 моль/дм 3 и выдерживают 8 — 10 ч. Если появляется окраска, операцию повторяют.
Очищенный уголь отмывают дистиллированной водой до нейтральной реакции по универсальной индикаторной бумаге, затем промывают бидистиллированной водой. Хранят в склянке с бидистиллированной водой.
После пропускания каждой пробы воды уголь в колонке регенерируют промыванием 0,4 %-ным раствором гидроксида натрия до исчезновения окраски последнего, затем дистиллированной до нейтральной реакции, после чего промывают бидистиллированной водой.
Методика
приготовления аттестованного раствора сульфат-ионов для установления градуировочных характеристик приборов и контроля точности измерений массовой концентрации сульфатов турбидиметрическим методом AP1-SО4 2-
Б.1. Назначение и область применения
Настоящая методика регламентирует процедуру приготовления аттестованного раствора сульфат-ионов, предназначенного для установления градуировочных зависимостей и контроля точности результатов измерений массовой концентрации сульфатов в природных и очищенных сточных водах турбидиметрическим методом.
Б.2. Метрологические характеристики
Б.2.1. Аттестованное значение массовой концентрации сульфат-ионов в аттестованном растворе составляет 0,250 мг/см 3 .
Б.2.2. Абсолютная величина погрешности аттестованного значения массовой концентрации сульфат-ионов в аттестованном растворе с вероятностью 0,95 не превышает 0,0025 мг/см 3 .
Б.3. Средства измерений, вспомогательные устройства, реактивы
Б.3.1. Весы аналитические не ниже 2 класса точности по ГОСТ 24104-2001.
Б.3.2. Шкаф сушильный общелабораторного назначения.
Б.3.3. Колба мерная не ниже 2 класса точности по ГОСТ 1770-74 вместимостью 500 см 3 .
Б.3.4. Стаканчик для взвешивания (бюкс) по ГОСТ 25336-82.
Б.3.5. Воронка лабораторная по ГОСТ 25336-82 диаметром 56 мм.
Б.3.8. Калий сернокислый (сульфат калия) по ГОСТ 4145-74. х. ч.
Б.3.9. Вода дистиллированная по ГОСТ 6709-72.
Б.4. Процедура приготовления аттестованного раствора сульфат-ионов
Для приготовления аттестованною раствора сульфат-ионов на аналитических весах взвешивают в бюксе с точностью до четвертого знака после запятой 0,227 г K 2 SO 4 предварительно высушенного в сушильном шкафу при 105 ° C в течение 1 ч. Количественно переносят навеску в мерную колбу вместимостью 500 см 3 , растворяют в дистиллированной воде, доводят объём раствора до метки и перемешивают.
Переносят раствор в склянку с хорошо притертой стеклянной или пластиковой пробкой.
Полученному раствору приписывают массовую концентрацию сульфат-ионов 0,250 мг/см 3 .
Б.5. Расчет метрологических характеристик аттестованного раствора
Аттестованное значение массовой концентрации сульфат-ионов C , мг/см 3 рассчитывают по формуле

где m — масса навески сульфата калия, г;
V — вместимость мерной колбы, см 3 .
Расчет предела возможных значений погрешности приготовления аттестованного раствора сульфат-ионов с массовой концентрацией 0,250 мг/см 3 выполняют по формуле

где C — приписанное раствору значение массовой концентрации сульфат-ионов, мг/см 3 ;
µ — массовая доля основного вещества (K 2 SO 4 ) в реактиве, приписанная реактиву квалификации «х. ч.»;
D µ — предельное значение возможного отклонения массовой доли основного вещества в реактиве от приписанного значения µ;
m — масса навески сульфата калия, г;
D m — предельная возможная погрешность взвешивания, равная 0,0002 г;
V — вместимость мерной колбы, равный 500 см 3 ;
D V — предельное значение возможного отклонения вместимости мерной колбы от номинального значения, равное 0,4 см 3 .
Значение величины погрешности приготовления аттестованного раствора равно:
Б.6. Требования безопасности
Необходимо соблюдать общие требования техники безопасности при работе в химических лабораториях.
Б.7. Требования к квалификации операторов
Аттестованный раствор может готовить инженер или лаборант со средним специальным образованием, прошедший специальную подготовку и имеющий стаж работы в химической лаборатории не менее 6 мес.
Б.8. Требования к маркировке
На склянку с аттестованным раствором должна быть наклеена этикетка с указанием массовой концентрации сульфат-ионов, погрешности ее установления и даты приготовления.
Аттестованный раствор следует хранить в стеклянной склянке с притертой стеклянной или пластиковой пробкой при комнатной температуре не более 6 месяцев.
Федеральная служба по гидрометеорологии и мониторингу окружающей среды
ГОСУДАРСТВЕННОЕ УЧРЕЖДЕНИЕ «ГИДРОХИМИЧЕСКИЙ ИНСТИТУТ»
344090, г. Ростов-на-Дону пр. Стачки, 198
СВИДЕТЕЛЬСТВО № 57.24-2004
об аттестации методики выполнения измерений
Методика выполнения измерений массовой концентрации сульфатов в водах турбидиметрическим методом, разработанная ГУ «Гидрохимический институт» (ГУ ГХИ) и регламентированная P Д 52.24.405-2005 аттестована в соответствии с ГОСТ Р 8.563-96 с изменениями 2002 г.
Аттестация осуществлена по результатам экспериментальных исследований.
В результате аттестации установлено, что методика соответствует предъявляемым к ней метрологическим требованиям и обладает следующими основными метрологическими характеристиками:
1. Диапазон измерений, значения характеристик погрешности и ее составляющих (Р = 0,95)
Диапазон измерений массовой концентрации сульфатов X , мг/дм 3
Показатель повторяемости (среднеквадратическое отклонение повторяемости) s r,
Показатель воспроизводимости (среднеквадратическое отклонение воспроизводимости) s R, мг/дм 3
Показатель правильности (границы систематической погрешности при вероятности Р = 0,95) ± D c, мг/дм 3
Показатель точности (границы погрешности при вероятности Р = 0,95) ± D , мг/дм 3
источник