Главными источниками соединений железа в поверхностных водах являются процессы химического выветривания горных пород, сопровождающиеся их механическим разрушением и растворением. В процессе взаимодействия с содержащимися в природных водах минеральными и органическими веществами образуется сложный комплекс соединений железа, находящихся в воде в растворенном, коллоидном и взвешенном состояниях. Значительные количества железа поступают с подземным стоком и со сточными водами предприятий металлургической, металлообрабатывающей, текстильной, лакокрасочной промышленности и сельскохозяйственными стоками.
Фазовые равновесия зависят от химического состава вод, рН , Е h (окислительно-восстановительного потенциала) и в некоторой степени от температуры. В рутинном анализе во взвешенную форму выделяются частицы размером более 0,45 мкм. Она представлена преимущественно железосодержащими минералами, гидратом оксида железа и соединениями железа, сорбированными на взвесях. Истинно растворенную и коллоидную формы обычно рассматривают совместно. Растворенное железо представлено соединениями, находящимися в ионной форме в виде гидроксокомплексов и комплексов с растворенными неорганическими и органическими веществами природных вод. В ионной форме мигрируют главным образом Fe ( II ), а Fe ( III ) в отсутствие комплексообразующих веществ не может в значительных количествах находиться в растворенном состоянии.
Железо обнаруживается в основном в водах с низкими значениями Eh .
В результате химического и биохимического (при участии железобактерий) окисления Fe ( II ) переходит в Fe ( III ), которое, гидролизуясь , выпадает в осадок в виде Fe (ОН)3 Как для Fe ( II ), так и для Fe ( III ) характерна склонность к образованию гидрооксокомплексов типа [ Fe (ОН)2 ] + , [ Fe 2 (ОН)2 ] 4+ , [ Fe 2 (ОН)3 ] 3+ , [ Fe (ОН)3] — и других, сосуществующих в растворе в разных концентрациях в зависимости от рН и в целом определяющих состояние системы железо-гидроксил. Основной формой нахождения Fe ( III ) в поверхностных водах являются его комплексные соединения с растворенными неорганическими и органическими соединениями, главным образом гумусовыми веществами. При рН 8,0 основной формой является Fe (ОН)3. Коллоидная форма железа наименее изучена, она представляет гидрат оксида Fe (ОН)3 и комплексы с органическими веществами.
Содержание железа в поверхностных водах суши составляет десятые доли милиграмма в 1 дм 3 , вблизи болот – единицы миллиграммов в 1 дм 3 . Повышенное содержание железа наблюдается в болотных водах, в которых оно находится в виде комплексов с солями гуминовых кислот – гуматами . Наибольшие концентрации железа (до нескольких десятков и сотен миллиграммов в 1 дм 3 ) наблюдаются в подземных водах с низкими значениями рН .
Являясь биологически активным элементом, железо в определенной степени влияет на интенсивность развития фитопланктона и качественный состав микрофлоры в водоеме.
Концентрация железа подвержена заметным сезонным колебаниям. Обычно в водоемах с высокой биологической продуктивностью в период летней и зимней стагнации заметно увеличение концентрации железа в придонных слоях воды. Осенне-весеннее перемешивание водных масс ( гомотермия ) сопровождается окислением Fe ( II ) в Fe ( III ) и выпадением последнего в виде Fe ( OH )3.
Содержание железа в воде выше 1-2 мг Fe /дм 3 значительно ухудшает органолептические свойства, придавая ей неприятный вяжущий вкус, и делает воду малопригодной для использования в технических целях.
ПДК железа составляет 0,3 мг Fe /дм 3 (лимитирующий показатель вредности – органолептический), ПДК – 0,1 мг /дм 3 (лимитирующий показатель вредности – токсикологический).
Железо образует 2 рода растворимых солей, образующих катионы F е 2+ и F е 3+ , однако в растворе железо может находиться и во многих других формах, в частности:
1) в виде истинных растворов ( аквакомплексов ) [ F е( H 2 O )6] 2+ , содержащих железо ( II ). На воздухе железо ( II ) быстро окисляется до железа ( III ), растворы которого имеют бурую окраску из-за быстрого образования гидроксосоединений (сами растворы F е 2+ и F е 3+ практически бесцветны);
2) в виде коллоидных растворов из-за пептизации (распада агрегированных частиц) гидроксида железа под воздействием органических соединений;
3) в виде комплексных соединений с органическими и неорганическими лигандами . К ним относятся карбонилы , ареновые комплексы (с нефтепродуктами и др. углеводородами), гексацианоферраты [ F е( С H )6] 4- и др.
В нерастворимой форме железо может быть представлено в виде различных взвешенных в воде твердых минеральных частиц различного состава.
При рН >3,5 железо ( III ) существует в водном растворе только в виде комплекса, постепенно переходящего в гидроксид . При рН >8 железо ( II ) тоже существует в виде аквакомплекса , претерпевая окисление через стадию образования железа ( III ):
F е( II ) Þ F е(Ш) Þ F еО (ОН)•Н2О
В качестве примера сложных превращений железа в разных его формах, присутствующих иногда в природных водах, приведем уравнения реакций, протекающих в болотных водах и объясняющих часто встречающийся красный цвет воды (феномен «красных рек»). В условиях пониженного значения рН , характерного для болотных вод, протекают окислительные реакции с участием растворенного кислорода. В частности, встречающийся в природе практически нерастворимый в воде дисульфид железа (минерал пирит) окисляется до сульфата железа ( II ):
Далее, также под воздействием кислорода, протекает окисление сульфата железа ( II ):
4 F е 2+ +О 2 +4Н + =4 F е 3+ +2Н2О
Заключительной стадией процесса является реакция гидролиза, приводящая к образованию красно-бурого осадка гидроксида железа ( III ):
источник
Железо является характерным элементом природных вод зоны избыточного увлажнения. На территории этой природной зоны расположены города Центральной части России, Сибири и Дальнего Востока. В подземных водах Москвы и Московской области содержание железа превышает значение ПДК практически повсеместно.
Железо – один из самых распространенных элементов в природе. Его содержание в земной коре составляет около 4,7 % по массе, поэтому железо, с точки зрения его распространенности в природе, принято называть макроэлементом. Известно свыше 300 минералов, содержащих соединения железа. Среди них – магнитный железняк альфа FеО(ОН), бурый железняк Fе3О4*Н2О, гематит (красный железняк) и другие. Главными источниками соединений железа в поверхностных водах являются процессы химического выветривания горных пород, сопровождающиеся их механическим разрушением и растворением. В процессе взаимодействия с содержащимися в природных водах минеральными и органическими веществами образуется сложный комплекс соединений железа, находящихся в воде в растворенном, коллоидном и взвешенном состояниях. Значительные количества железа поступают с подземным стоком и со сточными водами предприятий металлургической, металлообрабатывающей, текстильной, лакокрасочной промышленности и сельскохозяйственными стоками.
Железо является жизненно важным микроэлементом для животных и растений, то есть элементом, необходимым для жизнедеятельности живых организмов в малых количествах. В организме человека железо входит в состав важнейших в биологическом отношении органических соединений – гемоглобина крови и ряда ферментов. Около 70% железа, содержащегося в организме человека, входит в состав гемоглобина. Основным физиологическим назначением железа является участие в процессе кроветворения.
В природных водах вода может содержать железо в разных формах. Чаще всего встречается двух- и трех- валентное железо. Чистая, прозрачная вода, изливающаяся из скважины, постояв некоторое время на воздухе, буквально на глазах начинает мутнеть, приобретая характерную рыжевато-бурую окраску. Это происходит потому, что соединения двухвалентного железа, вступив в контакт с кислородом воздуха, окисляются и переходят в нерастворимую форму трехвалентного железа — осадок, называемый ржавчиной. Содержание железа в воде выше 1-2 мг Fe /дм 3 значительно ухудшает органолептические свойства, придавая ей неприятный вяжущий вкус, и делает воду малопригодной для использования даже в технических целях. ПДК железа составляет 0,3 мг Fe /дм 3 (лимитирующий показатель вредности – органолептический).
Ржавчина очень часто встречается в водопроводной воде. Одна из основных причин — устаревшие системы водоснабжения. Пройдя очистку на муниципальных водопроводных очистных сооружениях, вода обычно содержит небольшое количество железа, укладывающиеся в медицинские нормы, но проходя до конечного потребителя через многие километры труб распределительной водопроводной сети, она подвергается вторичному загрязнению, растворяя продукты коррозии стальных труб.
В результате на выходе мы вновь имеем «железистую» воду с желтоватым оттенком. Насыщенная соединениями железа вода имеет не только неприятный вид. Она портит запорную арматуру, оставляет ржавые подтеки на керамических поверхностях сантехники. Кроме того, медиками доказано, что вода с повышенным содержанием железа (свыше 0,3 мг/л) приводит к заболеваниям печени, увеличивает риск инфарктов, негативно влияет на репродуктивную функцию организма, а также служит причиной появления аллергических реакций.
Повышенное содержание железа в воде создает благоприятные условия для развития железобактерий, особенно в подогретой воде. Эти микроорганизмы образуют ветвящиеся колонии, которые осложняют работу гидротехнических сооружений. Продукты жизнедеятельности железобактерий являются канцерогенами. Железообрастания внутри труб – идеальная среда для развития кишечной палочки, гнилостных бактерий, различных других микроорганизмов. Все это ухудшает химические и бактериологические показатели воды.
В природных водах может присутствовать двухвалентное (закисное) или трехвалентное (окисное) железо. Наиболее часто в воде подземных источников железо встречается в виде бикарбоната закиси железа Fe(HCO3)2, то есть двууглекислого железа. Из подземных вод двухвалентное железо может быть устранено при помощи аэрации воды. Надо отметить, что двууглекислое железо в воде частично гидролизуется, теряя углекислоту. Гидрат закиси железа Fe(OH)2, соединяясь с кислородом, превращается в коллоидную гидроокись железа Fe(OH)3, которая при коагулировании переходит в окись железа Fe2O33H2O, выпадающую в виде бурых хлопьев. Поэтому после аэрации нужно пропускать воду через контактные резервуары и фильтры.
Если в воде содержится сернокислое железо FeSO4, то при аэрации такой воды ее обезжелезивание не достигается, так как при гидролизе растворенной соли железа образуется угольная кислота, понижающая рН воды до величины, меньшей 6,8, при которой гидролиз почти прекращается. Поэтому из воды СО2 удаляется путем ее предварительного известкования, после которого необходимы отстаивание и фильтрование воды.
Чтобы установить наиболее экономичный для данной воды способ обезжелезивания, надо произвести пробное удаление железа. Обезжелезивание воды для хозяйственно-питьевых нужд производят при содержании в исходной воде железа в количестве более 0,3 мг/л, при этом специальные установки предусматриваются только в тех случаях, когда железо не может быть удалено попутно при обработке воды на других очистных сооружениях.
Для того, чтобы решить, какой именно способ обезжелезнивания воды необходим именно вам, нужно понять, в каких формах железо представлено в вашей воде. Для этого рекомендуется обратиться к специалистам-аналитикам, а также профессионалам водоподготовки. Все эти вопросы находятся в компетенции лаборатории MSU LAB.
источник
Содержание железа в воде – распространенное явление. В большинстве своем оно приносит пользу организму, но не стоит безоглядно пользоваться водой, содержащей данную примесь.
Поведение железа в воде зависит от валентности и взаимодействий с другими соединениями.
Железо в воде может быть в нескольких видах:
- Трехвалентное – не растворяется, придает воде желтый оттенок и оседает в виде бурого осадка;
- Соединенное с молекулами органики – придает воде желтый цвет и не выпадает в осадок;
- Двухвалентное – хорошо растворяется и не окрашивает воду;
- Бактериальное – образует радужную пленку и желеобразные отложение в водопроводе.
Возникновение железа в питьевой воде обусловлено коррозией водопроводных труб и очистных сооружений, которые фильтруют воду перед подачей в дома и квартиры.
Появление железа в воде из скважины связано с процессами растворения горных пород, а также с подземными стоками промышленных предприятий и сельскохозяйственных производств.
Для нормального функционирования организма человеку нужно употреблять в сутки 1-2 мг железа, но накопленный избыток негативно отражается на здоровье и угрожает жизни.
Чрезмерное содержание данной примеси в воде вызывает коррозию металлов и сокращает срок эксплуатации водопроводной системы.
ПДК железа в воде составляет 0,3 мг на литр. Данное значение установлено санитарными нормами. В связи тем, что влияние железа на организм не до конца изучено, а потребление элемента в сутки зависит от массы тела человека, ВОЗ не устанавливает определенных границ.
Самым надежным способом определения содержания железа в воде будет лабораторный анализ.
К первичным признакам избытка железа относятся:
- Ржавый налет на дне металлической посуды;
- «Металлический» привкус воды;
- Ржавые потеки на сантехнике;
- Обесцвечивание белья после стирки.
Чтобы анализ воды на железо показал точный результат, необходимо правильно собрать исследуемый материал. Для начала необходимо слить воду в течении 10 минут и хорошо промыть тару в исходной воде без моющих средств. Затем набрать воду тонкой струей под самую крышку, выдавить воздух, плотно закрыть емкость и доставить в пункт приема проб.
Что делать, если в воде много железа? Правильнее всего будет установить фильтр. Очистка в воде железа с помощью фильтра происходит двумя способами:
- Ионный обмен – гранулированные ионные смолы заменяют железо натрием, используется для технологических целей;
- Использование сильных окислителей – с помощью гипохлорида натрия или марганцовки; требует тщательной дозировки; дорогостоящий метод, больше подходит для технологических целей;
- Аэрация – создание интенсивного воздухообмена искусственным путем, в результате чего вода насыщается кислородом, который окисляет железо;
- Осмос – самая эффективная система очистки от двухвалентного железа.
В лаборатории «ИОН» вы сможете провести анализ вашей воды, узнать все о ее состоянии и получить рекомендации по улучшению качества. Мы работаем более 20-ти лет, используя современное оборудование и качественные материалы. Наши сотрудники – профессионалы своего дела. Лаборатория проводит исследование питьевой, талой, морской, технологической, водоемной и других видов вод. Мы сотрудничаем с крупнейшими разработчиками аналитического оборудования и постоянно ищем новые методы диагностики веществ и материалов. Мы осуществляем пробы с материалов Москвы и московской области.
Марганец в воде – довольно распространенное явление. Это вещество представляет из себя легкорастворимый минерал, занимающий 14 место среди общего количества. Содержание марганца в воде способно как принести организму пользу, так и причинить вред.
Сероводород — это газ, имеющий характерный неприятный запах (запах тухлых яиц). Содержание данной примеси практически не меняет цвет воды, но придает ей сладковатый привкус. Воду с повышенным содержанием сероводорода нельзя употреблять в пищу.
* Бесплатный выезд для физических лиц в пределах МКАД при заказе на сумму более 5 000 ₽. Подробнее в разделе Доставка и оплата
© 1997-2019 — Лаборатория ИОН. Все права защищены.
Для химического анализа необходимо заполнить водой чистую пластиковую тару (оптимально 1,5 л). Использовать бутылки из-под сладких, газированных или ароматизированных напитков, а также солёной или минеральной воды недопустимо.
Если выбранный Вами анализ включает определение содержания нефтепродуктов, необходимо заполнить дополнительную стеклянную тару объемом 0,2 л.
Если выбранный Вами анализ включает определение содержания сероводорода, необходимо заполнить дополнительную стеклянную тару объемом 0,5 л (необходимо использовать консервант).
При отборе воды из проточного источника, непосредственно перед отбором необходимо пролить воду сильной струёй в течение 3-5 минут. Перед отбором проб ёмкости и крышки необходимо 3 раза промыть изнутри водой, подлежащей анализу. Использование моющих средств недопустимо. Наполнять тару необходимо тонкой струёй по стенке сосуда «под горлышко». Это снижает насыщение воды кислородом и предотвращает протекание реакций.
Для микробиологического анализа необходимо использовать стерильный контейнер для биоматериалов объемом 150-200 мл.
Перед взятием пробы необходимо протереть водопроводный кран спиртовой салфеткой, уделив особое внимание месту выхода воды.
При отборе воды из водопровода, скважины или колонки необходимо пролить воду сильной струёй в течение 3–5 минут.
При отборе воды из колодца с помощью ведра необходимо обдать ведро кипятком для дезинфекции. Отбор пробы через поливочные шланги и предметы, контактирующие с почвой, не допускается.
Для отбора пробы необходимо надеть перчатки и вскрыть упаковку стерильного контейнера. Не касаясь внутренней поверхности ёмкости, отобрать образец воды (2/3 объема контейнера) и закрыть крышкой.
Рекомендуем доставлять пробу сразу после отбора.
Если сразу после отбора нет возможности доставить пробу в лабораторию, допускается хранение образцов при температуре 2–10 °C в течение 1 суток.
Съезд на ул. Руставели, на первом светофоре поворот налево на ул. Яблочкова.
Через 300 м поворот направо на ул. Гончарова, через 500 м поворот налево (напротив дома №6), через 200 метров вы на месте — ул. Добролюбова, 21А, корпус А, 3-й подъезд (серая дверь, белый козырек из поликарбоната), помещение 14.
Поворот на ул. Руставели, на светофоре поворот направо на ул. Добролюбова, через 300м на светофоре поворот налево на ул. Гончарова, напротив дома №6 поворот направо, через 200 метров вы на месте — ул. Добролюбова, 21А, корпус А, 3-й подъезд (серая дверь, белый козырек из поликарбоната), помещение 14.
Двигаясь по ул. Милошенкова, поворачиваем на ул. Добролюбова
Через 150 метров поворот направо, за домом 21АкБ поворот налево, через 100-120 метров вы на месте — ул. Добролюбова, 21А, корпус А, 3-й подъезд (серая дверь, белый козырек из поликарбоната), помещение 14.
Ближайшее станция метро – Фонвизинская (600 м)
Последний вагон из центра. Выход в сторону улицы Фонвизина. Из стеклянный дверей направо. Перейти через пешеходный переход и идти через дворы в соответствии со схемой. Пункт назначения — ул. Добролюбова, 21А, корпус А, 3-й подъезд (серая дверь, белый козырек из поликарбоната), помещение 14.
Анализ «Минимальный» содержит минимальный и обязательный перечень загрязнителей, часто встречающихся в питьевой воде, и включает 16 показателей:
- органолептические: мутность, цветность, запах, привкус;
- общехимические: рН, жесткость, окисляемость перманганатная, минерализация, электропроводность, щелочность общая, щелочность свободная;
- катионы: железо, аммоний;
- анионы: нитраты, карбонат, гидрокарбонат.
Данный набор рекомендуется для исследования воды хозяйственно-бытового назначения. Анализ «Минимальный» не обладает достаточной информативностью для подбора системы водоочистки, так как не позволяет получить полную картину о безопасности воды. Если Вы планируете использовать воду в питьевых целях, рекомендуем обратить внимание на наборы, содержащие большее число параметров.
- Точность определения
- Подходит для воды, применяемой в хоз-бытовом назначении
- Срок выполнения — 3-4 рабочих дня
- Не подходит для воды, применяемой в питьевых целях
- Не подходит для корректного подбора/оценки работы фильтров
- Не включает определение тяжелых металлов
- Не включает определение органических загрязнителей
Анализ «Начальный» предназначен для выявления наиболее часто встречающихся вредных веществ в питьевой воде и включает 23 параметра:
- органолептические: мутность, цветность, запах, привкус;
- общехимические: рН, жесткость, окисляемость перманганатная, минерализация, электропроводность, щелочность общая, щелочность свободная;
- катионы: железо, аммоний, марганец, калий, магний, кальций;
- анионы: фториды, хлориды, нитраты, сульфаты, карбонаты, гидрокарбонаты.
Данный анализ рекомендуется для воды централизованных систем водоснабжения. По протоколу анализа «Начальный» также можно сделать вывод о корректности работы системы водоочистки. В перечень определяемых параметров входят органолептические показатели, общие химические показатели, а также содержание катионов и анионов.
- Точность определений
- Подходит для водопроводной воды
- Позволяет оценить эффективность работы системы водоочистки
- Позволяет корректно настроить водоочистное оборудование
- Срок выполнения — 5 рабочих дней
- Не включает определение тяжелых металлов
- Не включает определение органических загрязнителей
- Не подходит для полной проверки воды из колодца или скважины
Анализ «Расширенный» содержит перечень наиболее часто встречающихся загрязнителей воды, вне зависимости от источника, и включает 31 показатель:
- органолептические: мутность, цветность, запах, привкус;
- общехимические: рН, жесткость, окисляемость перманганатная, минерализация, электропроводность, щелочность общая, щелочность свободная;
- катионы: железо, аммоний, марганец, калий, магний, кальций, алюминий, натрий;
- анионы: фториды, хлориды, нитраты, сульфаты, карбонаты, гидрокарбонаты;
- тяжелые металлы и металлоиды: медь, мышьяк, свинец, кадмий, цинк, стронций.
Данный набор рекомендуется, в первую очередь, владельцам колодцев и скважин. Помимо катионов и анионов, органолептических и общих химических параметров содержит перечень основных тяжелых металлов и метталоидов. Перед покупкой системы водоподготовки рекомендуем провести исследование воды с данным перечнем загрязнителей. Ориентируясь на полученную информацию, Вы сможете подобрать оборудование водоочистки с эффективностью до 98%, а так же корректно его настроить. Если вода из Вашего источника имеет выраженный запах сероводорода (запах тухлых яиц), рекомендуем дополнительно проверить воду на содержание сероводорода.
- Точность определений
- Подходит для подбора водоочистного оборудования
- Подходит для колодцев и скважин
- Содержит перечень тяжелых металлов
- Позволяет оценить эффективность фильтрующей загрузки в фильтре и всей системы в целом
- Позволяет корректно и экономично настроить водоочистное оборудование
- Срок выполнения — 5-6 рабочих дней
Анализ «СанПиН» предназначен для исследования воды по максимальному перечню загрязнителей, вне зависимости от источника, и включает 61 параметр:
- органолептические: мутность, цветность, запах, привкус;
- общехимические: рН, жесткость, окисляемость перманганатная, минерализация, электропроводность, щелочность общая, щелочность свободная, сероводород, хлор общий, хлор остаточный свободный, нефтепродукты;
- катионы: железо, аммоний, марганец, калий, магний, кальций, алюминий, натрий, литий;
- анионы: фториды, хлориды, нитраты, нитриты, фосфаты, сульфаты, сульфиды, гидросульфиды, карбонаты, гидрокарбонаты;
- тяжелые металлы и металлоиды: барий, бериллий, бор, ванадий, молибден, кобальт, цинк, никель, хром, стронций, кадмий, мышьяк, медь, свинец, кремний, серебро, титан, ртуть;
- органические компаненты: АПАВ, фенол, формальдегид, бензол, толуол, о-ксилол, п-ксилол, м-ксилол, стирол.
Данное исследование рекомендуется тем, кто серьезно относится к выбору питьевой воды. Протокол анализа «Максимальный» позволяет со 100% уверенностью сделать вывод о пригодности воды для питья и приготовления пищи. Результаты исследования позволяют выбрать схему водоочиски, а также оценить эффективность уже установленного оборудования.
- Точность определений
- Подходит для подбора водоочистного оборудования
- Подходит для любых источников воды
- Позволяет оценить эффективность фильтрующей загрузки в фильтре и всей системы в целом
- Включает полный перечень тяжелых металлов
- Позволяет корректно и экономично настроить водоочистное оборудование
- Содержит полный перечень опасных органических веществ
- Срок выполнения — 5-6 рабочих дней
Помимо хичиеского анализа мы настоятельно рекомендуем провести микробиологическое исследование Вашей воды. Микробиологический анализ включает определение общего микробного числа (ОМЧ), общих колиформных и колиформных термотолерантных бактерий.
Важен правильный отбор проб и оперативная доставка образцов в лабораторию или пункт приема проб. Подробная информация здесь
Если у Вас есть точный перечень параметров, Вы можете заказать анализ по Индивидуальному перечню показателей. Минимальный чек на индивидуальный анализ — 1 500 руб! Для расчета стоимости позвоните нам по номеру +7 (495) 149-23-57 или напишите на почту info@ion-lab.ru.
Анализ «Водоем / Аквариум» включает в себя перечень параметров, превышения по которым чаще всего встречаются в водоемах. Анализ включает определение основных химических параметров.
Химические параметры:
- общехимические : рН, нефтепродукты, аммоний, ХПК, БПК5, АПАВ, фенол;
- анионы : нитраты, сульфаты, хлориды, нитриты, фосфаты, фториды;
- тяжелые металлы и металлоиды : марганец, железо общее, ртуть, цинк, никель, кадмий, мышьяк, медь, свинец, хром.
Нормирование осуществляется по №552 Минсельхоза РФ от 13.12.2016 г «Об утверждении нормативов качества воды водных объектов рыбохозяйственного значения, в том числе нормативов предельно допустимых концентраций вредных веществ в водах водных объектов рыбохозяйственного значения.»
источник
МАССОВАЯ КОНЦЕНТРАЦИЯ ЖЕЛЕЗА ОБЩЕГО В ВОДАХ.
МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ
ФОТОМЕТРИЧЕСКИМ МЕТОДОМ С 1,10-ФЕНАНТРОЛИНОМ
1 РАЗРАБОТАН ГУ «Гидрохимический институт»
2 РАЗРАБОТЧИКИ Л.В. Боева, канд. хим. наук, А.А. Назарова, канд. хим. наук, Т.С. Евдокимова
3 УТВЕРЖДЕН Заместителем Руководителя Росгидромета 27 марта 2006 г.
4 СВИДЕТЕЛЬСТВО ОБ АТТЕСТАЦИИ МВИ Выдано метрологической службой ГУ «Гидрохимический институт» 15.02.2006 № 4.24-2006.
5 ЗАРЕГИСТРИРОВАН ГУ ЦКБ ГМП за номером РД 52.24.358-2006 от 30.03.2006 г.
6 ВЗАМЕН РД 52.24.358-95 «Методические указания. Методика выполнения измерений массовой концентрации железа общего в водах фотометрическим методом с 1,10-фенантролином».
Железо является одним из самых распространенных элементов земной коры, что обусловливает его постоянное присутствие в природных водах. Наиболее распространенными природными минералами железа являются магнетит (магнитный железняк Fe 3 O 4 , гематит (красный железняк) FeO 3 , пирит (железный колчедан) Fe 2 S 3 .
Основным природным источником поступления железа в поверхностные воды являются процессы химического выветривания горных пород, сопровождающиеся их растворением. Значительная часть железа поступает также с подземным стоком.
Антропогенное загрязнение водных объектов соединениями железа обусловлено их выносом со сточными водами многих отраслей промышленности, прежде всего горнодобывающих, металлургических, химических предприятий.
Железо является одним из важнейших элементов, принимающих активное участие в биохимических процессах, протекающих в живых организмах. Недостаточное содержание железа в воде может быть лимитирующим фактором в развитии водной растительности. Этим объясняется то, что железо часто включают в группу биогенных элементов.
Соединения железа могут присутствовать в водах в двух степенях окисления — Fe(II) и Fe(III), которые представлены тремя миграционными формами — растворённой, коллоидной и взвешенной. Растворённое железо может находиться в ионной форме, в виде гидроксокомплексов типа [ Fe (OH )2] + ; [ Fe 2 (OH)2] 4+ ; [ Fe 2 (OH )3] + ; [ Fe 2 (OH )3] 3+ ; [ Fe (OH )3] и комплексных соединений с минеральными и органическими веществами вод (преимущественно в виде комплексов с гуминовыми и фульвокислотами).
На состав и формы нахождения соединений железа в водах оказывают существенное влияние такие факторы как величина pH и Eh , присутствие природных комплексообразователей (гуминовых и фульвокислот), содержание растворенного кислорода, сероводорода, диоксида углерода, а также наличие микроорганизмов, окисляющих и восстанавливающих железо.
Вследствие гидролиза ионы Fe(III) при pH > 3 превращаются в гидратированные нерастворимые оксиды железа, которые составляют значительную долю валового содержания железа в водах. Присутствие в водах гуминовых и фульвокислот за счет образования довольно прочных комплексов предотвращает в той или иной степени гидролиз Fe(III) и способствуют поддержанию его в растворенном состоянии. По этой причине в гумифицированных водах содержание растворенного железа как правило выше, чем в водах, где гумусовых веществ мало.
Для Fe (II) более характерной является ионная форма, однако существовать Fe (II) может только при низких значениях окислительно-восстановительного потенциала (при дефиците кислорода) и низких значениях рН. Восстановлению Fe (III) до Fe(II) способствует присутствие гуминовых, танниновых и фульвокислот.
Для обозначения суммарной концентрации всех растворенных форм железа в воде используют термин «железо общее». Термин «валовое содержание» или «валовая концентрация» используется, когда говорят о суммарном содержании в воде как растворенных, так и взвешенных форм железа.
В речных и озерных водах концентрация железа общего в большинстве случаев находится в пределах от 0,01 до 1,0 мг/дм 3 . Она подвержена заметным сезонным изменениям, обусловленным как участием этого металла в физико-химических и биологических процессах, активно протекающих в водной среде, так и гидрологическим режимом водного объекта. В болотных, кислых шахтных, грунтовых и термальных водах концентрации железа могут достигать нескольких десятков и даже сотен миллиграммов в кубическом дециметре.
Содержание железа общего в поверхностных водах нормируется. ПДК растворенного железа в воде водных объектов рыбохозяйственного назначения составляет 0,1 мг/дм 3 . В водных объектах хозяйственно-питьевого и культурно-бытового назначения нормируется валовое содержание железа, для них ПДК составляет 0,3 мг/дм 3 .
МАССОВАЯ КОНЦЕНТРАЦИЯ ЖЕЛЕЗА ОБЩЕГО В ВОДАХ.
МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ ФОТОМЕТРИЧЕСКИМ МЕТОДОМ С 1,10-ФЕНАНТРОЛИНОМ
1.1 Настоящий руководящий документ устанавливает методику выполнения измерений (далее — методика) массовой концентрации железа общего растворенного и железа валового в пробах природных и очищенных сточных вод в диапазоне от 0,02 до 4,00 мг/дм 3 фотометрическим методом.
При анализе проб воды с массовой концентрацией железа превышающей 4,00 мг/дм 3 , допускается выполнение измерений после соответствующего разбавления пробы дистиллированной водой.
1.2 Настоящий руководящий документ предназначен для использования в лабораториях, осуществляющих анализ природных и очищенных сточных вод.
В настоящем руководящем документе использованы ссылки на следующие государственные стандарты:
ГОСТ 12.1.005-88 ССБТ. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007-76 ССБТ. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 17.1.5.04-81 Охрана природы. Гидросфера. Приборы и устройства для отбора, первичной обработки и хранения проб природных вод. Общие технические условия
ГОСТ 17.1.5.05-85 Охрана природы. Гидросфера. Общие требования к отбору проб поверхностных и морских вод, льда и атмосферных осадков
ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
ГОСТ Р 51592-2000 Вода. Общие требования к отбору проб
МИ 2881-2004 Рекомендация. ГСИ. Методики количественного химического анализа. Процедуры проверки приемлемости результатов анализа.
Ссылки на остальные нормативные документы приведены в разделе 4.
3.1 При соблюдении всех регламентируемых методикой условий проведения измерений характеристики погрешности результата измерения с вероятностью 0,95 не должны превышать значений, приведенных в таблице 1 .
Таблица 1 — Диапазон измерений, значения характеристик погрешности и ее составляющих (Р = 0,95)
Показатель повторяемости (среднеквадратическое отклонение повторяемости) s r, мг/дм 3
Показатель воспроизводимости (среднеквадратическое отклонение воспроизводимости) s R , мг/дм 3
Показатель правильности (границы систематической погрешности при вероятности Р = 0,95) ± D c, мг/дм 3
Показатель точности (границы погрешности при вероятности Р = 0,95) ± D , мг/дм 3
При выполнении измерений в пробах с массовой концентрацией железа свыше 4,00 мг/дм 3 после соответствующего разбавления погрешность измерения не превышает величины D ´ η где D — погрешность измерения концентрации железа в разбавленной пробе; η — степень разбавления.
Предел обнаружения железа общего фотометрическим методом 0,01 мг/дм 3 .
3.2 Значения показателя точности методики используют при:
— оформлении результатов измерений, выдаваемых лабораторией;
— оценке деятельности лабораторий на качество проведения измерений;
— оценке возможности использования результатов измерений при реализации методики в конкретной лаборатории.
4.1 Средства измерений, вспомогательные устройства
При выполнении измерений применяют следующие средства измерений и другие технические средства:
4.1.1 Фотометр или спектрофотометр любого типа (КФК-3, КФК-2, СФ-46, СФ-56 и др.)
4.1.2 Весы лабораторные высокого ( II ) класса точности по ГОСТ 24104-2001 .
4.1.3 Весы лабораторные обычного ( IV ) класса точности по ГОСТ 29329-92 с наибольшим пределом взвешивания 200 г и 500 г.
4.1.4 Государственный стандартный образец состава раствора ионов железа ( III ) ГСО 7254-96.
4.1.5 Колбы мерные 2-го класса точности исполнения 2, 2а по ГОСТ 1770-74 вместимостью:
4.1.6 Пипетки градуированные 2-го класса точности исполнения 1, 2 по ГОСТ 29227-91 вместимостью:
4.1.7 Пипетки с одной отметкой 2-го класса точности исполнения 2 по ГОСТ 29169-91 вместимостью:
4.1.8 Цилиндры мерные исполнения 1, 3 по ГОСТ 1770-74 вместимостью:
4.1.9 Пробирка коническая (исполнения 1) по ГОСТ 1770-74 — 1 шт.
4.1.10 Стаканы, тип В, исполнения 1, ТХС по ГОСТ 25336-82 вместимостью:
4.1.11 Колбы конические плоскодонные КН или П, исполнения 2, ТС, по ГОСТ 25336-82 вместимостью 100 см 3 — 10 шт.
4.1.12 Стаканчик для взвешивания (бюкс) СВ-19/9 по ГОСТ 25336-82 — 1 шт.
4.1.13 Капельница с колпачком (исполнения 2) по ГОСТ 25336-82 — 1 шт.
4.1.14 Чашки выпаривательные 3 по ГОСТ 9147-80 вместимостью 100 см 3 — 6 шт.
4.1.15 Воронки лабораторные по ГОСТ 25336-82 диаметром 56 мм — 6 шт.
4.1.16 Устройство для обработки проб воды УФ-облучением типа УФР с комплектом кварцевых пробирок вместимостью не менее 60 см 3
4.1.18 Посуда стеклянная для хранения растворов вместимостью 0,1; 0,25; 0,5 и 1,0 дм 3 .
4.1.19 Посуда полиэтиленовая (полипропиленовая) для отбора и хранения проб вместимостью 0,25 дм 3 .
4.1.21 Печь муфельная по ТУ 79 РСФСР 337-72.
4.1.22 Щипцы муфельные стальные никелированные или из цветного сплава.
4.1.23 Устройство для фильтрования проб с использованием мембранных фильтров.
4.1.24 Электроплитки с закрытой спиралью и регулируемой мощностью нагрева по ГОСТ 14919-83 .
Допускается использование других типов средств измерений, вспомогательных устройств, в том числе импортных, с характеристиками не хуже, чем у приведенных в 4.1.
При выполнении измерений применяют следующие реактивы и материалы:
4.2.1 1,10-фенантролин, моногидрат C 12 H 8 N 2 ´ H 2 O по ТУ 6-09-08-399-76, 1,10-фенантролина гидрохлорид C 12 H 8 N 2 ´ HCl ´ H 2 O или сульфат C 12 H 8 N 2 ´ H 2 SO 4 по ТУ 6-09-05-90-80.
4.2.2 Гидроксиламина гидрохлорид по ГОСТ 5456-79 , ч.д.а.
4.2.3 Аммиак водный, концентрированный по ГОСТ 3760-79 , ч.д.а.
4.2.4 Аммоний уксуснокислый (ацетат аммония) по ГОСТ 3117-78 , ч.д.а.
4.2.6 Кислота уксусная ледяная по ГОСТ 61-75 , х.ч.
4.2.8 Калий надсернокислый (персульфат калия) по ГОСТ 4146-74 , х.ч.
4.2.9 Фильтры мембранные «Владипор МФАС-ОС-2», 0,45 мкм, по ТУ 6-55-221-1-29-89 или другого типа, равноценные по характеристикам.
4.2.10 Фильтры бумажные обеззоленные «белая лента» по ТУ 6-09-1678-86.
4.2.11 Универсальная индикаторная бумага по ТУ 6-09-1181-76.
Допускается использование реактивов, изготовленных по другой нормативно-технической документации, в том числе импортных, с квалификацией не ниже указанной в 4.2.
Метод измерения основан на восстановлении Fe (III ) гидроксиламином до Fe (II) и взаимодействии последнего с 1,10-фенантролином в кислой среде (pH около 3) с образованием окрашенного в оранжево-красный цвет комплекса с максимумом в спектре поглощения при 510 нм. Для разрушения комплексов железа с органическими и неорганическими лигандами используют предварительную термическую обработку или облучение пробы ультрафиолетом.
При анализе пробы, отфильтрованной через мембранный фильтр, определяют содержание растворенного общего железа. Валовое содержание (сумму растворенных и взвешенных форм) определяют, анализируя тщательно перемешанную нефильтрованную пробу.
6.1 При выполнении измерений массовой концентрации железа в пробах природных и очищенных сточных вод соблюдают требования безопасности, установленные в национальных стандартах и соответствующих нормативных документах.
6.2 По степени воздействия на организм вредные вещества, используемые при выполнении измерений, относятся ко 2, 3 классам опасности по ГОСТ 12.1.007 .
6.3 Содержание используемых вредных веществ в воздухе рабочей зоны не должно превышать установленных предельно допустимых концентраций в соответствии с ГОСТ 12.1.005 .
6.4 Вредно действующие вещества подлежат сбору и утилизации в соответствии с установленными правилами.
6.5 Дополнительных требований по экологической безопасности не предъявляется.
К выполнению измерений и обработке их результатов допускаются лица со средним профессиональным образованием или без профессионального образования, но имеющие стаж работы в лаборатории не менее 2 лет, освоившие методику.
При выполнении измерений в лаборатории должны быть соблюдены следующие условия:
температура окружающего воздуха (22 ± 5) °С;
атмосферное давление от 84,0 до 106,7 кПа (от 630 до 800 мм рт. ст.);
влажность воздуха не более 80 % при 25 °С;
напряжение в сети (220 ± 10) В;
частота переменного тока в сети питания (50 ± 1) Гц.
Отбор проб для определения железа общего производится в соответствии с ГОСТ 17.1.5.05 и ГОСТ Р 51592. Оборудование для отбора проб должно соответствовать ГОСТ 17.1.5.04 и ГОСТ Р 51592. Для определения растворенных форм железа общего пробу как можно быстрее после отбора (не позже 4 ч) фильтруют через мембранный фильтр 0,45 мкм, очищенный кипячением в течение 5 — 7 мин в 1 %-ном растворе соляной кислоты и двукратным кипячением в дистиллированной воде. Первые порции фильтрата отбрасывают. Пробу консервируют концентрированной соляной кислотой из расчета 2 см 3 на каждые 100 см 3 воды и проверяют pH с помощью универсальной индикаторной бумаги. Если pH будет больше 2, добавляют по каплям необходимое количество кислоты до достижения указанного значения pH. Пробы хранят до анализа в полиэтиленовой посуде не более 1 мес.
Для определения суммарного содержания в воде всех форм железа (валового железа) пробу не фильтруют, подкисляют соляной кислотой и хранят до анализа в полиэтиленовой посуде не более 1 мес.
10.1 Приготовление растворов и реактивов
К 1,00 г моногидрата фенантролина (C 12 H 8 N 2 ´ H 2 O), 1,18 г гидрохлорида (C 12 H 8 N 2 ´ HCl ´ H 2 O ) или 1,34 г сульфата фенантролина (C 12 H 8 N 2 ´ H 2 SO 4 ) приливают 250 см 3 дистиллированной воды, 1,0 см 3 концентрированной соляной кислоты, перемешивают до растворения. Хранят в холодильнике не более 3 мес.
10.1.2 Раствор гидрохлорида гидроксиламина, 10 %-ный
10 г гидрохлорида гидроксиламина ( NH 2 OH ´ HCl ) растворяют в 90 см 3 дистиллированной воды. Хранят в темной склянке в холодильнике не более 3 мес.
10.1.3 Аммонийно-ацетатный буферный раствор
Способ 1. Растворяют 250 г ацетата аммония в 250 см 3 дистиллированной воды и добавляют 700 см 3 ледяной уксусной кислоты.
Способ 2. 250 см 3 аммиака водного смешивают с 900 см 3 ледяной уксусной кислоты.
Хранят в склянке с плотной притертой пробкой не более 3 мес.
10.1.4 Раствор персульфата калия, 4 %-ный
2 г персульфата калия (K 2 S 2 O 8 ) вносят в колбу, в которую предварительно помещают 50 см 3 дистиллированной воды и 0,5 см 3 концентрированной серной кислоты, и перемешивают до растворения. Раствор хранят в темноте в склянке с притертой пробкой не более 2 недель.
10.1.5 Раствор соляной кислоты, 1 %-ный
5 см 3 соляной кислоты смешивают с 200 см 3 дистиллированной воды. Используют для очистки фильтров.
10.2 Приготовление градуировочных растворов
Градуировочные растворы готовят из стандартного образца (ГСО) с массовой концентрацией железа 1,00 мг/см 3 . Вскрывают ампулу и ее содержимое переносят в сухую чистую пробирку. Для приготовления градуировочного раствора № 1 отбирают 5 см 3 образца с помощью чистой сухой пипетки с одной отметкой вместимостью 5 см 3 и переносят в мерную колбу вместимостью 100 см 3 . Добавляют 1,0 см 3 концентрированной соляной кислоты, доводят объем в колбе до метки дистиллированной водой и перемешивают. Массовая концентрация железа в градуировочном растворе № 1 составит 50 мг/дм 3 (если концентрация железа в ГСО не равна точно 1,00 мг/см 3 , рассчитывают массовую концентрацию железа в градуировочном растворе № 1 в соответствии с концентрацией конкретного образца). Раствор хранят в плотно закрытой склянке в холодильнике не более 3 мес.
Для приготовления градуировочного раствора № 2 пипеткой с одной отметкой отбирают 10 см 3 градуировочного раствора № 1, помещают его в мерную колбу вместимостью 100 см 3 и доводят до метки дистиллированной водой. Массовая концентрация железа в градуировочном растворе № 2 составит 5,00 мг/дм 3 . Раствор хранят не более 10 дней.
10.3 Установление градуировочных зависимостей
10.3.1 Установление градуировочных зависимостей в диапазоне от 0,02 мг/дм 3 до 1,00 мг/дм 3
Для приготовления образцов для градуировки в мерные колбы вместимостью 50 см 3 градуированными пипетками вместимостью 1; 2 и 10 см 3 вносят 0; 0,2; 0,5; 1,0; 2,0; 4,0; 6,0; 10,0 см 3 градуировочного раствора № 2 с массовой концентрацией железа 5,00 мг/дм 3 , добавляют по 1 см 3 концентрированной соляной кислоты, доводят объём растворов до меток дистиллированной водой и тщательно перемешивают. Массовые концентрации железа в полученных образцах равны соответственно 0; 0,020; 0,050; 0,100; 0,200; 0,400; 0,600; 1,00 мг/дм 3 . Далее выполняют обработку полученных образцов, как описано в 11.1 — 11.3. Оптическую плотность измеряют в кюветах с толщиной поглощающего слоя 5 см относительно дистиллированной воды. Оптическую плотность холостого опыта вычитают из оптической плотности образцов, содержащих раствор железа.
Градуировочные зависимости оптической плотности образцов от массовой концентрации железа рассчитывают методом наименьших квадратов.
Градуировочные зависимости устанавливают один раз в год, а также при замене измерительного прибора.
10.3.2 Установление градуировочных зависимостей в диапазоне от 1,00 мг/дм 3 до 4,00 мг/дм 3
Для приготовления образцов для градуировки в мерные колбы вместимостью 50 см 3 градуированной пипеткой вместимостью 5 см 3 вносят 0; 1,0; 1,5; 2,0; 2,5; 3,0; 4,0 см 3 градуировочного раствора № 1 с массовой концентрацией железа 50,0 мг/дм 3 , добавляют по 1 см 3 концентрированной соляной кислоты, доводят объём растворов до меток дистиллированной водой и тщательно перемешивают. Массовые концентрации железа в полученных образцах равны соответственно 0; 1,00; 1,50; 2,00; 2,50; 3,00; 4,00 мг/дм 3 . Далее выполняют обработку полученных образцов, как описано в 11.1 — 11.3. Оптическую плотность измеряют в кюветах с толщиной поглощающего слоя 2 см относительно дистиллированной воды. Оптическую плотность холостого опыта вычитают из оптической плотности образцов, содержащих раствор железа.
Градуировочные зависимости оптической плотности образцов от массовой концентрации железа рассчитывают методом наименьших квадратов.
Градуировочные зависимости устанавливают один раз в год, а также при замене измерительного прибора.
10.4 . Контроль стабильности градуировочной характеристики
10.4.1 Контроль стабильности градуировочной характеристики проводят при использовании новых партий реактивов, но не реже одного раза в квартал. Средствами контроля являются образцы, используемые для установления градуировочных зависимостей по 10.3 (не менее 3 образцов). Допускается проводить контроль стабильности одной градуировочной зависимости, если другие зависимости не используются для расчета результатов анализа проб воды.
Градуировочная характеристика считается стабильной при выполнении следующих условий:
где Х — результат контрольного измерения массовой концентрации железа в образце, мг/дм 3 ;
С — приписанное значение массовой концентрации железа в образце, мг/дм 3 ;
s r — показатель воспроизводимости для концентрации С, мг/дм 3 (таблица 1).
Если условие стабильности не выполняется для одного образца для градуировки, необходимо выполнить повторное измерение этого образца для исключения результата, содержащего грубую погрешность. При повторном невыполнении условия, выясняют причины нестабильности, устраняют их и повторяют измерение с использованием других образцов, предусмотренных методикой. Если градуировочная характеристика вновь не будет удовлетворять условию (1), устанавливают новую градуировочную зависимость.
10.4.2 При выполнении условия ( 1 ) учитывают знак разности между измеренными и приписанными значениями массовой концентрации железа в образцах. Эта разность должна иметь как положительное, так и отрицательное значение, если же все значения имеют один знак, это говорит о наличии систематического отклонения. В таком случае требуется установить новую градуировочную зависимость.
11.1 Выполнение измерений с разрушением органической матрицы кипячением
Отбирают пипеткой 50 см 3 законсервированной анализируемой воды (фильтрата при определении железа общего растворенного и тщательно перемешанной нефильтрованной пробы при определении железа валового) и помещают ее в коническую или плоскодонную колбу вместимостью 100 см 3 , добавляют 1 см 3 раствора гидрохлорида гидроксиламина и кипятят 15 — 20 мин для перехода всех соединений железа в ионное состояние. Объем пробы после кипячения не должен превышать 25 см 3 , в противном случае продолжают кипячение до достижения этого объема. После охлаждения добавляют концентрированный раствор аммиака до pH около 4 по универсальной индикаторной бумаге, переносят пробу в мерную колбу вместимостью 50 см 3 , приливают 3 см 3 буферного раствора, 1 см 3 раствора 1,10-фенантролина и доводят объем раствора до метки на колбе. Для каждой пробы выполняют два параллельных измерения.
Если для анализа брали нефильтрованную пробу, то при переносе в мерную колбу ее фильтруют через бумажный фильтр, предварительно промытый 20 — 25 см 3 1 %-ного раствора соляной кислоты.
Одновременно с серией анализируемых проб выполняют обработку двух холостых проб, используя 50 см 3 дистиллированной воды с добавкой 1 см 3 концентрированной соляной кислоты.
Через 20 мин измеряют оптическую плотность холостых и анализируемых проб по отношению к дистиллированной воде на спектрофотометре или фотометре с непрерывной разверткой спектра при длине волны 510 нм (на фотометре, снабженном светофильтрами — при 490 нм) в кювете с толщиной поглощающего слоя 5 или 2 см в зависимости от интенсивности окраски пробы.
Если оптическая плотность пробы выше таковой для последней точки градуировочной зависимости (4 мг/дм 3 ), повторяют измерение с меньшей аликвотой анализируемой воды. Объем аликвоты (от 1 до 25 см 3 ) выбирают таким образом, чтобы концентрация железа в разбавленной пробе находилась в диапазоне от 1 до 4 мг/дм 3 . К аликвоте добавляют необходимое количество соляной кислоты с таким расчетом, чтобы ее концентрация соответствовала концентрации в исходной пробе, и доводят объем аликвоты в мерной колбе дистиллированной водой до 50 см 3 .
11.2 Выполнение измерений с разрушением органической матрицы прокаливанием
Отбирают по 50 см 3 законсервированной анализируемой воды (или меньший объем, если концентрация железа в пробе превышает 5 мг/дм 3 ), помещают в две фарфоровые чашки и выпаривают на кипящей водяной бане. Чашки с сухим остатком помещают в муфельную печь и прокаливают при температуре от 400 °С до 450 °С в течение 2 ч. К прокаленному остатку добавляют пипеткой 2 см 3 раствора соляной кислоты 1:1, смачивая им стенки чашки, и оставляют на 10 мин, периодически перемешивая. Добавляют 10 см 3 дистиллированной воды, перемешивают и количественно переносят пробы в мерные колбы вместимостью 50 см 3 через воронку с бумажным фильтром, предварительно промытым 20 — 25 см 3 1 %-ного раствора соляной кислоты. Чашку и фильтр промывают дважды по 5 см 3 дистиллированной воды, помещая промывные воды в те же колбы.
К полученным растворам добавляют по 1 см 3 раствора гидрохлорида гидроксиламина, перемешивают и добавляют концентрированный раствор аммиака до pH около 4 по универсальной индикаторной бумаге. Приливают 3 см 3 буферного раствора, 1 см 3 раствора 1,10-фенантролина, доводят объем растворов до 50 см 3 и через 20 мин выполняют измерение оптической плотности, как описано в 11.1.
Одновременно с серией анализируемых проб выполняют обработку двух холостых проб, используя 50 см 3 дистиллированной воды с добавкой 1 см 3 концентрированной соляной кислоты.
11.3 Выполнение измерений с разрушением органической матрицы УФ-облучением
Для разрушения органической матрицы УФ-облучением по 50 см 3 законсервированной отфильтрованной анализируемой воды (для выполнения измерений содержания валового железа использовать данный способ не рекомендуется) или меньшие аликвоты, доведенные до 50 см 3 дистиллированной водой, вносят в две кварцевые пробирки, добавляют в каждую по 0,5 см 3 раствора персульфата калия, помещают пробы в устройство для обработки проб воды УФ-облучением и облучают 25 — 30 мин.
После облучения полностью переносят пробы в конические или плоскодонные колбы вместимостью 100 см 3 , добавляют 1 см 3 раствора гидрохлорида гидроксиламина и перемешивают. Затем добавляют концентрированный раствор аммиака до pH около 4 по универсальной индикаторной бумаге, приливают 3 см 3 буферного раствора, предварительно ополоснув им кварцевую пробирку, 1 см 3 раствора 1,10-фенантролина и через 20 мин выполняют измерение оптической плотности, как описано в 11.1.
Одновременно с серией анализируемых проб выполняют обработку двух холостых проб, используя 50 см 3 дистиллированной воды с добавкой 1 см 3 концентрированной соляной кислоты.
11.4 Устранение мешающих влияний
Выполнению измерений мешают сильные окислители, цианиды, нитриты, полифосфаты, цинк при концентрациях в 10 и более раз превышающих содержание железа, кобальт и медь в концентрациях свыше 5 мг/дм 3 , никель — свыше 2 мг/дм 3 (что маловероятно для поверхностных вод суши), взвешенные и окрашенные вещества.
Мешающее влияние окислителей, цианидов, нитритов и полифосфатов устраняется при выполнении операций, предусмотренных в ходе анализа (кипячение пробы с кислотой, добавление избытка гидроксиламина), металлов — добавлением избытка 1,10-фенантролина. При кипячении пробы происходит также разрушение минеральных и органических комплексов железа.
При анализе сильно окрашенных проб или проб, содержащих большие количества органических веществ, кипячение с кислотой не всегда обеспечивает полноту разрушения комплексов железа. В этом случае проводят разрушение органической матрицы пробы с помощью УФ-облучения (см. 11.3) или прокаливания (см. 11.2). Последний способ предпочтителен при анализе загрязненных поверхностных или сточных вод. Если проба после термической обработки или УФ-облучения (до добавления 1,10-фенантролина. ) имеет окраску или опалесцирует, следует учесть собственное поглощение пробы. Для этого проводят аналогичную обработку третьей аликвоты пробы, за исключением добавления раствора 1,10-фенантролина, измеряют ее оптическую плотность и вычитают ее из оптической плотности проб, в которые добавлен 1,10-фенантролин.
Мешающее влияние взвешенных и коллоидных веществ устраняют фильтрованием пробы.
12.1 По соответствующей градуировочной зависимости находят массовую концентрацию ионов железа, отвечающую полученному значению оптической плотности.
Массовую концентрацию железа общего или железа валового X , мг/дм 3 , в анализируемой воде рассчитывают по формуле
где С — массовая концентрация ионов железа, найденная по градуировочной зависимости, мг/дм 3 ;
V — объём аликвоты пробы, взятый для выполнения измерений, см 3 ;
1 ,02 — коэффициент, учитывающий разбавление пробы при консервации.
12.2 Массовую концентрацию взвешенных форм железа рассчитывают по разности между массовой концентрацией железа общего растворенного и железа валового.
12.3 Результат измерения массовой концентрации железа в документах, предусматривающих его использование, представляют в виде:
где 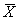
± D — границы характеристики погрешности измерения данной массовой концентрации железа общего, мг/дм 3 (таблица 1 ).
Численные значения результата измерения должны оканчиваться цифрой того же разряда, что и значения характеристики погрешности.
12.4 Допустимо представлять результат в виде
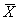
где ± D л — границы характеристик погрешности результатов измерений, установленные при реализации методики в лаборатории и обеспечиваемые контролем стабильности результатов измерений, мг/дм 3 .
Примечание — Допустимо характеристику погрешности результатов измерений при внедрении методики в лаборатории устанавливать на основе выражения D л = 0,84 ´ D с последующим уточнением по мере накопления информации в процессе контроля стабильности результатов измерений.
12.5 Результаты измерения оформляют протоколом или записью в журнале, по формам, приведенным в Руководстве по качеству лаборатории.
13.1.1 Контроль качества результатов измерений при реализации методики в лаборатории предусматривает:
— оперативный контроль исполнителем процедуры выполнения измерений (на основе оценки повторяемости, погрешности при реализации отдельно взятой контрольной процедуры);
— контроль стабильности результатов измерений (на основе контроля стабильности среднеквадратического отклонения повторяемости, среднеквадратического отклонения внутрилабораторной прецизионности, погрешности).
13.1.2 Периодичность оперативного контроля и процедуры контроля стабильности результатов выполнения измерений регламентируют в Руководстве по качеству лаборатории.
13.2 Алгоритм оперативного контроля повторяемости
13.2.1 Контроль повторяемости осуществляют для каждого из результатов измерений, полученных в соответствии с методикой. Для этого отобранную пробу воды делят на две части, и выполняют измерения в соответствии с разделом 11 .
13.2.2 Результат контрольной процедуры r к , мг/дм 3 , рассчитывают по формуле
где X 1 и Х2 — результаты измерений массовой концентрации железа в пробе воды, мг/дм 3 .
13.2.3 Предел повторяемости rn, мг/дм 3 , рассчитывают по формуле
где s r — показатель повторяемости, мг/дм 3 (таблица 1 ).
13.2.4 Результат контрольной процедуры должен удовлетворять условию
13.2.5 При несоблюдении условия ( 7 ) выполняют еще два измерения и сравнивают разницу между максимальным и минимальным результатами с нормативом контроля равным 3,6 ´ s r . В случае повторного превышения предела повторяемости, поступают в соответствии с разделом 5 ГОСТ Р ИСО 5725-6 .
13.3 Алгоритм оперативного контроля процедуры выполнения измерений с использованием метода добавок
13.3.1 Контроль исполнителем процедуры выполнения измерений проводят путем сравнения результатов отдельно взятой контрольной процедуры Кк с нормативом контроля К.
13.3.2 Результат контрольной процедуры Кк, мг/дм 3 , рассчитывают по формуле
Кк = | 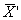
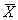
где 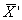
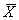
С — величина добавки, мг/дм 3 .
13.3.3 Норматив контроля погрешности К, мг/дм 3 , рассчитывают по формуле
где 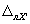
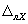
Примечание — Допустимо для расчета норматива контроля использовать значения характеристик погрешности, полученные расчетным путем по формулам 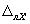
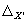
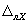
13.3.4 Если результат контрольной процедуры удовлетворяет условию
процедуру анализа признают удовлетворительной.
При невыполнении условия (10) контрольную процедуру повторяют. При повторном невыполнении условия (10), выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
Расхождение между результатами измерений, полученными в двух лабораториях, не должно превышать предела воспроизводимости R . При выполнении этого условия приемлемы оба результата измерений и в качестве окончательного может быть использовано их общее среднее значение. Значение предела воспроизводимости рассчитывают по формуле
При превышении предела воспроизводимости могут быть использованы методы оценки приемлемости результатов измерений согласно раздела 5 ГОСТ Р ИСО 5725-6 или МИ 2881.
Примечание — Проверка приемлемости проводится при необходимости сравнения результатов измерений, полученных двумя лабораториями.
Федеральная служба по гидрометеорологии и мониторингу окружающей среды
ГОСУДАРСТВЕННОЕ УЧРЕЖДЕНИЕ «ГИДРОХИМИЧЕСКИЙ ИНСТИТУТ»
об аттестации методики выполнения измерений
Методика выполнения измерений массовой концентрации железа общего в водах фотометрическим методом с 1,10-фенантролином.
разработанная ГУ «Гидрохимический институт» (ГУ ГХИ)
и регламентированная РД 52.24.358-2006
аттестована в соответствии с ГОСТ Р 8.563-96 с изменениями 2002 г.
Аттестация осуществлена по результатам экспериментальных исследований
В результате аттестации установлено, что методика соответствует предъявляемым к ней метрологическим требованиям и обладает следующими основными метрологическими характеристиками:
1 . Диапазон измеряемых концентраций, значения показателей точности и ее составляющих при доверительной вероятности Р = 0,95
Показатель повторяемости (среднеквадратическое отклонение повторяемости) s r, мг/дм 3
Показатель воспроизводимости (среднеквадратическое отклонение воспроизводимости) s R , мг/дм 3
Показатель правильности (границы систематической погрешности при вероятности Р = 0,95) ± D С, мг/дм 3
Показатель точности (границы погрешности при вероятности Р = 0,95) ± D , мг/дм 3
источник




