Настоящий документ устанавливает методику выполнения измерения массовой концентрации аммонийного азота (ионов аммония) в сточных водах в диапазоне содержаний от 0,15 до 120 мг/дм 3 (от 0,2 до 150 мг/дм 3 ).
Методика выполнения измерений обеспечивает с вероятностью P = 0,95 получение результатов измерений с погрешностью, не превышающей значений, приведенных в таблице 1.
Диапазон измерений массовой концентрации аммонийного азота (ионов аммония), C, мг/дм 3
Характеристика погрешности (границы интервала, в котором погрешность находится с заданной вероятностью),
± 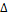
св. 60 до 120 (св. 80 до 150)
Примечание — Если определяемое содержание аммонийного азота выше установленного верхнего предела измерения, то допускается анализировать разбавленные пробы, проводя одновременно контроль точности результата измерения в соответствии с 12.2.
3.1 Метод измерения массовой концентрации ионов аммония и свободного аммиака заключается в образовании в щелочной среде с реактивом Несслера желтого соединения иодида меркураммония. При низких концентрациях аммиака это соединение находится в устойчивом коллоидном состоянии, пригодном для колориметрирования. При больших содержаниях аммиака выпадает бурый осадок — в этом случае определение необходимо проводить после разбавления пробы.
3.2 Определению мешают амины, хлорамины, альдегиды, спирты, фенолы, ацетон и другие органические соединения, реагирующие с реактивом Несслера. В их присутствии ионы аммония определяют после предварительной отгонки пробы.
Также определению мешают взвешенные вещества, мутность, компоненты, определяющие жесткость воды, железо, сульфиды и хлор.
Взвешенные вещества удаляют фильтрованием пробы.
Мешающее влияние жесткости воды устраняют добавлением 0,5 — 1,0 см 3 раствора трилона Б с массовой долей 50 % или такого же количества раствора калия-натрия виннокислого (Сегнетовой соли) с массовой долей 50 % на 50 см 3 пробы.
Мешающее влияние хлора устраняется добавлением раствора тиосульфата натрия с массовой концентрацией 3,5 г/дм 3 . Для удаления 0,5 мг хлора требуется 1 см 3 этого раствора.
Большое количество железа, сульфиды и муть удаляется добавлением раствора сульфата цинка. Для этого к 100 см 3 пробы добавляют 1 см 3 раствора сульфата цинка с массовой концентрацией 100 г/дм 3 , смесь тщательно перемешивают, доводят pH до 10,5 добавлением раствора гидроксида натрия или калия с массовой долей 25 %. После перемешивания и образования хлопьев осадок отфильтровывают через пористый фильтр (фильтр Шотта). Увеличение объема пробы необходимо учесть при расчете.
4.1.1 Спектрофотометр или фотоэлектроколориметр, обеспечивающие измерение оптической плотности в диапазоне длин волн от 425 нм до 440 нм, кюветы с толщиной оптического слоя 3 см.
4.1.2 Весы лабораторные общего назначения 2 класса точности с наибольшим пределом взвешивания 200 г по ГОСТ 24104-88.
4.1.3 pH-метр любой модели с пределом допускаемой погрешности до ±0,05 ед. pH.
4.1.4 Колбы мерные вместимостью 1000, 500, 200, 100 и 50 см 3 2 класса точности по ГОСТ 1770-74.
4.1.5 Пипетки градуированные вместимостью 1, 2, 10, 25, 50 см 3 2 класса точности по ГОСТ 29227-91.
4.1.6 Государственные стандартные образцы состава водных растворов ионов аммония ГСО 7015-93 ÷ 7017-93.
4.1.7 Цилиндры мерные вместимостью 500 см 3 по ГОСТ 1770-74.
4.2 Вспомогательные устройства
4.2.1 Колбы плоскодонные вместимостью 500 см 3 по ГОСТ 25336-82.
4.2.2 Воронки стеклянные для фильтрования по ГОСТ 25336-82.
4.2.3 Сушильный шкаф электрический общелабораторного назначения ОСТ 16.0.801.397-87.
4.2.4 Установка для обыкновенной перегонки или перегонки с водяным паром.
4.2.6 Колонка с катионитом КУ-2 или СБС.
4.2.8 Бумага индикаторная универсальная ТУ 6-09-1181-89.
4.2.9 Фильтры обеззоленные («белая» или «синяя» лента) ТУ 6-09-1678-86.
4.3.1 Аммоний хлористый ГОСТ 3773-72 (используется в случае отсутствия ГСО).
4.3.2 Реактив Несслера ТУ 6-09-2089-77.
4.3.3 Калий фосфорнокислый однозамещенный ГОСТ 4198-75.
4.3.4 Калий фосфорнокислый двузамещенный ГОСТ 2493-75.
4.3.6 Калия гидроксид ТУ 6-09-50-2322-77.
4.3.7 Натрий серноватистокислый ГОСТ 27068-86.
4.3.9 Калий-натрий виннокислый 4-х водный ГОСТ 5845-79.
4.3.11 Калий марганцевокислый ГОСТ 20490-75.
4.3.12 Натрий тетраборнокислый ГОСТ 4199-76.
4.3.13 Квасцы алюмокалиевые ГОСТ 4329-77.
Все используемые реактивы должны быть квалификации х.ч. или ч.д.а.
4.3.17 Вода дистиллированная по ГОСТ 6709-72.
5.1 При определении аммонийного азота в сточных водах необходимо соблюдать правила техники безопасности выполнения работы в химической лаборатории, включая общие правила безопасности работы с кислотами и щелочами.
5.2 Химик-аналитик, выполняющий анализ, должен быть проинструктирован о мерах предосторожности в соответствии с требованиями ГОСТ 12.0.004-90.
5.3 Правила электробезопасности при работе с электроустановками необходимо выполнять в соответствии с требованиями ГОСТ 12.1.019-79.
5.4 Помещение лаборатории должно соответствовать требованиям пожарной безопасности ГОСТ 12.1.004-91 и иметь средства пожаротушения в соответствии с требованиями ГОСТ 12.4.009-83.
Определение аммонийного азота в сточной воде может выполнять химик-аналитик, имеющий опыт работы в химической лаборатории не менее 2-х лет, освоивший данную методику выполнения измерения, и подтвердивший соответствие характеристик погрешности нормативам контроля точности по разделу 12.
Общие требования к отбору проб по ГОСТ Р 51592-2000 «Вода. Общие требования к отбору проб», или другой нормативной документации, утвержденной в установленном порядке.
Объем отбираемой пробы не менее 500 см 3 .
Анализ проводят в день отбора пробы. Если определение в день отбора не проводилось, пробу консервируют добавлением 1 см 3 концентрированной серной кислоты на 1 дм 3 пробы. Консервированная проба может храниться двое суток.
8.1 Спектрофотометр или фотоэлектроколориметр подготавливают к работе как указано в паспорте на прибор.
8.2 Приготовление растворов.
Безаммиачную воду готовят одним из двух способов:
1) дважды перегнанную воду пропускают через колонку с катионитом КУ-2 или СБС;
2) вторично перегоняют дистиллированную воду, предварительно подкислив серной кислотой и добавив марганцевокислый калий до чёткой малиновой окраски.
Полученную воду проверяют на наличие ионов аммония реактивом Несслера по ГОСТ 6709-72 и используют для приготовления реактивов и разбавления проб.
8.2.2 Основной градуировочный раствор с массовой концентрацией ионов аммония 1 мг/см 3 .
Основной раствор готовится из стандартного образца состава водных растворов ионов аммония согласно инструкции по применению ГСО. В случае отсутствия ГСО основной раствор готовится из хлористого аммония, подготовленного по ГОСТ 4212-76.
2,9650 г хлористого аммония растворяют в мерной колбе вместимостью 1000 см 3 в небольшом количестве безаммиачной воды, а затем доводят до метки безаммиачной водой. Раствор хранят в банке тёмного стекла в течение года.
8.2.3 Рабочий градуировочный раствор с массовой концентрацией ионов аммония 0,005 мг/см 3 .
1 см 3 основного раствора доводят до метки безаммиачной водой в мерной колбе вместимостью 200 см 3 . Применяется свежеприготовленным.
8.2.4 Боратный буферный раствор, pH = 9,5.
К 500 см 3 раствора тетраборнокислого натрия концентрации C (Na2B2O7) = 0,025 моль/дм 3 приливают 88 см 3 раствора гидроксида натрия концентрации C (NaOH) = 0,1 моль/дм 3 и разбавляют до 1 дм 3 безаммиачной водой.
8.2.5 Тетраборнокислый натрий, водный раствор концентрации C (Na2B2O7 ∙ 10 H2O) = 0,025 моль/дм 3 .
9,5 г 10-водного тетраборнокислого натрия растворяют в мерной колбе вместимостью 1000 см 3 безаммиачной водой.
8.2.6 Фосфатный буферный раствор, pH = 7,4.
В мерной колбе вместимостью 1000 см 3 растворяют 14,3 г безводного однозамещённого фосфорнокислого калия и 68,8 г безводного двузамещённого фосфорнокислого калия безаммиачной водой.
8.2.7 Цинк сернокислый, водный раствор с массовой концентрацией 100 г/дм 3 .
100 г сульфата цинка растворяют в безаммиачной воде в мерной колбе вместимостью 1000 см 3 .
8.2.8 Трилон Б, водный раствор с массовой концентрацией 500 г/дм 3 .
10 г гидроокиси натрия растворяют в 60 см 3 безаммиачной воды. К полученному раствору добавляют 50 г трилона Б и доводят до 100 см 3 .
8.2.9 Калий-натрий виннокислый, водный раствор, с массовой концентрацией 500 г/дм 3 .
Растворяют 50 г соли в безаммиачной воде, доводят объём той же водой до 100 см 3 . Полученный раствор кипятят до исчезновения реакции на аммиак. Затем охлаждают и доводят до 100 см 3 безаммиачной водой.
8.2.10 Натрий серноватистокислый, водный раствор, с массовой концентрацией 3,5 г/дм 3 .
3,5 г серноватистокислого натрия растворяют в безаммиачной воде и разбавляют такой же водой до 1 дм 3 .
8.2.11 Борная кислота, водный раствор, с массовой концентрацией 40 г/дм 3 .
Растворяют 40 г борной кислоты в безаммиачной воде и разбавляют такой же водой до 1 дм 3 .
8.2.12 Серная кислота, водный раствор концентрации C (1/2 H2SO4) = 1 моль/дм 3 (1 н).
27,3 см 3 серной кислоты, пл. 1,84 г/см 3 вносят небольшими порциями при перемешивании в 150 — 200 см 3 безаммиачной воды в мерную колбу вместимостью 1000 см 3 .
8.2.13 Гидроксид натрия, раствор с массовой долей 40 %.
40 г гидроксида натрия растворяют в 60 см 3 безаммиачной воды.
8.2.14 Гидроксид натрия, раствор с массовой долей 25 %.
25 г гидроксида натрия растворяют в 75 см 3 безаммиачной воды.
8.2.15 Гидроксид натрия, водный раствор концентрации C (NaOH) = 1 моль/дм 3 .
40 г гидроксида натрия растворяют в мерной колбе вместимостью 1000 см 3 в безаммиачной воде.
В ряд мерных колб вместимостью 50 см 3 вносят 1,0; 2,0; 3,0; 4,0; 6,0; 8,0; 10,0; 12,0 см 3 рабочего градуировочного раствора ионов аммония, разбавляя примерно до половины колбы безаммиачной водой, прибавляют 0,5 см 3 раствора калия-натрия виннокислого или трилона Б, перемешивают, затем добавляют 1 см 3 реактива Несслера, доводят до метки безаммиачной водой и снова перемешивают. Получают растворы с концентрациями ионов аммония 0,1; 0,2; 0,3; 0,4; 0,6; 0,8; 1,0; 1,2 мг/дм 3 , соответственно. Одновременно готовится холостая проба: в мерную колбу вместимостью 50 см 3 , наполовину заполненную безаммиачной водой, вносят 0,5 см 3 раствора калия-натрия виннокислого или трилона Б, 1 см 3 реактива Несслера, доводят до метки безаммиачной водой, перемешивают. Через 10 минут измеряют оптическую плотность полученных растворов в кювете с толщиной оптического слоя 3 см при выбранной длине волны из диапазона от 425 нм до 440 нм на спектрофотометре или фотоэлектроколориметре. В качестве раствора сравнения используется безаммиачная вода. Градуировочный график строят в координатах: оптическая плотность — массовая концентрация ионов аммония в фотометрируемой пробе.
Определение азота аммонийного в сточных водах производится одним из двух способов:
10.1 Определение без отгонки (при отсутствии мешающих примесей).
В мерную колбу вместимостью 50 см 3 помещают такое количество фильтрованной сточной воды, чтобы в ней содержалось не более 0,06 мг ионов аммония, приливают 0,5 см 3 раствора калия-натрия виннокислого или трилона Б, перемешивают, затем добавляют 1 см 3 реактива Несслера, доводят до метки безаммиачной водой и перемешивают. Одновременно готовят холостую пробу и поступают как в п. 9.
10.2 Определение с отгонкой (при наличии мешающих примесей).
Отгонку аммиака из воды, содержащей легко гидрализуемые органические соединения, проводят при pH = 7,4, добавляя к пробе фосфатный буферный раствор. В присутствии цианатов и большинства азотсодержащих органических соединений следует использовать боратный буферный раствор pH = 9,5. При необходимости анализа сточных вод предприятий, оборудующих в процессе производства фенолы (сбрасывающие фенол содержащие сточные воды), к пробе добавляют раствор гидроксида натрия с массовой долей 40 % до pH = 9,5. Если присутствуют вещества, гидролизующиеся в щелочной среде, то отгонку надо провести дважды: сначала при pH = 7,4, собирая отгон в разбавленный раствор серной кислоты, потом подщелочить этот отгон до сильнощелочной реакции и отогнать повторно, собирая отгон в раствор борной кислоты или безаммиачную воду.
Перегонку исследуемых проб проводят в комнате, воздух которой не содержит аммиака. Если проба содержит большое количество взвешенных веществ или нефтепродуктов, её предварительно фильтруют через фильтр «белая лента».
В колбу для отгона помещают 400 см 3 анализируемой пробы или отгона при pH = 7,4 или меньший объём, доведенный до 400 см 3 безаммиачной водой. В зависимости от предполагаемых загрязнений затем приливают 25 см 3 буферного раствора pH = 9,5 или 20 см 3 раствора гидроксида натрия с массовой долей 40 %. В приемник наливают 50 см 3 раствора борной кислоты и устанавливают объем жидкости так, чтобы конец холодильника был погружен в неё, добавляя при необходимости безаммиачную воду. Отгоняют примерно 300 см 3 жидкости, отгон количественно переносят в мерную колбу вместимостью 500 см 3 , добавляют водный раствор серной кислоты концентрации C (1/2 H2SO4) = 1 моль/дм 3 до pH = 6 и разбавляют до метки безаммиачной водой.
Отбирают аликвоту анализируемой пробы и далее поступают как в 10.1.
11.1 Расчёт массовой концентрации аммонийного азота, выраженной в мг/дм 3 , в исследуемой пробе воды проводят по формуле:
где: K — коэффициент градуировочного графика;
ΔD — оптическая плотность рабочей пробы за вычетом холостой пробы;
V1 — объём сточной воды, взятой для отгона, см 3 ;
V2 — объём дистиллята (отгона), см 3 ;
V3 — часть объёма дистиллята (отгона), взятая для анализа, см 3 ;
0,78 — коэффициент пересчета из концентрации по ионам аммония в концентрацию по аммонийному азоту.
где: CГ — массовая концентрация ионов аммония в i-той точке графика, мг/дм 3 ;
Dраб. — оптическая плотность на графике для этой точки;
Dхол. — оптическая плотность на графике для CГ = 0 мг/дм 3 .
При необходимости проверки приемлемости результатов измерений в условиях повторяемости (например, по требованию заказчика или в случае анализа сложных проб) получают два результата измерений массовой концентрации аммонийного азота (ионов аммония) в пробах сточных вод по разделу 10 в условиях повторяемости. Проверяют приемлемость результатов измерений с1 и с2, сравнивая расхождение между ними с пределом повторяемости r (см. таблицу 2). Если полученное значение расхождения не превышает предела повторяемости, то за результат измерений массовой концентрации аммонийного азота (ионов аммония) в пробе сточной воды принимают среднее из двух полученных значений с1 и с2. В противном случае процедуру повторяют.
11.2 Форма представления результатов измерений.
Результаты измерения массовой концентрации аммонийного азота в анализируемых пробах сточной воды в документах, предусматривающих их использование, представляют в виде:
12.1 Контроль стабильности результатов измерений
Контроль стабильности результатов измерений в лаборатории осуществляют по ГОСТ Р ИСО 5725-6, раздел 6, используя методы контроля стабильности стандартного отклонения промежуточной прецизионности и контроля стабильности правильности рутинного анализа. Средство контроля готовят из ГСО состава водных растворов аммонийного азота (ионов аммония) и дистиллированной воды и анализируют согласно разделу 10. При построении контрольных карт для расчета пределов действия и предупреждения используют значения стандартных отклонений промежуточной прецизионности при различиях по факторам «время», «оператор», «оборудование», приведенные в таблице 2.
Диапазон измерений массовой концентрации аммонийного азота, (ионов аммония), мг/дм 3
Предел повторяемости r , мг/дм 3
Стандартное отклонение промежуточной прецизионности (при различиях по факторам «время», «оператор», «оборудование»), σ1(Т,О,Е) мг/дм 3
св. 60 до 120 (св. 80 до 150)
При неудовлетворительных результатах контроля, например, превышение предела действия или регулярное превышение предела предупреждения, выясняют причины этих отклонений, в том числе повторяют градуировку прибора, проводят смену реактивов, проверяют работу оператора.
Периодичность проведения контроля стабильности результатов измерений устанавливают индивидуально для каждой лаборатории в соответствии с документами по внутрилабораторному контролю качества результатов анализа.
12.2 Оперативный контроль точности результатов измерений.
При внедрении методики в практику работы лаборатории проводят контроль точности результатов измерений массовой концентрации аммонийного азота (ионов аммония), используя метод добавок в пробы сточных вод, анализируемых в лаборатории. В качестве добавок используются растворы, приготовленные из ГСО состава водных растворов ионов аммония. Величина добавки рассчитывается таким образом, чтобы полученное после введения добавки значение массовой концентрации аммонийного азота (ионов аммония) в пробе (C) удовлетворяло условию:
где Cр — массовая концентрация аммонийного азота (ионов аммония) в пробе до введения добавки;
Cк — полученное после введения добавки значение массовой концентрации аммонийного азота (ионов аммония), мг/дм 3 .
Анализ пробы с добавкой производят в тех же условиях, что и исходной пробы.
Результаты контроля признаются удовлетворительными, если выполняется условие:
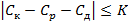
где Cд — действительное значение массовой концентрации аммонийного азота (ионов аммония) в добавке;
K — норматив оперативного контроля точности.
Значения норматива оперативного контроля точности рассчитываются по формуле:
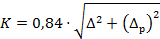
где Δ, Δр — значение характеристик погрешности, соответствующие массовой концентрации аммонийного азота (ионов аммония) в пробе с добавкой и пробе без добавки, приведенные в таблице 1.
При превышении норматива оперативного контроля точности эксперимент повторяют. В случае повторного превышения норматива K выясняют причины, приводящие к неудовлетворительным результатам контроля и решают вопрос о целесообразности использования внедряемой методики.
После внедрения МВИ в практику работы лаборатории при необходимости проверки приемлемости результатов измерений, полученных в условиях воспроизводимости, проводят межлабораторные сравнительные испытания с использованием данной методики для оценки стандартного отклонения воспроизводимости (см. приложение А). В случае невозможности организации межлабораторных сравнительных испытаний допускается, согласно МИ 2336-2002, оценить значение стандартного отклонения воспроизводимости, σR, по формуле: σR = 1,2 ∙ σ1(Т,О,Е). Проверку приемлемости результатов измерений в условиях воспроизводимости осуществляют по ГОСТ Р ИСО 5725-6-2002, пункт 5.3. Сопоставление альтернативных методов измерений проводят по ГОСТ Р ИСО 5725-6-2002, раздел 8.
Оценки стандартных отклонений повторяемости и воспроизводимости
В таблице А.1 представлены данные по результатам межлабораторных сравнительных испытаний (МСИ), проведенных Органом по аккредитации ЦИКВ среди аккредитованных лабораторий и обработанных в соответствии с п. 7.4 ГОСТ Р ИСО 5725-2-2002. Представленные данные не применимы для обобщений.
источник
Биогенный элемент, который активнейшим образом участвует в процессах биогидроценоза, — аммонийный азот.
В водоёмах можно наблюдать изменение содержания этого элемента: весной его становится меньше, зато летом, в связи с благоприятным температурным режимом, значительно увеличивается его концентрация, поскольку массированно разлагаются органические вещества.
И это кардинальным образом влияет на санитарное состояние водоёмов, что заставляет усиливать контроль за жизнеспособностью экосистемы. Предельно допустимой концентрацией в водоёмах, где ловят рыбу, считается та, где аммонийный азот не превышает 0,39 миллиграммов на литр.
Скопление белкового азота подвержено аммонификации, и этот процесс разлагает белки до аммонийного состояния. Сточные воды очищают при помощи этого источника азота, если в них имеется источник углеродного питания для клеток. Интенсивное использование наступает в периодах фазы их роста , а когда начинается окисление, аммонийный азот высвобождается в виде аммиака. Далее он окисляется до состояния нитритов и затем нитратов, или же повторно участвует в уже новом синтезе.
Для того чтобы аммонийный азот удалить из водоёма, применяется клиноптилолит, тогда вода восстанавливает свои качества. Ставятся градирни в тёплое время года, а зимой их заменяют ионообменные установки, благодаря которым вредные вещества удаляются из сточных вод. Постоянно проводятся анализы, берутся пробы на азот аммонийный в воде, который из взятой пробы отгоняется, а затем в полученном дистилляте определяется его количество.
Существует в природе ионообменный материал, который называется клиноптилолит (класс цеолитов). Именно с его помощью целесообразно восстанавливать чистоту воды. Азот аммонийный в воде растворяется не полностью, поэтому сначала нужно освободить её от всех взвешенных веществ, после чего подавать воду на клиноптилолитовые фильтры. Это довольно дорогая очистка, но зато самая эффективная — достигает девяноста семи процентов.
Регенерация потребует внесения раствора хлористого натрия — пяти- или десятипроцентного. Загрузку после этого нужно отмыть водой. Из раствора будет выделяться аммиак, который можно поглотить серной кислотой, чтобы образовался сульфат аммония, который очень хорош как удобрение. Азот аммонийный в сточных водах, а также азотосодержащие органические соединения удаляют различными видами перегонки, экстракции, адсорбции.
Этот метод хорош, если необходимо определение аммонийного азота. Другие его формы, которые встречаются в тех же удобрениях, — амидная, нитратная — именно этим методом определить нельзя. Сначала нужно извлечь азот аммонийный, в сточных водах, например, его предостаточно. Об этом методе написано выше. Далее навеску будущего удобрения нужно поместить в колбу и пролить раствором соляной кислоты (концентрация должна быть молярной — 0,05 моль на дм 3 ). Колбу необходимо встряхивать специальным аппаратом не менее получаса, после чего можно настаивать до пятнадцати часов.
Далее раствор снова взболтать и отфильтровать сквозь складчатый сухой фильтр. Тем же раствором соляной кислоты промыть содержимое фильтра как минимум трижды, затем объём фильтрата нужно довести до первоначального опять же раствором кислоты. Таким образом, во-первых, состоялось определение азота аммонийного в воде, а во-вторых — определение количества его в полученном удобрении. Последнее колеблется от сорока до ста пятидесяти миллиграммов на литр, а капролактама в этом же растворе содержится от восьми до восьмидесяти миллиграммов на литр. Если содержание аммонийного азота — менее двадцати миллиграммов, то опыт не удастся, и этот метод не применяется.
Самые характерные особенности производственных сточных вод — нестабильный химический состав, необходимый период адаптации для развития микрофлоры, избыток соединений органического и минерального происхождения азота. Перед произведением биологической очистки на очистных сооружениях сточные воды смешиваются с бытовыми и хозяйственными и таким образом усредняются. Азот аммонийный (формула NH4+) является обязательным компонентом сточных вод.
Источниками загрязнения могут являться сточные воды самых разных отраслей промышленности — от пищевой и медицинской до металлургической, коксохимической, микробиологической, химической и нефтехимической. Сюда же можно отнести все хозяйственно-бытовые стоки, навозные, сельскохозяйственные — с полей. В результате разлагаются белковые вещества и мочевина, а нитриты и нитраты анаэробно восстанавливаются.
На человеческий организм такие соединения влияют крайне отрицательно. Аммиак денатурирует белки, вступая с ними в реакцию. Тогда клетки и, соответственно, ткани организма перестают дышать, наблюдается поражение центральной нервной системы, печени, органов дыхания, нарушается работа сосудов. Если использовать регулярно воду с высоким содержанием аммония, страдает кислотно-щелочной баланс, начинается ацидоз.
Поэтому нельзя допускать использование выше нормы органических и минеральных удобрений в землепользовании, нужно постоянно бороться с излишним содержанием вредных веществ: например, азот аммонийный в почве обладает высокой растворимостью, поэтому и пища, и вода буквально отравлены им, его концентрации часто достигают токсического уровня. Особенно страдают от этого дети. Развивается метгемоглобинемия, кислородный режим в организме быстро разрушается, первым начинает страдать желудочно-кишечный тракт.
Единичные случаи заболевания метгемоглобинемией начинаются уже при содержании нитратов в воде до пятидесяти миллиграммов на литр, а когда концентрация их достигает девяноста пяти миллиграммов на литр, болезнь принимает массовый характер. В США, Франции, Нидерландах, ФРГ проведены детальные обследования, которые показали, что более пятидесяти миллиграммов нитратов на литр можно встретить в пятидесяти процентах случаев. Грунтовые и колодезные воды несут в десятки раз превышающую предел концентрацию нитратов — до полутора тысяч миллиграммов на литр, в то время как Всемирная организация здравоохранения установила предел в сорок пять миллиграммов. И это вода, которую пьют люди!
А уж сточные воды очищаются многими способами — и биологической фильтрацией, и окислением озоном, и гипохлоритами щёлочноземельных металлов, и аэрацией, и сорбцией, при которой используются цеолиты натриевой формы, и ионообменными смолами, и обрабатывают сильными щелочами, и флотацией, и восстанавливают аммоний металлическим магнием, и добавляют растворы хлорида магния с тринатрийфосфатом. Однако технологии очистки всегда намного отстают от технологий загрязнения.
В природных водах растворяется газ (NH3) аммиак, когда происходит биохимический распад органических соединений, в том числе и аммонийного азота. Тогда образуются и накапливаются другие соединения — аммоний-ион и азот аммонийный. Растворённый аммиак попадает в водоёмы с подземным или поверхностным стоком, со сточными водами, с атмосферными осадками. Если концентрация иона аммония (NH4+) превысит фоновое значение, это будет означать появление нового и близкого источника загрязнения. Это могут быть как животноводческие фермы или скопления навоза, так и бесхозно брошенные азотные удобрения, как отстойники промышленности, так и очистные коммунальные сооружения.
А соединения азота, углерода, фосфора, которые содержатся в сточных водах, попадая в водоёмы, приносят значительный ущерб экологии практически всех регионов России. Очистка сточных вод день ото дня становится всё более актуальной, поскольку концентрация вредных веществ, в том числе и азотных соединений, зачастую просто зашкаливает. Это сказывается не только на питьевой воде. Быстро накапливают нитраты практически все овощи и фрукты, они содержатся в траве и зерне, которые поедает скот.
Водоёмы всегда в нескольких переходных формах содержат азот: аммонийных солей и аммиака, альбуминоидного азота (органического), нитритов (солей азотистой кислоты) и нитратов (солей азотной кислоты). Всё это образуется вместе с процессом минерализации азота, но в большей мере поступает со сточными водами. Теперь водоёмы необходимо чистить. Соединения азота приходят на очистные сооружения в виде азота нитратов, азота нитритов, аммонийного азота и азота, связанного органическими соединениями. Сточные воды хозяйственно-бытового плана имеют небольшую концентрацию таких веществ, большую часть отправляет в водоёмы промышленность.
В процессе очистки соотношение массовых концентраций всех форм азотных соединений постоянно изменяется. Состав сточных вод становится другим уже при транспортировке, потому что мочевина, которая содержится в бытовых и хозяйственных сточных водах, взаимодействуя с бактериями, распадается и образует аммоний-ион. Чем протяжённее сеть канализации, тем дальше зайдёт этот процесс. Иногда содержание аммоний-иона при входе на очистку составляет до пятидесяти миллиграммов на кубический дециметр, что очень и очень много.
Это азот, который находится в составе органических веществ — протеидов и протеинов, полипепсидов (высокомолекулярных соединений), аминокислот, карбамидов (низкомолекулярных соединений), аминов, амидов. Вся органика, в том числе и азотосодержащая, попадает в сточные воды, после чего азотные соединения подвергаются аммонизации. Органического азота в сточных водах много, иногда до семидесяти процентов всех азотных соединений. Но в результате аммонизации на канализационном пути к очистным сооружениям приходит органического азота не более пятнадцати процентов.
Далее происходит уже рукотворная биологическая очистка. Первый этап — нитрификация, то есть переделка соединений азота за счёт определённых видов микроорганизмов, которые азот аммония окисляют, в нитрат-ион и нитрит-ион. Нитрифицирующих бактерий можно не опасаться — они к внешним условиям очень восприимчивы и легко вытесняются. А вот нитраты, если попадают в водоём, приводят его к гибели, поскольку являются великолепной питательной средой для разнообразной микрофлоры. Именно поэтому из экосистемы нитраты необходимо выводить.
Если сточные воды проникают сквозь почву, то аммонийный азот под влиянием некоторых бактерий превращается сначала в нитриты, потом в нитраты. Преобладание и содержание разнообразных форм зависит от тех условий, которые складываются на момент поступления соединений с присутствием азота в почву, а затем в водоём.
Во время паводка концентрация органических форм его значительно увеличивается, поскольку органические остатки бывают смыты с поверхности почвы, а летом уменьшаются так же значительно, потому что служат «едой» для различных водных организмов. Нитриты — промежуточная форма окисления аммонийного азота, стремящегося стать нитратами. В природных водах нитратов обычно не так много, если не случилось смыва удобрений с полей.
источник
Методы определения азотсодержащих веществ
Water. Methods for determination of nitrogen-containing matters
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены в ГОСТ 1.0-2015 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2015 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены»
1 ПОДГОТОВЛЕН Обществом с ограниченной ответственностью «Протектор» совместно с Закрытым акционерным обществом «Центр исследования и контроля воды»
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии, Техническим комитетом по стандартизации ТК 343 «Качество воды»
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 20 октября 2014 г. N 71-П)
За принятие проголосовали:
Краткое наименование страны по
МК (ИСО 3166) 004-97
Сокращенное наименование национального органа по стандартизации
Минэкономразвития Республики Армения
Госстандарт Республики Беларусь
Госстандарт Республики Казахстан
4 Приказом Федерального агентства по техническому регулированию и метрологии от 11 ноября 2014 г. № 1535-ст межгосударственный стандарт ГОСТ 33045-2014 введен в действие в качестве национального стандарта Российской Федерации с 1 января 2016 г.
5 Настоящий стандарт соответствует международному стандарту ISO 6777:1984* «Качество воды. Определение нитритов. Молекулярно-абсорбционный спектрометрический метод» («Water quality — Determination of nitrites. Molecular absorption spectrometric method», NEQ) в части раздела 7
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. — Примечание изготовителя базы данных.
6 ВЗАМЕН ГОСТ 4192-82, ГОСТ 18826-73
7 ИЗДАНИЕ (февраль 2019 г.) с Поправкой (ИУС 1-2017)
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
ВНЕСЕНА поправка, опубликованная в ИУС N 6, 2019 год
Поправка внесена изготовителем базы данных
Настоящий стандарт распространяется на питьевую (в том числе расфасованную в емкости), природную (поверхностную и подземную) и сточную воду и устанавливает следующие методы определения содержания минеральных азотсодержащих веществ:
— фотометрический метод определения содержания аммиака и ионов аммония (суммарно) с реактивом Несслера при массовой концентрации от 0,1 до 3,0 мг/дм без разбавления пробы. При необходимости определения более высоких концентраций пробу разбавляют, но не более чем в 100 раз (метод А);
— фотометрический метод определения содержания нитритов с использованием сульфаниловой кислоты при массовой концентрации от 0,003 до 0,3 мг/дм без разбавления пробы. При необходимости определения более высоких концентраций пробу разбавляют, но не более чем в 100 раз (метод Б);
— фотометрический метод определения азота нитритов с использованием 4-аминобензолсульфонамида при массовой концентрации от 0,25 до 10,0 мг/дм (метод В);
— фотометрический метод определения содержания азота нитратов с использованием фенолдисульфоновой кислоты при массовой концентрации от 0,1 до 6,0 мг/дм (метод Г);
— фотометрический метод определения содержания нитратов с использованием салициловокислого натрия при массовой концентрации от 0,1 до 2,0 мг/дм без разбавления пробы. При необходимости определения более высоких концентраций пробу разбавляют, но не более чем в 100 раз (метод Д).
Для определения нитритов арбитражным является метод Б, для нитратов — метод Д.
В настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ OIML R 76-1-2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 17.1.5.05-85 Охрана природы. Гидросфера. Общие требования к отбору проб поверхностных и морских вод, льда и атмосферных осадков
ГОСТ 61-75 Реактивы. Кислота уксусная. Технические условия
ГОСТ 83-79 Реактивы. Натрий углекислый. Технические условия
ГОСТ 1277-75 Реактивы. Серебро азотнокислое. Технические условия
ГОСТ 1770-74 (ISO 1042-83, ISO 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 2493-75 Реактивы. Калий фосфорнокислый двузамещенный 3-водный. Технические условия
ГОСТ 3760-79 Реактивы. Аммиак водный. Технические условия
ГОСТ 3773-72 Реактивы. Аммоний хлористый. Технические условия
ГОСТ 4197-74 Реактивы. Натрий азотистокислый. Технические условия
ГОСТ 4198-75 Реактивы. Калий фосфорнокислый однозамещенный. Технические условия
ГОСТ 4199-76 Реактивы. Hатрий тетраборнокислый 10-водный. Технические условия
ГОСТ 4204-77 Реактивы. Кислота серная. Технические условия
ГОСТ 4217-77 Реактивы. Калий азотистокислый. Технические условия
ГОСТ 4238-77 Реактивы. Квасцы алюмоаммонийные. Технические условия
ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия
ГОСТ 4329-77 Реактивы. Квасцы алюмокалиевые. Технические условия
ГОСТ 4517-87 Реактивы. Методы приготовления вспомогательных реактивов и растворов, применяемых при анализе
ГОСТ 4525-77 Реактивы. Кобальт хлористый 6-водный. Технические условия
ГОСТ ИСО 5725-6-2003* Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике*
_________________
* В Российской Федерации действует ГОСТ Р ИСО 5725-6-2002 «Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике».
ГОСТ 5845-79 Реактивы. Калий-натрий виннокислый 4-водный. Технические условия
ГОСТ 6552-80 Реактивы. Кислота ортофосфорная. Технические условия
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 9147-80 Посуда и оборудование лабораторные фарфоровые. Технические условия
ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
ГОСТ ИСО/МЭК 17025-2009 Общие требования к компетентности испытательных и калибровочных лабораторий
ГОСТ 18190-72 Вода питьевая. Методы определения содержания остаточного активного хлора
ГОСТ 20298-74 Смолы ионообменные. Катиониты. Технические условия
ГОСТ 20015-88 Хлороформ технический. Технические условия
ГОСТ 24147-80 Аммиак водный особой чистоты. Технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 27068-86 Реактивы. Натрий серноватистокислый (натрия тиосульфат) 5-водный. Технические условия
ГОСТ 28311-89 Дозаторы медицинские лабораторные. Общие технические требования и методы испытаний
ГОСТ 29227-91 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 31861-2012 Вода. Общие требования к отбору проб
ГОСТ 31862-2012 Вода питьевая. Отбор проб**
__________________
** В Российской Федерации действует ГОСТ Р 56237-2014 (ИСО 5667-5:2006).
ГОСТ 31868-2012 Вода. Методы определения цветности
ГОСТ 32220-2013 Вода питьевая, расфасованная в емкости. Общие технические условия
(Поправка).
Примечание — При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя «Национальные стандарты» за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3.2 Пробы воды, если они не могут быть проанализированы сразу, хранят при температуре от 2°С до 8°С не более 1 сут.
3.3 Пробы консервируют добавлением серной кислоты из расчета 1 см концентрированной серной кислоты на 1000 см воды (метод А) или добавлением хлороформа из расчета 2-4 см хлороформа на 1000 см воды (методы Б, В, Г и Д) и проводят определение не позднее чем через 2 сут.
3.4 Отбор проб питьевой воды, расфасованной в емкости, сроки и условия хранения — по ГОСТ 32220.
4.1 При подготовке и проведении измерений необходимо соблюдать условия, установленные в руководствах по эксплуатации или в паспортах средств измерений и вспомогательного оборудования.
4.2 Измерения объемов воды и растворов проводят при температуре окружающей среды от 15°С до 25°С. Допускается готовить растворы других номинальных объемов при условии соблюдения соотношений между объемами растворов и аликвот или массами навесок реагентов, регламентированных в настоящем стандарте.
Растворы следует хранить при комнатной температуре, если условия хранения не оговорены отдельно.
4.3 Лаборатории, проводящие определения, а также компетентность испытателей, должны соответствовать требованиям ГОСТ ИСО/МЭК 17025.
5 Фотометрический метод определения содержания аммиака и ионов аммония (суммарно) с использованием реактива Несслера (метод А)
5.1 Сущность метода
Настоящий метод основан на способности аммиака и ионов аммония взаимодействовать с реактивом Несслера с образованием окрашенного в желто-коричневый цвет соединения с последующим фотометрическим определением и расчетом массовой концентрации определяемых компонентов в пробе исследуемой воды.
5.1.1 Мешающие влияния
Мешающее влияние остаточного активного хлора устраняют добавлением эквивалентного количества серноватистокислого натрия; жесткости — добавлением раствора виннокислого калия-натрия и большого количества железа; цветности и мутности — осветлением гидроокисью алюминия, сульфатом алюминия, сульфатом цинка или сульфатом меди с последующей фильтрацией осветленных растворов.
5.2 Средства измерений, вспомогательное оборудование, реактивы, материалы
Фотометр, спектрофотометр, фотоэлектроколориметр, фотометрический анализатор (далее — прибор), позволяющие измерять оптическую плотность раствора в диапазоне длин волн от 400 до 600 нм при допускаемой абсолютной погрешности измерения спектрального коэффициента пропускания не более ±2% в оптических кюветах с толщиной поглощающего свет слоя от 1 до 5 см.
Межгосударственные стандартные образцы (МСО) состава водных растворов ионов аммония массовой концентрации 1 г/дм , с допускаемой относительной погрешностью аттестованного значения при доверительной вероятности =0,95 не более ±2%.
Весы неавтоматического действия по ГОСТ OIML R 76-1 высокого или специального класса точности с ценой деления (дискретностью отсчета) 0,1 мг, с наибольшим пределом взвешивания 220 и 500 г.
pH-метр любого типа, обеспечивающий измерение pH с допускаемой абсолютной погрешностью ±0,05 единиц pH.
Колбы мерные 2-50-2, 2-100-2, 2-200-2, 2-1000-2 по ГОСТ 1770.
Цилиндры мерные 2-10, 2-100, 2-500, 2-1000 по ГОСТ 1770.
Пипетки градуированные 1-1-2-1; 1-1-2-2; 1-1-2-5; 1-1-2-10 или других типов и исполнений по ГОСТ 29227.
Дозаторы пипеточные переменного объема с метрологическими характеристиками по ГОСТ 28311.
Колбонагреватель любого типа или водяная баня любого типа.
Электропечь лабораторная муфельная, поддерживающая температуру от 80°С до 300°С с погрешностью не более ±20°С.
Холодильник бытовой любого типа, обеспечивающий температуру от 2°С до 8°С.
Колбы конические по ГОСТ 25336, вместимостью 100, 1000, 1500 см .
Чашки выпарительные по ГОСТ 9147, вместимостью 100 или 150 см .
Стаканы по ГОСТ 9147, вместимостью 500 и 1000 см .
Воронки стеклянные для фильтрования по ГОСТ 25336.
Стаканы лабораторные по ГОСТ 25336.
Колбы плоскодонные по ГОСТ 25336, вместимостью 500 и 250 см .
Установка для обыкновенной перегонки или перегонки с водяным паром.
Фильтр мембранный с диаметром пор 0,45 мкм.
Бумага фильтровальная лабораторная по ГОСТ 12026.
Фильтр обеззоленный «белая» и «синяя» лента.
Аммиак по ГОСТ 3760, 25%-ный водный раствор.
Аммоний хлористый по ГОСТ 3773, ч.д.а.
Натрий серноватистокислый (тиосульфат натрия) 5-водный по ГОСТ 27068, х. ч. или стандарт-титр (фиксанал) тиосульфата натрия.
Калий-натрий виннокислый 4-водный по ГОСТ 5845, ч.д.а.
Калий фосфорнокислый однозамещенный по ГОСТ 4198, х.ч. или ч.д.а.
Калий фосфорнокислый двузамещенный по ГОСТ 2493, х.ч. или ч.д.а.
Натрия гидроокись по ГОСТ 4328, х.ч. или ч.д.а.
Натрий тетраборнокислый по ГОСТ 4199, х.ч. или ч.д.а.
Натрий углекислый по ГОСТ 83, х.ч.
Квасцы алюмокалиевые по ГОСТ 4329 или квасцы алюмоаммонийные по ГОСТ 4238, ч.д.а.
Кислота серная по ГОСТ 4204, ч.д.а.
Реактив Несслера.
Вода, не уступающая по значениям массовой концентрации веществ, восстанавливающих КМnO , и удельной электрической проводимости значениям по ГОСТ 6709 (далее — дистиллированная вода).
Хлороформ (трихлорметан) по ГОСТ 20015.
Уголь активированный марки БАУ.
Катиониты по ГОСТ 20298.
Примечание — Допускается применять другие средства измерений, вспомогательные устройства с метрологическими и техническими характеристиками и реактивы по качеству не ниже указанных в настоящем стандарте.
5.3 Подготовка к проведению измерений
5.3.1 Приготовление безаммиачной воды
Дистиллированную воду проверяют на содержание аммиака и ионов аммония (к 5 см воды прибавляют 0,1 см реактива Несслера, приготовленного, например, по ГОСТ 4517, пункт 2.134). При обнаружении аммиака (появляется желтоватое окрашивание) дистиллированную воду пропускают через колонку с активированным углем, катионитом в Н -форме или кипятят в колбе до уменьшения объема на 1/3. Затем повторно проверяют на отсутствие аммиака и ионов аммония.
На безаммиачной дистиллированной воде (далее — дистиллированная вода) готовят реактивы и растворы, ее используют в анализе для разбавления пробы.
5.3.2 Приготовление основного раствора массовой концентрации ионов аммония 1 мг/см (при отсутствии МСО по 5.2)
В мерную колбу вместимостью 1000 см вносят 2,965 г хлористого аммония, предварительно высушенного до постоянной массы при температуре от 100°С до 105°С, растворяют в небольшом количестве дистиллированной воды (5.3.1) и доводят до метки этой же водой.
Срок хранения раствора в емкости из темного стекла — не более 1 года.
Раствор пригоден к использованию, если нет помутнения, хлопьев, осадка.
5.3.3 Приготовление рабочего раствора массовой концентрации ионов аммония 0,05 мг/см
В мерную колбу вместимостью 100 см вносят 5 см основного раствора (5.3.2) или стандартного образца (СО) состава водных растворов ионов аммония номинальной массовой концентрацией 1 г/дм (5.2) и доводят до метки дистиллированной водой (5.3.1).
Раствор готовят в день использования.
5.3.4 Приготовление реактива Несслера
Применяют готовый реактив по 5.2 или готовят его по ГОСТ 4517 пункт 2.134 на безаммиачной дистиллированной воде (5.3.1).
Срок хранения раствора — не более 3 лет.
5.3.5 Приготовление раствора виннокислого калия-натрия
В мерную колбу вместимостью 1000 см , наполовину заполненную дистиллированной водой (5.3.1) вносят 500 г виннокислого калия-натрия и доводят до метки дистиллированной водой (5.3.1). Затем прибавляют 5-10 см реактива Несслера (5.3.4).
После осветления раствор не должен содержать ион аммония (контроль по качественной реакции раствора с реактивом Несслера — отсутствие окраски), в противном случае прибавляют еще 2-5 см реактива Несслера (5.3.4).
Срок хранения раствора — не более 6 мес.
5.3.6 Приготовление суспензии гидроокиси алюминия
В колбу вместимостью 1000 см вносят 125 г алюмокалиевых квасцов (5.2) и растворяют в 1000 см дистиллированной воды (5.3.1), нагревают до 60°С и постепенно прибавляют 55 см 25%-ного раствора аммиака (5.2) при постоянном перемешивании.
После отстаивания осадок переносят в большой стакан и промывают декантацией дистиллированной водой (5.3.1) до отсутствия реакции на аммиак. Контроль промывки осуществляют по качественной реакции промывной воды с реактивом Несслера (5.3.4). Промывку проводят до исчезновения окраски при контроле.
Срок хранения — не более 1 года.
5.3.7 Приготовление основного раствора серноватистокислого натрия молярной концентрации 0,1 моль/дм
В мерной колбе вместимостью 1000 см , наполовину заполненной дистиллированной водой, растворяют 25,0 г серноватистокислого натрия, добавляют 0,2 г углекислого натрия и доводят объем раствора в колбе до метки дистиллированной водой. В случае применения стандарт-титра (фиксанала) раствор готовят в соответствии с инструкцией по приготовлению.
Срок хранения раствора в емкости из темного стекла в защищенном от прямых солнечных лучей месте — не более 3 мес.
5.3.8 Приготовление рабочего раствора серноватистокислого натрия молярной концентрации 0,01 моль/дм
В мерную колбу вместимостью 1000 см вносят 100 см основного раствора серноватистокислого натрия молярной концентрации 0,1 моль/дм (5.3.7), добавляют 0,2 г углекислого натрия и доводят объем раствора в колбе до метки дистиллированной водой по 5.3.1.
Срок хранения раствора в емкости из темного стекла — не более 3 мес.
5.3.9 Приготовление раствора тетраборнокислого натрия молярной концентрации 0,025 моль/дм
9,5 г 10-водного тетраборнокислого натрия растворяют в мерной колбе вместимостью 1000 см в дистиллированной воде по 5.3.1.
Срок хранения раствора — не более 3 мес.
5.3.10 Приготовление раствора гидроокиси натрия молярной концентрации 0,1 моль/дм
В мерной колбе вместимостью 1000 см , наполовину заполненной дистиллированной водой по 5.3.1, растворяют 4 г гидроокиси натрия и доводят объем раствора до метки дистиллированной водой по 5.3.1.
Срок хранения раствора в емкости из полимерных материалов — не более 3 мес.
5.3.11 Приготовление боратного буферного раствора со значением pH 9,5
В мерной колбе вместимостью 1000 см к 500 см раствора тетраборнокислого натрия молярной концентрации 0,025 моль/дм (5.3.9) приливают 88 см раствора гидроокиси натрия молярной концентрации 0,1 моль/дм (5.3.10) и разбавляют до 1 дм дистиллированной водой по 5.3.1.
Срок хранения раствора — не более 3 мес.
5.3.12 Приготовление фосфатного буферного раствора со значением pH 7,4
В мерной колбе вместимостью 1000 см растворяют 14,3 г безводного однозамещенного фосфорнокислого калия и 68,8 г безводного двузамещенного фосфорнокислого калия в дистиллированной воде по 5.3.1.
Срок хранения раствора — не более 3 мес.
5.3.13 Приготовление раствора серной кислоты молярной концентрацией 1 моль/дм
В мерную колбу вместимостью 1000 см , заполненную на 150-200 см дистиллированной водой по 5.3.1, вносят небольшими порциями при перемешивании 27,3 см серной кислоты и доводят объем раствора до метки дистиллированной водой (5.3.1).
Срок хранения раствора — не более 1 года.
5.3.14 Приготовление раствора гидроокиси натрия массовой долей 40%
В фарфоровом стакане вместимостью 500 см в 60 см дистиллированной воды по 5.3.1 осторожно при перемешивании порциями растворяют 40 г гидроокиси натрия.
Срок хранения раствора в емкости из полимерных материалов — не более 1 года.
5.3.15 Приготовление градуировочных растворов
5.3.15.1 В мерные колбы вместимостью 50 см каждая вносят 0,0; 0,1; 0,2; 0,5; 1,0; 1,5; 2,0; 3,0 см рабочего раствора (5.3.3) и доводят до метки дистиллированной водой (5.3.1).
Массовая концентрация ионов аммония в приготовленных градуировочных растворах составляет соответственно 0,0; 0,1; 0,2; 0,5; 1,0; 1,5; 2,0; 3,0 мг/дм .
Градуировочный раствор, не содержащий ионов аммиака, является холостой пробой для градуировки.
Градуировочные растворы готовят в день использования.
5.3.15.2 Подготовка градуировочных растворов к измерениям
В каждую колбу с градуировочными растворами (5.3.15.1) прибавляют 1 см раствора виннокислого калия-натрия (5.3.5), перемешивают, затем прибавляют 1 см реактива Несслера (5.3.4) и снова перемешивают. Через 10 мин проводят градуировку по 5.3.17.
5.3.16 Подготовка прибора
Подготовку прибора к работе проводят в соответствии с руководством (инструкцией) по эксплуатации прибора.
5.3.17.1 Измеряют оптическую плотность подготовленных градуировочных растворов и холостой пробы (5.3.15.2) три раза при длине волны от 400 до 425 нм в оптической кювете с выбранной толщиной поглощающего слоя, используя в качестве раствора сравнения дистиллированную воду (5.3.1).
Для каждого градуировочного раствора и холостой пробы рассчитывают среднеарифметическое значение полученных значений оптической плотности.
где — массовая концентрация ионов аммония в i -м градуировочном растворе, мг/дм ;
— среднеарифметическое значение оптической плотности i -ого градуировочного раствора за вычетом среднеарифметического значения оптической плотности для холостой пробы, ед.опт.пл.;
— число градуировочных растворов.
Примечание — В случае, если компьютерная (микропроцессорная) система сбора и обработки информации прибора рассчитывает угловой коэффициент b , то коэффициент градуировочной характеристики (К) устанавливают равным 1/ b .
где — массовая концентрация ионов аммония в i-м градуировочном растворе, мг/дм ;
— среднеарифметическое значение оптической плотности i -гo градуировочного раствора за вычетом среднеарифметического значения оптической плотности холостой пробы, ед.опт.пл.
Результаты контроля признают удовлетворительными, если выполняется условие
где — значение коэффициента градуировочной характеристики i -го градуировочного раствора, рассчитанного по формуле (2);
К — значение коэффициента градуировочной характеристики, рассчитанного по формуле (1) при градуировке прибора;
N — норматив контроля приемлемости градуировочной характеристики, равный 10%.
Если условие (3) не выполняется, то установление градуировочной характеристики повторяют. Градуировку также проводят после ремонта прибора и смены реактивов.
5.3.17.4 Контроль стабильности градуировочной характеристики
Стабильность градуировочной характеристики контролируют с каждой серией проб. Для контроля используют два или три градуировочных раствора по 5.3.15.
Проводят измерение контрольных градуировочных растворов по 5.3.17.1.
Градуировочную характеристику считают стабильной при выполнении условия
где — массовая концентрация ионов аммония в градуировочном растворе, полученная при контрольном измерении, мг/дм ;
С — массовая концентрация ионов аммония в градуировочном растворе, полученная по процедуре приготовления, мг/дм ;
— норматив контроля стабильности градуировочной характеристики, равный 10%.
Если условие (4) не выполняется, то проводят повторное измерение для этого градуировочного раствора (свежеприготовленного). Если градуировочная характеристика вновь нестабильна, выясняют причины нестабильности, устраняют их и повторяют контроль с использованием не менее двух других свежеприготовленных градуировочных растворов. При повторном обнаружении нестабильности устанавливают новую градуировочную характеристику.
5.3.18 Подготовка пробы исследуемой воды
5.3.18.1 Устранение мешающих влияний
При содержании в пробе исследуемой воды активного остаточного хлора в количестве более 0,5 мг/дм добавляют эквивалентное количество раствора серноватистокислого натрия по 5.3.8 (определяют в отдельной аликвоте пробы исследуемой воды по ГОСТ 18190).
Мутную или цветную воду (при цветности выше 20°, например, по ГОСТ 31868) подвергают коагуляции гидроокисью алюминия следующим образом: на 250-300 см исследуемой воды прибавляют 2-5 см суспензии гидроокиси алюминия (5.3.6), встряхивают вручную, после осветления отбирают прозрачный слой для анализа. При необходимости воду с коагулянтом фильтруют через обеззоленный фильтр «синяя лента», предварительно промытый горячей дистиллированной водой (5.3.1) до отсутствия в фильтрате ионов аммония. Контроль промывки осуществляют по качественной реакции промывной воды с реактивом Несслера (5.3.4). Промывку проводят до исчезновения окраски при контроле. При фильтровании пробы первые порции фильтрата от 30 до 50 см отбрасывают.
5.3.18.2 Подготовка проб с отгонкой
5.3.18.2.1 Отгонку аммиака из исследуемой пробы (раздел 3) выполняют, как правило, для проб сточных вод. Отгонку аммиака из исследуемой пробы (раздел 3), содержащей легко гидролизуемые органические соединения, проводят при значении pH 7,4, добавляя к пробе фосфатный буферный раствор (5.3.12). В присутствии цианатов и большинства азотсодержащих органических соединений используют боратный буферный раствор со значением pH 9,5 (5.3.11). При необходимости анализа сточных вод предприятий, образующих в процессе производства фенолы (сбрасывающие содержащие фенол сточные воды), к пробе добавляют раствор гидроокиси натрия массовой долей 40% до значения pH 9,5 (5.3.14). Если присутствуют вещества, гидролизующиеся в щелочной среде, то отгонку проводят дважды: сначала при значении pH 7,4, собирая отгон в разбавленный раствор серной кислоты, потом подщелачивают этот отгон до сильнощелочной реакции и отгоняют повторно, собирая отгон в раствор борной кислоты или дистиллированную воду (5.3.1).
5.3.18.2.2 Если проба содержит большое количество взвешенных веществ или нефтепродуктов, ее предварительно фильтруют через фильтр «белая лента». Мешающие влияния (5.1.1) устраняют по 5.3.18.1.
5.3.18.2.3 В колбу для отгона помещают 400 см анализируемой пробы или отгона при pH 7,4, или меньший объем, доведенный до 400 см дистиллированной водой по 5.3.1. Затем, в зависимости от предполагаемых загрязнений, приливают 25 см буферного раствора со значением pH 9,5 (5.3.11), или 20 см раствора гидроокиси натрия с массовой долей 40% (5.3.14). В приемник наливают 50 см раствора борной кислоты и устанавливают объем жидкости так, чтобы конец холодильника был погружен в нее, добавляя при необходимости дистиллированную воду по 5.3.1. Отгоняют примерно 300 см жидкости, отгон количественно переносят в мерную колбу вместимостью 500 см , добавляют водный раствор серной кислоты молярной концентрации 1 моль/дм (5.3.13) до значения pH 6,0, и разбавляют до метки дистиллированной водой по 5.3.1. Далее пробу готовят по 5.3.18.3.
5.3.18.3 К 50 см исследуемой (раздел 3), осветленной (5.3.18.1) или подготовленной (5.3.18.2) пробы (или к меньшему объему, содержащему не более 0,15 мг NH и разбавленному дистиллированной водой по 5.3.1 до 50 см ) прибавляют 1 см раствора виннокислого калия-натрия (5.3.5), перемешивают, затем прибавляют 1 см реактива Несслера (5.3.4) и снова перемешивают. Через 10 мин проводят определение по 5.4.
5.4 Проведение измерений
Измеряют оптическую плотность аликвоты подготовленной пробы исследуемой воды (5.3.18.3), как при построении градуировочной характеристики (5.3.17.1) с последующим расчетом массовой концентрации аммиака и ионов аммония (5.5). В качестве холостой пробы используют дистиллированную воду, подготовленную аналогично пробе исследуемой воды (5.3.18.3).
5.5 Обработка результатов измерений
5.5.1 При наличии компьютерной (микропроцессорной) системы сбора и обработки информации порядок обработки результатов определяется руководством (инструкцией) по эксплуатации прибора.
где К — коэффициент градуировочной характеристики, рассчитанный по формуле (1), мг/(дм · ед.опт.пл.);
А — измеренное значение оптической плотности пробы анализируемой воды за вычетом измеренного значения оптической плотности холостой пробы, ед.опт.пл.;
V — объем аликвоты пробы, взятой для анализа, см ;
f — коэффициент разбавления пробы анализируемой воды, при этом если пробу не разбавляли, то принимают равным 1, если разбавляли, то f рассчитывают по формуле
где — вместимость мерной колбы, использованной при разбавлении пробы анализируемой воды, см ;
— объем аликвоты пробы анализируемой воды, взятый для разбавления, см .
Примечание — При расчете учитывают объемы кислоты, добавленной в пробу (раздел 3).
Для проб, подготовленных по 5.3.18.2, значение X , мг/дм , рассчитывают по формуле:
где — вместимость мерной колбы, использованной при подготовке пробы анализируемой воды для измерения (в данном случае равен 50 см ), см ;
5.5.3 При необходимости представления результата в пересчете на массовую концентрацию аммонийного азота результат, полученный по формуле (5) или (7), умножают на коэффициент 0,78.
где R — значение предела воспроизводимости по таблице 1, %.
При невыполнении условия (9) для проверки приемлемости в условиях воспроизводимости каждая лаборатория должна выполнить процедуры согласно ГОСТ ИСО 5725-6 (пункты 5.2.2; 5.3.2.2)*.
________________
* В Российской Федерации — согласно Рекомендации МИ 2881-2004 «Государственная система обеспечения единства измерений. Методики количественного химического анализа. Процедуры проверки приемлемости результатов анализа».
5.6 Метрологические характеристики
Метод обеспечивает получение результатов измерения с метрологическими характеристиками, не превышающими значений, приведенных в таблице 1, при доверительной вероятности Р= 0,95.
Таблица 1
Предел повторяемости (относительное значение допускаемого расхождения между двумя результатами параллельных определений, полученными в условиях повторяемости при Р =0,95) r , %
Предел воспроизводимости (относительное значение допускаемого расхождения между двумя результатами определений, полученными в условиях воспроизводимости при Р= 0,95) R, %
источник