Показания к проведению исследования: воспалительные заболевания нижних отделов дыхательных путей при отсутствии мокроты.
1. Стерильный физиологический раствор.
2. Стерильный горловой шприц или аппарат Боброва.
3. Стерильный широкогорлый контейнер.
Взятие исследуемого материала:
Исследование промывных вод бронхов проводят при отсутствии или скудости мокроты. Это связано не только с технической сложностью взятия этого вида материала, но и с меньшей диагностической ценностью результата из-за значительного его разбавления (концентрация микроорганизмов в промывных водах в 10—1000 раз ниже чем в мокроте).
Простейший метод взятия трахеобронхиального смыва: гортанным шприцем с помощью аппарата Боброва в трахею вводят около 10 мл стерильного физиологического раствора, и после возникновения кашля собирают откашлянный трахеобронхиальный смыв в стерильный широкогорлый контейнер. У маленьких детей через катетер вводят в трахею 5—10 мл физиологического раствора и затем отсасывают трахеобронхиальный смыв.
Бронхиальные смывы могут быть получены при бронхоскопии. В том случае не рекомендуется вводить в бронх более 5 мл физиологического раствора.
Большое значение для качества воды имеет способ ее сбора и хранение. Хранить воду для инъекций необходимо в закрытых сосудах, защищенных от попадания углерода диоксида и пыли. Сосуды необходимо часто мыть и стерилизовать.
Вода — одно из самых удивительных веществ в природе. Например, ее теплоемкость — 4,1868 кДж/кг, что почти вдвое превышает таковую растительных масел, ацетона, фенола, глицерина, спирта, парафина.
Вода подземных источников, поступающая в систему водоочистки, должна соответствовать стандартам на питьевую воду. Несмотря на то, что природная вода должна быть пригодна для питья.
Для получения воды очищенной применяются последовательные многоступенчатые схемы. При выборе конкретной схемы необходимо учитывать результаты анализа исходной воды и имеющееся в наличии оборудование. Следует отметить.
Вода — важнейший фактор формирования внутренней среды организма и в то же время один из факторов внешней среды. Там, где нет воды, нет жизни. В воде происходят все процессы, характерные для живых организмов, населяющих нашу Землю.
Централизованное водоснабжение позволяет резко поднять уровень санитарной культуры населения, способствует уменьшению заболеваемости лишь при бесперебойной подаче достаточного количества воды определенного качества.
Различают острый и хронический бронхиты. Острый бронхит развивается обычно вместе с другими признаками острого воспаления верхних дыхательных путей, воспаление как бы спускается вниз от верхних дыхательных путей к бронхам.
Препараты, содержащие в водном или водно-спиртовом растворе эфирные масла. Приготовление ароматных вод с водяным паром было известно в Древнем Египте, однако особую популярность они получили в эпоху арабской фармации, причем арабам.
2. Анализ исследования питьевой воды и воды бассейнов, проведенных в централизованной бактериологической лаборатории за 2008-2010 гг.
Мною были также проанализированы результаты исследований воды бассейнов, т.к. качество пресной воды.
Питьевые минеральные воды различного химического состава воздействуют на регуляцию функциональной деятельности гастро-дуоденальной системы [9]. Известно, что выделение панкреатического сока.
1.Описание. Бесцветная прозрачная жидкость без запаха и вкуса. рН. от 5,0 до 7,0 (к 100 мл воды прибавляют 0,3 мл насыщенного раствора калия хлорида и измеряют рН раствора потенциометрически. 2.Сухой остаток.
Минеральные воды — сложные растворы, в которых вещества содержатся в виде ионов, недиссоциированных молекул, газов, коллоидных частиц. Критерии для отнесения вод к «минеральным» в той или иной степени отличаются у разных исследователей.
На фармацевтическом производстве вода очищенная является исходной при получении воды для инъекций. Вода очищенная должна отвечать требованиям по ионной и органической химической, а также микробиологической чистоте.
На фармацевтическом производстве вода очищенная является исходной при получении воды для инъекций. Вода очищенная должна отвечать требованиям по ионной и органической химической, а также микробиологической чистоте.
источник
Наиболее характерные изменения в анализах крови.У больных с начальными формами туберкулеза в крови содержится нормальное количество эритроцитов и гемоглобина. По мере нарастания патологических изменений в легочной ткани может развиться гиперхромная анемия, при резком исхудании больного могут наблюдаться явления гипохромной анемии. Может наблюдаться лейкоцитоз в пределах 12—15∙109. или количество лейкоцитов в норме. Более характерен нейтрофильный сдвиг влево.
Тяжелые формы туберкулеза протекают с эозинопенией и лимфопенией. При малых и свежих формах туберкулеза обычно наблюдается лимфоцитоз.
Повышенная СОЭ зависит от процесса туберкулеза, только при туберкулезном менингите она может быть в пределах нормы.
Обнаружение микобактерий.Имеет решающее значение не только для диагностики туберкулеза, оно чрезвычайно важно при прогнозировании течения процесса, выборе рациональной схемы лечения и правильной оценке его эффективности.
Основными методами лабораторной диагностики туберкулеза являются классические микробиологические методы: бактериоскопия; культуральное исследование, или посев; биологическая проба на чувствительных к туб. инфекции лабораторных животных.
Сбор материала на исследование. От соблюдения правил сбора, хранения и транспортировки биолог. материала зависит не только достоверность результатов, но и эпидемиологическая безопасность окружающих.
Материал для исследования собирают в стерильные контейнеры (стеклянные банки) с плотно завинчивающимися крышками. Это предотвращает попадание содержимого и загрязнение окружающей среды микобактериями и обеспечивает изоляцию исследуемого материала от широко распространенных в окружающей среде кислотоустойчивых бактерий.
Для исследования может быть использован разнообразный патологический материал: мокрота, аспират, содержимое бронхов и другие материалы, получаемые при бронхоскопии, промывные воды бронхов и желудка, экссудаты, гной, отделяемое ран, спинномозговая жидкость, кровь, моча, операционный материал, смывы с предметов и др.
У больных легочными формами объектом исследования чаще служит мокрота. Желательно, чтобы сбор мокроты производился в отдельной, хорошо вентилируемой комнате. Собирают утреннюю порцию. Если больной выделяет мало мокроты, ее следует собирать в течение суток, при этом обязательно собранный материал хранить в холодильнике. Если исследование проводится на фоне лечения, за 2 суток до сбора мокроты прием противотуберкулезных препаратов отменяется. Сбор мокроты должен производиться в присутствии и при непосредственном участии среднего мед. персонала.
Лица, ответственные за сбор мокроты, руководствуются следующими правилами:
1. Объяснить больному причины исследования и необходимость откашливать содержимое глубоких отделов дыхательных путей, а не собирать слюну или носоглоточную слизь. Необходимо предупредить больного, что он должен предварительно почистить зубы и прополоскать полость рта кипяченой водой, чтобы механически удалить основную часть микрофлоры, вегетирующей в ротовой полости.
2. Присутствующий при сборе мокроты мед. работник должен открытьь стерильный контейнер, снять с него крышку и передать больному только донную часть контейнера.
3. Стоя позади больного, следует рекомендоватьему держать контейнер как можно ближе к губам и сразу же сплевывать в него мокроту по мере ее откашливания.
4. По завершении сбора мокроты мед. работник оценивает ее количество и качество; контейнер с порцией мокроты не менее 3-5 мл, содержащей уплотненные или гнойные комочки без слюны, тщательно закрывают завинчивающейся крышкой, маркуруют и помещают в специальный ящик для транспортировки в лабораторию.
Если больной не выделяет мокроту или выделяет ее только эпизодически и в скудном количестве, то накануне и рано утром в день сбора мокроты больному следует дать отхакивающее средство или применить раздражающие аэрозольные ингаляции (усиливаются секреция бронхов, кашль и отделение мокроты). Для этого используют портативные аэрозольные ингаляторы. В качеств ингалируемой смеси можно использовать 15% р-р хлорида натрия в 1% р-ре бикарбоната натрия (150г NaCl и 10г NaHCO3 на 1 литр дистиллированной воды).
Если мокроту не удалось получить, используют промыные воды бронхов или желудка (преимущественно у детей младшего возраста, которые плохо откашливают мокроту и заглатывают ее).
Промывные воды желудка берут натощак, предварительно дав больному выпить или введя через зонд 100—150 мл раствора бикарбоната натрия (питьевой соды). Промывные воды желудка должны исследоваться немедленно, чтобы исключить повреждающее воздействие на возбудителя желудочных ферментов.
Более ценным материалом для исследования при отсутствии мокроты являются аспираты из трахеи и бронхов, бронхоальвеолярная лаважная жидкость, а также материалы прицельной биопсии, получаемые при бронхологических исследованиях.
Исследование кала на микобактерии необходимо производить при наличии признаков туберкулеза кишечника. Для исследования берут несколько комочков кала со слизью или гноем, размешивают с 5%-м изотоническим раствором хлорида натрия и фильтруют. В настоящее время туберкулез кишечника встречается исключительно редко, а поэтому исследование кала на БК практически не производится.
Для обнаружения микобактерии в плевральном экссудате, в пунктатах и отделяемом из свищей препарат приготавливают так же, как и при исследовании мокроты.
Особого методического подхода требует исследование менструальной крови. Этот материал незамедлительно доставляют в лабораторию.
Сбор мочи. Для исследования используют обычно среднюю порцию утренней мочи, полученной после тщательного туалета наружных половых органов растворами антисептиков (слабый раствор перманганата калия, риванола и пр.)
Хранение, консервация и транспортировка диагностического материала. В противотуберкулезных учреждениях функционируют специализированные лаборатории, производящие бактериологические исследования.
В стационарах стерильные контейнеры с мокротой или другим патологическим материалом доставляются непосредственно в лабораторию. Сбор материала от амбулаторных больных производится под непосредственным наблюдением среднего медицинского работника.
Если в лечебном учреждении не проводятся исследования для выявления кислотоустойчивых микобактерий, собранный диагностический материал должен централизованно доставляться в лабораторию. Обычно такая доставка осуществляется один или два раза в неделю. Следовательно, материал должен накапливаться в течение нескольких дней. Для этого используют биксы или специальные транспортировочные ящики, вмещающие 10 — 20 контейнеров, которые хранятся в холодильнике.
Во время транспортировки материал необходимо предохранять от воздействия прямых солнечных лучей и тепла. В определенных ситуациях используют консервант — 2 —3%-й раствор борной кислоты в соотношении 1:1 или глицерин. В качестве консерванта можно также использовать 10%-й раствор трехзамещенного фосфата натрия или 0,05—0,1%-й раствор хлоргексидин биглюконата в соотношении 1:1; Рост микобактерий может быть получен даже после хранения мокроты с консервантом при температуре 30 °С в течение 10—12 дней.
Бактериоскопическое исследование. Оно является одним из основных и наиболее распространенных методов. Преимущества его заключаются в простоте, дешевизне и быстроте получения результатов. Однако возможности метода ограничены. В препарате можно обнаружить единичные микобактерии, если в 1 мл материала содержится не менее 10 000— 100 000 бактериальных клеток (предел метода).
Наиболее распространенным методом окраски для выявления кислотоустойчивых микобактерий является способ Циля—Нильсена.
Мокроту на предметном стекле окрашивают карболовым фуксином, при одновременном воздействии нагревания обесцвечивают мазок в 3%-м растворе солянокислого спирта (приводит к обесцвечиванию всех некислотоустойчивых структур) и докрашивают метиленовым синим. Только микобактерии, обладающие выраженной кислото- и спиртоустоичивостью, стойко удерживают краситель и остаются окрашенными в красный цвет.
Микобактерии обнаруживаются в препарате в виде тонких, прямых или слегка изогнутых ярко-красных палочек.
В настоящее время применяется метод окраски люминисцентными красителями (более высокая информативность).
В тех случаях, когда в патологическом материале не удается обнаружить микобактерии методом бактериоскопии, производят бактериологическое исследование. Культуральный метод — посев материала на питательные среды. Преимущество метода в высокой чувствительности. Достаточно 20—100 микобактерий в 1 мл материала. Недостаток метода заключается в длительности роста колоний: 1 — 3 мес.
Применение двух методов в совокупности позволяет более точно количественно оценить степень бактериовыделения.
Исследуемый материал высевают на специальные среды после предварительной обработки. Наиболее часто используют яичные среды. Первые колонии микобактерий появляются на 18 —30-й день, а иногда и через 3 месяца.
Бактериологическое и бактериоскопическое исследование необходимо проводить в сочетании.
Биологический метод заражения животных сейчас применяется только в научно-исследовательских институтах.
В настоящее время началось использование молекулярно-биологического метода — полимеразной цепной реакции (ПЦР). Сначала выделяется ДНК микобактерии, затем она клонируется и идентифицируется. Метод очень чувствительный (достаточно 1 МБТ), однако без одновременной оценки клинической картины заболевания использовать его надо осторожно. Это — перспективный метод, но его роль еще до конца не определена.
Определение лекарственной устойчивости микобактерий.В настоящее время разработаны и внедрены в практическую деятельность диспансеров методы определения лекарственной чувствительности (устойчивости) микобактерий к туберкулостатическим препаратам. Различают первичную лекарственную устойчивость у больных, не леченных противотуберкулезными препаратами, и вторичную, развивающуяся в процессе лечения. Частота первичной устойчивости составляет 20 —80 %.
Лекарственная устойчивость микобактерий может быть: моно — к одному препарату, множественная — к смеси изониазида и рифампицина, полирезистентная — к двум и более препаратам кроме рифампицина и изониазида, перекрестная — к препаратам со сходной химической структурой.
В настоящее время внедряются генетические методы определения лекарственной устойчивости с помощью ПЦР-метода.
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Сдача сессии и защита диплома — страшная бессонница, которая потом кажется страшным сном. 8718 — 

195.133.146.119 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
источник
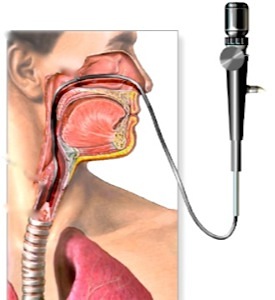
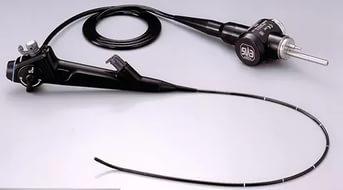
- Подозрение на опухоль трахеи и бронхов
- Кровохарканье
- Подозрение на наличие инородного тела в просвете дыхательных путей
- Ожоги нижних дыхательных путей
- Пневмония с затяжным течением, рецидивирующие пневмонии
- Деструктивная/аспирационная пневмония, абсцесс легкого
- Хронические заболевания бронхов и легких невыясненной причины
- Признаки диссеминированных патологических процессов на рентгене (мелких очагов, кист, полостей)
- Длительная одышка (при исключении бронхиальной астмы и сердечной недостаточности)
- Немотивированный кашель, продолжающийся свыше 1 месяца
В настоящее время врачи снижают количество противопоказаний к бронхоскопии. Но при некоторых патологиях обследование может принести больше вреда, чем пользы.
- Обострение хронической обструктивной болезни легких (ХОБЛ) и бронхиальной астмы (проведение процедуры в этот момент может усилить спазм бронхов и усугубить состояние больного).
- Инфаркт миокарда и инсульт, перенесенные менее 4 недель назад (стресс и спазм сосудов и некоторая нехватка кислорода во время процедуры могут вызвать повторный случай нарушения кровообращения).
- Неконтролируемая аритмия
- Выраженные нарушения свертываемости крови (тромбоцитопения менее 20000)
- Аневризма аорты
- Психические заболевания, такие как шизофрения и эпилепсия (стресс и снижение концентрации кислорода в крови могут спровоцировать приступ судорог)
- Исследование проводят строго натощак, полностью исключается прием пищи за 8-10 часов и жидкости за 4–6 часов до начала процедуры. Вечером накануне исследования (до 18:00) — лёгкий ужин. В день исследования от курения следует воздержаться.
- Отменить пероральные антикоагулянты (препараты для разжижения крови) накануне исследования, пауза п/к введения гепарина за 4-6 часов до процедуры.
- На обследование при себе необходимо иметь амбулаторную карту, результаты КТ грудной клетки или описание рентгенограммы легких, полотенце (так как после процедуры возможно непродолжительное кровохарканье). Если Вы страдаете бронхиальной астмой, то не забудьте ингалятор.
- Во время предварительной беседы сообщите врачу об аллергии на медикаменты (особенно если есть аллергия на обезболивающие препараты) и имеющихся у Вас хронических заболеваниях (бронхиальная астма, сердечная недостаточность).
Исследование проводят в положении сидя. При этом нельзя вытягивать вперед голову и выгибать грудную клетку, чтобы аппарат не травмировал слизистую дыхательных путей. С целью местной анестезии непосредственно перед исследованием проводится обработка носовой и ротовой полости 10% Лидокаин-спреем. Он вызывает онемение неба, чувство комка в горле, легкую заложенность носа. Анестезия помогает подавить кашлевой и рвотный рефлекс. В процессе исследования анестетиком поэтапно орошается слизистая гортани, голосовых связок, трахеи и бронхов. Вопреки тревожным ожиданиям большинства пациентов, во время бронхоскопии они совершенно не чувствуют боли.
Трубка бронхоскопа имеет очень маленький диаметр, поэтому дыханию обследуемого она не мешает. Во время продвижения трубки по дыхательным путям в них может ощущаться легкое давление, но выраженного дискомфорта Вы при этом не испытываете. Чтобы снизить рвотный рефлекс в момент введения бронхоскопа, рекомендуем Вам дышать поверхностно и как можно чаще.
После процедуры чувство онемения остается на протяжении получаса. Не рекомендуется курить и принимать пищу на протяжении 2-х часов после завершения процедуры.
Процедура бронхоскопии, выполненная на современном цифровом оборудовании, сопровождается фиксацией полученного материала в виде фото– или видеозаписи, что позволяет проследить изменения состояния слизистой органов в динамике.
О результатах исследования Вам сообщит врач–эндоскопист сразу же после обследования, результаты цитологического исследования будут готовы через 3-4 дня, морфологическое заключение будет готово через 8–12 дней
- Биопсия слизистой оболочки/новообразования
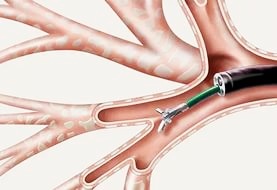
- Смыв со стенок бронхов

- Бронхоальвеолярный лаваж

Неясные изменения могут быть инфекционной, неинфекционной, злокачественной этиологии. Даже в тех случаях, когда лаваж не является диагностическим, по результатам его можно предположить диагноз, и тогда внимание врача будет сфокусировано на нужных дальнейших исследованиях. Например, даже в нормальной лаважной жидкости высока вероятность обнаружения различных нарушений. В дальнейшем бронхоальвеолярный лаваж потенциально используется в установлении степени активности заболевания, для определения прогноза и необходимой терапии.
- Санация трахеобронхиального дерева
Санация трахеобронхиального дерева — это лечебная мера, позволяющая устранить скопление слизи на пораженных бронхах. Основными задачами санационной бронхоскопии являются воздействие на характер секрета слизистых желез, улучшение дренажной функции бронхов за счет удаления секрета, проведение противовоспалительной терапии. Однократные курсы лечебной санационной бронхоскопии эффективны при пневмонии, нагноившейся кисте легкого, абсцессе легкого, а при хронической обструктивной болезни легких, хроническом обструктивном бронхите, бронхоэктазах, муковисцидозе необходимо многократное курсовое лечение.
Как правило, данное исследование хорошо переносится пациентами, но иногда возникают потеря или охриплость голоса, боль в горле, а в случае биопсии может наблюдаться кровохарканье. Эти явления носят временный характер. Вас должны насторожить длительное кровохарканье, интенсивная неослабевающая боль в груди, появление отёка на лице и вокруг шеи, тошнота и рвота, а также повышение температуры тела и озноб. При появлении указанных симптомов немедленно обратитесь к врачу.
Прохождение процедур бронхоскопии и ларингоскопии в нашем центре возможно только после предварительной записи в регистрационном журнале (см. раздел Контакты), при наличии на руках результатов КТ грудной клетки или описания рентгенограммы легких.
Бронхоскопия и ларингоскопия выполняются ИСКЛЮЧИТЕЛЬНО под местной анестезией.
На амбулаторном этапе процедура выполняется на платной основе. Оплатить исследование можно в регистратуре поликлиники центра на 1-м этаже.
Направление от других специалистов для прохождения исследования не требуется.
источник
В распознавании и дифференциальной диагностике туберкулеза, а также в определении эффективности проводимого лечения важную роль играют лабораторные методы исследования. Среди них большое значение имеют прежде всего способы обнаружения микобактерии туберкулеза в различных выделениях, воспалительных экссудатах, жидкостях и тканях организма больного.
При туберкулезе легких микобактерии находят прежде всего в мокроте. Частота, массивность и постоянство бацилловыделения зависят от формы процесса. Оно часто имеет место при инфильтративном и особенно деструктивном туберкулезе легких. Реже или периодически выделяют микобактерии больные очаговыми, диссеминированными и цирротическими формами туберкулеза без явного распада легочной ткани. Существенное значение имеет при этом состояние бронхов. При их специфическом поражении, но сохраненной дренажной функции микобактерии выявляются с мокротой сравнительно чаще и с большим постоянством, чем при нормальном состоянии бронхов или при их стенозе, вызывающем блокаду каверны.
Микобактерии туберкулеза находят в большом количестве в обильно выделяющейся мокроте, а в скудном отделяемом, наоборот, они встречаются реже и в виде единичных экземпляров. У больных, не выделяющих мокроту, лучшие результаты дает применение раздражающих аэрозольных ингаля пий 10—15% раствора поваренной соли в 1% растворе питьевой соды Н. М. Рудой и соавт. (1971) применяют с этой целью смесь, состоящую из 5 мл 10% раствора хлорида натрия, 1 мл химопсина, растворенного в физиологическом растворе, и 20 капель солутана.
Второе место по эффективности выявления бацилловыделения у больных, не выделяющих мокроту, занимает исследование промывных вод трахеи и бронхов, которое предложил Я. С. Зобин (1939). В настоящее время для анестезии гортани у взрослых применяют 0,25% раствор дикаина, разведенный в 10% растворе новокаина. Этот раствор наливают во время фонации на голосовые связки в количестве 0,5—1 мл. У больных с повышенным глоточным рефлексом этим раствором смазывают заднюю стенку глотки. Затем в трахею шприцем с напаянной канюлей вводят 10—20 мл физиологического раствора комнатной температуры.
При этом в результате раздражения слизистой оболочки бронхов возникает кашель, при котором из глубоких дыхательных путей вместе с введенной жидкостью выделяются слизь и мокрота. Это отделяемое исследуют на присутствие микобактерии туберкулеза или другой микробной флоры.
Исследование промывных вод бронхов редко сопровождается серьезными осложнениями. Только при сильном, длительном и приступообразном кашле иногда появляется кровохарканье, может аспирироваться инфекционный материал в здоровые участки легочной ткани, нарастает сердечная недостаточность. Такие явления отмечаются главным образом у больных с сопутствующей бронхиальной астмой, пороком сердца, гипертонией. В подобных случаях, очевидно, не следует прибегать к данному методу исследования. При отсутствии таких противопоказаний, особенно у больных с ограниченными формами процесса, у которых чаще всего и возникает необходимость в исследовании промывных вод бронхов, обычно не наблюдается каких-либо осложнений, и поэтому его можно производить не только в клинических, но и в амбулаторных условиях.
Менее эффективно производимое натощак исследование промывных вод желудка, в которых может содержаться бациллярная мокрота или бронхиальная слизь, чаще заглатываемая детьми, а иногда и взрослыми (Аrmand-Dellille, 1927). Кроме того, микобактерии могут проникать в желудок через его слизистую оболочку при гематогенном распространении инфекции в организме, а также при забрасывании бациоллосодержащей желчи (М. Д. Розанова, 1950). Пользоваться этим методом рекомендуется в тех случаях, когда не удается получить мокроту при раздражающих ингаляциях, при противопоказаниях к применению промывания бронхов или при невозможности их проведения по другим причинам.
Наблюдения показывают, что в промывных водах трахеи и бронхов микобактерии туберкулеза обнаруживают значительно чаще, чем в желудочном содержимом. При первом способе исследования больных туберкулезом легких, которые не выделяли мокроты, Suzuki (1951) получил положительные результаты у 31 % исследуемых, между тем как в промывных водах желудка — только у 4,7%. Castillo (1949), исследовавший промывные воды бронхов 2414 абациллярных больных, выявил микобактерии у 45,4% при ограниченных формах туберкулеза легких, у 17% — при отсутствии рентгенологических изменений в них и у 10% — субъективно здоровых «контактов».
Наименее информативно определение бацилловыделения с помощью исследований мазков слизи из гортани, а также промывания только верхних отделов дыхательных путей.
У части больных можно выделить микобактерии из крови. По наблюдениям 49 авторов, обобщенным в 1954 г. Dalencour, бациллемия отмечалась в среднем у 5,3% больных различными формами туберкулеза. П. И. Беневоленский (1945) установил ее у 3,7% больных туберкулезом легких (исключая страдающих гематогенным процессом). Чаще обнаруживают микобактерии в крови при туберкулезе кожи, обширных гематогенных диссеминациях в легких, при менингите. Однако, по сводным данным Kallos (1937). основанным на изучении гемокультур, выделенных от 14 502 больных, туберкулезная бациллемия имела место всего лишь у 1,13% из них.
Частота выявления микобактерии зависит не только от формы заболевания, метода получения материала, но и от способа его исследования (бактериоскопия, посев, заражение животных). Микобактерии туберкулеза обнаруживают при прямой бактериоскопии мазков мокроты, окрашенных по Цилю—Нельсену, при микроскопии с использованием метода обогащения — флотации и люминесцентного способа исследования. Методы обогащения повышают частоту обнаружения микобактерии туберкулеза в мокроте, промывных водах желудка и бронхов, в экссудате, спинномозговой жидкости, в каловых массах на 10—20% по сравнению с результатами прямой бактериоскопии.
Среди бактериоскопических методов выявления бацилловыделения наиболее чувствительным является люминесцентная микроскопия, повышающая возможность обнаружения в мокроте микобактерии на 15—20% по сравнению с обычной бактериоскопией, а при исследовании мазков из флотационных колец — на 8—10%. При этом облегчается изучение некоторых биологических свойств возбудителя — старения культур, аутолиза клеток и др.
Некоторые авторы утверждают, что при флюоресцентной (люминесцентной) микроскопии микобактерии туберкулеза можно выявить даже чаще, чем при посевах мокроты и других материалов на различные питательные среды. Kolbel (1955) обнаружил их при простой бактериоскопии у 39,7% больных, при бактериологическом методе — у 52,1%, а при люминесцентной микроскопии — у 73,6%. На преимущество последнего метода указывают Т. Н. Ященко и И. С. Мечева (1973), Н. С. Страхов и соавт. (1973).
Для суждения об эффективности проводимой антибактериальной терапии придают прогностическое значение уменьшению (или сохранению) в динамике массивности бацилловыделения. Поэтому целесообразно не только констатировать бацилловыделение, но и оценивать его количественный показатель. При этом при бактериоскопии бацилловыделение оценивается как обильное, если находят микобактерии в каждом поле зрения, умеренное — при наличии «единичных микробов в 40—50 полях зрения и скудное — при нахождении их единичных экземпляров в препарате.
источник
Показания к проведению исследования: воспалительные заболевания нижних отделов дыхательных путей при отсутствии мокроты.
1. Стерильный физиологический раствор.
2. Стерильный горловой шприц или аппарат Боброва.
3. Стерильный широкогорлый контейнер.
Взятие исследуемого материала:
Исследование промывных вод бронхов проводят при отсутствии или скудости мокроты. Это связано не только с технической сложностью взятия этого вида материала, но и с меньшей диагностической ценностью результата из-за значительного его разбавления (концентрация микроорганизмов в промывных водах в 10—1000 раз ниже чем в мокроте).
Простейший метод взятия трахеобронхиального смыва: гортанным шприцем с помощью аппарата Боброва в трахею вводят около 10 мл стерильного физиологического раствора, и после возникновения кашля собирают откашлянный трахеобронхиальный смыв в стерильный широкогорлый контейнер. У маленьких детей через катетер вводят в трахею 5—10 мл физиологического раствора и затем отсасывают трахеобронхиальный смыв.
Бронхиальные смывы могут быть получены при бронхоскопии. В том случае не рекомендуется вводить в бронх более 5 мл физиологического раствора.
Показания к проведению исследования: воспалительные заболевания нижних отделов дыхательных путей при отсутствии мокроты.
1. Бронхоскоп, другое оборудование и медикаменты, необходимое для проведения бронхоскопии.
2. Стерильный физиологический раствор.
3. Стерильные контейнеры и стерильные пробирки.
Взятие исследуемого материала:
С помощью бронхоскопии удается получить:
1. бронхоальвеолярный лаваж (предпочтительно);
2. смыв с бронхов (низкая чувствительность при диагностике пневмоний);
3. соскоб с бронхов (более значим, чем смыв);
Смыв с бронхов или получение бронхоальвеолярного лаважа проводят, вводя шприцем через биопсийный канал бронхоскопа отдельными порциями от 5—20 до 100 мл стерильного физиологического раствора. Перед введением каждой следующей порции отсасывают шприцом жидкость и переносят в стерильный контейнер. При этом для каждой новой порции используют новый контейнер. В дальнейшем по решению лечащего врача возможно объединение отдельных порций смыва, взятых в разных участках легких в одну. В направлении указывают общий объем введенного физиологического раствора.
Таблица 4. Некоторые специальные методы диагностики заболеваний, обусловленных отдельными пневмотропными микроорганизмами
Специальные приемы выделения возбудителя или диагностики заболевания.
Бактериоскопия мазков из обогащенной флотацией мокроты, окрашенных флюорохромом в люминесцентном микроскопе. Посев специальным образом обработанной мокроты на среду Левенштейна-Иенсена. Биопроба.
Заражение культур клеток (редко). Серодиагностика.
Индикация АГ в ИФА, выделение на элективных средах, серодиагностика.
Посев на специальные питательные среды и биопроба (редко). Серодиагностика..
Для получения соскоба с бронхов через биопсийный канал бронхоскопа вводят телескопический двойной катетер с обработанным полиэтиленгликолем (или другим соответствующим реактивом) дистальным концом для предотвращения контаминации пробы. Материал помещают в пробирку с тиогликолевой средой (средой СКС) или специальным консервантом для облигатных анаэробов.
Биоптаты доставляют в лабораторию в двух небольших пробирках (типа Эппендорф), заполненных стерильным физиологическим раствором или тиогликолевой средой.
источник
Присутствие кислотоустойчивых бактерий в клиническом диагностическом материале может быть подтверждено или микроскопией, или культуральным исследованием. Поскольку микобактерии не могут быть точно идентифицированы при микроскопическом исследовании, и поскольку существует много видов микобактерий, окончательный диагноз туберкулез или микобактериоз (за исключением лепры) может быть установлен только при выделении Mycobacterium из клинического образца.
Кратность и сроки микробиологических исследований в ходе лечения и наблюдения различных групп пациентов определены в инструкциях по химиотерапии больных туберкулезом и организации диспансерного наблюдения и учета контингентов противотуберкулезных учреждений.
Преимущества аккуратной деконтаминации проб, применения высокочувствительных питательных сред и простых схем идентификации выделенных штаммов не будут реализованы до тех пор, пока не будет обеспечено правильное взятие проб и их быстрая и правильная транспортировка в лабораторию.
Для получения оптимальных результатов при исследовании диагностического материала необходимо соблюдать следующие условия:
– сбор материала необходимо производить до начала химиотерапии, так как даже несколько дней применения лекарственной терапии может быть достаточно для того, чтобы убить значительное количество кислотоустойчивых микобактерий или снизить их жизнеспособность и исказить результаты исследования;
– материал для исследования должен собираться рано утром;
– при исследовании мокроты желательно собрать не менее 3 проб утренней мокроты в течение 3 последовательных дней. Это существенно повышает результативность исследования;
– собранный материал необходимо как можно быстрее доставить в лабораторию; в случае невозможности немедленной доставки материал сохраняется в холодильнике при 4-10°С не более 48 часов;
– при перевозке материала необходимо особенно тщательно следить за сохранностью флаконов и правильностью их маркировки.
Флаконы для сбора материала.
Материал для исследования на кислотоустойчивые микобактерии собирают в стерильные флаконы (баночки). Эти флаконы должны быть достаточно прочными, чтобы предупредить возможность их повреждения при транспортировке, и иметь широкую герметично закрывающуюся крышку, чтобы избежать вытекания материала и его загрязнения. Чтобы облегчить выбор оптимальных флаконов, необходимо помнить о следующих основных требованиях к ним:
— широкое горлышко (диаметром не менее 35 мм), чтобы больному было удобно собирать мокроту, не загрязняя наружной поверхности флакона;
— емкость флакона — около 50 мл;
— флакон должен быть из прозрачного материала, чтобы было можно определить объем пробы и ее качество, не открывая крышку;
— крышка должна быть плотно завинчивающейся или герметично закрывающейся, чтобы предотвратить вытекание потенциально опасного материала в процессе транспортировки;
— наружная поверхность не должна быть чрезмерно гладкой и скользкой, чтобы можно было легко маркировать флаконы;
— желательно использовать одноразовые флаконы, изготовленные из легкосжигаемого материала;
— при отсутствии одноразовых контейнеров можно применять толстостенные флаконы из стекла.
Поскольку наиболее частой формой туберкулезного поражения является туберкулез органов дыхания, основной материал исследования составляют мокрота; отделяемое верхних дыхательных путей, полученное после аэрозольных ингаляций; промывные воды бронхов; бронхоальвеолярные смывы; материал, получаемый при бронхоскопии, транстрахеальной и внутрилегочной биопсии; аспират из бронхов; ларингеальные мазки; экссудаты; мазки из торакальных ран; промывные воды желудка (преимущественно у детей).
Хотя M.tuberculosis могут вызывать поражение практически любого органа и любой системы, более 85% больных в странах с высокой распространенностью туберкулеза страдают легочной формой заболевания. Поэтому при проведении исследований на туберкулез основным клиническим материалом является мокрота, которую следует собирать у всех больных с подозрением на это заболевание.
Хороший клинический образец – это недавно собранная мокрота из бронхиального дерева, с минимальными примесями слюны или слизи из носоглотки. Качественным материалом можно считать мокроту, имеющую слизистый или слизисто-гнойный характер, а также содержащую плотные белесоватые включения. Желтоватый, серый или бурый цвет мокроты позволяет предположить диагностическую ценность материала. Достаточный объем исследуемой порции мокроты составляет 3 — 5 мл, однако допустимо исследование и меньших по объему порций. Некоторые больные выделяют микобактерии нерегулярно, поэтому в целях повышения информативности практикуется повторное (до 3 раз) исследование мокроты. Такая тактика позволяет повысить число положительных находок.
Необходимо, чтобы лабораторный персонал знал, как следует правильно собирать мокроту. Эта методика описана в инструкции по бактериоскопическому методу диагностики туберкулеза. Лучше всего, если пациент собирает мокроту утром до завтрака и приема лекарств (частицы пищи и лекарства могут препятствовать росту микобактерий туберкулеза). Если предполагается брать пробы мокроты для культуральной диагностики, не следует до этого момента начинать химиотерапию.
Материал для исследования должен быть доставлен в лабораторию сразу же после его сбора. Если транспортировка откладывается, то собранный материал следует обязательно хранить в холодильнике, чтобы предупредить рост контаминирующей микрофлоры.
Образцы мокроты нельзя объединять из-за риска перекрестного загрязнения материала. Всегда проводят обработку (разжижение и деконтаминацию) всей пробы, т.е. не выбирают какие-то части образца, как это обычно делают при бактериоскопическом исследовании мокроты. Так как чаще всего для культурального исследования на туберкулез в лабораторию присылают именно пробы мокроты, разработанные способы разжижения и деконтаминации рассчитаны прежде всего именно на этот биологический материал. Другие биологические жидкости и ткани требуют более тщательной обработки, так как в них обычно содержится меньшее количество микобактерий туберкулеза, чем в мокроте.
Индуцированная мокрота
Если у больного продуктивный кашель, то необходимость сбора мокроты вполне очевидна. Однако, если больной не может собрать мокроту, для получения других биологических материалов из легких можно использовать несколько специальных приемов.
Для аэрозольных ингаляций пользуются портативными или стационарными аэрозольными ингаляторами. Для ингаляций рекомендуется раствор, в 1 л которого содержится 150 г хлорида натрия (NaCl) и 10 г двууглекислого натрия (Na2CO3). Для приготовления раствора используется стерильная дистиллированная вода. Для провокации мокроты необходимо вдохнуть на протяжении 10–15 минут от 30 до 60 мл подогретой до 42–45°С смеси. В связи с тем, что аэрозольная ингаляция вызывает выделение водянистого секрета, напоминающего по консистенции слюну, во избежание выбраковки материала в бланке направления и на флаконе с материалом должна быть обязательная маркировка, указывающая на то, что материал получен после аэрозольной ингаляции.
У большинства пациентов после аэрозольной ингаляции в течение нескольких часов наблюдается остаточная гиперсекреция бронхиального отделяемого, поэтому пациенту рекомендуется в течение суток после ингаляции собрать мокроту для второго исследования.
При отсутствии мокроты, невозможности проведения аэрозольной ингаляции или безуспешности этой процедуры для исследования на микобактерии берут промывные воды бронхов или желудка.
3.2.3. Промывные воды бронхов.
Сбор промывных вод бронхов производится врачом-отоларингологом. Пациенту во время вдоха вводят шприцем в трахею 5–7 мл стерильного изотонического раствора, который вызывает кашлевой рефлекс. Вместе с изотоническим раствором откашливается секрет из глубоких отделов бронхиального дерева. Промывные воды бронхов собирают в стерильный флакон и немедленно направляют в лабораторию.
Пациентам с выраженным глоточным рефлексом указанную процедуру производят после предварительной анестезии надгортанника, гортани и задней стенки глотки.
Промывные воды желудка.
Промывные воды желудка исследуют преимущественно у детей младшего возраста, которые плохо откашливают мокроту и часто проглатывают ее. Во избежание смешивания проглоченной мокроты с пищей промывные воды желудка следует брать натощак. Последний прием пищи должен быть не менее чем за 12 часов до взятия промывных вод желудка. Перед сбором материала для нейтрализации желудочного содержимого больному дают выпить 100–150 мл раствора питьевой соды (1 чайная ложка соды на 1 стакан воды), приготовленного на стерильной дистиллированной воде для исключения возможности попадания в желудок кислотоустойчивых сапрофитов, которые могут содержаться в водопроводной воде. После этого вводят желудочный зонд и собирают содержимое желудка в стерильный флакон. Материал немедленно доставляют в лабораторию и подвергают обработке, чтобы исключить повреждающее влияние на возбудителя содержащихся в материале желудочных ферментов.
Особенно результативен метод получения промывных вод желудка в сочетании с предварительной аэрозольной ингаляцией. Промывные воды желудка следует собирать через 30 мин после аэрозольной ингаляции. Такая комбинация двух указанных методов дает значительно больший процент положительных результатов, чем каждый из них в отдельности. Этот метод получения диагностического материала может оказаться полезным также у пациентов с подавленным кашлевым рефлексом, у которых не удается получить материал даже при провоцирующих ингаляциях.
3.2.5. Другие пробы.
При внелегочных формах заболевания микобактерии могут поражать практически любой орган, поэтому для исследования пригоден самый разнообразный материал: спинномозговая, плевральная, перикардиальная, синовиальная и асцитическая жидкости, кровь, гной, пунктаты костного мозга, резецированные ткани, гнойно-некротические массы, соскобы синовиальных оболочек, биопсийный материал лимфатических узлов и др.
Если у больного заподозрена внелегочная форма туберкулеза, помимо других видов диагностического материала, желательно также исследовать и мокроту, так как это существенно повышает частоту выявления сочетанных легочных и внелегочных форм туберкулеза.
При внелегочных формах процесса можно выделить 2 группы диагностических материалов: асептически полученный материал, обычно свободный от загрязняющей сопутствующей микрофлоры, и заведомо загрязненный материал из открытых очагов поражения, в отношении которого заранее известно, что он контаминирован сопутствующей микробной флорой или собран без соблюдения правил асептики.
3.2.5.1. Асептически собранный материалчаще всего представляет собой полученные при биопсиях или оперативных вмешательствах резецированной ткани того или иного органа, гнойно-некротические массы, грануляции, соскобы синовиальных оболочек, лимфатических узлов или пунктатов их содержимого, а также плевральную, спинномозговую, синовиальную или асцитическую жидкость. Материал помещают в стерильный флакон без консервантов и немедленно доставляют в лабораторию. Если материал не может быть немедленно доставлен в лабораторию, во избежание высыхания к нему добавляют небольшое количество стерильного изотонического раствора и помещают в холодильник при 4-10°С или во флакон с сухим льдом. Биологические жидкости, а также кровь, гной и костный мозг следует брать в стерильный контейнер с соблюдением правил асептики. Если в собранной жидкости могут образоваться сгустки, то предварительно в контейнер следует внести стерильный раствор щавелевокислого натрия (из расчета 0,01–0,02 мл 10% нейтрального раствора оксалата на 1 мл образца биологической жидкости) или раствор гепарина (0,2 мл на 1 мл образца), или равный объем стерильного 3% раствора лимоннокислого натрия.
3.2.5.2.Заведомо загрязненные материалы.К этой категории относится основной и наиболее доступный при мочеполовом туберкулезе материал – моча.
3.2.5.3.1. Моча (средняя часть утренней порции или вся утренняя порция) собирается в стерильную посуду после тщательного туалета наружных половых органов. Анализ мочи на микобактерии должен предусматривать обязательное трехкратное исследование.
Сбор суточной мочи для бактериологического исследования не практикуется. Это объясняется тем, что при накоплении мочи в течение суток невозможно сохранить ее стерильность. Хранение емкости с мочой в холодном месте может привести к выпадению солей, что неблагоприятно отражается на последующей обработке осадка. Кроме того, в моче содержатся бактерицидные продукты, которые могут не только угнетать жизнеспособность микобактерий, но в течение суток даже разрушать микробные клетки. В то же время при длительном хранении мочи невозможно избежать размножения в ней контаминирующей микрофлоры. Ферменты жизнедеятельности этой флоры могут угнетать способность микобактерий к росту. И, наконец, при сборе мочи в течение длительного времени следует иметь в виду возможность попадания в нее кислотоустойчивых сапрофитов, что может привести к диагностическим ошибкам. В этом отношении особенно осторожно должны оцениваться результаты исследования мочи, полученной от мужчин, так как в ней могут обнаруживаться M.smegmatis и другие нетуберкулезные микобактерии, которые ошибочно могут быть приняты за микобактерии туберкулеза.
3.2.5.3.2. Менструальная кровь.Исследование менструальной крови требует особого методического подхода. Наличие в этом материале большого количества протеолитических, фибринолитических и других ферментов обусловливает необходимость незамедлительной доставки материала в лабораторию и тщательной его обработки. Менструальная кровь, с одной стороны, является весьма подходящим материалом для развития контаминирующей флоры, а с другой, обилие ферментов неблагоприятно влияет на жизнеспособность микобактерий. Менструальную кровь следует собирать не тампоном, а вакуумным отсосом или колпачком Кафки. Исследуют ее так же, как кровь или другие материалы с примесью крови.
3.2.5.3.3. Каловые массы собирают в стерильную посуду. Для посева небольшое количество кала (1 г) гомогенизируют в ступке с 3–5 мл дистиллированной воды, фильтруют через ватно-марлевый фильтр, центрифугируют и исследуют полученный осадок. Бактериологическое исследование кала производят редко, так как обычно положительный результат получить не удается.
3.2.5.3.4. Смывы с поверхностей. Исследование различных поверхностей применяется для контроля качества дезинфекционных мероприятий, а также при обследовании очагов туберкулезной инфекции в эпидемиологических целях. Метод основан на определении загрязненности поверхностей различных предметов микобактериями путем взятия смывов стерильным тампоном из мелкопористой поролоновой губки размером 15 мм х 15 мм х 15 мм.
При заборе материала стерильный поролоновый тампон берут стерильным пинцетом, погружают в пробирку с 5 мл 5% раствора трехзамещенного фосфорнокислого натрия, слегка отжимают о внутреннюю стенку пробирки и производят смыв с поверхности предмета, после чего тампон снова погружают в смачивающий раствор. Пинцет перед очередным смывом стерилизуют обжиганием над пламенем спиртовки.
Дата добавления: 2016-11-18 ; просмотров: 1255 | Нарушение авторских прав
источник
Забор мокроты проводится после провоцирующей отделение мокроты ингаляции. Для ингаляции рекомендуется использовать раствор, в 1 литре стерильной дистиллированной воды которого содержится 150 гр. NaCl и 10 гр Na2CO3 (двууглекислый натрий). Больной вдыхает за процедуру 30-60 мл данной смеси в течение 10-15 минут. После ингаляции усиливается отделение слюны еще до появления кашля, поэтому первую порцию слюны предлагается больному сплюнуть в специальный лоток с хлорамином, а затем собирать мокроту.
Забор промывных вод бронхов.
Промывные воды бронхов забираются у пациентов при отсутствии мокроты, невозможности проведения аэрозольной ингаляции или при безуспешности их.
Забор промывных вод бронхов осуществляет врач-отоларинголог или они забираются при проведении бронхоскопии. При этом во время вдоха вводят в трахею 5-7 мл стерильного изотонического раствора, в результате вызывается кашлевой рефлекс, и промывные воды бронхов собираются в стерильный флакон. У лиц с выраженным глоточным рефлексом при проведении процедуры рекомендуется предварительная анестезия надгортанника, гортани, задней стенки глотки.
Забор промывных вод желудка:
— промывные воды желудка забираются у детей младшего возраста, так как они плохо откашливают мокроту и проглатывают ее;
— мокрота забирается натощак, последний прием пищи должен быть не меньше, чем за 12 часов до взятия промывных вод желудка;
— больному дают выпить 100-150 мл раствора питьевой соды для нейтрализации желудочного содержимого. Для приготовления раствора питьевой соды берут 1 чайную ложку соды на 1 стакан стерильной дистиллированной, а не водопроводной воды, для исключения попадания в желудок кислотоустойчивых сапрофитов;
— больному вводят в желудок желудочный зонд и собирают содержимое желудка в специальный стерильный флакон, который быстро доставляют в лабораторию.
Имеются данные, что наиболее результативен в выявлении МБТ метод, включающий сочетание аэрозольных ингаляций с промывными водами желудка, которые должны забираться через 30 минут после ингаляции. В этом случае повышается процент положительных результатов выявления МБТ.
Забор операционного материала осуществляется в стерильные флаконы без консервантов с немедленной доставкой в лабораторию. Возможно хранение в холодильнике при температуре 4-10°С с небольшим количеством стерильного физиологического раствора или сухим льдом при невозможности быстрой доставки.
Забор анализа мочи на МБТ:
— забирается средняя утренняя порция мочи или вся утренняя порция с последующей доставкой в бактериологическую лабораторию;
— при невозможности быстрой доставки материал не должен храниться в холодильнике больше 48-72 часов, если больше, то добавляются консерванты: 2-3% раствор борной кислоты (срок хранения до 3 суток при комнатной температуре), 0,05-0,1% раствор хлоргексидина биглюконата (срок хранения 3-5 суток).
К микробиологическим методам диагностики туберкулеза относят:
4) молекулярно-биологический метод.
Из перечисленных выше, самым чувствительным методом выявления МБТ является биологический метод, его чувствительность составляет 1-5 микробных тел в 1мл исследуемого материала; на 2 месте — бактериологический метод (чувствительность — 20-100 микробных тел в 1 мл); на 3 месте – бактериоскопический метод (чувствительность более 100 тыс. и более микробных тел в 1 мл). Золотым стандартом выявления больных туберкулезом является сочетание бактериоскопического и бактериологического методов. Биологический метод более дорогой и используется в трудных диагностических случаях.
Разновидностями бактериоскопического метода являются:
— простая бактериоскопия с окраской по Цилю-Нильсену: вначале препарат обрабатывают карболовым раствором фуксина, затем обесцвечивают 5% раствором серной кислоты или 3% раствором солянокислого спирта и докрашивают 0,25% раствором метиленового синего. МБТ выглядят под микроскопом в виде красных палочек на синем фоне (приложение 2, рис. 2);
— люминесцентная микроскопия с применением флюорохромов: аурамин 00, родамин С и другие. Под люминесцентным микроскопом МБТ выглядят в виде желто-зеленых светящихся палочек на черном фоне. При использовании люминесцентной микроскопии информативность метода повышается на 30% (приложение 2, рис.3).
— метод седиментации, метод флотации повышают информативность микроскопического метода на 10%.
Бактериологический (культуральный) метод заключается в посеве мокроты на питательные среды. Стандартной питательной средой для выращивания МБТ служит твердая яичная среда Левенштейна- Йенсена. Существуют так же жидкие питательные среды (система ВАСТЕТ 460 ТВ и др.). Посевы длительно выдерживают в термостате при температуре 37-38°С. Рост колоний на твердых питательных средах происходит за 14-90 дней, на жидких -3-14 дней. Для МБТ человеческого и бычьего видов характерно образование плотных морщинистых колоний кремового цвета (приложение 2, рис. 4).
Преимущества данного метода:
— данным методом можно определить жизнеспособность культуры (способность размножаться, способность к образованию и росту колоний). Если микобактерии туберкулеза выявляются при простой микроскопии, но при посеве роста колоний не наблюдается, то это нежизнеспособные МБТ (образно говоря «микобактерии туберкулеза-трупы»);
— можно определить степень вирулентности МБТ. Быстрорастущие колонии МБТ, это, как правило, более вирулентная культура;
— можно дать количественную характеристику бактериовыделения. Если у больного выявляется при посеве от 1-20 колоний, то это свидетельствует о скудном бактериовыделении; от 21 до 100 колоний — умеренное бактериовыделение; более 100 колоний – обильное бактериовыделение.
Пациенты с обильным бактериовыделением более опасны для окружающих в плане заражения;
— можно определить чувствительность МБТ к противотуберкулезным препаратам и выявить лекарственную устойчивость. Основными методами определения лекарственной чувствительности МБТ являются методы абсолютных концентраций (применяется в России) и пропорций (применяется за рубежом). По своей информативности они равноценны. У больных туберкулезом можно выявить следующие виды лекарственной устойчивости МБТ к применяемым противотуберкулезным препаратам:
1) первичная лекарственная устойчивость – если больной вообще не принимал противотуберкулезные препараты или принимал их менее 3 недель, то есть он заразился изначально лекарственно-устойчивыми штаммами МБТ. Первичная лекарственная устойчивость характеризует состояние микобактериальной популяции на данной территории и важна для эпидемической характеристики заболеваемости;
2) вторичная лекарственная устойчивость – если больной принимал противотуберкулезные препараты более 3 недель и лекарственная устойчивость у него сформировалась в результате неэффективной и неадекватной химиотерапии;
3) множественная лекарственная устойчивость – если выявляется устойчивость как минимум к сочетанию изониазида и рифампицина, независимо от наличия или отсутствия лекарственной устойчивости к другим препаратам;
4) поливалентная лекарственная устойчивость- выявление лекарственной устойчивости к препаратам основной группы и резервным;
5) монорезистентность — выявление устойчивости к одному препарату;
6) перекрестная лекарственная устойчивость – выявление лекарственной устойчивости к препаратам одной группы по происхождению (например, группа аминогликозиды: стрептомицин, канамицин).
Важно отметить, что в последние годы отмечается рост лекарственноустойчивых форм туберкулеза среди взрослого населения.
В настоящее время за рубежом и в последние годы в России для выявления живых МБТ применяется радиометрическая система ВАСТЕТ. МБТ культивируют в жидкой питательной среде, где в качестве источника углерода используется меченая 14С пальмитиновая кислота. Преимуществом новой микробиологической методики является возможность быстрого получения результата исследования – через 12-24 дня. К недостаткам этого метода, ограничивающим возможность его широкого применения, относятся:
— высокая себестоимость исследования;
— необходимость применения радиоактивных изотопов и специального радиометрического оборудования, сложность работы с изотопной технологией;
— необходимость дополнительного посева на плотную питательную среду при возникновении проблем с идентификацией возбудителя или интерпретации результатов. Данная методика не дает качественной характеристики возбудителя и не позволяет определить лекарственную чувствительность возбудителя.
Биологический метод заключается в заражении морских свинок мокротой или другим патологическим материалом, предварительно обработанным серной кислотой для уничтожения неспецифической микрофлоры. Исследуемый материал вводится подкожно в паховую область, яичко, внутрибрюшинно. Ежедневно животному вводится кортизон для снижения иммунитета. При положительном результате через 1 месяц у животного формируется генерализованный туберкулез, животное забивают и выделенные органы исследуют макроскопически, гистологически и бактериологически. Биологический метод применяется для выявления не только типичных, но и биологически измененных форм возбудителя, в частности L- трансформированных и фильтрующихся форм.
Иммуноферментный анализ. Впервые его применил для выявления противотуберкулезных антител Е. Nassau в 1976 году. Он использовал в качестве антигена фильтрат M. tuberculosis H37Rv. Преимуществами данного метода являются:
— высокая производительность метода;
— простота в проведении анализа и регистрации результатов;
-возможность использования микроколичества диагностического
— более безопасен и экономичен по сравнению с радиоиммунологическим
— специфичность метода (частота отсутствия реакции на препарат у здоро
вых лиц) колеблется от 86-97%, чувствительность метода (частота положи
тельных ответных реакций у лиц с активной туберкулезной инфекцией) —
Молекулярно-генетические методы обнаружения М. tuberculosis основаны на полимеразной цепной реакции (ПЦР). Метод известен с 1985 года и сущность его состоит в выявлении в составе биологического материала фрагментов цепи ДНК или РНК, специфических для данного возбудителя. Для поиска возбудителя используют различный патологический материал (мокроту, промывные воды трахеи, бронхов, плевральную, спинномозговую жидкость и другие объекты). Принцип метода состоит в циклическом повторении трех стадий реакции:
1) денатурации ДНК при нагревании;
2) гибридизации искусственно синтезированных олигонуклеотидов с фланговыми участками цепей амплифицируемого фрагмента ДНК (так называемых «праймеров» или «затравочных» фрагментов);
3) синтеза (достройки) цепи фрагмента ДНК с помощью термостабильной ДНК-полимеразы. Многократное удвоение цепей ДНК (30-40 циклов) позволяет в течение нескольких часов умножить (амплифицировать) специальный участок ДНК в геометрической прогрессии, а затем идентифицировать его (при электрофорезе в агарозном геле в присутствии красителя этидия бромида синтезированный фрагмент ДНК выявляется в виде светящейся под действием ультрафиолета полосы).
— метод обладает высокой чувствительностью (теоретически можно определять единичные М. tuberculosis в образце). По сравнению с культуральными методами, при обследовании больных туберкулезом методом ПЦР число положительных результатов увеличивается на 50-70%.
— быстрота проведения анализа (1-2 дня), что чрезвычайно ценно для клинической практики.
— данный метод позволяет значительно улучшить распознавание этиологии патологического процесса у пациентов без выделения микобактерий.
— информативен при дифференциальной диагностике туберкулезного плеврита, менингита, мочеполового туберкулеза.
— эффективен в отношении возбудителей с высокой антигенной изменчивостью (в том числе L-форм), определение которых требует длительного культивирования и сложных питательных сред.
— перспективен при дифференциации М. tuberculosis и нетуберкулезных микобактерий (в том числе и после культивирования микобактерий, особенно на жидких питательных средах с использованием систем типа BACTEC).
— перспективен для быстрого определения лекарственной устойчивости и, следовательно, необходим для своевременной коррекции лечения (Gene Xpert MTB/RIF (R ) – получение результата через 90 мин, ТБ –Биочип ( HR Fq) — 24 ч, ДНК – стриповый Hain Lifescience ( HRE Fq Am/Сm)- 5ч).
— имеется возможность штаммовой идентификации, что позволяет определять внутривидовые различия возбудителя туберкулеза и представляет интерес для эпидемиологических исследований и определения роли суперинфекции при рецидивах туберкулеза.
— проблема специфичности ПЦР в диагностике туберкулеза обусловлена высоким риском ложноположительных результатов, поскольку продукты амплификации (фрагменты ДНК) легко могут попасть в исследуемые образцы и служить матрицей для новых реакций. Это определяет очень жесткие требования к технологии проведения анализов, в том числе раздельные помещения для каждой из трех стадий анализа. Проблема может быть решена за счет инактивации загрязняющих молекул специальными реагентами и совершенствования технологии подготовки клинических образцов (выделение ДНК на микропористых частицах стекла, иммуномагнитная сепарация микобактериий и пр.
— метод не позволяет определять степень жизнеспособности выявляемых микобактерий.
В связи с этим, использование методов, основанных на амплификации фрагментов генома микобактерий (ПЦР), допускается в России как дополнительный метод ускоренной дифференциальной диагностики туберкулеза для получения ориентировочных результатов при обязательном параллельном применении классических микробиологических методов.
Молекулярно-биологические методы могут проводиться в лабораториях краевых, областных и крупных городских противотуберкулезных учреждений, использующих учрежденные Минздравом России наборы реагентов (тест-системы) и имеющих лицензию на работу с микроорганизмами III-IV групп патогенности. Технология проведения ПЦР приводится в описаниях и инструкциях соответствующих наборов (тест-систем).
источник