Цель работы: ознакомление с фотометрическим методом определения нитратов в питьевой, сточной и других видах вод.
1.1. Общие сведения и характеристика метода определения нитратов
Нитраты – соли азотной кислоты, например NaNO3,KNO3, NH4NO3, Mg(NO3)2. Они являются нормальными продуктами обмена азотистых веществ любого живого организма – растительного и животного, поэтому «безнитратных» продуктов в природе не бывает.
Нитраты встречаются почти во всех видах вод. Большое количество нитратов в поверхностных и подземных водах указывает иногда на загрязнение в прошлом фекальными водами. Значительные количества нитратов содержат некоторые промышленные сточные воды. При современной технологии внесения удобрений в почву растения усваивают только 50 % их, остальные уходят со стоком. Азот поступает в почву в нескольких формах. Нитратная форма вследствие подвижности легко вымывается из почвы. Вода с повышенным содержанием нитратов — потенциальная опасность для здоровья животных и человека. Для воды питьевой (ГОСТ 2874-82) содержание нитратов (NO3) должно составлять не более 45 мг/л. Предельно допустимая концентрация (ПДК) нитратов (по азоту) в воде водоемов хозяйственно-питьевого и культурно-бытового водопользования составляет (по ЛПВ)
В производственных сточных водах, а также сельскохозяйственных водах (стоки от животноводческих ферм) содержание нитратов может достигать до 1000 мг/л. Такая сточная вода должна подвергаться очистке на сооружениях перед ее сбросом в поверхностный водоем или повторном использовании в производстве. Внесение больших доз нитратов при несбалансированности по фосфору, калию, молибдену и др. приводит к накоплению нитратов в растениях.
Определение нитратов в грунтовых водах может служить оценкой характера процессов минерализации при фильтровании воды через почвенные соли. При исследовании поверхностных вод по содержанию нитратов можно судить о протекающих процессах самоочищения, а при биологической очистке сточных вод – о процессе нитрификации.
Содержание нитратов в растениях выше 0,5 % представляет потенциальную опасность отравления животных. В кишечнике нитраты способны под действием бактерий переходить в нитриты, которые характеризуются значительной токсичностью. Они способны соединяться с гемоглобином крови вместо кислорода, переводя его в метгемоглобин, препятствующего переносу кислорода кровеносной системой. Это заболевание называется метгемоглобинемией. Поэтому для профилактики загрязнения окружающей среды, особенно в районах высоких норм применения азотных удобрений, необходимо наблюдение за составом грунтовых и поверхностных вод и содержанием в них нитратов.
Вода, забираемая в водопроводную сеть в качестве питьевой, а также для нужд производства, контролируется на содержание нитратов.
В производстве вода, используемая в водооборотных системах, также должна контролироваться на содержание нитратов. Их высокая концентрация может спровоцировать рост водорослей и микроорганизмов в трубопроводах (застойные зоны) и вторичное загрязнение циркулируемой воды в системе продуктами их жизнедеятельности и, соответственно, инициировать процессы биохимической коррозии. Кроме того, биообрастание внутри систем теплообмена снижает теплопередачу и эффективность их работы.
Разработано и применяется несколько способов определения нитратов в воде. Выбор метода зависит от концентрации нитратов и цели исследования.
Хорошие результаты даёт фотометрический метод с применением химического реагента — салицилата натрия. Интервал определяемых концентраций нитратов — 0,1-20 мг/л. Это определение основано на реакции взаимодействия нитратов с салицилатом натрия в среде концентрированной серной кислоты. При этом образуется смесь 3-нитросалициловой и 5-нитросалициловой кислот, соли которых в щелочной среде имеют жёлтую окраску. Фотометрирование желтоокрашенных растворов проводят при длине волны = 410 нм.При необходимости мешающее влияние окрашенных органических веществ устраняют предварительной обработкой пробы суспензией гидроксида алюминия и ее последующего осветления (фильтрования).
1.2. Фотометрический метод анализа
Фотоколориметрический метод анализа основан на измерении интенсивности светового потока, прошедшего через окрашенный раствор (предложен русским ученым В.М. Севергиным, 1795 г.).
Сущность анализа заключается в переводе различных исследуемых соединений (в составе газов, воды и почвы) в раствор с последующим их окрашиванием. Через окрашенный раствор пропускают световой поток и по светопоглощению такого окрашенного раствора определяют содержание окрашенного исследуемого соединения в анализируемом растворе.
Зависимость между интенсивностью окрашивания раствора и содержанием в нем окрашенного соединения может быть выражена зависимостью
| (закон Бугера-Ламберта-Бера), где, | (1) |
— интенсивность света, прошедшего через окрашенный раствор;
— интенсивность падающего света;
— коэффициент поглощения света (зависит от природы окрашенного вещества);
— концентрация окрашенного вещества в растворе;
— толщина слоя светопоглощающего раствора, см.
Если прологарифмировать уравнение (1) и изменить знаки на обратные, то уравнение примет вид:
| (2) |
— называют оптической плотностью (Д) раствора, которая прямо пропорциональна концентрации окрашенного вещества и толщине слоя раствора.
Прибор для фотоколориметрии – ФЭК (фотоэлектроколориметр).
В состав прибора КФК-2 входятLоптическая система) — источник света, светофильтры, линзы, фотоэлемент, преобразователь светового потока в электросигнал на гальванометре, гальванометр, кюветодержатель, ручки (чувствительность и длина волны), набор кювет для растворов.
2. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
2.1. Устройство и принцип работы фотоэлектроколориметра (КФК-2)
КФК-2 является однолучевым прибором и предназначен для измерения коэффициентов пропускания (в диапазоне длин волн 315-980 нм) и абсорбционности растворов. Пределы измерения коэффициентов пропускания от 100 до 5 % .
На рис. 1 приведена оптическая схема КФК-2.
Рис. 1 Оптическая схема КФК-2
1 — лампа накаливания ; 2 — конденсоры; 3 — диафрагма; 4,5 — объективы; 6,7,8 – светофильтры; 9,11 – защитные стекла ; 10 – кювета с раствором; 12 – фотодиод ; 13 – светофильтр ; 14 – делительная пластина ;15 – фотоэлемент.
Колориметр включают в сеть за 15 минут до начала измерений (кюветное отделение открыто).
Кюветы установленного размера подготавливают к работе следующим образом: рабочие поверхности кювет протирают обезжиривающей смесью. После каждого определения на приборе, кюветы промывают от рабочей смеси дистиллированной водой не менее трех раз и тщательно протирают фильтровальной бумагой.
В приборе КФК используют для измерения две кюветы. Одна – с «холостой» пробой и вторая – для анализа исследуемой пробы. Измерение оптической плотности начинают с «холостой» пробы (Д1), после нее измеряют оптическую плотность окрашенного исследуемого раствора (Д2). Разница между показаниями фиксируется в виде показателя Д – светопропускания. Данная величина будет расти по мере увеличения разницы концентраций «холостой» и контрольной пробами. Графическая зависимость оптической плотности (светопропускания) Д от концентрации анализируемого соединения называется калибровочным графиком. На нем принято указывать дату калибрования на приборе, чувствительность, светофильтр, размер кюветы для раствора.
На приборе левой ручкой устанавливают заданную измерением длину волны (светофильтр), а верхней правой — минимальную чувствительность прибора. В кюветодержатель прибора вставляют кювету с «холостой» пробой (дистиллированная вода + реактивы для определения анализируемого вещества), закрывают крышку кюветного отделения и ручками «чувствительность», «установка 100», «грубо» и «точно» устанавливают ноль по шкале абсорбционности (Д – оптическая плотность). Поворотом ручки кюветодержателя (снизу) кювету с «холостой» пробой заменяют на кювету с рабочим окрашенным раствором. Снимают отсчет по шкале микроамперметра. Измерения одной пробы проводят не менее 3-х раз и окончательное значение измеренной абсорбционности определяют как среднее арифметическое из полученных значений.
2.2. Методика проведения работы
2.2.1. Построение калибровочного графика.
Используя рабочий раствор нитрата калия, согласно таблице 1 готовят серию стандартных растворов, содержащих NO3. Рабочий раствор KNO3 содержит 10 мг/л . Для этого в мерные колбы на 50 мл вносят определенное количество рабочего раствора и доводят дистиллированной водой до метки.
Растворы для приготовления шкалы стандартов при определении
| № колбы | Количество рабочего раствора, мл | Содержание , мг/л |
| 1. | ||
| 2. | 0,2 | |
| 3. | 0,4 | |
| 4. | 0,6 | |
| 5. | 1,0 | |
| 6. | 2,0 | |
| 7. | 3,0 | |
| 8. | 4,0 | |
| 9. | 5,0 | |
| 10. | 6,0 | |
| 11. | 7,0 | |
| 12. | 8,0 | |
| 13. |
В фарфоровые чашки отбирают пробы по 20 мл с различным содержанием NO3, добавляют по 2 мл салицилата натрия и выпаривают на песчаной бане досуха. Затем охлаждают чашки с осадком, добавляют в них по 2 мл концентрированной серной кислоты и оставляют на 10 минут. По истечении этого времени в чашки приливают 15 мл дистиллированной воды, 15 мл раствора едкого натра и сегнетовой соли. Внимание. Реагенты приливать в указанном порядке! Далее полученную смесь количественно переносят в мерные колбы ёмкостью 50 мл, обмывая стенки чашек дистиллированной водой, колбы охлаждают до комнатной температуры.
После охлаждения доводят объём дистиллированной водой до метки и измеряют оптическую плотность растворов при длине 410 нм (фиолетовый фильтр) в кюветах толщиной слоя 5 см. Измерение нужно проводить не позднее, чем через 10 мин. после приливания гидрооксида натрия, в противном случае окраска раствора изменяется.
Для построения калибровочного графика можно сократить количество замеров (колб с пробами) до 4-5 штук.
Калибровочный график строят в координатах: оптическая плотность Д – концентрация нитрат-ионов ( )
2.2.2. Определение нитратов в пробах воды
Проводят анализ проб воды различных источников (по заданию преподавателя).
Перед началом работы необходимо внимательно осмотреть пробу. Если очевидно, что в ней присутствуют окрашенные органические соединения, необходимо отобрать 150 мл пробы, прибавить к ней 3 мл суспензии гидроксида алюминия. После тщательного перемешивания пробу воды отстаивают, затем фильтруют, отбрасывая первые порции фильтрата.
Затем отбирают 20 мл фильтрата и анализируют пробу как указано выше (см. п. 2.2.1.).
Параллельно проводят холостую пробу с 20 мл дистиллированной воды. Результаты анализов заносят в таблицу 2.
2.3. Обработка результатов эксперимента
Обработка результатов измерений ведется МНК с использованием ПЭВМ и представляется в графическом виде (см. рисунок 1) с указанием ошибки в определении ( ).
По полученным данным строится график зависимости оптической плотности Д от концентрации нитратов в пробах (шкала стандартов). На графике приводят данные по условиям анализа (номер светофильтра, толщина кюветы, чувствительность и дату выполнения калибровочного графика).
Рис.2. Калибровочный график
По оптической плотности анализируемых проб воды на калибровочном графике находят содержание нитратов в растворе. По найденным значениям рассчитывают содержание нитрат-ионов в исследуемых пробах (мг/л):
,
где С – концентрация нитрат-ионов, найденная по калибровочной кривой, мг/л;
V – объём пробы, взятой для анализа, мл.
Результаты анализа и расчета концентрации нитратов в пробах воды приводят в таблицу 2.
Результаты анализа воды различного происхождения
| № п/п | Образец пробы воды | Оптическая плотность, Д | Концентрация нитратов, , мг/л |
| Вода водопроводная сырая | |||
| Вода водопроводная кипяченая | |||
| Сточная вода НПЗ | |||
| Сточная вода химкомбината |
1. Построить калибровочный график.
2. Провести анализ проб воды различных источников (по заданию преподавателя).
3. На основании результатов анализа сделать вывод о качестве воды и ее пригодности для целевого использования (питьевое снабжение, водооборотная система производства, сброс в поверхностный водоем).
1. Опасно ли использовать воду как питьевую, если в ней содержание нитратов 35 мг/л?
2. Устройство и принцип работы фотоэлектроколориметра.
3. Теоретические основы колориметрии.
4. Принцип построения калибровочного графика. Точность определения анализируемого компонента.
5. С каким содержанием нитратов (после сооружений очистки сточных вод) можно сбрасывать очищенную сточную воду в поверхностный водоем?
6. Почему вводят ограничения на содержание в воде нитратов?
1. Перед работой ознакомиться с устройством и принципом работы фотоэлектроколориметра (КФК).
2. Всю работу с фарфоровыми чашками проводить только в вытяжном шкафу при включенной тяге.
3. С реактивами работать в резиновых перчатках.
4. Отбор серной кислоты проводить под тягой с помощью пипетки.
5. Реагенты приливать в строго указанном порядке.
6. По окончании работы вымыть руки с мылом.
ОПРЕДЕЛЕНИЕ ФОСФАТОВ В ПРИРОДНОЙ И СТОЧНОЙ ВОДЕ
В сточных водах, как и в природных водах, фосфор может присутствовать в различных видах. В жидкой фазе анализируемой воды он может быть в виде ортофосфорной кислоты и её ионов ( ), в виде мета-, пиро- и полифосфатов органических соединений (нуклеиновых кислот, нуклеопротеиды, фосфоролипиды и др.)
При взаимодействии ортофосфат-ионов с молибдатом в кислой среде образуется жёлтая гетерополикислота, которая под действием восстановителей превращается в интенсивно окрашенное синее соединение. Восстановление можно проводить оловом или аскорбиновой кислотой.
Восстановление аскорбиновой кислотой, сравнительно слабым восстановителем, происходит только при повышенной температуре, т.е. в условиях, когда полифосфат и органические эфиры фосфорной кислоты гидролизуются с образованием ортофосфорной кислоты. Для ускорения реакции при комнатной температуре и интенсификации окраски вводят соль сурьмы (антимонилтартрат калия – КSbH4O6·0,5H2O).
Мешающие вещества. Сильнокислые и сильнощелочные пробы предварительно нейтрализуют. Определению мешают сульфиды и Н2S, в концентрации, превышающих 3 мг/л. Мешающие влиянию можно устранить, прибавляя несколько мг КMnО4 на 100 мл пробы и встряхивая 1-2 мин; раствор должен быть розовым. Затем прибавляют требуемые для определения реактивы, но в обратном порядке: сначала раствор аскорбиновой кислоты, перемешивают и вливают раствор молибтана.
Для устранения влияния нитритов вводят сульфаминовой кислоты, которую вводят в состав применяемого реактива. При большом содержании железа следует ввести эквивалентное количество ЭДТА.
2. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Концентрацию фосфатов определяем в питьевой и сточной воде.
К 50 мл пробы, профильтрованной в день отбора через мембранный фильтр № 1 или через плотный бумажный фильтр (синяя лента), приливают 2 мл смешанного раствора через короткое время – 0,5 мл раствора аскорбиновой кислоты (в присутствии мешающих веществ, реактивы приливают в обратном порядке). Смесь перемешивают. Одновременно проводят холостое определение с 50 мл дистиллированной воды. Через 15 мин (20 мин.) определяют оптическую плотность. Измерение проводят при = 800 нм или при максимально возможном для данного прибора значении.
Содержание растворённых неорганических фосфатов (мг/л) ( ) определяют по формуле:
где С – концентрация фосфатов, определённая по калибровочной кривой, мг/л;
V – объём пробы, взятой для анализа, мл.
В диапазоне концентраций до 1 мг/л результаты округляют до сотых долей мг/л, свыше 1 мг/л – до десятых долей мг/л.
Построение калибровочного графика
Берут 0; 1,0; 2,5; 5,0…..50,0 мл рабочего стандартного раствора 2 фосфата калия, разбавляют каждый раствор до 50 мл дистиллированной Н2О и далее продолжают, как в ходе определения (общее содержание растворённых ортофосфатов, найденных экспериментально, выражают в мг/л ).
Измеряют оптическую плотность и строят график зависимости оптической плотности от концентрации ионов фосфорной кислоты.
Построение калибровочной кривой.
| Реактивы | Номер мерной колбы | |||||
| Количество ст. раствора 2, мл | 1,0 | 2,5 | 5,0 | 10,0 | ||
| Количество дист. Н2О, мл | 49,0 | 47,5 | 45,0 | 40,0 | 25,0 | |
| Содержание , мг/л | 0,02 | 0,05 | 0,1 | 0,2 | 0,5 | 1,0 |
1. Построить калибровочную кривую в диапазоне 0-1 мг/л (табл.1).
2. Провести определение фосфата в водопроводной воде (сравнить данные с ГОСТ на воду питьевую).
3. Рассчитать и построить калибровочную кривую на содержание фосфатов до 50 мг/л.
4. Провести определение содержание в пробе сточной воды (с учётом мешающего влияния отдельных компонентов сточной воды).
Давление насыщенного водяного пара
при температурах от 10 до 39 °С
| , °C | , мм.рт.ст. | , °C | , мм.рт.ст. | , °C | , мм.рт.ст. |
| 9.2 9.8 10.5 11.2 12.0 12.8 13.6 14.5 15.5 16.5 | 17.5 18.7 19.8 21.1 22.4 23.8 25.2 26.7 28.3 30.0 | 31.8 33.7 35.7 37.7 39.9 42.2 44.6 47.1 49.7 52.4 |
| Формула | Плотность, г/см 3 | Формула | Плотность, г/см 3 | Формула | Плотность, г/см 3 |
| Al Be Cd Co Cr Cu Fe | 2.70 1.85 8.64 8.80 7.16 8.93 7.86 | Mg Mn Mo Nb Ni Pb Si | 1.74 7.30 10.23 8.56 8.90 11.34 2.00 | Sn Ta Ti V W Zn Zr | 7.30 16.60 4.54 6.11 19.3 7.14 6.50 |
Десятибалльная шкала коррозионной стойкости металлов
| Группа стойкости | Скорость коррозии металла, мм/год | Балл |
| Совершенно стойкие Весьма стойкие Стойкие Пониженно-стойкие Малостойкие Нестойкие | Менее 0,001 Свыше 0,001 до 0,005 Свыше 0,005 до 0,01 Свыше 0,01 до 0,05 Свыше 0,05 до 0,1 Свыше 0,1 до 0,5 Свыше 0,5 до 1,0 Свыше 1,0 до 5,0 Свыше 5,0 до 10,0 Свыше 10,0 |
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Для студентов недели бывают четные, нечетные и зачетные. 9360 — 

195.133.146.119 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
источник
Со временем даже собственная скважина или колодец может стать причиной отравления жителей дома. Одна из самых распространенных причин ухудшения самочувствия жильцов – нитраты в воде, которые поступают в источник из водоносных пластов. Результат их действия на организм губителен. Наблюдается головокружение, рвота, слабость, головная боль и т.д. Причем попасть в воду нитраты могут из разных источников загрязнения.
Главная причина появления этих соединения в водоносных пластах – применение селитры в качестве удобрений в сельском хозяйстве. В этом случае человек сталкивается с солями азотной кислоты, которые растворяются в воде, и грунт естественным образом не может препятствовать их протеканию в колодец или скважину.
Есть и другие причины, по которым процентное содержание нитратов в жидкости превышает установленные нормы:
- Близость скоплений бытовых отходов и фекалий. В данном случае соединения образуются в результате распада органических отходов. Септик, баня, туалет, выгребная яма – потенциальные источники опасности.
- Слив отработанной моющей жидкости. Применение чистящих и моющих средств предполагает утилизацию грязной воды. Если она сливается в непосредственной близости от колодца или скважины, содержание нитратов резко возрастает.
- Массовые захоронения, и не только кладбища, являются источником проблемы, так как при разложении тканей животных образуются вредные вещества, способные нанести непоправимый урон организму человека.
В любом случае, выявить проблему поможет специализированная экспертиза и анализ контрольных проб. Заключения выдают специализированные санитарно-эпидемологические лаборатории. И как только проблема будет выявлена, нужно немедленно приступить к ее ликвидации.
Наличие нитратных загрязнений – не повод отказаться от использования источника. Если обнаружены нитраты в скважине, что делать подскажут сотрудники лаборатории, когда будут выдавать заключение.
Определение нитратов в воде в домашних условиях:
Еще один способ – воспользоваться рекомендациями, опубликованными далее. Все существует 2 способа решить проблему, которые достаточно эффективны, чтобы дать жильцам дома чистую питьевую воду.
Суть методики – перекачка жидкости через установку со специальной мембраной, удерживающей загрязнения. При этом молекулы воды беспрепятственно проходят сквозь нее, а удерживаются только нежелательные примеси. Способ нашел применение в промышленности и может применяться в домашних условиях.
Сама мембрана также требует периодической очистки, которую выполняют с применением перекрестного течения. С одной стороны напор направляет жидкость на мембрану для фильтрации. С другой – струя омывает саму мембрану, удаляя примеси. Чтобы направить жидкость в обратном направлении, потребуется специальная помпа.
Метод отличается эффективностью, но и не лишен недостатков:
- Требуется предварительная очистка механическим способом, чтобы удалить из скважинной или колодезной воды песок, глину, ил и другие твердые нерастворимые частицы.
- Очистка предполагает удаление всех имеющихся солей, включая те, которые приносят организму человека пользу. Если скважина артезианская, вода утратит свои целебные свойства.
- Стоимость нельзя назвать низкой. Для выхода из ситуации используют небольшие фильтрационные установки, производительности которых достаточно, чтобы перерабатывать воду для питья и приготовления пищи.
В любом случае жидкость, фильтруемая таким образом, будет лишена вредных примесей, которые содержатся в водном растворе.
Чтобы извлечь из раствора отрицательно заряженные частицы нитран-ионов используются селективные смолы. Очистка предполагает протекание химической реакции с применением специальных составов и веществ. Метод сложен тем, что необходимо заботиться о своевременной регенерации смолы, ионы которой замещаются ионами нитратов. Поэтому данный способ применяется крайне редко, тем более, что для этого требуется специальная установка, требующая обслуживания.
По нормам, принятым в Евросоюзе, нитратов не может содержаться в количестве, большем 50 мг/дм3.
А в соответствии с регламентом СанПин максимальный порог снижен до 45. Но есть еще более вредные примеси, которые являются производными нитрат-соединений. Их не может содержаться свыше 0,2 мг/дм3. Это критическая отметка, которая является критерием необходимости использования улавливающих станций.
источник
Химическое обозначение: NO — 3
Синонимы: селитры, азот нитратов, нитратный азот, нитрат-ион.
Азот нитратов или нитратный азот не является полным синонимом нитрат-иона. Дело в том, что в случае нитратного азота концентрация пересчитывается именно на азот. Нитраты в составе имеют один атом азота и три атома кислорода, поэтому массовая концентрация нитрат-ионов не совпадает с массовой концентрацией нитратного азота. Для пересчёта используются следующие формулы:
Концентрация нитратного азота = 0,225 ⋅ Концентрация нитрат-иона
Концентрация нитрат-иона = 4,428 ⋅ Концентрация нитратного азота
Описание: анионы сильной минеральной азотной кислоты. В сочетании с катионом (натрием, калием, кальцием, магнием и т.д.) образуют соли (нитраты натрия, нитраты калия, нитраты кальция, нитраты магния и т.д.). Нитраты практически всех катионов отлично растворяются в воде — это обуславливает их способность перемещаться с грунтовыми водами и загрязнять открытые источники водоснабжения, такие как колодцы, родники и открытые водохранилища на расстояниях до нескольких десятков километров.
Методы определения: потенциометрия, ионная хроматография, и спектрофотометрия.
Методики, используемые в Испытательном центре МГУ для определения концентрации нитрат-иона в природных средах
| Нормативный документ на методику | Метод определения | Оборудование |
|---|---|---|
| Вода | ||
| ПНД Ф 14.1:2:4.132 | ионная хроматография | DIONEX ICS-2000 |
| Почва | ||
| ПНД Ф 16.1.8-98 | ионная хроматография | DIONEX ICS-2000 |
| ГОСТ 26488-85 | спектрофотометрия | Hach Lange DR 2800 |
Контроль измерений проводят на оборудовании: UNICO 2100.
Распространённость: нитраты являются одними из основных соединений азота, который, будучи биогенным элементом, широко распространён в биосфере. Нитраты — это промежуточная стадия трансформации азота, поэтому данные соединения присутствуют во всех природных водах, попадая туда в процессе окисления и трансформации органического вещества. Повышенное содержание нитратов в воде сопряжено с активным применением этой формы азота в качестве минерального удобрения при выращивании практически всех агрономически ценных культур (овощи, зерновые, лен, хлопок и так далее).
Несмотря на то, что азот сам по себе важен и необходим для любого живого организма, нитратная его форма не играет положительной роли в организме человека. Поэтому в вашей питьевой воде по возможности нитратов быть не должно.
Нитраты не играют положительной биологической роли в организме человека.
Повышенное содержание нитратов в воде говорит о смещении баланса цикла азота и о возможном развитии процессов эвтрофикации водоёма. Также рост концентрации нитратов служит индикатором снижения содержания в воде растворённого кислорода — это особенно актуально для владельцев аквариумов. Поливная вода, в свою очередь, может (а в некоторых случаях даже должна) содержать в себе нитратный азот для обеспечения роста и развития растений.
Предельно допустимая концентрация (ПДК) нитрат-иона в различных водных объектах
| Нормирование | ПДК, мг/л |
|---|---|
| Бутилированная вода первой категории СанПиН 2.1.4.1116-02 | 0–20 |
| Бутилированная вода высшей категории СанПиН 2.1.4.1116-02 | 0–5 |
| Вода систем централизованного водоснабжения СанПиН 2.1.4.1074-01 | 0–45 |
| Водные объекты рыбохозяйственного значения Приказ Минсельхоза РФ № 552 | 0–40 |
| Объекты рекреационного водопользования СанПиН 2.1.5.980-00 | — |
| Вода плавательных бассейнов СанПиН 2.1.2.1188-03 | — |
| Хозяйственно-бытовые стоки Постановление Правительства РФ № 644 | — |
| Ливневые стоки Постановление Правительства РФ № 644 | — |
Опасность для организма представляют не сами нитраты, а продукты их трансформации: нитриты и нитрозамины. Нитратный азот в пищеварительном тракте и полости рта трансформируется в нитритный под действием фермента нитратредуктазы. В присутствии, например, мяса, активно образуются нитрозамины. Образование продуктов уменьшается при попадании нитратов в организм совместно с веществами, обладающими антиоксидантными свойствами — например, с витамином С.
Через нитриты и при поступлении отдельно от мясной пищи: они окисляются до оксида азота, который поступает в кровь, приводит к расширению сосудов и нормализации кровяного давления.
При метаболизме до нитритов:
- увеличение риска развития рака желудка;
- образование метгемоглобина, не способного переносить кислород (кислородное голодание) (особенно опасно для грудных детей);
- трансформация в нитрозамины.
При метаболизме до нитрозаминов:
- обладают высокой общей токсичностью;
- характеризуются канцерогенным действием (способствуют возникновению рака);
- в отдельных случаях, приводят к коме;
- поражают выделительную систему (включая печень и почки).
Ионный обмен. В результате использования ионообменных смол (специфических анионитов) в воде происходит замена нитратов на хлориды. Поскольку нитраты не имеют положительной роли их можно убирать из воды полностью. Этот метод мало распространён, т.е. применяется редко, поскольку аниониты распространены меньше, чем катиониты (смолы для фильтрации катионов).
Обратный осмос. Вместе с другими веществами обратный осмос убирает из воды нитраты. Этот метод используется чаще остальных для очистки воды от нитратов. При использовании реминерализатора убедитесь, что соли в нем не содержат нитраты.
Нитраты относится к веществам, которые характеризуются отрицательным влиянием на организм человека, поэтому необходимо контролировать содержание нитратов в питьевой воде. В связи с особенностями метаболизма, наибольшую опасность нитраты представляют для грудных детей и пожилых людей.
источник
Нитраты — это соли азотной кислоты, наличие которых, как правило, вызвано поступлением в источник водоснабжения хозяйственно-бытовых и промышленных стоков, а также стоков с сельскохозяйственных угодий, обрабатываемых азотосодержащими удобрениями.
В последние годы появляется все больше информации о глобальном распространении нитратов как в воде и почве, так и в продуктах питания и о пагубном воздействии нитратов на здоровье человека.
Превышение концентрации нитратов наиболее часто наблюдается в воде из колодцев, неглубоких скважин, рек и озер, поэтому при использовании воды из поверхностных и неглубоких подземных источников рекомендуется сделать анализ воды на нитраты.
Опасность нитратов обусловлена их токсичным действием на организм.
Различают первичную токсичность нитратов, вторичную — возникающую при образовании нитритов, и третичную — связанную с образованием нитрозаминов.
Накапливаясь в организме человека, нитраты вызывают метгемоглобинемию, то есть реагируют с гемоглобином крови, образуя метгемоглобин. Это вещество в отличие от гемоглобина не переносит кислород, что приводит к кислородному голоданию тканей. В результате ухудшается самочувствие, появляется вялость.
Нитраты губительно воздействуют на нервную, сердечно-сосудистую систему, желудочно-кишечный тракт и другие органы. Особую опасность нитраты представляют для маленьких детей, у которых еще не сформирована восстанавливающая ферментная система.
По этим причинам необходимо ограничивать поступление нитратов в организм — минимизировать потребление нитратсодержащих продуктов и не употреблять воду с повышенной концентрацией нитратов.
Содержание нитратов в питьевой воде регламентируется СанПиН 2.1.4.10749-01 «Питьевая вода. Гигиенические требования к качеству воды» и не должно превышать 45 мг/л.
В случае, если в Вашей исходной воде наблюдается повышенное содержание нитратов, необходима ее очистка.
На сегодняшний момент наиболее широкое распространение получили два метода удаления нитратов из воды:
- с помощью установок обратного осмоса
- специальными фильтрами с селективными анионными ионообменными материалами.
Иногда для удаления нитрат-ионов могут использоваться ионообменные смолы — универсальные сильноосновные аниониты, но, в подавляющем большинстве случаев, требуется применение специальных нитратселективных анионитов. Физическая суть данного метода сводится к замещению нитрат-ионом аниона смолы, как правило, хлорид-иона с последующей регенерацией материала раствором хлорида натрия (поваренной соли). Это обуславливает особенности и ограничения при использовании данного метода.
Ионообменная смола характеризуется ограниченной емкостью — тем количеством анионов, которое она может на себя принять, обеспечивая необходимую степень очистки воды. При полном насыщении смолы дальнейшее удаление извлекаемых ионов прекращается. При использовании стандартной сильноосновной смолы и присутствии в исходной воде сульфатов может даже наблюдаться выброс нитратов в очищенную воду при исчерпании ресурса фильтра. Это обусловлено большим сродством стандартной сильноосновной смолы к сульфатам, чем к нитратам, что ведет к вытеснению задержанных нитрат-ионов сульфат-ионами из смолы.
В случае выброса нитратов из фильтра, их концентрация в воде может достигать очень высоких значений, представляющих серьезную опасность для здоровья, при этом определить подобное превышение без анализа воды потребитель не может. По этой причине удаление нитратов с помощью ионных фильтров не рекомендуется для частных домов, где отсутствует возможность организации постоянного контроля за качеством очищенной воды.
Очистка воды от нитратов с помощью обратного осмоса является более надежным вариантом. Вода под давлением подается на полупроницаемую мембрану. Нитраты и другие примеси задерживаются мембраной, а к потребителю поступает очищенная вода. Степень извлечения примесей определяется селективностью мембраны. В зависимости от модели мембраны и конструкции установки обратного осмоса удаление нитратов может достигать до 96%.
В случае использования установок обратного осмоса качество очистки остается стабильным даже при значительном изменении состава исходной воды. Помимо удаления нитратов, установки обратного осмоса будут справляться с задачами по очистке воды от большого спектра загрязнений (железо, марганец, цветность и т. д).
Частое выявление присутствия нитратов в высоких концентрациях в источниках водоснабжения частных домов позволяет констатировать, что очистка воды от нитрат-ионов все чаще является насущной необходимостью. Для очистки воды от нитратов оптимальным решением является обратный осмос.
По всем вопросам очистки воды обращайтесь к нам — опытные специалисты по водоподготовке проконсультируют Вас по любой проблеме, связанной с водой для Вашего дома.
Для консультации с нашими специалистами позвоните нам или отправьте заявку
источник
Вряд ли найдётся человек, который бы не слышал о вреде нитратов. Мы привыкли думать, что основную опасность в плане содержания нитратов представляют ранние и несезонные овощи и фрукты. Но нитраты в питьевой воде – довольно распространённое явление. Откуда они там берутся, существует ли допустимая норма нитратов в воде и как обезопасить себя – узнаете из нашей статьи.
Для начала давайте выясним – что же такое нитраты и как они могут попасть в воду. Это соли азотной кислоты, которые могут оказывать токсичное воздействие на организм. Нитраты в воде, как правило, являются результатом попадания в источники водоснабжения стоков промышленных предприятий или азотосодержащих удобрений с полей.
Многие люди думают, что вода из скважины или колодца априори чище и здоровее той, что течёт из крана. Это далеко не так. Специалисты отмечают, что при анализе воды на нитраты, довольно часто бракуют как раз пробы воды из колодцев и скважин небольшой глубины. Также в зоне риска и поверхностные источники (реки, озёра). Причина этого заключается, в первую очередь, в использовании большого количества азотосодержащих удобрений и неразумной хозяйственной деятельности (например, когда колодец находится недалеко от места стоков с полей). Нитраты попадают в почву, а оттуда в грунтовые воды, а из них – в скважины и колодцы.
Если содержание нитратов в питьевой воде превышено, то её употребление может иметь довольно серьёзные последствия для здоровья. По статистике ВОЗ, во всём мире в результате отравления нитратами в воде умирает 3, 5 млн. человек. Подавляющее большинство из них (около 90%) –это дети до пяти лет. Именно поэтому нужно уделять внимание качеству питьевой воды, особенно, если в семье есть маленькие дети.
Чем же опасны нитраты в питьевой воде? При единоразовом попадании в организм большой дозы нитратов, они могут вызвать серьёзное отравление, вплоть до летального исхода (особенно у детей раннего возраста). Но даже если последствия отравления нитратами в воде вы заметили не сразу, накапливаясь в организме, они могут привести к развитию серьёзных заболеваний.
- Онкологические заболевания (в частности, желудочно-кишечного тракта).
- Нарушение работы поджелудочной и щитовидной железы
- Сердечная недостаточность
- Заболевания почек
- Заболевания сердечно-сосудистой системы
Накапливаясь в организме, нитраты провоцируют так называемую метгемоглобинемию. При этом заболевании гемоглобин в крови замещается метгемоглобином, который не выполняет функцию переноса кислорода. Это ведёт к таким серьёзным последствиям как кислородное голодание, резко ухудшается состояние здоровья.
Учитывая опасность попадания нитратов в организм, актуальным становится вопрос, сколько нитратов может содержаться в воде, чтобы она не представляла опасности для здоровья. Этот параметр регулируется Государственными санитарными нормами. Согласно гигиеническим требованиям к качеству питьевой воды, содержание в ней нитратов не должно превышать 50 мг/л.
Определение нитратов в воде лучше провести, отдав её на анализ в лабораторию. Конечно, существуют и специальные тест-полоски, которые можно использовать в домашних условиях. Но если вы хотите получить точную исчерпывающую информацию, то лучше обратится к специалистам. Кроме того, у вас будет возможность провести сравнительный анализ воды сразу из нескольких источников.
После того, как проведено определение нитратов в воде, и результаты показали превышение нормы, необходимо решать проблему как можно скорее. Очистку воды от нитратов можно эффективно провести при помощи фильтра обратного осмоса. Но проблема в том, что зачастую нитраты в воде обнаруживаются именно в колодцах и скважинах. Тут наладить систему фильтрации сложнее, но всё же возможно. Для этого можно использовать насос и фильтровать уже ту воду, которую он качает. Если же возможности наладить очистку нет, то безопаснее перестать пользоваться водой из данного источника.
Если в качестве источника водоснабжения вы используете скважину и колодец важно не забывать о простых правилах профилактики, которые помогут минимизировать или исключить содержание нитратов в питьевой воде.
- Размещайте колодец как можно дальше от уборной и хозяйственных построек.
- Не разбивайте грядки вблизи источника водоснабжения
- Правильно используйте удобрения на участке, не допускайте их «передозировки».
- Организуйте над колодцем крышку или навес – это поможет избежать механических загрязнений.
Соблюдая эти простые правила, вы защитите воду от загрязнения и сохраните своё здоровье.
источник
Фотометрический метод определения массовой концентрации нитрат-иона основан на взаимодействии нитрат-ионов с салициловой кислотой с образованием желтого комплексного соединения.
Настоящая методика обеспечивает получение результатов анализа с погрешностью, не превышающей значений, приведенных в таблице 1.
Диапазон измерений, значения показателей точности, повторяемости и воспроизводимости
Показатель точности (границы относительной погрешности при вероятности Р = 0,95), ± d , %
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости) s r, %
Показатель воспроизводимости (относительное среднеквадратическое отклонение воспроизводимости), s R, %
Значения показателя точности методики используют при:
— оформлении результатов анализа, выдаваемых лабораторией;
— оценке деятельности лабораторий на качество проведения испытаний;
— оценке возможности использования результатов анализа при реализации методики в конкретной лаборатории.
Спектрофотометр или фотоэлектроколориметр, позволяющие измерять светопоглощение при значениях l = 410 нм.
ГСО c аттестованным содержанием нитрат-ионов.
Кюветы кварцевые с толщиной поглощающего слоя 20 мм.
Весы лабораторные, 2 кл. точности ГОСТ 24104.
Колбы мерные наливные 2-50-2
ПНД Ф 14.1:2.4-95 G ) Внесены дополнения и изменения согласно протоколу № 23 заседания НТК ФГУ «ЦЭКА» МПР России от 30 мая 2001 г.
Стаканчики для взвешивания СВ ГОСТ 25336.
Стаканы термостойкие В-1-1000
Пробирки колориметрические П-2-10-0,1 ХС ГОСТ 1770.
3.2 . Вспомогательное оборудование, материалы
Сушильный шкаф электрический ОСТ 16.0.801.397.
Чашки выпарительные фарфоровые ГОСТ 9147.
Фильтры обеззоленные ТУ 6-09-1678.
Бутыли из стекла или полиэтилена с притертыми или винтовыми пробками вместимостью 500 — 1000 см 3 для отбора и хранения проб.
Активированный уголь БАУ-Э, ТУ 6-16-3075.
Натрий салициловокислый ГОСТ 17628 G ) .
ПНД Ф 14.1:2.4-95 G ) Внесены дополнения и изменения согласно протоколу № 23 заседания НТК ФГУ «ЦЭКА» МПР России от 30 мая 2001 г.
Калий-натрий виннокислый 4-водный (Сегнетова соль) ГОСТ 5845.
Серебро сернокислое ТУ 6-09-3703.
Все реактивы должны быть квалификации х.ч. или ч.д.а. и не содержать примесей нитрат-ионов.
4.1 . При выполнении анализов необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007 .
4.2 . Электробезопасность при работе с электроустановками по ГОСТ 12.1.019 .
4.3 . Организация обучения работающих безопасности труда по ГОСТ 12.0.004 .
4.4 . Помещение лаборатории должно соответствовать пожарной безопасности по ГОСТ 12.1.004 и иметь средства пожаротушения по ГОСТ 12.4.009 .
Выполнение измерений может производить химик-аналитик, владеющий техникой фотометрического и спектрофотометрического анализов, изучивший инструкцию по работе с соответствующими приборами.
Измерения проводятся в следующих условиях:
температура окружающего воздуха (20 ± 5) °С;
относительная влажность (80 ± 5) %;
атмосферное давление (84 — 106) кПа (630 — 800 мм рт.ст.);
частота переменного тока (50 ± 1) Гц;
напряжение в сети (220 ± 10) В.
7.1 . Подготовка посуды для отбора проб
Бутыли для отбора и хранения проб воды обезжиривают раствором CMC, промывают водопроводной водой, хромовой смесью, опять водопроводной водой, а затем 3 — 4 раза дистиллированной водой.
Отбор проб производится в соответствии с требованиями ГОСТ Р 51592-2000 «Вода. Общие требования к отбору проб». G )
ПНД Ф 14.1:2.4-95 G ) Внесены дополнения и изменения согласно протоколу № 23 заседания НТК ФГУ «ЦЭКА» МПР России от 30 мая 2001 г.
Пробы воды (объем не менее 200 см 3 ) отбирают в стеклянные или полиэтиленовые бутыли, предварительно ополоснутые отбираемой водой.
Если определение нитратов производят в день отбора пробы, то консервирование не требуется.
Если проба не будет проанализирована в день отбора, то ее консервируют добавлением концентрированной серной кислоты (на 1 дм 3 воды — 1 см 3 H 2 SO 4 конц.). Консервированная проба может храниться не более 2 суток при температуре (3 — 4) °С.
Проба воды не должна подвергаться воздействию прямого солнечного света. Для доставки в лабораторию сосуды с пробами упаковывают в тару, обеспечивающую сохранность и предохраняющую от резких перепадов температуры. При отборе проб составляют сопроводительный документ по утвержденной форме, в котором указывают:
— цель анализа, предполагаемые загрязнители;
— должность, фамилия отбирающего пробу, дата.
7.3 . Подготовка прибора к работе
Подготовку спектрофотометра или фотоэлектроколориметра к работе проводят в соответствии с рабочей инструкцией по эксплуатации прибора.
7.4 . Освобождение от мешающих влияний
1. Взвешенные, окрашен. органические вещества. Железо(> 5 мг/дм 3 )
К 150 см 3 пробы добавить 3 см 3 гидроксида алюминия, пробу перемешивают, дают отстояться и фильтруют через фильтр «белая лента», отбрасывая первую порцию фильтрата.
В ходе анализа добавляют сернокислое серебро в количестве, эквивалентном содержанию хлорид-иона. Осадок хлорида серебра отфильтровывают через фильтр «белая лента».
К 20 см 3 пробы добавляют 0,05 г сернокислого аммония и упаривают досуха на водяной бане, доводят до первоначального объема дистиллированной водой.
Основной раствор нитрат-ионов.
Навеску (0,1631 г) калия азотнокислого, предварительно высушенного при 105 °С, помещают в стакан вместимостью 100 см 3 , растворяют в 50 см 3 дистиллированной воды, переносят в мерную колбу вместимостью 1000 см 3 и доводят до метки дистиллированной водой.
1 см 3 содержит 0,1 мг нитрат-ионов. Раствор устойчив в течение 3 мес.
При наличии ГСО: раствор готовят в соответствии с прилагаемой к образцу инструкцией.
1 см 3 раствора должен содержать 0,1 мг нитрат-ионов.
Рабочий раствор нитрат-ионов.
10 ,0 см 3 основного раствора нитрат-ионов переносят в мерную колбу на 100 см 3 и доводят до метки дистиллированной водой.
1 см 3 раствора содержит 0,01 мг нитрат-ионов. Раствор готовят в день проведения анализа.
Раствор гидроксида натрия и сегнетовой соли.
400 г гидроксида натрия и 60 г сегнетовой соли помещают в стакан вместимостью 1000 см 3 , растворяют в 500 см 3 дистиллированной воды, охлаждают, переносят в мерную колбу вместимостью 1000 см 3 G ) и доводят до метки дистиллированной водой G ) .
ПНД Ф 14.1:2.4-95 G ) Внесены дополнения и изменения согласно протоколу № 23 заседания НТК ФГУ «ЦЭКА» МПР России от 30 мая 2001 г.
Раствор салициловой кислоты (о-гидроксибензойной).
Навеску (1,0 г) салициловой кислоты помещают в стакан вместимостью 100 см 3 , растворяют в 50 см 3 этилового спирта, переносят в мерную колбу вместимостью 100 см 3 , доводят до метки этиловым спиртом. Раствор готовят в день использования.
Навеску (0,5 г) натрия салициловокислого растворяют в 100 см 3 дистиллированной воды. Раствор готовят в день использования G ) .
ПНД Ф 14.1:2.4-95 G ) Внесены дополнения и изменения согласно протоколу № 23 заседания НТК ФГУ «ЦЭКА» МПР России от 30 мая 2001 г.
Суспензия гидроксида алюминия.
125 г алюмоаммонийных или алюмокалиевых квасцов растворяют в 1 дм 3 дистиллированной воды, раствор нагревают до 60 °С и медленно при непрерывном перемешивании прибавляют 55 см 3 концентрированного раствора аммиака. Дают смеси отстояться около 1 часа, фильтруют и промывают осадок гидроксида алюминия многократной декантацией дистиллированной водой до полного удаления свободного аммиака.
7.6 . Приготовление градуировочных растворов
В ряд колориметрических пробирок на 10 см 3 отбирают последовательно пипеткой 0,1; 0,5; 1,0; 2,0; 4,0; 6,0; 10,0 см 3 рабочего раствора нитрат-иона (0,01 мг/см 3 ) и доводят дистиллированной водой до метки. G ) Содержание нитрат-ионов в растворах соответственно равно 0,1; 0,5; 1,0; 2,0; 4,0; 6,0; 10,0 мг/дм 3 G ) .
ПНД Ф 14.1:2.4-95 G ) Внесены дополнения и изменения согласно протоколу № 23 заседания НТК ФГУ «ЦЭКА» МПР России от 30 мая 2001 г.
Растворы переносят в фарфоровые чашки, добавляют 2 см 3 раствора салициловой кислоты (или 2 см 3 раствора натрия салициловокислого) и выпаривают в фарфоровой чашке на водяной бане досуха. После охлаждения сухой остаток смешивают с 2 см 3 серной кислоты и оставляют на 10 мин. Затем содержимое чашки разбавляют 10 — 15 см 3 дистиллированной воды, приливают приблизительно 15 см 3 раствора гидроксида натрия и сегнетовой соли, переносят в мерную колбу вместимостью 50 см 3 , смывая стенки чашки дистиллированной водой, охлаждают колбу в холодной воде до комнатной температуры, доводят дистиллированной водой до метки и полученный окрашенный раствор сразу фотометрируют при l = 410 нм в кюветах с толщиной поглощающего слоя 20 мм. Одновременно с обработкой градуировочных растворов проводят «холостой опыт» с дистиллированной водой, который используют в качестве раствора сравнения.
Градуировочный график строят методом наименьших квадратов в координатах: А — оптическая плотность; С — концентрация нитрат-ионов в градуировочном растворе (мг/дм 3 ).
7.7 . Контроль стабильности градуировочной характеристики
Контроль стабильности градуировочной характеристики проводят не реже одного раза в квартал или при смене партий реактивов. Средствами контроля являются вновь приготовленные образцы для градуировки (не менее 3 образцов из приведенных в п. 7.6).
Градуировочную характеристику считают стабильной при выполнении для каждого образца для градуировки следующего условия:
где Х — результат контрольного измерения массовой концентрации нитрат-ионов в образце для градуировки;
С — аттестованное значение массовой концентрации нитрат-ионов;
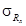
Примечание . Допустимо среднеквадратическое отклонение внутрилабораторной прецизионности при внедрении методики в лаборатории устанавливать на основе выражения: 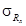
Значения s R приведены в таблице 1.
Если условие стабильности градуировочной характеристики не выполняется только для одного образца для градуировки, необходимо выполнить повторное измерение этого образца с целью исключения результата, содержащего грубую погрешность.
Если градуировочная характеристика нестабильна, выясняют причины и повторяют контроль с использованием других образцов для градуировки, предусмотренных методикой. При повторном обнаружении нестабильности градуировочной характеристики строят новый градуировочный график.
Пробу объемом 150 см 3 обрабатывают как указано в п. 7.4. Для анализа используют фильтрат. Его объем может составлять 5,0 — 10 см 3 в зависимости от концентрации нитрат-ионов в воде. Далее поступают, как описано в пункте 7.6. При анализе пробы воды выполняют не менее двух параллельных определений.
Содержание нитрат-ионов, X , мг/дм 3 вычисляют по формуле:
где С — содержание нитрат-ионов, найденное по графику, мг/дм 3 ;
V — объем исследуемой пробы, взятой на анализ, дм 3 .
За результат анализа Хср принимают среднее арифметическое значение двух параллельных определений Х1 и X 2
для которых выполняется следующее условие:
где r — предел повторяемости, значения которого приведены в таблице 2.
Значения предела повторяемости при вероятности Р = 0,95
Предел повторяемости (относительное значение допускаемого расхождения между двумя результатами параллельных определений), r, %
источник
Ценность воды в жизнедеятельности человека неоспорима. Наличие централизованного водоснабжения частично решает насущную проблему ее повсеместного загрязнения. Вода из крана проходит первичную очистку, для улучшения качества в квартирах устанавливают различные фильтры. А если обнаружены нитраты в воде из скважины, что делать? Для начала стоит разобраться во вредном влиянии нитратов на здоровье и источниках их поступления в воду. Также расскажем, как бороться с возникшей проблемой.
Нитратами именуют производные соли азотной кислоты. Своему широкому применению они обязаны селитре, которая активно задействована при возделывании сельскохозяйственных культур в качестве удобрения. Дешевизна химиката и эффективное влияние на рост и созревание растений зачастую приводят к его передозировке. Как результат – препарат вместе с осадками проникает в грунтовые воды, после чего вода попадает в колодец или скважину.
Существуют и другие причины, из-за которых в скважине или колодце находится вода с нитратами с превышенным уровнем допустимых норм. Источником заражения выступают:
- Недопустимо близкое соседство скважины с частным туалетом, септиком, баней или выгребной ямой.
- Применение бытовой химии, после чего раствор воды сливают в грунт поблизости скважины.
- Обустройство скважины неподалеку от массовых захоронений.
- Завышенная концентрация удобрений для роста огородных культур.
Нитраты входят в 3 класс опасности, по нормам Евросоюза их содержание не должно превышать 50 мг/дм 3 , регламент СанПин установил предел в 45 мг/дм 3 . Еще большую опасность для здоровья представляют производные нитратов – нитриты. Химическое соединение относится ко 2 классу опасности, уровень содержания примесей по директивам Евросоюза и СанПин не должно превышать 0,5 и 3,0 мг/дм 3 соответственно.
Употребление пищи, приготовленной на воде из скважины, и банальное питье – не единственный способ попадания в организм нитратов. Вредное соединение способно проникнуть через кожу в процессе принятия ванны. Поэтому рекомендуется регулярно следить за качеством воды из скважины.
Находясь в организме, нитраты взаимодействуют с гемоглобином. В результате химической реакции гемоглобин в крови человека замещается метгемоглобином. Новое соединение не способно насытить клетки тела необходимым кислородом, что вызывает ряд негативных последствий.
Кислородное голодание сопровождается рядом неприятных симптомов:
- развивается анемия;
- человека сопровождает постоянное чувство усталости;
- длительное воздействие нитратов в дозах, значительно превосходящих нормы, провоцирует обмороки и в крайних случаях заканчивается летальным исходом.
Кроме этого, регулярное употребление воды из скважины, в которой содержание нитратов выше установленных значений, может спровоцировать:
- развитие злокачественных образований;
- появление аллергических реакций;
- всевозможные раздражения на поверхности кожи и слизистых оболочках;
- оказывать угнетающее действие на функционирование щитовидной железы;
- нарушить работу нервной системы;
- проблемы с ЖКТ.
Еще большую опасность представляют нитраты в воде из скважины для здоровья младенцев и детей, не достигших подросткового возраста. Допустимые показатели содержания в организме нитратов для малышей в 4 раза меньше, нежели для взрослого человека.
Но спешить отказываться от пользования водой из скважины при обнаружении в ней вредных веществ, включая нитраты, не стоит. Учеными разработано два эффективных способа, как сделать воду из скважины пригодной для питья. Это ионный обмен и обратный осмос. Рассмотрим подробно, в чем заключается принцип действия обоих способов.
Очистка воды из скважины с применением обратного осмоса считается чрезвычайно эффективным процессом. Принцип действия основан на перегонке загрязненной воды через полупроницаемую мембрану. Устройство успешно задерживает вредные примеси, свободно пропуская молекулы воды.
Мембраны обратного осмоса для обработки воды из скважины представлены различными видами. Для самой очистки мембраны применяется перекрестное течение. С одной стороны, вода направляется через мембрану по дальнейшему пути водопровода. С другой – вода движется обратно и очищает саму мембрану.
Для обеспечения движения воды из скважины через мембрану в обратном направлении применяется помпа. Важным элементом в процедуре обратного осмоса при удалении из воды нитратов является ограничитель течения. На устройство возложена функция контроля над перекрестным течением. Ограничитель отслеживает объем воды, очищенной от нитратов и количество поступившей жидкости в систему канализации.
Помимо достоинств, способ очистки воды из скважины с применением обратного осмоса обладает рядом негативных моментов:
- Перед поступлением на мембрану, вода из скважины с содержанием нитратов нуждается в предварительной механической очистке.
- Очистительный процесс касается всех примесей, и не только вредных. Поэтому вода со скважины лишается всех солей и минералов в целом. Такая глубокая и неразборчивая очистка нивелируют пользу от употребления воды из скважины.
- Применение обратного осмоса с целью удаления из воды нитратов – занятие дорогостоящее. Целесообразно стать обладателем компактной установки, очищающей воду для питья и приготовления пищи. Для бытовых нужд вполне приемлемо пользоваться водой с содержанием нитратов.
Перед приобретением устройства обратного осмоса стоит взвесить все выигрышные и негативные стороны, чтобы понять целесообразность выбора.
Метод основывается на химическом процессе, когда вредные ионы воды из скважины замещаются полезными частицами. Нитраты, растворенные в жидкости, представлены нитрат-анионами, то есть элементами с отрицательным зарядом. Чтобы удалить их из жидкости, применяют селективные смолы, которым свойственны анионообменные функции. Подобная смола извлекает из воды исключительно ионы нитратов.
Если рассматривать смолу на уровне молекул, она представлена активным ядром с плюсовым зарядом, по краям которого движутся ионы со слабым отрицательным зарядом. Когда вода из скважины пропускается через смолу, происходит процесс замены ионов смолы с минусовым зарядом на ионы нитратов.
Перед окончательным решением остановиться на каком-либо из двух предложенных способов очистки от нитратов воды, необходимо организовать два мероприятия:
- Провести санитарное обследование скважины, с целью определения источника загрязнения. Если он будет установлен, по возможности нейтрализовать или ослабить его воздействие.
- Сдать воду из скважины в лабораторию для проведения бактериологических и химических анализов.
Проведенные исследования дадут основание для выбора того или иного способа. Первоначально выявить в воде содержание нитратов помогут химические тестеры одноразового действия или специальные приборы, именуемые нитратомерами. Большая точность и удобство применения свойственна электронным аппаратам. Всего за несколько секунд потребитель получит информацию с минимальным уровнем погрешности.
источник


