Если вам скажут, что проточная вода может не содержать железа, не верьте. Металл попадает в колодцы и скважины из растворенных горных пород (их частицы содержатся в грунте), из сточных вод сельскохозяйственных и промышленных предприятий, накапливается при прохождении жидкости через центральную систему водоснабжения (состояние труб зачастую оставляет желать лучшего). В такой ситуации анализ воды на железо становится насущной необходимостью.
При этом ВОЗ до сих пор не установила рекомендованных норм: по мнению ученых, железо не окажет негативного влияния на здоровье человека, даже если злоупотреблять «насыщенной» водой. Допустимый порог (0,3 мг/л) был обозначен СанПином на основании вкусовых, а не медицинских показателей.
Это интересно: в организме взрослого человека содержится около 5 граммов железа, которое входит в состав гемоглобина, миоглобина и различных ферментов. Без этого элемента невозможен нормальный процесс кроветворения. Часть железа «складирована» в печени и селезенке – этот резерв используется в случае истощения организма.
В воде содержится одно или несколько соединений железа:
- Двухвалентное (растворенное);
- Трехвалентное (в состоянии взвеси);
- Органическое (соединенное с другими веществами);
- Бактериальное (продукт жизнедеятельности некоторых микроорганизмов);
- Коллоидное (с микроскопическими частицами).
Наличие «добавок» не всегда видно невооруженным глазом, зачастую выявить проблему может только экспресс-анализ воды на железо.
Определить наличие примеси можно самостоятельно. Первый тревожный звоночек – появление ярко выраженного металлического привкуса (при сильном превышении нормы этот вкус ощущается даже в кофе или чае). На стенках посуды и поверхности сантехники проступает желтоватый или рыжий налет, который сложно оттереть без абразивных средств. Белое белье после стирки приобретает грязноватый оттенок, а цветное быстро теряет яркость красок. При этом внешний вид воды может вовсе не вызывать подозрений.
Важно! Если вы обустроили скважину или колодец на участке, сделать анализ воды на железо нужно через 2-3 недели после начала ее эксплуатации. Впоследствии процедуру можно проводить раз в 2 года (либо при изменении цвета или вкуса воды).
Первичный анализ воды на железо в домашних условиях можно провести несколькими способами:
- Смешать 25 мл воды и по 1 мл сульфосалициловой кислоты, аммиака и нашатырного спирта. Если через 15-20 минут раствор окрасится в ярко-желтый цвет, в нем есть примесь железа.
- Смешать слабый раствор марганцовки с пробой воды. Тревожный «звоночек» – изменение цвета на желтовато-бурый оттенок.
- Использовать экспресс-анализ воды на железо («набор аквариумиста»). Смешайте реагент с пробами жидкости по инструкции и определите степень загрязнения по интенсивности цвета.
- Трехвалентное железо можно выявить простой процедурой – отстаиванием воды. Железо вступает в реакцию с кислородом и выпадает в виде красновато-бурого осадка.
Более подробный анализ воды на железо (общее либо двухвалентное) можно сделать в аккредитованных лабораториях. В идеале эту процедуру нужно проводить на месте – при транспортировке может начаться процесс окисления, что исказит результаты. Если такой возможности нет, нужно провести забор проб по всем правилам:
- Используйте чистую пластиковую или стеклянную посуду объемом не менее 1,5 литра (можно взять бутылку от негазированной минералки).
- Наполняйте емкость до самого верха и тщательно закручивайте пробку, чтобы перекрыть доступ воздуха.
- Доставьте образцы в течение 2 часов. Этот срок критичен при выявлении ионов железа – именно они влияют на образование накипи.
Анализ на общее железо выявляет остаток металла в воде (то, что остается после реакции элемента с кислородом). Именно этот осадок отвечает за ржавые потеки на сантехнике и желтоватый налет на посуде.
В воде из скважин и колодцев чаще всего выявляется двухвалентное (растворенное) железо. Избавиться от него можно с помощью довольно сложной системы фильтров. На входе устанавливают ионообменные картриджи, в которых происходит процесс окисления металла и образование твердого осадка. Получившийся «песок» собирается в фильтре (картриджи нужно периодически менять). Более дорогая и эффективная система – фильтры с обратным осмосом – под высоким давлением прогоняет загрязненную воду через специальные мембраны, а все загрязнения и отходы утилизирует в канализацию.
От трехвалентного железа можно избавиться с помощью аэратора – открытого резервуара, в котором отстаивается вода. Для ускорения процесса окисления жидкость насыщают кислородом при помощи компрессора. Простым аналогом системы может стать обычное ведро: наберите воду, а через сутки аккуратно слейте примерно две трети.
Для бытовой очистки воды можно использовать активированный уголь. Заверните таблетки в вату и пропустите жидкость сквозь импровизированный фильтр.
Важно! Не забывайте, что домашние процедуры очистки могут носить лишь временный характер. Чтобы не подвергать здоровье риску, своевременно проводите анализ воды на железо и используйте профессиональные системы фильтрации.
источник
Железо является характерным элементом природных вод зоны избыточного увлажнения. На территории этой природной зоны расположены города Центральной части России, Сибири и Дальнего Востока. В подземных водах Москвы и Московской области содержание железа превышает значение ПДК практически повсеместно.
Железо – один из самых распространенных элементов в природе. Его содержание в земной коре составляет около 4,7 % по массе, поэтому железо, с точки зрения его распространенности в природе, принято называть макроэлементом. Известно свыше 300 минералов, содержащих соединения железа. Среди них – магнитный железняк альфа FеО(ОН), бурый железняк Fе3О4*Н2О, гематит (красный железняк) и другие. Главными источниками соединений железа в поверхностных водах являются процессы химического выветривания горных пород, сопровождающиеся их механическим разрушением и растворением. В процессе взаимодействия с содержащимися в природных водах минеральными и органическими веществами образуется сложный комплекс соединений железа, находящихся в воде в растворенном, коллоидном и взвешенном состояниях. Значительные количества железа поступают с подземным стоком и со сточными водами предприятий металлургической, металлообрабатывающей, текстильной, лакокрасочной промышленности и сельскохозяйственными стоками.
Железо является жизненно важным микроэлементом для животных и растений, то есть элементом, необходимым для жизнедеятельности живых организмов в малых количествах. В организме человека железо входит в состав важнейших в биологическом отношении органических соединений – гемоглобина крови и ряда ферментов. Около 70% железа, содержащегося в организме человека, входит в состав гемоглобина. Основным физиологическим назначением железа является участие в процессе кроветворения.
В природных водах вода может содержать железо в разных формах. Чаще всего встречается двух- и трех- валентное железо. Чистая, прозрачная вода, изливающаяся из скважины, постояв некоторое время на воздухе, буквально на глазах начинает мутнеть, приобретая характерную рыжевато-бурую окраску. Это происходит потому, что соединения двухвалентного железа, вступив в контакт с кислородом воздуха, окисляются и переходят в нерастворимую форму трехвалентного железа — осадок, называемый ржавчиной. Содержание железа в воде выше 1-2 мг Fe /дм 3 значительно ухудшает органолептические свойства, придавая ей неприятный вяжущий вкус, и делает воду малопригодной для использования даже в технических целях. ПДК железа составляет 0,3 мг Fe /дм 3 (лимитирующий показатель вредности – органолептический).
Ржавчина очень часто встречается в водопроводной воде. Одна из основных причин — устаревшие системы водоснабжения. Пройдя очистку на муниципальных водопроводных очистных сооружениях, вода обычно содержит небольшое количество железа, укладывающиеся в медицинские нормы, но проходя до конечного потребителя через многие километры труб распределительной водопроводной сети, она подвергается вторичному загрязнению, растворяя продукты коррозии стальных труб.
В результате на выходе мы вновь имеем «железистую» воду с желтоватым оттенком. Насыщенная соединениями железа вода имеет не только неприятный вид. Она портит запорную арматуру, оставляет ржавые подтеки на керамических поверхностях сантехники. Кроме того, медиками доказано, что вода с повышенным содержанием железа (свыше 0,3 мг/л) приводит к заболеваниям печени, увеличивает риск инфарктов, негативно влияет на репродуктивную функцию организма, а также служит причиной появления аллергических реакций.
Повышенное содержание железа в воде создает благоприятные условия для развития железобактерий, особенно в подогретой воде. Эти микроорганизмы образуют ветвящиеся колонии, которые осложняют работу гидротехнических сооружений. Продукты жизнедеятельности железобактерий являются канцерогенами. Железообрастания внутри труб – идеальная среда для развития кишечной палочки, гнилостных бактерий, различных других микроорганизмов. Все это ухудшает химические и бактериологические показатели воды.
В природных водах может присутствовать двухвалентное (закисное) или трехвалентное (окисное) железо. Наиболее часто в воде подземных источников железо встречается в виде бикарбоната закиси железа Fe(HCO3)2, то есть двууглекислого железа. Из подземных вод двухвалентное железо может быть устранено при помощи аэрации воды. Надо отметить, что двууглекислое железо в воде частично гидролизуется, теряя углекислоту. Гидрат закиси железа Fe(OH)2, соединяясь с кислородом, превращается в коллоидную гидроокись железа Fe(OH)3, которая при коагулировании переходит в окись железа Fe2O33H2O, выпадающую в виде бурых хлопьев. Поэтому после аэрации нужно пропускать воду через контактные резервуары и фильтры.
Если в воде содержится сернокислое железо FeSO4, то при аэрации такой воды ее обезжелезивание не достигается, так как при гидролизе растворенной соли железа образуется угольная кислота, понижающая рН воды до величины, меньшей 6,8, при которой гидролиз почти прекращается. Поэтому из воды СО2 удаляется путем ее предварительного известкования, после которого необходимы отстаивание и фильтрование воды.
Чтобы установить наиболее экономичный для данной воды способ обезжелезивания, надо произвести пробное удаление железа. Обезжелезивание воды для хозяйственно-питьевых нужд производят при содержании в исходной воде железа в количестве более 0,3 мг/л, при этом специальные установки предусматриваются только в тех случаях, когда железо не может быть удалено попутно при обработке воды на других очистных сооружениях.
Для того, чтобы решить, какой именно способ обезжелезнивания воды необходим именно вам, нужно понять, в каких формах железо представлено в вашей воде. Для этого рекомендуется обратиться к специалистам-аналитикам, а также профессионалам водоподготовки. Все эти вопросы находятся в компетенции лаборатории MSU LAB.
источник
ГОСУДАРСТВЕННЫЙ СТАНДАРТ СОЮЗА ССР
Методы измерения массовой концентрации
Methods for determination
Настоящий стандарт распространяется на питьевую воду и устанавливает колориметрические методы измерения массовой концентрации общего железа.
1.1. Пробы воды отбирают по ГОСТ 2874 и ГОСТ 24481.
1.2. Объем пробы воды для измерения массовой концентрации железа должен быть не менее 200 см 3 .
1.3. Способы консервирования, сроки и условия хранения проб воды, предназначенных для измерения массовой концентрации общего железа, — по ГОСТ 24481.
(Измененная редакция, Изм. № 2).
Метод основан на взаимодействии ионов железа в щелочной среде с сульфосалициловой кислотой с образованием окрашенного в желтый цвет комплексного соединения. Интенсивность окраски, пропорциональную массовой концентрации железа, измеряют при длине волны 400-430 нм. Диапазон измерения массовой концентрации общего железа без разбавления пробы 0,10-2,00 мг/дм 3 . В этом интервале суммарная погрешность измерения с вероятностью Р=0,95 находится в пределах 0,01-0,03 мг/дм 3 .
Фотоколориметр любого типа с фиолетовым светофильтром ( 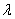
Кюветы с толщиной рабочего слоя 2-5 см.
Весы аналитические лабораторные, класс точности 1, 2 по ГОСТ 24104.
Колбы мерные 2-го класса, вместимостью 50, 100, 1000 см 3 по ГОСТ 1770.
Пипетки мерные без делений вместимостью 50 см 3 и пипетки мерные с ценой наименьшего деления 0,1-0,05 см 3 , вместимостью 1, 5 и 10 см 3 2-го класса по нормативно-техническому документу.
Колбы стеклянные лабораторные конические номинальной вместимостью 100 см 3 , типа Кн по ГОСТ 25336.
Аммоний хлористый по ГОСТ 3773.
Аммиак водный по ГОСТ 3760, 25 %-ный раствор.
Квасцы железоаммонийные по нормативно-техническому документу.
Кислота соляная по ГОСТ 3118.
Кислота сульфосалициловая по ГОСТ 4478.
Вода дистиллированная по ГОСТ 6709.
Все реактивы, используемые для анализа, должны быть квалификации химически чистые (х. ч.) или чистые для анализа (ч.д.а).
2.3.1. Приготовление основного стандартного раствора железо-аммонийных квасцов
0,8636 г железоаммонийных квасцов FeNH 4 ( SO 4 )2 × 12 H 2 O взвешивают с точностью, не превышающей 0,0002 г по шкале весов, растворяют в мерной колбе вместимостью 1 дм 3 в небольшом количестве дистиллированной воды, добавляют 2,00 см 3 соляной кислоты плотностью 1,19 г/см 3 и доводят до метки дистиллированной водой. 1 см 3 раствора содержит 0.1 мг железа.
Срок и условия хранения раствора — по ГОСТ 4212.
2.3.2. Приготовление рабочего стандартного раствора железоаммонийных квасцов
Рабочий раствор готовят в день проведения анализа разбавлением основного раствора в 20 раз. 1 см 3 раствора содержит 0,005 мг железа.
2.3.3. Приготовление раствора сульфосалициловой кислоты
20 г сульфосалициловой кислоты растворяют в мерной колбе вместимостью 100 см 3 в небольшом количестве дистиллированной воды и доводят этой водой до метки.
2.3.4. Приготовление раствора хлористого аммония молярной концентрации 2 моль/дм 3
107 г NH 4 Cl растворяют в мерной колбе вместимостью 1 дм 3 в небольшом количестве дистиллированной воды и доводят этой водой до метки.
2.3.5. Приготовление раствора аммиака (1:1)
100 см 3 25 %-ного раствора аммиака приливают к 100 см 3 дистиллированной воды и перемешивают.
При массовой концентрации общего железа не более 2,00 мг/дм 3 отбирают 50 см 3 исследуемой воды (при большей массовой концентрации железа пробу разбавляют дистиллированной водой) и помещают в коническую колбу вместимостью 100 см 3 . Если проба при отборе не консервировалась кислотой, то к 50 см 3 добавляют 0,20 см 3 соляной кислоты плотностью 1,19 г/см 3 . Пробу воды нагревают до кипения и упаривают до объема 35-40 см 3 . Раствор охлаждают до комнатной температуры, переносят в мерную колбу вместимостью 50 см 3 , ополаскивают 2-3 раза по 1 см 3 дистиллированной водой, сливая эти порции в ту же мерную колбу. Затем к полученному раствору прибавляют 1,00 см 3 хлористого аммония, 1,00 см 3 сульфосалициловой кислоты, 1,00 см 3 раствора аммиака (1:1), тщательно перемешивая после добавления каждого реактива. По индикаторной бумаге определяют значение рН раствора, которое должно быть 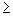
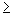
Объем раствора в мерной колбе доводят до метки дистиллированной водой, оставляют стоять 5 мин для развития окраски. Измеряют оптическую плотность окрашенных растворов, используя фиолетовый светофильтр ( 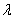
Для построения градуировочного графика в ряд мерных колб вместимостью 50 см 3 наливают 0,0; 1,0; 2,0; 5,0. 10,0; 15,0; 20,0 см 3 рабочего стандартного раствора, доводят до метки дистиллированной водой, перемешивают и анализируют, как исследуемую воду. Получают шкалу растворов, соответствующих массовым концентрациям железа 0,0; 0,1; 0,2; 0,5; 1,0; 1,5; 2,0 мг/дм 3 .
Строят градуировочный график, откладывая по оси абсцисс массовую концентрацию железа, а по оси ординат — соответствующие значения оптической плотности. Построение градуировочного графика повторяют для каждой партии реактивов и не реже одного раза в квартал.
Массовую концентрацию железа (X) в анализируемой пробе, мг/дм 3 с учетом разбавления вычисляют по формуле
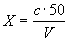
где с — концентрация железа, найденная по градуировочному графику, мг/дм 3 ;
V — объем воды, взятый для анализа, см 3 ;
50 — объем, до которого разбавлена проба, см 3 .
За окончательный результат анализа принимают среднее арифметическое результатов двух параллельных измерений, допустимое расхождение между которыми не должно превышать 25 % при массовой концентрации железа на уровне предельно допустимой. Результат округляют до двух значащих цифр.
Сходимость результатов анализа ( А) в процентах вычисляют по формуле
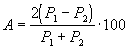
где Р1 — больший результат из двух параллельных измерений;
Р 2 — меньший результат из двух параллельных измерений.
Разд. 2. (Измененная редакция, Изм. № 2).
Метод основан на реакции ортофенантролина с ионами двухвалентного железа в области рН 3-9 с образованием комплексного соединения, окрашенного в оранжево-красный цвет. Интенсивность окраски пропорциональна концентрации железа. Восстановление железа до двухвалентного проводится в кислой среде гидроксиламином. Окраска развивается быстро при рН 3,0-3,5 в присутствии избытка фенантролина и устойчива в течение нескольких дней. Диапазон измерения массовой концентрации общего железа без разбавления пробы 0,05-2,0 мг/дм 3 . В этом интервале суммарная погрешность измерения с вероятностью Р = 0,95 находится в пределах 0,01-0,02 мг/дм 3 .
(Измененная редакция, Изм. № 2).
3.2. Аппаратура, материалы и реактивы
Фотоэлектроколориметр различных марок.
Кюветы с толщиной рабочего слоя 2-5 см.
Колбы мерные 2-го класса точности по ГОСТ 1770, вместимостью 50 и 1000 см 3 .
Пипетки мерные без делений, вместимостью 10, 25 и 50 см 3 и пипетки мерные с делениями 0,1-0,01 см 3 вместимостью 1, 2 и 5 см 3 2-го класса точности по нормативно-техническому документу.
Колбы плоскодонные по ГОСТ 25336, вместимостью 150-200 см 3 .
Аммоний уксуснокислый по ГОСТ 3117.
Гидроксиламин солянокислый по ГОСТ 5456.
Квасцы железоаммонийные по нормативно-техническому документу.
Кислота соляная по ГОСТ 3118.
Кислота уксусная по ГОСТ 61.
Вода дистиллированная по ГОСТ 6709.
Аммиак водный по ГОСТ 3760, 25 %-ный раствор.
Все реактивы, используемые для анализа, должны быть квалификации чистые для анализа (ч. д. а.).
3.3.1. Приготовление раствора ортофенантролина
0,1 г моногидрата ортофенантролина ( C 12 Н8 N 2 × H 2 O ), взвешенного с погрешностью не более 0,01 г, растворяют в 100 см 3 дистиллированной воды, подкисленной 2-3 каплями концентрированной соляной кислоты. Реактив сохраняют на холоде в темной склянке с притертой пробкой. 1 см 3 этого реактива связывает в комплекс 0,1 мг железа.
3.3.2. Приготовление 10%-ного раствора солянокислого гидроксиламина
10 г солянокислого гидроксиламина ( NH 2 OH × HCl ), взвешенного с погрешностью не более 0,1 г, растворяют в дистиллированной воде и доводят объем до 100 см 3 .
3.3.3. Приготовление буферного раствора
250 г уксуснокислого аммония ( N Н4С2Н3 O 2 ), взвешенного с погрешностью не более 0,1 г, растворяют в 150 см 3 дистиллированной воды. Добавляют 70 см 3 уксусной кислоты и доводят объем до 1 дм 3 дистиллированной водой.
(Измененная редакция, Изм. № 2).
3.3.4. Приготовление основного стандартного раствора железоаммонийных квасцов — по п. 2.3.1.
3.3.5. Приготовление рабочего стандартного раствора железоаммонийных квасцов — по п. 2.3.2.
3.3.4; 3.3.5. (Измененная редакция, Изм. № 2).
Определению мешают цианиды, нитриты, полифосфаты; хром и цинк в концентрации, превышающей в 10 раз массовую концентрацию железа; кобальт и медь в концентрации более 5 мг/дм 3 и никель в концентрации 2 мг/дм 3 . Предварительное кипячение воды с кислотой превращает полифосфаты в ортофосфаты, добавлением гидроксиламина устраняется мешающее влияние окислителей. Мешающее влияние меди уменьшается при рН 2,5-4.
При отсутствии полифосфатов исследуемую воду тщательно перемешивают и отбирают 25 см 3 (или меньший объем, содержащий не более 0,1 мг железа, разбавленный, до 25 см 3 дистиллированной водой) в мерную колбу вместимостью 50 см 3 . Если при отборе пробы вода была подкислена, то ее нейтрализуют 25 %-ным раствором аммиака до рН 4-5, контролируя потенциометрически или по индикаторной бумаге. Затем добавляют 1 см 3 солянокислого раствора гидроксиламина, 2,00 см 3 ацетатного буферного раствора и 1 см 3 раствора ортофенантролина. После прибавления каждого реактива раствор перемешивают, затем доводят объем до 50 см 3 дистиллированной водой, тщательно перемешивают и оставляют на 15-20 мин для полного развития окраски.
Окрашенный раствор фотометрируют при сине-зеленом светофильтре ( 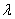
Массовую концентрацию железа находят по градуировочному графику.
В присутствии полифосфатов 25 см 3 исследуемой пробы помещают в плоскодонную колбу вместимостью 100-150 см 3 , прибавляют 1 см 3 концентрированной соляной кислоты, нагревают до кипения и упаривают до объема 15-20 см 3 . После охлаждения раствора его переносят в мерную колбу вместимостью 50 см 3 , добавляют дистиллированную воду до объема примерно 25 см 3 и доводят 25 %-ным раствором аммиака до рН 4-5, контролируя потенциометрически или по индикаторной бумаге.
Далее прибавляют реактивы и проводят анализ, как указано выше (при отсутствии полифосфатов).
Для построения градуировочного графика в мерные колбы вместимостью 50 см 3 вносят 0,0; 0,5; 1,0; 2,0; 3.0; 4,0; 5,0; 10,0; 20,0 см 3 рабочего стандартного раствора, содержащего в 1 см 3 0,005 мг железа, доводят объем дистиллированной водой приблизительно до 25 см 3 и анализируют так же, как и исследуемую воду. Получают шкалу стандартных растворов с массовой концентрацией железа 0,0; 0,05; 0,1; 0,2; 0,3; 0,4; 0,5; 1,0 и 2,0 мг/дм 3 . Фотометрируют в тех же условиях, что и пробу. Строят градуировочный график, откладывая по оси абсцисс массовую концентрацию общего железа в мг/дм 3 а на оси ординат — соответствующие значения оптической плотности.
(Измененная редакция, Изм. № 2).
3.5. Массовую концентрацию общего железа вычисляют по п. 2.5.
(Измененная редакция, Изм. № 2).
Метод основан на взаимодействии ионов двухвалентного железа с 2,2-дипиридилом в области рН 3,5-8,5 с образованием окрашенного в красный цвет комплексного соединения. Интенсивность окраски пропорциональна массовой концентрации железа. Восстановление трехвалентного железа до двухвалентного проводится гидроксиламином. Окраска развивается быстро и устойчива в течение нескольких дней. Диапазон измерения массовой концентрации общего железа без разбавления пробы 0,05-2,00 мг/дм 3 .
В этом интервале суммарная погрешность измерения с вероятностью Р=0,95 находится в пределах 0,01-0,03 мг/дм 3 .
(Измененная редакция, Изм. № 2).
4.2. Аппаратура, материалы, реактивы
Фотоэлектроколориметр любой марки.
Кюветы с толщиной оптического слоя 2-5 см.
Колбы мерные 2-го класса точности по ГОСТ 1770, вместимостью 50, 100 и 1000 см 3 .
Пипетки мерные без делений, вместимостью 25 см 3 н пипетки мерные с делениями 0,1-0,01 см 3 , вместимостью 1, 5 и 10 см 3 2-го класса точности по нормативно-техническому документу.
Аммоний уксуснокислый по ГОСТ 3117.
Гидроксиламин солянокислый по ГОСТ 5456.
2,2-дипиридил ( 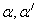
Квасцы железоаммонийные по нормативно-техническому документу.
Кислота уксусная по ГОСТ 61.
Спирт этиловый ректификованный по ГОСТ 18300, высшего сорта.
Вода дистиллированная по ГОСТ 6709.
Все реактивы, используемые для анализа, должны быть квалификации химически чистые (х. ч.) или чистые для анализа (ч. д. а.).
(Измененная редакция, Изм. № 2).
4.3.1. Приготовление основного стандартного раствора железоаммонийных квасцов — по п. 2.3.1.
4.3.2. Приготовление рабочего стандартного раствора железоаммонийных квасцов — по п. 2.3.2.
4.3.1; 4.3.2. (Измененная редакция, Изм. № 2).
4.3.3. Приготовление 10 %-ного раствора солянокислого гидроксиламина — по п. 3.3.2.
4.3.4. Приготовление ацетатного буферного раствора — по п. 3.3.3.
4.3.5. Приготовление 0,1 %-ного раствора 2,2-дипиридила.
0,1 г 2,2-дипиридила, взвешенного с погрешностью не более 0,01 г, растворяют в 5,00 см 3 этилового спирта и разбавляют в 100 см 3 дистиллированной воды.
Для определения массовой концентрации общего железа исследуемую воду тщательно перемешивают и отбирают 25 см 3 (или меньший объем, содержащий не более 0,1 мг железа) в мерную колбу вместимостью 50 см 3 . Прибавляют 1 см 3 раствора гидроксиламина солянокислого, 2,00 см 3 ацетатного буферного раствора, 1,00 см 3 раствора 2,2-дипириднла и доводят до метки дистиллированной водой. После добавления каждого реактива содержимое колбы перемешивают. Раствор оставляют на 15-20 мин для полного развития окраски. Окрашенный раствор фотометрируют, применяя зеленый светофильтр ( 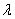
Массовую концентрацию железа находят по градуировочному графику.
Для построения градуировочного графика в мерные колбы вместимостью 50 см 3 вносят 0,0; 2,0; 5,0; 10,0; 15,0; 20,0 см 3 рабочего стандартного раствора железоаммонийных квасцов. Добавляют дистиллированной воды до объема примерно 25 см 3 . Далее растворы проводят через весь ход анализа так же, как исследуемую воду. Получают шкалу стандартных растворов с массовой концентрацией железа 0,0; 0,2; 0,5; 1,0; 1,5; 2,0 мг/дм 3 . Оптическую плотность измеряют в тех же условиях, что и пробы. Строят градуировочный график, откладывая по оси абсцисс массовую концентрацию железа в мг/дм 3 , а по оси ординат — соответствующие значения оптической плотности.
Массовую концентрацию общего железа вычисляют по п. 2.5.
4.3.5; 4.4; 4.5. (Измененная редакция, Изм. № 2).
1. УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Государственного комитета стандартов Совета Министров СССР от 09.10.72 № 1855
3. ССЫЛОЧНЫЕ НОРМАТИВНО-ТЕХНИЧЕСКИЕ ДОКУМЕНТЫ
источник
Дачники, а иногда и жители частных домов не всегда имеют возможность пользоваться централизованным водопроводом. Нередко им приходится добывать воду для питья и бытовых нужд самостоятельно, выкапывая колодцы или пробуривая скважины. Но в таком случае нет никаких гарантий в том, что вода из земли окажется безопасной. Часто в грунтовых водах содержатся примеси тяжёлых металлов, например, железа. Давайте узнаем, чем вредно высокое содержание железа в воде из скважины и как можно её очистить.
Железо – жизненно важный для функционирования организма элемент. Только в крови взрослого человека его содержится порядка 5 г. Однако, выведение попавшего в организм железа происходит очень медленно. Через стенки кишечника выводится не более 10 мг. в сутки.
Таким образом, мужчинам не рекомендуется потреблять в сутки более 6-10 мг. Для женщин этот показатель немного выше (учитываются дополнительные кровопотери) – он составляет от 12 до 18 мг. в сутки.
Казалось бы, исходя из этих значений и того, что в сутки человек выпивает около 2 литров воды, определить допустимую концентрацию этого элемента в воде нетрудно. Но проблема в том, что 90% железа попадает в организм не из жидкости, а из пищи. Особенно богаты данным элементом мясо, печень, морепродукты, яблоки, фасоль и другие бобовые культуры.
Это интересно: Удивительно, но санитарная норма допустимого содержания железа в воде, составляющая 0,3 мг./л., была установлена вовсе не по медицинским, а лишь по вкусовым критериям.
Дело в том, что Всемирная Организация Здравоохранения до сих пор не установила какое-то значение концентрации железа в потребляемой жидкости как нормальное. По мнению экспертов организации, данных, свидетельствующих о негативном воздействии этого элемента на организм человека, пока собрано недостаточно.
Также исследования ВОЗ помогли определить переносимый суточный уровень потребления (ПСП) человеком железа. Он составляет 0,8 мг. на каждый кг. веса тела.
Исходя из того, что средняя масса человека – 75 кг., получается, что можно потреблять не более 60 мг. железа в сутки. Учитывая, что из воды организм получает около 10% данного элемента, можно сделать вывод, что нормальной концентрацией является значение в 2-3 мг./л.
Таким образом, по мнению экспертов ВОЗ, регулярное потребление воды, содержание железа в которой составляет менее 3 мг./л., не приведёт к каким-либо негативным последствиям для здоровья. Но в действительности это огромное значение. Вода, содержащая столь большое количество железа, будет пускай и безвредной, но приобретёт достаточно неприятный вкус.
Если в воде из скважины содержание железа не превышает 3 мг./л., её очищают лишь с целью улучшения вкусовых качеств. Если же концентрация больше указанного значения –появляются причины заботиться о здоровье.
Это интересно: Разовое потребление жидкости с высоким содержанием железа не навредит организму. Но её систематическое использование для питья и приготовления пищи приведёт к ухудшению самочувствия. Причина в том, что при перенасыщении железом организм теряет запасы других важнейших химических элементов, среди них – медь, кальций, цинк и т.д. А это приводит к развитию всяческих недомоганий.
Распространёнными последствиями чрезмерного содержания железа (в том числе двувалентного) в организме являются:
- Раздражение кожи, неприятные ощущения при прикосновении к ней. Возможны аллергические реакции, незначительное пожелтение кожных покровов и слизистых оболочек.
- Увеличение размера печени.
- Постепенное изменение морфологического состава крови.
- Утрата веса, бледность, высокая утомляемость, слабость.
- Нарушения нормального сердечного ритма.
- Ухудшение памяти, невозможность сосредоточиться.
- Частые расстройства желудка, воспаления органов пищеварительной системы.
- Проблемы со щитовидной железой.
Если человек потребляет воду с высоким содержанием железа годами, этот химический элемент постепенно оседает в организме. Причём сосредотачивается он в самых важных внутренних органах – почках, печени, сердце, лёгких, кишечнике и поджелудочной железе.
В итоге в зрелом возрасте (примерно к 50 годам) повышенное содержание железа в воде может внести вклад в появление нервных патологий, развитие сахарного диабета, ухудшение работы суставов и затруднение умственной деятельности.
Откуда же берётся в глубинных водах железо? Главными источниками данного элемента являются такие минералы, как красный, бурый и магнитный железняк. Определить содержание железа в воде из скважины можно с помощью лабораторного анализа и по косвенным признакам.
Лучшим способом будет взять пробу воды из скважины и отнести её в соответствующую лабораторию. Конечно, придётся заплатить некоторую сумму, зато вы получите точную информацию, которая поможет выбрать оптимальную стратегию очистки.
Важно понимать, что итоговый результат будет зависеть от правильности взятия пробы. Сотрудники санитарно-эпидемической станции не всегда акцентируют внимание на этом аспекте. Поэтому результат может получиться недостоверным, вследствие чего человек начнёт бороться с несуществующей проблемой загрязнения. Причём это относится не только к железу, но и к другим веществам.
Избежать таких казусов можно, следуя нижеперечисленным правилам водозабора:
- Противопоказано использовать металлическую тару. Оптимальные варианты – стекло и пищевая пластмасса.
- Можно использовать бутылку из-под минеральной воды. Сладкая газировка содержит стойкие красители и консерванты. Они оседают на внутренних стенках тары, не смываясь даже при полоскании кипятком.
- Максимальная ёмкость тары – 1,5 литра.
- Бутылку необходимо несколько раз прополоскать горячей водой (стекло – обязательно кипятком), после чего промыть водой из скважины, откуда вы будете осуществлять водозабор. Нельзя использовать любые химические моющие средства. Даже сода может изменить полученные при анализе показания.
- Прежде чем брать воду из скважины, позвольте ей стечь не менее 5-10 минут. Так вы устраните внутренние застои в трубах и сможете избавиться от посторонних частичек металла (отделённых от железного трубопровода). Вам ведь нужно оценить именно качество воды, а не труб, не так ли?
- Чтобы при водозаборе в бутылку не попало чрезмерное количество кислорода, вызывающего побочные химические реакции, следует включать минимальный напор. Жидкость должна стекать медленно, тонкой струёй.
- Заполняйте тару до конца. Когда будете закручивать пробку, желательно, чтобы немного воды даже вылилось наружу. Так внутри бутылки не останется прослойки воздуха.
- Подготовленную бутылку нужно плотно завернуть в пакет и отвезти на сдачу на протяжении ближайших 2-3 часов. В крайнем случае тару можно поместить в холодильник и продержать там до момента сдачи, максимум – 48 часов.
Важная информация: Сдавать воду на анализ хозяева свежевырытой скважины должны в обязательном порядке. Людям, уже пользующимся источником, следует повторять его каждые 2 года. Но, если вы заметили, что из скважины начала литься мутная вода, или если жидкость приобрела металлический привкус – отправьте её на анализ сразу же, не дожидаясь истечения двухлетнего срока.
Помимо этого, определить примерное содержание железа можно по нескольким косвенным признакам.
Прежде всего, стоит знать, что при повышении концентрации железа до значения в 0,3 мг./л. и выше меняется вкус воды. Во рту появляется неприятный металлический привкус. Если же содержание этого элемента превышает 1 мг./л., этот вкус отчётливо ощущается даже в напитках – чае и кофе.
На стенках посуды, в которой хранится вода с большой концентрацией железа (чайники, кастрюли, вёдра и т.д.), появляется ржавый налёт. Цветное бельё при стирке быстро обесцвечивается.
При этом вода необязательно должна иметь желтоватый оттенок, она может оставаться и совершенно прозрачной. Это зависит от того, в какой форме в ней содержится железо.
Железо может присутствовать в воде в нескольких формах – двухвалентной, трёхвалентной, бактериальной и т.д. Самыми распространёнными являются первые две:
- Двухвалентное железо легко растворяется в воде. Поэтому жидкость с повышенным содержанием этого вещества остаётся прозрачной и бесцветной. Но если налить её в открытую емкость – через время на дно выпадет осадок бурого цвета.
- Трехвалентное железо в воде не растворяется. При его высокой концентрации вода приобретает желтоватый оттенок. В отстоянной воде, опять же, выпадает буроватый осадок.
Чаще всего в воде из скважин наблюдается повышенное содержание двухвалентного железа. Логично, что основная задача обезжелезивания воды – вызвать окислительные реакции, после которых металл выпадет в виде твёрдого осадка. Он будет отфильтрован из системы.
Непосредственно внутри скважины сделать что-либо не представляется возможным.
Выходом является установка специальных ионообменных картриджей на месте входа трубопровода в дом. Их внутренние стенки покрыты специальным окислительным составом. При прохождении воды сквозь них железо вступает в химическую реакцию. Образуется твёрдый осадок, который собирается фильтром. Ясно, что по мере забивания фильтра функцию обезжелезивания он начинает выполнять всё менее эффективно. Поэтому подобные картриджи необходимо регулярно менять.
Самым же эффективным способом, пускай и дорогостоящим, является установка так называемого обратного осмоса для скважины – системы из нескольких фильтров и полупроницаемой мембраны, сквозь которую под большим давлением прогоняется загрязнённая вода. Жидкость очищается не только от железа (даже в самых высоких концентрациях), но и от широкого ряда других вредных веществ. Все они отводятся в канализацию. Из крана же течёт идеально чистая вода. Дополнительным плюсом такого способа очистки является то, что в нём не задействуются никакие химические окислители.
Это интересно: Проблемы в работе ионообменных картриджей и фильтрационной системы обратного осмоса возникают, если в воде, помимо двухвалентного железа, в высоких концентрациях присутствует ещё и его трёхвалентная форма. Тогда фильтры забиваются быстрее, очищать (заменять) их приходится в несколько раз чаще.
Перейдём к последнему способу. Системы аэрации для очистки воды от трёхвалентного железа выглядят, как большие открытые резервуары, в которых вода отстаивается длительное время. Чтобы сделать процесс окисления (и последующего выпадения железа в осадок) более интенсивным, через жидкость с помощью компрессора пропускается воздух. Очищенная вода становится пригодной для питья и любых бытовых нужд. Система аэрации может применяться для очистки воды с содержанием железа в 10-20 мг/л.
Последний процесс можно повторить, воспользовавшись обычным ведром. Достаточно набрать в него воду и оставить её на сутки. После этого верхнюю часть следует аккуратно слить, стараясь не взбаламучивать осадок. После таких нехитрых манипуляций концентрация железа в воде уменьшится как минимум в 3–4 раза.
К другим методам очистки относятся:
- Заморозка. Бутылка наполняется водой из скважины и кладётся в морозилку. Когда большая часть жидкости превращается в лёд, нужно слить остаток. В нём останутся почти все вредные примеси. При разморозке же необходимо выбросить и последние льдинки.
- Кремний и шунгит. Данные минералы также способны эффективно обеззаразить воду. Их нужно класть на дно ёмкости, заполненной жидкостью. Настаивать необходимо минимум 48 часов. Сливать для дальнейшего использования можно лишь верхний слой воды, в нижней части содержится осадок.
- Уголь. Заверните активированный уголь в толстый слой ваты и пропустите воду через этот самодельный фильтр. Он поможет избавиться от основных механических примесей и устранит выпавший осадок.
Воспользовавшись перечисленными рекомендациями, вы сможете провести эффективное обезжелезивание воды. А это – одна из наиболее распространённых проблем, с которыми сталкиваются владельцы скважин. Вода станет пригодной не только для бытовых нужд, но и для регулярного питья.
источник
Нормы качества питьевой воды СанПиН 2.1.4.1074-01. Питьевая вода. (ВОЗ, ЕС, USEPA).питьевой воды, расфасованной в емкости (по СанПиН 2.1.4.1116 – 02), показателей водок (по ПТР 10-12292-99 с изменениями 1,2,3), воды для производства пива и безалкогольной продукции, сетевой и подпиточной воды водогрейных котлов ( по РД 24.031.120-91), питательной воды для котлов (по ГОСТ 20995-75), дистиллированной воды (по ГОСТ 6709-96), воды для электронной техники (по ОСТ 11.029.003-80, ASTM D-5127-90), для гальванических производств ( по ГОСТ 9.314-90), для гемодиализа (по ГОСТ 52556-2006), воды очищенной (по ФС 42-2619-97 и EP IV 2002), воды для инъекций (по ФС 42-2620-97 и EP IV 2002), воды для полива тепличных культур.
В данном разделе приведены основные показатели нормативов качества воды для различных производств.
Вполне достоверные данные отличной и уважаемой компании в области водоочистки и водоподготовки «Альтир» из Владимира
1. Нормы качества питьевой воды СанПиН 2.1.4.1074-01. Питьевая вода. (ВОЗ, ЕС, USEPA).
с.-т. – санитарно-токсикологический
орг. – органолептический
Величина, указанная в скобках, во всех таблицах может быть установлена по указанию Главного государственного санитарного врача.
Требования по микробиологическим и паразитологическим показателям воды
Требования к органолептическим свойствам воды
Требования по радиационной безопасности питьевой воды
2. Нормы качества питьевой воды, расфасованной в емкости (по СанПиН 2.1.4.1116 – 02).
3.1. Оптимальные значения физико-химических и микроэлементных показателей водок
Водородный показатель (рН)
7,5
— кальция
— магния
— железа
— сульфатов
— хлоридов
— кремния
— гидрокарбонатов
— натрия+калия
— марганца
— алюминия
— меди
— фосфатов
— нитратов
0,5
0,15
18,0
18,0
3,0
75
60
0,06
0,10
0,10
0,10
2,5
1,0
0,12
15,0
15,0
2,5
60
50
0,06
0,06
0,06
0,10
2,5
1,5
0,10
12,0
12,0
2,0
40
50
0,06
0,06
0,06
0,10
2,5
1,2
0,04
15,0
9,0
1,2
25
25
0,06
0,06
0,06
0,10
2,5
1,5
0,02
6,0
6,0
0,6
15
12
0,06
0,06
0,06
0,10
2,5
3.2. Нижние пределы содержания микроэлементов в технологической воде для приготовления водок
4. Нормы качества питьевой воды для производства пива и безалкогольной продукции.
5. Нормы качества сетевой и подпиточной воды водогрейных котлов ( по РД 24.031.120-91).
- В числителе указаны значения для котлов на твердом топливе, в знаменателе — на жидком и газообразном.
- Для тепловых сетей, в которых водогрейные котлы работают параллельно с бойлерами, имеющими латунные трубки, верхний предел рН сетевой воды не должен превышать 9,5.
- Содержание растворенного кислорода указано для сетевой воды; для подпиточной воды оно не должно превышать 50 мкг/кг.
6. Нормы качества питательной воды для котлов (по ГОСТ 20995-75).
* В числителе указаны значения для котлов, работающих на жидком топливе при локальном тепловом потоке более 350 кВт/м 2 [3*10 5 ккал/(м 2 *ч)], а в знаменателе — для котлов, работающих на других видах топлива при локальном тепловом потоке до 350 кВт/м 2 [3*10 5 ккал/(м 2 *ч)] включительно.
** При наличии в системе подготовки добавочной воды промышленных и отопительных котельных фазы предварительного известкования или содоизвесткования, а также при значениях карбонатной жесткости исходной воды более 3,5 мг-экв/дм 3 и при наличии одной из фаз водоподготовки (натрий—катионирования или аммоний—натрий—катионирования) допускается повышение верхнего предела значения рН до 10,5.
При эксплуатации вакуумных деаэраторов допускается снижение нижнего предела значения рН до 7,0.
7. Нормы качества дистиллированной воды (по ГОСТ 6709-96).
8. Нормы качества воды для электронной техники (по ОСТ 11.029.003-80, ASTM D-5127-90).
9.Нормы качества воды для гальванических производств ( по ГОСТ 9.314-90)
* Нормы ингредиентов для воды 3-й категории определяются по ГОСТ 6709.
Примечание. В системах многократного использования воды допускается содержание вредных ингредиентов в очищенной воде выше, чем в табл.1 но не выше допустимых значений в промывной ванне после операции промывки (табл.2).
Кислый или цианистый
100
Кислый
Цианистый
50
10
Сушка
10
Хромирование, сушка
10
- За основной компонент (ион) данного раствора или электролита принимают тот, для которого критерий промывки является наибольшим.
- При промывке изделий, к которым предъявляются особо высокие требования, допустимые концентрации основного компонента могут устанавливаться опытным путем.
Концентрации основных ингредиентов в воде на выходе из гальванического производства приведены в табл.3
1.3. В гальваническом производстве следует применять системы многократного использования воды, обеспечивающие
10. Нормы качества воды для гемодиализа (по ГОСТ 52556-2006).
11. Нормы качества «Вода очищенная» (по ФС 42-2619-97 и EP IV 2002).
12.Нормы качества «Вода для инъекций» (по ФС 42-2620-97 и EP IV 2002).
13. Рекомендуемое качество воды для полива тепличных культур.
источник




