Исследовательский проект «Использование метода спектрофотомерии для определения концентрации фенола в воде»
1. Общие сведения о фенолах
Фенолы- это производные ароматических углеводородов, в которых отдельные атомы водорода замещены гидроксильной группой. Фенолы представляют собой производные бензола с одной или нескольким гидроксильными группами. Их принято делить на две группы – летучие с паром фенолы (фенол, крезолы, ксиленолы, гваякол, тимол) и нелетучие фенолы (резорцин, пирокатехин, гидрохинон, пирогаллол и другие многоатомные фенолы).
Фенол – кристаллическое вещество, с температурой плавления 43°С, температурой кипения 181°С, растворяется в воде (при 15°С – около 8%). С водой дает гидрат (температура плавления 16°С), называемый обычно карболовой кислотой. Небольшие количества воды сильно снижают температуру плавления фенола. Он обладает характерным запахом. Фенол вызывает ожоги на коже. Вдыхание фенола влечет сильное раздражение слизистых оболочек, контакт с кожей – ожоги, а хроническое отравление приводит к поражению печени и почек, патогенному изменению крови. Является одним из первых примененных в медицине антисептиков.
Фенол содержится в моче человека и животных, так как белковые аминокислоты, содержащие бензольное кольцо, при расщеплении в организме дают фенол.
2. Объекты исследования
Объектом моего исследования является сточные воды завода ООО «ЭГГЕР ДРЕВПРОДУКТ» и питьевая вода.
3. Актуальность проблемы
Фенолы являются одним из наиболее распространенных загрязнителей, поступающих в поверхностные воды со стоками предприятий нефтеперерабатывающей, сланцеперерабатывающей, лесохимической, коксохимической, анилинокрасочной промышленности и др.
При обработке хлором воды, содержащей примеси фенола, могут образовываться очень опасные органические токсиканты – диоксины. Удаление фенолов из сточных вод газовых и коксохимических заводов, заводов по перегонке бурого угля, от перегонки смолы в процессах гидрирования, от генераторных установок, предприятий по переработке нефти и предприятий химической промышленности является, поэтому необходимым. Оно может быть выполнено путем извлечения фенола из сточных вод или ликвидацией его. В загрязненных фенолами природных водах содержание их может достигать десятков и даже сотен микрограммов в 1 л. ПДК фенолов в воде для России составляет 0,001 мг/дм 3 .
Сброс фенольных вод в водоемы и водотоки резко ухудшает их общее санитарное состояние, оказывая влияние на живые организмы не только своей токсичностью, но и значительным изменением режима биогенных элементов и растворенных газов (кислорода, углекислого газа).
Процесс самоочищения водоемов от фенола протекает относительно медленно и его следы могут уноситься течением реки на большие расстояния, поэтому до сброса фенолсодержащие стоки подвергают достаточной очистке.
Наряду с токсичностью и возможностью связать кислород, что в целом отрицательно сказывается на качестве воды в водоеме, фенольные сточные воды наносят вред рыболовству и представляют опасность для хозяйственно-питьевого водоснабжения. Присутствие даже очень малых количеств фенола в воде, предназначенной для хозяйственно-питьевых целей, значительно ухудшает ее качества. Анализ воды на фенол важен для природных и сточных вод. Необходимо проверять воду на содержание фенола, если есть подозрение в загрязнении водотоков промышленными стоками. ПДК фенола в воде – 3*10 -5 (моль/л).
Подходит ли метод спектрофотометрии для выявления содержания фенола в воде?
5. Цель исследования.
Выявить содержание фенола в воде методом спектрофотометрии.
1. Методы очистки сточных вод от фенола.
- Парофазное окисление
- Озонирование
- Метод обработки хлором и хлорсодержащими агентами
- Метод окисления диоксидом хлора
- Пероксид водорода
- Биологическая очистка
- Ионообменная очистка
- Очистка перегонкой и ректификацией
2. Спектрофотометрия.
СПЕКТРОФОТОМЕТРИЯ – метод исследования и анализа веществ, основанный на измерении спектров поглощения в оптической области электромагнитного излучения.
Спектрофотометрию широко применяют для исследования органических и неорганических веществ, для качественного и количественного анализа различных объектов (в частности, природных), для контроля технологических процессов. Различают спектрофотометрию в ИК (Инфракрасная спектроскопия), видимой и УФ(Ультрафиолетовая спектроскопия) областях спектра. В качестве источников излучения применяют дейтериевую (или водородную) лампу (в УФ области) и вольфрамовую лампу накаливания или галогенную лампу (в видимой и ближней ИК областях). Приемниками излучения служат фотоэлектронные умножители (ФЭУ) и фотоэлементы (фоторезисторы на основе PbS). Диспергирующими элементами прибора являются призменный монохроматор или монохроматор с дифракционными решетками. Спектр получают в графической форме, а в приборах со встроенной мини-ЭВМ-в графической и цифровой формах. Графически спектр регистрируют в координатах: длина волны (нм) и (или) волновое число (см-1)-пропускание (%) и(или) оптическая плотность. Основные характеристики спектрофотометров: точность определения длины волны излучения и величины пропускания, разрешающая способность и светосила, время сканирования спектра. Мини-ЭВМ (или микропроцессоры) осуществляют автоматизированное управление прибором и различную математическую обработку получаемых экспериментальных данных.
3. Закон Бугера-Ламберта-Бера
Закон Бугера-Ламберта-Бера связывает уменьшение интенсивности света, прошедшего через слой светопоглощающего вещества, с концентрацией этого вещества и толщиной слоя. Чтобы учесть потери света на отражение и рассеяние, сравнивают интенсивность света, прошедшего через раствор исследуемого вещества я растворитель.
При одинаковой толщине кювет, изготовленных из одинакового Материала и содержащих один и тот же растворитель, потери на отражение и рассеяние света будут примерно одинаковы в обоих пучках, и уменьшение интенсивности света будет зависеть практически только от концентрации вещества.
Уменьшение интенсивности света, прошедшего через раствор, характеризуется коэффициентом пропускания (или просто пропусканием) Т:
где I и I – соответственно интенсивность света, прошедшего через раствор и растворитель.
Десятичный логарифм коэффициента светопропускания, взятый с обратным знаком, называется оптической плотностью А:
Уменьшение интенсивности при прохождении света через раствор подчиняется закону Бугера-Ламберта-Бера:
ε – молярный коэффициент погашения,
b – толщина светопоглощающего слоя,
C – молярная концентрация раствора,
А – оптическая плотность
4. Характеристика объекта исследования (Завод ООО «ЭГГЕР ДРЕВПРОДУКТ»)
В производстве древесностружечных плит при изготовлении и сортировке щепы, изготовлении стружки, при механической обработке плит (обрезка, шлифование, раскрой) выделяются отходы древесины, в том числе древесная пыль. В процессе пропитки стружки смолой, горячего прессования, охлаждения, выдержки плит выделяются вредные парогазовоздушные смеси из расходуемых смолосодержащих материалов. В атмосферу поступает 40 % от валового количества свободного формальдегида и фенола. Предприятие по производству древесно-стружечных плит, согласно санитарным правилам и нормам, относится к III классу опасности. Санитарно-защитная зона для такого производства 300 м. Экологическая экспертиза выявила, что на предприятии находятся источники выбросов 30 загрязняющих веществ, в том числе оксидов азота, диоксида серы, серной кислоты, сажи, сероводорода, оксида углерода, предельных углеводородов различных групп (природный газ и различные типы нефтепродуктов), ароматических углеводородов, фенола, формальдегида, метанола, пыли древесной, пыли абразивной и др. На заводе в Ивановской области не предусмотрено никакой очистки газообразных выбросов. В соответствии с материалами экологической экспертизы прямое влияние проектируемого ЗПДМ ООО «Эггер Древпродукт» на водные экосистемы реки Теза и оз. Яскинского и качество воды в ней будет отсутствовать. Возможно воздействие на данные природный объекты только через атмосферные осадки, а также посредством поверхностного и грунтового стока. В числе других выбросов в атмосферу фенол, в результате выпадения осадков, может оказаться в водоемах.
Спектрофотометр СФ-46
- Заменим раствор сравнения в кювете на раствор фенола без добавки.
- Поместим кювету в измерительную ячейку и закроем крышку кюветного отделения.
Снятие спектра
- Установим в кюветное отделение кювету с раствором сравнения (вода или 0,1 М HCl) и исследуемым раствором. Запишем положение растворов
- Откроем фотоэлемент.
- Установим требуемую длину волны.
- Измерим оптическую плотность при установленной длине волны и запишем ее значение.
Построение калибровочного графика.
- Выберем длину волны (волн) для построения калибровочного графика (измерения коэффициентов светопоглощения).
- Установим требуемую длину волны.
- Установим в кюветное отделение вместо ранее используемого рабочего раствора, кювету с исследуемым раствором минимальной концентрации
- Измерим оптическую плотность.
Оборудование
- Глюкоза (в порошке)
- Фенол
- Серная кислота (H2SO4)
- Дистиллированная вода.
Готовим раствор фенола. Для этого берем 2,4 грамма фенола, добавляем 5 мл серной кислоты, перемешиваем.
Берем 0,9 грамма глюкозы, разбавляем дистиллированной водой, доводим до метки. Отдельно в другую колбу отмеряем 5 мл серной кислоты. В колбе смешиваем серную кислоту и 2 мл раствора фенола. Реакция не наблюдается. С помощью дозатора берем 1 мл раствора глюкозы и добавляем в полученный раствор. Наблюдаем экзотермическую реакцию с появлением красно-коричневой окраски.
Реакции конденсации с фенольными соединениями. SE в ядро.
В результате реакции получается ауриновый краситель розово-красного цвета. Электронный спектр поглощения данного соединения представлен ниже (рис. 1). Из данного рисунка видно, что продукт реакции глюкозы с фенолом в среде серной кислоты имеет максимум поглощения на длине волны 480 нм. В дальнейшем данную длину волны использовали для построения калибровочного графика (рис. 2).
- 5,56*10 -5 моль/литр
- 1,11*10 -4 моль/литр
- 1,67*10 -4 моль/литр
- 2,78*10 -4 моль/литр
Рис. 1
Построение калибровочного графика
Рис. 2
Y – коэффициент экстинции
R 2 – отклонение от 100%
Определяем исходную концентрацию
- Метод не подходит для определения концентрации фенола в питьевой воде, т.к. из-за хлорирования концентрация фенола меньше 10-5 (моль/л).
- В промышленности концентрация фенола до очистки может быть в 5-10 раз выше, поэтому данный метод можно применять для определения концентрации фенола в сточных водах.
Использовать данный метод для определения фенола в сточных водах предприятий с целью дальнейшей очистки.
источник
Фенолы являются одним из наиболее распространенных загрязнителей, поступающих в поверхностные воды со стоками предприятий. Фенолами называют вещества, имеющие в своей молекуле бензольное ядро, содержащее одну или более гидроксильных групп. Фенол ядовит, вызывает нарушение функций нервной системы. Пыль, пары и раствор фенола раздражают слизистые оболочки глаз, дыхательных путей, кожу. ПДК фенола (ГН 2.1.5.1315-03) — 0,001 мг/л для суммы летучих фенолов, придающих воде хлорфенольный запах при хлорировании (метод пробного хлорирования). Эта ПДК относится к водным объектам хозяйственно-питьевого водопользования, при условии применения хлора для обеззараживания воды в процессе ее очистки на водопроводных сооружениях или при определении условий сброса сточных вод, подвергающихся обеззараживанию хлором. В иных случаях допускается содержание суммы летучих фенолов в воде водных объектов в концентрациях 0,1 мг/л.
В настоящее время для определения фенолов в воде применяются следующие методы анализа:
- Фотометрический метод;
- Метод газо-жидкостной хроматографии;
- Метод высокоэффективной жидкостной хроматографии;
- Метод броматометрического титрования;
- Флуориметрический метод.

При определении фенола в воде методом газо-жидкостной хроматографии с пламенно-ионизационным детектированием (МУК 4.1.752-99) осуществляют концентрирование вещества из воды в 2 стадии: экстракцией диэтиловым эфиром и испарением последнего под вакуумом. Фенол переходит в воду, оставшуюся после испарения эфира. Диапазон измеряемых концентраций: 0,0005 – 0,010 мг/дм 3 . Нижний предел измерения – 0,001 мкг. Погрешность методики при Р=0,95 составляет ±21,3%.
Для определения больших концентраций летучих одноатомных фенолов (более 50 мг/л) рекомендуется броматометрический метод, основой которого является бромирование одноатомных фенолов, выделенных из пробы перегонкой с водяным паром. Расход брома пропорционален содержанию фенола. При определении фенола методом броматометрического титрования в анализируемый раствор вводится избыток бромат-бромидной смеси, которая в кислой среде выделяет свободный бром. Образующийся бром реагирует с фенолом. При добавлении к этому раствору иодида калия избыточный, не прореагировавший бром окисляет иодид до йода, который титруют стандартным раствором тиосульфата натрия.
Метод высокоэффективной жидкостной хроматографии обеспечивает получение результатов измерений массовой концентрации фенола в пробах воды в диапазоне от 0,10 до 20 мкг/дм 3 . Подготовка проб к измерениям включает следующие этапы: 1) Извлечение фенола из пробы методом твердофазной экстракции; 2) Элюирование фенола с ТФЭ-картриджа; 3) Подготовка пробы для ввода в хроматограф. Погрешность методики при Р=0,95 составляет 25 – 28%.
Флуориметрический метод измерения массовой концентрации общих фенолов (метод А, ПНД Ф 14.1:2:4.182-02) основан на извлечении фенолов из воды бутилацетатом, реэкстракции их в водный раствор гидроксида натрия и измерении их содержания по интенсивности флуоресценции фенолов после подкисления реэкстракта. В процессе измерения происходит возбуждение флуоресценции фенолов, ее регистрация и автоматическое вычисление массовой концентрации фенола при помощи градуировочной характеристики, заложенной памяти анализатора жидкости «Флюорат-02».
Флуориметрический метод измерения массовой концентрации летучих фенолов (метод Б, ПНД Ф 14.1:2:4.182-02) включает операцию перегонки пробы воды с помощью перегонного устройства и измерение массовой концентрации фенолов в отгоне по методу А. Метод рекомендуется для анализа окрашенных, мутных вод, а также вод с большим содержанием органических веществ, препятствующих разделению фаз при экстракции, и проб, содержащих гуминовые кислоты и лигнин. Мешающее влияние нефтепродуктов устраняется при подготовке проб к анализу. Диапазон измеряемых концентраций: 0,0005 – 25 мг/дм 3 . Погрешность методики при Р=0,95 ( ±δ, %): 17 – 50% (для питьевых вод), 25 – 60% (для природных и сточных вод).
В нашей лаборатории содержание фенола определяется во всех типах вод. Точность и достоверность получаемых в нашем центре результатов подтверждена неоднократным успешным прохождением межлабораторных сличительных испытаний.
Определение содержания ксантогенатов в природной и сточной воде

Методы определения бенз(а)пирена в почвах и грунтах
источник
Качество водопроводной воды в квартирах большинства украинцев оставляет желать лучшего. И дело не всегда в экологии. Даже если изначально вода и была неплохой (например, поднятой с подземного горизонта), то пройдя по изношенным трубам, она становится практически непригодной для питья. Но банальная ржавчина – это далеко не самый страшный «сюрприз» из вашего крана. Гораздо опаснее загрязнение химическими соединениями, например, такими как фенолы. Оказывается, фенол в питьевой воде – не такое уж редкое явление. Давайте разберёмся, откуда он берётся и как можно решить проблему.
Для начала стоит разобраться: что же такое фенолы и какую опасность они могут представлять. Выражаясь языком химии, фенолы – это органические соединения ароматического ряда, которые применяются в производстве различных феноло-альдегидных смол, полиамидов, эпоксидных смол, антиоксидантов и т.п. То есть, фенолы могут попадать в воду как следствие хозяйственной деятельности предприятий нефтеперерабатывающей, лакокрасочной, лесохимической и т.п. промышленности. Но не только. Оказывается, фенолы в воде могут появиться даже просто из-за некачественных труб и материалов, – утверждают специалисты. Трубы, прокладки, жидкие уплотнители, герметики для труб могут содержать в своём составе фенолы. Получается, что поменяв старые ржавые трубы на новые, вы можете получить фенол взамен ржавчины. Согласитесь, результаты такого «замещения» не радуют. Чтобы такая проблема не возникла, тщательно подбирайте материалы для ремонта, изучайте сертификаты качества.
Фенол – очень токсичное вещество. При попадании в организм он способен вызвать тяжёлые последствия. Раствор фенола в воде оказывают разрушающее воздействие на почки и головной мозг. Значительное превышение допустимых показателей содержания фенола в воде даже может приравниваться к экологической катастрофе (как, например, произошло в 1990 году в Уфе, когда в реку попали отходы местного химического предприятия). Именно поэтому анализ фенолов в воде чрезвычайная важная составляющая исследований качества воды.
Согласно государственным санитарно-гигиеническим нормам, содержание фенола в воде не должно превышать 0, 001 мг/дм3. Если этот показатель превышен, нужно устранять проблему. Оказывается, для этого даже не нужно устанавливать в квартире сложные и дорогие системы фильтрации. Даже бюджетные модели, в том числе и обычные угольные фильтры, отлично справляются с этой проблемой.
Фенолы могут негативно влиять на здоровье человека и окружающую среду, если превышено их количество в поверхностных водах. Вообще фенол – один из самых распространённых промышленных загрязнителей. Предприятия должны очищать свои стоки, для того, чтобы избежать попадания фенола в поверхностные воды. Но риск превышения допустимого уровня загрязнения всё равно присутствует. Если, к примеру, ваш приусадебный участок, находится по соседству с предприятиями химической промышленности, которые используют фенол, то определение наличия фенолов в воде будет совсем не лишним.
Определение фенола в сточной воде поможет вовремя обратить внимание на проблему и принять меры.
Определение фенолов в воде входит в перечень показателей расширенного анализа воды, который делает лаборатория «УкрХимАнализ». Чтобы не переживать за качество воды, которую вы пьёте – просто сделайте анализ воды на фенол. На сайте лаборатории вы всегда сможете выбрать оптимальный пакет по количеству показателей (максимальный, базовый, расширенный). Специалисты «УкрХимАнализ» проведут качественный и точный анализ предоставленных образцов воды, а также дадут все необходимые консультации, помогут расшифровать показатели и подскажут, что делать, чтобы улучшить качество воды.
источник
Настоящий документ устанавливает методику количественного химического анализа проб природных и очищенных сточных вод для определения в них массовой концентрации летучих фенолов в диапазоне от 2 до 25 мкг/дм 3 в пересчете на фенол экстракционно-фотометрическим методом без разбавления и концентрирования пробы.
Если массовая концентрация летучих фенолов в анализируемой пробе превышает верхнюю границу, то допускается разбавление пробы таким образом, чтобы концентрация фенолов соответствовала регламентированному диапазону.
Определению мешают интенсивно окрашенные соединения кислого характера, в частности нафтеновые кислоты при концентрации более 1 мг/дм 3 , гуминовые кислоты при концентрации более 2 мг/дм 3 , а также активный хлор.
Устранение мешающих влияний осуществляется в соответствии с п. 10.
Экстракционно-фотометрический метод определения массовой концентрации летучих фенолов основан на экстракции фенолов из воды бутилацетатом, реэкстракции их щелочью и образовании в реэкстракте окрашенных соединений фенолов с 4-аминоантипирином в присутствии гексацианоферрата (III) калия. Полученные соединения вновь экстрагируют бутил ацетатом и измеряют оптическую плотность экстракта на спектрофотометре (λ = 470 нм) или фотометре со светофильтром, имеющим максимум пропускания в диапазоне λ = 460 — 490 нм.
Настоящая методика обеспечивает получение результатов анализа с погрешностью, не превышающей значений, приведённых в таблице 1.
Значения показателя точности методики используют при:
— оформлении результатов анализа, выдаваемых лабораторией;
— оценке деятельности лабораторий на качество проведения испытаний;
— оценке возможности использования результатов анализа при реализации методики в конкретной лаборатории.
Диапазон измерений, значения показателей точности, повторяемости, воспроизводимости, правильности
Диапазон измерений (в пересчете на фенол), мкг/дм 3
Показатель точности (границы относительной погрешности при вероятности Р = 0,95), ±δ, %
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемо сти), σ r %
Показатель воспроизводимости (относительное среднеквадрати ческое отклонение воспроизводи мости), σ R , %
Показатель правильности (границы относительной систематической погрешности при вероятности Р = 0,95), ±δс, %
Спектрофотометр или фотометр, позволяющий измерять оптическую плотность при длине волны λ = 460 — 490 нм
Кюветы с толщиной поглощающего слоя 50 мм
Весы лабораторные общего назначения с наибольшим пределом взвешивания 200 г и ценой наименьшего деления 0,1 мг любого типа
Весы лабораторные общего назначения с наибольшим пределом взвешивания 200 г и ценой наименьшего деления 10 мг любого типа
СО с аттестованным содержанием фенола с погрешностью не более 1 % при Р = 0,95 (или фенол, п. 4.3)
рН-метр или иономер с погрешностью измерения pH не более 0,05 единиц pH.
Термометр с диапазоном 0 — 100 °С
Плитки электрические с закрытой спиралью и регулируемой мощностью нагрева
Шкаф сушильный лабораторный с температурой нагрева до 130 °С
Стаканчики для взвешивания (бюксы)
Установка из стекла для перегонки растворителей в составе: колба К-1-1000-29/32 ТС, дефлегматор 350-19/26-29-32 ТС, холодильник ХПТ-1-400-14/23 ХС
Флаконы аптечные с навинчивающимися пробками и полиэтиленовыми вкладышами вместимостью 50 см 3
Средства измерений должны быть поверены в установленные сроки. Допускается использование других, в том числе импортных, средств измерений и вспомогательных устройств с характеристиками не хуже, чем у приведенных в п.п. 4.1 и 4.2.
Фенол кристаллический, очищенный
Бутиловый эфир уксусной кислоты (бутилацетат)
Карбонат натрия безводный Na2CО3,
или карбонат натрия декагидрат Na2CО3∙10H2О
Аммиак водный, концентрированный
Гексацианоферрат (III) калия K3[Fe(CN)6]
Сульфат натрия безводный Na2SО4
Тиосульфат натрия, пентагидрат
Бумага индикаторная универсальная
Фильтры обеззоленные «белая лента»
Вата хлопковая или вата стеклянная
Все реактивы, используемые для анализа, должны быть квалификации ч.д.а. или х.ч.
Допускается использование реактивов, изготовленных по другой нормативно-технической документации, в том числе импортных, с квалификацией не ниже ч.д.а.
5.1. При выполнении анализов необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007.
5.2. Электробезопасность при работе с электроустановками обеспечивается по ГОСТ 12.1.019.
5.3. Организация обучения работающих безопасности труда проводится по ГОСТ 12.0.004.
5.4. Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004 и иметь средства пожаротушения по ГОСТ 12.4.009.
Выполнение измерений может производить химик-аналитик, владеющий техникой экстракционно-фотометрического анализа и изучивший инструкцию по эксплуатации спектрофотометра или фотометра.
При выполнении измерений в лаборатории должны быть соблюдены следующие условия:
• температура окружающего воздуха
не более 80 % при температуре 25 °С;
8.1. Отбор проб производится в соответствии с требованиями ГОСТ Р 51592-2000 «Вода. Общие требования к отбору проб».
8.2. Посуду, предназначенную для отбора и хранения проб, промывают насыщенным раствором кальцинированной соды (карбоната натрия), а затем дистиллированной водой. При мытье сильно загрязненной посуды рекомендуется использовать хромовую смесь, после чего тщательно (не менее 20 раз) промывать водопроводной водой и споласкивать дистиллированной водой.
8.3. Пробы воды отбирают в стеклянные бутыли с плотно завинчивающимися пробками вместимостью 1 дм 3 .
Объем отбираемой пробы должен быть не менее 1 дм 3 .
8.4. Пробы анализируют не позднее, чем через 4 часа после отбора или в течение суток при условии хранения в холодильнике при t 3 с плотным полиэтиленовым вкладышем и завинчивающейся пробкой. Экстракт может храниться в темном прохладном месте в течение 1 месяца.
8.5. При отборе проб составляется сопроводительный документ по утвержденной форме, в котором указывается:
— цель анализа, предполагаемые загрязнители,
— должность, фамилия отбирающего пробу, дата.
9.1. Приготовление растворов и реактивов
9.1.1. Аммонийно-аммиачный буферный раствор с pH 10,0 — 10,2.
50 г хлорида аммония растворяют в 50 см 3 дистиллированной воды, добавляют 350 см 3 концентрированного раствора аммиака и проверяют pH раствора рН-метром. Если значение pH раствора отличается от величины 10,0 — 10,2, необходимо добавить раствор аммиака (при pH 10,2). На следующий день необходимо опять провести контроль pH и при необходимости довести его до нужной величины. Контроль следует осуществлять каждые 7 дней. Раствор устойчив при хранении в полиэтиленовой посуде до 4 мес.
9.1.2. Раствор 4-аминоантипирина, 2 %.
1,0 г 4-аминоантипирина растворяют в 50 см 3 дистиллированной воды, фильтруют и переносят в посуду из темного стекла. Раствор хранят в холодильнике в течение 7 дней, при комнатной температуре в темном месте не более 3 дней. Для выполнения определений пригоден раствор, имеющий бледно-желтую окраску. При появлении темно-желтой или бурой окраски следует приготовить свежий раствор реактива, либо взять другой 4-аминоантипирин.
9.1.3. Раствор гексацианоферрата (III) калия, 8 %.
4 г K3[Fе(СN)6] растворяют в 50 см 3 дистиллированной воды, фильтруют, переносят в склянку из темного стекла. Раствор хранят в холодильнике в течение 7 дней, при комнатной температуре в темном месте не более 3 дней.
9.1.4. Раствор соляной кислоты, 1:1.
К 250 см 3 дистиллированной воды приливают 250 см 3 концентрированной соляной кислоты. Раствор устойчив при хранении в плотно закрытой посуде в течение 6 мес.
9.1.5. Раствор серной кислоты, 1:1.
К 100 см 3 дистиллированной воды, помещенной в термостойкий химический стакан, при непрерывном перемешивании приливают 100 см 3 концентрированной серной кислоты. Раствор охлаждают и переносят в толстостенную склянку. Раствор устойчив при хранении в плотно закрытой склянке в течение 1 года.
9.1.6. Раствор гидроксида натрия, 1 моль/дм 3 .
40 г NaOH растворяют в 1 дм 3 дистиллированной воды. Раствор устойчив при хранении в плотно закрытой полиэтиленовой посуде в течение 3 мес.
9.1.7. Раствор гидроксида натрия, 5 моль/дм 3 .
100 г NaOH растворяют в 500 см 3 дистиллированной воды. Раствор устойчив при хранении в плотно закрытой полиэтиленовой посуде в течение 3 мес.
9.1.8. Раствор карбоната натрия, 0,1 моль/дм 3 .
10,6 г Nа2СO3 или 28,6 г Na2CO3∙10H2O растворяют в 1 дм 3 дистиллированной воды. Раствор устойчив при хранении в плотно закрытой полиэтиленовой посуде в течение 6 мес.
9.1.9. Раствор тиосульфата натрия, 0,1 моль/дм 3 .
2,5 г Na2S2O3∙5H2O растворяют в 100 см 3 дистиллированной воды. Хранят в темной склянке не более 3 мес.
9.2. Приготовление градуировочного раствора
Градуировочный раствор, аттестованный по процедуре приготовления, готовят из стандартного образца (СО) или кристаллического фенола.
При использовании СО производят разбавление исходного раствора в соответствии с инструкцией по его применению. Массовая концентрация фенола в градуировочном растворе должна составлять 5,00 мкг/см 3 . Хранят раствор в холодильнике не более 3 суток.
Приготовление градуировочного раствора из кристаллического фенола выполняют в соответствии с Приложением Б.
9.3. Построение градуировочного графика
Для построения градуировочного графика необходимо приготовить образцы для градуировки с массовыми концентрациями фенола 0 — 25,0 мкг/дм 3 . Условия проведения анализа должны соответствовать п. 7.
Состав и количество образцов для градуировки для построения градуировочного графика приведены в табл. 2.
Для всех градуировочных растворов погрешности, обусловленные процедурой приготовления, не превышают 3 % относительно приписанного значения массовой концентрации фенола.
Состав и количество образцов для градуировки
при определении летучих фенолов
Концентрация фенола, мкг/дм 3
Объем градуировочного раствора, см 3
Объем дистиллированной воды, см 3
При построении градуировочного графика в делительные воронки вместимостью 1000 см 3 помещают с помощью мерного цилиндра 800 см 3 свежепрокипяченной и быстро охлажденной дистиллированной воды и приливают градуированными пипетками вместимостью 1 и 5 см 3 аликвотные части градуировочного раствора фенола в соответствии с табл. 2.
Анализ образцов для градуировки проводят в порядке возрастания их концентрации согласно п. 11.
Оптическую плотность проб с добавками градуировочного раствора фенола и без него измеряют по отношению к бутилацетату. Каждую пробу фотометрируют 3 раза с целью исключения случайных результатов и усреднения данных.
Усредненную оптическую плотность холостого опыта (проба, не содержащая фенола) вычитают из усредненной оптической плотности проб с добавками фенола.
Градуировочный график строят в координатах: массовая концентрация фенола, мкг/дм 3 , — оптическая плотность.
9.4. Контроль стабильности градуировочной характеристики
Контроль стабильности градуировочной характеристики проводят не реже одного раза в месяц или при смене основных реактивов (4-аминоантипирина, K3[Fе(СN)6], буферного раствора). Средствами контроля являются вновь приготовленные образцы для градуировки (не менее 3 образцов из приведенных в табл. 2).
Градуировочную характеристику считают стабильной при выполнении для каждого образца для градуировки следующего условия:
│Х — С│ ≤ 1,96 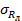
где X — результат контрольного измерений массовой концентрации фенола в образце для градуировки;
С — аттестованное значение массовой концентрации фенола в образце для градуировки;
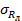
Примечание . Допустимо среднеквадратическое отклонение внутрилабораторной прецизионности при внедрении методики в лаборатории устанавливать на основе выражения: 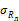
Значения σ R приведены в табл. 1.
Если условие стабильности градуировочной характеристики не выполняется только для одного образца для градуировки, необходимо выполнить повторное измерение этого образца с целью исключения результата, содержащего грубую погрешность.
Если градуировочная характеристика нестабильна, выясняют причины нестабильности градуировочной характеристики и повторяют контроль ее стабильности с использованием других образцов для градуировки, предусмотренных методикой. При повторном обнаружении нестабильности градуировочной характеристики строят новый градуировочный график.
9.5. Регенерация бутилацетата
Использованный бутилацетат собирают в отдельную склянку и затем регенерируют. Для этого слив бутилацетата помещают в делительную воронку вместимостью 1 дм 3 , добавляют равный объем дистиллированной воды и встряхивают воронку 2 мин. После расслоения фаз воду из воронки удаляют, вновь добавляют равный объем воды и повторяют промывание. Вода после второго промывания должна иметь pH не выше 7. В противном случае промывание повторяют еще раз. После отстаивания воду как можно полнее удаляют, а бутилацетат фильтруют через слой ваты или 2 — 3 неплотных бумажных фильтра в перегонную колбу. Перегоняют бутилацетат, отбирая фракцию, кипящую при 108 °С. Первые 50 — 100 см 3 отгона возвращают в слив, а остаток после отгонки (около 50 см 3 ) отбрасывают.
Мешающее влияние нафтеновых и гуминовых кислот, окрашивающих бутилацетатный экстракт в бурый или коричневый цвет, устраняют промыванием экстракта перед реэкстракцией 50 см 3 раствора карбоната натрия 0,1 моль/дм 3 в течение 1 мин.
Если в пробе присутствует активный хлор, его удаляют, добавляя эквивалентное количество раствора тиосульфата натрия и давая постоять пробе 5 мин.
Мерным цилиндром вместимостью 1000 см 3 отбирают 800 см 3 анализируемой воды и помещают ее в делительную воронку вместимостью 1000 см 3 . Добавляют 40 г хлорида натрия, 1,5 см 3 раствора серной кислоты 1:1, 50 см 3 бутилацетата и экстрагируют фенолы в течение 3 мин. Дают пробе расслоиться в течение нескольких минут, сливают воду как можно полнее, затем круговыми движениями перемешивают экстракт и вновь удаляют отслоившуюся воду.
Экстракт переносят в делительную воронку вместимостью 250 см 3 , добавляют 50 см 3 раствора гидроксида натрия 1 моль/дм 3 и реэкстрагируют фенолы в течение 1 — 1,5 мин. После расслоения нижний водный слой переносят в делительную воронку вместимостью 100 см 3 , приливают 6 — 7 см 3 раствора соляной кислоты 1:1, затем добавляют эту же кислоту по каплям до pH 7 — 9 по универсальной индикаторной бумаге. Приливают 2 см 3 буферного раствора, затем по 1 см 3 растворов 4-аминоантипирина и гексацианоферрата (III) калия, перемешивая пробу после добавления каждого раствора.
Через 5 мин добавляют 23 см 3 бутилацетата и экстрагируют окрашенное соединение в течение 1 мин. После расслоения фаз нижний водный слой отбрасывают, а экстракт перемешивают круговыми движениями и дают отстояться еще 2 — 3 мин. Вновь удаляют водную фазу, а экстракт фильтруют через комочек хлопковой или стеклянной ваты в мерную колбу или пробирку вместимостью 25 см 3 . Объем экстракта доводят до метки бутилацетатом, одновременно промывая вату, через которую фильтровали экстракт. Аналогично выполняют холостой опыт, используя 800 см 3 свежепрокипяченной и охлажденной дистиллированной воды.
В тех случаях, когда при экстракции окрашенного соединения образуется очень стойкая, не расслаивающаяся в течение 15 — 20 мин эмульсия, экстракт из делительной воронки переносят в стакан вместимостью 50 см 3 , добавляют при непрерывном перемешивании палочкой безводный сульфат натрия до тех пор, пока не образуется прозрачный экстракт. Последний осторожно сливают в мерную колбу или пробирку, а сульфат натрия в стакане промывают 1 — 2 раза небольшим количеством бутилацетата, который переносят в ту же колбу или пробирку.
Оптическую плотность экстракта измеряют в кюветах с толщиной поглощающего слоя 50 мм на спектрофотометре при λ = 470 нм или на фотометре при λ = 460 — 490 нм относительно чистого растворителя. Оптическую плотность холостого опыта вычитают из оптической плотности проб.
Если массовая концентрация фенола в анализируемой воде превышает 25 мкг/дм 3 , пробу разбавляют свежепрокипяченной дистиллированной водой и анализируют повторно. В результат определения вводят соответствующую поправку.
При анализе сильно загрязненных и сильно эмульгирующихся вод пробу следует предварительно промыть хлороформом. Для этого к пробе в делительной воронке добавляют 16 см 3 раствора NaOH 5 моль/дм 3 , хлорид натрия, затем 50 см 3 хлороформа и экстрагируют 2 мин. После расслоения фаз нижний хлороформный слой сливают, добавляют к пробе 6 см 3 раствора серной кислоты 1:1, бутилацетат и далее проводят определение, как описано выше.
При таком промывании минерализованных проб на границе раздела фаз может образоваться объемный осадок гидроксидов, затрудняющий отделение хлороформа. В этом случае отделяют хлороформ до границы осадка, затем приливают. 4 см 3 раствора серной кислоты и осторожно перемешивают пробу, не переворачивая и не встряхивая воронку. Отслоившийся хлороформ быстро удаляют, после этого приливают остальное количество раствора серной кислоты
Массовую концентрацию летучих фенолов в анализируемой пробе воды X находят по градуировочному графику.
Если перед определением проводилось разбавление пробы, результат, найденный по градуировочному графику, умножают на коэффициент K = 800/V, где V — аликвота пробы воды, взятая для анализа, см 3 .
Расхождение между результатами анализа, полученными в двух лабораториях, не должно превышать предела воспроизводимости. При выполнении этого условия приемлемы оба результата анализа, и в качестве окончательного может быть использовано их среднее арифметическое значение. Значения предела воспроизводимости приведены в таблице 3.
При превышении предела воспроизводимости могут быть использованы методы проверки приемлемости результатов анализа согласно раздела 5 ГОСТ Р ИСО 5725-6.
Значения предела воспроизводимости при вероятности Р = 0,95
Диапазон измерений (в пересчете на фенол), мкг/дм 3
Предел воспроизводимости (относительное значение допускаемого расхождения между двумя результатами измерений, полученными в разных лабораториях), R , %
источник
Разъяснения РАВВ по использованию методик выполнения измерений показателя «Фенолы (сумма)» в сточных водах
Разъяснения РАВВ по использованию методик выполнения измерений показателя «Фенолы (сумма)» в сточных водах
При проведении анализа фенолы разделяют на две группы: летучие с водяным паром (фенол, крезолы, ксиленолы и т. п.) и нелетучие (ди — и триоксисоединения). Первая группа особенно важна по её влиянию на вкус воды. Для определения фенолов первой группы проводят предварительную перегонку с водяным паром, а мешающие вещества удаляют. К примеру, осаждением. Летучие с паром фенолы более токсичны, обладают более интенсивным запахом, чем нелетучие, и потому допустимые концентрации их в водоёмах чрезвычайно малы. По этой причине при анализе вод в первую очередь определяют в них содержание группы летучих фенолов.
Согласно ст.5 гл.2 Федерального закона от 26 июня 2008 г. «Об обеспечении единства измерений» при измерении показателя «Фенолы (сумма)» в сточных водах, соответствующая Методика выполнения измерений (далее – МВИ) должна соответствовать следующим требованиям:
· Наличие МВИ в свидетельстве об аккредитации лаборатории, выполняющей измерения
Согласно ст.5 гл.2 Федерального закона от 01.01.01 г. «Об обеспечении единства измерений» для измерения показателя «Фенолы (сумма)», согласно перечню методик, включенных в реестр ПНД Ф РОСПРИРОДНАДЗОРА, существуют несколько МВИ, часть которых представлена ниже, при этом ни одна из МВИ не обладает приоритетом при использовании:
· Методика выполнения измерения массовой концентрации фенола и его нормируемых нитропроизводных в пробах сточных вод методом ВЭЖХ с предварительным сорбционным концентрированием ПНД Ф 14.1.80-96
· Методика выполнения измерений массовой концентрации фенола в питьевых, природных и сточных водах методом жидкостной хроматографии ПНД Ф 14.1:2:4.170-2000 (изд. 2006 г.)
· Методика измерений массовой концентрации фенола в пробах питьевых, природных и сточных вод методом газожидкостной хроматографии ПНД Ф 14.1:2:4.177-02 (издание 2011 г.)
· Методика измерений массовой концентрации фенолов (общих и летучих) в пробах природных, питьевых и сточных вод флуориметрическим методом на анализаторе жидкости «Флюорат‑02» ПНД Ф 14.1:2:4.182-02 (издание 2010 г.)
· Методика измерений массовых концентраций фенола и фенолопроизводных в питьевых, природных и сточных водах газохроматографическим методом ПНД Ф 14.1:2:4.225-2006 (издание 2013 г.)
· Методика измерений массовой концентрации летучих фенолов в питьевых, поверхностных, подземных пресных и сточных водах газохроматографическим методом ПНД Ф 14.1:2:3:4.244-2007 (издание 2011 г.)
Каждая из представленных методик может быть использована в рамках области значений и области аккредитации для выполнения измерения показателя «Фенолы (сумма)». Данных по официальному установлению той или иной МВИ в качестве референтной при возникновении споров хозяйствующих субъектов у Российской ассоциации водоснабжения и водоотведения нет. Тем не менее, некоторые МВИ, например определение ряда фенолов в поверхностных и сточных водах методом ВЭЖХ с электрохимическим детектированием, применяют в научных исследованиях и при проведении арбитражных анализов (в качестве референтных методик), поскольку они являются универсальными (пригодны для вод любого типа, позволяют определять любые фенолы) и дают весьма точные результаты. Недостатком данных способов является необходимость использования сложного и дорогостоящего хроматографического оборудования, трудоемкость и длительность анализа.
При использовании различных МВИ для определения показателя «Фенолы (сумма)» необходимо учитывать область аккредитации для лаборатории, проводящей анализы. Так, к примеру, если область аккредитации касается только следующий веществ: крезолы, ксиленолы, алкил — и изоалкилфенолы, то речь идет об определении летучих фенолов. В тоже самое время, определение общих фенолов, т. е. показателя «Фенолы (сумма)», подразумевающего определение общих и летучих фенолов, должно быть отдельно прописано в области аккредитации лаборатории.
источник
Н астоящий документ устанавливает методику количественного химического анализа проб природных и очищенных сточных вод для определения в них массовой концентрации летучих фенолов в диапазоне от 2 до 30 мкг/дм 3 в пересчете на фенол фотометрическим методом после отгонки с водяным паром без разбавления и концентрирования пробы.
Е сли массовая концентрация летучих фенолов в анализируемой пробе превышает верхнюю границу, допускается разбавление пробы таким образом, чтобы концентрация фенолов соответствовала регламентированному диапазону.
М ешающие влияния на определение фенолов могут оказать сильные восстановители (например, сульфиты) при концентрациях более 5 мг/дм 3 , а также способные отгоняться с паром окрашенные соединения кислого характера. При отгонке окрашенной пробы наличие мешающего влияния окрашенных органических соединений обнаруживают по окраске отгона или хлороформного экстракта из него без добавления раствора 4-амино-антипирина.
М ешающее влияние других веществ устраняется в процессе отгонки.
Ф отометрический метод определения массовой концентрации летучих фенолов основан на отгонке фенолов из подкисленной пробы воды, взаимодействии фенолов в отгоне с 4-аминоантипирином в присутствии гексацианоферрата ( III ) калия и экстракции образующегося окрашенного соединения хлороформом. Оптическую плотность экстракта измеряют на спектрофотометре (λ = 470 нм) или фотометре со светофильтром, имеющим максимум пропускания в диапазоне λ = 460 — 490 нм.
Н астоящая методика обеспечивает получение результатов анализа с погрешностью, не превышающей значений, приведённых в таблице 1 .
З начения показателя точности методики используют при:
— оформлении результатов анализа, выдаваемых лабораторией;
— оценке деятельности лабораторий на качество проведения испытаний;
— оценке возможности использования результатов анализа при реализации методики в конкретной лаборатории.
Д иапазон измерений, значения показателей точности, повторяемости, воспроизводимости, правильности
Показатель точности (границы относительной погрешности при вероятности Р = 0,95), ± δ, %
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости), σr, %
Показатель воспроизводимости (относительное среднеквадратическое отклонение воспроизводимости), σR , %
Показатель правильности (границы относительной систематической погрешности при вероятности Р = 0,95), ± δc , %
Кюветы с толщиной поглощающего слоя 50 мм
Весы лабораторные общего назначения с наибольшим пределом взвешивания 200 г и ценой наименьшего деления 0,1 мг любого типа
Весы лабораторные общего назначения с наибольшим пределом взвешивания 200 г и ценой наименьшего деления 10 мг любого типа
СО с аттестованным содержанием фенола с погрешностью не более 1 % при Р = 0,95 (или фенол, п. 4.3 )
рН-метр или иономер с погрешностью измерения рН не более 0,05 единиц рН
Термометр с диапазоном 0 — 100 °С
Шкаф сушильный лабораторный с температурой нагрева до 130 °С
Стаканчики для взвешивания (бюксы)
Установки для отгонки фенолов (колбы плоскодонные П-1-1000-29/32 ТХС, переход П1-1-29/32-14/23 ТС, каплеуловитель с отводом КО-14/23-100, холодильник ХПТ-3-400-14/23 ХС)
Колбы конические или плоскодонные
Колба для перегонки КП-1-50-19/26 ТХС
Установка из стекла для перегонки растворителей в составе: колба К-1-1000-29/32 ТС, дефлегматор 350-19/26-29-32 ТС, холодильник ХПТ-1-400-14/23 ХС
С редства измерений должны быть поверены в установленные сроки.
Д опускается использование других, в том числе импортных, средств измерений и вспомогательных устройств с характеристиками не хуже, чем у приведенных в п.п. 4.1 и 4.2 .
Аммиак водный, концентрированный
Гексацианоферрат ( III ) калия К3 [Fe( CN )6]
Тиосульфат натрия, пентагидрат
Бумага индикаторная универсальная
Фильтры обеззоленные «белая лента»
В се реактивы, используемые для анализа, должны быть квалификации ч.д.а. или х.ч.
Д опускается использование реактивов, изготовленных по другой нормативно-технической документации, в том числе импортных, с квалификацией не ниже ч.д.а.
5.1 . При выполнении анализов необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007 .
5.2 . Электробезопасность при работе с электроустановками обеспечивается по ГОСТ 12.1.019 .
5.3 . Организация обучения работающих безопасности труда проводится по ГОСТ 12.0.004 .
5.4 . Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004 и иметь средства пожаротушения по ГОСТ 12.4.009 .
В ыполнение измерений может производить химик-аналитик, владеющий техникой экстракционно-фотометрического анализа и изучивший инструкцию по эксплуатации спектрофотометра или фотометра.
П ри выполнении измерений в лаборатории должны быть соблюдены следующие условия:
• относительная влажность не более 80 % при температуре 25 °С;
8.1 . Отбор проб производится в соответствии с требованиями ГОСТ Р 51592-2000 «Вода. Общие требования к отбору проб».
8.2 . Посуду, предназначенную для отбора и хранения проб, промывают насыщенным раствором кальцинированной соды (карбоната натрия), а затем дистиллированной водой. При мытье сильно загрязненной посуды рекомендуется использовать хромовую смесь, после чего тщательно (не менее 20 раз) промывать водопроводной водой и споласкивать дистиллированной водой.
8.3 . Пробы воды отбирают в стеклянные бутыли с плотно завинчивающимися пробками вместимостью 1 дм 3 .
О бъем отбираемой пробы должен быть не менее 1 дм 3 .
8.4 . Пробы анализируют не позднее, чем через 4 часа после отбора или в течение суток при условии хранения в холодильнике при t
8.5 . При отборе проб составляется сопроводительный документ по утвержденной форме, в котором указывается:
— цель анализа, предполагаемые загрязнители,
— должность, фамилия отбирающего пробу, дата.
9.1.1 . Аммонийно-аммиачный буферный раствор с рН 10,0 — 10,2.
50 г хлорида аммония растворяют в 50 см 3 дистиллированной воды, добавляют 350 см 3 концентрированного раствора аммиака и проверяют рН раствора рН-метром. Если значение рН раствора отличается от величины 10,0 — 10,2, необходимо добавить раствор аммиака (при рН 10,2). На следующий день необходимо опять провести контроль рН и при необходимости довести его до нужной величины. Контроль следует осуществлять каждые 7 дней. Раствор устойчив при хранении в полиэтиленовой посуде до 4 мес.
1 ,0 г 4-аминоантипирина растворяют в 50 см 3 дистиллированной воды, фильтруют и переносят в посуду из темного стекла. Раствор хранят в холодильнике в течение 7 дней, при комнатной температуре в темном месте не более 3 дней. Для выполнения определений пригоден раствор, имеющий бледно-желтую окраску. При появлении темно-желтой или бурой окраски следует приготовить свежий раствор 4-аминоантипирина, либо взять реактив из другой партии.
4 г K 3 [ Fe (СN)6] растворяют в 50 см 3 дистиллированной воды, фильтруют, переносят в склянку из темного стекла. Раствор хранят в холодильнике в течение 7 дней, при комнатной температуре в темном месте не более 3 дней.
К 450 см 3 дистиллированной воды, помещенной в термостойкий химический стакан, при непрерывном перемешивании приливают 28 см 3 концентрированной серной кислоты и охлаждают. Раствор устойчив при хранении в плотно закрытой склянке в течение 1 года.
50 г CuSO 4 · 5 H 2 O растворяют в 450 см 3 дистиллированной воды. Раствор устойчив в течение 6 мес.
9.1.6 . Раствор гидроксида натрия, 0,05 моль/дм 3 .
2 г NaOH растворяют в 1 дм 3 дистиллированной воды. Раствор устойчив при хранении в плотно закрытой полиэтиленовой посуде в течение 3 мес.
9.1.7 . Раствор тиосульфата натрия, 0,1 моль/дм 3 .
2 ,5 г Na 2 S 2 O 3 · 5H 2 O растворяют в 100 см 3 дистиллированной воды. Хранят в темной склянке не более 3 мес.
Г радуировочный раствор, аттестованный по процедуре приготовления, готовят из стандартного образца (СО) или кристаллического фенола.
П ри использовании СО производят разбавление исходного раствора в соответствии с инструкцией по его применению. Массовая концентрация фенола в градуировочном растворе должна составлять 5,00 мкг/см 3 . Хранят раствор в холодильнике не более 3 суток.
П риготовление градуировочного раствора из кристаллического фенола выполняют в соответствии с Приложением Б .
Д ля построения градуировочного графика необходимо приготовить образцы для градуировки с массовыми концентрациями фенола 0 — 30,0 мкг/дм 3 . Условия проведения анализа должны соответствовать п. 7 .
С остав и количество образцов для градуировки для построения градуировочного графика приведены в табл. 2 .
Д ля всех градуировочных растворов погрешности, обусловленные процедурой приготовления, не превышают 3 % относительно приписанного значения массовой концентрации фенола.
С остав и количество образцов для градуировки при определении летучих фенолов
Концентрация фенола, мкг/дм 3
Объем градуировочного раствора, см 3
Объем дистиллированной воды, см 3
П ри построении градуировочного графика в делительные воронки вместимостью 1000 см 3 помещают с помощью цилиндра 500 см 3 свежепрокипяченной и быстро охлажденной дистиллированной воды и приливают градуированными пипетками вместимостью 1 и 5 см 3 аликвотные части градуировочного раствора фенола в соответствии с табл. 2 .
А нализ образцов для градуировки проводят в порядке возрастания их концентрации согласно п. 10 .
О птическую плотность проб с добавками градуировочного раствора фенола и без него измеряют по отношению к хлороформу. Каждую пробу фотометрируют 3 раза с целью исключения случайных результатов и усреднения данных. Усредненную оптическую плотность холостого опыта (проба, не содержащая фенола) вычитают из усредненной оптической плотности проб с добавками фенола.
Г радуировочный график строят в координатах: массовая концентрация фенола, мкг/дм 3 , — оптическая плотность.
К онтроль стабильности градуировочной характеристики проводят не реже одного раза в месяц или при смене основных реактивов (4-амино-антипирина, K 3 [ Fe (CN)6], буферного раствора). Средствами контроля являются вновь приготовленные образцы для градуировки (не менее 3 образцов из приведенных в табл. 2 ).
Г радуировочную характеристику считают стабильной при выполнении для каждого образца для градуировки следующего условия:
где X — результат контрольного измерения массовой концентрации фенола в образце для градуировки;
С — аттестованное значение массовой концентрации фенола в образце для градуировки;
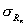
Примечание. Допустимо среднеквадратическое отклонение внутрилабораторной прецизионности при внедрении методики в лаборатории устанавливать на основе выражения: 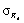
З начения σR приведены в таблице 1 .
Е сли условие стабильности градуировочной характеристики не выполняется только для одного образца для градуировки, необходимо выполнить повторное измерение этого образца с целью исключения результата, содержащего грубую погрешность.
Е сли градуировочная характеристика нестабильна, выясняют причины ее нестабильности и повторяют контроль стабильности с использованием других образцов для градуировки, предусмотренных методикой. При повторном обнаружении нестабильности градуировочной характеристики строят новый градуировочный график.
И спользованный хлороформ собирают в отдельную склянку и затем регенерируют. Для этого слив хлороформа помещают в делительную воронку вместимостью 1 дм 3 , добавляют равный объем дистиллированной воды и встряхивают воронку 2 мин. После расслоения фаз хлороформ переносят в другую воронку, вновь добавляют равный объем воды и повторяют промывание. После отстаивания хлороформ фильтруют через слой ваты или 2 — 3 неплотных бумажных фильтра в перегонную колбу. Перегоняют хлороформ, отбирая фракцию, кипящую при t = 60,5 — 62,0 °С. Первую порцию отгона, кипящую ниже 60,5 °С, возвращают в слив, а остаток после отгонки отбрасывают.
М ерным цилиндром отбирают 500 см 3 анализируемой воды и помещают ее в колбу для отгонки. Если в пробе присутствует активный хлор, приливают эквивалентное количество раствора тиосульфата натрия и дают постоять 5 мин. Добавляют 5 см 3 10 % раствора сульфата меди и 10 см 3 10 % раствора серной кислоты. Колбу помещают на электроплитку, присоединяют каплеуловитель и холодильник. Для уменьшения теплообмена колбу оборачивают стеклотканью. Выходной отросток холодильника опускают в колбу вместимостью 500 см 3 , в которую предварительно помещают 10 см 3 раствора гидроксида натрия 0,05 моль/дм 3 . Нижний конец трубки холодильника должен быть погружен в этот раствор. При необходимости его можно удлинить, пристыковав вплотную к трубке холодильника стеклянную трубку нужной длины.
Н агрев колбы должен быть достаточно сильным так, чтобы время отгонки пробы не превышала 3 ч, однако кипение пробы должно быть равномерным, спокойным; бурное кипение недопустимо. По мере увеличения объема отгона колбу опускают так, чтобы трубка холодильника была погружена в отгон не более, чем на 3 см. Когда объем отгона в колбе составит около 460 см 3 (на колбе заранее следует сделать соответствующую метку), отгонку прекращают.
О тгон переносят в делительную воронку вместимостью 1000 см 3 , споласкивают колбу 30 — 40 см 3 дистиллированной воды и переносят ее в ту же воронку. Прибавляют 10 см 3 буферного раствора, 3 см 3 2 % раствора 4-аминоантипирина и 3 см 3 8 % раствора гексацианоферрата (III) калия, перемешивая пробу после добавления каждого раствора. Оставляют пробу на 10 — 15 мин, затем дважды экстрагируют ее хлороформом, используя для первой экстракции 20 см 3 , второй — 10 см 3 хлороформа. Первую экстракцию выполняют в течение 2 мин, вторую — 1 мин. После расслоения фаз хлороформные экстракты фильтруют через комочек хлопковой или стеклянной ваты в мерную колбу или градуированную пробирку вместимостью 25 см 3 и доводят объем до метки хлороформом. Оптическую плотность экстракта измеряют на спектрофотометре при длине волны 460 нм или фотометре при длине волны 460 — 490 нм в кюветах с толщиной поглощающего слоя 50 мм.
О дновременно с пробами выполняют холостой опыт, используя 500 см 3 свежепрокипяченной дистиллированной воды. Оптическую плотность холостого опыта вычитают из оптической плотности проб.
Е сли содержание фенолов превышает 30 мкг/дм 3 , для отгонки берут меньшую аликвоту анализируемой воды и разбавляют ее свежепрокипяченной дистиллированной водой до объема 500 см 3 .
М ассовую концентрацию летучих фенолов в анализируемой пробе воды X находят по градуировочному графику.
Е сли перед определением проводилось разбавление пробы, результат, найденный по градуировочному графику, умножают на коэффициент К = 500/ V , где V — аликвота пробы воды, взятая для анализа, см 3 .
Р асхождение между результатами анализа, полученными в двух лабораториях, не должно превышать предела воспроизводимости. При выполнении этого условия приемлемы оба результата анализа, и в качестве окончательного может быть использовано их среднее арифметическое значение.
З начения предела воспроизводимости приведены в таблице 3 .
П ри превышении предела воспроизводимости могут быть использованы методы проверки приемлемости результатов анализа согласно раздела 5 ГОСТ Р ИСО 5725-6 .
З начения предела воспроизводимости при вероятности Р = 0,95
Предел воспроизводимости (относительное значение допускаемого расхождения между двумя результатами измерений, полученными в разных лабораториях), R, %
источник
