Иммуногистохимическое исследование (ИГХ) – основа современной морфологической диагностики опухолевых заболеваний, определяющая правильность постановки диагноза, дальнейший прогноз и, в ряде случаев, формирования показаний для назначения таргетной терапии.
Основная цель ИГХ исследования – определение дифференцировки и гистогенеза (тканевой принадлежности) опухоли.
Иммуногистохимическое исследование (ИГХ) — дополнительный метод диагностики, применяемый в дополнение к основной гистологической окраске гематоксилином и эозином, который позволяет выявлять и дифференцировать доброкачественные и злокачественные новообразования. Зачастую постановка окончательного диагноза, кроме специфической морфологической картины, требует уточнения иммунофенотипа или биологических свойств опухоли, которые играют важную роль в прогнозе заболевания и определения показаний для назначения препаратов таргетного ряда. На сегодняшний день современная наука смогла доказать, что именно определение биологических свойств опухоли и обнаружение генетических детерминант (генетических свойств опухоли), является залогом успешного лечения в онкологии.
В последнее время ИГХ анализ стал широко применяться в каждодневной диагностической практике врачей патологоанатомов и перестал быть методом сугубо научных исследований.
Основная цель ИГХ исследования – определение дифференцировки и гистогенеза (тканевой принадлежности) опухоли.
1. Гистогенез опухоли — это ее тканевое происхождение. Выяснение этого факта имеет важное диагностическое значение и позволяет подобрать обоснованное лечение. Ведь от происхождения опухоли зависит ее чувствительность к процедурам химической или лучевой терапии.
2. Степень дифференцировки показывает, насколько опухолевая клетка отличается от нормальной по строению и функциям.
В зависимости от степени дифференцировки клетки опухолевого субстрата бывают:
- дифференцированные, когда строение опухоли максимально приближено к структуре ткани-предшественника;
- малодифференцированные, сходство которых с исходной тканью стерто;
- недифференцированные (анаплазия) — клетки, утратившие какое-либо сходство с нормальными (исходными).
- Гистологическая диагностика опухолей;
- Определение нозологического варианта опухоли;
- Возможность определения первичной опухоли по метастазу;
- Определение прогноза опухолевого заболевания;
- Определение возможностей и показаний к таргетной терапии и др.
Возможности иммуногистохимического исследования в современной практической онкологии выглядят следующим образом:
Этот тест назначают при подозрении на наличие опухолевого заболевания. Материал для исследований берут во время оперативного вмешательства или методом биопсии с помощью специальных щипцов и игл. Из ткани делают тонкий микросрез, который затем обрабатывают раствором специфических антител (иммуногистохимические препараты), которые вступают в реакцию с белками опухоли (антигены). Прореагировавшие участки излучают свечение различной интенсивности, на основании чего врач делает выводы.Например, наличие экспрессии клетками опухоли таких маркеров как CD15 и CD30 позволяет поставить диагноз лимфома Ходжкина; CD117– гастроинтестинальные стромальные опухоли; CD20 – В-клеточные лимфомы; CD3 – Т-клеточные лимфомы; HMB45, MelanА – меланома и др.
Для ИГХ анализа первичных опухолей и их метастазов используется широкий спектр маркеров — антител (маркер – индикатор нормальных биологических процессов, патогенных процессов или фармакологического ответа к терапевтическому вмешательству, который может быть объективно измерен и оценен). Антитела бывают цитоспецифичные, тканеспецифичные, могут отражать процессы клеточной пролиферации и ассоциированные с опухолью антигены и, наконец, могут являться собственно опухолевыми маркерами, такими как онкофетальные антигены, ферменты, белковые продукты клеточных онкогенов и др.
В нашей лаборатории имеется исчерпывающий набор антител, одобренных к применению в качестве диагностических тестов опухолевых и неопухолевых поражений различных органов и систем.
Количество используемых антител зависит от конкретного случая и предполагаемого диагноза. «Расширенная панель антител» — это набор антигенов к разным опухолевым структурам. Существует также «малая панель», где представлены самые распространенные опухоли. Выбор панели антител может происходить двояко: поэтапно, постепенно увеличивая их спектр, либо можно сразу применять широкую панель реагентов. С одной стороны значительная экономия реактивов и средств с более высокими трудозатратами и длительным сроком выполнения, с другой – большой расход антител, часть которых помогает установить окончательный диагноз в кротчайшие сроки.
Специалисты нашей лаборатории приверженцы того, что ИГХ анализ, являясь дополнительным методом, должен включать как положительные результаты экспрессии маркеров, характеризующие определенный иммунофенотип опухоли, так и отрицательные, что дает возможность исключить другие гипотезы и свести объем диагностических ошибок к минимуму.
Рак молочной железы является наиболее часто встречающимся видом рака у женщин и второй по частоте причиной смерти, связанной с раком. Ранняя диагностика, своевременно и правильно проведенное лечение могут значительно повысить шансы на выздоровление. Традиционные техники иммуногистохимии (ИГХ) позволяют работать с очень небольшими образцами ткани. Это обстоятельство в сочетании с применением антител, специфичных по отношению к антигенам опухолевых клеток, делает данный метод эффективным средством в руках патоморфолога, занимающегося диагностикой и прогнозированием течения онкологических заболеваний.
Основные диагностические маркеры:
- Estrogen Receptor
- Progesterone Receptor
- HER-2/neu
- Ki-67
- p120 Catenin
- CadherinE
- «Золотой стандарт» диагностики опухолей молочной железы — гормональный профиль PR, ER, HER-2/neu, Ki-67 — это диагностика всех доступных рецепторов, которые отвечают за активность раковой ткани. Включает в себя исследование нескольких показателей.
- PR, ER — это специфические белки-рецепторы, которые реагируют на выработку эстрогенов и прогестерона. Большинство раковых образований молочной железы (около 80 процентов) активно реагируют на изменения фона гормонов. Определение реактивности этих рецепторов играет важнейшую роль при оценке возможностей терапии гормонами.
- HER-2/neu — это генная белковая структура, которая расположена в раковой ткани. Представляет собой рецептор, который реагирует на выработку специфических антител. Исследовать данный параметр целесообразно с точки зрения определения прогноза лечения рака. При высокой активности HER-2/neu опухоль плохо поддается лечению, требуется сначала моноклональная терапия, направленная на подавление активности этой структуры.
- Ki-67 — это белковая структура, обладающая способностью активизироваться при активном росте опухоли. Исследование этого показателя дает возможность оценить прогноз для жизни больного. Чем выше экспрессивные характеристики Ki-67, тем меньше опухолевая дифференцировка, тем меньше шансов у больной женщины на выздоровление.
Рак предстательной железы – одно из самых распространенных онкологических заболеваний в мире. Большинство случаев (50 – 70%) диагностируется на 3-4 стадиях, в том числе 25% — с генерализацией опухолевого процесса. К сожалению, ранняя диагностика рака затруднена из-за частого отсутствия характерных симптомов. Наряду с клиническими методами, наиболее информативным является метод гистологического исследования биоптатов предстательной железы.
Основные диагностические маркеры:
Рак легкого является одной из наиболее частых причин смерти. В мире ежегодно от данного заболевания умирает около 1 миллиона человек. У мужчин рак легкого в 85-90% случаев связан табакокурением. Прогноз при раке легкого остается неблагоприятным. При отсутствии лечения с момента установления диагноза в течение 2 лет погибает до 90 % больных. При хирургическом лечении 5-летняя выживаемость составляет около 30%. Хирургическое лечение в сочетании с лучевой и медикаментозной терапией увеличивает 5-летнюю выживаемость на 40 %. Наличие метастазов значительно ухудшает прогноз. Современная диагностика и лечение больных раком легкого не может обходиться без морфологической верификации опухоли с уточнением гистологической структуры и степени анаплазии (дифференцировки) опухолевых клеток. Иммуногистохимический метод остается одним из самых информативных методов на данном этапе диагностики
Основные диагностические маркеры:
Мелано́ма (лат. melanoma, melanoma malignum от др.-греч. μέλας — «черный») (уст. Меланобластома) — злокачественная опухоль, развивающаяся из меланоцитов — пигментных клеток, продуцирующих меланины. Одна из трёх разновидностей рака кожи, и самая опасная из них. Преимущественно локализуется в коже, реже — сетчатке глаза, слизистых оболочках (полость рта, влагалище, прямая кишка). Одна из наиболее опасных злокачественных опухолей человека, часто рецидивирующая и метастазирующая лимфогенным и гематогенным путем почти во все органы. Верификация меланомы кожи и ее метастазов остается одной из наиболее сложных задач для онкоморфолога. Среди беспигментных меланом встречаются узловые, поверхностно-распространяющиеся, типа лентиго, светлоклеточные, веретеноклеточные, плеоморфные, мелкоклеточные, миксоидые, «невоидные», перстевидноклеточные и другие формы.
Основные диагностические маркеры:
- MelanomaAssociatedAntigen (MAA);
- CD63;
- Melanoma Marker (HMB45);
- MART-1/Melan-A;
- Melanoma (gp100);
- Tyrosinase;
- Microphthalmia Transcription Factor (MiTF);
- Nerve Growth Factor Receptor (NGFR);
- S100;
- Melanoma Pan (HMB45 + A103 + T311);
- MART-1 + Tyrosinase;
- Vimentin.
Стандартная панель содержит около пяти иммуногистохимических маркеров:
- р53 — степень активности митоза меланомы;
- Ki-67 — оценка интенсивности пролиферации, определяет прогноз болезни;
- bcl-2 — белок, который препятствует естественному апоптозу меланомы кожи, оценивается вероятность метастазирования;
- HMB-45 — оценка функции меланоцитов;
- S-100 — типичный антиген, встречающийся только при меланоме, позволяющий отличить от других опухолей или доброкачественных образований.
Лимфома – злокачественное опухолевое заболевание лимфатической системы. Среди лимфом выделяют лимфогранулематоз (лимфому Ходжкина) и все остальные виды лимфом — неходжкинские лимфомы (НХЛ). По тому, из каких именно видов лимфоидных клеток возникает опухоль, выделяют В-, Т- и (редко) NK-клеточные лимфомы. Большинство лимфом – В-клеточные. Диагностика лимфопролиферативных заболеваний в настоящее время занимает передовые позиции в современной патологии и требует одну из самых обширных панелей маркеров. Суммарная заболеваемость всеми видами неходжкинских лимфом в европейских странах составляет 12-15 случаев на 100 тысяч населения в год. Риск их возникновения увеличивается с возрастом. Инфицирование вирусом Эпштейна-Барр связано с повышенным риском заболевания различными видами лимфом, включая лимфому Беркитта. У детей неходжкинские лимфомы сравнительно редки: к детскому и подростковому возрасту относится не более 5% всех случаев НХЛ. Однако все же лимфомы занимают в структуре злокачественных заболеваний детского возраста третье место по частоте – после лейкозов и опухолей центральной нервной системы.
Основные диагностические маркеры:
СОЖКТ возникают преимущественно в желудке (60 %) и тонком кишечнике (25 %), но также наблюдаются в прямой кишке (5 %), пищеводе (5 %) и ряде других мест (5 %), в том числе аппендикс, желчный пузырь, мезентерий и сальнике. Возраст заболевших пациентов колеблется в диапазоне от подросткового возраста до 90-летних, но большинство больных старшего возраста с пиком около 60 лет. В большинстве исследований наблюдается незначительная предрасположенность мужчин. В 1998 было показано, что СОЖКТ экспрессирует тирозинкиназный рецептор KIT (CD117). Причиной возникновения этих опухолей оказались интерстициальные клетки Кахаля (ICC). Подобно СОЖКТ, клетки Кахаля экспрессируют KIT и большинство положительно на CD34. Последующие исследования с большим числом разных лабораторий подтвердили, что KIT – это единственный наиболее специфичный маркер СОЖКТ. Иммуноопределяемый KIT присутствует на клеточной поверхности и/или в цитоплазме опухолевых клеток СОЖКТ приблизительно в 90 % случаев. В подавляющем большинстве опухолей экспрессия KIT бывает сильной и однородной, но в некоторых случаях демонстрируется только фокальная положительная реактивность и KIT отсутствует в небольшой подгруппе (
5%) опухолей, которые по другим мофологическим и иммунофенотипическим признакам соответствуют СОЖКТ. Среди KIT-положительных СОЖТК экспрессия CD34 определяется в 60-70 % случаев, тогда как 30-40 % имеют положительную реакцию на гладкомышечный актин (SMA), а 5% — на белок S-100. Ни один из этих антигенов не является специфичным для СОЖКТ. Экспрессия десмина в истинных KIT-положительных СОЖКТ является крайне редкой (1-2 % случаев) и обычно фокальной. Данная форма онкологических заболеваний тяжело поддается морфологической диагностике. Используя современные панели маркеров возможно четко и обоснованно диагностировать разные формы описываемой патологии. Иммуногистохимическоее исследование является обязательным.
Основные диагностические маркеры:
Колоректальный рак является третьим по частоте диагностируемым раком в Соединенных Штатах (за исключением рака кожи) среди мужского и женского населения. Показатели заболеваемости колоректальным раком снижаются на протяжении последних двух десятилетий (с 66,3 случаев на 100000 человек в 1985 году до 45,5 случаев в 2006 году). Это связывают с увеличением использования колоректальных скрининг-тестов, которые позволяют обнаруживать и удалять полипы ЖКТ до их перерождения в рак. В отличие от общего сокращения, среди взрослого молодого населения в возрасте до 50 лет, для которого скрининг не рекомендуется из-за средней степени риска, заболеваемость раком ободочной и прямой кишки увеличивались с 1994 года примерно на 2% в год у мужчин и женщин. В 2016 году США смертность от колоректального рака составила 49500 случаев. Смертность от колоректального рака снизились в обоих группах мужчин и женщин за последние несколько десятилетий, с более крутым снижением в последний период времени. Это снижение отражает снижение показателей заболеваемости и улучшение ранней диагностики и лечения. Ранние стадии рака ободочной и прямой кишки обычно не имеют симптомов, поэтому, чтобы выявить заболевание на этой ранней стадии часто необходим скрининг. Прогрессирование болезни может вызвать кровотечение из прямой кишки, появление крови в кале, изменение в опорожнении кишечника, схваткообразные боли в нижней части живота. Применение ИГХ при раках толстого кишечника рассматривается на нескольких уровнях: для характеристики опухолей (эндокринный или эпителиальный тип), наследственной предрасположенности и для целей прогноза. Преобладающее использование ИГХ — это определение возможных или предполагаемых метастазов, в которых толстой кишки является возможным первичным. Типичной локализацией для метастазов толстой кишки являются печень и легкие, оба органа, которые могут производить морфологию рака идентичную метастазам из толстой кишки. ИГХ, (класс I правил регулирования FDA), используется после первичной диагностики опухоли путем гистопатологического исследования и не включается для клиницистов как независимое исследование.
Основные диагностические маркеры:
Наиболее часто применение иммуногистохимии в изучении опухолей печени – это определение источника метастаза, когда первичная локализация опухоли не известна. Развитие и применение панели для иммунных окрашиваний может помочь решить почти все диагностические проблемы. 2-6 Цитокератины (CK) 7 и CK 20 – первая ступень в идентификации многих опухолей и с дополнительными иммунными реакциями относительно специфичными для опухолей женского и мужского полового тракта, нередко дает возможность идентифицировать первичную локализацию метастатической опухоли.
Основные диагностические маркеры:
- Цитокератины различного молекулярного веса (CK 18, CK 19, CK 7, и CK 20 и др.).
Также в диагностическую панель рекомендуется включать ИГХ тесты, направленные на экспрессию НER2/neu и Ki-67.
- НER2/neu — представляет собой мембранный белок, который кодируется геном ERBB2. Повышение его экспрессии имеет важное значение в патогенезе и прогрессировании определенных злокачественных процессов. Тестирование данного рецептора является важным биологическим маркером рака желудка, молочной железы, матки и ее придатков.;
- Ki-67 — ядерный антиген, состоящий из двух полипептидных цепей и являющийся основной частью нуклеарного матрикса. Его экспрессия позволяет выделить пролиферирующие клетки опухолевидного образования, которые находятся в активной фазе жизненного цикла клетки. Данный маркер позволяет определить фенотип и скорость роста опухоли, риск ее метастазирования, потенциальную ответную реакцию на лечебные мероприятия и исход патологического процесса.
Иммуногистохимические исследования (ИГХ) , как правило, не требуются для оценки доброкачественных и злокачественных эпителиальных опухолей желудка, так как гистопатология, как правило, обеспечивает диагностику, но ИГХ нужна при изучении метастатического рака желудка, когда источник происхождения опухоли не ясен, или когда макроскопические / рентгенологическое проявления опухоли сбивают с толку (например, рак желудка напрямую и широко прорастает в печень и гистологически неотличим от холангиокарциномой). К тому же, ИГХ может быть полезна для идентификации некоторых вариантов желудочных карцином, включая гепатоидную аденокарциному, в которой печеночная дифференцировка может быть подтверждена позитивной реакцией на альфа-фетопротеин AFP. Аденокарциномы желудка будут реагировать со многими антителами против кератинов, включая, CK 18, CK 19, CK 7, и CK 20. Когда CK 7 и CK 20 используются вместе, многие аденокарциномы желудка будут окрашиваться как CK 7 так и CK 20. Примерно 25% случаев будет иметь фенотип CK 7 + / CK 20-, или CK 7- / CK 20+), и небольшое число случаев будет отрицательным для обоих маркеров. Первоначально считалось, что CDX-2 — специфический маркер для рака толстой кишки, будет реактивными в более чем 50% случаев и может быть свидетельством меньшей степени инвазивности. Аденокарцинома желудка, как кишечного типа, так и типа перстневидноклеточной карциномы, могут иметь нейроэндокринную дифференцировку и что может быть не очевидно по гистологической картине, но проявляться по окрашиванию хромогранином и /или синаптофизином
Иммуногистохимическое (ИГХ) определение экспрессии рецептора EGFR при колоректальном раке и опухолях легкого, а также при опухолях шеи и головы, проводят для адекватного выбора схем химиотерапевтического лечения.
EGFR (Epidermal Growth Factor Receptor) является одним из трансмембранных рецепторов, экспрессируется на поверхности эпителиальных клеток и принимает участие в регуляции роста клеток и дифференцировки. Деление клеток в его присутствии происходит намного быстрее. При активации рецептора EGFR после связывания с факторами роста (EGF и TGF-a), запускаются механизмы, которые приводят к росту опухоли и пролиферация раковых клеток повышается, также стимулируется процесс метастазирования.Экспрессия EGFR — это показатель, свидетельствующий о том, что рост опухоли стимулируется деятельностью рецептора эпидермального фактора роста. Так как активация рецептора происходит за счет веществ самого новообразования, то правильнее будет говорить о экспрессии EGFR опухолью.Экспрессия EGFR обнаружена при следующих формах рака: легких, шеи и головы, толстой и прямой кишки. Иммуногистохимическое определение экспрессии EGFR позволяет установить статус этих рецепторов и назначить лечение. Экспрессия EGFR напрямую связана со степенью злокачественности и стадией развития опухоли.Специалист в соответствии с полученными данными иммуногистохимического исследования классифицирует опухоль как EGFR-отрицательную или EGFR-положительную.
Гиперэкспрессия EGFR говорит о высокой злокачественности, поздних сроках развития опухоли и метастатических процессах. Этот фактор является неблагоприятным в отношении прогноза болезни и свидетельствует о высокой пролиферативной активности опухоли, агрессивности, устойчивости к проводимой терапии.
Низкая степень экспрессии EGFR свидетельствует о регрессе опухоли положительной динамике в лечении.
Иммуногистохимическое исследование рецепторной чувствительности к эстрогенам и прогестерону в эндометрии
Иммуногистохимическое исследование рецепторной чувствительности к эстрогенам и прогестерону в эндометрии проводится для выявления причин отсутствия фертильности, а также для оценки злокачественности процессов в тканях матки. Исследование сложное, проводится планово, необходима соответствующая квалификация патологоанатома.
Рецепторы к эстрогенам (ER) и прогестерону (PR) — это чувствительные маркеры, которые реагируют на колебания некоторых гормонов, влияющих на рост опухолей и развитие гиперпластических процессов в эндометрии. Расположены они как в тканях эпителия матки, так и в клетках молочной железы. Их определение дает возможность оценить влияние гормональных факторов на прогрессию злокачественного роста, а кроме того, выявить наличие других очагов активности, помимо маточного. Входят в программу обязательного скрининга у больных женщин с подозрением на инфильтративную активность рака.
Иммуногистохимическое исследование проводят при:
- бесплодии;
- опухолях эндометрия;
- дисфункции менструаций;
- гиперпластических процессов в эндометрии.
При бесплодии методика позволит выяснить, может ли плодное яйцо прикрепится к стенке матки. Для рака метод не является способом ранней диагностики. Оценка рецепторной активности позволяет выявить наличие метастазирования, и оценить эффективность лечения в полости матки. При нарушениях овуляции методика выясняет эффективность гормональной терапии. При изменениях в полости матки гиперпластического характера усиление активности рецепторов к эстрогенам и прогестеронусвидетельствует о развитии низкодифференцированных опухолей, потенциально опасных для жизни женщины.
Общий принцип результата — чем больше экспрессия рецепторной активности, тем выше вероятность прогрессирования опухоли. Чем ниже активность, тем меньше возможность естественного оплодотворения.
Хроническим эндометритом называют воспаление мукозного слоя матки, которое провоцируют различные вирусы или патогенные микроорганизмы. В патологическом очаге происходят морфологические и функциональные изменения эндометрия.Хронический эндометрит – клинико-морфологический синдром, при котором в результате повреждения эндометрия инфекционным агентом возникают множественные вторичные морфофункциональные изменения, нарушающие циклическую биотрансформацию слизистой оболочки матки, что приводит к стойкому нарушению менструальной и генеративной функций.Частота встречаемости хронического эндометрита в популяции составляет 2,6- 51%. Причём среди этих женщин бесплодны 60,4%, а неудачные попытки ЭКО и переноса эмбрионов отмечены у 37%. В 2006 г. Международная Федерация Гинекологии и Акушерства уравняла понятия «неразвивающаяся беременность» и «хронический эндометрит».
Причины хронического эндометрита:
- инфекции органов малого таза, влагалища и цервикального канала;
- внутриматочная спираль;
- ранние интимные контакты;
- радиотерапия тазовых органов;
- хирургическое вмешательство в полость матки;
- злоупотреблением алкоголем и курение.
Практикующие специалисты относят воспалительные процессы, происходящие в органах малого таза, к аутоиммунной патологии. Для определения характера нарушений и выявления пациенток с патологическим ответом иммунной системы, который провоцирует воспаление эндометрия, назначается иммуногистохимическое исследование, которое проводят с использованием стандартной панели моноклональных антител:CD16, CD20, CD138, CD56, HLA-DR.
Рецептивность эндометрия – комплекс структурно -функциональных характеристик эндометрия, определяющий способность его к имплантации. С начала 90-х годов прошлого столетия понятие «рецептивность эндометрия» начинает обретать своё современное значение как процесс сложной интеграции и многоуровневого «диалога» между эндометрием и эмбрионом в специфический период «окна имплантации».Продолжительность «окна имплантации» у человека составляет в среднем 4 дня: с 6-го по 8-10 — й день после пика секреции ЛГ, или 20-24 день менструального цикла (при 28 -дневном менструальном цикле).В настоящее время различают три уровня рецептивности: генетический, протеомный и гистологический. При открытии «окна имплантации» в эндометрии усиливается экспрессия 395 генов (АроЕ, PLA2) и снижается экспрессия 186 генов (ITF, различные протеазы, внеклеточные матриксные белки и др.). Среди протеомных маркёров, связанных с рецептивностью эндометрия, выделяют различные молекулы адгезии, факторы роста, цитокины и рецепторы: семейство IL-1, LIF и LIF-R, αVβ3, TNF-α, IFN-γ и др. Из них наиболее изученным является лейкемия-ингибирующий фактор (LIF) – член семейства IL-6. Максимальная его экспрессия в эндометрии наблюдается на 20-й день цикла.Третий уровень рецептивности – гистологический. «Окну имплантации» в эндометрии соответствует средняя стадия фазы секреции менструального цикла.Эндометрий может обладать рецептивными свойствами только в том случае, если молекулярные маркёры рецептивности выявляются точно в среднюю стадию фазы секреции менструального цикла.Одним из ключевых ультраструктурных образований, участвующих в формировании рецептивности, являются пиноподии. Это микроскопические выпячивания в апикальной части поверхностного эпителия эндометрия, образующиеся на месте микроворсинок в «окно имплантации» и выступающие в полость матки. Предполагают, что основные рецепторы для прикрепления бластоциты располагаются на поверхности пиноподий, где также концентрированно экспрессируется LIF.Любой дисбаланс в экспрессии стероидных рецепторов может привести к нарушению морфофункциональных свойств эндометрия, его рецептивности. Поэтому определение уровня ER и PR в среднюю стадию фазы секреции позволяет дополнить морфологическое исследование эндометрия, оценить его рецептивность. В норме показатель соотношения PR/ER в строме колеблется от 2 до 4.В среднюю стадию фазы секреции наблюдается физиологическое снижение уровня ERα в эндометрии. Это – критическое событие, освобождающее от подавляющего влияния определённые гены и обеспечивающее сигнал для начала внутриматочной рецептивности.
Гиперэкспрессия ER α в среднюю стадию фазы секреции вызывает нарушение экспрессии биологических маркёров имплантации, нарушает рецептивность эндометрия.
Программа комплесного исследования состоит из следующей панели антител: ER, PgR, CD56, CD138, LIF, а также подсчет количества пиноподий.
*(количество рабочих дней, без учета дня доставки материала)
Материал для исследования: операционный и биопсийный материал, а также готовые парафиновые блоки со стеклами (образец опухоли). Желательно предоставить выписку из истории болезни, результаты КТ, МРТ и предыдущего гистологического заключения (в случае, если диагностика опухоли не первичная).
Прием материала: в часы работы медицинского центра.
Подготовка к исследованию: не требуется.
источник
Поставить точно диагноз «онкология» без проведения специальных исследований практически невозможно. В настоящее время медицина обладает такими возможностями. Поэтому если имеется подозрение на рак, то проводится иммуногистохимическое исследование. Рассмотрим, что собой представляет данный анализ, в каких случаях назначается и что позволяет выявить.
Под данным исследованием подразумевается изучение образца тканей под микроскопом. Их получают при помощи биопсии и предварительно обрабатывают специфическими антителами.
Онкологические заболевания давно находятся в поле зрения врачей и ученых. В ходе многочисленных исследований было установлено, что злокачественные клетки в процессе жизнедеятельности продуцируют специфические белки, которые называют антигенами. Они связываются с антителами, именно на этом основано иммуногистохимическое исследование, когда ткань пациента, взятая для изучения, после обработки тщательно изучается при помощи микроскопии.
Когда антитела взаимодействуют с раковыми клетками, то можно наблюдать явление флуоресценции. Это дает основания практически на 100 % быть уверенным, что имеет место онкология.
Сейчас уже разработаны и активно внедрены в медицинскую практику антитела практически ко всем новообразованиям.
Иммуногистохимическое исследование при раке позволяет:
- Распознать новообразование и определить его разновидность.
- Выяснить распространенность первичного очага по организму.
- При взятии биологического материала из вторичных очагов можно определить источник распространения метастазов.
- Исследование позволяет оценить эффективность терапии.
- При помощи анализа можно выяснить, на какой стадии развития находится раковая опухоль.
- Иммуногистохимическое исследование позволяет также выяснить скорость роста новообразований.
Данный метод исследования считается более информативным по сравнению с обычным гистологическим. Если использовать оба метода исследования, то можно получить полнейшую картину, поэтому на практике чаще всего врачи так и поступают.
Исследовать при помощи этого метода можно практически все ткани человеческого организма, но чаще всего такой анализ назначают при подозрении на онкологию.
- Для определения первичных новообразований.
- Для выявления метастазов.
- Данный анализ помогает определить прогноз развития и протекания патологии.
- Анализ служит одним из методов исследования рецепторов к ряду гормонов.
- ИГХ-исследование позволяет обнаружить микроорганизмы.
- Метод исследования применяют для выяснения чувствительности раковых клеток к химиотерапии и радиотерапии.
Иммуногистохимическое исследование проводится в несколько этапов, первым из них является сбор биологического материала. Его получают путем биопсии или изъятия материала во время проведения операции.
Кусочек ткани помещают в формалин и направляют в лабораторию, где его подвергают изменениям:
- Материал обезжиривают специальными составами и заливают парафином. В таком состоянии он может храниться практически вечно, поэтому при необходимости исследование можно повторять.
- На следующем этапе получают тончайшие срезы — проводят микротомирование. Их размещают на специальных стеклах.
- Приготовленные срезы обрабатывают растворами антител определенной концентрации. Использовать для обработки могут составы, содержащие разное количество антител. Какие из них вступят во взаимодействие с раковыми клетками, будет зависеть от разновидности опухоли.
Такой анализ просто незаменим, если есть подозрение на наличие раковых клеток в груди. Обязательно определение количества рецепторов эстрогена и прогестерона. При их повышении активизируется процесс роста злокачественных клеток.
ИГХ-исследование позволяет не только распознать онкологическое заболевание, но и определить его стадию. При помощи исследования врачи выясняют, показана ли гормональная терапия.
Опухоли, имеющие большую концентрацию гормонов, чаще всего вполне эффективно лечатся антигормональными препаратами.
Во время проведения анализа обязательно определяют показатель Ki-67, он помогает определить злокачественность процесса. Если иммуногистохимическое исследование молочной железы показывает Ki-67 до 15 %, то исход заболевания считается благоприятным. Если показатель доходит до 30 %, то без химиотерапии не обойтись, потому что опухоль растет довольно быстро. Отметка в 90 % чаще всего свидетельствует о неизбежности летального исхода.
Данный анализ назначается не только при подозрении на онкологию груди, но еще он оказывается довольно информативным, если:
- Имеется бесплодие.
- Обнаружены злокачественные образования матки.
- Наблюдаются патологические изменения в репродуктивной системе.
Такой анализ проводится, если:
- Часто наблюдаются выкидыши.
- У женщины было несколько неудачных попыток ЭКО.
- Диагностирована хроническая форма эндометрита.
Данное исследование помогает выяснить, имеются ли клетки, мешающие зачатию естественным путем.
ИГХ-исследование тканей эндометрия назначается женщинам, у которых уже было несколько неудачных попыток искусственного оплодотворения.
Взятие тканей эндометрия проводится в разные дни цикла, которые назначает врач.
Необходимо иметь в виду, что исследовать подготовленные образцы тканей имеет право только врач, имеющий сертификат, подтверждающий специальную подготовку по проведению анализов по методу ИГХ.
В заключении должно быть указано:
- Показатели антител, к которым определена тропность исследуемой ткани.
- Указывается разновидность раковых клеток и их количество.
- Указываются выявленные антигены, которые помогают установить вид онкологии.
По результатам исследования нельзя ставить окончательный диагноз. Врач-онколог имеет право это сделать только после получения интерпретации всех диагностических процедур.
Таким образом, можно сделать вывод, что эффективно иммуногистохимическое исследование при раке молочной или других желез и других видах онкологии. Анализ дает исчерпывающую информацию и позволяет распознать начинающийся патологический процесс на клеточном уровне.
источник
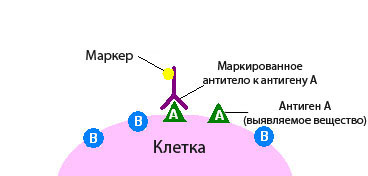
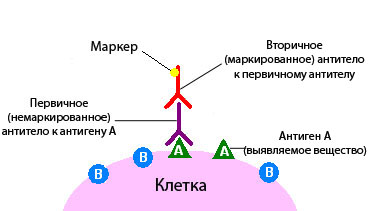
Иммуногистохимическое исследование в онкологии – это разновидность исследования ткани с помощью специальных реактивов по принципу антиген-антитело.
При иммуногистохимическом исследовании используются реактивы, которые содержат антитела, отмеченные специальными веществами.
Антитело – это белок, который связывается в тканях с определенными молекулами — антигенами, после чего возникает реакция. Если же таких молекул нет, то и реакции не будет.
По этому признаку можно судить, присутствует в ткани интересная нам молекула или нет. Это похоже на то, если нанести на белый стол бесцветный клей. Невооруженным глазом на белом фоне он практически незаметен, но стоит насыпать на стол мелкого песка, как клей становится виден за счет прилипших песчинок.
По правилам иммуногистохимическое исследование при раке всегда проводится в специализированной лаборатории. Для его проведения необходима опухолевая ткань, полученная в результате биопсии или операции.
Иммуногистохимическое исследование проводится для определения наличия в опухолевых клетках различных точек приложения, например, наличие рецепторов эстрогенов (ER) и прогестеронов (PR). Также иммуногистохимия выполняется для определения показателя Ki-67 (индекс пролиферативной активности опухолевых клеток), гиперэкспрессии белка Her2neu, VEGF (сосудистый фактор роста), р53.
Иммуногистохимическое исследование при раке выполняется для того, чтобы понять, какими препаратами можно лечить злокачественную опухоль, и к каким видам препаратов она чувствительна.
Самый распространённый анализ, определяемый при иммуногистохимическом исследовании, это наличие рецепторной чувствительности к гормонам у опухоли.
ER и PR — протеиновые рецепторы на поверхности опухолевых клеток.
В организме человека постоянно вырабатываются гормоны — эстроген и прогестерон. Эти гормоны воздействуют на ER и PR рецепторы, что приводит к стимуляции роста опухолевых клеток.
Определение Эстрогеновых и Прогетестероновых рецепторов является одним из важнейших моментов, определяющих чувствительность опухоли к терапии гормональными препаратами.
Чаще всего наличие рецепторов ER/PR определяют при раке молочной железы. Их наличие дает возможность, помимо стандартных методов лечения, применить гормональную терапию.
При гормон позитивном раке молочной железы, назначаются препараты: Тамосксифен, Экземестан (Аромазин), Летрозол (Фемара), Анастразол (Аримидекс), Гексэстрол (Синестрол) и другие.Также, считается, что гормонально-зависимый рак молочной железы отличается спокойным течением и редким метастазированием.
Чувствительность опухолевых клеток к гормональной терапии выражается в баллах от до 10. Опухоль считается гормонозависимой, начиная с 2-х баллов. и требует добавления к лечению гормональной терапии.
Her2Neu — это рецептор эпидермального фактора роста раковой клетки. Это — ген, который воздействует на мембранные рецепторы клетки, и стимулирует её к усиленному делению.
В некоторых опухолях (чаще всего рак молочной железы, рак пищевода, рак желудка) присутствует гиперэкспрессия (повышенная активность) Her2Neu, что вызывает быстрое деление опухолевой клетки и её повышенную активность.
Также снижается эффективность химиотерапии, лучевой терапии, гормональной терапии. Из-за этого опухоли с Her2neu позитивным статусом отличаются агрессивным течением.
Существует две методики определения наличия у опухоли гена Her2neu:
Результаты иммуногистохимического исследования выражаются в баллах:
- 0-1 означает, что опухоль без гиперэкспрессии Her2neu.
- 3 означает, что опухоль с гиперэкспрессией Her2neu.
2. Метод FISH (Флуоресцентная гибридизация in situ)
В отличие от иммуногистохимического исследования, при котором определяются белки, при методе FISH определяется наличие генов, кодирующих протеины Her2neu. В зависимости от их наличия, определяется гиперэкспрессия Her2neu.
Определение гиперэкспрессии рецептора Her2neu в опухоли молочной железы является очень важным для дальнейшего назначения лечения.
В современной онкологии гиперэкспрессию Her2neu определяют, чтобы понять, необходимо ли добавление к лечению ингибиторов Her2neu. Для лечения опухолей с гиперэкспрессией рецептора Her2Neu активно и успешно используются таргетные препараты Трастузумаб (Герцептин), Пертузумаб (Перьета), Трастузумаб-эмтанзин (Кадсила), Бейодайм (Трастузумаб+Пертузумаб). Эти препараты прицельно блокируют рецепторы Her2neu, тем самым останавливая активный рост опухолевых клеток и повышая их чувствительность к химиопрепаратам. Добавление таргетной терапии к стандартной химиотерапии при лечении Her2neu позитивных опухолей, серьезно увеличивает общую выживаемость и результат противоопухолевого лечения.
Ki-67 — это маркер пролиферативной активности опухолевой клетки. Данный параметр оценивается в процентах и показывает, сколько процентов опухолевых клеток активно делятся.
Если Ki-67 меньше 15%, опухоль считается слабоагрессивной, при показателе Ki-67 от 30 до 50% опухоль считается агрессивной, а при показателе Ki-67 выше 50% опухоль является высокоагрессивной.
Также Ki-67 является фактором прогноза течения опухолевого заболевания и ответа опухоли на химиотерапевтическое лечение. Определяется это простым способом: чем ниже показатель Ki-67, тем хуже опухоль реагирует на химиотерапевтическое лечение. И наоборот — чем выше показатель Ki-67, тем лучше опухоль будет отвечать на химиотерапию.
Белок p53 — это транскрипционный фактор, регулирующий клеточный цикл. В быстро делящихся клетках обнаружено увеличение концентрации белка р53 по сравнению с клетками, делящимися медленно, что обусловлено высоким риском их онкогенности.
Белок p53 предотвращает образование злокачественных опухолей в нашем организме. В норме, антионкоген р53 находится в неактивном состоянии, а при появлении повреждений ДНК в здоровой клетке — активируется.
Функция белка р53 состоит в удалении тех клеток, которые являются потенциально онкогенными. Это называется — индуцированный апоптоз, уничтожение потенциально опасной клетки.
При иммуногистохимическом исследовании, повышенное содержание белка p53 обнаруживается в 50% злокачественных клеток, что позволяет им беспрепятственно делиться и избегать апоптоза (уничтожения).
Количество белка p53, определяют в дополнение к показателю Кi67, для того, чтобы понять насколько агрессивна опухоль и определить дальнейшее течение болезни. Если уровень белка p53 высокий, значит опухоль не агрессивная и не склонна к метастазированию и быстрому росту. Если же, показатель белка p53 низкий, то значит опухоль агрессивна и склонна к быстрому росту в окружающие ткани и метастазированию.
VEGF – это сигнальный белок, вырабатываемый клетками для активного роста новых сосудов в уже существующей сосудистой системе.
Есть несколько видов белка VEGF, и каждый воздействует на определенный рецептор VEGFR (Vascular endothelial growth factor receptor). Для того чтобы активно делиться, опухоли нужно питание, а для этого нужны сосуды, по которым это питание будет поступать. Именно по этой причине в опухолевых клетках содержится повышенное содержание белка VEGF — для того, чтобы в короткие сроки строить сосудистые сети.
Наличие белка VEGF в опухоли говорит о возможности применения таргетной терапии такими препаратами, как Бевацизумаб (Авастин), Рамуцирумаб (Цирамза), Афлиберцепт (Залтрап). Они перестраивают сосудистую сеть опухоли, тем самым лишая её питания.
Иммунотерапия в онкологии появилась сравнительно недавно, но уже успела показать удивительные результаты в лечении опухолей. Механизм иммунотерапии рака заключается в том, что препарат позволяет иммунитету увидеть опухоль и уничтожить её. Ответственные за «видимость» опухоли белки PD-1, PDL-1 и PDL-2 в достаточном количестве присутствуют не во всех опухолях. Именно поэтому одним пациентам иммунотерапия помогает, а другим нет.
Чаще всего определение гиперэкспрессии белка PD-1 и его лиганд PDL-1 и PDL-2 необходимо при меланоме, немелкоклеточном раке легкого, раке желудка и раке почки.
Для того чтобы отобрать пациентов, которым показана иммунотерапия, проводится определение наличия экспрессии PD-1 и его лиганд PDL-1 и PDL-2, при помощи флюоресцентной гибридизации in situ (FISH). При наличии экспрессии PD-1 и его лиганд PDL-1 и PDL-2, показано применение иммунотерапии препаратами Пембролизумаб (Кейтруда), Ниволумаб (Опдиво), Атезолизумаб (Тецентрик).
В современной онкологии иммуногистохимическое исследование играет очень важную роль, так как при помощи этого исследования онкологи определяют наличие тех или иных факторов в опухоли, которые позволяют грамотно и адекватно составить дальнейшее лечение пациента и говорить о прогнозах заболевания.
источник
Важнейшим пунктом при диагностике раковых заболеваний является иммуногистохимическое исследование. Ежедневно в организм человека проникают микроорганизмы, способные запустить развитие патологического процесса. Защитные силы противостоят этому, образуя антитела. Эта реакция и легла в основу создания ИГХ-исследования.
Данный способ диагностики раковых заболеваний является наиболее современным и достоверным. В процессе развития опухолевого процесса образуются чужеродные организму белки – антигены. В это же время иммунная система вырабатывает антитела, главная цель которых – предотвращение размножения патогенных микроорганизмов.
Задачей иммуногистохимического исследования является своевременное выявление раковых клеток. Для этого биологический материал пациента обрабатывается множеством антител, после чего тщательно изучается под микроскопом. Если данные белковые соединения свяжутся с опухолевыми клетками, будет визуализироваться их свечение. Возникновение эффекта флюоресценции и свидетельствует о наличии в организме раковых клеток.
На сегодняшний день в распоряжении специалистов, осуществляющих ИГХ-исследование, имеются практически все антитела к различным видам опухолей, что служит залогом получения достоверных результатов.
Современный вид диагностики позволяет определить:
- распространение опухолевого процесса;
- скорость роста злокачественных новообразований;
- вид опухоли;
- источник метастазов;
- уровень злокачественности.
Кроме того, с помощью иммуногистохимического исследования может оцениваться степень эффективности лечения раковых заболеваний.
С помощью данного способа существует возможность изучения любых тканей человеческого организма. Главным основанием для назначения иммуногистохимического исследования является подозрение о наличии злокачественного образования.
В этом случае метод используется для:
- определения вида опухоли и области её локализации;
- обнаружения метастазов;
- оценки активности опухолевого процесса;
- выявления патологических микроорганизмов.
Также анализ эффективен при проблемах с зачатием.
Иммуногистохимическое исследование эндометрия показано при:
- бесплодии;
- заболеваниях матки;
- наличии патологий в органах репродуктивной системы;
- невынашивании беременности;
- хронических заболеваниях эндометрия.
Кроме того, ИГХ-исследование назначается пациенткам, у которых не наступает беременность даже после нескольких попыток экстракорпорального оплодотворения. Метод позволяет определить, имеются ли в организме клетки, снижающие вероятность зачатия.
Противопоказаний к ИГХ-исследованию не существует. Единственным фактором, из-за которого невозможно провести анализ, является непреодолимая сложность при заборе биоматериала пациента.
В первую очередь методом биопсии получают образец ткани больного. Реже забор материала осуществляется в процессе эндоскопического обследования или хирургического вмешательства. Способ получения образца зависит от вида опухоли и её локализации.
Важным нюансом является то, что забор материала при первичном обследовании должен осуществляться до начала лечения. В противном случае результаты исследования могут быть искажены.
После забора биоматериала его помещают в формалин и отправляют в лабораторию, где он подвергается следующей обработке:
- Образец ткани обезжиривается и заливается парафином. В данном виде биологический материал может храниться очень долго, за счёт чего ИГХ-исследование может быть проведено повторно.
- С образца собирают несколько тонких срезов и перемещают их на специальные стёкла.
- На них биоматериал окрашивается растворами различных антител. На данном этапе может применяться как малая панель, так и большая. В первом случае изучаются реакции после использования 5 видов антител, во втором – до нескольких десятков.
- В процессе иммуногистохимического исследования при раке любого органа появляется эффект флюоресценции, что даёт возможность специалисту определить вид злокачественных клеток.
Как правило, заключение готово через 7–15 дней. Срок зависит от вида используемой панели (малой или большой). Расширенный способ занимает больше времени.
Изучением срезов биоматериала занимается патологоанатом, имеющий знания и навыки (подтверждённые официальным документом), необходимые для проведения анализа.
При интерпретации результатов особое внимание обращается на показатель Ki-67. Именно он предоставляет информацию о степени злокачественности процесса. Например, если результат показателя после проведения иммуногистохимического исследования при раке молочной железы составляет не более 15%, считается, что прогноз более чем благоприятный. Уровень в 30% свидетельствует об активности опухолевого процесса, т.е. о быстрой скорости его развития. Как правило, она останавливается после курса химиотерапии.
По некоторым статистическим данным, если Ki-67 составляет менее 10%, итог заболевания будет благоприятным (в 95% случаев). Отметка в 90% и выше означает почти 100%-ный летальный исход.
Кроме показателя злокачественности, в заключении указываются:
- антитела, к которым выявлено сходство (тропность);
- вид раковых клеток, их количественное значение.
Важно понимать, что точный диагноз ставится после получения и изучения информации, собранной посредством всех проведённых диагностических процедур. Несмотря на то, что ИГХ-анализ считается наиболее информативным методом по сравнению с гистологией, иногда необходимо использовать оба способа. Расшифровкой иммуногистохимического исследования занимается исключительно онколог.
В современной медицине особое внимание уделяется диагностике раковых заболеваний. Наиболее современным и информативным методом считается иммуногистохимическое исследование. С его помощью выявляется не только наличие раковых клеток, но и определяется их вид и скорость развития злокачественного процесса. Кроме того, на основании результатов производится оценка эффективности назначенного лечения.
источник