Лабораторные анализы крови и мочи — информативные диагностические мероприятия, которые проводятся для выявления артрита и установления его вида. Клинические исследования позволяют обнаружить изменения количественного состава эритроцитов, тромбоцитов, лейкоцитов. Биохимические анализы крови проводятся для определения уровня сиаловых и мочевых кислот, белков, вырабатываемых организмом при сильном воспалительном процессе. Иммуноферментные исследования — это тестирование специфических маркеров для выявления антител — диагностических критериев ревматоидного, реактивного артритов.
При выставлении диагноза врачи учитывают результаты анализов кала и мочи. Их параметры позволяют не только дифференцировать артрит от других патологий, но и обнаружить причину некоторых заболеваний, например, хламидийную урогенитальную инфекцию.
Важно знать! Врачи в шоке: «Эффективное и доступное средство от боли в суставах существует. » Читать далее.
Образец синовиальной жидкости получают при проведении пункции — прокола суставной сумки специальными инструментами. Его исследование часто позволяет выявить происхождение патологии. При обнаружении в синовии примесей крови и (или) мелких фрагментов гиалинового хряща, врач предполагает развитие у пациента посттравматического артрита.
Если в синовиальной жидкости содержится гнойный экссудат, то проводятся дальнейшие исследования для установления причины его появления, например, патогенных микроорганизмов. Наличие в синовии кристаллов мочевой кислоты указывает на тяжелое течение подагры.
В процессе исследований выявляется изменения в количественном составе красных и белых кровяных телец. Повышенный уровень лейкоцитов прямо указывает на протекание в организме пациента воспалительного процесса. По этому критерию можно косвенно судить о его интенсивности. Чем больше по сравнению с нормой в системном кровотоке лейкоцитов, тем сильнее воспаление.
Еще один из самых информативных методов лабораторной диагностики — скорость оседания эритроцитов. В норме СОЭ не превышает 15 мм/ч у женщин, 10 мм/ч — у мужчин. Если в организме развивается патология, то в крови присутствуют его промежуточные и конечные продукты. Они прочно крепятся к эритроцитам, утяжеляя их. Поэтому скорость оседания красных кровяных телец на дно пробирки повышается. Значение СОЭ позволяет также судить о тяжести патологии. При показателях выше 4,0*109/л врач может предположить наличие у пациента:
- волчанки;
- склеродермии;
- ревматоидного артрита.
При этих аутоиммунных заболеваниях критерий СОЭ тесно связан со степенью активности воспалительного процесса.
При развитии любого вида артрита в кровеносном русле наблюдается небольшое снижение уровня эритроцитов (3,7*1012/л у женщин и 4,5*1012/л у мужчин). Уменьшается и количество гемоглобина, способного обратимо связываться с кислородом, обеспечивая его перенос в ткани. Для ревматоидного, реактивного, инфекционного артритов характерно его снижение менее 120 г/л и выявление монохромной, гипохромной, нормоцитарной, микроцитарной анемии. Значительно реже течение патологии сопровождается железодефицитной, апластической или гемолитической анемией.
При ревматоидном артрите совокупность клинико-гематологических синдромов встречается чаще, но при реактивном заболевании выраженность признаков малокровия несколько сильнее. Это объясняется высоким уровнем медиаторов цитокинов, вырабатываемых в ответ на острый воспалительный процесс.
| Лабораторные анализы для обнаружения артрита | Наименование исследований |
| Общий анализ мочи | Проводится для дифференциации артрита от других патологий. Для большинства артритов характерны нормальные значения. При системной волчанке и склеродермии повреждаются почки, поэтому в урине обнаруживаются кровь, глюкоза, белки (более 0,14 г/л). Пониженный уровень мочевой кислоты (менее 0,27 г/сут) — признак подагры |
| Посев биологического образца, взятого с мочеиспускательного канала | Посев проводится в питательные среды при подозрении на развитие хламидийного артрита. По количеству сформировавшихся колоний можно установить интенсивность воспалительного процесса, спровоцированного патогенными микроорганизмами |
В процессе серологического исследования крови качественно определяется ревматоидный фактор (РФ). Это не самый информативный критерий ревматоидного артрита, так как примерно такие же его значения характерны для красной волчанки и склеродермии. Но повышение уровня ревматоидного фактора более 10 Ед/мл с высокой вероятностью указывает на развитие пока еще окончательного неизлечимого вида артрита. РФ — иммуноглобулины, вырабатывающиеся синовиальной оболочкой для атаки на собственные клетки организма. Это происходит только при развитии аутоиммунных патологий, к которым и относится ревматоидный артрит.
Принцип обнаружения аномальных антител основан на их способности взаимодействовать с Fc-фрагментами иммуноглобулинов. В крови здорового человека допустимо присутствие некоторого количества РФ (менее 10-20 Ед/мл.), который остается после перенесенных инфекционных заболеваний.
Даже «запущенные» проблемы с суставами можно вылечить дома! Просто не забывайте раз в день мазать этим.
В лабораториях ревматоидный фактор определяется в качественном и в количественном значениях, причем в разных учреждениях полученные параметры могут немного отличаться из-за использования различных реагентов и оборудования. Для качественного выявления проводится латекс-тестирование или реакция Ваалера-Роуза. Установить количество позволяют результаты нефелометрического или турбидиметрического исследования. Но в последнее время предпочтение отдается ИФА – иммуноферментному анализу, обнаруживающему РФ и другие патологические иммуноглобулины.
Любая аутоиммунная реакция сопровождается выработкой антинуклеарных антител, атакующих белковые ядра клеток суставных структур. Поэтому при их обнаружении в крови врач подозревает развитие реактивного или ревматоидного артрита. Если при клиническом анализе высока скорость оседания эритроцитов, то это становится показанием для выявления уровня антинуклеарных антител. Диагностический маркер не специфичен, так как его высокие значения характерны и для других заболеваний:
- склеродермии;
- различных форм гепатита.
С высокой достоверностью на развитие ревматоидного артрита указывают высокие параметры АЦЦП (антицитруллиновых антител). Они продуцируются иммунной системой в ответ на обнаружение циклических цитруллиновых пептидов, по химической структуре схожих с аминокислотой, содержащейся в белковых молекулах синовиальной капсулы. Точность этого диагностического критерия — более 90%.
Биохимические анализы при артрите помогают установить причину его развития. Обязательно определяется уровень мочевой кислоты. Ее повышенные значения при норме до 5,8 мг/дл позволяют предположить у пациента подагру, протекающую на фоне накопления в суставах и почках солей мочевой кислоты. Большое содержание мочевины в системном кровотоке обнаруживается при подагрических атаках. Устанавливаются уровни креатинина (конечного продукта креатин-фосфатной реакции) и мочевины (конечный продукт белкового метаболизма). Если параметры соответственно выше 110 мкмоль/л и 7,5 ммоль/л, то это указывает на поражение почечных структур, характерное для системных патологий, или вторичную подагру.
Обнаруженные в кровеносном русле биохимические компоненты могут стать маркером воспалительного процесса и его интенсивности. Например, во время обострения ревматоидного артрита обнаруживается высокий уровень гаптоглобина. Появление этого белка свидетельствует о разрушении большого количества эритроцитов. В процессе биохимических исследований устанавливаются количественные значения и таких компонентов:
- фибриноген — специфический белок плазмы в растворенном виде. При сворачивании крови именно из него формируются тромбы. У людей с ревматоидным артритом его содержится в сыворотке значительно больше нормы (2-4 г/л);
- сиаловые кислоты — производные нейраминовой кислоты, входящие в состав гликопротеидов, гликолипидов. Сыворотка здорового человека содержит их около 2,33 ммоль/л. Более высокие значения свидетельствуют о развитии воспалительного процесса в соединительных тканях суставов;
- серомукоиды — сывороточные гликопротеины (сложные белки, содержащие углеводы). Обычно при превышении нормальных значений указывает на прогрессирование ревматоидного или реактивного артрита, необходимость срочного врачебного вмешательства.
Выявляется и С-реактивный белок, который относится к протеинам острой фазы. Концентрация таких белков всегда высока при сильном воспалении. Его обнаружение позволяет предположить наличие у пациента инфекционного, реактивного, ревматоидного артрита.
С-реактивный белок усиленно продуцируется иммунной системой в ответ на внедрение в организм патогенных бактерий или агентов аллергии. Установление его количества позволяет дифференцировать артриты от артрозов, не сопровождающихся интенсивным воспалением. Уровень С-реактивного белка не является специфическим диагностическим маркером артритов аутоиммунного или инфекционного происхождения. Но его повышение практически всегда наблюдается при системных патологиях, которые поражают суставные структуры одновременно или последовательно вместе с внутренними органами.
источник
Ревматоидный артрит – сложно диагностируемое заболевание, в рамках диагностики которого назначают множество анализов для определения формы болезни. В статье подробно расписаны все самые эффективные анализы.
Ревматоидный артрит – заболевание, которое по симптомам долгое время способно вводить в заблуждение. Подробно о болезни уже писалось в этой статье. Аутоиммунный характер болезни провоцирует поражение всё новых областей суставных механизмов, тканей и органов. Таким образом, больной в начальной стадии болезни сталкивается со следующими признаками:
- Дискомфортные ощущения в суставах, в том числе при пальпации.
- Затруднение подвижности после долгого нахождения в одной позе.
- Появление подкожных шишек.
- Отёчность и покраснение суставных фаланг кистей рук.
- Наблюдение симметричного развития воспаления в мелких суставах кистей и стоп.
- Быстрая утомляемость, апатия, снижение веса.
- Специфические — дают однозначное подтверждение или опровергают факт заболевания с высокой достоверностью.
- Неспецифические – работают только в совокупной расшифровке с остальными данными обследования, так как выявляют лишь отдельные признаки.

Определить, какие при ревматоидном артрите нужно сдать анализы, должен лечащий врач. План обследования пациента включает прохождение ёмкого диагностического комплекса мероприятий:
- биохимия крови, её клиническое исследование, определение АЦЦП (антицитруллиновых тел), иммунологический анализ;
- общий анализ мочи;
- анализ внутрисуставной жидкости;
- биоптата оболочки сустава.
Специфические показатели способны выдать ревматоидный артрит ещё до проявления первых сигналов о заболевании. Пациенты с наследственной предрасположенностью могут использовать этот способ для предупреждения болезни, её перехода в хроническую стадию.
Установление точного диагноза при ревматоидном артрите суставов основывается на грамотной расшифровке клинических результатов и профессиональном умении интерпретировать их в комплексе. Чтобы получить достоверные показатели, необходима специальная подготовка перед сдачей крови. Направление на лабораторные исследования должен выписывать один из лечащих специалистов: врач общей терапии, ревматолог, хирург или иммунолог. Для полного исследования показателей нужно сдать кровь из вены, соблюдая для этого условия:
- Не принимать пищу за 12 часов до взятия анализа (детям до года – за полчаса, от 1 до 5 лет – за 3 часа).
- Не употреблять алкогольные напитки в течение суток.
- Прекратить приём медикаментов за сутки с разрешения врача.
- Не допускать физической нагрузки и нервных стрессов за час до анализа.
- Запрещается курить минимум за 30 минут перед анализом.
Нарушение диеты, употребление лекарственных препаратов или курение искажают клинические данные состава крови и вводят в заблуждение при интерпретации результатов.
Стартовый набор на выявление воспалительного процесса в организме – общий анализ крови и мочи пациента. Данные анализы определяют также характер возникновения симптомов (инфекция, аутоиммунное заболевание). Так, общий анализ определяет следующие патологические изменения показателей крови у больного человека:
- Рост скорости оседания эритроцитов (СОЭ) – от 25 мм/ч при норме 2–15 мм/ч.
- Снижение гемоглобина — у женщин до 120 г/л и мужчин до 135 г/л.
- Количественный рост лейкоцитов – выше 9000 при норме 4000–9000.
Обострение ревматоидного артрита сопровождается лейкоцитозом и тромбоцитозом умеренной степени тяжести, нормоцитарной нормохромной анемией. Иногда происходит хроническая кровопотеря через желудочно-кишечный тракт и, как следствие, недостаток железа и анемия.
Анализ мочи даёт неспецифические сведения и определяет только повышение содержания белка и уровень лейкоцитов, что лишь подтверждает присутствие факторов воспаления.
Оседание эритроцитов изучается в пробирке на протяжении определённого времени. Показатель характеризует интенсивность развития патологии, активность распространения разрушительных процессов. Высокие показатели СОЭ указывают на прогрессирование заболевания и необходимость в принятии эффективных медикаментозных мер. При этом, чем выше скорость оседания, тем активнее фаза. Этот процесс объясняется образованием в крови больного воспалительных белков, которые являются причиной соединения эритроцитов в агрегаты, увеличения силы тяжести и скорости их оседания.
Биохимия крови на ревматоидный артрит для анализа состояния тканей суставов играет решающую роль. Несмотря на признание метода неспецифическим, его показатели определяют:
- Развитие ревматоидных признаков в соединительных тканях суставах.
- Протекание воспалительного процесса.
- Активность аутоиммунного заболевания.
Биохимия крови включает следующие данные:
- Присутствие гаптоглобина – характерно для острой фазы. Его норма составляет 0,8-2,7 г/л.
- Активность фибриногена в плазме – норма 2–4 г/л. Увеличение свидетельствует об активности аутоиммунного характера.
- Уровень пептидов, γ — глобулинов, криоглобулинов (IgM, IgG, IgA).
- Действие серомукоидов – сывороточных белков крови. Норма составляет 1,2–1,6 ммоль/л.
- Уровень сиаловых кислот – превышение нормы в 2-2,33 ммоль/л указывает на разрушительные процессы коллагена в клетках даже на стадии прогнозирования болезни.
- С – реактивный белок — норма 0-5 мг/л у здорового человека.
Рост фибриногена в крови выше 4 г/л означает повышение свёртываемости крови, что характерно при ревматоидном артрите. Высокий уровень этого показателя является сигналом о риске образования тромбов и ишемических изменениях в органах.
источник
Для диагностики реактивного артрита важное значение имеет правильно собранный анамнез и использование адекватных лабораторных и инструментальных методов обследования больных. Вместе с тем клиническая картина реактивного артрита практически никогда не ассоциируется с предшествующей перенесенной инфекцией, в связи с чем диагноз заболевания в большинстве случаев основан на клинических проявлениях внесуставного инфекционного процесса, данных анамнеза и результатах лабораторных тестов.
Программа лабораторной диагностики при подозрении на реактивный артрит включает исследование периферической крови и мочи, синовиальной жидкости, мазков из уретры, цервикального канала, конъюнктив, копрокультур с целью идентификации этиологического фактора. Используются также иммунологические, культуральные и молекулярно-биологические методы исследования.
Лабораторные и инструментальные методы диагностики реактивного артрита
| Методы исследования | Урогенитальные реактивные артриты | Постэнтероколитические реактивные артриты |
| Общеклиническое исследование крови | Ускорение СОЭ | Нейтрофильный лейкоцитоз, ускорение СОЭ |
| Анализ мочи | Лейкоцитурия | Норма |
| «Острофазовые» реакции (СРБ, сиаловые кислоты, фибриноген) | Содержание повышено соответственно активности заболевания | Содержание повышено соответственно активности заболевания |
| Ревматоидный фактор | Отсутствует | Отсутствует |
| Антинуклеарные антитела | Отсутствует | Отсутствует |
| Антиген HLA-B 27 | Выявляется в 80-90 % случаев | Выявляется в 70 % случаев |
| Микроскопия мазков из уретры, цервикального канала, конъюнктив | Выявление хламидий | Результат отрицательный |
| Посев кала на дизгруппу | Результат отрицательный | Высев патогенной микрофлоры |
| Серологическое исследование (РИГА с иерсиниями, сальмонеллами, шигеллами, кампилобактером) | Результат отрицательный | Выявление антител в диагностическом титре (1 : 200 и выше) |
| Реакция иммунофлюоресценции (прямая и непрямая) | Обнаружение антигенов хламидий в сыворотке крови и СЖ | Результат отрицательный |
| Иммуноферментный анализ | Обнаружение хламидийных антител (lg различных классов) в сыворотке крови и СЖ | Результат отрицательный |
| Серологические методы (РСК с хламидийным антигеном) | Выявление антител к хламидиям в диагностическом титре (1 : 64 и выше) | Результат отрицательный |
| Культуральные методы | Выделение С. trachomatis в культуре клеток in vitro | Результат отрицательный |
| Молекулярно-биологические методы | Выявление хламидийной ДНК (РНК) | Выявление ДНК причинных микроорганизмов |
| Исследование СЖ | Нейтрофильный лейкоцитоз при остром течении, преобладание лимфоцитов и моноцитов при хронических формах; снижение вязкости СЖ; повышение уровня белка и комплемента | |
| Ректороманоскопия, фиброколоноскопия | Воспалительные изменения толстой кишки (у 25 % больных) | Гистологическая картина острого или хронического воспаления толстой кишки |
| Рентгенографическое исследование | Отек околосуставных тканей; кистовидная перестройка эпифизов; околосуставной остеопороз; единичные эрозии при хронических формах РеА; периостит; энтезит; спондилит; сакроилеит (чаще односторонний) | |
У некоторых больных постэнтероколитическими реактивными артритами при посеве кала на дизгруппу может выявляться патогенная микрофлора. При серологическом исследовании на антитела в РИГА к иерсиниям (сальмонеллам, шигеллам, кампилобактеру) определяются соответствующие антитела в диагностических титрах (1 : 200 и выше).
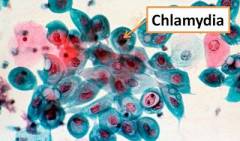
Бактериоскопия клинического материала от больного урогенитальным реактивным артритом (выделений из уретры, цервикального канала, конъюнктив) в некоторых случаях позволяет выявить цитоплазматические включения хламидий (тельца Хальберштедтера — Провацека) — крупные ретикулярные тельца (окрашиваются в синий цвет по Романовскому — Гимзе) и (или) мелкие элементарные тельца (окрашиваются в фиолетово-красный цвет).
Наиболее распространенными иммунологическими методами диагностики хламидийной инфекции являются реакция иммунофлюоресценции (прямая и непрямая), основанная на взаимодействии хламидийных антител с родоспецифическими хламидийными антигенами, и иммуноферментный анализ. Первый метод в настоящее время широко используется для лабораторной диагностики урогенитальных хламидиозов, однако отличается невысокой специфичностью и чувствительностью (65-97 %). Иммуноферментный метод позволяет определить наличие хламидийных антител в сыворотке крови больного (иммуноглобулинов различных классов), он удобен для скрининговых исследований, но его результаты во многом зависят от качества тест-систем. При этом в ранней фазе иммунного ответа (острая стадия) у больных обнаруживаются, как правило, антитела класса IgM. Пик концентрации приходится на вторую неделю после инфецирования, затем титр постепенно снижается, и через 2,5-3 мес. специфические IgM в крови не выявляются. Антитела класса IgG начинают обнаруживаться примерно через 1 мес. после начала заболевания и могут выявляться на низком уровне в течение многих лет. IgA-антитела появляются в крови в конце 1-го месяца после инфецирования и выявляются до тех пор, пока хламидийный антиген остается доступным для иммунокомпетентных клеток.
Серологическая диагностика хламидийной инфекции затруднена из-за наличия у больных недостаточно напряженного иммунного ответа вследствие низкой иммуногенности хламидий. Вместе с тем использование реакции связывания комплемента (РСК) у пациентов с хроническими вариантами течения заболевания может подтвердить диагноз, который считается положительным только при значении титра антител больше 1 : 64.
Культуральный метод дает возможность выделять возбудитель в культуре клеток in vitro и в настоящее время считается «золотым стандартом» лабораторного обнаружения хламидий. Вместе с тем эта методика трудоемкая, относительно дорогая, а получение результатов отсрочено до 72 ч. Кроме того, диагностическая ценность этого метода снижается у больных с хроническими вариантами заболевания, многократно получающих курсы антибактериальной терапии.
Среди молекулярно-биологических методов исследования наиболее часто используется метод полимеразной цепной реакции (ПЦР-анализ), в основе которого лежит многократное увеличение числа копий специфического участка хламидийной ДНК (РНК). Метод дает возможность определять антигены возбудителя в различном клиническом материале (кровь, сыворотка, синовиальная жидкость, слюна, выделения из уретры, цервикального канала, эякулят и др.). Данный метод является относительно недорогим, а с учетом его высокой чувствительности и специфичности (80-100 %) он по праву занимает лидирующее место в лабораторной диагностике.
Вместе с тем к интерпретации результатов ПЦР-анализа необходимо подходить критично. Это связано с несколькими причинами. Во-первых, в нашей стране отсутствуют стандартизированные реактивы (праймеры) для постановки этой реакции. Во-вторых, с помощью этого метода можно определить только небольшую часть генома хламидии, что зачастую не является абсолютным критерием жизнеспособности микроорганизма. В частности, в литературе имеются сведения о том, что применение панбактериальных 16S РНК-праймеров позволило идентифицировать в СЖ больных реактивным артритом, остеоартрозом, а также здоровых лиц фрагменты нуклеиновых кислот одного или нескольких микроорганизмов, в том числе и тех, которые в обычных условиях не вызывают воспаления суставов. Этот факт подтверждает существующую точку зрения об отсутствии абсолютной стерильности суставов в норме, а также свидетельствует о возможном случайном заносе в суставную полость фрагментов микробов — «свидетелей» перенесенной инфекции. Следует учитывать тот факт, что хламидийная ДНК может выявляться у пациентов еще длительное время после окончания курса антибактериальной терапии, в связи с чем положительные результаты ПЦР-анализа могут быть причиной гипердиагностики хламидиоза.
Таким образом, для идентификации возбудителя реактивного артрита предпочтительно последовательно использовать несколько диагностических методов: для определения антигенов хламидий — иммунофлюоресцентный метод или ПЦР-анализ, для определения титров антител к хламидиям — иммуноферментный анализ, при контроле эффективности лечения лучше использовать культуральный метод.
Рентгенологически на ранних этапах болезни обычно не выявляется каких-либо изменений со стороны суставов, за исключением признаков отека околосуставных мягких тканей и синовита. В более поздние сроки обнаруживаются периостит, кистевидная перестройка в эпифизах костей, костные разрастания в местах прикрепления ахиллова сухожилия и подошвенной фасции. Околосуставной остеопороз развивается при длительном воспалительном процессе в суставах. Эрозивные поражения суставных поверхностей встречаются, как правило, при хронических вариантах течения реактивного артрита у HLA-B27+ больных, чаще при синдроме Рейтера.
При хроническом течении реактивного артрита у 25 % HLA-B27+ больных наблюдается асимметричное поражение подвздошно-крестцовых сочленений. При рентгенографии позвоночника у 20 % больных выявляются признаки спондилита, энтезита, иногда анкилоза.
Рентгенограмма. Реактивный артрит. Двусторонний сакроилеит
Из новых диагностических методов все чаще стали применять КТ и ЯМРТ. Использование этих методов позволяет выявлять изменения костей и околосуставных тканей, визуализация которых при выполнении обычной рентгенографии не представляется возможной.
Для диагностики синовита и выявления патологических изменений в костях скелета применяется сцинтиграфия — метод лучевой диагностики, основанный на оценке распределения радиофармацевтического препарата технеция 99тТс в изучаемом органе или ткани. При активном воспалении синовиальной оболочки сустава при реактивном артрите отмечается повышенное диффузное накопление 99тТс в этой зоне, при сакроилеите — гиперфиксация его в области подвздошно-крестцовых сочленений. Метод сцинтиграфии суставов характеризуется более высокой чувствительностью по сравнению с рентгенологическим методом и во многих случаях позволяет выявить изменения значительно раньше.
В последние годы для исследования суставов более широко стали применять метод ультразвукового сканирования суставов. С его помощью можно визуализировать те анатомические структуры, которые плохо доступны исследованию другими методами. Ультразвуковое сканирование позволяет диагностировать минимальный суставной выпот, определять в динамике состояние синовиальной оболочки, хряща и суставной капсулы, дает возможность выявить изменения пяточной кости, уплотнения сухожилий, прилегающих мышц и др.
Для диагностики характера поражения суставов используются и инвазивные методы, в частности артроскопия. Наиболее часто артроскопия проводится при поражении коленного сустава, который удобен для данной процедуры благодаря своим анатомическим особенностям. Для осмотра доступны синовиальная оболочка, суставной хрящ, верхняя поверхность менисков, передняя и задняя крестовидные связки. При хроническом синовите наблюдаются утолщение и гиперемия синовиальной оболочки, ворсины утрачивают свою прозрачность и увеличиваются в размерах. Нередко в полости сустава визуализируются свободно лежащие или фиксированные на синовиальной оболочке сгустки фибрина или хрящевой детрит.
Помимо осмотра сустава, при проведении артроскопии имеется возможность выполнить биопсию тканей сустава с последующим морфологическим исследованием. При микроскопическом исследовании полученного материала в ряде случаев удается идентифицировать этиологический фактор (хламидии), а при использовании иммунофлюоресцентных методов — антигенный материал, входящий в состав иммунных комплексов.
Следует подчеркнуть, что артроскопия может использоваться не только с диагностической, но и с лечебной целью. Так, интенсивное орошение сустава изотоническим раствором хлорида натрия с последующим введением глюкокортикоидов (дипроспана) позволяет добиться быстрого купирования активности воспалительного процесса.
В ряде случаев для диагностики внесуставных проявлений у больных реактивным артритом используют ректоромано- или фиброколоноскопию, при этом у большинства больных постэнтероколитическим реактивным артритом нередко обнаруживаются изменения слизистой оболочки, характерные для острого или хронического колита.
источник
Реактивные артриты относятся к ревматологическим заболеваниям и лечатся в отделениях этого профиля. Они встречаются приблизительно в 2,5% случаев после перенесенных кишечных инфекций и в 0,8% случаев после перенесенной мочеполовой инфекции. Болезнь поражает в основном людей в возрасте от 20 до 40 лет. Мужчины по данным различных исследований заболевают примерно в 10 – 15 раз чаще, чем женщины (особенно большая разница в распространенности при синдроме Рейтера). Также замечено неравномерное распределение заболеваемости в зависимости от географического расположения. Это объясняется различной распространенностью инфекций, способных вызвать реактивные артриты.
Определенную предрасположенность к развитию реактивных артритов и синдрома Рейтера имеют представители некоторых народов. Это объясняется генетическими факторами. Антигенами, повышающими вероятность появления данной патологии, обладает почти 20% населения скандинавских стран, приблизительно 4% населения стран северной Африки, всего 0,5 – 2% японцев. В Европе, в среднем, распространенность этих антигенов составляет 5 – 8%.
Связь между инфекцией и клетками объясняется тем, что в строении бактерий и клеток организма есть схожие по строению белки (данное явление называется также молекулярной мимикрией). Иммунитет по данным белкам распознает возбудителя болезни и атакует его. Клетки же суставов оказываются атакованными по ошибке из-за сходств структурных белков. Определенную роль при этом играет и генетический фактор. На сегодняшний день однозначно установлено, что наличие специфических генов повышает риск развития артрита после инфекции.
При синдроме Рейтера пораженными оказываются не только суставы, но и слизистая оболочка глаз. При классическом течении присутствуют также признаки хронической мочеполовой инфекции. Механизм развития воспаления при синдроме Рейтера такой же, как и при других реактивных артритах. Поскольку иммунной системе необходимо время, чтобы распознать болезнь и образовать специфические антитела, поражение суставов наступает через некоторое время после дебюта инфекционного заболевания. Обычно этот срок составляет от 2 недель до 2 месяцев.
Чаще всего реактивные артриты развиваются после следующих инфекционных заболеваний:
- хламидиоз;
- другие мочеполовые инфекции;
- кишечные инфекции;
- дыхательные инфекции;
- другие инфекционные болезни.
Хламидии представляют собой бактерии шарообразной формы, важным звеном жизненного цикла которых является обязательное внутриклеточное паразитирование. Вне клетки их жизнь практически невозможна. Из–за большого сходства в жизненном цикле с вирусами хламидии долгое время относили к данному классу. В настоящее время они относятся к семейству Chlamydiaceae, которое включает один род Chlamydia. Род, в свою очередь, включает три вида, которые являются патогенными для человека и некоторых животных.
Наиболее распространенными видами хламидий являются:
- C. psittaci;
- C. pneumoniae;
- C. trachomatis.
Последний вид имеет наибольшее значение в развитии синдрома Рейтера. Именно он является возбудителем урогенитального хламидиоза более чем в 90% случаев. Причиной запуска аутоиммунного процесса являются антигены – особые белки, присутствующие в строении хламидий.
Наиболее важными антигенами хламидий являются:
- термостабильный антиген;
- термолабильный антиген.
Данные антигены являются визитной карточкой бактерии. Благодаря им можно определить вид и подтип возбудителя. Антигены стимулируют выработку антител, на поиск которых направлены серологические исследования.
Урогенитальный хламидиоз является одной из самых распространенных мочеполовых инфекций как у мужчин, так и у женщин. Это отчасти объясняет и частоту случаев реактивных артритов в медицинской практике (а именно – синдрома Рейтера).
Помимо хламидий в редких случаях заболевание может быть спровоцировано уреаплазменной или микоплазменной инфекцией. Эти микроорганизмы также являются носителями антигенов, способных запустить патологическую цепочку, ведущую к развитию реактивных артритов. В отличие от хламидиоза в случае микоплазмоза редко поражается слизистая оболочка глаз. Таким образом, речь идет о поражении только суставов.
В группу микоплазм, способных вызвать реактивный артрит, входят:
- M. Genitalium;
- M. Hominis;
- M. Fermentans;
- Ureaplasma urealyticum.
Реактивные артриты могут возникать также после определенных кишечных инфекций. Возбудителями в данном случае будут бактерии, паразитирующие в пищеварительном тракте. Они попадают в организм преимущественно с пищей и водой, так как могут длительное время выживать вне организма. В строении этих бактерий также присутствуют антигены, способные запустить аутоиммунную реакцию.
К развитию реактивного артрита могут привести следующие кишечные инфекции:
- сальмонеллез;
- дизентерия (возбудитель – бактерии из рода Shigella);
- иерсиниоз.
Типичного для синдрома Рейтера поражения глаз после этих инфекций, как правило, не наблюдается. Данные микроорганизмы способны сохраняться в организме длительное время, поддерживая воспалительный процесс в суставах. В связи с этим необходима тщательная диагностика и полноценное лечение инфекции, чтобы достичь выздоровления.
В редких случаях реактивные артриты могут развиться после вирусных гепатитов, при ВИЧ или других вирусных или бактериальных инфекциях. Механизм развития воспаления при этом остается таким же, как и при вышеперечисленных инфекциях. Важнейшей особенностью является то, что собственно микроорганизмы при реактивных артритах никогда не обнаруживаются в суставах. Поражение соединительной ткани происходит исключительно антителами. Многие врачи спешат с постановкой диагноза, из-за чего определяют реактивный артрит, не исключив обычного септического поражения (когда сам микроб попадает с током крови в сустав и вызывает воспаление).
Отдельно рассматривают реактивные артриты, развившиеся после вакцинации у детей. Они являются редким осложнением, которое наблюдается не более чем в 0,2 – 0,5% случаев. Поражение суставов в этих случаях вызвано введением в организм микробных агентов, которые запускают аутоиммунную реакцию. Первые симптомы болезни возникают в течение месяца после вакцинации. Наряду с поражением суставов обычно отмечают умеренное повышение температуры, общее беспокойство, плохой аппетит. Обычно реактивные артриты у детей после вакцинации протекают легко, нередко наблюдается спонтанное выздоровление в течение 10 – 15 дней. Тем не менее, чтобы избежать развития болезни, необходимо обратиться к ревматологу за консультацией.
Реактивные артриты в редких случаях развиваются после применения вакцин против следующих инфекций:
- корь;
- краснуха;
- дифтерия;
- коклюш;
- эпидемический паротит;
- туберкулез;
- вирусные гепатиты.
Вакцинация взрослых по особым показаниям также может запустить аутоиммунный процесс. У взрослых артрит будет протекать несколько тяжелее и потребует отдельного курса лечения.
Помимо инфекционных агентов определенную роль в развитии реактивных артритов и синдрома Рейтера играют генетические факторы. В первую очередь, это особый антиген HLA-B27. Это белок, расположенный на поверхности клеток, который предрасполагает к развитию аутоиммунного поражения суставов. При наличии этого антигена шанс, что инфекционный процесс осложнится реактивным артритом, повышается в 5 – 10 раз. Кроме того, болезнь в этих случаях будет тяжелее протекать и хуже реагировать на лечение. Предполагается, что существуют и другие врожденные генетические факторы, которые могут предрасполагать к развитию реактивных артритов.
В некоторых случаях реактивный артрит может развиться и параллельно с инфекционным заболеванием. Это случается, если организм пациента уже входил в контакт с данной инфекцией ранее. Например, если пациент в прошлом перенес хламидиоз, его организм сохранил клеточную память. Тогда при повторном попадании хламидий в организм антитела выработаются быстрее, и артрит разовьется параллельно с мочеполовой инфекцией.
Симптомы при реактивных артритах можно условно разделить на следующие группы:
- общие симптомы;
- симптомы сопутствующих инфекций;
- суставные проявления;
- симптомы при синдроме Рейтера;
- кожные симптомы;
- специфические поражения других органов.
Как уже объяснялось выше, реактивные артриты развиваются после перенесенных инфекционных заболеваний. Некоторые из них на момент поражения суставов уже проходят, но некоторые – приобретают хроническое течение. В таких случаях помимо симптомов собственно артрита у пациента будут наблюдаться умеренные симптомы инфекционных заболеваний. Они предопределяются местоположением первичного очага инфекции в организме.
Параллельно с поражением суставов могут наблюдаться признаки следующих типов инфекции:
- Мочеполовые инфекции. Признаками мочеполовой инфекции является покраснение отверстия мочеиспускательного канала (у мужчин), жжение при мочеиспускании, частые позывы на мочеиспускание. У женщин при хроническом течении инфекции может наблюдаться дисменорея (сбои менструального цикла) и усиленные боли при менструации. Кроме того, мочеполовые инфекции при обострении ведут к выделениям из уретры (данный симптом более заметен у мужчин).
- Кишечные инфекции. При хронических кишечных инфекциях симптоматика обычно скудная. Однако больные могут припомнить эпизоды диареи (длившейся от нескольких дней до нескольких недель), рвоты. Также типичными признаками являются тошнота, умеренные боли в животе, потеря аппетита, повышенное газообразование.
- Дыхательные инфекции. Основными симптомами при респираторных заболеваниях будут длительный сухой кашель, чихание, осиплость голоса, выделения из носа, умеренное покраснение слизистой оболочки горла. Все это симптомы, типичные для обыкновенной простуды. Тем не менее, как уже упоминалось выше, такие инфекции тоже способны запустить аутоиммунный процесс с поражением суставов.
Признаки поражения суставов являются ведущими при любом варианте реактивных артритов. Как правило, они появляются уже на 2 – 3 неделе после начала заболевания. Интенсивность проявлений может нарастать медленно, в течение нескольких дней, или развиться быстро, за 12 – 24 часа. В большинстве случаев именно симптомы, связанные с воспалением суставов, приводят пациента на консультацию к врачу.
Суставы поражаются преимущественно на нижних конечностях. Признаки воспаления несимметричны (то есть если на правой ноге поражен коленный сустав, то на левой аналогичных симптомов обычно не наблюдается). Одновременно признаки воспаления появляются на 3 – 4 суставах (олигоартрит). Поражение происходит по восходящему типу – от нижерасположенных суставов вверх. Нередко первыми затрагиваются суставы пальцев ног.
Типичными суставными проявлениями реактивных артритов являются:
- Умеренные боли в суставах. Как правило, они более выражены утром и могут усиливаться при движении.
- Припухлость суставов. Припухлость иногда заметна даже невооруженным глазом. При пальпации (прощупывании) ткани вокруг сустава не плотные, слегка отечные.
- Покраснение кожи над суставом. Покраснение кожи объясняется воспалительным процессом, при котором кровь приливает к тканям.
- Поражение околосуставных структур. Воспалительный процесс при реактивных артритах не ограничивается суставными поверхностями костей. По мере развития болезни наблюдается воспаление суставной сумки (бурсит), сухожилий (тендинит) и сухожильных влагалищ (тендовагинит). Если эти воспалительные процессы развиваются в области стопы (плантарный фасциит), то пациент может испытывать сильные боли при ходьбе. Внешне это проявляется заметной хромотой.
- Увеличение лимфатических узлов. При выраженном воспалительном процессе лимфатические узлы увеличиваются из-за усиленного оттока жидкости из тканей. При поражении суставов верхних конечностей прощупываются лимфоузлы в подмышечных впадинах, а при поражении суставов нижних конечностей – паховые лимфоузлы. Во время пальпации они обычно безболезненны и мобильны (легко двигаются под кожей).
В зависимости от других предрасполагающих факторов (наличие антигена HLA-B27, предшествующие травмы в области сустава, и т. п.) симптомы реактивного артрита могут прогрессировать. Иногда болезнь протекает в форме полиартрита (множественного поражения суставов). Пик обычно приходится на 5 – 7 неделю после стихания острых инфекционных проявлений.
При реактивных артритах могут поражаться следующие суставы (от более часто затрагиваемых суставов к более редким вариантам):
- коленные;
- голеностопные;
- межфаланговые суставы пальцев ног и рук;
- локтевые;
- лучезапястные (кисть руки);
- другие (межпозвонковые, крестцово-подвздошные, грудино-ключичные, нижнечелюстные).
Для синдрома Рейтера характерен особый комплекс симптомов, который отличает его даже от многих других реактивных артритов. Другое название синдрома Рейтера – уретроокулосиновиальный синдром. Это указывает на основные области поражений. В первую очередь появляются симптомы мочеполовой инфекции (обычно хламидиоза), затем – признаки воспаления слизистой оболочки глаз, а потом суставные симптомы. Так выглядит типичная триада при синдроме Рейтера. Тем не менее, нередко наблюдаются и другие симптомы, характерные для реактивных артритов.
Отличительными симптомами при синдроме Рейтера являются:
- Симптомы поражения глаз. Они могут наблюдаться уже через 1 – 2 недели после обострения хламидиоза. Симптомы могут быть как односторонними, так и двусторонними. В первую очередь, больные жалуются на покраснение глаз, их сухость или, наоборот, слезоточивость, умеренную режущую боль. При выраженном воспалительном процессе может появиться ощущение инородного тела в глазу или светобоязнь. Однако конъюнктивит (воспаление слизистой оболочки глаза) в ряде случаев может протекать и бессимптомно. Если проявления болезни длились 1 – 2 дня и не вызывали серьезного дискомфорта, больные могут и не заметить патологию.
- Сосискообразоное утолщение пальцев ног является следствием воспалительного отека и припухлости в области межфаланговых суставов.
- Признаки поражения мочеполового тракта (описаны выше в соответствующем разделе). Кроме того, из-за хронической хламидийной инфекции могут параллельно развиваться простатит (у мужчин) и цервицит или вагинит (у женщин).
Для синдрома Рейтера характерно хроническое рецидивирующее течение. Другими словами, вышеуказанные симптомы то появляются, то исчезают на некоторое время. В основном это связано с обострениями хламидийной инфекции. При условии окончательного излечения хламидиоза артрит пропадет. Однако после незащищенного полового акта и повторного контакта с хламидиями болезнь разовьется вновь.
Кожные симптомы у больных с реактивным артритом отмечаются относительно редко. Обычно они возникают одновременно с суставными проявлениями болезни, но могут встречаться и в другие периоды болезни. Кожные симптомы могут быть разнообразными – от покраснения отдельных участков кожи до появления небольших эрозий. Последние напоминают поражения кожи при псориазе. На ощупь пораженные участки кожи уплотненные, но безболезненные. Иногда наблюдается кератодермия – огрубение кожи и ее повышенное шелушение. В первую очередь этот симптом затрагивает кожу ладоней и стоп.
Наряду с поражением кожи нередко появляются признаки поражения слизистых оболочек. Эрозии на слизистой оболочке рта и половых органов могут дополнять основную триаду симптомов при синдроме Рейтера. Поражения кожи и слизистых при реактивных артритах никогда не бывает гнойным, потому что гной предполагает наличие микробов.
В редких случаях аутоиммунный процесс может влиять на работу других органов и систем, приводя к воспалению тканей. Это приведет к появлению необычных для реактивных артритов симптомов. Тогда у врача могут возникнуть проблемы с диагностикой, особенно если признаки поражения суставов незначительны.
В редких случаях при реактивных артритах могут появиться симптомы поражения следующих органов и тканей:
- Поражение почек. Может проявиться задержкой мочи и изменениями в ее биохимическом и клеточном составе.
- Поражение сердечной мышцы. Поражение миокарда проявляется периодическими нарушениями сердечного ритма. Специфические признаки можно заметить на ЭКГ (электрокардиограмме).
- Поражение перикарда (сердечной сумки).Перикардиты после перенесенной инфекции могут вызвать умеренные боли в груди и шум трения перикарда при аускультации (прослушивании).
- Полиневрит (воспаление периферических нервов). Полиневрит развивается крайне редко при запущенных формах болезни. Пациент при этом может жаловаться на умеренные мигрирующие боли, нарушения чувствительности, быстрое затекание конечностей.
Таким образом, симптомы при реактивных артритах могут быть очень разнообразными. Признаки поражения суставов присутствуют практически всегда. Воспаление слизистой оболочки глаз и сопутствующие симптомы характерны для синдрома Рейтера после хламидийной инфекции. Остальные проявления болезни могут варьировать от случая к случаю.
В зависимости от длительности вышеупомянутых симптомов различают следующие формы течения реактивных артритов:
- острое течение реактивного артрита – до полугода;
- затяжное течение – от полугода до года;
- хроническое течение — более 1 года.
Данная классификация играет определенную роль при подборе лечения. Если болезнь приобретает затяжной или хронический характер, необходимо обратить особое внимание на искоренение инфекции, которая, по всей видимости, плохо поддается лечению.
Общий осмотр проводится на приеме у врача. Первичное обследование может провести врач-терапевт или семейный врач, но наибольшую информацию о поражении суставов сможет собрать ревматолог. При сопутствующих признаках поражения глаз или других органов прибегают к помощи соответствующих специалистов.
Во время общего осмотра врач обращает внимание на следующие особенности:
- Характер поражения суставов. При реактивном артрите, в том числе при синдроме Рейтера, суставы обычно поражаются несимметрично. Кроме того, в отличие от многих других заболеваний воспалительный процесс затрагивает суставную сумку и сухожилия мышц. Соответствующие симптомы врач обнаруживает именно при объективном осмотре пациента.
- Эрозии на слизистой оболочке полости рта. Эрозии на слизистых оболочках рта (реже половых органов или на коже) также повышают вероятность того, что у пациента именно реактивный артрит. Нередко пациенты замечают небольшие изъязвления, но не придают им большого значения, так как не могут связать их с поражением суставов. Из-за этого врач должен сам внимательно осмотреть слизистые оболочки.
- Симптомы поражения глаз. Поражение глаз и суставов характерно для синдрома Рейтера. При других вариантах реактивных артритов оно чаще всего отсутствует. Таким образом, признаки воспаления глаз показывают, что нужно делать дальнейшие анализы, направленные на поиски именно мочеполовой инфекции.
- Признаки хронической мочеполовой инфекции. При подозрении на реактивный артрит врачу нужно осмотреть наружные половые органы. Покраснение слизистой оболочки могут указывать на хронический воспалительный процесс. Это предопределит направление диагностических тестов и поможет исключить другие заболевания суставов.
Кроме того, врач уточняет, не болел ли пациент в последние месяцы различными инфекционными заболеваниями. Обращают внимание на такие характерные проявления как зуд в области половых органов, жжение во время мочеиспускания, рвота или диарея, а также кашель и признаки простуды. Отсутствие этих симптомов при опросе пациента не исключает диагноз реактивного артрита. Дело в том, что такие инфекции нередко протекают скрыто, без симптомов и заканчиваются спонтанным выздоровлением (без определенного лечения). Тем не менее, отсутствие признаков острой инфекции при опросе снижает вероятность диагноза.
Лабораторные методы исследования являются наиболее информативными при диагностике реактивного артрита и синдрома Рейтера. С их помощью можно определить характерные для данного заболевания изменения в анализе крови, а также обнаружить признаки инфекционного процесса, который запустил патологическую цепочку. По результатам лабораторных исследований возможна окончательная постановка диагноза.
Для диагностики реактивных артритов применяют следующие лабораторные методы исследования:
- анализы крови;
- анализ мочи;
- анализ кала;
- типирование антигена HLA-B27
- микробиологические исследования;
- серологические исследования;
- исследование синовиальной жидкости.
Анализ крови при реактивном артрите имеет огромное значение, так как в нем можно обнаружить много характерных изменений. В зависимости от цели исследования может быть взята как кровь из вены, так и кровь из пальца. При необходимости по ходу лечения кровь будут брать еще несколько раз, чтобы подтвердить положительную тенденцию. Изменения при реактивном артрите и синдроме Рейтера будут наблюдаться как в общем, так и в биохимическом анализе крови. В первую очередь они указывают на наличие воспалительного процесса.
При реактивном артрите в анализе крови могут наблюдаться следующие изменения:
- Лейкоцитоз. Повышение уровня лейкоцитов более 9 млн/мл является признаком воспалительного процесса. При реактивных артритах лейкоцитоз будет умеренным, обычно до 11 – 12 тысяч.
- Повышение скорости оседания эритроцитов (СОЭ). Данный показатель также является признаком воспалительного процесса. Норма составляет у мужчин до 10 мм/ч, у женщин – до 15 мм/ч. Ложное повышение СОЭ может наблюдаться во время беременности или у пожилых людей (после 60 лет).
- Умеренная анемия. Понижение уровня эритроцитов и гемоглобина (менее 110 г/л).
- Обнаружение в крови С-реактивного белка. Этот белок свидетельствует о наличии в организме острого воспалительного процесса. Его концентрация обычно прямо пропорциональна интенсивности воспаления. Кроме С-реактивного белка могут быть обнаружены и другие признаки воспалительного процесса — сиаловые кислоты, серомукоид.
Анализ мочи в определенных случаях также может указать на присутствие воспалительного процесса. Кроме того, многие ревматические заболевания, поражающие суставы, влияют и на работу почек. Таким образом, анализ мочи проводят, в том числе и для того, чтобы обнаружить поражение почек.
Характерными изменениями в анализе мочи при реактивном артрите являются:
- Протеинурия – выделение с мочой повышенного количества белков крови.
- Микрогематурия – присутствие в моче небольшого количества крови. Обычно это количество настолько мало, что не меняет цвет мочи и не может быть замечено невооруженным глазом. Кровь обнаруживают с помощью специального биохимического анализа.
- Лейкоцитурия – повышенное выделение лейкоцитов с мочой. Может наблюдаться вследствие лейкоцитоза, инфекционного или воспалительного процесса в почках.
Как уже отмечалось выше, данный антиген сильно повышает риск развития ряда заболеваний суставов, в том числе и реактивных артритов. Анализ назначается пациентам с признаками поражения суставов на ранней стадии, когда симптомы, позволяющие точно поставить диагноз, еще не появились. При наличии антигена HLA-B27 у пациента вероятность, что поражение суставов вызвал реактивный артрит, очень высока. Поэтому врач сможет раньше начать лечение и предотвратить возможные осложнения.
Анализ проводится методом ПЦР (полимеразной цепной реакции). Она позволяет с высокой точностью определить наличие генов в ДНК, отвечающих за образование данного антигена. Для анализа необходима венозная кровь пациента. Перед сдачей крови не рекомендуется курить (хотя бы за час до анализа), так как это может повлиять на конечные результаты.
Если результат анализа оказывается положительным, это повышает вероятность того, что у пациента реактивный артрит примерно в 20 раз. Другими словами, врач может быть почти уверен в правильности постановки диагноза уже на ранней стадии болезни. Шанс того, что при положительном результате теста воспаление суставов все же не аутоиммунной природы составляет приблизительно 10 – 15%. Отрицательный результат анализа на HLA-B27 не исключает диагноз «реактивный артрит», но сильно снижает его вероятность.
Микробиологическое исследование делается для обнаружения различных инфекций, которые могли привести к развитию реактивного артрита либо к поражению суставов другой природы. В первую очередь, ищут мочеполовые и кишечные инфекции, так как именно они обычно осложняются воспалением суставов. В диагностике дыхательных инфекций микробиологические методы исследования почти не применяются.
Для обнаружения инфекций, которые привели к реактивному артриту, можно исследовать следующие материалы от пациента:
- кровь;
- моча;
- кал;
- синовиальная жидкость (жидкость, полученная из полости сустава при пункции);
- мазок со слизистой оболочки половых органов.
Суть микробиологических исследований состоит в точном определении вида бактерий. При исследовании крови микробиологический анализ будет положительным только при бактериемии (когда возбудитель болезни циркулирует в крови). Для реактивных артритов это не характерно, но анализ может быть назначен для исключения других форм поражения суставов. В моче патогенные микроорганизмы могут появиться при одновременном поражении почек или при развитии инфекции в нижних отделах мочевыводящих путей. Надежнее, однако, в этом случае брать мазок или соскоб со слизистой оболочки.
Для обнаружения инфекции у больных с реактивным артритом применяют следующие микробиологические методы:
- Микроскопия. Микроскопическое исследование подразумевает обычный анализ пробы под микроскопом. Врач при этом обращает внимание на форму бактерий и их восприимчивость к тем или иным красителям. Микроскопию можно делать при взятии мазка со слизистой оболочки половых органов или при исследовании кала.
- Посев на питательные среды. Другим способом обнаружения микробов является их посев на специальные питательные среды. В благоприятных условиях микроорганизмы размножатся, образовав целые колонии. Наблюдая за ростом колоний и их особенностями, врач может установить вид возбудителя. Посев можно делать из образцов анализа кала, мочи, крови, синовиальной жидкости, мазка со слизистой оболочки.
- Антибиотикограмма. Антибиотикограмма – это микробиологический анализ, который проводят после получения колонии возбудителя. В лабораторных условиях врачи проверяют, к каким антибиотикам наиболее чувствителен данный возбудитель. Это помогает назначить наиболее эффективное лечение. Антибиотикограмма назначается пациентам с хроническими кишечными или мочеполовыми инфекциями, которые в прошлом уже проходили курс лечения.
- ПЦР. Полимеразная цепная реакция, о которой уже говорилось выше, может с успехом применяться и для обнаружения различных инфекций. При этом ведется поиск ДНК возбудителя. Исследование является дорогостоящим, но дает очень надежные результаты. ПЦР выявляет признаки инфекции, даже когда острый период болезни закончился, и другие микробиологические анализы не дали результатов. При реактивных артритах это очень важно, потому что поражение суставов обычно наступает через несколько недель после перенесенной болезни.
Серологические исследования – это группа анализов, которые основываются на поиске в крови специфических антител против определенной инфекции. Эти тесты не дают стопроцентного результата, так как инфекционный процесс на момент поражения суставов уже закончился. Тем не менее, антитела продолжают циркулировать в крови еще некоторое время (обычно от 2 недель до 2 месяцев, в зависимости от заболевания). В этот период с помощью серологических тестов можно подтвердить, что пациент перенес ту или иную инфекцию.
Для серологического исследования берется кровь пациента. Результат обычно получают в течение суток. При синдроме Рейтера, например, анализ на антитела против хламидий обнаруживаются у 50 – 65% пациентов. Достаточно высокие показатели и для других возбудителей. Обнаружение антител указывает на высокую вероятность именно реактивного поражения суставов в ответ на инфекцию, позволяя исключить другие ревматологические заболевания.
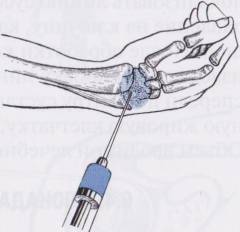
Синовиальную жидкость получают путем пункции воспаленного сустава. В норме эта жидкость способствует лучшему скольжению суставных поверхностей и улучшает движение в суставе. Пункцию проводят под местным обезболиванием. Врач вводит специальную иглу и набирает некоторое количество синовиальной жидкости. Ее впоследствии используют для микробиологических и цитологических исследований. При реактивных артритах в синовиальной жидкости не обнаруживают возбудителей болезни, так как воспаление вызвано не инфекцией, а воздействием собственного иммунитета организма. В то же время в ней можно найти антитела к соответствующей инфекции (чаще всего – к хламидиям). Также будет высоким уровень лейкоцитов, что говорит об интенсивном воспалительном процессе.
Инструментальная диагностика необходима, прежде всего, для уточнения характера поражения суставов. Многие ревматологические заболевания связаны с деформацией суставных поверхностей, которые легко определяются в ходе специальных исследований. При реактивных артритах характерных изменений обычно не наблюдается. Поэтому на первых этапах заболевания, при остром течении, назначать инструментальные исследования бессмысленно. Однако если артрит носит затяжной или хронический характер (что не слишком характерно для реактивных аутоиммунных процессов) возникает необходимость в дополнительных диагностических процедурах. Длительное воспаление на этот момент уже приводит к некоторым структурным изменениям.
В диагностике реактивных артритов используют следующие методы инструментального обследования:
- рентгенография;
- ультразвуковое исследование (УЗИ);
- артроскопия.
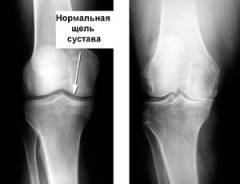
Рентгенография – это диагностический метод, основанный на получении картинки с помощью рентгеновского излучения. Лучи проходят сквозь толщу тканей и попадают на специальную чувствительную пленку. Впоследствии по получившемуся изображению врачи делают заключения об изменениях в суставе.
При хроническом течении артрита могут отмечаться следующие изменения на рентгенограмме:
- Околосуставной остеопороз. На снимке он проявляется участком размягчения костной ткани возле сустава, под хрящом.
- Сужение суставной щели. В норме между костями на снимке есть определенное расстояние. При интенсивном воспалении из-за отека и набухания хряща оно уменьшается.
- Эрозии суставной поверхности. Данный дефект на снимке выглядит как неровность или шероховатость поверхности хряща в полости сустава.
- Костные шпоры. Костные шпоры – это небольшие наросты, которые обычно локализуются на пяточных костях, но иногда могут появляться и на костях запястья или на позвонках.
- Признаки поражения межпозвонковых суставов.
Несмотря на то, что рентгенография является быстрым, дешевым и безболезненным методом обследования, ее назначают не так часто. Только у 8 – 10% пациентов с реактивным артритом или синдромом Рейтера удастся заметить характерные изменения на снимке. Тем не менее, именно с помощью рентгенографии можно исключить ряд других ревматологических патологий. Дело в том, что многие из них ведут к выраженной деформации суставов, которая не характерна для реактивных артритов.
Рентгенография суставов может проводиться, в том числе и беременным женщинам, если в этом возникает острая необходимость. Современные аппараты позволяют максимально снизить дозу облучения и сфокусировать лучи в пределах сустава. Кроме того, для защиты наиболее чувствительных частей тела будут использованы специальные экраны.
Ультразвуковое исследование заключается в обследовании сустава с помощью звуковых волн. Оно позволяет выявить ряд патологий, которые незаметны на рентгеновском снимке. В частности, речь идет о воспалительных процессах в околосуставных тканях.
На УЗИ можно обнаружить следующие признаки реактивного артрита:
- бурсит;
- тендинит;
- тендовагинит.
Кроме того, УЗИ может дать информацию о поражении почек или перикарда, если воспалительный процесс будет протекать очень интенсивно.
УЗИ также является безболезненным, быстрым и дешевым исследованием, которое практически не имеет противопоказаний. Исследование длится 3 – 5 минут для каждого из пораженных крупных суставов. Применение данного способа исследования при поражении мелких суставов бессмысленно, потому что аппараты не обладают достаточно высоким разрешением. Другими словами, минимальные очаги воспаления и изменения в суставах различить попросту не удастся.
Артроскопия является сравнительно редким методом исследования при реактивных артритах. Суть метода заключается во введении в полость сустава специальной камеры. С ее помощью врач получает возможность своими глазами оценить состояние тканей в пределах сустава. В подавляющем большинстве случаев под артроскопией понимают исследование коленного сустава. Он является достаточно крупным для данной процедуры. Другие суставы в силу анатомического строения хуже подходят для данного исследования.
При артроскопии врач может оценить состояние следующих структур коленного сустава:
- суставный хрящ;
- синовиальная оболочка;
- крестовидные связки;
- поверхность менисков.
При реактивных артритах во время артроскопии отмечаются очаги воспаления. Нередко в суставе обнаруживается небольшое количество жидкости и отложения фибрина. Синовиальная оболочка может быть гиперемирована (покрасневшая из-за усиленного притока крови).
Данная процедура является болезненной, поэтому выполняется под анестезией. Кроме того, для ее проведения требуется специальная аппаратура, что повышает цену исследования. Из возможных осложнений наиболее опасным является занесение инфекции в полость сустава с развитием септического артрита. Все это ограничивает применение артроскопии во врачебной практике. Ее назначают только в случаях, когда уточнить диагноз или эффективность лечения другими способами невозможно.
Помимо вышеперечисленных признаков реактивного артрита существует ряд показаний для исключения данного диагноза. Обнаружение любого из этих критериев у пациента заставит врача продолжить поиски правильного диагноза, несмотря на наличие антигена HLA-B27, недавно перенесенную инфекцию и другие типичные признаки.
Критериями для исключения реактивного артрита являются следующие диагностические данные:
- обнаружение в крови ревматоидного фактора (характерно для других ревматических поражений суставов);
- обнаружение тофусов – специфических узлов с солями мочевой кислоты (характерно для подагры);
- ревматические и ревматоидные узелки на коже;
- псориаз волосистой части головы;
- повышенный титр антистрептолизина-О.
Лечение реактивных артритов и синдрома Рейтера может проводиться как в стационарных условиях (в больнице), так и в домашних условиях. Как правило, на первых порах больного кладут в больницу для проведения надлежащего обследования и постановки точного диагноза. При умеренной интенсивности симптомов госпитализация не обязательна. Тогда ответственность за проведение всех диагностических процедур ложится на самого пациента.
Для безусловной госпитализации пациента на первых этапах существуют следующие показания:
- необходимость индивидуального подбора противовоспалительных препаратов;
- обострение болезни во время лечения базовыми противовоспалительными препаратами;
- появление атипичных форм болезни (перикардит, нефрит, васкулит – воспалительное поражение сосудов);
- подозрение на септический (бактериальный) артрит;
- необходимость проведения артроскопии или других инвазивных исследований;
- высокая температура и тяжелое общее состояние пациента.
Независимо от того, лечится пациент в больнице или дома, основная роль отводится медикаментозному лечению. Только правильно подобранные препараты смогут быстро улучшить состояние пациента и предотвратить развитие болезни. Самолечение или лечение народными средствами при реактивных артритах опасно, так как может вызвать ухудшение состояния больного.
Медикаментозное лечение реактивных артритов можно разделить на несколько основных направлений:
- устранение воспалительного процесса;
- лечение кишечной или дыхательной инфекции;
- лечение хламидиоза;
- лечение конъюнктивита при синдроме Рейтера.
| Группа препаратов | Препарат | Рекомендуемая доза | Лечебный эффект |
| Нестероидные противовоспалительные средства (НПВС) | Диклофенак | 100 – 300 мг в сутки в 2 – 3 приема в зависимости от массы тела пациента. | Препараты обладают противовоспалительным и обезболивающим эффектом. Это связано с угнетением медиаторов воспалительного процесса и прерыванием биохимической цепочки воспаления. Побочным эффектом при неправильном употреблении является поражение слизистой оболочки желудка (гастрит, язва). Эффективность конкретного препарата оценивается через 7 – 10 дней после начала его приема. |
| Мелоксикам | 0,3 – 0,5 мг препарата на 1 кг массы тела (мг/кг) 1 раз в сутки. | ||
| Нимесулид | 5 мг/кг 2 – 3 раза в сутки. | ||
| Напроксен | 15 – 20 мг/кг в сутки, дозу разбить на 2 приема. | ||
| Ибупрофен | 35 – 40 мг/кг в течение дня в 2 – 4 приема. | ||
| Иммуносупрессоры | Метотрексат | 7,5 – 15 мг, доза принимается за несколько раз в течение недели по схеме, предписанной врачом. | Данная категория препаратов воздействует не на цепочку воспаления, а непосредственно на иммунную систему. Они вызывают ее угнетение, из-за чего синтез антител нарушается и воспаление стихает. Данные препараты назначаются только в самых тяжелых случаях реактивного артрита. |
| Азатиоприн | 150 мг/сутки | ||
| Сульфасалазин | 2 г/сутки, срок приема определяет лечащий врач в зависимости от переносимости препарата. | ||
| Глюкокортикоиды | Преднизолон, реже его аналоги (в других дозах!) – кортизон, дексаметазон | 30 – 60 мг/сутки, доза снижается постепенно, по мере исчезновения симптомов. | Данные препараты обладают более выраженным, чем НПВС противовоспалительным действием. Побочным эффектом являются гормональные сбои и ослабление иммунитета. |
| Метилпреднизолон | 1000 мг в течение 3 дней, внутривенно в виде капельницы (в рамках пульс-терапии). |
При моноартритах (поражении одного сустава) могут назначить также внутрисуставное введение глюкокортикоидов. Это можно осуществить параллельно с проведением артроскопии. Полость сустава промывают специальным раствором, после чего в нее вводится некоторое количество гормонального противовоспалительного препарата. Обычно для достижения выраженного улучшения достаточно одной инъекции. Прогресс, однако, коснется только сустава, в который ввели препарат. Последующее поражение других суставов этот способ лечения не исключает.
Для лечения кишечной инфекции прибегают к антибиотикотерапии. Нередко на момент развития реактивного артрита возбудители болезни уже погибли. Тогда лечение ограничивается приемом противовоспалительных препаратов. Перед назначением антибиотиков рекомендуется провести микроскопическое исследование кала или ПЦР для обнаружения конкретного возбудителя. В зависимости от результатов этих обследований врач назначит тот или иной антибактериальный препарат. Идеальным вариантом является составление антибиотикограммы.
Дыхательные инфекции, как правило, вызваны вирусами. Специфического лечения против них не существует. На момент развития артрита симптомы дыхательной инфекции уже отсутствуют либо идут на спад. При затяжном течении простуды или при продуктивном кашле (с мокротой) берут на посев мокроту. При обнаружении в ней возможных возбудителей болезни назначается соответствующий курс лечения.
| Фармакологическая группа | Препарат и его аналоги | Рекомендуемая доза |
| Макролиды | Эритромицин (эрмицед) | 0,5 г дважды в сутки или 0,25 г четырежды в сутки в течение недели. |
| Азитромицин (сумамед) | Лечение дробное. В первый день – 1 г препарата раз в сутки за час до еды. Со второго дня до конца лечения — 0,5 г раз в сутки. Курс лечения длится 5 – 10 дней. | |
| Кларитромицин (клацид) | 0,25 г два раза в день в течение 1 – 2 недель. | |
| Рокситромицин (рулид) | По 150 мг утром и вечером перед едой. Курс лечения – 1 – 2 недели. | |
| Мидекамицин (макропен) | 0,4 г три раза в сутки не менее 2 недель. | |
| Джозамицин (вильпрафен) | 0,5 г дважды в сутки в течение 10 – 15 дней. | |
| Тетрациклин | Тетрациклин | 0,5 г 4 раза в сутки в течение 7 – 14 дней. |
| Доксициклин | 0,1 г 2 раза в сутки в течение 7 – 14 дней. | |
| Фторхинолоны | Офлоксацин | 200 мг 2 раза в сутки или 400 мг 1 раз в сутки, курс лечения 7 – 10 дней. |
Каждая группа препаратов имеет свои преимущества и недостатки. Лечение тетрациклинами позволяет быстро достигать высокой концентрации антибиотика в крови, но при сокращении сроков приема до 1 недели возрастает риск рецидивов или появления устойчивых к антибиотикам видов хламидий. Однако прием максимальных доз и продолжительный курс приема антибиотика не гарантирует полного выздоровления. Это приводит в 5 – 15 % к рецидивам или возникновению устойчивых к антибиотикам форм хламидий. В подобных ситуациях рекомендуется повторный курс антибиотиков через 7 – 14 дней при использовании преимущественно других эффективных противохламидийных препаратов. В среднем курс лечения мочеполовой хламидийной инфекции составляет от 7 – 14 дней до 3 недель. В комплексной терапии реактивных артритов тетрациклины используют редко, так как они плохо сочетаются с другими препаратами и обладают рядом побочных эффектов. К ним прибегают, когда хламидии не чувствительны к другим препаратам.
Эритромицин обладает схожей с тетрациклинами эффективностью при лечении различных форм мочеполового хламидиоза. Он успешно очищает организм даже при бессимптомном течении инфекции. Однако следует помнить, что при лечении макролидами в 10 – 15% случаев не достигается выраженного клинического и микробиологического эффекта. Также возможны рецидивы как ранние (до 1 месяца после завершения лечения), так и поздние. В этих случаях повышается риск и повторного реактивного воспаления суставов.
Кроме того, при обнаружении реактивного артрита после хламидийной инфекции необходимо воздержаться от незащищенных половых контактов. Повторное попадание хламидий вызовет новое обострение болезни и усложнит лечение. Чтобы этого избежать следует найти постоянных половых партнеров пациента или пациентки и провести профилактическое обследование. Нередко у них будет обнаружения хроническая хламидийная инфекция в бессимптомной форме. Тогда назначается параллельное лечение и половых партнеров.
Сроки лечения, указанные в таблице, являются ориентировочными. В 30 – 40% случаев эти курсы лечения не позволяют полностью искоренить инфекцию. Это связано с особенностями строения и жизненного цикла хламидий. Единственным критерием выздоровления является отрицательный итоговый анализ. Порой для этого приходится повторять курсы антибиотикотерапии в течение 2 – 3 месяцев. Точные сроки и режим приема устанавливает лечащий врач.
Если конъюнктивит в рамках синдрома Рейтера длится более 2 дней и сопровождается выраженными симптомами со стороны глаз, необходимо пройти отдельный курс лечения данного заболевания. Он включает местное применение противовоспалительных препаратов, которые уменьшат воспалительный процесс. Для уточнения диагноза и полноценного лечения больных с выраженными глазными симптомами обычно помещают в стационар.
Стандартной схемой лечения конъюнктивита и увеита при синдроме Рейтера является:
- Циклопентолат. Применяется в виде 1% раствора, закапывать в глаза по 1 – 2 капли дважды в день. Назначают в первые 5 – 10 суток терапии.
- Дексаметазон. Применяется в виде 0,1% раствора, закапывать по 1 – 2 капли от 3 до 6 раз в сутки (в зависимости от интенсивности воспаления). Применяется 15 – 30 суток.
- Диклофенак. Применяется в виде 0,1% раствора по 1 – 2 капли в сутки в течение 2 – 4 недель.
- Фенилэфрин. Назначается только при сильном воспалительном процессе с угрозой осложнений. Применяется в виде 1% раствора по 0,2 мл в сочетании с дексаметазоном (0,25 мл) 1 раз в сутки. Курс лечения составляет 5 – 10 суток.
При отсутствии клинического эффекта могут быть назначены парабульбарные инъекции (уколы под глаз) с глюкокортикоидными препаратами. Препаратом выбора при этом является дексаметазон в дозе 2 – 3 мг/сут. При угрозе осложнений в клетчатке около глаза можно создать депо из противовоспалительного препарата. Тогда рекомендуется введение 40 мг метилпреднизолона 1 раз в неделю в течение месяца. К данной мере прибегают после окончания основного курса лечения. Все вышеперечисленные препараты могут иметь противопоказания при хронических болезнях глаз. В связи с этим ни один врач не может их назначить без предварительной консультации офтальмолога.
Физиотерапевтические процедуры при реактивных артритах назначаются редко. При выраженном поражении определенного сустава может быть назначена его иммобилизация (обездвиживание) с помощью специальной шины или даже гипсовой повязки. После окончания лечения повязку снимают и начинают лечебную физкультуру и массаж. Это необходимо, чтобы предотвратить окостенение суставов, вернуть им подвижность и восстановить тонус мышц.
После выздоровления и восстановления рекомендуется соблюдение следующих профилактических мер для предотвращения обострений:
- Воздержание от незащищенных половых актов.
- Обязательное обращение к врачу при дыхательных или кишечных инфекциях.
- Предупреждение врача перед вакцинацией об эпизодах реактивного артрита в прошлом.
- Соблюдение общих правил личной гигиены (мытье рук, кипячение воды и т. п.).
- Соблюдение диеты. Данный пункт не является полноценным компонентом лечения, поскольку даже самое строгое соблюдение диеты не ослабит симптомы без приема соответствующих медикаментов. Обострение же может спровоцировать обилие жирной пищи и регулярное употребление алкоголя.
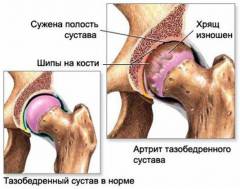
Наиболее распространенными являются следующие последствия реактивных артритов:
- хронизация воспалительного процесса;
- ограничение подвижности в суставе;
- хронические боли в суставе;
- хронические болезни внутренних органов;
- снижение остроты зрения.
источник