Российским исследователям впервые удалось использовать стволовые клетки для адресной доставки онкопрепаратов. Их применение для лечения рака вызывало у ученых опасения, так как они способны стимулировать рост опухолей. Однако оказалось, что так происходит не всегда. Специалисты берут клетки костного мозга пациента и загружают в них специальные капсулы, в которых содержится токсичное вещество. Попадая в пораженные раком ткани, капсула под воздействием лазера высвобождает токсин, который убивает и саму клетку, и опухоль. Такая терапия уже показала свою эффективность на модели меланомы.
В современной онкомедицине существует острая проблема: эффективность большинства лекарств зависит от вводимой дозы противоопухолевого препарата — чем она выше, тем эффективнее терапия. Однако рано или поздно наступает предел, когда воздействие лекарства еще недостаточно эффективно, а используемая дозировка подходит к критической отметке и становится токсичной для организма в целом. Чтобы преодолеть этот барьер, необходимо рационально использовать препарат, доставляя его направленно в очаг заболевания.
Кроме того, при стандартном подходе большая доза вводимого токсичного противоопухолевого лекарства распространяется по всему организму вместе с кровотоком. Это может создать очередной барьер на пути доставки лекарства в зону интереса: зачастую опухоли представляют собой достаточно плотные образования, а значит, кровоток в них затруднен. Таким образом, при стандартном введении противоопухолевый препарат не всегда может свободно накапливаться в достаточном количестве в области новообразований.
В Университете ИТМО нашли способ направленно доставлять лекарство в зону опухоли и высвобождать его с помощью инфракрасного излучения. Как пояснил «Известиям» один из авторов исследования, магистрант физико-технического факультета Олексий Пельтек, в качестве доставщиков выбраны стволовые клетки, которые будут брать из костного мозга пациента.
— Эти клетки способны к патотропизму, то есть к направленной миграции в очаг новообразования из-за большого скопления там лейкоцитов и макрофагов (клеток, реагирующих на воспаление. — «Известия»), — пояснил ученый. — Понятно, что мигрирующие стволовые клетки невозможно нагрузить напрямую токсичными противоопухолевыми препаратами, так как это может негативно влиять на их биологические функции. Следовательно, противоопухолевые лекарства должны быть сначала изолированы, а затем загружены в стволовые клетки, что мы и сделали в нашей работе.
Чтобы решить эту задачу, исследователи разработали субмикронные полые носители на основе полимеров и диоксида кремния — полиэлектролитные капсулы (субмикрокапсулы). После того как лекарства были размещены в оболочке, стволовые клетки модифицировали и загрузили капсулы внутрь них.
— Разработанные капсулы светочувствительны, то есть они способны разрушаться под действием инфракрасного излучения и дистанционно высвобождать лекарство, — отметил Олексий Пельтек.
Светочувствительность позволяет высвобождать препарат в нужное время и в нужном месте. Таким образом, ученые разработали умную систему для доставки противоопухолевых лекарств непосредственно в область злокачественных новообразований. Исследователи предполагают, что капсулы можно будет вводить пациенту инъекционно в сосуды, окружающие опухоль.
Стволовые клетки, полученные из мышц человека
Исследования на клетках показали, что на раскрытие и высвобождение действующего вещества таким микроносителям необходимо три дня. По истечении этого срока на область локализации опухоли предлагают воздействовать инфракрасным излучением. Стволовые клетки также могут применяться для борьбы с метастазами. Но так как выяснить, где именно они находятся, сложно, разработчики предлагают использовать для этой цели носители, которые высвобождают лекарство без облучения. Работа над их разработкой уже ведется.
Эффективность адресной доставки полученных систем была протестирована на первичных клетках меланомы — модели опухолевых сфероидов, которые были выделены из тканей реальных онкопациентов.
Стволовые клетки способны мигрировать в опухолевые очаги, так как опухоль специально их привлекает с помощью особых биологически активных веществ и заставляет работать на себя, поддерживая рост и метастазирование, сообщил «Известиям» директор научно-клинического центра прецизионной и регенеративной медицины Казанского федерального университета Альберт Ризванов. Однако в данном случае ученым удалось «обмануть» рак.
— Упаковка лекарств в микрокапсулы, загрузка таких носителей в стволовые клетки и высвобождение под действием света в опухоли действительно отчасти решает задачу адресной доставки. Более того, таким способом стволовые клетки доставят свой смертельный груз не только в первичный очаг, но и во все метастазы в организме, — отметил ученый.
Начальник лаборатории компьютерного моделирования лекарственных средств ЮУрГУ (вуза – участника проекта «5-100» ) Владимир Потемкин считает, что пока еще рано говорить об успехах таких систем умной доставки.
— Разработка требует клинических испытаний, которые занимают не один год. Но двигаться в этом направлении нужно. Основная проблема лечения опухолевых заболеваний — это похожесть здоровых и опухолевых клеток, — пояснил ученый. — Поэтому об эффективности нового способа доставки можно будет говорить только после длительных исследований.
Ученые ИТМО также отмечают, что, несмотря на первые успехи, для внедрения разработанных систем умной доставки в клиническую практику необходимо пройти сложный путь доклинических и клинических исследований, которые требуют времени и финансовых вложений.
Следующим шагом ученых ИТМО станут эксперименты на модельных животных.
источник
Применение стволовых клеток сейчас очень популярно в косметологии. Что это за клетки такие и почему церковь, часть общественности и ученых против данного метода омоложения?
Самые начальные клетки человеческого организма – это стволовые клетки. Они образуются сразу после зачатия в оплодотворенной яйцеклетке. Способность становиться любой клеткой – это основное их отличительное качество, так называемая полипотентность. Стволовые клетки зародыша, пока он растет, образуют его мозг, печень, желудок, сердце.
Даже после рождения в организме ребенка их еще очень много, но с каждым годом их становится меньше, к 20 годам у человека практически отсутствуют стволовые клетки. Это научно доказанный факт. Но взрослому эти клетки тоже необходимы – они всегда заменяют пораженные в случае болезни какого-либо органа.
На протяжении жизни органов с заболеваниями становится гораздо больше, а вот стволовые клетки уменьшаются, поэтому человек старится.
Идея ввести в организм столовые клетки и стать моложе на 10-20 лет кажется заманчивой, но пока никто не знает, как они действуют. Возможно, они только стимулируют к дальнейшей жизнедеятельности погибающую клетку, а может сами становятся на ее место и начинают активно трудиться. К сожалению, вопросов вокруг стволовых клеток пока больше, чем ответов. Когда ученые выяснят, как происходит действие стволовых клеток, тогда в медицине произойдет настоящий прорыв.
Безусловно, у стволовых клеток есть будущее. А пока к их использованию врачи советуют подходить крайне осмотрительно. К сожалению, в России нет ограничений на применение эмбриональных стволовых клеток и поэтому сейчас во многих косметологических салонах можно найти рекламные букеты, обещающие омолодить и оздоровить стволовыми клетками.
Но на практике это инъекции вытяжек из тканей эмбрионов, а они могут вызвать аллергические реакции и даже отторжение.
А если же процедура проводится не в лаборатории, то есть риск, что клеточный материал может быть заражен.
Сейчас в российских косметических центрах используют несколько видов стволовых клеток:
- Эмбриональные стволовые клетки. Их получают из печени, поджелудочной железы, мозга абортированных человеческих зародышей, а затем культивируют в материале, по составу похожем на сыворотку крови. Весь полученный биоматериал после проверки на наличие вирусов помещается на хранение в жидкий азот.
- Клетки пуповины новорожденных, костный мозг человека. Лечение пуповинными клетками особенно эффективно между членами одной семьи. В России есть банк стволовых клеток, в котором могут хранить пуповинную кровь. Пункцию костного мозга берут из подвздошных костей таза взрослого человека, после чего в лаборатории выращивают многомиллионную колонию.
- Стволовые клетки, выделенные из жировой ткани.
С этической точки зрения применение стволовых клеток ради омоложения скомпрометировано скандалами вокруг забора эмбриональных стволовых клеток от абортивного материала. При этом считается, чем на более позднем сроке проводится аборт, тем лучше качество стволовых клеток. Поэтому в странах, где активно используются клеточные технологии, отмечается резкий рост количества абортов на поздних сроках… По мне вообще бесчеловечный метод, из абортированных детей выделять клетки. На смерти строить бизнес..
После инъекций клетки организма начинают делиться «как у младенца» активно, поэтому человек как бы молодеет. Но какие последствия может оказать такое омоложение конкретному человеку, пока никто сказать не может. В любом случае — это стресс для немолодого организма, на фоне которого может развиваться любая патология.
Последние исследования американских ученых показали, что стволовые клетки действительно обладают противоположными свойствами. Одни из них препятствуют развитию рака , а другие сами могут перерождаться в раковые клетки, которые и дают начало развитию опухоли . В лечении стволовыми клетками пока много неясного и необходимы дальнейшие научные исследования, чтобы можно было гарантировать 100% безопасность лечения и омоложения ими организма.
Все больше в прессе появляется информации о том, что в преждевременной смерти известных актёров Дмитрия Хворостовского, Жанны Фриске, Александра Абдулова, Олега Янковского, Валентины Толкуновой, Анны Самохиной и Любови Полищук свою роль сыграло лечение эмбриональными стволовыми клетками. Все они прибегали к помощи клеточной терапии. Верить ли этим слухам? Не знаю. Я вообще сомнительно отношусь к таким информациям. Одно я знаю точно, пока стволовые клетки и их действия до конца не изучены лучше воздержатся от такого метода омоложения. Тем более если эти клетки эмбрионального происхождения..Нельзя омолаживаться за счет мертвых! Ни к чему хорошему это не приведет
источник
Объясняем по пунктам, почему это не сложно, но очень важно
24 сентября во всем мире отмечают День борьбы с лейкозом. Единственный способ спасти тех, кто столкнулся с этой болезнью, — трансплантация костного мозга. Процедура не имеет ничего общего с торговлей органами на черном рынке, однако до сих пор она окутана множеством мифов и небылиц. Что из них правда, разбираемся вместе с «Фондом борьбы с лейкемией».
Костный мозг — вообще не мозг. В нем нет нервных клеток, зато есть большое количество гемопоэтических стволовых клеток, из которых в дальнейшем образуются клетки крови: лейкоциты, эритроциты и тромбоциты. Это главный кроветворный орган человека — ежедневно он вырабатывает приблизительно 500 миллиардов кровяных клеток, в том числе взамен погибающих и отмирающих. По виду костный мозг — мягкая ярко-красная полужидкая ткань, похожая на губку, заполняющая кости изнутри. Больше всего костного мозга содержится в тазовых костях, ребрах, грудине и длинных трубчатых костях.
Процедура донорства костного мозга, как правило, безболезненна и осуществляется двумя способами. При первом врач забирает костный мозг из тазовых костей донора под общим наркозом — вы точно ничего не почувствуете. При втором способе гемопоэтические стволовые клетки выделяются из крови донора. Чтобы выгнать стволовые клетки из костного мозга в кровь, донору дают специальные препараты. Эта процедура проводится без наркоза. Кровь берется из вены на одной руке и возвращается обратно через вену на другой руке, стволовые клетки оседают в специальном аппарате. Это не больно, но вы проведете до шести часов в донорском кресле.
Во время донации забирают 2–5 % костного мозга, который через две-три недели полностью восстанавливается. Способность к регенерации гемопоэтических стволовых клеток настолько высока, что повторно донором можно становиться уже через три месяца.
При взятии костного мозга под общим наркозом самое неприятное — сама анестезия. Уровень гемоглобина снижается незначительно. Возможны ощущения легкой слабости и головокружения, болезненность в тазовых костях, увеличивающаяся при движении. При получении кроветворных клеток из периферической крови донор может испытывать симптомы, похожие на недомогание при гриппе: боли в костях и суставах, головные боли, иногда повышение температуры.
Противопоказания сходны с противопоказаниями по донорству крови (это онкологические заболевания, ВИЧ, гепатит, сифилис и так далее. Посмотреть полный список противопоказаний можно здесь). Перед трансплантацией донора тщательно обследуют. Кстати, недавно отечественные страховые компании начали страховать доноров на случай осложнений, что говорит о низком риске для здоровья.
Идентичные (однояйцевые) близнецы действительно идеальные доноры друг для друга. В других случаях вероятность совместимости для родных братьев и сестер только 25 %. Родители же не могут быть донорами костного мозга, потому что лишь 50 % ДНК каждого из них составляет ДНК ребенка. Зато полностью или почти полностью подходящего донора можно найти среди совершенно посторонних людей в регистрах доноров костного мозга. Это огромные базы данных, где хранятся сведения о генах тканевой совместимости миллионов добровольцев.
Сегодня, чтобы сдать кровь на типирование и войти в российский регистр доноров костного мозга, можно обратиться в любое отделение лабораторий Invitro. При этом забор и типирование проводится совершенно бесплатно для донора, а при себе нужно иметь только паспорт. Сдать кровь на типирование можно без специальной подготовки — в любое время дня и не на голодный желудок. Также кровь на типирование можно сдать на донорских акциях благотворительных фондов.
В интернете можно встретить объявления о вознаграждении или продаже костного мозга. Это обман. Во всех странах донорство костного мозга безвозмездно, добровольно и анонимно. Продать стволовые клетки невозможно, их можно только пожертвовать. Также за процедуру сдачи костного мозга донору не выдают больничный.
Вступая в регистр потенциальных доноров стволовых гемопоэтических клеток, вы свидетельствуете о своем желании стать донором. Если вы подойдете как донор, с вами свяжется представитель регистра и спросит о согласии на дачу гемопоэтических стволовых клеток. Отказаться от донорства можно практически на любом этапе, но не позднее чем за десять дней до намеченной даты трансплантации костного мозга. За десять дней до пересадки пациенту делают высокодозную химиотерапию, полностью уничтожающую его кроветворную и иммунную системы, поэтому отказ в последнюю минуту практически равносилен убийству человека, ожидающего пересадки костного мозга.
С момента забора крови на типирование (определение HLA-фенотипа, то есть набора генов, отвечающих за совместимость тканей) до момента донорства гемопоэтических стволовых клеток может пройти несколько лет. По статистике, в России донором становится приблизительно каждый 700-й человек, сдавший кровь на типирование. Вероятность встретить своего генетического близнеца — 1 на 10 тысяч, поэтому звонок от сотрудника регистра можно расценить как редкую удачу: ваш фенотип оказался совместим с реальным пациентом, вы можете спасти чью-то жизнь.
Да, министерство здравоохранения выделяет квоты на проведение трансплантации, но активация донора, забор и доставка трансплантации до места операции оплачиваются пациентом. В этот момент на помощь приходят благотворительные организации, например «Фонд борьбы с лейкемией». Стоимость трансплантации костного мозга от донора из российского регистра составляет от 300 до 500 тысяч рублей, из германского — 20 тысяч евро. Национальный регистр доноров костного мозга имени Васи Перевощикова объединяет 12 региональных российских регистров и один казахский. Сегодня в национальном регистре около 100 тысяч человек, из них донорами стали уже почти 300 человек. Германский регистр — самый крупный в Европе — насчитывает 8,7 миллиона потенциальных доноров. Благодаря ему удается найти донора для 60–80 % пациентов.
Миф 10: Стволовые клетки россиян отправляют за границу и могут использовать для создания биологического оружия
В интересах всего мира и каждого из нас, чтобы страны не только пользовались международной базой, но и пополняли ее. Однако национальный регистр доноров костного мозга имени Васи Перевощикова пока не включен в международную поисковую систему доноров костного мозга BMDW. Биологи считают, что создание этноспецифического оружия нереально. Русские слишком мало отличаются от европейцев, чтобы создать для них специальную инфекцию.
источник
В странах, где донорство костного мозга хорошо развито, врачи давно изучают, какие последствия оно может иметь для донора. Нам, конечно, хотелось бы заявить, что донорство костного мозга совершенно безопасно, но это было бы нечестно по отношению к потенциальным донорам, которые доверяют нам, вступая в Национальный регистр имени Васи Перевощикова. Некоторая небольшая опасность для доноров существует. Изучив масштабные исследования на эту тему, мы составили список самых интересных наблюдений.
Отдавать свой костный мозг, а точнее, стволовые кроветворные клетки, может быть страшновато. Даже если знаешь, что берут только небольшую часть этих клеток и что они восстановятся. Суммировать распространенные страхи можно так. Взятие кроветворных клеток из тазовых костей – это все-таки настоящая операция под общим наркозом. А если получать их из крови (это наиболее распространенный сейчас способ), чтобы клетки вышли из костей в кровь, донор несколько дней принимает специальные препараты. И как они скажутся на здоровье в долгосрочной перспективе? Работ на эту тему в России мы не нашли, зато в иностранных исследованиях Русфонд обнаружил много интересного.
Такой результат принесло исследование «Пониженный риск серьезных осложнений и отсутствие увеличенного риска рака после донации стволовых клеток из периферической крови в сравнении с донацией костного мозга из тазовых костей» большой группы авторов, опубликованное в 2014 году. Объектом наблюдения были около 10 тыс. доноров: у 2726 кроветворные клетки были взяты из тазовых костей, у 6768 – из крови (обычно говорят «из периферической крови»). Все они стали донорами в 2004–2009 годах, среднее время наблюдения за ними после донации составило три года (максимальное – восемь лет). Авторы хотели, среди прочего, проверить «теоретическое соображение, что кратковременный прием гранулоцитарного колониестимулирующего фактора (того самого препарата, который выгоняет кроветворные клетки в кровь. – Русфонд) может повысить вероятность заболеть раком крови и другими видами рака».
Оказалось, что риск онкологических заболеваний у доноров меньше, чем у «не доноров», то есть остального населения примерно того же возраста. «Доноры здоровее остальной популяции и имеют меньшие онкологические риски», – отмечают исследователи. Искать объяснение этого факта они не пытаются: состояние здоровья доноров тщательно проверяется перед донацией, но оценка риска онкологических заболеваний в проверку не входит.
Похожий результат принесло и самое, видимо, масштабное из существующих исследований здоровья доноров – «Серьезные осложнения у доноров после аллогенной донации гемопоэтических стволовых клеток». В нем участвовали 51 тыс. доноров, а максимальное время наблюдения за ними составило 13 лет. Вероятность онкогематологических заболеваний у доноров периферической крови оказалась несколько выше, чем у доноров стволовых клеток из тазовых костей. Но и те, и другие заболевали реже остального населения.
Донорство костного мозга, даже из периферической крови – это все-таки не анализ из пальца. Среди последствий, которые могут возникнуть, – жар, боль в костях, головокружение, слабость. В большом исследовании «Анализ влияния расы, социально-экономического статуса и размеров медицинского центра на последствия донации для неродственных доноров», опубликованном в 2016 году, была сделана попытка определить вероятность неприятных ощущений у разных групп доноров. В результате выяснилось, что женщинам и тем, у кого есть лишний вес, при заборе периферической крови в целом больнее и неприятнее, чем всем остальным. Впрочем, признают исследователи, опыт центра, где проводился забор клеток, оказывается все-таки более существенным фактором, чем пол и вес. Чем больше операций проводилось в центре, тем лучше себя чувствовали доноры.
«Болевые ощущения чернокожих после донации стволовых клеток из тазовых костей существенно острее, чем у представителей европеоидной расы», – это еще один вывод, сделанный в упомянутом выше исследовании. Более сильную боль испытывают при таком способе донации также женщины и «те, кому за 30». Хуже всех приходится немолодым чернокожим женщинам.
Еще одно исследование – «Острые токсические эффекты у неродственных доноров костного мозга в сравнении с донорами стволовых клеток из периферической крови» – было посвящено изучению длительности последствий донорства. Возможные последствия – жар, чувство усталости, кожные высыпания, тошнота, бессонница, головокружение. Степень выраженности этих недомоганий от вида донорства не зависела. Но после сдачи периферической крови они проходили заметно быстрее, чем при заборе стволовых клеток из костей. Через неделю после донации неприятные последствия для организма ощущали 15% из 6768 доноров, сдавших периферическую кровь, и 43% из 2726, сдавших костный мозг из тазовых костей. Через месяц после процедуры в обеих группах неприятные ощущения практически исчезли. Хотя у очень немногих из тех, кто сдал костный мозг из тазовых костей, отдельные последствия давали о себе знать даже через полгода.
Среди 51 тыс. доноров из уже упоминавшегося исследования в течение месяца после донации умерло пять человек. Одна смерть произошла прямо во время процедуры из-за серьезной врачебной ошибки. Еще один человек умер от легочной эмболии (закупорки легочной артерии тромбами) через две недели после процедуры, еще один – от кровоизлияния в мозг, двое – в результате остановки сердца. Эти четыре случая в принципе могли быть связаны с процедурой донации и анестезией, отмечают исследователи, но уверенности нет. Важнее другое: все пять погибших собирались поделиться своим костным мозгом с родственниками. Родственные доноры – условная группа риска, рассуждают исследователи: «По понятным причинам критерии отбора для родственных доноров могут быть менее строгими, чем для неродственных». Иными словами, там, где неродственного донора врачи, опасаясь возможных осложнений, скорее всего, отстранят от донации, родственный донор может настоять на своем праве попытаться спасти близкого человека, даже рискуя жизнью. Но бывает, что на риск решает пойти и неродственный донор. Узнав от врачей о серьезных противопоказаниях для такой процедуры именно в его конкретном случае, донор принимает сознательное решение подвергнуться опасности ради спасения чьей-то жизни. И да, такое решение может привести к трагической развязке. Мы об этом рассказывали.
В Японии было проведено большое исследование «Качество жизни неродственных доноров костного мозга, связанное с состоянием их здоровья». Объектом наблюдения стали 565 доноров. Каждому из них пришлось трижды отвечать на вопросы анкеты для оценки качества своей жизни: накануне донации, через неделю и через три месяца после нее. Анкета позволила оценить по 100-балльной шкале восемь параметров: общее состояние здоровья, наличие болей, эмоциональное состояние, социальное взаимодействие, душевное здоровье и др. Доноры с самого начала были отчасти «избранными»: все восемь показателей у них превышали среднеяпонский уровень. Через неделю после процедуры семь показателей – все, кроме душевного здоровья, – снизились. В особенности – физическое состояние. Зато через три месяца показатели не просто восстановились, но в основном превысили начальный уровень. Особенно благотворной донация оказалась для душевного здоровья и социального взаимодействия. Эти результаты – неплохая реклама донорства.
источник
Будущее медицины сегодня напрямую связывают с развитием клеточных технологий. Появился реальный шанс в успешном лечении даже самых тяжелых заболеваний и процессов старения организма. Эти технологии позволяют, не меняя поврежденный орган, «обновлять» его клеточный состав. Список болезней, при лечении которых клеточные технологии уже используются или их применение планируется в ближайшем будущем, быстро растет. Это, как правило, такие заболевания, медикоментозное лечение которых малоэффективно.
В Европе и Америке уже давно уделяется большое внимание созданию специализированных учреждений по заготовке, хранению, культивированию и применению стволовых клеток человека для лечения многих заболеваний. Один только штат Калифорния намерен в ближайшие 10 лет ежегодно тратить на исследования стволовых клеток $295 миллионов. При таких бюджетах научные исследования в этой области множатся год от года. Однако еще быстрее растут общественные ожидания и надежды. От клеток, способных превращаться в любой вид наших тканей, ждут излечения абсолютно всех недугов.
Термин «стволовая клетка» (по-английски «stem cell») означает, что каждая такая клетка дает начало целому древу потомков, в основании ствола которого она и находится. Среди клеток-потомков будут как клетки, идентичные стволовой и как бы формирующие ствол древа, так и специализированные клетки (мышечные, эпителиальные, нервные и др.), которые образуют ветви.
Стволовая клетка – это незрелая клетка, способная к активному делению и преобразованию в любые специализированные клетки организма (нервные, мышечные, печеночные и т.д.), это своего рода строительный материал, из которого получаются все остальные клетки.
Суть лечения заключается в ведении в организм стволовых клеток, которые встраиваются в поврежденные или стареющие органы и ткани, где под влиянием микроокружения, начинают размножаться и дифференцироваться в клетки данного органа и ткани, восстанавливая их структуру и функцию. В настоящее время именно с клеточной терапией связывают большие надежды на излечение таких заболеваний, как болезнь Паркинсона, болезнь Альцгеймера, сахарный диабет, циррозы печени, сердечно-сосудистые заболевания, а также на возможность замедления процессов старения организма.
Первые в мировой науке работы по стволовым клеткам еще в 1960–1970-е гг. выполнили советские ученые Чертков и Фриденштейн, но широкую известность стволовые клетки приобрели после «переоткрытия» их американскими учеными.
Самый богатый источник стволовых клеток (СК) — это ткань эмбриона. Когда оплодотворенная яйцеклетка начинает делиться, образуются первые тотипотентные стволовые клетки, которые могут превращаться в любую ткань. Примерно через четыре дня они начинают «специализироваться» (дифференцироваться) и становятся плюрипотентными стволовыми клетками, которые могут превращаться в не менее чем две возможные ткани (например, костную и мышечную). Со временем они становятся еще более специализированными стволовыми клетками — мультипотентными, из которых могут образовываться 2-3 вида клеток (из одних — различные клетки крови, из других — нервной системы и т. д.).
СК могут при необходимости могут трансформироваться в любую нужную клетку. Предположим, человек имеет несколько заболеваний. Каждый орган сигнализирует о своем нездоровье и посылает сигналы СОС. Когда СК попадают в организм, они улавливают эти сигналы и устремляются туда, где они нужны больше всего. СК — это клетки скорой помощи. Что они делают? Они создают новые клетки того органа, к которому пришли на помощь, или способствуют восстановлению поврежденных. Попадая в поражённое инфарктом сердце, они преобразуются в клетки сердечной мышцы, в поражённом инсультом головном мозгу — в нейроны и глиальные клетки. Стволовые клетки могут превращаться в клетки печени, костного мозга и т. д. При помощи клеточной терапии появилась возможность излечения огромного количества самых различных заболеваний.
Лучший источник стволовых клеток — эмбриональная ткань. Одна проблема — этическая. Использовать эмбриональную ткань — значит неминуемо погрязнуть в спорах, этично ли лечить клетками неродившегося ребенка, потворствовать абортам и т. д. Вторая проблема — потенциальная способность индуцировать развитие злокачественных образований, что было показано в исследованиях на животных. Онкологическая настороженность возникает при использовании только эмбриональных клеток. Теоретически если в организм вводится эмбриональная ткань, то появляются клетки с достаточно интенсивным делением и это небезопасно. Именно по этой причине большинство исследователей в клиниках работает с собственными стволовыми клетками пациентов или клетками из плаценты и пуповины. Стволовые клетки можно получить также из крови, но концентрация их там очень невелика, из костного мозга грудины, подвздошных костей, трубчатых костей.
Настоящий бум «ревитализации» (или есть еще неудачный термин «омоложение») начался в 1995 году, когда американцы обнародовали сведения о результатах введения этих клеток пожилым людям. У пациентов темнели седые волосы, разглаживались морщины, у мужчин увеличивалась потенция, а у женщин прекращались менопаузы. Такие сообщения породили во многом преждевременный оптимизм. Дело в том, что мы сейчас имеем в руках золотой ключик (стволовые клетки), с помощью которого пытаемся найти ту самую сокровенную дверь, ведущую нас к пониманию закономерностей жизненных процессов и сохранению здоровья человека.
Известно, что в процессе старения количество стволовых клеток в тканях снижается. Когда мы рождаемся, у нас в костном мозге на сто тысяч кроветворных клеток приходится десять стволовых, к 50-ти годам на миллион – две-три стволовых, а к 70 годам – в лучшем случае — одна на миллион. Из-за этого возможности человека по регенерации сильно ограничены. В результате страдает способность ткани к физиологической регенерации и к восстановлению после болезни или травмы. Результатом трансплантации стволовых клеток является значительное повышение регенераторных и адаптивных возможностей организма. Вызываемое этими клетками «обновление» организма может препятствовать развитию процессов, ведущих к старению. Отсюда перспективность и целесообразность использования клеточных технологий в лечении целого ряда заболеваний, обусловленных старением организма.
Пересадка стволовых клеток с целью замедления процессов старения имеет некоторые особенности. Количество трансплантаций и их повторяемость подбираются индивидуально, так как невозможно до начала лечения определить уровень дефицита стволовых клеток в тканях и степень их активности. Введенные стволовые клетки могут по разному использоваться организмом, т.е. дифференцироваться в разные виды клеток, в связи с чем проявление эффекта может быть различным. Пациенты могут ощущать повышение жизненного тонуса, прилив сил. Улучшается способность к концентрации внимания, острота мышления. Значительно уменьшаются проявления депрессии, нормализуется сон и аппетит. У творческих людей повышается вдохновение, продлевается активная творческая жизнь. Отмечается усиление полового влечения и потенции у мужчин при условии отсутствия органических причин (склероз сосудов, диабет, эндокринные расстройства). Встречаются и неожиданные эффекты, такие, как улучшение слуха, цветоощущения.
Клинические проявления и субъективные ощущения пациентом результатов лечения могут быть относительно скудными, так как изменения происходят на клеточном уровне и могут не сразу проявиться. Прослеживается отчетливая закономерность – чем лучше состояние здоровья пациента, тем меньше он ощущает изменений в организме. Это вполне объяснимо: невозможно дать организму здоровья больше, чем ему дала природа.
Сегодня клеточная терапия является альтернативой трансплантации органов и тканей человека, а также надежным способом продления молодости, здоровья и долголетия. Прежде всего надо сказать о трансплантации стволовых клеток при онкогематологических заболеваниях. Это зачастую единственный способ лечения лейкозов и других тяжелых заболеваний крови. В неврологии трансплантационная клеточная технология была впервые применена при лечении болезни Паркинсона. Весьма обнадеживающие результаты применения клеточной технологии получены при лечении болезни Хагинтона. Значительный опыт в лечении травматических поражений головного и спинного мозга накоплен в Новосибирском центре иммунотерапии и клеточной трансплантации. Ведущие медицинские центры Москвы, Новосибирска и некоторых других городов уже успешно использует клеточную терапию для лечения отдаленных последствий мозгового инсульта и рассеянного склероза. Было показано, что трансплантация низкодифференцированных клеток во взрослый организм может способствовать восстановлению кровотока за счет роста кровеносных сосудов в ишемизированных органах и тканях.
В Клинике восстановительной интервенционной неврологии и терапии «Нейровита» стволовыми клетками лечили участников чеченской войны, получивших боевые травмы головного мозга. Солдаты, у которых наряду с другими методами использовались и стволовые клетки, восстанавливались на 40% быстрее. Целый ряд других клинических наблюдений показывает, что использование клеточной терапии вполне оправдано в качестве основного или дополнительного метода лечения при самых различных заболеваниях.
Так, профессор Dohman и его коллеги из Техасского Центра Медицинских Исследований (Хьюстон) добились улучшения функции сердца у 14 больных с тяжелой сердечной недостаточностью. Терапия включала инъекцию стволовых клеток костного мозга пациента в левый желудочек. Одна из выдвигаемых гипотез объясняет эффективность пересадки стволовых клеток формированием новых кардиомицитов и кровеносных сосудов. Возможно, стволовые клетки запускают химическую реакцию, улучшающую работу клеток вблизи места инъекции.
В Научном центре сердечно-сосудистой хирургии им. Бакулева ведутся активные работы по лечению стволовыми клетками ишемии нижних конечностей. Обычно такое состояние лечат специальной операцией на сосудах, но для этих больных она была признана бесполезной. До сих пор это означало неизбежную ампутацию ноги. Но в центре «неоперабельным» больным в пораженные участки вводили стволовые клетки и в результате они не только избежали ампутации, но и кровообращение у них восстановилось быстрее, чем у тех пациентов, кому были сделаны традиционные операции.
Еще одна перспективная область применения стволовых клеток – эстетическая медицина. Введение стволовых клеток с помощью метода мезотерапии значительно улучшает состояние кожи, усиливает её кровообращение, устраняет морщины. Попадая в стволовые ниши кожи (на уровне дермального пространства), стволовые клетки способны надолго задержать процессы старения. При этом эти клетки позаботятся не только о вашей красоте, но и о здоровье, так как даже при местном введении наблюдаются общие положительные эффекты. Косметология и реконструктивная хирургия — особые области применения стволовых клеток. Косметология давно уже вышла за пределы чисто эстетической медицины. И врачам, и пациентам сегодня ясно, что выглядеть хорошо — значит не только не иметь морщин. Настоящий косметолог обязан сочетать в себе универсального врача, способного выявить у пациента все существующие (и начинающиеся) заболевания, поставить правильный диагноз, назначить адекватное лечение и лишь затем приступить к омоложению и устранению эстетических дефектов. Разумеется, к косметологу не обращаются тяжелобольные пациенты, но специфика нашего времени такова, что абсолютное большинство людей, считающих себя здоровыми, имеют те или иные недуги. Своевременное их распознавание и корректировка лежат в основе современного подхода в эстетической медицине.
Сегодня можно говорить только о том, что стволовые клетки способны заполнить дефект на уровне тканей, но никак не жизненно важных органов. Можно вырастить кожу, стенку сосуда, нервное волокно, но нельзя промоделировать и вырастить орган, выполняющий тысячи жизненно важных функций, например, печень. Здесь остаются, по-прежнему, актуальны работы по созданию «искусственных органов», таких, например, как разработанный недавно под руководством профессора Рябинина В.Е. аппарат «Биоискусственная печень». В настоящее время на основе сотрудничества между Челябинской медицинской академией, Южно-Уральского научного центра РАМН и Миасского завода медицинского оборудования создан промышленный образец этого аппарата и начались клинические исследования его терапевтической эффективности при лечении печеночной недостаточности на базе Челябинской областной клинической больницы.
Клеточная культура — это трансплантат, а не лекарственное средство. Методическая база по применению стволовых клеток определена не на законодательном, а на ведомственном уровне (Минздравсоцразвития РФ): имеется временная инструкция о порядке исследований в области клеточных технологий и их использования в учреждениях здравоохранения (2002 г.), приказ Минздравсоцразвития «О развитии клеточных технологий в Российской Федерации» (2003 г.), созданы положения о банке стволовых клеток. Для того, чтобы заниматься клеточной терапией необходимо иметь соответствующую медицинскую лицензию, положительные результаты доклинических и ограниченных клинических исследований предлагаемого метода лечения, решения Ученых советов и этических комитетов, разрешения Федеральной службы по надзору в сфере здравоохранения на клинические испытания и регистрацию клеточного материала.
источник
Кому и зачем нужна трансплантация костного мозга? Кто может стать донором, и чем это обернется для него?
В феврале 2016 в нескольких городах России проходила акция «Спаси жизнь ребенку с лейкозом», организованная «Русфондом» и медицинской лабораторией «Инвитро». Ее участники сдавали кровь на типирование, чтобы войти в Национальный регистр доноров костного мозга.
Трансплантация костного мозга (ТКМ) используется, прежде всего, при лечении онкологических заболеваний, таких как лейкозы, поражения лимфатической системы, нейробластома, а также при апластической анемии и ряде наследственных дефектов крови.
Не следует думать, что больному «меняют» его костный мозг на чей-то еще. На самом деле пациент получает внутривенно гемопоэтические стволовые клетки здорового человека, которые восстанавливают способность организма к кроветворению. Эти клетки могут развиваться, превращаясь в эритроциты, лейкоциты и тромбоциты.
В России применять ТКМ начали в 1990-х годах. Введение здоровых гемопоэтических стволовых клеток бывает необходимо, когда онкологический больной получает высокие дозы лекарств, иногда в сочетании с лучевой терапией, в результате чего кроветворение подавляется и не может восстановиться самостоятельно.
Иногда это единственный способ спасти человека, но он несет в себе и серьезные риски. Возможны острые иммунные реакции, когда клетки донора распознаются клетками реципиента как чужеродные и наоборот. В этом случае может произойти отторжение донорских стволовых клеток организмом больного или иммунная атака донорских клеток на его ткани.
Врачи могут не решиться проводить трансплантацию до наступления у пациента прочной ремиссии, как в случае с Евгенией Герасимовой, героиней программы «Пусть говорят».
Опасно также проводить эту процедуру при тяжелых сопутствующих заболеваниях, например, инфекционных.
Донором для пересадки костного мозга может быть и сам пациент. Это наиболее простой способ, поскольку иммунологические проблемы при нем не возникают. Если у онкологического больного не поражен костный мозг, у него могут заранее взять некоторое количество кроветворных стволовых клеток, а потом, после проведения интенсивной терапии, ввести ему их обратно.
Добровольные доноры требуются для так называемой аллогенной трансплантации, когда клетки берутся у другого человека. Чтобы проверить, подходит ли костный мозг для пересадки, у потенциального донора берется на анализ кровь и проводится типирование – определение HLA-фенотипа, то есть набора генов, отвечающих за совместимость тканей.
Большая вероятность такой совместимости есть у родственников, причем отец или мать обычно реже подходят на роль донора, чем брат или сестра. Однако идеальным донором – с таким же HLA-типом, как у больного — может оказаться и совершенно незнакомый человек, живущий в другом полушарии. Найти такого человека возможно только с помощью специальных регистров.
Регистры для поиска потенциальных доноров костного мозга начали создаваться в Европе и США еще в 80-х гг. Одними из первых возникли Фонд Энтони Нолана в Англии и Фонд Стефана Морша в Германии. В настоящее время в некоторых странах существуют национальные регистры, в которых объединены данные различных специализированных организаций. Так, национальный регистр NMDP в США содержит сведения о 9 млн доноров, DKMS в Германии – о 5 млн. Международный регистр IBMTR объединяет информацию о 20 млн доноров из всех мировых регистров.
В России на данный момент зарегистрировано лишь 43 тысячи потенциальных доноров.
Этого недостаточно для подбора подходящего HLA-типа для каждого больного, нуждающегося в ТКМ. Между тем поиск и привлечение российских доноров в десять с лишним раз дешевле, чем те же действия с использованием международных регистров и доноров-иностранцев. А главное, поиск в национальном регистре экономит время, важное для успешного лечения.
В 2013 году «Русфонд» совместно с Первым Санкт-Петербургским медицинским университетом и рядом других организаций создал Национальный регистр доноров костного мозга имени Васи Перевощикова. Он состоит из восьми локальных регистров. Среди них – Петербургский (на базе НИИ детской онкологии, гематологии и трансплантологии имени Р.М. Горбачевой), Челябинский (Челябинская областная станция переливания крови), Самарский (Самарская областная станция переливания крови), Ростовский (Ростовская областная станция переливания крови), Екатеринбургский (Свердловская областная клиническая больница № 1).
Врачи считают, что процедура забора костного мозга у донора намного проще, чем обычное хирургическое вмешательство. Под общим или эпидуральным наркозом с помощью полой иглы в шприц закачивается небольшая часть костного мозга (это жидкость) из верхнего края тазовых костей. Обычно приходится делать несколько проколов, чтобы набрать необходимое количество этой жидкости. После этого донор проводит в стационаре около двух дней.
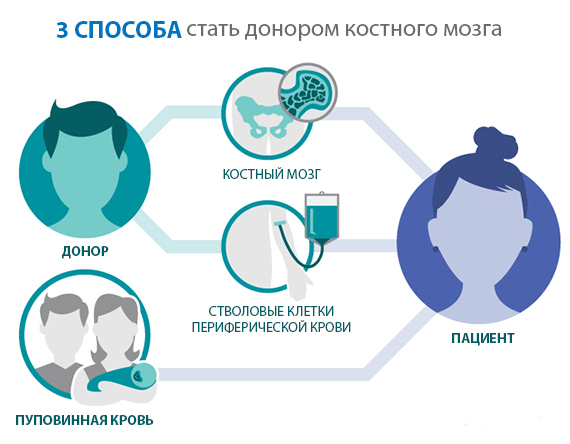
Самым неприятным моментом во всей процедуре забора костного мозга является анестезия, считают врачи. Уровень гемоглобина снижается незначительно. Костный мозг восстанавливается приблизительно месяц. Болезненные ощущения в спине проходят через несколько дней.
Второй способ – получение кроветворных клеток из периферической крови. Предварительно донору дают препарат, «выгоняющий» нужные клетки из костного мозга. Затем из вены берут кровь, она проходит через прибор, разделяющий ее на компоненты, гемопоэтические стволовые клетки собираются, а остальная кровь возвращается в организм через вену на другой руке. Для отбора нужного количества клеток вся кровь человека должна несколько раз пройти через сепаратор. Процедура продолжается пять-шесть часов. После нее донор может испытывать симптомы, похожие на недомогание при гриппе: боли в костях и суставах, головные боли, иногда повышение температуры.
Донором может стать любой человек в возрасте от 18 до 50 лет, если у него не было гепатитов В и С, туберкулеза, малярии, ВИЧ, нет онкологического заболевания или диабета.
Если вы решили стать потенциальным донором костного мозга, то сначала надо сдать 9 мл крови на типирование и подписать соглашение о вступлении в регистр. В случае, если ваш HLA-тип подойдет какому-нибудь больному, нуждающемуся в ТКМ, то вам предложат пройти дополнительные обследования. Безусловно, вы должны будете подтвердить свое согласие выступить в роли донора.
На сайте «Русфонда» опубликован список лабораторий, где можно сдать кровь, чтобы оказаться в Национальном регистре доноров.
В России трансплантацию костного мозга проводят всего в нескольких медицинских учреждениях: в Москве, Санкт-Петербурге и Екатеринбурге. Количество специализированных коек ограничено, как и число квот на бесплатное лечение.
ФНКЦ «Детская гематология, онкология и иммунология» им. Дмитрия Рогачева Миндзрава РФ ежегодно делает до 180 пересадок гемопоэтических стволовых клеток у детей.
Институт детской гематологии и трансплантологии им. Р. М. Горбачевой в Санкт-Петербурге в 2013 году, по данным «Коммерсанта», провел 256 таких процедур по квоте и 10 платных, в 2014 году Минздрав выделил этому учреждению в общей сложности 251 квоту.
В Свердловской областной детской клинической больнице № 1 с 2006 года было сделано немногим более 100 трансплантаций костного мозга, а в Свердловской областной клинической больнице № 1 (для взрослых) на 2015 год было запланировано всего 30 ТКМ.
Что касается количества специализированных коек, то в Институте им. Горбачевой, например, их 60, а в Свердловской областной детской клинической больнице № 1 — 6.
Между тем, по данным благотворительного фонда «Подари жизнь», ежегодно в трансплантации костного мозга в России нуждается не менее 800-1000 детей — не считая взрослых.
Если лечиться за свои деньги, то оплата одного только койко-дня в отделении трансплантации гемопоэтических стволовых клеток института им. Рогачева обойдется как минимум в 38500 рублей. В целом же стоимость ТКМ в Москве, по данным компании Мед-Коннект, может доходить до 3 миллионов рублей, а в Санкт-Петербурге — до двух миллионов рублей.
За лечение в Германии приходится платить до 210 тысяч евро, а в Израиле — до 240 тысяч долларов. И все это без учета поиска донора в Международном регистре, который выльется еще в 21 тысячу евро. В России этот поиск оплачивают, как правило, благотворительные фонды — такие как «Русфонд», «Подари жизнь», «AdVita».
источник
В современной медицине нет темы более спорной и скандальной, чем стволовые клетки. Косметические салоны как по волшебству обещают омолодить и оздоровить клиентов клеточными методами, а ученые бьют тревогу. В прессе звучат грозные предупреждения и леденящие душу истории о неблагоприятных последствиях такого лечения.
Так что же такое стволовые клетки – эликсир вечной молодости и здоровья или очередной рекламный трюк? Слово – специалисту в данной проблеме, Сергею Георгиевичу ИВАНОВУ, доктору медицинских наук, профессору, академику Международной академии наук информации и информационных технологий, научному руководителю по терапии центральной клинической больницы Главного медицинского управления УД президента РФ.
В числе его пациентов – артисты и звезды шоу-бизнеса, кто всегда готов опробовать на себе передовые (пусть даже не до конца изученные) технологии, лишь бы как можно дольше сохранять свой рабочий инструмент – привлекательную внешность. – Действительно, наши звезды частенько спрашивают моего совета в отношении клеточной терапии, – говорит Сергей Георгиевич. – Причем это не обязательно люди в возрасте. Многие юные дарования за 2–3 года успешных выступлений умудряются истратить большую часть своей энергии. И хотя они уверены, что стареть человек начинает где-то после 30 лет, мысль привести себя в норму новомодным методом приходит в голову даже им.
Миф 1. Стволовые клетки – лекарство против старения.
К сожалению, активное старение начинается уже в 15 лет, а самые высокие его темпы наблюдаются у двадцатилетних. В 40–50 лет скорость, с которой появляются морщины и теряет упругость тело, заметно снижается. Панацеи от старости и болезней пока не найдено. Что касается стволовых клеток, раздутая вокруг них шумиха скорее связана с большими деньгами, нежели с уникальными результатами. Судите сами – минимальный курс из 4 инъекций в швейцарской клинике стоит около 15 тысяч евро. Не стану отрицать, домой пациент вернется отдохнувшим, помолодевшим, полным сил и жизненной энергии. Но этот эффект в большей степени объясняется размером суммы, потраченной на себя, любимого, целебным климатом и сказочно роскошной обстановкой (вплоть до постельного белья, подобранного под цвет глаз), ежедневным массажем под тихую музыку и ароматическими ваннами. А на долю стволовых клеток в восстановлении жизненного тонуса выпадет совсем небольшая заслуга. Дело в том, что они в принципе не могут поворачивать вспять биологическое время и все рассказы об омолаживающем действии клеточной терапии – не более чем миф.
Как работают стволовые клетки.
После слияния яйцеклетки и сперматозоида образуется первая клетка будущего организма – зигота. Она-то и дает начало эмбриональным стволовым, из которых в дальнейшем развиваются все прочие, составляющие основу органов и тканей. Однако часть стволовых клеток ускользает от развития и остается в законсервированном виде, пока в теле не возникнут какие-либо нарушения, травмы или заболевания. Тогда дремавшие до поры до времени клетки, как члены слаженной ремонтной бригады, поспешат на помощь поврежденным тканям. Чем чаще болеете, тем меньше таких ремонтных клеток остается в запасе. При современном образе жизни их количество заметно уменьшается уже к 20 годам, а после 40 лет микроскопических ремонтников, как говорится, днем с огнем не сыщешь. Именно поэтому идея ввести в организм столовые клетки извне кажется заманчивой и логичной. Но никто пока не знает, каким образом они действуют. Возможно, они играют роль агитаторов – стимулируют погибающую клетку к дальнейшей жизнедеятельности, но не исключено, что и сами становятся на ее место и начинают активно трудиться.
Терапия собственными стволовыми клетками – самый безопасный и грамотный, но и наиболее наукоемкий метод, осуществляемый только на базе крупнейших университетских клиник. В последнее время на Западе, где религиозные организации выступают против использования клеток человеческого эмбриона, начинают применять стволовые клетки животных, чаще всего акулы и черной овцы. Последняя пользуется наибольшим спросом – ее проще разводить в научных целях, контролируя все этапы роста.
Миф 2. Стволовые клетки – панацея от всех болезней.
Бум на клеточную терапию в России начался в 2001–2002 году. Как грибы после дождя, стали плодиться медицинские центры и клиники, предлагавшие подобные технологии. А вернее – то, что за них выдавалось, поскольку для выделения настоящих стволовых клеток и изготовления препаратов на их основе требуются колоссальные финансовые средства, сверхсовременное оборудование и лицензионные технологии. Ничего подобного у большинства клиник не было и в помине.
Тем не менее в Москве действует более 50 медицинских центров и косметических салонов, которые помимо радикального омоложения и избавления от морщин с помощью клеточных технологий обещают пациентам восстановить потенцию и зрение, исцелить от синдрома хронической усталости, мигрени и прочих заболеваний. Когда зарубежные коллеги слышат подобные посулы, у них возникает масса вопросов к тем, кто предоставляет такого рода услуги. Разумеется, ответов на них никто не получит. Иной раз просто волосы дыбом встают! В самых прогрессивных западных институтах еще только начали проводить клинические исследования клеточной терапии на первых добровольцах, а в России уже лечат всех желающих и гарантируют им 100%-ный результат.
Эмбриональные стволовые клетки первыми выделили западные ученые в 1998 году. Но клеточные технологии применяли наши врачи еще в XIX веке. Во время крымской войны Н. И. Пирогов измельчал ткани поджелудочной железы лошадей и заполнял этой кашицей гнойные раны, которые на удивление быстро заживали. Сам великий хирург приписывал такое действие уникальным свойствам поджелудочной железы, но сегодня ученые не исключают, что в раны попадали и стволовые клетки, содержавшиеся в лошадиных тканях.
Миф 3. Стволовые клетки гарантируют результат, который долго сохранится.
В косметологических салонах очень популярна мезотерапия – введение в кожу лица и область декольте клеточных препаратов. Вот только что это и откуда они взялись? Тщательная проверка показала, что в большинстве случаев в инъекционном материале находилось не более 2% живых клеток. В лучшем случае использовали биологически активные клеточные компоненты, в худшем – все что угодно.
Сомнительные препараты вызывают побочные эффекты. Но даже при введении стволовых клеток результат непредсказуем. Это – настолько новый и неизученный метод, что на сегодняшний день не существует стандартов на клеточный материал и отработанных способов его клинического применения. Например, при обкалывании лица косметологи “на глазок” дозируют инъекционный препарат, содержащий фибробласты. Когда пациенту назначают антибиотики или витамины, ему четко говорят, сколько лекарства принимать, а клеточный материал вводят как Бог на душу положит! Введешь мало – никакого видимого эффекта. Клиент, заплативший солидную сумму, предъявит претензии. А вколешь от души – и в местах инъекций могут образоваться рубцы.
Но даже если вам действительно введут фибробласты или стволовые клетки, а не дешевый суррогат и даже каким-то чудом не ошибутся с дозировкой, нужно понимать, на что способен этот биологический материал. Эффект от применения стволовых клеток очень недолгий. Максимум – 1–1,5 года. Пациенту об этом не скажут, напротив, гарантируют от 5 до 20 лет счастливой жизни без морщин и болезней.
Впрочем, пообещать могут все что угодно. Например, избавить от облысения клеточными препаратами. Увидев подобное объявление во время визита в Москву, мои коллеги – врачи из Германии были потрясены до глубины души. Оказывается, в Европе до такой процедуры – в косметическом салоне колоть в лысину стволовые клетки еще не додумались. Это полная профанация метода – не проведя клинических исследований, браться за лечение пациентов!
Запретить этот спорный метод, на мой взгляд, было бы крайне неразумно, да и невозможно. У стволовых клеток, безусловно, есть будущее. Это только в России все клеточные страсти кипят вокруг косметологии. За рубежом исследования ведутся в рамках “медицины отчаяния” – лечения тяжелых хронических заболеваний. Именно такое направление клеточной терапии считается наиболее перспективным. Хотя научные изыскания начались недавно, результаты впечатляют: обреченные на смерть пациенты продолжают жить и работать.
К сожалению, вопросов тут пока намного больше, чем ответов. Когда ученые выяснят, как все происходит на самом деле, в медицине произойдет настоящий прорыв.
А пока. к использованию клеточных методов нужно подходить с крайней осмотрительностью. Тем, кто решился на подобное лечение, я посоветую обращаться только в специализированные клиники, располагающие качественными препаратами, владеющие технологиями их применения, где в состоянии контролировать лечение.
источник
Стволовые клетки: мифы и реальность
«Ни одна область биологии при своем рождении не была окружена такой сетью предубеждений, враждебности и кривотолков, как стволовые клетки», – считает член-корреспондент РАМН, специалист в области медицинской клеточной биологии Вадим Сергеевич Репин (Московский Центр медико-биологических технологий).
Хотя термин «стволовая клетка» был введен в биологию еще в 1908 году, статус большой науки эта область клеточной биологии получила в последнее десятилетие ХХ века. В 1999 году журнал Science признал открытие стволовых клеток третьим по значимости событием в биологии после расшифровки двойной спирали ДНК и программы «Геном человека». Один из первооткрывателей структуры ДНК, Джеймс Уотсон, комментируя открытие стволовых клеток, отметил, что устройство стволовой клетки уникально, поскольку под влиянием внешних инструкций она может превратиться в зародыш либо в линию специализированных соматических клеток.
Действительно, стволовые клетки – прародительницы всех без исключения типов клеток в организме. Они способны к самообновлению и, что самое главное, в процессе деления образуют специализированные клетки различных тканей. Таким образом, все клетки нашего организма возникают из стволовых клеток.
Стволовые клетки обновляют и замещают клетки, утраченные в результате каких-либо повреждений во всех органах и тканях. Они призваны восстанавливать и регенерировать организм человека с момента его рождения. Потенциал стволовых клеток только начинает использоваться наукой. Ученые надеются в ближайшем будущем создавать из них ткани и целые органы, необходимые больным для трансплантации взамен донорских органов. Их преимущество в том, что их можно вырастить из клеток самого пациента, и они не будут вызывать отторжения.
Потребности медицины в таком материале практически неограниченны. Только 10-20 процентов людей вылечиваются благодаря удачной пересадке органа. 70-80 процентов пациентов погибают без лечения на листе ожидания операции. Таким образом, стволовые клетки в каком-то смысле действительно могут стать «запчастями» для нашего организма. Но для этого вовсе не обязательно выращивать искусственные эмбрионы – стволовые клетки содержатся в организме любого взрослого человека.
Откуда берутся стволовые клетки
По своему происхождению стволовые клетки разделяют на эмбриональные, фетальные, стволовые клетки пуповинной крови и стволовые клетки взрослого человека.
Источником эмбриональных стволовых клеток является бластоциста – зародыш, который формируется к пятому дню оплодотворения. Эти стволовые клетки способны дифференцироваться абсолютно во все типы клеток взрослого организма. Но у этого источника стволовых клеток есть недостатки. Во-первых, эти клетки способны спонтанно перерождаться в раковые клетки. Во-вторых, в мире пока не выделена безопасная линия истинно эмбриональных стволовых клеток, годных для клинического применения.
Фетальные стволовые клетки получают из абортивного материала на 9-12 неделе беременности. Помимо этических и юридических трений, использование непроверенного абортивного материала чревато осложнениями, такими, как заражение пациента вирусом герпеса, вирусными гепатитами и даже СПИДом. Если же проводить диагностику материала на вирусы, увеличивается себестоимость метода, что в конечном итоге приводит к увеличению стоимости самого лечения, которое в определенных случаях может быть весьма эффективным.
Источником стволовых клеток является также плацентарно-пуповинная кровь, собранная после рождения ребенка. Эта кровь очень богата стволовыми клетками. Взяв эту кровь и поместив в криобанк стволовых клеток, в дальнейшем можно использовать ее для восстановления практически любых тканей и органов, а также для лечения любых заболеваний, в том числе и онкологических. Однако количество стволовых клеток в пуповинной крови не достаточно велико, и эффективное их применение возможно только однократно для самого ребенка до 10 лет.
Самым доступным источником стволовых клеток является костный мозг человека, так как концентрация стволовых клеток в нем максимальная. В костном мозге выделяют сразу два вида стволовых клеток: первый – это гематопоэтические стволовые клетки, из которых формируются абсолютно все клетки крови, второй – это мезенхимальные стволовые клетки, которые регенерируют практически все органы и ткани.
Зачем нужны стволовые клетки
Если у человека есть свои стволовые клетки, то почему органы сами не регенерируют после повреждения? Причина в том, что в процессе взросления человека наблюдается катастрофическое снижение количества стволовых клеток: при рождении – 1 стволовая клетка встречается на 10 тысяч, к 20 – 25 годам – 1 на 100 тысяч, к 30 – 1 на 300 тысяч. К 50-летнему возрасту в организме уже остается всего 1 стволовая клетка на 500 тысяч, причем именно в этом возрасте, как правило, уже появляются такие болезни, как атеросклероз, стенокардия, гипертония и т.д. Истощение запаса стволовых клеток вследствие старения или тяжелых заболеваний, а также нарушение механизма их выброса в кровь лишает организм возможностей эффективной регенерации, в результате чего жизнедеятельность тех или иных органов истощается.
Увеличение количества стволовых клеток в организме приводит к интенсивной регенерации и восстановлению поврежденных тканей и больных органов за счет образования молодых, здоровых клеток на месте утраченных. Современная медицина уже обладает такой технологией – она называется клеточной терапией.
Что такое клеточная терапия
Организм человека развивается до 25 лет, после чего начинается процесс старения, когда с каждым днем человек замечает за собой не самые приятные изменения своего тела. Возрастные изменения кожи, изменения в деятельности эндокринных и половых желез, мышечных тканей, иммунной и нервной систем также связаны с истощением запаса стволовых клеток. Для компенсации этого запаса и необходима клеточная терапия. Здоровым людям нет необходимости начинать поддерживающую терапию ранее 35 лет. Напротив, всем кто перенес серьезные болезни, травмы, ожоги или отравления процедуры показаны в любом возрасте.
Отечественная наука и медицина обладают одним из лучших потенциалов в области исследования и применения клеточной терапии в мире. Первые направленные поиски в области стволовых клеток костного мозга человека начались в результате методического прорыва, осуществленного Александром Яковлевичем Фриденштейном в середине 70-х годов ХХ века. В его лаборатории впервые была получена однородная культура стволовых клеток костного мозга. После прекращения деления стволовые клетки под влиянием условий культивирования превращались в костную, жировую, хрящевую, мышечную или соединительную ткань. Пионерские разработки А.Я.Фриденштейна заслужили международное признание.
Сейчас с помощью терапевтической трансплантации стволовых клеток имеется возможность лечить или использовать в качестве сопровождающей терапии целый спектр заболеваний – сахарный диабет, атеросклероз, ишемическую болезнь сердца, хронические заболевания суставов, застарелые травмы, гепатиты и циррозы печени, аутоиммунные заболевания, болезни Альцгеймера и Паркинсона, синдром хронической усталости.
С помощью клеточной терапии быстро заживают ожоги, раны, язвы и рубцы кожи, осуществляется реабилитация после инсультов и черепно-мозговых травм, проводится комплексная программа регенерации (улучшение функциональных способностей организма и качества жизни) и мезотерапия лица, рук, проблемных (вялых) зон и всего тела. Клеточная терапия используется как поддерживающая терапия при рассеянном склерозе, сексопатологиях и бесплодии у мужчин и женщин, онкологических заболеваниях.
Безусловно, использование стволовых клеток не является панацеей. Так, их применение в онкологии не приводит к излечению от рака. Однако имеется ряд уникальных программ, направленных на реабилитацию больных в период ремиссии и перерывов между курсами химиотерапии. Больные, получающие такой курс, значительно лучше переносят все процедуры, уменьшается количество осложнений, появляется возможность повторить процедуры раньше. Таким образом, шансы на успех значительно возрастают. Помимо этого, стволовые клетки обладают и доказанным противораковым эффектом: они сдерживают процессы развития опухоли и активизируют иммунную систему.
Как проводится клеточная терапия
После проведения обследования и сбора анализов пациенту предлагают сдать кровь (костный мозг), в которой постоянно присутствует некоторое количество стволовых клеток. Современные технологии позволяют выделить стволовые клетки, после чего вырастить эти клетки в специальной среде в значительно большем количестве. По окончании процесса культивации пациенту назначают индивидуальный курс введения родного клеточного материала. Все лечение протекает амбулаторно и не требует изменения обычного ритма жизни.
Для сбора собственного клеточного материала необходима пункция костного мозга. Подготовка к процедуре, сама процедура забора костного мозга и отдых после нее длятся 1,5 часа (сама процедура занимает не более 20 минут), после чего пациенту необходимо прийти к врачу через 7 дней для первичного введения и далее посещать его для последующих введений согласно составленному графику.
Введение клеточного материала – безболезненная процедура, проводимая амбулаторно в стерильных условиях. Клеточный материал может вводиться внутривенно, внутримышечно, внутрисуставно, подкожно, а также в виде аппликаций – в зависимости от метода лечения и характера заболевания.
Средняя продолжительность курса (в зависимости от выбранной программы) – 2,5-3 месяца. Помимо начального этапа, пациенту не требуется посещать врача более чем 1-2 раза в неделю на протяжении всего курса.
Как правило, половина всех пациентов интересуется комплексной программой регенерации организма. Другая половина пациентов – это больные различных возрастов, с разными заболеваниями и их осложнениями – после серьезных травм, аварий, инсультов, ожогов, после операций, стрессов, кардиологических осложнений.
Клеточная терапия – это будущее современной медицины, это направление интенсивно развивается во всем мире. Приятно, что наша страна в этой области не только не отстает от других стран, но кое в чем их опережает.
источник