Простые одноклеточные микробы способны нанести человеку большой вред, убить иммунную систему и сделать уязвимым к привычным болезням. Протозойные инфекции, возбудителями которых являются паразиты, при попадании в организм могут спровоцировать серьезные (даже смертельные) заболевания. В мире существует много видов патогенных микроорганизмов, но не все они одинаково опасны.
В процессе жизнедеятельности большинство микробов используют органические вещества, которые есть в организмах людей, домашних животных. Угрозу здоровью человека представляют только 50 видов паразитов. Протозойные инфекции – это паразитарные инфекции, которые способны оккупировать здоровые органы и ткани тела. Некоторые микроорганизмы не вредят человеку со здоровым иммунитетом, но для пациентов с вирусом иммунодефицита могут стать смертельным приговором. Клиническая картина болезни зависит от вида протозооза, диагностики и выбора метода лечения.
Где можно заразиться паразитами класса протозоозов (основные пути попадания возбудителя в организм человека):
- употребление плохо помытой еды или неочищенной воды;
- нарушение правил гигиены;
- контакт с болеющими животными (даже без признаков острого заболевания);
- укусы насекомых (они переносят инфекции);
- половой путь.
Ученые выделяют одноклеточные микроорганизмы в отдельный класс «простейших». Возбудителями протозойной инфекции могут стать только те микроорганизмы, которые приспособлены к паразитарному образу жизни. Для их размножения не нужен половой путь, они способны быстро увеличивать свое количество в организме путем деления. Паразиты состоят из одной клетки, которая содержит все необходимое для жизнедеятельности и размножения. Жертвой протозойного заболевания может стать любой человек, ведь иммунная система организма не всегда может справиться с инфекцией.
Возбудитель заболеваний проходит в организме человека определенные этапы жизнедеятельности. Жизненный цикл паразитов состоит из 3 стадий:
- этап заражения человека (попадание возбудителя в организм);
- размножение, в результате которого создается большое количество паразитов;
- откладывание паразитом цист и выведение их из организма с фекалиями.
Паразиты, попадая в организм человека, вызывают его интоксикацию и разрушают иммунную систему. Некоторые заболевания, вызываемые протозоозами, широко распространены в странах с жарким климатом и плохими санитарными условиями. В нашем регионе известны такие протозойные заболевания: лямблиоз, токсоплазмоз. Болезни, вызываемые простейшими, могут протекать бессимптомно, но в некоторых случаях (неправильная расшифровка результатов анализов, некачественное изучение симптомов либо упущенное время) могут привести к смерти.
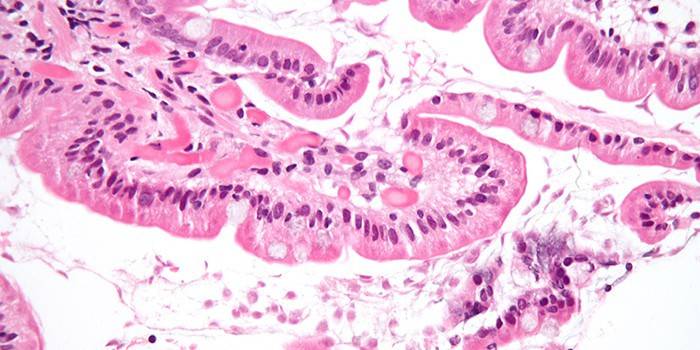
По внешним признакам ученые выделяют несколько видов одноклеточных паразитов (протозоозов), способных вызвать протозойные заболевания:
- корненожки – представитель амеба;
- жгутиконосцы – опасный паразит лейшмания, трипаносомы (провоцируют сонную болезнь, переносятся мухой Цеце);
- ресничные инфузории – возбудитель балантидий;
- споровики – представитель малярийный плазмодий.
Признаки протозойных заболеваний отличаются в зависимости от вида возбудителя и работы иммунной системы организма, но есть и такие, которые характерны для большинства болезней. Симптомами протозойной инфекции могут быть диарея, рвота и расстройства желудочно-кишечного тракта, слабость в теле, повышенная температура, сонливость или воспаление слизистых оболочек. При обнаружении этих признаков, нужно пройти обследования (анализы крови, кала). Протозойные болезни могут протекать бессимптомно, а могут приобретать острую или хроническую (рецидивирующую) форму.
Другие названия этой протозойной болезни – амебная дизентерия или «болезнь грязных рук». Амебиаз зачастую проходит бессимптомно, но бывают ситуации, когда его признаки путают с банальным аппендицитом, поэтому важна достоверность результатов лабораторных исследований и диагностики. Вероятность заражения этим паразитом выше в жарком климате, странах с низким уровнем санитарных условий. Возбудитель попадает в организм с загрязненной пищей. Инкубационный период длится от 1 недели до 2-3 месяцев.
Амебы, попадая в организм человека, вызывают нарушения в работе желудочно-кишечного тракта. Симптомы заражения:
- частая дефекация;
- кал с примесями крови, слизи;
- лихорадка;
- метеоризм, вздутие, диарея;
- болезненные ощущения в спине, животе;
- запоры.
Зачастую промежуточными хозяевами и носителями лямблий становятся собаки, кошки и домашний скот. Заражение протоозами происходит фекально-оральным путем. Для большинства случаев заболеванию характерно бессимптомное протекание, но оно может проявляться и в острой форме. Лямблиоз вызывают кишечные протозоозы, поэтому они, в основном, поражают желудочно-кишечный тракт. Особенно часто при заражении появляются такие симптомы: отсутствие аппетита, метеоризм, вздутие, жидкий стул, изжога, диарея и понос, боли в животе.
Одна из самых опасных болезней, вызванных протоозами – малярия. Инфицирование происходит через контакт со слюной комара, симптомы проявляются через неделю после заражения. Малярия зачастую начинается с тяжелого течения, с повышением температуры до 40-41 градусов, сильной головной боли, нарушений сердечного ритма, одышки, анемии. После окончания приступа человек обильно потеет, температура спадает, состояние улучшается до следующего рецидива. При отсутствии лечения и помощи, болезнь может привести к церебральной малярии, смертельному исходу.
Разные виды возбудителей малярии отличаются симптомами и длительностью вызываемого протозойного заболевания:
- Plasmodium falciparum – возбудитель болезни тропическая малярия (высокая смертность);
- Р. vivax (вивакс-малярия) – возбудитель болезни 3-дневная малярия (приступы через 40-45 часов);
- Р. ovale – возбудитель болезни овале-малярия (приступы через 40-45 часов);
- Р. malariae – возбудитель болезни 4-дневная малярия (приступы через 72 часа).
Болезнь, вызванная токсоплазмами, зачастую носит хронический характер. Острая фаза встречается у пациентов очень редко, но может привести к летальному исходу. Переносят это заболевание кошки, возбудитель попадает в пищевой тракт через плохо вымытые продукты или сырое мясо. Очень опасно заражение токсоплазмозом для женщин, во время беременности недуг может передаваться плоду и вызывать пороки развития организма и даже гибели.
Часто симптомы протозойной инвазии токсоплазмозом путают с проявлениями гриппа, другими инфекциями или расстройствами желудочно-кишечного тракта. Признаки токсоплазмоза:
- лихорадка, повышение температуры;
- увеличение печени;
- головная боль, боль в животе;
- заболевания желудочно-кишечного тракта (рвота, диарея, запор, частая дефекация, метеоризм, вздутие).
Для подтверждения предварительного диагноза проводят лабораторную диагностику протозойных инфекций. Зачастую лаборатории ограничиваются анализом кала или соскобом со слизистой оболочки толстой кишки, но более информативным является анализ крови на обнаружение следов паразита. Поскольку у паразитов есть способность размещаться в разных органах и тканях, необходимо точно определить предмет исследования. Это может быть моча, костный мозг, кровь, мокрота.
Методы лабораторной диагностики на наличие в организме разных видов паразитов
Дизентерийные амебы (корненожки)
Анализ кала, анализ крови мало информативен.
Жгутиконосцы (трихомонады, лямблии, лейшмании)
- лямблии – анализ кала и мочи;
- лейшмании – мазки крови, исследования костного мозга.
- трихомонады – лабораторный анализ соскобов со слизистых оболочек.
Споровики (малярия, бабезиоз, кокцидоз, изоспороз)
Исследования мазков крови и толстых капель крови.
Основная задача исследования фекалий – выявить цисты паразитов, которые выходят из организма. Анализы кала на протозоозы проводятся при подозрении на заражение, при поступлении в детские учреждения и во время госпитализации. Чтобы результаты были достоверными, нельзя принимать перед забором кала слабительные препараты. Фекалии нужно собрать в чистую банку, без мочи, поставить в прохладное место и на протяжении 10-12 часов занести на лабораторные исследования. Если нужно обнаружить живые микробы, кал на копрограмму сдают не позднее, чем через час после сбора.
Каждый возбудитель имеет свои особенности, поэтому схема лечения очень отличается в зависимости от симптомов. Лечение протозойных инфекций зачастую проводят в условиях стационара, особенно если есть симптомы острого течения заболевания. Для быстрого снятия тяжелых симптомов, приступов и рецидивов используют антибактериальные препараты, но их можно применять только наблюдаясь у специалиста. Если обнаружены негативные изменения в работе организма или другие признаки, необходимо обязательно посоветоваться с врачом.
Обезопасить себя от риска заражения инфекцией можно, если правильно проводить профилактику от протозойных заболеваний. Меры профилактики заключаются в следующем:
- качественное мытье еды;
- термическая обработка мяса и рыбы;
- соблюдение правил содержания животных;
- при контакте с грунтом надевать защитные перчатки;
- личная гигиена;
- минимальное посещение стран с высоким риском заражения паразитами;
- защита от насекомых-носителей.
Для того чтобы вылечить протозойные заболевания, необходимо использовать противомалярийные и противоамебные лекарственные препараты. Они отпускаются по рецепту врача, существуют разные формы выпуска. Антипротозойные препараты нельзя применять без консультации с врачом, ведь только специалист может назначить правильную дозировку и метод применения (зависит от клинической картины пациента). Взаимодействие с другими лекарственными средствами и влияние на организм больного с хроническими болезнями не изучено. В таком случае схема лечения требует корректировки.
Для устранения бактериальных инфекций применяют разные лекарственные препараты, один из самых эффективных Трихопол. Существуют разные формы выпуска лекарства: для орального или наружного применения. Препарат назначают для лечения инфекций дыхательных путей, при заболеваниях кожи (также внешних половых органов) и поддержки центральной нервной системы Курс лечения препаратом Трихопол не менее 10 дней, желательно перейти на диетическое питание. Лечение Трихополом имеет побочные эффекты – уничтожение полезных бактерий, появление вторичных симптомов.
источник
Попадая в организм человека, простейшие могут носить патогенный характер и активизироваться от негативных факторов окружающей среды. Заражение опасными микроорганизмами происходит бытовым или половым путем, и избежать негативных изменений в организме чрезвычайно трудно.
Лямблиоз, малярия, хламидиоз и прочие распространенные недуги имеют схожую природу – возбудителя, способного поразить человека в самый неподходящий момент. Все виды инвазии, относящиеся к следствиям размножения простейших, требуют срочного медикаментозного лечения.
Угрозы из-за активного размножения простейших подстерегают каждого, кто вовремя не распознал патогенные процессы в собственном организме. В каждом отдельном случае микроорганизмы способствуют развитию сложных заболеваний с последствиями для человека:
Недуг, который передается через пищу и переносится с помощью насекомых, чаще поражает кишечник, но в иногда могут поражаться и другие органы.
Заболевание, которым можно заразиться через пищу (в основном через мясные продукты). Последствия заражения балантидиями – перфорация кишечника и развитие перитонита. Должная гигиена тела, особенно рук, и обработка мясных продуктов, которое употребляет в ежедневном рационе человек, предотвратят развитие балантидиаза.
Болезнь, переносчиком которой являются насекомые (москиты), способствует развитию анемии и лихорадки. Опасный недуг приводит к увеличению внутренних органов, что влечет за собой нарушения в их работе.
Опасные цисты проникают в организм через пищу, фрукты или овощи. Немытые руки, грязная посуда – мелочи, которые способствуют заражению лямблиозом. Заболевание такого рода сопровождается болью в животе и правом подреберье, тошнотой и интоксикацией.
По статистике более 1 миллиарда человек заражено паразитами. Вы даже можете не подозревать, что стали жертвой паразитов.
Определить наличие паразитов в организме легко по одному симптому — неприятному запаху изо рта. Спросите близких, пахнет ли у вас изо рта утром (до того, как почистите зубы). Если да, то с вероятностью 99% вы заражены паразитами.
Заражение паразитами приводит к неврозам, быстрой утомляемости, резкими перепадами настроениями, в дальнейшим начинаются и более серьезные заболевания.
У мужчин паразиты вызывают: простатит, импотенцию, аденому, цистит, песок, камни в почках и мочевом пузыре.
У женщин: боли и воспаление яичников. Развиваются фиброма, миома, фиброзно-кистозная мастопатия, воспаление надпочечников, мочевого пузыря и почек. А так же сердечные и раковые заболевания.
Сразу хотим предупредить, что не нужно бежать в аптеку и скупать дорогущие лекарства, которые, по словам фармацевтов, вытравят всех паразитов. Большинство лекарств крайне неэффективны, кроме того они наносят огромный вред организму.
Что же делать? Для начала советуем почитать статью с главного института паразитологии Российской Федерации. В данной статье раскрывается метод, с помощью которого можно почистить свой организм от паразитов без вреда для организма. Читать статью >>>

Лихорадка, озноб и острая анемия – основные симптомы сложного недуга. Опасность малярии заключается не только в неприятных симптомах, но и в затяжном инкубационном периоде, за который микроорганизмы активно делятся по всему организму.
Пневмоцисты через воздух проникают в человеческий организм и приводят к проблемам в работе легких. В сочетании с ВИЧ-инфекцией пневмоцистная пневмония может быть смертельно опасной.
Мышечный саркоцистоз может быть бессимптомным, а кишечный недуг приводит к постоянным вздутиям живота и другим проблемам со стороны ЖКТ.
Болезнь, в тяжелых случаях напрямую угрожающая жизни человека и влечет за собой нарушение нервной системы. Особенно опасен токсоплазмоз при беременности.

Опасные микроорганизмы проникают в кровоток человека при укусе мухи це-це или клопов. Без лечения болезнь приводит к 100% летальному исходу.
Заболевание коварно тем, что больной быстро заражает окружающих.
Инфекционное заболевание, которое является генитальной инфекцией лечится только под наблюдением опытного специалиста, ведь последствия самолечения хламидиоза крайне опасны.
Каждое заболевания, которое вызывают простейшие, несет прямую угрозу здоровью человека и его семье.
Метод, особенно эффективный при выявлении сложных заболеваний – лямблиоз, балантидиаз или саркоцистоз. Для сбора биоматериала используется одноразовый контейнер с герметичной крышкой. Образец доставляется в лабораторию в течение часа, двух, иначе результат будет неточным. Исследование повторяется, спустя две недели, после получения первых результатов и служит подтверждением или опровержением диагноза.
В тех случаях, когда микроорганизмы пребывают в вегетативной форме, пациенту назначаются слабительные препараты. Объем биоматериала должен составлять около 15 грамм, этого количества будет достаточно для дальнейшего исследования.
источник
Комплексное лабораторное обследование для выявления основных гельминтозов и протозойных инфекций человека, включающее общеклинические и специфические тесты.
Анализы для диагностики гельминтозов и протозойных инфекций.
Синонимы английские
Laboratory diagnosis of protozoal and helminthic infections; CBC, Stool Ova and Parasites test, Cellulose tape test, Protozoal and Helminthic Serology.
Какой биоматериал можно использовать для исследования?
Венозную кровь, кал, отпечаток с перианальной области.
Как правильно подготовиться к исследованию?
- Исключить из рациона алкоголь в течение 24 часов до исследования.
- Детям в возрасте до 1 года не принимать пищу в течение 30-40 минут до исследования.
- Детям в возрасте от 1 до 5 лет не принимать пищу в течение 2-3 часов до исследования.
- Не принимать пищу в течение 8 часов до исследования, можно пить чистую негазированную воду.
- Исключить прием слабительных препаратов, введение ректальных свечей, масел, ограничить (по согласованию с врачом) прием медикаментов, влияющих на перистальтику кишечника (белладонна, пилокарпин и др.), и препаратов, влияющих на окраску кала (железо, висмут, сернокислый барий), в течение 72 часов до сбора кала.
- Полностью исключить (по согласованию с врачом) прием лекарственных препаратов в течение 24 часов перед исследованием.
- Исключить физическое и эмоциональное перенапряжение в течение 30 минут до исследования.
- Не курить в течение 30 минут до исследования.
- Сбор биоматериала на исследование проводится только утром (до 10:00), до дефекации. Накануне взятия биоматериала не проводить туалет кожных покровов в области ануса и ягодиц.
Общая информация об исследовании
Гельминтозы и протозойные инфекции наблюдаются повсеместно и особенно распространены среди детей и людей, по роду деятельности контактирующих с домашними и дикими животными. Как правило, инфицирование человека является одним из этапов развития гельминтов или простейших. Многие из паразитов имеют фекально-оральный механизм передачи инфекции и по крайней мере на одном этапе жизненного цикла поражают различные отделы пищеварительного тракта. Несмотря на то что некоторые гельминтозы и паразитозы человека имеют специфические клинические признаки, в целом дифференцировать эти заболевания на основании клинической картины очень сложно. Основную роль в диагностике этих заболеваний играют лабораторные тесты. С учетом того, что у одного и того же человека может наблюдаться сочетание нескольких гельминтозов и паразитозов, рекомендуется выполнение сразу нескольких тестов или, что более удобно для врача и пациента, комплексного анализа на распространенные гельминтозы и паразитозы.
Комплексное лабораторное обследование включает общеклинические и специфические анализы на самые распространенные и важные в клиническом плане гельминтозы и протозойные инфекции. Общеклинические тесты: общий анализ крови, лейкоцитарная формула, анализ кала на яйца гельминтов и анализ кала на цисты простейших.
Общий анализ крови и лейкоцитарная формула используются для того, чтобы определить, является ли гельминтоз или паразитоз инвазивным, и также позволяет выявить возможные осложнения, связанные с инфекцией (анемию). Об инвазивности гельминтозов и паразитозов свидетельствует эозинофилия. Она характерна для амебиаза, эхинококкоза, описторхоза, токсокароза, трихинеллеза и аскаридоза (в фазу миграции личинок). Эозинофилия не характерна для кишечного аскаридоза, энтеробиоза и лямблиоза. Любая длительно текущая инфекция может приводить к развитию анемии (анемии хронического заболевания). Гельминтозы и паразитозы, протекающие с изъязвлением слизистой оболочки пищеварительного тракта (например, амебиаз), приводят к развитию железодефицитной анемии.
Анализ кала на яйца гельминтов и анализ кала на цисты простейших включают макроскопическую оценку кала (цвет, консистенция, наличие крови, избытка слизи, макроскопически определяемых паразитов), микроскопию нативного образца кала (наличие цист простейших – трофозоитов, личинок и взрослых особей гельминтов) и микроскопию окрашенного мазка кала (наличие цист и трофозоитов). Анализ кала на яйца гельминтов позволяет выявить большинство кишечных нематод, цестод и трематод. Анализ кала на цисты простейших позволяет выявить Giardia lamblia, Entamoeba histolytica, Balantidium coli и других простейших. Учитывая, что поступление яиц гельминтов или цист простейших в кал может носить непостоянный характер, однократное исследование кала малоинформативно — рекомендуется исследование трех образцов кала. Следует учитывать, что при некоторых гельминтозах (например, описторхоз) появление яиц в кале начинается только через 2-4 недели после возникновения симптомов заболевания. Отрицательный результат исследований не позволяет полностью исключить наличие гельминтоза или паразитоза.
К специфическим тестам для диагностики гельминтозов и паразитозов относятся серологические тесты и анализ на энтеробоз.
Echinococcus, IgG – определение специфических антител IgG к возбудителю эхинококкоза (Echinococcus granulosus или Echinococcus multilocularis). Чувствительность серологических тестов в отношении E. granulosus при поражении печени (самая частая локализация) составляет около 80 %, при поражении других органов (легкие, головной мозг, кости скелета) – несколько ниже.
Opistorchis, IgG — определение специфических антител IgG к возбудителю описторхоза (Opistorchis felineus или Opistorchis viverrini). Из-за невысокой специфичности серологические тесты являются дополнительным способом диагностики описторхоза (главный тест – анализ кала на яйца гельминта).
Toxocara, IgG, титр — количественное определение специфических антител IgG к возбудителю токсокароза (Тохосаra canis). Серологические тесты обладают достаточно высокой чувствительностью (78 %) и специфичностью (92 %) и могут служить хорошим дополнением или даже альтернативой «золотому стандарту» диагностики данного заболевания — микроскопическому исследованию биопсии ткани, содержащей личинки гельминта (частая локализация – печень и легкие), учитывая, что многие пациенты с токсокарозом — маленькие дети.
Учитывая системный характер таких инфекций, как эхинококкоз, описторхоз и токсокароз, при подозрении на эти заболевания проводят дополнительные обследования, в том числе оценку функции печени.
Trichinella, IgG — определение специфических антител IgG к возбудителю трихинеллеза (Trichinella spiralis и родственные виды). Серологические тесты становятся положительными через 3 недели после инфицирования. Учитывая, что личинки гельминта поражают мышечную ткань, при данном заболевании также могут быть повышены следующие клинико-лабораторные маркеры: креатинкиназа (КК), лактатдегидрогеназа (ЛДГ) и аспартатаминотрансфераза (АСТ).
Ascaris lumbricoides, IgG — определение специфических антител IgG к возбудителю аскаридоза. Аскаридоз – это самый распространенный гельминтоз человека. Серологические тесты являются дополнительным способом диагностики аскаридоза (главный тест – выявление взрослых особей в области рта и ануса, а также анализ кала на яйца гельминта).
Giardia lamblia, антитела — определение специфических антител к возбудителю лямблиоза. Серологические тесты являются дополнительным способом диагностики лямблиоза (главный тест — анализ кала на цисты паразита). Серологический тест становится отрицательным через 1 год после перенесенной инфекции. Также может быть использован тест на антиген G. lamblia в кале.
Энтеробиоз – распространенный гельминтоз, вызываемый Enterobius vermicularis (острица). Яйца остриц не выделяются с калом, поэтому микроскопическое или любые другие исследования кала не применяются. Лабораторная диагностика энтеробиоза осуществляется с помощью специального метода — микроскопического исследования мазков-отпечатков с кожи перианальной области. Микроскопическое исследование позволяет произвести дифференциальную диагностику энтеробиоза с аскаридозом, а также другими неинфекционными заболеваниями, сопровождающимися зудом перианальной области (контактным дерматитом, сахарным диабетом). Учитывая повышенную активность самки в ночные часы, оптимально производить мазок-отпечаток с утра, до совершения утреннего туалета.
Комбинация общеклинических и специфических тестов позволяет достичь наибольшей точности при диагностике гельминтозов и паразитозов. При эффективном лечении изменения, выявленные в общеклинических тестах, нормализуются, а яйца/личинки/взрослые особи гельминтов или цисты простейших перестают определяться, но серологические тесты могут оставаться положительными в течение некоторого времени даже при эффективном лечении.
Для чего используется исследование?
- Для диагностики кишечных гельминтозов и протозойных инфекций.
Когда назначается исследование?
- При обследовании детей и людей из группы риска заражения гельминтами и простейшими (ветеринары, фермеры, работники, занятые в санитарно-гигиентической сфере);
- при наличии признаков глистной инвазии или протозойной инфекции: хронической диареи, мальабсорбции, тошноты, потери веса, а также признаков реакции гиперчувствительности (крапивницы и других сыпей);
- при оформлении ребенка в детский сад, лагерь, бассейн, при госпитализации.
Для каждого показателя, входящего в состав комплекса:
В норме яйца, личинки и взрослые особи гельминтов, цисты и вегетативные формы простейших в кале отсутствуют. Их обнаружение свидетельствует о текущей инфекции.
Серологические тесты могут оставаться положительными в течение некоторого времени даже при эффективном лечении.
Что может влиять на результат?
- Время, прошедшее с момента заражения: яйца гельминтов и цисты простейших могут быть обнаружены через 2-4 недели и позже после заражения.
- Характер и скорость образования яиц гельминтов и цист простейших: часто наблюдается прерывистый характер их поступления в кал, что может привести к получению ложноотрицательного результата и обуславливает необходимость исследования трех, а не одного образца кала.
- Для получения точного результата необходимо следовать рекомендациям по подготовке к тесту;
- результат комплексного анализа следует интерпретировать с учетом анамнестических, клинических и инструментальных данных;
- отрицательный результат исследований не позволяет полностью исключить наличие гельминтоза или паразитоза.
Кто назначает исследование?
Врач общей практики, педиатр, инфекционист.
источник
Из-за постоянно возрастающей заболеваемости паразитарными инфекциями, люди все чаще сдают анализ кала на кишечные протозоозы. Простейшие микроорганизмы, попав в организм человека, могут стать причиной серьезных заболеваний. Они не только способствуют образованию воспалительных процессов и питаются за счет носителя, но и способны поражать внутренние органы, вплоть до летального исхода. Именно поэтому следует проверять себя на наличие кишечных паразитов с помощью лабораторных анализов.
Каждая протозойная инфекция обладает собственной симптоматикой, поэтому определить ее наличие бывает довольно сложно. Однако имеется общий список проявлений, которые могут стать поводом для проведения анализа кала:
- понос более 20 раз в сутки, нередко с присутствием слизи и крови в каловых массах;
- обезвоживание организма;
- болевой синдром в брюшной области;
- вздутие живота;
- тошнота и рвота;
- желтушность белков глаз и кожи;
- общее недомогание, упадок сил;
- резкое снижение веса;
- лихорадка.
Помимо общепринятых симптомов, человека могут беспокоить проявления, характерные для борьбы с интоксикацией организма:
- повышение температурных показателей;
- нарушение координации движений;
- боли в мышцах, суставах, сердце;
- непрекращающийся кашель;
- рассеянность, потеря концентрации внимания.
Не стоит заниматься самолечением. Отсутствие качественной диагностики и своевременной терапии способно привести к серьезным последствиям, вплоть до смерти пациента. Незамедлительное обращение к врачу необходимо сразу после обнаружения нарушений в работе организма.
Сепсисы и внутренние кровотечения, а также тромбы возможны в случае тяжелого течения заболевания. При обнаружении первичных симптомов помощь медиков требуется незамедлительно.
Для получения наиболее достоверных результатов нужно правильно собрать материал, и выполнить ряд несложных условий. Особенно готовиться к анализу не нужно, необходимо соблюсти ряд простых правил, которые позволят получить полную картину заболевания:
- за 9 часов до дефекации нужно отказаться от еды и питья, или резко ограничить потребление жидкости;
- за пару дней до исследования отменить применяемые слабительные средства и очистительные клизмы;
- за неделю до анализа исключить прием антибиотиков и других лекарственных средств;
- кал следует помещать в простерилизованную тару, соблюдая рекомендации представителей лаборатории.
Подойдут стеклянные банки от детского пюре или похожая тара из стекла и пластика. Для создания стерильной среды банку нужно максимально тщательно промыть проточной водой и обдать кипятком. Но лучше всего купить специальный контейнер для анализа в аптеке. Он очень удобен еще и тем, что к крышке прикреплена специальная лопатка.
Перед сбором материала следует помочиться, так как попавшая в тару жидкость может существенно исказить полученные при исследовании результаты. Затем проводят сбор кала на анализ. Всего необходимо около столовой ложки массы. Ее забирают из разных мест (снаружи и внутри). После помещения биомассы в контейнер, его плотно закрывают, наклеивают на него листок с личными данными пациента, а также датой и временем сбора кала. Емкость необходимо незамедлительно доставить в лабораторию.
Годность материала при отрицательных температурах, например при помещении контейнера в холодильник, составляет 10-12 часов. Температура должна варьироваться в пределах +4 – +8 градусов. Но для получения наиболее достоверного результата и обнаружения живой патогенной микрофлоры в фекалиях пациента, следует доставить баночку не позднее, чем за 1 час после сбора кала. В идеале время доставки не должно превышать 30-40 минут с момента дефекации и сбора биоматериала.
Однократно проведенный анализ на кишечные протозоозы может не показать наличие возбудителей заболевания. Для постановки верного диагноза сдавать материал нужно трижды, с интервалом в пару дней. Только при отрицательном результате сразу нескольких анализов можно говорить об отсутствии инфекции и безопасности для окружающих. В противном случае лечащий врач должен назначить качественное и быстрое лечение. Человек обрекает себя на серьезные осложнения, и даже смерть, затягивая с терапией заболевания.
| Наименование | Грудные дети | Взрослые пациенты и дети старше 1 года |
| Бифидобактерии | 1*10⁹ и более | 1*10⁸ и более |
| Лактобактерии | 1*10⁷ | 1*10⁶ |
| Патогенная микрофлора | Отсутствует | Отсутствует |
| Кишечная палочка | 1-7*10⁸ | 3-4*10⁸ |
| Энтеробактер лактозоотрицательные | Не превышает 5% | Не превышает 5% |
| Кокки в соотношении от общего количества микрофлоры | Не превышает 25% | Не превышает 25% |
Это показатели, которые указывают на нормальное состояние пациента. Если результаты копрограммы соответствуют нормативам, человек считается здоровым. Для уточнения диагноза анализ проводят повторно через некоторое время.
В зависимости от выявленной патогенной микрофлоры в каловых массах делают вывод об имеющемся заболевании. Изучен ряд инфекционных патологий, которые спровоцированы вредоносными микробами. •
Этот диагноз ставится пациенту в том случае, когда по результатам анализа в кале обнаружены амебы. Заболевание легко передается от человека к человеку, если правила гигиены часто не исполняются. Возбудитель попадает в ЖКТ человека и паразитирует там. Заболеванию чаще, чем женщины, подвержены представители сильной половины человечества в возрасте от 20 до 40 лет.
Проникая в отдаленные отделы кишечника, амеба изъязвляет слизистые. С кровотоком она также способна проникать в головной мозг, легкие, печень и другие внутренние органы. Это приводит к серьезным нарушениям работы организма.
Лямблии занимают дистальные отделы тонкого кишечника, питаясь и паразитируя там. Передается при несоблюдении элементарной гигиены или от животного к человеку.
Колонизация возбудителей происходит в тонком и толстом кишечнике. Проникая в орган, изъязвляет слизистые. Передается обычно при нарушении правил гигиены или от инфицированного животного. Распространено среди работников фермерских хозяйств.
Заражение происходит аналогично лямблиозу и амебиазу при нарушении правил чистоты, а также от инфицированных животных и людей. Вредоносные микроорганизмы локализуются в дистальных отделах толстого кишечника. Нередко обнаруживается у здоровых людей. Симптоматика может полностью отсутствовать.
Срок латентного периода заболевания составляет около двух недель. Возбудитель, в ряде случаев, расселяется в тонком кишечнике. Поражая слизистые и питаясь хозяином, активно размножается. Способ заражения – фекально-оральный.
При подозрении на кишечную инфекцию анализ кала нужно обязательно включать в процедуры общего обследования пациента. При этом отсутствие возбудителей в каловых массах по результатам первого анализа, не означает, что патогенная флора полностью отсутствует. Возможно цисты не попали именно в эту порцию биоматериала.
Для подтверждения диагноза и установления точной клинической картины следует сдать анализ еще пару раз, с интервалом в несколько дней. Оценивать результаты должен лечащий врач. При выявлении вредоносных микробов, доктор способен назначить качественное и своевременное лечение. Не стоит заниматься самолечением и применять народные способы борьбы с возбудителями заболеваний. Это может быть смертельно опасно.
источник
В наше время проблема наличия у человека кишечных проблем, вызываемых наличием там посторонних живых организмов, значительно обострилась. Специалистами выделяется 2 основные группы паразитарных заболеваний, поражающих людей – это гельминтозы и протозоозы.
К первой относятся многочисленные виды глистов, поражающих людей, а ко второй простейшие. Несмотря на то, что попавшие в организм представители этих групп существенно различаются в размерах, они одинаково опасны и могут вызвать у заражённого пациента большое количество серьёзных патологий.
Гельминтозы и кишечные протозоозы, несущие серьёзные проблемы здоровью, а иногда даже способствующие развитию патологий, заканчивающихся смертью пациента, необходимо выявлять своевременно и проводить необходимые специфические мероприятия по уничтожению их возбудителей. Для этого не только выполняется лабораторная диагностика кала, мочи, крови и мокрот, но и полное обследование пациента. Только это позволит избавить пациента от проблем, вызываемых этими простейшими микроорганизмами и низшими червями.
Для выявления возбудителей инфицирования организма пациента и связанных с этим болезней применяются следующие лабораторные методы обследования:
- Прямые паразитологические методы. Для их проведения используется непосредственное исследование соответствующего развивающейся патологии биоматериала (анализы крови, мочи, кала и содержимого язв);
- Непрямые, к которым относятся серологические (иммунологические) исследования крови. Этот анализ основан на выявлении протозоозов и гельминтозов по наличию в ней антител к антигенам глистов и простейших. Этот вид диагностики обладает высокой степенью чувствительности и удобен для массового применения.
В клинической практике иммунологические лабораторные исследования проводятся как дополняющие к комплексу клинико-инструментальной диагностики, выполняемой для дифференциального выделения гельминтозов и протозоозов от патологий со сходной симптоматической картиной. Лабораторный диагноз кишечных протозойных инфекций ставится после обнаружения в анализах соскобов со слизистой кишки, свежего, ещё тёплого кала или содержимом язв и абсцессов вегетативных форм простейших, подтверждающих наличие у пациента протозоозов. Для точности обнаружения глистной инвазии одной лабораторной диагностики исследования крови и кала бывает недостаточно. Человеку, у которого подозревается наличие этой напасти, могут быть назначены такие обследования, как рентгеноскопия, с помощью которой можно обнаружить эхинококкоз или цистицеркоз, и КТ или УЗИ при некоторых других видах гельминтозов.
Реабилитация при протозойных болезнях и гельминтозах требуется в обязательном порядке всем людям, проходящим лечение от этих патологий. Это связано с тем, что применяемые в терапевтических целях лекарственные средства обладают высокой токсичностью и не только нарушают микрофлору пищеварительных органов, но и отравляют организм, вызывая развитие тяжёлых кишечных патологий. Все реабилитационные мероприятия, необходимые при гельминтозах и протозоозах, должны назначаться только специалистом и проводиться под его контролем. В число реабилитационных мероприятий, рекомендуемых лечащим врачом для восстановления организмов взрослого или ребёнка от таких патологий, как протозоозы и гельминтозы обычно включается следующее:
- Назначение препаратов фолиевой кислоты, железа и витамина В12;
- Безуглеводная диета (исключается мучное, сладости);
- Применение ферментных препаратов, улучшающих пищеварение;
- Витаминотерапия.
Люди часто интересуются тем, какие глисты и другие паразиты могут жить в организме.
При выявлении паразитов каждый человек самостоятельно решает, чем проводить терапию. Несомненно, эффективное средство.
Существует ошибочное мнение, что паразиты появляются только у нечистоплотных людей, которые не соблюдают.
Анти Токсин Нано – неумолимо уничтожает все виды паразитов в человеческом организме и вычищает продукты их жизнедеятельности.
Bactefree – это уникальная и эффективная комбинация растительных экстрактов, которая оказывает убийственное действие на жизнедеятельность паразитов.
Уничтожает всех паразитов за 1 курс! Оздоравливает, создает защитный барьер, выводит токсины и продукты распада!
Очищает от паразитов за 1 курс благодаря дубильным веществам. Оздоравливает и защищает от паразитов печень, сердце, легкие, желудок, обезвреживает яйца паразитов благодаря медвежьей желчи.
Многие люди пренебрегают опасностью, которую вызывают паразиты, живущие в организме человека. Глисты не только едят нашу пищу, но и питаются нашими клетками.
ВНИМАНИЕ! ИНФОРМАЦИЯ, ОПУБЛИКОВАННАЯ НА САЙТЕ, НОСИТ ИСКЛЮЧИТЕЛЬНО ОЗНАКОМИТЕЛЬНЫЙ ХАРАКТЕР И НЕ ЯВЛЯЕТСЯ РЕКОМЕНДАЦИЕЙ К ПРИМЕНЕНИЮ. ОБЯЗАТЕЛЬНО
ПРОКОНСУЛЬТИРУЙТЕСЬ С ВАШИМ ЛЕЧАЩИМ ВРАЧОМ!
Оставьте комментарий 2,139
С каждым годом растет количество больных, инфицированных различными паразитами. Исследования на гельминтозы и протозоозы — наиболее часто встречаемые у зараженных людей. Протозоозы — одноклеточные паразиты, активно размножающиеся в человеческом организме, приводя к нарушениям функциональности многих органов и систем. Последствия этих сбоев могут носить необратимый характер и способны привести к серьезным последствиям.
Возбудители гельминтозов и протозоозов располагаются чаще у представителей животного мира, но по ряду следующих причин они переходят к человеку:
- употребление в пищу немытых продуктов;
- использование для питья загрязненной воды;
- незащищенный половой акт с незнакомым партнером;
- укус членистоногого.
Основными путями заражения врачи называют:
- Фекально-оральный. Протозоозы покидают организм больного с испражнениями, из которых проникают в почву, воду, растения, а далее проникают через ротовую полость к новому носителю, употребившего данные продукты.
- Контактный. Посредством непосредственного контакта зараженного и здорового человека.
Хорошая иммунная система способна влиять на процесс деления протозоозы.
Кишечные протозоозы после проникновения в организм начинают активно делиться.Если индивид имеет хорошую иммунную систему, то это является гарантией замедления процесса размножения. Вероятность заражения велика для представителей всех возрастных категорий, пола и национальностей. Но к первоочередной группе риска заражения можно отнести:
- детей;
- лица со сниженным иммунитетом.
В медицине есть описание множества видов протозоозов, каждый из которых имеет особенности. Предлагается 2 основных классификационных делений протозоозов:
- Разделение на 4 видовые классы:
- сардоковые;
- споровики;
- жгутиковые;
- инфузории.
- Разновидности по месту паразитирования простейших:
- тонкокишечные;
- толстокишечные;
- полостные;
- легочные;
- из ротовой полости.
Наиболее изученные протозойные инфекции — это:
Инфекции, вызваны укусом малярийного комара могут привести к летальному исходу.
- Амебиаз (вызывается амебами), которому подвержены жители стран с жаркими климатическими условиями, а их переносчиками являются тараканы и мухи.
- Лейшманиоз, заражение которым происходит посредством укуса москитов, а возбудителей в этой группе имеется более 20-ти.
- Малярия, возникающая через укус комара или других инфицированных насекомых, протекает тяжело и является неизлечимым заболеванием.
- Лямблиоз, возбудители которого попадают в организм вместе с продуктами и водой, а также посредством контактирования с другими, поражает тонкую кишку и реже желчный пузырь.
- Балантидиаз, когда паразиты попадают в человеческий организм с мясом зараженных животных (чаще свиней), приводят к развитию перфорации кишечника и перитонита.
Симптомы и их выраженность зависят напрямую от места локализации паразитов. Наиболее распространенными признаками, по которым можно говорить о том, что пациент имеет протозойные инфекции, считаются:
- общая слабость;
- головные боли;
- понос;
- лихорадка;
- мышечная боль;
- желтуха;
- ломота в суставах;
- болевые ощущения в подреберье с правой стороны и районе сердца;
- неестественные выделения из половых органов.
При первых признаках, указывающих на паразитарные заболевания, следует немедленно обратиться в медицинское учреждение для полной диагностики. Первоочередной задачей диагностики является определение места локализации и типа патогенного агента. Продолжительность обследования составляет в среднем до 1,5 дней. Получив все результаты, доктор может переходить к терапевтической стадии.
Обследование организма на наличие кишечных протозоозов начинается с осмотра пациента, сбора его анамнеза. Дальнейшая диагностика включает в себя в основном лабораторные методы, основными из которых считаются:
- общий анализ крови;
- пробы крови для микробиологической диагностики;
- биопсия;
- биохимия крови;
- анализ кала (его микроскопия);
- рекомендуется сдавать кровь и прочие физиологические жидкости по методу толстой капли.
В зависимости от состояния иммунитета человека и его способности бороться с патогенными агентами врачи различают 3 типа протекания болезни:
- легкий — лечится амбулаторно и проходит без особых осложнений;
- тяжелый — требует незамедлительной госпитализации;
- хронический — рецидивы лечатся исключительно с госпитализацией, а всю жизнь требует контроль общего состояния организма.
Протозойные инвазии лечатся только под наблюдением врача.
Медикаментозное лечение для каждого пациента подбирается индивидуально в соответствии с типом протозоозы и состоянием организма, поэтому назначение лекарств носит специфический характер. Но существуют следующие общепринятые принципы:
- противопаразитарные медикаменты, влияющие на самого возбудителя заболевания (например, «Метронидазол»);
- растворы внутривенно через капельницу при интоксикации (например, физраствор, глюкоза);
- противовоспалительные препараты для устранения высокой температуры тела (анальгин, «Ибупрофен»);
- средства от кашля для отхаркивания («АЦЦ», «Лазолван»);
- в случаях присоединения вторичной бактериальной инфекции назначаются антибиотики.
Во время всего курса лечения за состоянием пациента ведется строгое наблюдение. Если протозойные инвазии после приема назначенных препаратов не угасают, то оперативно корректируется план лечения. Тогда главное — не упустить время, иначе возможно развитие таких осложнений, как:
- обезвоживание;
- частая потеря сознания;
- реже внутренние кровотечения;
- сепсис или абсцесс;
- наступление комы;
- в крайних случаях — летальный исход.
Профилактика протозойных болезней включает в себя соблюдение правил личной гигиены, отказ от случайных половых контактов, использование средств защиты от насекомых для индивидуального пользования и употребление только тщательно вымытых продуктов, очищенной воды. Для тех, кто собирается выезжать в места широкой распространенности подобных инфекций, рекомендуется применить дополнительные средства защиты и профилактики (например, прививки).
Копирование материалов сайта возможно без предварительного согласования в случае установки активной индексируемой ссылки на наш сайт.
Внимание! Информация, опубликованная на сайте, носит исключительно ознакомительный характер и не является рекомендацией к применению. Обязательно проконсультируйтесь с вашим лечащим врачом!
Протозойные болезни крайне распространены на всей планете. Это заболевания паразитарной этиологии и практически каждый человек является окончательным хозяином того или иного вида простейших паразитов.
Микроорганизмы могут быть патогенными изначально, а могут активироваться под воздействием внешних и внутренних факторов.
Все паразитарные заболевания делятся на:
Протозоозы (протозоонозы) – это группа болезней, возбудителями которых являются одноклеточные микроорганизмы, которые паразитируют в тканях и органах человеческого организма, разрушая его, с целью поддержания собственной жизнедеятельности.
Передаются такие болезни половым или бытовыми путями (через общие предметы личной гигиены, пищу, воду, грязные руки).
Течение болезни, принципы проявления и возможный урон здоровью варьируется в каждом конкретном случае, однако все эти виды инвазии требуют своевременного медикаментозного лечения.
Гардиаз – кишечный протозооз, поражающий слизистые оболочки тонкого кишечника и желчный пузырь, отличительной особенностью которого является развитие неврологических симптомов. Болезнь распространена в Азии, Африке, Южной Америке.
Возбудителем являются лямблии – жгутиковые одноклеточные паразиты. Они передаются человеку бытовым путем (через грязную воду, овощи и фрукты, не подвергнутые термической обработке). Имеют способность к цистообразованию (покрытию защитными оболочками при агрессивных условиях внешней среды), двигательные органоиды представлены 4-мя парами жгутиков.
Питание производится через всю поверхность тела, размножение – продольным делением. Жизненный цикл начинается с попадания в человеческий организм лямблиозных цист. По достижению тонкого кишечника из каждой цисты образуется 2 паразита.
Лямблиоз бывает острым и хроническим. Острая форма длится неделю, потом болезнь переходит в хроническую стадию. Болезнь не имеет специфических симптомов, что значительно затрудняет её диагностику.
Клиническая картина хронической стадии довольно размыта, характеризуется дисбактериозом, диспепсией, неврологическими проявлениями (раздраженность, эмоциональная нестабильность, выраженная бледность, мраморность носа).
Отсутствие лечение приводит к серьезной травматизации слизистой оболочки тонкого кишечника, атрофии функции всасывающих клеток, анорексии.
Большое количество токсичных продуктов жизнедеятельности лямблий пагубно влияет на работу ЦНС (центральной нервной системы).
Болотная лихорадка – острый протозонооз, возбудителями которого являются плазмодии. Переносчик плазмодий – комары из рода анофелес. Самое широкое распространение болезнь получила в Африке, 90% всех заболевших – африканцы.
Выделяют 4 виды малярии, которые вызываются 4-мя разными видами плазмодий, однако самой распространенной и опасной является тропическая малярия (возбудитель – плазмодий falciparum).
Специфическая особенность – сезонность, что обусловлено наличием благоприятных условия внешней среды для развития патогенных клеток, а также для жизни основного переносчика – комара анофелес (температура воздуха от 16°С до 30°С, наличие открытых водоемов).
Заражение происходит через укус насекомого, а также может быть вертикальным (межплацентарный переход при беременности от матери к плоду) или при обмене лимфатической жидкостью (во время родов, при выполнении инъекций одним шприцом, при переливании крови).
Течение заболеваний скачкообразное, хроническо-рецидивирующее, характеризуется чередование периодов острых проявлений и сна.
Приступы характеризуются следующими симптомами:
При своевременном лечении возможно полное выздоровление, однако такие осложнения как отек мозга могут спровоцировать летальный исход.
Токсоплазмозом инфицировано более 70% населения Земли. Эта форма паразитарной инвазии практически всегда протекает бессимптомно и без направленной лабораторной диагностики его выявить нельзя.
Человеческий организм является промежуточным носителем. Наличие ВИЧ усугубляет течение болезни и приводит к развитию энцефалита. Люди заражаются от кошек, либо при контакте с сырым мясом.
Заражение токсоплазмами в период вынашивания ребенка грозит передачей паразитов плоду, что провоцирует задержку внутриутробного развития, самопроизвольное прерывание беременности и т.д.
Человек не является источником распространения возбудителей инфекции. Общая симптоматика не выражена, клиническая картина скрыта.
Амебы – одноклеточные микроорганизмы, способные менять форму тела, отдельные виды которых могут быть патогенными. К их числу относится дизентерийная амеба. Амебиаз может приобретать кишечную и внекишечную формы.
Переносчиками инфекции являются мухи и тараканы, заражение происходит фекально-оральным путем, через грязные руки, употребление немытых овощей и фруктов, водопроводной воды. Острая форма дизентерийного амебиаза сопровождается:
При длительном течении болезни наблюдается истощение организма. Внекишечные формы заболевания предполагают локализацию очага размножения амеб в печени или других тканях организма, что приводит к образованию множественных абсцессов и летальному исходу при отсутствии должного лечения.
Транмиссивное заболевание, переносчиками которого являются различные виды москитов. Возбудитель – лейшмания – жгутиковое простейшее, имеющее 2 формы существования: безжгутиковую у человека и жгутиковую у москита.
В зависимости от того, какой именно формой лейшмании был заражен человек, выделяют антропозную и зоонозную формы лейшманиоза. Они различаются по интенсивности выраженности симптомов и скорости течения.
Лейшманиозы поражают кожные покровы, слизистые оболочки и некоторые внутренние органы человека (селезенка), вызывая их патологическое увеличение.
Россия не является эндемичной территорией для лейшманиоза, однако имеют место диагностированные случаи инвазии при заражении людей в туристических и деловых поездках в страны Азии и Африки. Является препятствием для экономического развития некоторых стран Африки.
К основным симптомам относят неспецифичные проявления:
Кроме того, кожная и кожно-слизистая формы предполагают образование язв на месте укуса насекомого.
Источниками болезни являются цисты балантидий, которые формируются и развиваются у свиней. В связи с тем, что промежуточным хозяином является домашняя свинья, часто инфицированию подвергаются жители сельской местности, работники ферм, животноводческих предприятий.
Инвазия происходит фекально-оральным путем.
Диагностика крайне затруднена, что обусловлено полным совпадением балантидиаза с энтероколитом по его проявлениям:
- диарея с кровяными и слизистыми включениями;
- боли в абдоминальной области;
- крайнее истощение организма;
- рвота;
- слабость;
- сухость во рту;
- мигрени.
Это кишечная форма болезни приводит к травматизации и иъязвлению стенок тонкого кишечника, а впоследствии и перитонита при отсутствии своевременного лечения. Инкубационная стадия длится 2-4 недели.
Возбудителем этой паразитарной инфекции являются пневмоцисты. Заражение происходит воздушно-капельным путем, поэтому профилактика заболевания затруднена.
Вспышки заболевания, в большинстве случаев, ограничиваются детскими домами, отделениями для новорожденных или детскими отделениями. Носителями пневмоцист могут быть человек и домашние животные. Болезнь смертельно опасна в сочетании с иммунодефицитами (ВИЧ), особенно при отсутствии лечения.
Есть определенные сложности в первичной диагностике по причине протекания заболевания в форме хронической пневмонии. Возбудитель поражает бронхи и альвеолы.
- приступообразный кашель;
- одышка;
- потемнение носогубного треугольника (у новорожденных);
- устойчивая температура тела 37°С-38°С.
Летальный исход наступает в 10% случаев, при повторном заражении – в 40%. Лечение пневмоцистоза у ВИЧ-положительных проводится посредством химиотерапии.
Человек может являться и промежуточным и окончательным хозяином саркоцист. Возбудители заболевания передаются человеку от свиней и крупного рогатого скота (коров), инвазия происходит путем употребления в пищу говядины или свинины инвазированных животных при недостаточной термической обработке.
Саркоцистоз может быть кишечным или мышечным. Кишечная форма сопровождается тошнотой, вздутием живота и жидким стулом, мышечная – протекает скрыто, сопровождается незначительной эозинофилией.
Трансмиссивное заболевание, переносчиками которого является муха Цеце и триатомовый клоп. В зависимости от эндемичного района и промежуточного хозяина выделяют американский трипаносомоз (болезнь Шагаса) и африканский (сонная болезнь).
Кроме трансмиссивного способа передачи паразитов существует вероятность вертикального и трансплацентарного способов.
Американский трипаносомоз ведет к поражению ЦНС и параличу, а африканский – к отеку головного мозга или энцефалиту мозговых оболочек. Симптомы либо не выражены, либо характеризуются повышенной температурой тела, увеличением лимфатических узлов, болями в области сердца, лихорадкой.
Лечение может иметь эффект в незначительных количествах случаев при обнаружении заболевания на начальной стадии, на последующих этапах лечение сводится к облегчению симптомов.
Трихомонады обитают в человеческом организме, не вызывая патологий. Однако существуют условно-патогенные виды трихомонад. К ним относят влагалищная и кишечная трихомонады.
Трихомоноз – человеческая болезнь, заражение происходит половым путем.
Основные симптомы трихомоноза:
- обильные выделения;
- зуд наружных половых органов и внутренней поверхности бедер;
- жжение;
- болезненность при половых актах;
- неприятный запах выделений.
У мужчин болезнь протекает бессимптомно.
Очень опасно при вынашивании плода, может вызывать серьезные осложнения в течении беременности и быть причиной патологий плода. Является распространенной причиной бесплодия.
Хламидии передаются от человека к человеку через половые контакты, а также с грязных рук на слизистые оболочки. Возможна передача паразитарной инфекции в процессе естественных родов. Хламидии могут впадать в состояние анабиоза, что помогает им не идентифицироваться иммунной системой.
Хламидиоз характеризуется обильными гнойными выделениями и у мужчин и у женщин, зудом, жжение, болями при мочеиспускании.
Разнообразие форм протозойных болезней обуславливает тот факт, что их диагностикой и лечение занимаются разные врачи или группы врачей. Все протозоонозы делятся на группы (кишечные, половые ит.д.) и в зависимости от преобладающих симптомов определяется раздел медицины, изучающий конкретные болезни.
Изначально лечащим врачом становится терапевт или гинеколог (уролог, венеролог), дальнейшее лечение назначается им же, однако для дополнительных исследований и анализов могут привлекаться другие специалисты.
Что такое анализ на протозоозы пациента консультирует лечащий врач, он же дает направления на дополнительные процедуры по выявлению инородных микроорганизмов в теле человека.
Показаниями к сдаче такого анализа становится субъективное мнение врача, основанном на подробном анамнезе и ручном осмотре пациента.
Любой человек должен периодически сдавать любые анализы для контроля собственного здоровья, даже если к этому нет никаких показаний.
Для постановки верного диагноза специалисту необходимы данные ряда исследований. Клиническая картина многих болезней не всегда ярко выражена, бывают случаи бессимптомного течения заболеваний.
Чтобы восполнить недостающую информацию и скорректировать лечение в каждом конкретном случае врач может использовать методы общей диагностики, а может назначить специфические исследования для обнаружения определенного вида паразита или группы паразитов.
К общим методам исследований относят:
- сбор анамнеза;
- ручной визуальный осмотр;
- УЗИ;
- рентген;
- ОАК и БАК (общий и биохимический анализы крови);
- ФГС;
- развернутые исследования пунктатов;
- биопсия пораженных органов;
- гомоскопия мазков крови;
- исследование отпечатков пораженных органов;
- гистологические срезы;
- соскобы кожи и слизистых;
- биопробы;
- мазки мочевыводящих путей.
Актуально при лямблиозе, амебиазе, балантидиазе, саркоцистозе.
Биоматериал для достоверного результата анализа должен быть собран в чистую емкость и доставлен в лабораторию в течениеминут. Исследование проводится троекратно с периодичностью вдней. Таким способом можно обнаружить цисты паразитов. В некоторых случая рекомендуется прием слабительного для выявления вегетативных форм микроорганизмов.
Для проведения анализа достаточнограмм биоматериала.
В случае подозрения на протозоозную инфекцию назначается анализ на наличие антител М и G. Положительный анализ IgМ иллюстрирует наличие инфицирования и течения острого воспалительного процесса. Положительный результат на IgG говорит о хронической форме.
Биоматериалом является венозная кровь, забираемая натощак. Результаты готовятся в течение нескольких дней.
На основании наличия и количества антител можно сделать вывод о том, имеет ли место инвазия:
- Титр 1/200-1/400 говорит о ранее перенесенном заболевании и выработанном иммунитете.
- Титр 1/100 говорит о том, что не было ранее перенесенных инвазий.
- Титр 1/600 и более иллюстрирует острую форму течения заболевания.
Предполагает исследование крови или влагалищных (уретральных) соскобов, окрашенных специальными веществами. Одноклеточные паразиты вступают в реакцию с клетками окрашивающего материала и подсвечиваются.
Этот метод не дает 100% точного результата, поэтому используется в совокупности с другими методами.
Реакция связывания комплементов. Предполагает введение в образец биоматериала коровьего кардиолипина. Клетки, содержащиеся в реагенте, и одноклеточные вступают в реакцию. Интенсивность реакции указывает на тяжесть формы заболевания.
Из-за высокой стоимости этот метод используется редко, однако он обладает высокой чувствительностью, что обуславливает его точность. Исследованию подвергается генетический материал пациента. Суть метода состоит в том, чтобы с помощью специальных ферментов искусственно увеличить объем материала, а, соответственно, и патогенной среды, что позволит более детально рассмотреть её в микроскоп и дать точные количественные и качественные данные.
Вышеописанные анализы делаются на основании полученного генетического материала (крови, соскобов со слизистых). В расшифровке указываются значения нормы и полученные данные для сравнения. Подготовка результатов занимает несколько дней, однако в коммерческих клиниках возможна услуга получения срочного результата за отдельную плату.
Все виды биоматериала берутся в утреннее время, натощак. Предполагается, что задней до сдачи анализа, пациент прекращает прием любых медикаментозных средств. За 2 дня до проведения исследования и в день исследования нежелательно курение. Накануне перед сдачей анализов не рекомендуется употребление соленой, острой и копченой пищи, а также алкоголя.
Важно помнить, что ни один из вышеперечисленных методов исследований не может быть использован единично. Для получения достоверных результатов, необходимых для коррекции лечения, важно использовать одновременно несколько различных методов обнаружения инородных микроорганизмов в теле человека.
В некоторых случаях предупреждение протозойной инвазии невозможно.
В случаях с малярией или трипаносомозом человек не способен предусмотреть возможные контакты с насекомыми-переносчиками, однако не рекомендуется пренебрежение косвенными мерами предосторожности:
- отказ от поездок в эндемичные районы;
- в случае совершения поездки использовать отпугивающие насекомых средства, носить закрытую одежду, не посещать места возможного скопления насекомых.
В остальных случаях к мерам профилактики можно отнести:
- отказ от беспорядочных половых контактов;
- минимизация контактов с домашними и сельскохозяйственными животными;
- следование правилам личной гигиены;
- подвергание продуктов питания термической обработке.
Одноклеточные паразиты могут стать причиной заболеваний, приводящих к летальному исходу. Об этом необходимо помнить, когда меры профилактики заболеваний кажутся неэффективными.
При возникновении любых проявлений нарушений в организме, необходимо незамедлительно обратиться к лечащему врачу.
Специалистами рекомендуется сдавать анализы на все виды протозоозов не реже, чем 1 раз в полгода для предупреждения развития тяжелых стадий болезней, которые протекают бессимптомно.
то такое анализ на протозоозы? Одноклеточные организмы, способствующие развитию этих опасных недугов, выявляются только с помощью специальных анализов. Простые микроорганизмы являются возбудителями инфекционных заболеваний, и паразитируют в тканях или внутренних органах человека. Общее название для подобных заболеваний – протозоозы или протозойные инфекции.
Попадая в организм человека, простейшие могут носить патогенный характер и активизироваться от негативных факторов окружающей среды. Заражение опасными микроорганизмами происходит бытовым или половым путем, и избежать негативных изменений в организме чрезвычайно трудно.
Лямблиоз, малярия, хламидиоз и прочие распространенные недуги имеют схожую природу – возбудителя, способного поразить человека в самый неподходящий момент. Все виды инвазии, относящиеся к следствиям размножения простейших, требуют срочного медикаментозного лечения.
Угрозы из-за активного размножения простейших подстерегают каждого, кто вовремя не распознал патогенные процессы в собственном организме. В каждом отдельном случае микроорганизмы способствуют развитию сложных заболеваний с последствиями для человека:
Недуг, который передается через пищу и переносится с помощью насекомых, чаще поражает кишечник, но в иногда могут поражаться и другие органы.
Заболевание, которым можно заразиться через пищу (в основном через мясные продукты). Последствия заражения балантидиями – перфорация кишечника и развитие перитонита. Должная гигиена тела, особенно рук, и обработка мясных продуктов, которое употребляет в ежедневном рационе человек, предотвратят развитие балантидиаза.
Болезнь, переносчиком которой являются насекомые (москиты), способствует развитию анемии и лихорадки. Опасный недуг приводит к увеличению внутренних органов, что влечет за собой нарушения в их работе.
Опасные цисты проникают в организм через пищу, фрукты или овощи. Немытые руки, грязная посуда – мелочи, которые способствуют заражению лямблиозом. Заболевание такого рода сопровождается болью в животе и правом подреберье, тошнотой и интоксикацией.
Лихорадка, озноб и острая анемия – основные симптомы сложного недуга. Опасность малярии заключается не только в неприятных симптомах, но и в затяжном инкубационном периоде, за который микроорганизмы активно делятся по всему организму.
Пневмоцисты через воздух проникают в человеческий организм и приводят к проблемам в работе легких. В сочетании с ВИЧ-инфекцией пневмоцистная пневмония может быть смертельно опасной.
Мышечный саркоцистоз может быть бессимптомным, а кишечный недуг приводит к постоянным вздутиям живота и другим проблемам со стороны ЖКТ.
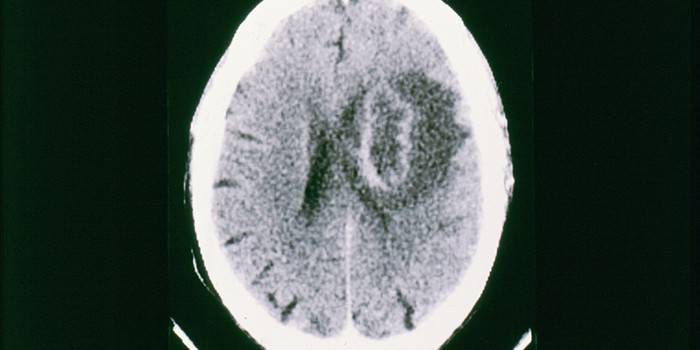
Болезнь, в тяжелых случаях напрямую угрожающая жизни человека и влечет за собой нарушение нервной системы. Особенно опасен токсоплазмоз при беременности.
Источники инфицирования человека токсоплазмой
Опасные микроорганизмы проникают в кровоток человека при укусе мухи це-це или клопов. Без лечения болезнь приводит к 100% летальному исходу.
Заболевание коварно тем, что больной быстро заражает окружающих.
Инфекционное заболевание, которое является генитальной инфекцией лечится только под наблюдением опытного специалиста, ведь последствия самолечения хламидиоза крайне опасны.
Каждое заболевания, которое вызывают простейшие, несет прямую угрозу здоровью человека и его семье.
Простейшие паразитируют во всем организме человека и нарушают обменные процессы в кишечнике и желудочно-кишечном тракте. Всего в природе существует свыше 50 видов опасных, патогенных микроорганизмов, способствующих развитию сложных недугов. Общее название для подобных заболеваний – протозойные инфекции.
После попадания в организм микроорганизмы начинают активно размножаться. Предотвратить этот процесс способен только крепкий иммунитет. В зоне риска возникновения тяжелых недугов оказываются дети или взрослые, перенесшие ранее сложные заболевания. Анализа на протозоозы назначаются лечащим врачом для определения точного диагноза.
Анализ на протозоозы что это? Это, в первую очередь анализ на выявление простейших, а также надежный способ установить степень запущенности заболевания и определить точный возбудитель инфекционного недуга. Каждый клинический случай – уникален, и требует тщательного рассмотрения. Кишечные протозоозы проявляются неприятной симптоматикой, а вот те, при которых микроорганизмы, которые поражают печень, не беспокоят человека долгое время. Для этих видов возбудителей опасных заболеваний существуют отдельные анализы, входящие в комплексное обследование организма.
Диагностика каждого инфекционного недуга включает общие и специальные анализы.
Дополнительные исследования, которые помогут выявить точный тип микроорганизмов в организме человека:
- общий и биохимический анализы крови;
- биопробы;
- анализ кала;
- иммуноферментный анализ;
- реакция Вассермана.
На основе полученных результатов опытный специалист воссоздает картину заболевания.
Метод, особенно эффективный при выявлении сложных заболеваний – лямблиоз, балантидиаз или саркоцистоз. Для сбора биоматериала используется одноразовый контейнер с герметичной крышкой. Образец доставляется в лабораторию в течение часа, двух, иначе результат будет неточным. Исследование повторяется, спустя две недели, после получения первых результатов и служит подтверждением или опровержением диагноза.
В тех случаях, когда микроорганизмы пребывают в вегетативной форме, пациенту назначаются слабительные препараты. Объем биоматериала должен составлять около 15 грамм, этого количества будет достаточно для дальнейшего исследования.
Несомненный плюс подобного метода в его простоте, но результаты анализа кала не всегда точные и требуют последующего подтверждения.
Иммуноферментное исследование крови позволяет безошибочно выявить инфекционное заболевание, которые вызывают простейшие. Положительные результаты ИФА свидетельствуют об острой форме недуга.
96-луночный микропланшет, используемый для ИФА
Кровь для анализа забирается исключительно утром и натощак, а результаты исследования будут готовы в течение нескольких дней. Выведенный «титр» говорит о стадии развития протозойной инфекции. Низкий титр является подтверждением перенесенного заболевания в прошлом. Высокие показатели указывают на острый инфекционный процесс в организме.
Преимущества ИФА в точных развернутых результатах, которым доверяет каждый опытный врач.
Исследование посредством специального соскоба, который берется с влагалища (уретры) или путем забора крови пациента, позволяет поставить точный диагноз за считанные дни. Биоматериал окрашивается реагентами и подсвечивается в лабораторных условиях.
Недостатком метода является его недостоверность, поэтому анализ на непрямую реакцию назначают в комплексе с другими видами исследования биоматериала.
Исследование, основанное на биохимических реакциях, широко применяется в современной диагностике инфекций, вызванных микроорганизмами. Биоматериал, взятый на анализ, взаимодействует с кардиолипином в ходе лабораторных исследований. Чем интенсивнее биохимическая реакция, тем тяжелее степень заболевания. Реакция связывания комплемента — результативный метод диагностики заболеваний, вызванных размножением микроорганизмов.
Для исследований подобного рода у пациента берется генетический образец. Специальные синтетические ферменты увеличивают образец вместе с микроорганизмами. Детальное изучение пробы под микроскопом выявляет точный вид инфекции, досаждающей пациенту. Недостаток метода – дороговизна исследования.
Простейшие – это возбудители серьезных инфекционных недугов, которые не стоит оставлять без внимания. Своевременная диагностика и комплексное лечение позволит избежать нежелательных последствий заболеваний.
Лабораторные исследования на гельминтозы и протозоозы проводятся клинико-диагностическими лабораториями лечебно-профилактических учреждений, ведомственными лабораториями (НИИ, вузов, военных госпиталей, частных клиник и т.п.), а также другими лабораториями, имеющими лицензии или аккредитованными в системе Госстандарта и Госсанэпиднадзора для проведения данных исследований в независимости от формы собственности.
На центры Госсанэпиднадзора возлагается организация работы по обследованию населения на гельминтозы и протозоозы, методическое руководство, контроль за качеством работы, проводимой клинико-диагностическими лабораториями лечебно-профилактических учреждений и ведомственных лабораторий, обследование населения по эпидемиологическим показаниям и с консультативной целью.
В настоящих методических указаниях использованы ссылки на:
— Санитарные правила и нормы СанПиН 3.2.»Профилактика паразитарных болезней на территории Российской Федерации». Госкомсанэпиднадзор России. — М., 1988;
— Санитарные правила СП 3.1/3.2.»Общие требования по профилактике инфекционных и паразитарных заболеваний». Госкомсанэпиднадзор России. — М., 1997;
— Инструкция по проектированию санитарно-эпидемиологических станций. СН. Госгражданстрой. — М., 1982;
— Система аккредитации испытательных лабораторий (центров) государственной санитарно-эпидемиологической службы Российской Федерации. Минздрав России и Госстандарт России, Федеральный центр Госсанэпиднадзора России. — М., 1997;
— Санитарные правила СП 1.2.»Безопасность работы с микроорганизмами III — IV групп патогенности и гельминтами». Федеральный центр госсанэпиднадзора Минздрава России. — М., 1999.
Настоящие методические указания являются обязательными при выполнении лабораторных исследований биологического материала от людей с целью обнаружения паразитирующих в организме гельминтов и простейших.
Насчитывается свыше 250 видов паразитирующих у человека гельминтов, вызывающих заболевания — гельминтозы. На территории нашей страны обнаружено около 100 видов гельминтов, из них более 20 имеют широкое, практически повсеместное распространение. К паразитарным заболеваниям относятся также протозойные инвазии, возбудителями которых являются простейшие одноклеточные организмы. В настоящее время известно около 50 видов простейших, способных вызывать у человека заболевания.
Важность качественной лабораторной диагностики паразитарных заболеваний определяется во многих случаях трудностью их клинической и эпидемиологической диагностики. Многие инвазии у людей, в т.ч. у детей, нередко протекают субклинически, латентно.
В связи с этим грамотная лабораторная диагностика инвазий приобретает неоценимое значение. Качество лабораторной диагностики и уровень выявляемости зависят от тщательного выполнения всех требований любой методики, правильного выбора материала для исследования, знания циклов развития гельминтов, простейших, а также путей выделения из организма человека, морфологического строения яиц гельминтов и различных форм простейших. На результат анализа также влияет: неправильный забор материала или длительное его хранение, а также отсутствие подготовки больного лечащим врачом перед лабораторным обследованием.
Разнообразие возбудителей, форм паразитирования, и способов выделения диагностических стадий определяет достаточно широкий спектр методов диагностики.
Методы лабораторной диагностики паразитарных заболеваний применяются:
— для контроля эффективности лечения паразитарных заболеваний;
— для оценки качества проведения комплекса противопаразитарных мероприятий;
— с целью выявления источников заражения;
— для установления уровня пораженности населения.
Данный документ включает паразитологические методы лабораторной диагностики наиболее распространенных паразитарных заболеваний.
Материалом для лабораторных паразитологических исследований на гельминтозы и протозоозы служит различный биологический материал от человека: дуоденальное содержимое, кал, ректальная слизь, моча, мокрота, отделяемое бронхов, кровь, биопсийные ткани и др.
— Фекалии после дефекации отбирают из разных участков в количестве не менее 50 г (объем примерно от чайной до столовой ложки).
— Помещают в чистую (прокипяченную), сухую, стеклянную или пластмассовую посуду с крышками.
— Стерильная стеклянная (пластиковая) посуда требуется при заборе кала, для исследования на амебиаз.
— Кал должен быть доставлен в лабораторию и исследован в день дефекации, поэтому, как правило, доставляется утренний кал.
— Для обнаружения яиц стронгилоидеса кал доставляется и исследуется не позднее 1 ч после дефекации.
— Для обнаружения личинок стронгилоидеса, яиц анкилостомид и трихостронгилоид исследуется кал не позднее 4 ч после дефекации.
— Для обнаружения вегетативных (подвижных) форм дизентерийной амебы необходимо кал доставить и провести исследование не позднее 20 мин после дефекации или 40 мин, если это время кал сохранялся при температуре 4 °С.
— Для обнаружения вегетативных форм кишечных простейших (лямблий, диэнтамебы и др.) в жидком и полуоформленном «стуле» время от дефекации до исследования должно быть по возможности сокращено до минимума (не более 1 — 1,5 ч).
— при невозможности исследования кала сразу же после дефекации или в день поступления материала в лабораторию.
Физический способ хранения фекалий:
— при низкой температуре от 0 до 4 °С не более суток.
1. Жидкость Барбагалло: раствор формалина на физиологическом растворе (3 мл формалина 40 % + 97 мл физраствора или 1 л дистиллированной воды + 30 мл формалина 40 % + 8,5 г хлорида натрия).
2. Раствор формалина 4 %-ный.
3. Смесь 4 %-ного раствора формалина с равным количеством глицерина.
4. Раствор уксусной кислоты от 3 до 10 %.
5. Растворы детергентов 1 — 1,5 %-ные — моющие средства типа «Лотос», «Экстра» (кроме биоактивных); перед приготовлением раствора из порошка удаляют влагу, выдерживая в сухожаровом шкафу при 100 °С в течение 2 ч.
Заливается кал одним из приготовленных консервантов в объеме 1:1 или 1 часть фекалий и 2 части раствора консерванта, при этом тщательно перемешивается индивидуальной палочкой.
Хранить фекалии в растворах консервантов можно от нескольких месяцев до года, при более длительном хранении возможно разрушение яиц гельминтов.
6. Для консервации простейших кишечника фекалии можно поместить в консервант Турдыева: 80,0 мл 0,2 %-ного раствора азотистокислого натрия (0,16 г NaNO2 + 80,0 мл воды дистиллированной) + 2,0 мл глицерина + 10 мл концентрированного формалина (аптечного) + 8,0 мл концентрированного раствора Люголя (см. п. 4.2.4.1).
Смешивать в соотношении: 1 часть кала и 3 части консерванта.
7. Химические консерванты для консервации и хранения взрослых гельминтов или их фрагментов:
8. Для консервации мышц с личинками трихинелл используется концентрированный раствор хлористого натрия (на 100 мл водыг NaCl).
— Соскоб с перианальных складок можно забирать у обследуемого в лаборатории, или заранее выдавать пробирки с ватными тампонами, смоченными в глицерине, на шпателях или флаконы с глазными палочками, покрытыми специальным клеевым слоем (п. 4.2.3), предварительно проинструктировав обследуемого (если обследуется ребенок, то родителей ребенка) о способе забора материала и доставке его в лабораторию.
— Утром (вечером и утром обследуемому не подмываться) собрать соскоб с перианальных складок вокруг ануса методом «смыва» или «отпечатка» приготовленным ватным тампоном, смоченным в глицерине, или липкой лентой, или глазными стеклянными палочками со специальным клеевым слоем, как описано в п. 4.2.3.
— После забора соскоба шпатели вкладываются обратно в пробирку, липкая лента наклеивается на предметное стекло, а глазные палочки вкладываются в соответствующий флакон или специальный контейнер с штативами. Пробирки, флаконы, предметные стекла предварительно маркируются (при массовых обследованиях маркируются цифрами согласно списку обследуемых).
— Материал доставляется в лабораторию в чистых химических или центрифужных пробирках сразу после зондирования пациента натощак.
— Доставляют все три фракции (порции «А», «В», «С») и исследуют сразу после поступления в лабораторию.
— Порцию «А» доставляют для исследования на патогенные простейшие двенадцатиперстной кишки (лямблии), личинки стронгилоидеса, трихостронгилид, анкилостомид.
— Порции «В» и «С» доставляют для исследования на яйца гельминтов, паразитирующих в протоках печени и поджелудочной железы.
— Доставляется в лабораторию мокрота, выделенная при откашливании (не слюна и не слизь с носоглотки), в стерильной посуде с крышками (можно в чашках Петри).
— Исследуется сразу после поступления.
— Доставляется в лабораторию моча утреннего сбора в чистых стеклянных банках с крышками.
— Исследуется сразу после поступления в лабораторию.
— На шистосомоз — доставляется моча, собранная между 10 ч утра и 14 ч дня, или все порции суточной мочи; желательно собрать мочу после физической нагрузки (например,приседаний).
— С участков кожи (где изменения кожи или зуд) делают несколько срезов.
— Поверхностные срезы кожи диаметроммм делают бескровно, с соблюдением асептики, стерильным лезвием бритвы или глазным скальпелем, предварительно приподняв кожу кончиком стерильной иглы.
— Помещают кусочки кожи в стерильную стеклянную посуду (можно чашки Петри) с физраствором.
— Исследуют сразу после забора материала.
— Хирургическим путем получают биопсированные кусочки двуглавой или икроножной мышц (ближе к сухожилию).
— Помещают в стерильную стеклянную посуду с физраствором.
— Исследуют сразу после биопсии.
— Если лабораторное исследование откладывается на какой то срок, пробы мышц помещают в консервант или замораживают. Консервантом может служить концентрированный раствор хлорида натрия (%).
— После лечения геогельминтозов кишечника кал отбирается (п. 2.1) через месяц после проведенного лечения, а после лечения протозоозов кишечника кал отбирается (п. 2.1 и 2.1.1) в зависимости от выявленного заболевания: при амебиазе, балантидиазе — сразу после лечения, при лямблиозе — через неделю.
— После лечения контактных гельминтозов: при гименолепидозе кал отбирается (п. 2.1) через 1 и 6 месяцев после лечения; при энтеробиозе перианальный соскоб отбирается (п. 2.1.2) черездней после лечения.
— После лечения биогельминтозов кал отбирается (п. 2.1 и 2.1.1) черезмесяца после проведенного курса лечения.
— При первом отрицательном результате (исследования фекалий), отбор проб проводится еще двукратно с интерваломдня, после чего ставится окончательный результат лабораторного анализа.
— После лечения инвазий желчевыводящих путей контроль эффективности можно проводить как при исследовании кала, так и желчи, применяя соответствующие методы лабораторного исследования.
— При стронгилоидозе контроль эффективности проводится только при исследовании желчи (даже, если паразит был обнаружен копроскопическими методами) через месяц после лечения.
Макро- и микроскопические паразитологические методы лабораторной диагностики являются прямыми методами обнаружения гельминтов, их фрагментов, яиц и личинок гельминтов; вегетативных и цистных форм патогенных простейших, при обнаружении и идентификации которых не требуются косвенные методы исследования.
Все микроскопические методы применяются по показаниям (см. описание в конце каждого метода).
При плановых и профилактических осмотрах детского контингента, а также при обследовании декретированных групп населения необходимо обследовать пациента одновременно методом перианального соскоба в сочетании с одним из копроовоскопических методов и методом нативного мазка с раствором Люголя.
При обследовании больного в направлении для лаборатории необходимо указать предварительный диагноз, что позволит лаборанту выбрать соответствующую методику для выявления или исключения данного вида возбудителя. При отсутствии в направлениях врачей четкого диагноза и затруднении в выборе эффективного метода лабораторного исследования на кишечные простейшие и гельминты больного лучше обследовать с применением «комплексного» метода исследования фекалий из консерванта или универсального метода формалин-эфирного (уксусно-эфирного) осаждения.
При применении большинства паразитологических методов лабораторной диагностики учитывается эпидемиологический анамнез пребывания обследуемого на эндемичной по тем или иным паразитарным заболеваниям территории, контакт с домашними животными, геофагия или употребление в пищу продуктов питания, которые могут явиться источником заражения, и т.д., а также результаты косвенных и клинических методов обследования больного (серологические исследования, результаты рентгеноскопии, УЗИ, результаты общего анализа крови и т.д.)
Макроскопические методы служат для обнаружения в кале целых половозрелых гельминтов или их фрагментов невооруженным глазом или с помощью ручной лупы.
4.1.1. Метод визуального осмотра фекалий с последующим последовательным промыванием фекалий
На поверхности кала после дефекации можно видеть активно ползающих остриц; иногда выделяются с калом аскариды; у больных дифиллоботриозом могут выделяться обрывки стробилы лентеца (в виде «лапши»), а у инвазированных тениидами (свиной или бычий цепень) с калом часто отходят членики гельминтов (в виде «белых обсечек»), членики бычьего цепня могут активно выползать из анального отверстия.
Фекалии сначала осматривают целиком, затем разводят дистиллированной водой до жидкой консистенции и небольшими порциями исследуют при хорошем освещении.
Для лучшего просмотра фекалий применяют способ отстаивания.
Необходимые реактивы и оборудование
2. Физиологический раствор
9. Предметные стекла большие (6×10; 8×12 см)
11. Лупа, микроскоп и стереоскопический микроскоп типа МБС
— Размешать фекалии в большом количестве воды, в высоких стеклянных стаканах, банках и поставить отстаивать.
— Надосадочную жидкость слить, а осадок снова смешать с водой (таким образом проделывают несколько раз, пока надосадочный слой не станет прозрачным).
— Отливать отдельные небольшие порции в чашки Петри и тщательно просматривать под лупой, а лучше под стереоскопическим микроскопом МБС.
— Извлекать пинцетом или препаровальной иглой все подозрительные частицы и крупные образования на отдельное предметное стекло или чашку Петри.
— Образования, подозрительные на фрагменты гельминтов, рассматривать под лупой между двумя предметными стеклами или лучше под микроскопом МБС.
— Мелких гельминтов или сколексы цестод рассматривать в капле глицерина или физраствора под микроскопом при увеличении: окуляр ×7 или ×10, объектив ×8 или ×10.
— Микроскопия всех визуально обнаруженных в кале паразитов или фрагментов обязательна для уточнения морфологических особенностей и идентификации паразита.
— Эффективен для дифференциальной диагностики половозрелых гельминтов кишечника от непереваренных частиц и других включений кала и идентификации найденных паразитов.
— Достоверный метод при идентификации члеников бычьего и свиного цепня (т.к. обнаруживаемые при микроскопическом исследовании онкосферы у них идентичны, что не дает возможности дифференциальной диагностики), и наиболее эффективен в сочетании с методом опроса на отхождение у больного в момент дефекации «инородных» частиц.
— Перед методами микроскопии фекалий.
— При контроле эффективности лечения после применения лекарственных препаратов, не вызывающих деструкцию паразита.
— При идентификации зрелых паразитов или их фрагментов, например: для дифференциальной диагностики члеников цестод (бычьего, свиного цепня и широкого, чаечного лентеца).
4.2.1. Копроовоскопия (исследование фекалий на яйца гельминтов)
4.2.1.1. Метод толстого мазка под целлофаном по Като и Миура
Толстый мазок представляет собой тонкий слой фекалий на предметном стекле под гигроскопическим целлофаном, пропитанным смесью глицерина и фенола.
Необходимые реактивы и оборудование
2. Фенол — 6 %-ный раствор (100 мл дистиллированной воды + 6 г фенола)
3. Малахитовый зеленый — 3 %-ный раствор (2,5 г малахитовой зелени + 75 мл дистиллированной воды)
4. Целлофан (гигроскопический)
6. Палочки стеклянные или деревянные
7. Валик или резиновая пробка
Приготовление рабочего раствора Като
100 мл 6 %-ного р-ра фенола + 100 мл глицерина + 1,2 мл 3 %-ного р-ра малахитового зеленого (раствор можно хранить длительное время в склянке из темного стекла с притертой крышкой).
Фенол дезинфицирует препарат; глицерин просветляет мазок; малахитовая зелень снимает напряжение глаз микроскописта.
При отсутствии фенола и малахитовой зелени можно использовать раствор глицерина (50 мл глицерина + 50 мл дистиллированной воды).
Подготовка целлофановых полосок
Нарезать полоски из гидрофильного целлофана (гидрофильный целлофан горит, в отличие от полиэтиленовой пленки, которая плавится и непригодна для исследования), чтобы их размер соответствовал размеру предметного стекла.
Полоски поместить в рабочий раствор Като не менее чем на 24 ч до проведения анализа. В 200 мл рабочего раствора можно обрабатывать до 5 тыс. новых целлофановых полосок.
— На предметное стекло нанестимг фекалий (размером с горошину). Растереть индивидуальной палочкой (стеклянной, деревянной).
— Фекалии накрыть целлофановой полоской, обработанной в растворе Като.
— Целлофан сверху притереть резиновой пробкой или специальным валиком, ширина которого соответствует или немного больше ширины предметного стекла, до получения тонкого, равномерного, прозрачного слоя.
— Препарат выдержать при комнатной температуре в течение 1 ч или в термостате при 40 °С в течениемин.
— Микроскопировать при увеличении: объектив ×8 или ×10, окуляр ×7 или ×10 (для уточнения морфологического строения яиц гельминтов объектив ×40).
— Позволяет просмотреть враз больше фекалий, чем в нативном мазке.
— Выявляет яйца кишечных и печеночных гельминтов при высокой и средней интенсивности инвазии.
— Менее эффективен для выявления инвазий низкой интенсивности.
— Рекомендуется при массовых обследованиях населения на кишечные гельминтозы, например: при обследовании декретированных контингентов взрослого населения и детей организованных коллективов.
— В клинико-диагностических лабораториях, когда в направлениях врачей отсутствуют конкретные диагнозы или указания, на какие инвазии необходимо обследовать больного, что не позволяет лаборанту выбрать специальные методы лабораторной диагностики.
— Препараты, приготовленные методом Като, можно сохранять при комнатной температуре в течение длительного времени (за исключением яиц анкилостомид и карликового цепня) в качестве музейных препаратов.
4.2.1.2. Формалин-эфирный метод (седиментация)
Необходимые реактивы и оборудование
1. Раствор формалина 10 %-ный (10 мл формалина аптечного + 90 мл дистиллированной воды)
2. Этиловый эфир медицинский
4. Центрифужные градуированные пробирки
6. Металлическое ситечко чайное или бинт (марля)
7. Предметные и покровные стекла
8. Деревянные и стеклянные палочки
12. Центрифуга на 3000 об/мин.
— В центрифужные градуированные пробирки налить 7 мл 10 %-ного раствора формалина.
— Добавить 1 г фекалий (такое количество фекалий, чтобы раствор в пробирке поднялся до 8 мл).
— Фекалии тщательно смешать при помощи палочки (индивидуальной для каждого обследуемого) с формалином до образования однородной смеси.
— Процедить через воронку с металлическим ситечком или двухслойным бинтом в другую центрифужную пробирку (чтобы в новой пробирке процеженного раствора снова было 8 мл, если меньше, то дополнительно можно сполоснуть 10 %-ным раствором формалина воронку с бинтом, через который процеживали раствор фекалий).
— Добавить в эту пробирку 2 мл эфира, т.е. до метки 10 мл, закрыть пробкой и энергично встряхивать в течение 30 с (встряхивать желательно в вытяжном шкафу, в горизонтальном положении, придерживая при этом пробку).
— Смесь центрифугируют при 3000 об/мин в течение 1 мин (или в течение 2 мин при 1500 об/мин).
— После центрифугирования в пробирке образуется 4 слоя: эфир, «каловая пробка», раствор формалина и на дне осадок, в котором будут содержаться яйца гельминтов и цисты простейших.
— «Каловую пробку» палочкой отделить от стенок пробирки и вместе с надосадочной жидкостью вылить, перевернув пробирку вверх дном, с краев пробирки убрать ватным тампоном лишнюю влагу, чтобы она не стекала на дно пробирки, перевернуть пробирку опять дном вниз.
— Осадок, оставшийся на дне пробирки, (весь) нанести на предметное стекло пипеткой или непосредственно из пробирки; капли должны быть небольшими, по 2 капли на одном предметном стекле.
— При исследовании на цисты простейших в одну из капель осадка внести каплю 1 %-ного раствора Люголя (приготовление в п. 4.2.4.1).
— Капли накрыть покровным стеклом (жидкость не должна выступать за края стекла или затекать на покровное стекло).
— Каплю с раствором Люголя исследуют на цисты и ооцисты простейших, а каплю без Люголя исследуют на яйца и личинки гельминтов.
— Микроскопировать: на яйца и личинки гельминтов при увеличении — объектив х 8 или ×10, окуляр ×7 или ×10, для уточнения морфологического строения яиц гельминтов — объектив ×40; на цисты простейших — объектив ×40.
— Эффективно выявляет инвазии с высокой, средней и низкой интенсивностью.
— Применяется для выявления яиц, личинок гельминтов кишечника и печени, цист и ооцист простейших кишечника, но практически не выявляет стадии трофозоитов.
— Не снижает эффективности при исследовании фекалий из консервантов.
— Применяется как универсальный метод диагностики кишечных и печеночных гельминтозов и протозоозов при диагностических и эпидемиологических обследованиях населения.
— Используется как специальный метод для диагностики трематодозов, включая описторхоз.
— Используется как количественный метод диагностики.
4.2.1.3. Уксусно-эфирный метод (седиментация)
Необходимые реактивы и оборудование
1. Водный раствор уксусной кислоты 5 %-ный (5 мл ледяной уксусной кислоты + 95 мл дистиллированной воды)
3. Этиловый эфир медицинский
4. Центрифужные градуированные пробирки
6. Металлическое ситечко чайное или двухслойный бинт
7. Предметные и покровные стекла
8. Палочки деревянные и стеклянные
13. Центрифуга на 3000 об/мин
— В центрифужные градуированные пробирки налить 5 мл 5 %-ного раствора уксусной кислоты.
— Добавить 1 г фекалий (количество фекалий, чтобы раствор в пробирке поднялся до 6 мл).
— Фекалии тщательно смешать с уксусной кислотой при помощи палочки (индивидуальной для каждого обследуемого), закрыть пробирку резиновой пробкой и интенсивно встряхнуть до образования однородной смеси и дать постоять 1 мин.
— Процедить через воронку с металлическим ситечком или двухслойным бинтом в другую центрифужную пробирку (чтобы в новой пробирке процеженного раствора снова было 6 мл, если меньше, то дополнительно можно сполоснуть 5 %-ным раствором уксусной кислоты воронку с бинтом, через который процеживали суспензию фекалий).
— Добавить в эту пробирку 4 мл эфира, т.е. до метки 10 мл, закрыть пробкой и энергично встряхивать в течение 30 с, держа при этом пробирку в горизонтальном положении (встряхивать в вытяжном шкафу, придерживая пробку), до получения эмульгированной смеси.
— Смесь центрифугируют при 3000 об/мин в течение 1 мин или в течение 2 мин при 1500 об/мин.
— После центрифугирования в пробирке различают 4 слоя: в верхней части пробирки эфирный экстракт, образовавшаяся «каловая пробка», раствор уксусной кислоты и на дне небольшой осадок.
Уксусная кислота эмульгирует фекалии, проникает в непереваренные частицы, состоящие преимущественно из клетчатки; удельный вес смеси эфира с уксусной кислотой меньше удельного веса воды, поэтому фекалии вместе с непереваренными крупными частицами клетчатки поднимаются в виде пробки в верхнюю часть пробирки, а яйца гельминтов и цисты простейших, обладающие большим удельным весом, выпадают в осадок.
— «Каловую пробку» круговым движением палочки отделить от стенок пробирки и вместе с надосадочной жидкостью вылить, при этом излишки влаги удалить ватным тампоном с края пробирки, оставив на дне осадок.
— Осадок (как правило, небольшой, бесцветный) нанести на предметные стекла пипеткой или непосредственно из пробирки, капли должны быть небольшими, по 2 капли на одном предметном стекле.
— Перед исследованием на цисты простейших в одну из капель осадка внести каплю 1 %-ного раствора Люголя.
— Обе капли накрыть покровным стеклом (осадок не должен выступать за края стекла или затекать на покровное стекло).
— Каплю с раствором Люголя исследуют на цисты и ооцисты простейших, а каплю без Люголя исследуют на яйца и личинки гельминтов.
— Микроскопировать: на яйца и личинки гельминтов при увеличении — объектив х 8 или ×10, окуляр ×7 или ×10, для уточнения морфологического строения яиц гельминтов — объектив ×40; на цисты простейших — объектив ×40.
— Эффективно выявляет инвазии с высокой, средней и низкой интенсивностью.
— Применяется для выявления яиц, личинок гельминтов кишечника и печени, цист и ооцист простейших кишечника, т.к. 5 %-ный раствор уксусной кислоты не оказывает деформирующего воздействия на цисты и ооцисты простейших (при исследовании оформленных и неоформленных фекалий), но не сохраняет стадии трофозоитов.
— Не снижает эффективности при использовании фекалий из консервантов.
— Применяется как универсальный метод диагностики кишечных и печеночных гельминтозов и протозоозов при диагностических и эпидемиологических обследованиях населения.
— Используется как специальный метод для диагностики трематодозов, включая описторхоз.
— Используется как количественный метод диагностики.
Необходимые реактивы и оборудование
2. Раствор уксусной кислоты 1 %-ный
3. Раствор уксусной кислоты 10 %-ный
4. Эфир этиловый медицинский
9. Предметные и покровные стекла
11. Стеклянные или деревянные палочки
Приготовить рабочие растворы:
1) азотно-кислого натрия с удельным весом 1,15
— готовят из расчета г вещества (необходимо подобрать количество индивидуально, т.к. химическое вещество из разных расфасовок может дать разный удельный вес) на 1 л горячей воды в эмалированной посуде, соль кладут в емкость с горячей водой порциями при подогревании на плите и постоянном помешивании до полного растворения;
— после остывания приготовленного раствора проводят измерение удельного веса ареометром при комнатной температуре.
Если раствор готовится заранее, необходимо приготовить с более высоким удельным весом, т.к. уже через 24 ч удельный вес начинает падать;
2) растворы уксусной кислоты 1 %-ный и 10 %-ный.
— В градуированную центрифужную пробирку налить 6 мл рабочего раствора азотнокислого натрия.
— В другую пробирку налить 7 мл 1 %-ного раствора уксусной кислоты.
— В пробирку с уксусной кислотой внести пробу фекалий 0,5 — 1 г (до отметки 7,5 — 8 мл).
— Тщательно перемешать фекалии стеклянной палочкой.
— Процедить через воронку с одним слоем марли (бинта) в пробирку с азотно-кислым натрием.
— Центрифугировать при00 об/мин в течение 5 мин.
— Слить надосадочную жидкость из пробирки.
— В пробирку с осадком добавитьмл 10 %-ного раствора уксусной кислоты и 0,5 мл эфира.
— Закрыть резиновой пробкой и, придерживая пробку, энергично встряхнуть (в вытяжном шкафу).
— Провести повторное центрифугирование в течение 1 мин.
— Слить надосадочную жидкость.
— Осадок перенести на предметное стекло пипеткой.
— Каплю (или несколько капель) осадка накрыть предметным стеклом.
— Микроскопировать при увеличении: объектив ×8 или ×10, окуляр ×7 или ×10; для уточнения морфологического строения яиц гельминтов — объектив ×40.
— После дополнительной обработки осадка химреактивами в нем остаются только яйца гельминтов, что облегчает их выявление.
— По эффективности выявления примерно одинаков с уксусно-эфирным осаждением, но более трудоемок.
Применяется для выявления яиц гельминтов кишечника, печени.
Примечание . В основе методов седиментации (осаждения), описанных в п. п. 4.2.1.2, 4.2.1.3, 4.2.1.4 лежит разность удельного веса используемых химреактивов и яиц гельминтов, когда удельный вес яиц большой и они концентрируются в осадке.
В основе методов флотации (всплывания) лежит разность удельного веса флотационного раствора и яиц гельминтов, удельный вес флотационного раствора выше, в результате яйца гельминтов всплывают на поверхность жидкости и обнаруживаются в поверхностной пленке.
Необходимые реактивы и оборудование
1. Один из флотационных растворов
3. Проволочная петля (из нескольких круглых петель диаметром от 0,5 до 1 см)
4. Предметные стекла (обезжиренные)
6. Химические стаканчики емкостьюмл
9. Стеклянные или деревянные палочки
Приготовление флотационного раствора (по одной из нижеописанных прописей).
1. Раствор нитрата аммония NH4NO3 (гранулированной или обычной селитры) плотностью 1,3 готовят из расчета 1500 г вещества на 1 л горячей воды.
2. Раствор нитрата натрия NaNO3 или азотнокислого натрия (предложенный автором Калантарян) с плотностью 1,38 — 1,4 готовят из расчета 1000 г вещества на 1 л горячей воды.
3. Раствор тиосульфата натрия Na2S2O3 × 5H2O (гипосульфита натрия) с плотностью 1,4 готовят из расчета 1750 г вещества на 1 л горячей воды.
А. Раствор сульфата натрия Na2SO4 или английской соли с плотностью 1,26 — 1,28 готовят из расчета 920 г вещества на 1 л горячей воды.
5. Насыщенный раствор хлорида натрия NaCl (поваренной соли) с плотностью 1,18 — 1,2 (предложенный автором Фюллеборном) готовят из расчета г соли на 1 л кипящей воды.
Любую из выше предложенных солей растворяют в горячей воде в эмалированной посуде, причем кладут соль в емкость с горячей водой порциями при подогревании на плите и постоянном перемешивании до полного растворения.
Удельный вес флотационных растворов измеряется ареометром только после остывания раствора при комнатной температуре.
Измерение удельного веса флотационного раствора ареометром строго обязательно, т.к. приготовление раствора по прописи не гарантирует получение нужного удельного веса (например, когда используемая соль недостаточно химически чистая).
Фильтровать приготовленные растворы не обязательно. Если раствор приготовлен в большом количестве, то в последующие дни перед исследованием его подогревают с размешиванием осадка и после остывания раствора снова измеряют ареометром удельный вес.
Подготовка предметных стекол: предметные стекла обязательно обезжирить, например в смеси Никифорова (равные части этилового спирта и эфира).
— В химический стаканчик объемоммл налить немного одного из выше описанных флотационных растворов (стаканчик лучше предварительно поставить в чашку Петри).
— Поместить в стаканчик 2,5 г фекалий (объем с большой «боб»).
— Тщательно размешать палочкой (индивидуальной для каждого обследуемого).
— Удалить сразу же после размешивания всплывшие крупные частицы палочкой (или ложечкой с дырочками).
— Одновременно добавлять постепенно солевой раствор до 50 мл.
— При снятии поверхностной пленки предметным стеклом, стекло должно соприкасаться с жидкостью, поэтому стаканчик накрывается предметным стеклом, а флотационный раствор добавляется пипеткой до полного соприкосновения с предметным стеклом.
— Оставить взвесь на несколько мин, экспозиция зависит от того какой флотационный раствор применяется: при применении прописи №№ 1 и 5 — экспозициямин; №№ 2, 3,мин.
— После вышеуказанной экспозиции снять предметное стекло с химического стаканчика, перевернув кверху ту его поверхность, которой оно соприкасалось с жидкостью, и положить сухой поверхностью на стекло большего размера.
— Микроскопировать без покровного стекла при увеличении: объектив ×8, ×10, окуляр ×7, ×10, уточнение морфологического строения — окуляр ×40.
— При снятии поверхностной пленки проволочной петлей (лучше использовать петли с несколькими ячейками) целесообразно исследовать не менее 8 капель. Микроскопировать под покровным стеклом (можно и без покровного стекла, предварительно на предметное стекло нанеся каплю глицерина, в которой размазывают каплю с петли).
— Петли перед и после исследования обжигать на пламени спиртовой горелки.
Примечание . Целесообразнее использовать для снятия пленки предметные стекла, т.к. это наиболее просто в применении и площадь снятия поверхностной пленки значительно увеличивается.
— Наиболее эффективны методы флотации для обнаружения яиц нематод и цестод.
— Наиболее эффективно использование флотационного раствора с удельным весом 1,38 — 1,40 (всплывают и неоплодотворенные яйца аскарид).
— Неэффективен для выявления яиц трематод.
— Для обнаружения яиц гельминтов кишечника.
2. Стеклянная воронка (диаметром 10 см)
3. Металлическое сито или сетка «мельничный газ»
4. Резиновая трубка с зажимом
6. Стеклянные или деревянные палочки
Собрать аппарат Бермана, для чего закрепить в штативе стеклянную воронку с металлическим ситом. На нижний конец воронки надеть резиновую трубку с зажимом.
— Пробу фекалийг поместить на металлическое сито или мелкоячеистую металлическую сетку, или сетку «мельничный газ».
— Сетку с пробой фекалий приподнять и в воронку налить нагретую до°С воду таким образом, чтобы нижняя часть сетки с калом была погружена в воду.
— Черезч зажим на резиновой трубке быстро открыть и жидкость спустить в центрифужную пробирку.
— Полученную жидкость центрифугироватьмин.
— Надосадочную жидкость быстро слить.
Осадок нанести на предметное стекло или в чашку Петри.
Микроскопировать при увеличении: объектив ×8 или ×10, окуляр ×7 или ×10 (можно использовать стереоскопический микроскоп МБС), уточнение морфологического строения при увеличении: объектив ×40, окуляр ×10.
— Является эффективным методом выявления рабдитовидных личинок стронгилоидес.
— Эффективность методики возрастает при увеличении экспозиции фекалий в воде.
— Применяется как специальный метод для диагностики стронгилоидоза.
Необходимые реактивы и оборудование
6. Стереоскопический микроскоп МБС
— В химический стаканчик положить порцию фекалийг (величиной с орех).
— Залить теплой (40 °С) дистиллированной водой, чтобы фекалии были полностью покрыты.
— Черезмин слить жидкость в центрифужные пробирки.
— Отстаиваютмин или центрифугируют 1 мин при 1500 об/мин.
— Слить осторожно надосадочную жидкость, осадок поместить в чашку Петри.
— Исследовать осадок в чашке Петри под бинокулярным стереоскопическим микроскопом МБС (с нижней подсветкой) объектив ×2, окуляр ×12, ×14; обращая внимание на подвижных, слабоподвижных и неподвижных личинок.
— Неподвижные личинки микроскопируют с увеличением: объектив ×8, ×10 и ×40; окуляр ×10.
— Эффективен при высокой и средней интенсивности инвазии и менее эффективен при низкой интенсивности инвазии.
— Рекомендуется сочетать с исследованием дуоденального содержимого.
— Чаще используется для диагностики стронгилоидоза при массовых обследованиях.
— Данная методика может быть использована для диагностики простейших — балантидий, при экспозиции фекалий в воде до 1,5 — 2 ч (п. 4.2.4.3).
4.2.2.3. Метод культивирования личинок на фильтровальной бумаге (метод Харада-Мори в модификации Маруашвили)
1. Фильтровальная бумага (размером 16×3,5 см)
2. Стеклянная банка (0,7 — 0,8 л)
— На фильтровальную бумагу нанести свежевыделенные фекалии в виде мазка, оставляя края фильтровальной бумаги свободными.
— Смочить стенки банки водой, опустить в банку фильтровальную бумагу и поверхностью без фекалий зафиксировать ее на стенках банки.
— Налить в банку воды так, чтобы в нее был погружен нижний конец бумаги без фекалий.
— Верх банки закрыть полиэтиленовой пленкой или чашкой Петри.
— Банку поставить в термостат при температуре 28 °С надней (в теплое время года банку можно оставлять при комнатной температуре, увеличив экспозицию додней).
— Часть личинок может подняться вверх по фильтровальной бумаге, поэтому работа должна проводиться с соблюдением техники безопасности.
— Для безопасности можно предварительно убить личинки, поместив пробирку в водяную баню при температуре 50 °С на 15 мин.
— Эффективен для обнаружения и идентификации личинок анкилостомид.
— Для диагностики анкилостомидозов.
Необходимые реактивы и оборудование
Кроме микроскопа, необходимое оборудование зависит от способа получения соскоба: деревянный шпатель, шпатель с ватным тампоном, предметные и покровные стекла, полоски прозрачной липкой ленты, глазные палочки со специальным клеевым слоем и др.
При массовых обследованиях населения (в основном детского) заранее подготовить шпатели с тампонами и пробирки, или предметные стекла с липкой лентой, флаконы, или специальные штативы с глазными палочками, покрытыми клеевым слоем. Промаркировать предметные стекла, пробирки или флаконы, либо маркировать во время забора материала у обследуемых, согласно номеру по списку. Методы отбора соскобов с перианальных складок см. п. 2.1.2.
Ход исследования: зависит от способа отбора материала.
4.2.3.1. Метод перианального соскоба липкой лентой по Грэхем
Примечание . Пригодна полиэтиленовая прозрачная пленка с липким слоем для детского технического творчества, но лучше использовать операционную пленку ЛПО-1, ЛПО-2.
— Подготовить отрезок липкой ленты длинойсм, предварительно наклеить его на предметное стекло.
— Перед взятием соскоба отклеить полоску липкой ленты от предметного стекла, держа полоску за концы, плотно прижать всей липкой поверхностью к анусу и перианальным складкам, стараясь пальцами рук не касаться перианальной области.
— Отклеить полоску от кожи перианальной области и перенести на предметное стекло липким слоем вниз, приклеить к стеклу равномерно для избежания образования воздушных пузырей, мешающих микроскопии.
— Концы ленты, выходящие за края стекла, отрезать.
— Микроскопировать при увеличении: объектив ×8 или ×10, окуляр ×7 или ×10.
Примечание . Метод применяется как для индивидуального, так и для массового обследования.
4.2.3.2. Метод перианального соскоба с применением стеклянных глазных палочек с клеевым слоем по Рабиновичу
Пропись клея: клеол — 10 мл, касторовое масло — 2,5 мл, этиловый эфир — 5 мл, этиловый спирт 96,5 %-ный — 2,5 мл (хранение во флаконе по 20,0 мл с плотно притертой пробкой).
— Подготовить стеклянные глазные палочки (лучше с широкими лопаточками): промыть, обезжирить и простерилизовать (кипячением или автоклавированием), высушить; сухую лопаточку глазной палочки обмакнуть в клей; просушить не менееч (глазная палочка при этом должна находиться лопаточкой вверх для стекания избытка клея и образования равномерной пленки).
— Клей, обтекая лопаточку, образует прозрачную клейкую пленку, сохраняющуюся после высыхания не менее недели (что позволяет готовить палочки заранее).
— Установить глазные палочки в специальный штатив, где каждая ячейка имеет свой номер, или использовать пронумерованные пенициллиновые флаконы, предварительно закрепив ручку глазной палочки в резиновой пробке от этого пузырька.
— Взять соскоб путем соприкосновения или «отпечатка» плоской частью лопаточки обеих сторон с кожей перианальных складок.
— Снова укрепить палочку в штативе или пенициллиновых пузырьках (промаркированных соответственно номеру, присвоенному обследуемому по списку, или регистрационному номеру в журнале) для доставки в лабораторию.
— Укрепить глазную палочку в специальном держателе для просмотра под микроскопом.
— Микроскопировать непосредственно плоскую поверхность лопаточки поочередно с обеих сторон при увеличении: окуляр ×7 или ×10, объектив ×8 или ×10.
— Использованные палочки дезинфицировать кипячением в мыльном растворе, тщательно промыть, прополоскать, обезжирить в смеси Никифорова, просушить в сухожаровом шкафу. Штатив и кассеты обработать 70 %-ным спиртом и промыть мыльно-содовым раствором. Пенициллиновые пузырьки и резиновые пробки дезинфицировать кипячением или автоклавированием.
Примечание . Метод гигиеничен и достаточно прост в применении, применяется как для индивидуального, так и для массового обследования.
4.2.3.3. Метод перианального соскоба по Торгушину
— Ватный тампон, накрученный на деревянном или стеклянном шпателе, смочить в растворе глицерина.
— Обтереть тампоном перианальные складки вокруг ануса.
— На предметное стекло поместить каплю глицерина.
— Слегка ударяя по предметному стеклу, обмыть тампон в капле глицерина.
— Полученный препарат микроскопировать без покровного стекла; увеличение: объектив ×8 или ×10, окуляр ×7 или ×10.
Примечание . Недостаток метода: часть яиц остается на ватном тампоне — неудобен при массовых обследованиях.
4.2.3.4. Метод перианального соскоба по Кеворковой
— Налить в центрифужную пробирку около 5 мл кипяченой или дистиллированной воды.
— Поместить в него шпатель (палочку) с ватным тампоном.
— Перед забором соскоба слегка отжать тампон о внутреннюю стенку пробирки.
— Обтереть тампоном перианальные складки.
— Вложить шпатель с тампоном в пробирку с водой.
— Тщательно прополоскать тампон в пробирке с водой и удалить шпатель с тампоном из пробирки.
— Полученный смыв центрифугировать в течение 3 мин при 1500 об/мин.
— Слить надосадочную жидкость.
— Осадок перенести на предметное стекло, покрыть покровным стеклом.
— Микроскопировать при увеличении: объектив ×8 или ×10, окуляр ×7 или ×10.
Примечание . Недостаток метода: неудобен при массовых обследованиях.
Эффективность методов соскоба
— Эффективны для выявления яиц гельминтов, находящихся на перианальных складках: яйца остриц и онкосферы тениид.
— Методы перианального соскоба применяются для диагностики энтеробиоза, тениаринхоза и тениоза при индивидуальной диагностике или массовом обследовании детского и взрослого населения.
4.2.4. Копропротозооскопия (исследование фекалий на кишечные простейшие)
4.2.4.1. Метод нативного мазка с физраствором и раствором Люголя
Необходимые реактивы и оборудование
3. Буферный раствор метиленового синего
4. Уксусно-кислый спиртовой раствор йода
5. Предметные и покровные стекла
8. Стерильная стеклянная или пластиковая посуда (для забора фекалий)
Для исследования выбирают в первую очередь неоформленные фекалии, участки слизи или прожилки крови в кале.
Фекалии исследуют теплыми, т.е. не позднеемин после дефекации, когда возможно обнаружение подвижных вегетативных форм (трофозоитов) простейших (время можно увеличить до 45 мин и до 1 ч, если фекалии сохранялись это время в холодильнике при температуре°С).
Физиологический раствор подогреть до°С.
Приготовление маточного 5 %-ного раствора Люголя: 10 г иодида калия растворить в 30 мл дистиллированной воды + 5 г кристаллического йода, размешать до полного растворения и долить до 100 мл дистиллированной водой. Хранить после приготовления в склянке из темного стекла.
Приготовление рабочего 1 %-ного раствора Люголя: 5 мл маточного 5 %-ного раствора Люголя соединить с 20 мл физиологического раствора, хорошо перемешать. Хранить в склянке из темного стекла не более 14 дней.
Приготовление буферного метиленового синего: 50 мл дистиллированной воды + 46,3 мл раствора уксусной кислоты (1,2 мл ледяной уксусной кислоты + 98,8 мл дистиллированной воды) + 3,7 мл раствора уксуснокислого натрия (1,6 г уксуснокислого натрия + 100 мл дистиллированной воды) + 0,5 г метиленового синего. Приготовленный раствор хорошо перемешивается, настаивается 15 мин и фильтруется.
Приготовление уксусно-кислого спиртового раствора йода: 10 мл спиртового раствора Люголя (40 мл 70 %-ного этилового спирта + несколько кристаллов йода, хорошо перемешать, раствор должен иметь цвет «крепкого чая») + 10 мл 25 %-ного раствора уксусной кислоты.
— Нанести на предметное стекло 1 каплю изотонического теплого (°С) раствора в левой половине и 1 каплю 1 %-ного раствора Люголя в правой половине предметного стекла.
— Выбрать из пробы фекалий деревянной палочкой патологические примеси или немного фекалий (с булавочную головку) и перенести в каплю физраствора и растереть до получения равномерной негустой эмульсии, а затем поместить в каплю с Люголем и также растереть.
— Накрыть капли покровным стеклом (через правильно приготовленный мазок можно видеть газетный шрифт).
— Микроскопировать при увеличении: сначала — объектив ×8 или ×10, окуляр ×10, затем объектив ×40, в т.ч. для дифференциальной диагностики амеб и жгутиковых, включая лямблии и диэнтамебу.
1. Для дифференциальной диагностики трофозоитов дизентерийной амебы с непатогенными амебами необходимо приготовить препарат с буферным раствором метиленового синего: нанести на предметное стекло большую каплю буферного раствора метиленового синего, в нее внести деревянной палочкой небольшое количество слизи, фекалий с прожилками крови, накрыть покровным стеклом, дать постоятьмин, чтобы краска проникла в трофозоиты, и сразу микроскопировать для исключения перекрашивания трофозоитов.
Результат окрашивания: трофозоиты амеб окрашиваются в разные оттенки синего — ядро синее, цитоплазма голубая, эритроциты синие. Цисты амеб, трофозоиты, цисты жгутиковых и ооцисты кокцидий не окрашиваются.
2. Для выявления ооцист кокцидий: при выполнении вышеописанной методики приготовления нативного мазка с физраствором и 1 %-ным раствором Люголя, в одну из капель вместо 1 %-ного р-ра Люголя вносится капля уксусно-кислого спиртового раствора йода. Палочкой внести небольшое количество фекалий, растереть, накрыть покровным стеклом; микроскопировать при тех же увеличениях. Ооцисты изоспоры выявляются, благодаря хорошей окраске ядер.
— Позволяет выявлять вегетативные формы патогенных простейших и комменсалов, анализировать тип их движения (что имеет важное значение при видовой идентификации простейших, особенно жгутиковых).
— Диагностика амебиаза эффективна только при строгом соблюдении стерильного забора фекалий и микроскопического исследования не позднеемин после дефекации.
— Позволяет определять видовые признаки цист амеб и жгутиковых, ооцист кокцидий, благодаря эффективной окраске йодом ядер, жгутикового аппарата, гликогена.
— Применяется для диагностики кишечных протозоозов: лямблиоза, балантидиаза, амебиаза, кокцидиоза (изоспороза).
— Для исследования на кишечные простейшие, в т.ч. на лямблии используются также методы: формалин-эфирного (уксусно-эфирного) осаждения и исследование дуоденального содержимого (см. описание методик в п. 4.2.1.2, 4.2.1.3, 5.1).
Примечание . В нативных препаратах с физиологическим раствором при интенсивной инвазии также можно обнаружить яйца гельминтов и личинки стронгилоидеса.
4.2.4.2. Комплексный метод исследования фекалий на кишечные простейшие и гельминты из консерванта
Универсальный метод диагностики кишечных паразитозов, вызываемых простейшими (амебы, жгутиковые, в т.ч. диентамеба, балантидии и кокцидий) и гельминтами (нематоды, трематоды и цестоды).
В основе метода лежит «диагностическая система» КТ-ФЭО-МЦН: консервант Турдыева, формалин-эфирное обогащение, модифицированный метод окраски Циля-Нильсена.
Принцип метода: отбор проб фекалий производят в консервант Турдыева (п. 2.1.1), где паразиты фиксируются, и морфологические признаки простейших, яиц и личинок гельминтов сохраняются неизменными длительное время, это обеспечивает дальнейшее исследование материала из единой пробы:
— методом влажного мазка из консерванта;
— методом мазка из осадка после эфир-формалинового обогащения консервированного материала;
— модифицированным методом окрашивания по Цилю-Нильсену мазка из осадка после обогащения материала из консерванта.
Эффективность комплексного метода
— Выявляет весь спектр кишечных паразитов, в т.ч. редко диагностируемых простейших (диэнтамеба, изоспора), яиц и личинок гельминтов, не требующих специальных методов исследования (например, культивирования и т.п.) включая возбудителей оппортунистических инвазий (кокцидий, стронгилоидес).
— Повышается выявляемость сочетанных инвазий.
Условия отбора материала: максимально быстро после дефекации с помощью деревянной палочки фекалии переносят в стерильный флакон с консервантом Турдыева (п. 2.1.1), если фекалии оформленные, то количество должно быть в объеме с лесной орех, если жидкие — объемом с чайную (столовую) ложку. Соблюдая соотношение: 3 части консерванта и 1 часть фекалий. Флакон закрывают крышкой, предварительно тщательно размешав фекалии деревянной палочкой до гомогенной суспензии.
Необходимое оборудование и реактивы
3. Предметные и покровные стекла
— На предметном стекле готовятся два препарата: пипеткой из консерванта с фекалиями, очень осторожно, не взбалтывая содержимое флакона, нанести две капли придонного осадка (в правой и левой части стекла).
— Растереть деревянной палочкой.
— В одну из капель добавить каплю раствора Люголя 1 %-ного.
— Каждую каплю накрывают покровным стеклом (покровные стекла можно окантовать вазелином для предотвращения высыхания и смещения покровного стекла).
— Микроскопируют при увеличении: объектив ×8 или ×10, окуляр ×7 или ×10, затем объектив ×40 (в отдельных случаях, например для криптоспоридий, применяют увеличение объектива ×90 или ×100 и микроскопируют с масляной иммерсией).
— Эффективен для выявления цист и трофозоитов простейших, включая редко выявляемую диентамебу, а также яиц и личинок гельминтов.
— Для диагностики кишечных протозоозов.
Примечание . Ооцисты при достаточном количестве обнаруживаются в верхнем слое мазка непосредственно под покровным стеклом по эффекту негативного окрашивания раствором Люголя.
Необходимое оборудование и реактивы
1. Физиологический раствор
4. Раствор формалина 10 %-ный нейтральный (для нейтрализации — во флакон темного стекла с раствором формалина на дно слоем всм насыпать порошкообразный углекислый кальций)
6. Центрифужные градуированные пробирки
9. Стекла предметные и покровные
— Перенести пипеткой в центрифужную пробирку осадок фекалий со дна флакона с консервантом в объеме 1,5 — 2 мл.
— Добавитьмл 10 %-ного нейтрального формалина.
— Закрыть пробирку резиновой пробкой и тщательно перемешать, энергично встряхивая пробирку в течение 5 с.
— Полученную взвесь перелить в другую центрифужную пробирку через стеклянную воронку с двухслойным бинтом (марлей).
— Добавитьмл этилового эфира.
— Закрыть пробирку пробкой и энергично встряхивать в течение 30 с.
— Убрать пробку и дать постоять пробирке в течение 2 мин в вытяжном шкафу.
— Затем центрифугировать 2 мин при 1500 об/мин или 1 — 1,5 мин при 3000 об/мин.
— Отделить палочкой образовавшуюся «каловую пробку» от стенок пробирки.
— Перевернуть пробирку дном вверх и вылить содержимое (можно ватным тампоном обтереть стенки пробирки, чтобы жидкость не стекала на дно и не увеличивала объем осадка), пробирку поставить в штатив.
— На предметное стекло по обе стороны от центра нанести по капле физиологического раствора и раствора Люголя.
— Перенести в каждую каплю осадок из центрифужной пробирки, размешать деревянной палочкой и накрыть каждую каплю покровным стеклом.
— Микроскопировать при увеличении: объектив ×8 или ×10, окуляр ×7 или ×10, затем с объективом ×40 (при необходимости использовать окуляр ×90 или ×100 с масляной иммерсией).
— Для диагностики цист кишечных простейших и яиц гельминтов.
Необходимые реактивы и оборудование
7. Химические стаканчики или «мостики» для окрашивания мазков
— На предметное стекло нанести пипеткой каплю осадка из центрифужной пробирки после обогащения (п. 4.2.4.2.2) и круговым движением палочки приготовить мазок (можно добавить каплю физиологического раствора, чтобы мазок не был густым).
— Высушить на воздухе (тщательно).
— Фиксировать мазок в смеси Никифорова в течениемин.
— После фиксации мазок высушить на воздухе.
— Окрашивать мазок в растворе карболового фуксина (приготовление в п. 4.2.4.4), поместив мазок в химический стаканчик с этой краской на 45 мин!
— Промыть мазок проточной водой.
— Обесцветить мазок в 10 %-ном растворе серной кислоты до прекращения отхождения розовых «облачков» красителя.
Промыть тщательно проточной водой.
— Подкрасить мазок 5 %-ным раствором малахитового зеленого, приготовленного на 10 %-ном этиловом спирте в течениемин.
— Высушить мазок на воздухе.
— Микроскопировать при увеличении: окуляр ×10, объектив ×90 или ×100 с масляной иммерсией.
— Для выявления ооцист кокцидий, включая криптоспоридии и изоспоры.
— Предварительная фиксация в консерванте и обогащение осаждением повышает выявляемость ооцист по сравнению со стандартной методикой диагностики ооцист кокцидий, включая криптоспоридии и изоспоры.
Необходимые реактивы и оборудование
— В химический стаканчик или в чашку Петри положить порцию фекалийг (величиной с орех), предварительно перемешав фекалии.
— Залить теплой (45 °С) дистиллированной водой, чтобы фекалии были полностью покрыты.
— Через 1,5 — 2 ч слить жидкость в центрифужные пробирки.
— Центрифугировать 2 мин при 1500 об/мин.
— Надосадочную жидкость слить, осадок с помощью стелянной пипетки перенести на предметное стекло (по 2 капли на каждое стекло), накрыть покровными стеклами.
— Микроскопировать при увеличении: объектив ×10, окуляр ×10; для уточнения морфологических особенностей: объектив ×40; окуляр ×10.
— Позволяет выявлять трофозоиты балантидий при низкой интенсивности инвазии.
— Для диагностики балантидиаза.
Необходимые реактивы и оборудование
1. Реактивы: фуксин основной, этиловый спирт, фенол, раствор серной кислоты 7 %-ный (%-ный), раствор малахитовой зелени 5 %-ный в 10 %-ном этиловом спирте, водный раствор метиленового синего 0,2 %-ный, раствор малахитового зеленого 5 %-ный, азур-эозин по Романовскому-Гимзе 10 %-ный раствор, флотационные растворы
3. Стеклянные или деревянные палочки
6. Мостики стеклянные или «контейнеры» для окраски мазков
7. Пипетки, стеклянные капилляры
10. Центрифужные пробирки объемом 15 мл
Приготовление рабочего раствора краски по Цилю-Нильсену
— Фуксина основного 2 г растворить в 12 мл спирта 96°-ного.
— Фенола 5 г растворить в 50 мл дистиллированной воды.
— Слить вместе растворы фуксина и фенола, долить дистиллированной воды до 100 мл, перемешать.
Подготовка материала для исследования
Из фекалий приготовить мазок одним из следующих способов.
— Нанести на предметное стекло небольшое количество фекалий
— Растереть фекалии тонким слоем (при необходимости к комочку фекалий добавляюткапли физиологического раствора или воды)
— Тщательно высушить мазок на воздухе (не менее 30 мин)
Б) Обогащение флотационным методом
— Приготовить флотационный раствор (в качестве флотационного раствора использовать насыщенный раствор хлористого натрия или насыщенный раствор сульфата цинкаг сульфата цинка на 1 л водопроводной воды)
— Разбавить фекалии водой, размешать
— Процедить разбавленные фекалии через 2-слойный бинт в центрифужную пробирку
— Центрифугировать при 1500 об/мин в течениемин
— Удалить супернатант (объем оставшегося осадка не должен превышать 1 мл)
— Добавить флотационную жидкость до половины объема пробирки
— Размешать содержимое пробирки стеклянной палочкой
— Добавить флотационную жидкость до верхнего края пробирки
— Центрифугировать при 1500 об/мин в течениемин
Собрать поверхностную пленку металлической петлей или стеклянным капилляром и поместить на предметное стекло
В) Обогащение методом седиментации
— Поместить в пробирку 0,5 — 1 г фекалий
— Залитьмл изотонического раствора хлорида натрия
— Перемешать содержимое пробирки до образования однородной суспензии
— Процедить суспензию через двойной слой марли в другую пробирку
— Слить надосадочную жидкость
— Повторно залить осадок изотоническим раствором хлорида натрия
— Слить надосадочную жидкость
— Перенести осадок пипеткой на предметное стекло
— Приготовить из осадка мазок
Высушить мазки на воздухе (мазки, приготовленные одним из способов, описанных в п.п. А, Б, В).
— Фиксировать мазки в смеси Никифорова в течениемин.
— Фиксированные и высушенные мазки быстро провестираз над пламенем горелки.
— Поместить мазок в рабочий раствор карбол-фуксина намин.
— Промыть мазок водопроводной водой.
— Обесцветить мазок 7 %-ным раствором серной кислоты в течениес.
— Подкрасить в течение 5 мин 5 %-ным раствором малахитовой зелени.
— Микроскопировать при увеличении: окуляр ×10, объектив ×90 или ×100 с масляной иммерсией.
— Метод окраски фиксированных мазков по Цилю-Нильсену считается одним из наиболее надежных для выявления ооцист криптоспоридий.
Результат: ооцисты криптоспоридий окрашиваются в разные оттенки ярко-красного цвета и имеют вид округлых образований диаметром около 5 мкм. Оболочка ооцист окрашивается фуксином неравномерно. Сопутствующая микрофлора окрашивается в зеленые цвета.
— Применяется для диагностики криптоспоридиоза.
Примечание . Для окрашивания фиксированных мазков можно применять и другие красители, например: Азур-эозином по Романовскому-Гимзе окрашивать от 10 домин в 10 %-ном растворе красителя при этом ооцисты не окрашиваются или слабо окрашиваются и имеют вид округлых образований, внутри ооцист (по периферии) могут быть в виде бледно-голубых удлиненных и слегка изогнутых телец (спорозоиты) с красноватыми гранулами внутри.
Количественными методами определяют число яиц гельминтов в 1 г или 1 мл фекалий. Данные методы дают ориентировочное представление об интенсивности инвазии, позволяют судить об эффективности лечения гельминтозов при частичном паразитологическом излечении.
4.2.5.1. Метод толстого мазка под целлофаном по Като-Кац (количественная модификация метода Като и Миура)
Необходимые реактивы и оборудование
4. Валик или резиновая пробка
6. Пластинка размером 40×30 мм (из пластмассы или металла) с отверстием в центре диаметром 6 мм
— На предметное стекло поместить пластинку с отверстием.
— Произвольную навеску фекалий поместить на отверстие пластинки.
— Прокатать резиновой пробкой или пластмассовой разовой палочкой материал так, чтобы через отверстие в пластинке на стекло выдавилась стандартная навеска.
— Препарат обработать по стандартной методике Като (см. п. 4.2.1.1).
— При микроскопии просматривается весь мазок и ведется подсчет обнаруженных яиц гельминтов.
— Чтобы определить количество яиц в 1 г фекалий: число яиц, обнаруженных в данном препарате, следует умножить на коэффициент, равный 24.
— Применяется для определения интенсивности инвазии при клинико-диагностических обследованиях и при массовых обследованиях для определения напряженности очага инвазии.
4.2.5.2. Методы формалин-эфирного и уксусно-эфирного осаждения
Методы основаны на исследовании 1 г фекалий (количество фекалий, внесенное в пробирку и вызвавшее подъем жидкости на 1 мл, равно 1 г). При просмотре всего осадка полностью методы дают возможность провести количественный учет обнаруженных яиц, т.к. количество яиц в осадке соответствует нахождению их в 1 г фекалий.
Необходимые реактивы и оборудование
7. Палочки стеклянные или деревянные
Желчь в лабораторию должна быть доставлена сразу после зондирования. При подозрении на лямблиоз, стронгилоидоз, анкилостомоз, трихостронгилез тщательно исследуют порцию «А», исследование порций «Б» и «С» более информативно на печеночные трематодозы.
В желчи, исследуемой сразу после зондирования, обычно обнаруживаются вегетативные подвижные формы лямблий и подвижные личинки стронгилоидеса. При исследовании желчи через несколько часов после зондирования (но в день забора материала) обычно подвижность личинок стронгилоидеса и вегетативных форм лямблий не наблюдается.
5.1.1. Исследования нативного мазка желчи
— Выбрать сгустки слизи, волокон, патологические примеси.
— Палочкой стеклянной или деревянной (можно пипеткой) нанести тонким слоем желчь на предметное стекло (мазок не должен стекать с предметного стекла).
— При исследовании в чашке Петри налить желчь тонким слоем на дно чашки.
— Микроскопировать без покровного стекла при увеличении: объектив ×8 или ×10, окуляр ×10; для уточнения морфологии яиц гельминтов и для исследования на простейших — объектив ×40.
Для обнаружения подвижных личинок стронгилоидеса можно микроскопировать в чашках Петри под стереомикроскопом МБС (окуляр ×2; объектив ×12,5 — 14).
5.1.2. Исследования желчи с центрифугированием
— При наличии в желчи большого количества слизи или гноя взболтать все порции с равным количеством эфира.
— Центрифугировать в центрифужных пробирках все порции дуоденального содержимого не менее 20 мин при00 об/мин.
— Надосадочную часть желчи слить в отдельную емкость.
— Осадок перенести пипеткой или прямо из пробирки на предметное стекло.
— Микроскопировать без покровного стекла при увеличении: объектив ×8 или ×10, окуляр ×10; и для уточнения морфологии яиц гельминтов и для исследования на простейших — объектив ×40.
Для обнаружения подвижных личинок стронгилоидеса можно микроскопировать в чашках Петри под стереомикроскопом МБС (окуляр ×2; объектив ×12,5 — 14).
— Наиболее эффективно сочетание исследования желчи нативно и с центрифугированием.
— Исследование желчи на яйца трематод эффективно только при центрифугировании.
Для выявления яиц трематод (описторхиса, клонорха, фасциол, дикроцелий), вегетативных и цистных форм простейших — лямблий, личинок стронгилоидеса, трихостронгилид и анкилостомид.
Необходимые реактивы и оборудование
1. Раствор NaOH или КОН 0,5 %-ный
3. Предметные стекла, большие предметные стекла
Мокроту, представляющую собой патологический секрет дыхательных путей вместе с отделяемым носоглотки и полости рта, собрать в стерильную (можно прокипяченную) стеклянную емкость с крышкой и исследовать сразу после доставки в лабораторию.
Исследуется мокрота, выделенная при откашливании (не слюна и не слизь с носоглотки).
При слизисто-гнойной мокроте для лучшего растворения слизи, гноя:
— мокроту смешать с равным объемом 0,5 %-ного раствора едкой щелочи;
— слегка подогреть пробирку на водяной бане;
— пробирку энергично встряхивать в течение 5 мин.
5.2.1.1. Исследование нативного мазка мокроты
— Мокроту из стеклянной емкости пипеткой переносят на предметное стекло (лучше большое).
— Приготовить мазок путем равномерного растирания между двумя предметными стеклами или нанесения и равномерного растирания палочкой на большом предметном стекле.
— Микроскопировать при увеличении: объектив ×8 или ×10, окуляр ×10, для уточнения морфологических особенностей окуляр ×40.
5.2.1.2. Исследование мокроты с центрифугированием
— Перелить мокроту в центрифужные пробирки.
— Центрифугировать в течениемин при 1500 об/мин.
— Слить надосадочную жидкость.
— Перенести осадок пипеткой или сразу из пробирки на предметное стекло.
— Микроскопировать при увеличении: объектив ×8 или ×10, окуляр ×10, для уточнения морфологических особенностей окуляр ×40.
— Эффективен для выявления яиц гельминтов, паразитирующих в легких, бронхах (яйца парагонимуса, томинкса), иногда яиц шистосом.
— Менее эффективен при диагностике личиночных стадий кишечных нематод в период миграции через легкие (личинки аскарид, анкилостомид, стронгилоидеса).
— Иногда можно обнаружить личиночные стадии эхинококков (сколексы эхинококка, альвеококка) при поражении легких и прорыве пузырей в бронх.
— Для диагностики легочных гельминтозов.
5.2.1.3. Исследование окрашенных мазков на пневмоцистоз
Необходимые реактивы и оборудование
1. Для приготовления мазков — муколитики (0,3 %-ный дитиотреитол в 0,02 М ЭДТА, рН = 7,0) или ацетилцистеин, или 4 %-ный р-р NaOH; формалин, спирт.
2. Для окраски мазков по Романовскому-Гимзе — смесь Никифорова; сульфатно-уксусный реагент (45 мл ледяной уксусной кислоты и 15 мл концентрированной серной кислоты) — 10 %-ная краска Романовского-Гимзы в фосфатном буфере рН = 7,2.
3. Для окраски мазков толуидиновым синим — толуидиновый синий 0,15 %-ный (75 мг толуидинового синего + 15 мл дистиллированной воды + 0,5 мл концентрированной соляной кислоты + 35 мл абсолютного спирта); водный метиловый желтый 0,25 %-ный.
4. Для окраски по Гомори-Грохотту — формалин 10 %-ный; дистиллированная вода; раствор хромовой кислоты (5 г хромовокислого оксида + 95 мл дистиллированной воды), 1 %-ный раствор метабисульфита калия (или натрия); рабочий раствор серебра (100 мл водного 3 %-ного раствора метенамина или уротропина + 5 мл водного 5 %-ного нитрата серебра) — готовится непосредственно перед употреблением; 5 %-ный водный тетраборат натрия (бура); диметилсульфоксид; раствор хлорного золота 0,2 %-ный; водный раствор тиосульфата соды 2 %-ный; лихтгрюн (0,02 г лихтгрюна + 100 мл дистиллированной воды + 5 капель ледяной уксусной кислоты).
5. Для окраски акридиновым оранжевым — маточный раствор: 100 мл акридина оранжевого растворяют в 100 мл дистиллированной воды, рабочий раствор готовится при разведении маточного раствора враз физиологическим раствором, абсолютный метанол (получают обезвоживанием с помощью окиси кальция с последующей дистилляцией).
— Мокроту или другой материал рекомендуется исследовать немедленно. В исключительных случаях возможно временное сохранение лаважной жидкости с помощью консервации:
а) лаважную жидкость слить в стоящую во льду посуду с 50 мл раствора Хенкса коммерческого, рН = 7,2 — 7,4;
б) лаважную жидкость заморозить до -4 °С.
Подготовка предметных стекол: желательно использовать альбуминизированные стекла.
Приготовление мазков мокроты
— Поместить мокроту в центрифужную пробирку.
— Добавить равное количество муколитика.
— Полученную смесь быстро перемешать.
— Поместить в термостат при температуре 37 °С намин.
— Развести смесью формалина и спирта (1:1).
— Центрифугировать 10 мин при 1500 об/мин.
— Слить надосадочную жидкость.
— Осадок перенести напредметных стекол.
— Осадок нанести на стекло в виде тонкого мазка.
— Мазок высушить на воздухе.
Приготовление мазков лаважной жидкости
— Поместить лаважную жидкость в центрифужную пробирку.
— Добавить равное количество 50°-ного спирта и перемешать.
— Центрифугировать 20 мин при 2500 об/мин.
— Слить надосадочную жидкость.
— Осадок перенести напредметных стекол.
— Осадок нанести на стекло в виде тонкого мазка.
— Мазок высушить на воздухе.
A) Скрининговая окраска по Романовскому-Гимзе
— Высушенный мазок фиксируют в смеси Никифорова в течениемин.
— Опустить мазок в сульфатно-уксусный реагент на 10 мин.
— Промывать проточной водой в течение 5 мин.
— Высушить мазок на воздухе.
— Окрашивать 10 %-ной краской Романовского-Гимзы в течение 30 мин.
Результат: цитоплазма трофозоитов голубоватая, ядро — розовое, внутрицистные тельца имеют фиолетовое ядро.
Б) Окончательная или специфическая окраска толуидиновым синим
— Высушенный мазок фиксируют в 10 %-ном растворе формалина.
— Промыть дистиллированной водой.
— Опустить мазок в сульфатно-уксусный реагент на 5 мин.
— Реагент перемешать стеклянной палочкой.
— Оставить мазок в сульфатно-уксусном реагенте еще на 10 мин.
— Высушить мазок на воздухе.
— Окрашивать 0,15 %-ным толуидиновым синим в течение 3 мин.
— Высушить мазок на воздухе.
— Докрашивать в 0,25 %-ном растворе водного метанилового желтого в течение 2 мин.
Результат: четко дифференцируется стенка пневмоцист, но не дает представления о клеточном содержимом; цисты сине-фиолетовые, тканевые элементы и фон — зелено-желтые.
B) Окончательная или специфическая окраска по Гомори-Грохоту
— Высушенные мазки фиксируют в 10 %-ном растворе формалина в течениемин.
— Промыть дистиллированной водой.
— Быстро подогреть раствор хромовой кислоты в стакане до 65 °С.
— В нагретый раствор быстро погрузить мазки на 1 мин.
— Промыть дистиллированной водой.
— Опустить мазки в 1 %-ный раствор метабисульфита калия на 1 мин.
— Приготовить раствор: 25 мл рабочего раствора серебра + 25 мл дистиллированной воды + 2 мл 5 %-ного водного тетрабората натрия + 15 мл диметилсульфоксида.
— Опустить мазки в приготовленный раствор.
— Подогреть до°С, пока мазки не станут темно-коричневыми, а раствор светло-серым.
— Прополоскать мазки в трех сменах дистиллированной воды.
— Опустить мазки в 0,2 %-ный водный раствор тиосульфата соды на 1 мин.
— Промыть дистиллированной водой.
— Окрашивать лихтгрюном в течение 5 мин.
— Промыть дистиллированной водой.
Результат: цисты светло- или темно-коричневые (цвет зависит от толщины мазка), округлой или чашеобразной формы, окружающий фон и тканевые элементы зелено-желтые.
Г) Окраска акридином оранжевым.
— Высушенные мазки фиксируют в абсолютном метаноле в течение 2 мин.
— Окрасить рабочим раствором акридина оранжевого 10 мин.
— Промыть дистиллированной водой.
— Высушить окрашенные мазки на воздухе.
— Микроскопировать под масляной иммерсией при увеличении: объектив ×90 или ×100, окуляр ×7 или ×10.
— Метод эффективен при условии немедленного исследования материала и использования двух вариантов окрашивания параллельно.
— Метод применяют для диагностики пневмоцистоза.
— Другой материал на пневмоцистоз (слизь из горла и гортани, аспираты из бронхов, биоптаты и мазки-отпечатки легочной ткани) исследуется так же, как и мокрота.
— Всю разовую порцию мочи отстаивать в высоких банках или цилиндрах в течениемин.
— Слить верхнюю часть, оставивмл осадка, который перелить в центрифужные пробирки.
— Оставшуюся часть центрифугировать в течение 5 мин при 1500 об/мин, илимин при 3000 об/мин.
— Слить надосадочную жидкость.
— Осадок перенести пипеткой на предметное стекло.
— Микроскопировать без покровного стекла: объектив ×8 или ×10, окуляр ×10.
— Эффективен при диагностике мочеполового шистосомоза и редко встречаемой инвазии почечных лоханок: диоктофимозе.
— Иногда у девочек и женщин в моче можно обнаружить яйца остриц (смываемые мочой с промежности).
— Чаще применяется как специальный метод диагностики мочеполового шистосомоза.
мл мочи от порции, собранной с 11 ч утра до 15 ч дня, или все порции суточной мочи смешивают с равным количеством детергента — типола.
— Фильтруют под вакуумом через фильтровальную бумагу (или фильтры № 1).
— На увлажненных фильтрах обнаруживают яйца и личинки гельминтов при микроскопии.
— Микроскопируют при увеличении: объектив ×8 или ×10, окуляр ×10.
— Эффективен при слабой шистосомозной инвазии.
— Для диагностики мочеполового шистосомоза.
Необходимые реактивы и оборудование
1. Физиологический раствор
3. Стерильное лезвие бритвы или глазной скальпель
5. Физиологический раствор
6. Предметные и покровные стекла
— Кончиком иглы приподнимают эпидермис кожи и лезвием бритвы или острым глазным скальпелем срезают кусочек кожи диаметроммм (бескровно, соблюдая правила асептики).
— Делают одновременно несколько срезов, главным образом с тех участков, на которых заметны изменения кожи и отмечается зуд (чаще в области гребешков подвздошной кости, боковых поверхностей грудной клетки).
— Помещают в стерильную чашку Петри с физраствором.
— Биоптат эпидермиса кожи помещают на предметное стекло в каплю изотонического раствора хлорида натрия.
— Микроскопируют сразу после приготовления препарата при увеличении: объектив ×8 или ×10, окуляр ×10.
Примечание . Из положительных препаратов можно приготовить постоянные препараты: высушить, зафиксировать метанолом, окрасить по Романовскому-Гимзе.
— Срезы кожи помещают в пробирку с физраствором или средой с коллагеназой и оставляют при температуре°С нач.
— Надосадочную жидкость сливают.
— Осадок переносят на предметное стекло и микроскопируют при увеличении: объектив ×8 или ×10, окуляр ×10.
— Эффективен при диагностике онхоцеркоза, кожного дипеталонематоза (стрептоцеркоза).
— Менее эффективен при кожных поражениях типа линейного дерматита, вызываемых мигрирующими личинками нематод, шистосом и др.
— При диагностике онхоцеркоза, кожного дипеталонематоза (стрептоцеркоза).
Материал на исследование: поперечно-полосатая мышечная ткань, кроме мышцы сердца.
1. Стеклянный компрессорий или предметные стекла (размером 12×6 или 15×8 см)
2. Стереоскопический микроскоп МБС
7.1.1. Компрессорная трихинеллоскопия
— Каждую пробу мышц перед исследованием помещают в чашки Петри, расположенные на эмалированных кюветах, куда помещают и необходимый инструментарий (ножницы, пинцеты, препаровальные иглы), предметные стекла. Работа проводится в перчатках с соблюдением правил техники безопасности.
— Из каждой пробы мышц (от одного больного) ножницами делают срезы строго вдоль мышечных волокон, величиной с «овсяное зерно». Всего из разных участков пробы делают 24 среза, а при отрицательных результатах враза больше.
— Каждый срез помещают на отдельный квадрат нижнего стекла компрессория (всего в компрессории 24 квадрата) и сдавливают верхним стеклом, путем завинчивания закрепляющих винтов компрессория. При отсутствии компрессория срезы помещают на большое предметное стекло, причем на значительном расстоянии друг от друга, чтобы во время сдавливания они не сливались. Накрывают сверху покровным стеклом меньших размеров и сдавливают до толщины папиросной бумаги.
— Микроскопируют все срезы (каждый срез в отдельности) применяя стереоскопический микроскоп МБС с увеличением: объектив ×2 или ×4, окуляр ×12; ×14; ×14,5.
— При обнаружении в мышцах хотя бы одной личинки трихинелл все пробы мышц утилизируют, перед этим засыпаются или заливаются дезинфектантами: 10 %-ным раствором лизола А, сухой хлорной известью или белильной термостойкой известью, или применяют водяной насыщенный пар под давлением 1,5 кГс/см 2 (0,15 МПа) 126 +- 2 °С. Инструментарий и лабораторная посуда обезвреживается кипячением в течение 60 мин (с момента закипания), или автоклавируются (при вышеуказанном режиме).
Диагностика личинок трихинелл бывает затруднена, если срезы толстые или кусочки мышц подсохли, или в срезах обильные включения жира, или пробы мышц фиксированы формалином, или личинки находятся в обызвествленных капсулах.
— можно поместить срезы мышц в 5 %-ный раствор едкой щелочи и выдержать в течение 1 ч при комнатной температуре или 10 мин в термостате при температуре 45 °С;
— срезы с обызвествленными капсулами, где личинки не видны, помещают предварительно в%-ный раствор соляной кислоты нач, чтобы растворить известь, затем помещают в глицерин или молочную кислоту для просветления.
Результат микроскопирования: инкапсулированная личинка трихинелл в мышцах представляет собой капсулу личинки лимоновидной или овальной формы; размеры 0,5 — 0,7×0,2 — 0,3 мм; внутри капсулы одна, реже две или три спиралевидно свернутых личинки. При бескапсульном варианте обнаруживаются только спиралевидно свернутые личинки (см. приложение 5).
7.1.2. Трихинеллоскопия методом переваривания в искусственном желудочном соке
— Соляная кислота концентрированная (или 1 %-ная для 2-го варианта прописи)
— Медицинский пепсин кристаллический (или 3 %-ный для 2-го варианта прописи)
— Мышечную ткань измельчают до состояния фарша.
— Готовят раствор искусственного желудочного сока по одной из прописей:
1) 1 л дистиллированной воды + 7 мл 1 %-ного раствора соляной кислоты + 5 мл 3 %-ного раствора пепсина;
2) 1 л дистиллированной воды + 7 мл концентрированной соляной кислоты +г пепсина кристаллического.
— Количество искусственного желудочного сока на мышечную массу рассчитывается из расчета: на 10 частей искусственного желудочного сока — 1 часть мышечной массы (например: на 100 мл желудочного сока — 10 г мышечного фарша).
— В химический стакан с желудочным соком помещают мышечную массу и тщательно размешивают.
— Помещают в термостат при температуре 37 °С нач, периодически помешивая стеклянной палочкой.
— После переваривания всю массу помещают в аппарат Бермана, на сито из мельничного газа (№ 26).
— Через 1,5 — 2 ч все личинки оседают на дно пробирки, пробирку снимают, отсасывают верхний надосадочный слой пипеткой.
Осадок переносят в чашку Петри или предметные стекла и микроскопируют под стереоскопическим микроскопом МБС, увеличение: объектив ×2 или ×4, окуляр ×12 или ×14.
При использовании 2-го варианта прописи желудочного сока реакция ускоряется и ход проведения методики меняется.
— Фарш помещают в пробирку с желудочным соком (в соотношении 1:25 или 1:50) и ставят в термостат при температуре°С на 3,5 ч.
— Личинки осаждают в химическом стаканчике емкостью 50 мл в течениемин.
— Надосадочную жидкость сливают.
— Осадок микроскопируют в чашке Петри с использованием стереоскопического микроскопа МБС, увеличение: окуляр ×12, ×14, ×14,5; объектив ×2, ×4.
— Непереваренные мышечные волокна можно окрасить 0,25 %-ным раствором бриллиантового зеленого, в результате хорошо видны недекапсулированные личинки трихинелл.
— Метод компрессионной трихинеллоскопии эффективен при высокой и средней интенсивности трихинеллезной инвазии.
— Для повышения эффективности обнаружения личинок трихинелл следует увеличить количество исследуемых мышечных срезов враза, т.е. вместо 24 исследоватьсрезов.
— При низкой интенсивности инвазии более эффективен метод переваривания в искусственном желудочном соке.
Применяется как метод прямой диагностики для обнаружения личинок трихинелл в мышечной ткани.
Материал на исследование: костный мозг, язвенный краевой инфильтрат, содержимое кожных бугорков.
Отбор материала на исследование
— Бугорок или участок инфильтрата протирают ватным спиртовым тампоном.
— Стерильным скальпелем делают поверхностный надрез кожи (при этом сдавливают пальцами бугорок для обескровливания).
— Со дна и краев надреза этим же скальпелем берется соскоб пораженной ткани (в случае появления крови при разрезе, ее удаляют стерильным марлевым тампоном).
— Соскоб со скальпеля быстро перенести на предметное стекло и равномерно растереть (готовят несколько мазков).
— Приготовленный мазок высушить на воздухе.
— Фиксировать метанолом или в смеси Никифорова.
— Окрашивать по Романовскому (как мазки крови на малярию).
— Микроскопировать с масляной иммерсией: объектив ×90 или ×100; окуляр ×7 или ×10.
1) Лейшмании обнаруживаются в макрофагах, а также вне клеток в виде округлых, овальных или удлиненных телец размероммкм; цитоплазма лейшманий светло-голубого или синеватого цвета, ядра — красно-фиолетовые; кинетопласт — окрашен интенсивнее ядра.
2) В правильно приготовленном препарате хорошо различимы клетки инфильтрата (макрофаги, эндотелиальные, плазматические, лимфоидные клетки, фибробласты и небольшая примесь клеток периферической крови).
— Наличие в препарате эпителиальных клеток, а также бесструктурных глыбок, окрашивающихся в равномерно сиреневый цвет, означает, что соскоб был взят слишком поверхностно и должен быть повторен.
— Лейшмании легко обнаруживаются в бугорках и в краевом инфильтрате язвы на начальных стадиях изъязвления; в гнойном отделяемом язвы могут быть обнаружены лишь деформированные и разрушающиеся лейшмании (по которым трудно поставить диагноз); на стадии заживления в пораженных тканях лейшмании обнаруживаются редко; при туберкулоидном лейшманиозе в бугорках обнаруживаются с трудом.
— Для диагностики кожного лейшманиоза.
— Материал, полученный при пункции костного мозга, немедленно после взятия переносят на предметное стекло.
— Очень осторожно, чтобы не деформировать клетки, распределить при помощи шлифовального стекла тонким слоем.
— Если пунктат плотный, то мазок можно сделать по принципу «отпечатков», держа комочек пунктата пинцетом или иглой, или прикасаясь к нему предметным стеклом.
— Мазок высушить на воздухе.
— Фиксировать: в абсолютном этиловом спирте или в смеси Никифорова 30 мин, или в метиловом спирте 5 мин.
— Окрашивать краской по Романовскому (рабочий раствор готовится непосредственно перед окраской и на буферном растворе рН = 6,9 — 7,1)мин.
— Промыть дистиллированной водой.
— Микроскопировать с масляной иммерсией: объектив ×90 или ×100, окуляр ×7 или ×10.
Результат: лейшмании обнаруживаются в макрофагах или внеклеточно; они имеют вид округлых, овальных или рисовидных телец диаметроммкм; цитоплазма окрашена в серовато-голубой цвет, ядро в красно-фиолетовый; в цитоплазме имеется кинетопласт в виде округлого или палочковидного образования и окрашивается более интенсивно, чем ядро. Иногда принимают за лейшмании кровяные пластинки или «осколки» клеток (комочки цитоплазмы, содержащие ядерное вещество). В редких случаях источником ошибки при микроскопии могут служить посторонние микроорганизмы (дрожжевые грибки, одноклеточные водоросли), которые могут попасть со стенок посуды — в мазке они окрашиваются более интенсивно (темно-синяя цитоплазма, ярко-малиновое ядро) и кинетопласт отсутствует.
— Для диагностики висцерального (внутреннего) лейшманиоза.
Примечание. При висцеральном лейшманиозе есть вероятность обнаружения паразитов и в периферической крови; в отдельных случаях для диагностики висцерального лейшманиоза исследуют пунктаты селезенки, печени и лимфатических узлов.
9. Особенности техники микроскопирования при исследовании на яйца, личинки гельминтов и цисты простейших
1. Важным условием успешного микроскопирования является регулирование света с помощью конденсора и других приспособлений светорегуляции: например, полностью опущенный конденсор обеспечивает максимальную контрастность, полностью поднятый конденсор обеспечивает максимальную яркость изображения. При исследовании на яйца гельминтов желательна большая контрастность, при исследованиях на простейшие необходимо обеспечить достаточную яркость изображения.
2. Поле зрения микроскопа при малом увеличении не должно быть слишком ярким (конденсор опустить вниз или уменьшить освещение), т.к. яйца гельминтов с прозрачной оболочкой могут остаться незамеченными. Это касается и простейших.
3. Во время просмотра препаратов при малом увеличении конденсор микроскопа опускают вниз, что уменьшает освещенность поля зрения и повышает четкость исследуемого материала. Переводя объектив на большое увеличение (×40), конденсор поднимают, что усиливает освещенность поля зрения.
4. Яйца и личинки в препарате могут находиться внизу, на поверхности и в толще капли (мазка), поэтому препарат просматривают по вертикали на всех уровнях. При этом очень важно отработать определенный автоматизм: одной рукой фиксировать и передвигать предметное стекло, а другой постоянно, плавно вращать винт макро- и микронаводки то в одну, то в другую сторону, чтобы исследовать всю толщину препарата.
5. Начинают исследовать препарат с правого или левого края предметного стекла, зигзагообразно, как при исследовании мазка крови, при этом препарат перемещают на одно поле зрения. Микропрепарат просматривают полностью, даже если были находки уже в первых полях зрения, т.к. может быть смешанная инвазия.
6. При гельминтоовоскопии лучше использовать объектив ×8, ×10 и ×40, окуляр ×7 и ×10 (поиск яиц ведется при малом увеличении, морфологическое строение и идентификация проводятся при большом увеличении); при протозооскопии работают с объективом ×40 и окуляром ×10.
7. При работе с микроскопом «БИОЛАМ» лучше пользоваться дневным естественным освещением или светом от ламп дневного освещения (настенных, настольных). В микроскопах «БИМАМ» (или импортных марок типа «Leica», «Zeiss») используется свет от вмонтированного электрического осветителя, при этом матовое стекло должно быть вставлено перед конденсором микроскопа.
8. Лаборанту начинать микроскопировать необходимо на микроскопе одной и той же марки, где он изучает не только морфологическое строение яиц гельминтов, но и учится визуально без измерительных приборов соизмерять величину обнаруженных объектов (яиц гельминтов, цист простейших и т.д.). При использовании одних и тех же увеличений микроскопы разных марок (разных фирм-производителей) дают разные размеры объектов, что может привести к диагностическим ошибкам.
9. Для исследования на личинки гельминтов можно использовать микроскоп стереоскопический системы МБС (увеличения: объектив ×12, ×14, окуляр ×2).
10. При идентификации яиц и личинок гельминтов, а также протозойных объектов можно использовать микрометрический метод диагностики. Измерения яиц гельминтов под микроскопом можно проводить с помощью окуляр-микрометра, но предварительно для каждого микроскопа и для тех увеличений, с которыми работает исследователь, нужно определить значение одного деления окулярной линейки в микронах.
10. Микрометрический метод протозоо- и гельминтоскопии
1. Микроскоп с необходимым набором окуляров и объективов
2. Окуляр-микрометр со шкалой, разделенной на миллиметровые интервалы с дополнительными делениями — штрихами
3. Объект-микрометр (линейка на стекле длиной 1 мм, значение величины одного деления 0,01 мм или 10 мкм)
Определить до начала наблюдения значение цены одного деления шкалы окуляр-микрометра для каждой применяемой комбинации объектив-окуляр*.
— Поместить объект-микрометр на предметный столик микроскопа и сфокусировать окуляр на линейке объект-микрометра так, чтобы шкала делений стала резкой.
— Заменить простой окуляр на окуляр-микрометр, с которым предстоит выполнять измерения объекта, и удостовериться, что деление линеек окуляра и объект-микрометра расположены в одной плоскости.
— При малом увеличении объектива совместить шкалы линеек окуляр-микрометра и объект-микрометра параллельно друг под другом.
— Выделить (найти) такое положение линеек, где определенное число делений окуляр-микрометра полностью совпадает с целым числом делений объект-микрометра.
— Определить цену одного деления окуляр-микрометра: число интервалов на линейке объект-микрометра (У), строго соответствующих целому числу делений окуляр-микрометра, умножить на 10 мкм и затем разделить на число совпадающих делений шкалы окуляр-микрометра (X), т.е. цена одного деления шкалы окуляр-микрометра в данной оптической системе определяется по формуле (10×У:X).
— Аналогичным образом определить цену деления шкалы окуляр-микрометра для всех объективов микроскопа, с которыми предполагается проводить микрометрические исследования.
— При особо ответственных исследованиях проверять цену деления окуляр-микрометра при смене объективов даже в пределах одного типа.
* Следует помнить, что величина деления окуляр-микрометра меняется в зависимости от длины тубуса и увеличения окуляра и объектива используемого микроскопа.
— Выбрать соответствующий окуляр и объектив для работы**.
— Сфокусировать систему объектив — окуляр на объекте, который должен быть измерен.
— Заменить простой окуляр на окуляр-микрометр.
— Определить число делений (интервалов) шкалы окуляр-микрометра, покрывающих длину и (или) ширину измеряемого объекта.
Определить действительный размер объекта путем умножения полученного числа на значение цены деления шкалы окуляр-микрометра при данной системе объектива и окуляра.
** Измерение протозойных объектов, также как и яиц гельминтов, для получения более точных данных следует проводить при увеличении в раз.
Примечание . Во избежание необходимости при каждом измерении умножать полученное число на значение цены одного деления окуляр-микрометра можно заранее составить таблицу, в которой вычислены значения 1, 2, 3 и т.д. делений окуляр-микрометра.
Метод позволяет осуществлять проведение прямых измерений величины объекта, не требует сложных расчетов, дорогой аппаратуры, доступен для лабораторий разного уровня.
— Для уточнения видовой принадлежности паразитарных объектов на основе размера — одного из основных морфофункциональных критериев видовой характеристики паразита.
— Дифференциальная диагностика псевдопаразитарных образований.
Материал для исследования
Применяется для диагностики заболеваний
толстый мазок по Като и Миура
описторхоз, клонорхоз, фасциолез, дикроцелиоз, метагонимоз, нанофиетоз, дифиллоботриоз, гименолепидоз, аскаридоз, трихоцефалез, анкилостомидозы, дипилидиоз
описторхоз, клонорхоз, фасциолез, дикроцелиоз, метагонимоз, нанофиетоз, дифиллоботриоз, гименолепидоз, аскаридоз, трихоцефалез, анкилостомидозы, стронгилоидоз, трихостронгилез, некатороз, шистосомоз, кишечные протозоозы (лямблиоз, криптоспоридиоз, изоспороз)
аскаридоз, трихоцефалез, анкилостомидозы, трихостронгилез, некатороз, гименолепидоз, дифиллоботриоз, тениидозы
Бермана и его модификации
стронгилоидоз, трихостронгилез, анкилостомидоз, некатороз, балантидиаз
нативный мазок с физраствором и раствором Люголя
лямблиоз, балантидиаз, амебиаз, инфекции вызванные диентамебой, бластоцистоз
окрашенный мазок по Романовскому и др.
Торгушина, Кеворковой, Грэхэм, Рабиновича
тениаринхоз, тениоз, энтеробиоз
описторхоз, клонорхоз, фасциолез, дикроцелиоз, стронгилоидоз, трихостронгилез, анкилостомидоз, некатороз, лямблиоз, изоспороз, криптоспоридиоз
микроскопия окрашенных мазков по Цилю-Нильсену и др.
микроскопия окрашенных «тонких» мазков
малярия, филяриитозы, трипаносомозы
микроскопия «толстой» капли
Послеоперационный материал, пунктаты, срезы кожи и патматериал
личиночные стадии: эхинококкозы, трихинеллез, цистицеркоз, филяриетозы, амебиаз, балантидиаз
Спинно-мозговая жидкость, костный мозг
Биопсированная поперечно-полосатая мускулатура
Информативность серологических методов* исследования на паразитарные заболевания
описторхоз, клонорхоз, фасциолез, эхинококкоз, альвеококкоз, цистицеркоз, трихинеллез, токсокароз, криптоспоридиоз, пневмоцистоз, лямблиоз, амебиаз
описторхоз, эхинококкоз, альвеококкоз, трихинеллез, амебиаз
* Серологические методы относятся к косвенным методам исследования, которые направлены на определение антител или антигенов в сыворотке крови или фекалиях, поэтому в данные методические указания не вошли. Следует при использовании тест-систем и диагностикумов для определения паразитарных заболеваний руководствоваться инструкциями к их применению, утвержденными Минздравом России.
Возбудители гельминтозов и протозоозов относятся к «патогенным биологическим агентам» (ПБА) III и IV групп патогенности, что определяет режим работы паразитологических лабораторий (подразделений), выполняющих диагностические, производственные или экспериментальные работы с патогенными биологическими агентами.
1.1. Паразитологические исследования биологического материала от людей на паразитарные заболевания, санитарно-паразитологические исследования объектов внешней среды и пищевых продуктов на цисты патогенных простейших, яйца и личиночные формы гельминтов проводятся в лабораториях (подразделениях), лицензированных или аккредитованных в установленном порядке на данный вид деятельности.
1.2. При отсутствии аккредитации и лицензии паразитологические исследования проводятся по договорам с лабораториями других организаций и учреждений, аккредитованными в установленном порядке.
1.3. Для проведения лабораторных паразитологических исследований допускаются метрологически аттестованные методики, соответствующие НТД, ГОСТам, а также методики, утвержденные или допущенные к применению Госстандартом России, Минздравом и госсанэпидслужбой России.
1.4. Отбор проб для паразитологических исследований проводится в соответствии с требованиями государственных стандартов; методических указаний, утвержденных Департаментом госсанэпиднадзора Минздрава России.
1.5. Работа с возбудителями III — IV групп патогенности и биологическим материалом (кровь, другие жидкости и экскреты организма), подозрительным на содержание патогенных простейших, гельминтов и их личинок проводится только в лабораториях, имеющих разрешение, выданное в установленном порядке Комиссией за соблюдением требований биологической безопасности центров Госсанэпиднадзора административных территорий сроком до 5 лет.
2. Основные требования к размещению, набору помещений, оборудованию паразитологических лабораторий
2.1. Паразитологическая лаборатория может быть расположена в отдельно стоящем здании или специально приспособленной части здания. Допускается размещение на первом этаже в изолированной части жилого здания с отдельным входом.
2.2. Должно быть два входа: для сотрудников и для доставки материала на исследование, но допускается и наличие одного входа при условии передачи материала через передаточное окно.
2.3. Лаборатории должны размещаться в хорошо освещенных комнатах. Не допускается размещение в цокольных и подвальных этажах. На первом этаже нельзя размещать, если имеется затемнение перед окнами деревьями или постройками. При ориентации окон рабочих комнат на юг необходимо обеспечить защиту рабочих столов и оптики от прямого попадания солнечного света путем использования жалюзи из материала, устойчивого к дезинфицирущим средствам.
2.4. Лаборатория должна иметь вентиляцию, канализацию, отопление, водопровод, искусственное и естественное освещение (в соответствии с действующими нормативными документами).
2.5. Площадь рабочей комнаты принимается из расчета на бригаду (не менее 2 рабочих мест) и оборудование, т.е. не менеем 2 .
2.6. Лаборатория должна иметь набор рабочих комнат, в соответствии с производственной мощностью и номенклатурой исследований. Выделяются отдельные лабораторные комнаты для работы с биологическим материалом, для санитарно- паразитологических исследований и серологических исследований.
В отдельных случаях допускается совмещение в одной лабораторной комнате исследований биологического материала и санитарно-паразитологических исследований, но при условии организации рабочих мест на каждый вид исследований и соблюдения норм площади на каждое рабочее место. А также разделение движения инвазионного и чистого материала во времени.
2.7. В лаборатории должна обеспечиваться «поточность», т.е. деление на «чистую» (врачебная, гардероб, кладовая, комната приема пищи и другие подсобные помещения) и «заразную» (приема материала, подготовки проб, моечная, стерилизационная или автоклавная для обеззараживания, термостатная, комнаты для проведения исследований) половины.
2.8. Если паразитологическая лаборатория размещена отдельно, то моечная может быть совмещена со стерилизационной и комнатой пробоподготовки.
2.9. Комнаты пробоподготовки, приготовления химреактивов, варки солевых растворов должны быть оборудованы вытяжной вентиляцией (приточно-вытяжного, или вытяжного типа через общую вытяжную сеть или индивидуально через окно, с выводной трубой выше здания). Вследствие использования при выполнении методик летучих и легко воспламеняющихся веществ (эфир, кислоты и т.п.) не разрешается совмещение вентиляции паразитологических лабораторий с лабораториями, где используется обжиг или муфельные печи.
2.10. При размещении в одном блоке нескольких профильных лабораторий общими для них могут быть: гардеробная, комната приема материала, моечная, стерилизационная, автоклавная, врачебные комнаты, комната приема пищи и другие подсобные помещения. При этом площадь помещений должна быть увеличена. Например: нормы моечной комнаты в баклаборатории 12 м 2 (СНиП), а при совмещении с моечной паразитологической лаборатории площадь увеличивается на 8 м 2 и составит 20 м 2 .
2.11. Лабораторные комнаты оборудуются раковинами для мытья рук, в моечной — для мытья посуды.
2.12. Стены облицовывают на 1,5 метра от пола кафельной плиткой или другими современными строительными материалами, которые поддаются мойке и дезинфекции, или окрашиваются масляной краской.
2.13. Полы покрываются линолеумом, релином или плиткой для пола (не должны быть скользкими).
2.14. Лабораторные столы используются с пластиковым покрытием или другим покрытием, легко поддающимся дезинфекционной обработке.
3. Режим и правила работы с инвазионным материалом
3.1. Работу с ПБА III — IV групп патогенности выполняют специалисты с высшим и средним специальным образованием, прошедшие специализацию по лабораторной диагностике гельминтозов и протозоозов. Для центров госсанэпиднадзора и некоторых ведомственных (производственных) лабораторий необходима специализация по санитарно-паразитологическим исследованиям пищевых продуктов и объектов окружающей среды.
3.2. Персонал лаборатории допускается к работе после проведения инструктажа по соблюдению требований биологической безопасности.
3.3. Приборы, оборудование и средства измерения в лаборатории должны быть аттестованы, технически исправны, проходить метрологический контроль в установленные сроки и иметь технический паспорт. Количество оборудования в лаборатории определяется объемами и характером проводимых и планируемых (согласно номенклатуре) паразитологических исследований.
3.4. Обеззараживание материала и дезинфекция помещений.
3.4.1. Банки с фекалиями, желчью, мокротой и т.п. помещают в эмалированные кюветы или на отдельные столы стационарные или передвижные (с пластиковым или другим легко поддающимся дезинфекции покрытием).
3.4.2. Пробирки с кровью устанавливают в штативы, помещенные в эмалированные, пластиковые кюветы.
3.4.3. При отсутствии пластикового покрытия на столах для микроскопии используют легко поддающиеся дезинфекции стеклянные, металлические, пластиковые пластины или эмалированные кюветы, где раскладывают мазки, препараты, материал для исследования.
3.4.4. Отработанные предметные стекла, пипетки, пробки, пробирки, стеклянные палочки, химические стаканчики и т.п. складывают в течение рабочего дня в емкости с дезинфицирующим раствором до полного вертикального погружения (отечественные: 10 %-ный хлорамин, «Велтолен», «Аламинаг», или импортные дезсредства типа «Септодор», «Дианокс», «Виркон» и т.д., допущенные к применению в установленном порядке) для предварительного обеззараживания.
3.4.5. Заключительное обеззараживание лабораторной посуды проводится путем кипячения в воде (с момента закипания не менее 30 мин) с добавлением хозяйственного мыла или жидкого моющего средства. При соответствующих условиях можно использовать автоклавирование. После дезинфекции посуда допускается для мытья и стерилизации.
3.4.6. Ватно-марлевый материал, бумажные фильтры и разовые деревянные палочки уничтожаются путем сжигания или выброса в контейнер для мусора после экспозиции в одном из дезинфицирующих растворов, или предварительно засыпаются сухим порошком хлорной извести или хлорамина.
3.4.7. Пробы фекалий, мокроты, желчи, мочи засыпаются сухой хлорной известью или белильной термостойкой известью, или хлорамином перед выбросом в контейнеры или сливом в общую канализационную систему (при соответствующих условиях для обезвреживания используют автоклавирование).
3.4.8. Полистироловые планшеты, наконечники, микропробирки, пробирки, пипетки и др., используемые при работе с кровью или сывороткой крови, обеззараживаются в 6 %-ном растворе перекиси водорода с экспозицией 3 ч в термостате при 50 °С. После этого промывают под проточной водой, затем промываютмин в дистиллированной воде и высушивают в термостате при 50 °С в течение 15 мин.
3.4.9. Сгустки крови и сыворотку крови перед утилизацией в общую канализационную сеть обезвреживают только с применением дезинфицирующих растворов (в соответствии с действующими инструкциями по обеззараживанию).
3.4.10. Рабочие поверхности лабораторных столов обеззараживают 70 %-ным спиртом, с последующим фламбированием.
3.4.11. Дезинфекционная обработка оборудования (центрифуги, микроскопы, холодильники и др.) проводится раствором 70 %-ного спирта или с применением соответствующих дезсредств.
3.4.12. Дезинфекция халатов и полотенец проводится методом кипячения.
3.4.13. Текущая уборка лабораторных помещений проводится ежедневно после окончания рабочего дня влажным способом с применением дезинфицирующих средств, в «чистой» зоне — с применением моющих средств.
3.4.14. Для мусора используются ведра с педальным приспособлением для поднятия крышек и разовые полиэтиленовые пакеты для мусора.
3.4.15. Для дезинфекции воздуха лабораторного помещения и поверхностей используются бактерицидные лампы или аэрозольные дезинфицирующие вещества.
— работа с фекалиями, желчью, мокротой, кровью и другим биологическим материалом от людей проводится обязательно в резиновых перчатках, особенно в период подготовки материала и проведения методик;
— обработка рук после работы с инвазионным материалом заключается в предварительном мытье рук с мылом под проточной водой, затем обработка ватным тампоном с 70 %-ным спиртом (можно использовать дезсредства для гигиенической и хирургической обработки рук, например: «Велтосепт», «Асептинол С» и т.п.);
— при длительной микроскопии лаборанту для профилактики утомляемости глаз необходимо делать зарядку: попеременно прикрывая рукой (руки перед этим тщательно вымыть!) один глаз, при этом другим смотреть вдаль — на деревья, строения, дома; прикрыть глаза, положить пальцы рук на веки и слегка надавить, преодолевая сопротивление пальцев, посмотреть вверх, вниз, направо и налево (повторить дораз); быстро, быстро поморгать; потянуться нижней губой к носу для лучшего оттока венозной крови из глаз; очень мягко, осторожно подушечками пальцев круговыми движениями помассируйте глазные яблоки через веки, дотроньтесь до слезных косточек у переносицы и помассируйте, как будто моете, переместите пальцы к наружным уголкам глаз и «промойте» их тоже; посидите так около минуты; сожмите кулаки, напрягите плечи, руки, потянитесь всем телом, отряхнитесь и снова можно приступить к микроскопированию (работа на микроскопе должна у лаборанта занимать не более 60 % рабочего времени в день);
— перед выходом из лабораторного помещения снимать лабораторные халаты; иметь шкафы для халатов, сменной обуви и хранить отдельно от личной одежды.
Соблюдение правил дезинфекции, техники безопасности при работе с инвазионным и подозрительным на содержание возбудителей паразитарных болезней материалом как части противоэпидемического режима лабораторий, обязательно для всех сотрудников лаборатории. Текущий контроль за выполнением требований техники безопасности осуществляет руководитель лаборатории.
Главный государственный санитарный врач
Первый заместитель Министра здравоохранения
источник