Несоответствие воды микробиологическим нормам, так же как и химическим, делает ее непригодной для питья. Если Ваш источник водоснабжения не защищен от прямого воздействия окружающей среды или коммунальные системы устарели или давно не чистились, то сделать микробиологический анализ воды просто необходимо. От этого зависит Ваше здоровье и безопасность! Особенно это важно для тех, кто пользуется колодцем. Колодезная вода – грунтовая, она на прямую контактирует с почвами, а значит, грозит «напоить» Вас и нитратами, и тяжелыми металлами, и аммиаком, и, конечно, вредными органическими веществами, которые попадают в почву в результате деятельности сельскохозяйственных ферм или угодий.
В таблице 1 представлены микробиологические показатели действующего норматива СанПиН 2.1.4.1074-01 для питьевой воды:
Таблица 1. Микробиологические нормативы для питьевой воды
| Показатель | Норматив СанПиН 2.1.4.1074-01 |
|---|---|
| Общая микробная численность | Не более 50 КОЕ в 1 мл |
| Общие колиформные бактерии | Отсутствие в 100 мл |
| Термотолерантные колиформные бактерии | Отсутствие в 100 мл |
| Колифаги | Отсутствие в 100 мл |
| Споры сульфитредуцирующих бактерий | Отсутствие в 20 мл |
Стандартный микробиологический анализ питьевой воды в МГУ включает определение трех показателей: общего микробного числа, количества общих колиформных и термотолерантных колиформных бактерий.
Расширенный микробиологический анализ воды включает анализ пяти показателей: общего микробного числа, количества общих колиформных бактерий, количества термотолерантных колиформных бактерий, титр колифагов и содержание спор сульфитредуцирующих бактерий.
Часто на наших участках или поблизости имеются водоемы, где мы и наши дети с удовольствием любим провести время. Конечно, вода в данных водоемах не является питьевой, но ее безопасность для человека также, как и питьевая, регламентируется. В таблице 2 представлены микробиологические показатели действующего норматива по гигиеническим требованиям к охране поверхностных вод (СанПиН 2.1.5.980-00)
Таблица 2. Микробиологические нормативы для рекреационного водопользования, а также в черте населенных мест
| Показатель | Норматив СанПиН 2.1.5.980-00 |
|---|---|
| Общие колиформные бактерии | Не более 500 КОЕ в 100 мл |
| Термотолерантные колиформные бактерии | Не более 100 КОЕ в 100 мл |
| Колифаги | Не более 100 БОЕ в 100 мл |
| Возбудители кишечных инфекций (анализ бактерий из сем. Enterobacteriaceae рода Salmonella) | Вода не должна содержать возбудителей кишечных инфекций (полное отсутствие в 1000 мл) |
Микробиологический анализ воды, предназначенной не для питья, включает определение количества двух показателей: общих колиформных и колиформных термотолерантных бактерий.
Помимо двух основных показателей мы предлагаем провести дополнительный анализ на содержание: колифагов, условно-патогенных дрожжей и микромицетов (частых спутников опортунистических заболеваний) и индекса самоочищения водоёма.
При значительном превышении нормативов СанПиН 2.1.5.980-00, а также возможном фекальном загрязнении водоёма, мы предлагаем провести анализ на наличие возбудителей кишечных инфекций (род Salmonella и Enterococcus).
Метод определяет в питьевой воде общее число мезофильных аэробных и факультативно анаэробных микроорганизмов (ОМЧ), способных образовывать колонии на питательном агаре при температуре 37 °С в течение 24 часов, видимые с увеличением в 2 раза. Данный индикатор выявляет потенциальных бактерий, способных причинить вред здоровью человека.
Общие колиформные бактерии (ОКБ) – грамотрицательные, оксидазоотрицательные, не образующие спор палочки, способные расти на дифференциальных лактозных средах, ферментирующие лактозу до кислоты, альдегида и газа при температуре (37+1) °С в течение (24-48) часов. Многие представители данной группы являются микроорганизмами нормальной микрофлоры желудка, поэтому превышение данной группы микроорганизмов может говорить о возможно антропогенном (в том числе и фекальном) загрязнении воды.
Термотолерантные колиформные бактерии (ТКБ) входят в число общих колиформных бактерий, обладают всеми их признаками и, кроме того, способны ферментировать лактозу до кислоты, альдегида и газа при температуре (44±0,5) °С в течение 24 часов. Также, как и ОКБ являются индикаторной группой, однако более устойчивые в окружающей среде: вот почему обнаружение данной группы микроорганизмов в воде может говорить об однозначном загрязнении ее продуктами жизнедеятельности человека.
Колифаги, определяемые стандартным методом (МУК 4.2.1018-01), являются вирусами кишечной палочки (Escherichia coli) и рассматриваются эпидемиологами как дополнительный, а порой и более чувствительный, метод в определении загрязнения воды микроорганизмами группы кишечной палочки. Вирусные частицы, и в частности колифаги, более устойчивы к окружающей среде, чем их бактерии-хозяева. В связи с этим, наличие колифагов может служить достоверной меткой о более давнем фекальном загрязнении источника воды. Показана прямая корреляция между содержанием колифагов в воде и опасных для человека энтеровирусов, поэтому наличие колифагов в воде может говорить о вирусном заражении источника. Действующий нормативный документ (СанПиН 2.1.4.1074-01) подразумевает отсутствие колифагов в 100 мл воды.
Сульфитредуцирующие клостридии – спорообразующие анаэробные палочковидные микроорганизмы, являющиеся дополнительным микробиологическим показателем фекального загрязнения водоема. В отличие от относительно неустойчивых колиформных и термотолерантных колиформных бактерий, споры клостридий могут сохраняться в водоемах долгое время. Клостридии встречаются в кишечнике человека и домашних животных, однако, при попадании с водой в большом количестве могут вызвать пищевые отравления. К сульфитредуцирующим клостридиям относятся в том числе и опасные для человека клостридии (Clostridiumbotulinum, Clostridium perfringens, Clostridium tetani), вызывающие тяжелейшие заболевания. Согласно действующему нормативу (СанПиН 2.1.4.1074-01) споры клостридий должны отсутствовать в 20 мл воды.
К условно-патогенным дрожжам и микромицетам (плесени) относят большую неоднородную группу грибных организмов, способных сапротрофно расти при 37 °С. В нее входят такие представители, как Candida albicans и Cryptococcus neoformans, которые являются частым фактором оппортунистических заболеваний человека, вызывая кандидозы (грибковые заболевания кожи), молочницы и проч. Другие организмы микромицеты (Cladosporium cladosporioides, Aspergillusniger) могут являться активными сенсебилизаторами аллергических реакций, а иногда и самими аллергенами. В РФ не нормируется вода по плесеням и дрожжевым организмам в воде.
Общее число микроорганизмов не нормируется в воде водоемов в зонах рекреаций, поскольку уровень этой группы микроорганизмов в большей мере зависит от природных особенностей каждого объекта, времени года и т.п.
Однако при выборе нового источника водоснабжения или места рекреации в воде водоёмов дополнительно следует определять общую микробную численность, вырастающую:
- при температуре 37 °С в течение 24 часов;
- при температуре 22 °С в течение 72 часов.
- ОМЧ при 37 °С представлена большей частью алохтонной микрофлорой (внесенную в водоем в результате антропогенного загрязнения, в том числе фекального);
- ОМЧ при 20-22 °С представлена, помимо алохтонной, аборигенной микрофлорой (естественной, свойственной для данного водоёма).
Соотношение численности этих групп микроорганизмов позволяет судить об интенсивности процесса самоочищения. При завершении процесса самоочищения коэффициент ОМЧ 22 °С/ ОМЧ 37 °С. В местах загрязнения хозяйственно-бытовыми сточными водами численные значения обеих групп близки.
Показатель позволяет получить дополнительную информацию о санитарном состоянии водоемов, источниках загрязнения, процессах самоочищения.
источник
Цель занятия.Ознакомить студентов с основными методами и показателями, необходимыми для санитарно-микробиологической оценки объектов внешней среды.
Оборудование и материалы. Прибор для подсчета колоний, колбы с пробами воды, бактериологические пробирки с 9 мл воды, пробирки с 10 мл расплавленного агара, мерные стерильные пипетки на 2 мл, стерильные чашки Петри, чашки Петри с МПА, чашки Петри с кровяным МПА, навески почвы, стерильная водопроводная вода в колбе — 270 мл, пробирки со средой Кесслера, Вильсона—Блера.
Для оценки санитарно-гигиенического состояния объектов окружающей среды проводят санитарно-бактериологические исследования, цель которых состоит в определении эпизоотологической и эпидемиологической безопасности. Показателем неблагополучия служит выявление патогенных микроорганизмов. Однако прямое их обнаружение связано с большими трудностями, и прежде всего с низкой концентрацией данных микробов, которые в основном не могут размножаться в воде, воздухе и почве. Поэтому в санитарно-микробиологической практике используют косвенные методы, направленные на определение микробной обсемененности объекта и обнаружение в нем так называемых санитарно-показательных бактерий. О бактериальной обсемененности судят по микробному числу — общему количеству микроорганизмов, содержащихся в единице объема или массы (1 мл воды, 1 г почвы, 1 м 3 воздуха).
Содержание санитарно-показательных бактерий определяют по двум показателям: титру и индексу. Титром называют минимальный объем или массу, в которых выявляют данные бактерии, индексом — количество санитарно-показательных бактерий, содержащихся в соответствующем количестве среды.
К санитарно-показательным бактериям относят представителей облигатной микрофлоры организма человека и теплокровных животных, для которых среда обитания — кишечник или воздушно-дыхательные пути. Они характеризуются следующими свойствами: 1) постоянно выделяются с калом или капельками слизи из воздушно-дыхательных путей; 2) не имеют других мест обитания; 3) способны сохраняться в окружающей среде то же время, что и патогенные бактерии, паразитирующие в кишечнике или воздушно-дыхательных путях; 4) не способны интенсивно размножаться вне организма хозяина и изменять свои свойства.
Перечисленные признаки присущи бактериям, признанным санитарно-показательными для различных объектов окружающей среды.
Санитарно-показательные бактерии группы кишечных палочек принадлежат к различным родам семейства энтеробактерий.
Обнаружение кишечной палочки в разных объектах окружающей среды считают наиболее достоверным признаком свежего фекального загрязнения. Наличие в этих же объектах бактерий родов Citrobacter и Enterobacter указывает на относительно давнее фекальное загрязнение.
Присутствие С. perfringens, С. sporogenes и других клостридий в почве свидетельствует о ее фекальном загрязнении, причем как свежем, так и давнем, поскольку эти бактерии образуют споры, что позволяет им длительно переживать в окружающей среде (в частности, в почве).
Обнаружение в объектах окружающей среды Streptococcus faecalis также свидетельствует об их фекальном загрязнении. Резкое увеличение количества этих бактерий в саморазогревающемся навозе и компостах может свидетельствовать о загрязнении почвы разлагающимися отбросами.
Гемолитические стрептококки, будучи облигатными обитателями носоглотки и зева, выделяются с капельками слизи орально-капельным путем. Сроки выживания гемолитических стрептококков в окружающей среде практически не отличаются от сроков, характерных для большинства других возбудителей воздушно-капельных инфекций. Обнаружение гемолитических стрептококков в воздухе помещений указывает на возможное его загрязнение микроорганизмами, содержащимися в зеве, носоглотке, верхних дыхательных путях и вызывающими инфекции, передаваемые воздушно-капельным путем.
Staphylococcus aureus — также факультативный обитатель носоглотки и зева. Его присутствие в воздухе помещений служит показателем орально-капельного загрязнения.
Одновременное обнаружение золотистого стафилококка и гемолитических стрептококков свидетельствует о высокой степени загрязнения воздуха.
Санитарно-микробиологическое исследование воды. Вода — естественная среда обитания микробов, которые в большом количестве поступают из почвы, воздуха, с отбросами, стоками. Особенно много микроорганизмов в открытых водоемах и реках. Кроме сапрофитов в воде могут находиться возбудители инфекций животных и человека.
При контроле санитарного состояния воды исследованию подлежат: вода централизованного водоснабжения, колодцев, открытых водоемов (реки, озера), плавательных бассейнов, сточные жидкости.
Отбор проб воды. Из открытых водоемов пробы воды отбирают с глубины 10. 15 см от поверхности и на расстоянии 10. 15 см от дна. Водопроводную воду набирают в стерильные флаконы объемом 0,5 л с притертой пробкой. Предварительно кран обжигают и спускают воду в течение 10. 15 мин. Хлорированную воду перед исследованием нейтрализуют тиосульфатом натрия из расчета 10 мл на 1л воды. Бактериологическое исследование проб воды следует проводить в течение двух часов после отбора или шести часов при температуре хранения 1. 5°С.
Определение микробного числа воды. Водопроводную воду засевают в количестве 1мл, воду открытых водоемов — по 1,0; 0,1; 0,01 мл. Все пробы вносят в стерильные чашки Петри, после чего их заливают 10. 12 мл расплавленного и охлажденного до 40. 45 °С питательного агара, который тщательно перемешивают с водой. Посевы инкубируют при 37 °С в течение 1. 2сут. Воду из открытых водоемов засевают параллельно на две серии чашек, одну из которых инкубируют при 37 ºС в течение суток, другую — 2 сут при 20 °С. Затем подсчитывают количество выросших на поверхности и в глубине колоний и вычисляют микробное число воды — количество микроорганизмов в 1 мл.
Определение коли-титра и коли-индекса воды. Минимальное количество воды в мл, в котором обнаруживают бактерии группы кишечных палочек (БГКП), называют коли-титром воды, количество БГКП, содержащихся в 1л исследуемой воды, называют кол и-и ндексом воды. Коли-титр и коли-индекс воды определяют титрационным (бродильным) методом или методом мембранных фильтров.
Титрационный метод. В глюкозо-пептонную среду (1%-я пептонная вода, 0,5%-й раствор хлорида натрия, 0,5%-й раствор глюкозы, индикатор Андреде и поплавок) проводят посевы различных объемов воды.
Воду открытых водоемов исследуют в объемах 100; 10; 1 и 0,1 мл. Для анализа водопроводной воды делают посевы трех объемов по 100 мл, трех объемов по 10 мл и трех объемов по 1 мл. Посевы инкубируют при 37 °С в течение суток. О брожении судят по образованию пузырьков газа в поплавке. Из забродивших или помутневших проб делают посевы на среду Эндо. Из выросших колоний готовят мазки, окрашивают по Граму и ставят оксидазный тест, с помощью которого дифференцируют бактерии родов Escherichia, Citrobacter и Enterobacter от грамотрицательных бактерий семейства Pseudomonadaceae и других оксидазоположительных бактерий, обитающих в воде. С этой целью 2. 3 изолированные колонии наносят «штрихом» на фильтровальную бумагу, смоченную диметил-n-фенилендиамином. При отрицательном оксидазном тесте цвет бумаги не изменяется, при положительном она окрашивается в синий цвет в течение 1 мин. Грамотрицательные палочки, не образующие оксидазу, вновь исследуют в бродильном тесте — вносят в полужидкий питательный агар с 0,5 % глюкозы и инкубируют при 37 °С в течение суток. При положительном результате определяют коли-титр и коли-индекс по статистической таблице.
Метод мембранных фильтров. Определенный объем воды пропускают под давлением через мембранный фильтр № 3, предварительно стерилизованный кипячением в дистиллированной воде. Водопроводную воду и воду артезианских скважин фильтруют в объеме 333 мл. Чистую воду открытых водоемов фильтруют в объеме 100, 10, 1 и 0,1 мл, более загрязненную воду перед фильтрованием разводят стерильной водой. Фильтры накладывают на агар Эндо в чашки Петри и после инкубации при 37 °С в течение суток подсчитывают количество выросших красных колоний. Из двух-трех колоний делают мазки, окрашивают их по Граму и ставят оксидазный тест. Грамотрицательные палочки, не образующие оксидазу, принадлежат к БГКП. По существующим нормативам (ГОСТ 2874—82) питьевую воду считают качественной, если ее коли-индекс не более 3, а микробное число — не более 100.
Общепринятым дополнительным показателем фекального загрязнения воды служит количество S.faecalis. Для определения его титра цельную воду и ее 10-кратные разведения засевают в жидкую элективную среду (щелочная полимиксиновая среда). После инкубирования при 37 ºС в течение двух суток, а затем еще через сутки и двое суток делают высевы на плотные элективные среды. Фекальные стрептококки идентифицируют по морфологическим, культуральным и тинкториальным свойствам.
Есть данные о корреляции между содержанием в воде фекальных кишечных палочек и фагами бактерий группы кишечных палочек. Поэтому определение данных фагов служит косвенным показателем возможного присутствия кишечных палочек в исследуемой пробе воды.
Санитарно-микробиологическое исследование воздуха. Микрофлора воздуха зависит от микрофлоры почвы и воды. Воздух — неблагоприятная среда для обитания микроорганизмов из-за отсутствия питательных веществ, действия солнечных лучей, высушивания. Наряду с сапрофитами в воздухе могут находиться патогенные бактерии, споры грибов родов Aspergillus, Mucor и др.
Санитарную оценку воздуха осуществляют по двум показателям: 1) определение микробного числа воздуха; 2) определение количества санитарно-показательных бактерий — гемолитических стрептококков и стафилококков.
Количественные микробиологические методы исследования воздуха основаны на принципах осаждения (седиментации), аспирации или фильтрации.
Седиментационный метод осаждения Коха. Чашки Петри с МПА оставляют открытыми на 5. 10 мин. Для определения санитарно-показательных бактерий берут чашки Петри с кровяным МПА и время экспозиции увеличивают до 40 мин. Чашки выдерживают при 37 °С и комнатной температуре 24 ч и подсчитывают выросшие колонии.
Микробное число воздуха (общее количество бактерий в 1 м3) определяют по формуле Омелянского
Х= а * 100 * 1000 * 5 / (b * 10 * T),
где X— количество микробов в 1 м 3 (1000 л) воздуха; а — количество выросших колоний в чашках; b — площадь чашки; Т— время, в течение которого чашка была открыта; 5 — время по правилу Омелянского; 10 — объем воздуха в литрах. (Правило Омелянского предусматривает, что на поверхности агара в чашке Петри площадью 100 см 3 за 5 мин из воздуха оседает такое количество микробов, которое находится в его 10 л.)
Прямое обнаружение патогенных микробов воздуха проводят только при специальных показаниях.
Аспирационный метод. Более точный количественный способ определения микробного числа воздуха, так как посев микроорганизмов из воздуха производят с помощью приборов. При использовании аппарата Кротова воздух с заданной скоростью засасывается через щель плексигласовой пластины и ударяется о поверхность питательной среды открытой чашки Петри, находящейся на вращающейся подставке, благодаря чему происходит равномерный посев бактерий из воздуха на поверхность МПА (при определении микробного числа) или кровяного МПА (при выделении гемолитических стафилококков и стрептококков). После инкубации в термостате в течение двух суток подсчитывают количество выросших колоний и определяют микробное число воздуха. При исследовании воздуха могут быть использованы и другие приборы (Дьякова, Киктенко, ПАБ-1 — прибор аэрозольный бактериологический и ПОВ-1 — прибор для отбора воздуха). В практику входят ускоренные методы индикации микрофлоры воздуха с помощью мембранных фильтров, каскадных им-пакторов, фильтров Петрякова и др.
Санитарно-микробиологическое исследование почвы. Анализ почвы включает в себя определение микробного числа, коли-тит-ра, перфрингенс-титра и титра термофильных бактерий. По эпидемиологическим признакам проводят определение в почве патогенных микроорганизмов: сальмонелл, шигелл, возбудителей столбняка, ботулизма, злокачественного отека, сибирской язвы. Бактериологический анализ почвы нужен при выборе территории под пастбище, ферму, хозяйственные постройки, детские сады, больницы и др.
Предварительно делают отбор проб почвы. На обследуемой территории площадью до 1000 м 3 выделяют два участка по 25 м 3 (один — вблизи источника загрязнения, другой — в отдалении от него), берут пробы из 5 точек (4 — по углам участка, 1 — в центре) на глубине 10. 20 см стерильным совком (из более глубоких мест — с помощью специального бура Некрасова или Френкеля). Пробы почвы по 200. 300 г отбирают в широкогорлые стеклянные банки с ватными пробками (можно все взятые с одного участка пробы перемешать и на исследование направить 1 кг). На банки наклеивают этикетки, отправляют с нарочным и сопроводительным письмом. Пробы почвы полагается исследовать сразу же или в течение 6. 18 ч, сохраняя их при температуре не выше 1. 5ºС.
В лаборатории почву измельчают, освобождают от камней, осколков стекол, корней растений, просеивают через сито, тщательно перемешивают и отвешивают 30 г. В колбу на 500 мл наливают 270 мл стерильной водопроводной воды и вносят в нее отвешенную пробу почвы, все интенсивно встряхивают 10 мин, не давая отстояться частицам суспензии, готовят серию десятикратных последовательных разведений. Для относительно чистых почв достаточно 4 степени разведения, для загрязненных — 6. 9 разведений. В штатив ставят нумерованные пробирки с 9 мл стерильной воды в каждой. В первую вносят 1 мл суспензии пробы почвы, смешивают, затем 1 мл из первой пробирки вносят во вторую, смешивают, из нее — 1 мл в третью и т. д. В результате в пробирке № 1 получается разведение 1 : 100, № 2 — 1 : 1000 и т.д. Подготовленные таким образом пробы почвы исследуют.
Определение общего микробного числа. Из последних 3. 4 пробирок с разведенной суспензией отдельными стерильными пипетками вносят по 1 мл в стерильные чашки Петри (каждое разведение в отдельности). В каждую чашку добавляют еще по 10. 15 мл расплавленного и охлажденного до 45 ºС МПА. Равномерными осторожными круговыми движениями содержимое чашек перемешивают, оставляют на столе для уплотнения (затвердения) агара. С застывшей средой чашки перевертывают вверх дном, надписывают и помещают в термостат для культивирования на 24. 48 ч при 37 °С. Выросшие колонии подсчитывают в каждой чашке, умножают на степень разведения, полученные числа суммируют и вычисляют среднеарифметическое число, что составит количество микробов, содержащихся в 1 г почвы.
Определение коли-титра, перфрингенс-титра и титра термофильных бактерий почвы. Для определения коли-титра почвы различные разведения почвенной взвеси засевают по 1 мл в пробирки со средой Кесслера (на 1л дистиллированной воды — 10г пептона, 50 мл бычьей желчи — 2,5 г лактозы, 4 мл 1%-го водного раствора генцианвиолета) и инкубируют при 43 ºС в течение 48 ч. В дальнейшем исследования проводят по схеме, применяемой при определении коли-титра воды. Наибольшее разведение почвенной суспензии, в котором отмечена ферментация лактозы (газообразование), соответствует коли-титру почвы. Для определения перфрингенс-титра почвы различные разведения почвенной суспензии по 1 мл засевают в пробирки со стерильным обезжиренным молоком или железосульфитной средой Вильсона— Блера, приготовленной ex tempore. Посевы инкубируют при 43 °С в течение 24. 48 ч, после чего учитывают результаты по свертыванию молока или по образованию черных колоний С. perfringens в агаровом столбике среды Вильсона—Блера. Из колоний делают мазки, окрашивают по Граму, микроскопируют и вычисляют перфрингенс-титр, который соответствует наибольшему разведению почвы, вызвавшему почернение и разрыв среды Вильсона— Блера в первые 12 ч роста.
Для определения титра термофильных бактерий разведения почвенной суспензии по 1 мл вносят в чашки Петри, заливают расплавленным и охлажденным агаром. Посевы инкубируют в течение суток при 60 ºС, а затем подсчитывают количество выросших колоний и пересчитывают на 1 г почвы.
Санитарно-микробиологическую оценку почвы проводят по комплексу показателей, из которых наиболее важный ление степени фекального загрязнения.
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОЙ РАБОТЫ
1. Определить микробное загрязнение воздуха.
2. Провести исследование воды с целью установления микробного числа и коли-титра.
3. Определить микробное число и перфрингенс-титр почвы.
1. Что такое санитарно-показательные микроорганизмы?
2. Как определяют коли-титр воды?
3. Как определяют микробное число почвы?
4. Как определяют перфрингенс-титр почвы?
5. Какие методы применяют для определения микробного числа воздуха?
6. Что такое санитарно-показательные микробы воздуха и как их определяют?
источник
Мазок на флору у женщин. Мазок со слизистой влагалища на чистоту — расшифровка результатов, как подготовиться, зачем производят? Нормальные показатели микрофлоры влагалища.
Мазок на флору у женщин – лабораторное исследование, определяющее виды бактерий, которые присутствуют во влагалище. Это самый распространенный и простой метод выявления воспалений и ЗППП (заболеваний, передающихся половым путем).
Исследование абсолютно безболезненное. Оно производится во время обычного гинекологического осмотра. Врач берет материал одноразовым шпателем со стенок влагалища и шейки матки. Содержимое влагалища (влагалищный секрет) наносится на стекло. В лаборатории материал окрашивают, для того, чтобы бактерии стали четко различимы.
- определить состояние микрофлоры влагалища;
- выявить половые инфекции и их возбудителя;
- определить степень воспалительного процесса;
- оценить степень чистоты влагалища, что обязательно перед дальнейшими диагностическими исследованиями и гинекологическими операциями – прижиганием эрозий, удалением полипов, выскабливанием;
- оценить состояние здоровья беременных женщин.
- жалобы на зуд или выделения из влагалища, другие симптомы воспаления;
- профилактические осмотры;
- контроль проведенного лечения;
- прием гормональных препаратов и иммуносупрессоров;
- контроль микрофлоры на фоне длительного приема антибиотиков;
- беременность. Проводится 3 раза за беременность (при постановке на учет, на 30-ой и 36-ой неделе).
Данное исследование имеет множество названий: мазок на флору, общий мазок, бактериоскопия, мазок на чистоту. Существуют также мазки на флору из мочеиспускательного канала и канала шейки матки. Обычно эти три вида мазка проводят совместно.
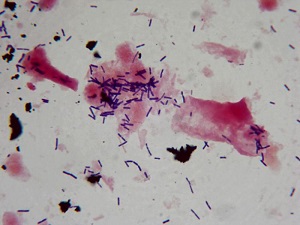
Наиболее многочисленными являются лактобактерии и бифидобактерии, которые прикрепляются к эпителию влагалища. Они вырабатывают спирты, перекись, молочную и другие кислоты, обеспечивающие кислую реакцию влагалищного секрета. А также лизоцим и другие ферменты, сдерживающие размножение других видов бактерий.
| Микроорганизмы | Количество КОЕ/мл |
| Лактобактерии или палочки Додерлейна Lactobacillus spp | 10 7 -10 9 |
| Бифидобактерии Bifidobacterium spp. | 10 3 -10 7 |
| Клостридии Clostridium spp. | До 10 4 |
| Пропионибактерии Propionibacterium spp. | До 10 4 |
| Мобилункус Mobiluncus spp. | До 10 4 |
| Пептострептококки Peptostreptococcus spp | 10 3 -10 4 |
| Коринебактерии Corynebacterium spp. | 10 4 -10 5 |
| Стафилококки Staphylococcus spp. | 10 3 -10 4 |
| Стрептококки Streptococcus spp. | 10 4 -10 5 |
| Энтеробактерии Enterobacteriaceae | 10 3 -10 4 |
| Бактероиды Bacteroides spp. | 10 3 -10 4 |
| Превотеллы Prevotella spp. | До 10 4 |
| Порфиромонады Porphyromonas spp. | До 10 3 |
| Фузобактерии Fusobacterium spp. | До 10 3 |
| Вейлонеллы Veilonella spp. | До 10 3 |
| Микоплазмы M.hominis | До 10 3 |
| Уреаплазмы U.urealyticum | 10 3 |
| Кандиды — дрожжеподобные грибы | 10 4 |
Аббревиатура КОЕ/мл означает – колониеобразующих единиц в 1 мл питательной среды. Каждая колониеобразующая единица – это микроорганизм, из которого может образоваться колония.
Число бактерий выражают в десятичных логарифмах, для того, чтобы не писать числа с большим количеством нолей.
В описании влагалищной микрофлоры часто можно встретить названия грамположительные или грамотрицательные бактерии. Эти термины означают, что первые бактерии окрашиваются по методу, разработанному микробиологом Граммом, а другие при этом не изменяют свою окраску.
Грамположительные палочки в мазке, к которым относятся лактобактерии, являются хорошим признаком. В норме они преобладают у женщин репродуктивного возраста. В период менопаузы (климакса) и постменопаузы на первое место выходят грамотрицательные бактерии.
В зависимости от потребности в кислороде бактерии разделяют на
- аэробные – те, что развиваются при наличии кислорода;
- анаэробные – для жизнедеятельности которых не нужен кислород.
Во влагалище здоровой женщины большинство бактерий анаэробы 10 8 –10 9
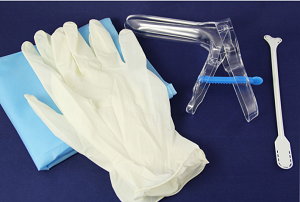
Процедура включает несколько этапов.
- Женщина размещается в гинекологическом кресле.
- Введение стерильных гинекологических зеркал для получения доступа к стенкам влагалища и шейке матки.
- Сбор материала с задней стенки влагалища. Эта процедура абсолютно безболезненна. Неприятные ощущения могут возникнуть льшь при прикосновении шпателя к воспаленному участку.
- Нанесение материала на предметное стекло. Влагалищный секрет распределяют штриховыми движениями по обезжиренному стеклу максимально тонким слоем, чтобы клетки располагались в один ряд и не закрывали друг друга.
- Фиксация мазка необходима, если его доставят в лабораторию более чем через 3 часа. Обработка позволяет избежать деформации клеток при высыхании и дает возможность сохранить препарат.
- Окраска мазка по методу Грама. В качестве красителя используется метиленовый синий. После окрашивания легче установить вид бактерий и определить состав микрофлоры.
- Оценка результата, которая состоит из 3-х частей: подсчет лейкоцитов, видовой состав микрофлоры, оценка чистоты влагалища.
Зачастую мазок берут сразу из трех точек:
- отверстия мочеиспускательного канала и парауретральных ходов (узких каналов, расположенных параллельно уретре);
- стенок влагалища;
- канала шейки матки.
Анатомическая близость этих участков приводит к тому, что инфекции и воспаления протекают взаимосвязано. Для каждого участка используется отдельный стерильный шпатель, щеточку или ватный тампон. Взятый материал наносят на 3 стерильных предметных стекла, отдельно для каждого участка.
Мазок на флору из влагалища абсолютно безвредная процедура, которая разрешена, в том числе и беременным женщинам. Во время забора материала слизистая не травмируется, поэтому после процедуры нет никаких ограничений. Разрешается принимать ванну, плавать, вступать в половые контакты и т.д.
| Степень | Выявленные изменения | О чем говорит |
| I | Среда кислая. Лейкоциты – до 10. Эпителиальные клетки – 5-10. Большинство микроорганизмов – лактобактерии (палочки Дедерлейна). Другие бактерии – единично. Слизь – небольшое количество. | Идеальное состояние микрофлоры влагалища. Крайне редко встречается у женщин детородного возраста, живущих половой жизнью. |
| II | Среда слабокислая. Лейкоциты – до 10. Эпителиальные клетки 5-10. Большинсто – палочки Дедерлейна. Грамположительные кокки в небольшом количестве. Слизь в небольшом количестве. | Нормальное состояние. Встречается у большинства здоровых женщин. |
| III | Среда нейтральная. Лейкоциты – свыше 10. Эпителиальные клетки – свыше 10. Микроорганизмы в умеренном или большом количестве. Присутствуют грамотрицательные и грамотрицательные палочки и кокки. Единичные палочки Дедерлейна. Присутствуют «ключевые» клетки. Слизь – умеренное количество. | Воспаление влагалища – кольпит. Могут возникнуть симптомы: кремообразные выделения из влагалища, зуд, жжение, дискомфорт во время полового акта. У некоторых женщин это состояние протекает бессимптомно. |
| IV | Среда нейтральная или щелочная, рН свыше 4,5. Лейкоциты – свыше 30-ти или все поле зрения. Эпителиальные клетки – в большом количестве. Микроорганизмы в массивном количестве. Микрофлора представлена различными условно-патогенными и болезнетворными микроорганизмами. Палочки Дедерлейна могут отсутствовать. Слизь в большом количестве. | Выраженный воспалительный процесс. Симптомы: обильные выделения из влагалища (белые, желтоватые, зеленоватые), часто с неприятным запахом. Зуд, жжение, сухость, дискомфорт. Неприятные ощущения, боль при половом акте. |
Существует большое количество антибиотиков, но не все они одинаково эффективны по отношению к разным группам бактерий (на вирусы антибиотики не влияют). Случается, что после курса антибиотиков пациентка не выздоровела или болезнь вернулась через несколько дней/недель. Это произошло, потому что для лечения были назначены антибиотики, слабо влияющие на возбудителя болезни.
Для того чтобы лечение было максимально эффективным необходимо определить, какие антибиотики:
- полностью уничтожают бактерию — возбудителя болезни;
- останавливают рост возбудителя;
- не влияют на жизнедеятельность данной бактерии.
На основе проведенного исследования составляется антибиотикограмма. Это перечень антибиотиков, к которым чувствительны бактерии.
После того, как были определены бактерии, вызвавшие болезнь, их распределяют в несколько пробирок с питательными средами. В каждую пробирку добавляют определенный антибиотик. Пробирки помещают в термостат, где созданы оптимальные условия для их размножения.
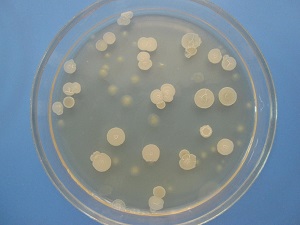
После культивации (около 7 дней) анализируют рост бактерий в пробирках. Там, где бактерии чувствительны к антибиотику, колоний не образуется. Этот препарат оптимальный для лечения пациентки. В пробирку, где добавлены препараты, к которым антибиотики нечувствительны, рост бактерий самый интенсивный. Такие лекарственные средства не могут быть использованы для лечения данного заболевания.
Посев мазка или бактериологический посев (бакпосев) мазка – это лабораторное исследование, при котором содержимое влагалища помещают в питательную среду и создают оптимальные условия для роста бактерий.
Цели исследования:
- определить возбудителя инфекции половых органов;
- установить степень обсемененности – количество бактерий во влагалище;
- контролировать состояние микрофлоры после длительного лечения антибиотиками, цитостатическими препаратами. Проводится через 7-10 дней после отмены препарата.
В каком случае назначают посев мазка?
- всем беременным женщинам при постановке на учет;
- при воспалительных процессах в половых органах;
- в мазке обнаружены грамотрицательные диплококки – для подтверждения гонококковой инфекции (гонореи);
- при вульвовагините рецидивирующем или хроническом.
Как проводится микробиологическое исследование?
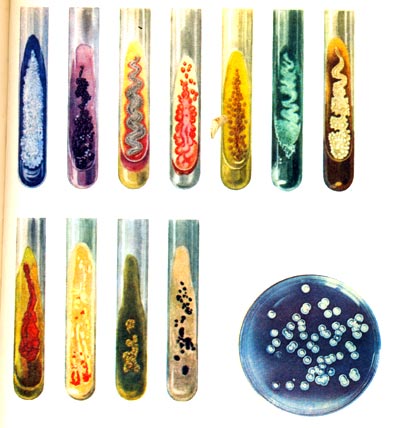
После культивации лаборант оценивает результаты. Из каждого микроорганизма в процессе деления вырастает целая колония бактерий. По ее внешнему виду лаборант определяет вид возбудителя. А по количеству колоний можно судить о концентрации данных микроорганизмов во влагалище. Далее концентрацию сравнивают с нормальными показателями.
Значимыми считаются те бактерии, концентрация которых превышает 10 4 КОЭ/мл. При данной концентрации микроорганизмы способны вызвать заболевание. При обнаружении такого количества бактерий результат анализа считается положительным.
В заключении, выдаваемом лабораторией, указывается:
- вид микроорганизма, который преобладает в мазке;
- патогенность микроорганизма – способность вызывать заболевание:
- Патогенный – присутствие которого может быть вызвано только болезнью.
- Условно-патогенный – бактерии, которые вызывают болезнь только при снижении иммунитета, при значительном увеличении их численности.
- концентрация микроорганизма во влагалище. В числовом показателе и в виде словесной характеристики: «скудно», «умеренный рост», «обильный рост».
В лабораторном заключении количество и рост бактерий может характеризироваться степенью:
источник
Вряд ли найдется кто-то, кто еще ни разу не сдавал кровь из пальца на анализы. Общий анализ крови берут практически при любом заболевании. Так в чем же его диагностическая ценность и какие диагнозы он может подсказать? Разбираем по-порядку.
Основные показатели, на которые врач обращает внимание при расшифровке общего анализа крови — это гемоглобин и эритроциты, СОЭ, лейкоциты и лейкоцитарная формула. Остальные скорее являются вспомогательными.
Чаще всего общий анализ крови назначают, чтобы понять, есть ли в организме воспаление и признаки инфекции, и если да, то какого происхождения — вирусного, бактериального или другого.
Также общий анализ крови может помочь установить анемию — малокровие. И если в крови есть ее признаки — назначают дополнительные анализы, чтобы установить причины.
Еще общий анализ крови назначают, если есть подозрение на онкологический процесс, когда есть ряд настораживающих симптомов и нужны зацепки. В этом случае кровь может косвенно подсказать, в каком направлении двигаться дальше.
Другие показания обычно еще реже.
Сейчас на бланках с результатом анализов в основном используют англ. аббревиатуры. Давайте пройдемся по основным показателям и разберем, что они значат.
Это более детальная информация о тех самых WBC из предыдущего блока.
Лейкоциты в крови очень разные. Все они в целом отвечают за иммунитет, но каждый отдельный вид за разные направления в иммунной системе: за борьбу с бактериями, вирусами, паразитами, неспецифическими чужеродными частицами. Поэтому врач всегда смотрит сначала на общий показатель лейкоцитов из перечня выше, а затем на лейкоцитарную формулу, чтобы понять, а какое звено иммунитета нарушено.
Обратите внимание, что эти показатели обычно идут в двух измерениях: абсолютных (абс.) и относительных (%).
Абсолютные показывают, сколько штук клеток попало в поле зрения, а относительные — сколько эти клетки составляют от общего числа лейкоцитов. Это может оказаться важной деталью — например, в абсолютных цифрах лимфоциты вроде как в пределах нормы, но на фоне общего снижения всех лейкоцитов — их относительное количество сильно выше нормы. Итак, лейкоцитарная формула.
А теперь пройдемся по каждому из этих показателей и разберем, что они значат.
Гемоглобин — это белок, который переносит по организму кислород и доставляет его в нужные ткани. Если его не хватает — клетки начинают голодать и развивается целая цепочка симптомов: слабость, утомляемость, головокружение, выпадение волос и ломкость ногтей, заеды в уголках губ и другие. Это симптомы анемии.
В молекулу гемоглобина входит железо, а еще в его формировании большую роль играют витамин В12 и фолиевая кислота. Если их не хватает — в организме нарушается синтез гемоглобина и развивается анемия.
Есть еще наследственные формы анемии, но они случаются гораздо реже и заслуживают отдельного разбора.
В норме гемоглобин составляет 120−160 г/л для женщин и 130-170 г/л для мужчин. Нужно понимать, что в каждом конкретном случае нормы зависят от лаборатирии. Поэтому смотреть нужно на референсные значения той лаборатории, в которой вы сдавали анализ.
Повышенные цифры гемоглобина чаще всего случаются из-за сгущения крови, если человек излишне потеет во время жары, или принимает мочегонные. Еще повышенным гемоглобин может быть у скалолазов и людей, которые часто бывают в горах — это компенсаторная реакция на недостаток кислорода. Еще гемоглобин может повышаться из-за заболеваний дыхательной системы — когда легкие плохо работают и организму все время не хватает кислорода. В каждом конкретном случае нужно разбираться отдельно.
Снижение гемоглобина — признак анемии. Следующим шагом нужно разбираться какой.
Эритроциты — это красные клетки крови, которые транспортируют гемоглобин и отвечают за обменные процессы тканей и органов. Именно гемоглобин, а точнее — его железо, красит эти клетки в красный.
Нормы для мужчин — 4,2-5,6*10*9/литр. Для женщин — 4-5*10*9/литр. Которые опять-таки зависят от лаборатории.
Повышаться эритроциты могут из-за потери жидкости с потом, рвотой, поносом, когда сгущается кровь. Еще есть заболевание под названием эритремия — редкое заболевание костного мозга, когда вырабатывается слишком много эритроцитов.
Снижении показателей обычно является признаком анемии, чаще железодефицитной, реже — другой.
Норма — 80-95 для мужчин и 80-100 для женщин.
Объем эритроцитов уменьшается при железодефицитной анемии. А повышается — при В12 дефицитной, при гепатитах, снижении функции щитовидной железы.
Повышается этот показатель редко, а вот снижение — признак анемии или снижения функции щитовидной железы.
Повышение значений почти всегда свидетельствует об аппаратной ошибке, а снижение – о железодефицитной анемии.
Это процентное соотношение форменных элементов крови к ее общему объему. Показатель помогает врачу дифференцировать, с чем связана анемия: потерей эритроцитов, что говорит о заболевании, или с избыточным разжижением крови.
Это элементы крови, ответственные за формирование тромботического сгустка при кровотечениях. Превышение нормальных значений может свидетельствовать о физическом перенапряжении, анемии, воспалительных процессах, а может говорить о более серьезных проблемах в организме, среди которых онкологические заболевания и болезни крови.
Снижение уровня тромбоцитов в последние годы часто свидетельствует о постоянном приеме антиагрегантов (например, ацетилсалициловой кислоты) с целью профилактики инфаркта миокарда и ишемического инсульта головного мозга.
А значительное их снижение может быть признаком гематологических заболеваний крови, вплоть до лейкозов. У молодых людей — признаками тромбоцитопенической пурпуры и других заболеваний крови. Так же может появляться на фоне приема противоопухолевых и цитостатических препаратов, гипофункции щитовидной железы.
Это основные защитники нашего организма, представители клеточного звена иммунитета. Повышение общего количества лейкоцитов чаще всего свидетельствует о наличии воспалительного процесса, преимущественно бактериальной природы. Также может оказаться признаком так называемого физиологического лейкоцитоза (под воздействием боли, холода, физической нагрузки, стресса, во время менструации, загара).
Нормы у мужчин и женщин обычно колеблются от 4,5 до 11,0*10*9/литр.
Снижение лейкоцитов – признак подавления иммунитета. Причиной чаще всего являются перенесенные вирусные инфекции, прием некоторых лекарств (в том числе нестероидных противовоспалительных и сульфаниламидов), похудение. Гораздо реже — иммунодефициты и лейкозы.
Самый большой пул лейкоцитов, составляющий от 50 до 75% всей лейкоцитарной популяции. Это основное звено клеточного иммунитета. Сами нейтрофилы делятся на палочкоядерные (юные формы) и сегментоядерные (зрелые). Повышение уровня нейтрофилов за счёт юных форм называют сдвигом лейкоцитарной формулы влево и характерно для острой бактериальной инфекции. Снижение — может быть признаком вирусной инфекции, а значительное снижение — признаком заболеваний крови.
Второй после нейтрофилов пул лейкоцитов. Принято считать, что во время острой бактериальной инфекции число лимфоцитов снижается, а при вирусной инфекции и после неё – повышается.
Значительное снижение лимфоцитов может наблюдаться при ВИЧ-инфекции, при лейкозах, иммунодефицитах. Но это случается крайне редко и как правило сопровождается выраженными симптомами.
Редкие представители лейкоцитов. Повышение их количества встречается при аллергических реакциях, в том числе лекарственной аллергии, также является характерным признаком глистной инвазии.
Самая малочисленная популяция лейкоцитов. Их повышение может говорить об аллергии, паразитарном заболевании, хронических инфекциях, воспалительных и онкологических заболеваниях. Иногда временное повышение базофилов не удается объяснить.
Самые крупные представители лейкоцитов. Это макрофаги, пожирающие бактерии. Повышение значений чаще всего говорит о наличии инфекции — бактериальной, вирусной, грибковой, протозойной. А также о периоде восстановления после них и о специфических инфекциях — сифилисе, туберкулезе. Кроме того может быть признаком системных заболеваниях — ревматоидный артрит и другие.
Если набрать кровь в пробирку и оставить на какое-то время — клетки крови начнут падать в осадок. Если через час взять линейку и замерить, сколько миллиметров эритроцитов выпало в осадок — получим скорость оседания эритроцитов.
В норме она составляет от 0 до 15 мм в час у мужчин, и от 0 до 20 мм у женщин.
Может повышаться, если эритроциты чем-то отягощены — например белками, которые активно участвуют в иммунном ответе: в случае воспаления, аллергической реакции, аутоимунных заболеваний — ревматоидный артрит, системная красная волчанка и другие. Может повышаться при онкологических заболеваниях. Бывает и физиологическое повышение, объясняемое беременностью, менструацией или пожилым возрастом.
В любом случае — высокий СОЭ всегда требует дополнительного обследования. Хоть и является неспецифическим показателем и может одновременно говорить о многом, но мало о чем конкретно.
В любом случае по общему анализу крови практически невозможно поставить точный диагноз, поэтому этот анализ является лишь первым шагом в диагностике и некоторым маячком, чтобы понимать, куда идти дальше. Не пытайтесь найти в своем анализе признаки рака или ВИЧ — скорее всего их там нет. Но если вы заметили любые изменения в анализе крови — не откладывайте визит к врачу. Он оценит ваши симптомы, соберет анамнез и расскажет, что делать с этим анализом дальше.
Мы заметили, что в комментариях очень много вопросов по расшифровке анализов, на которые мы не успеваем отвечать. Кроме того, чтобы дать хорошие рекомендации — важно задать уточняющие вопросы, чтобы узнать ваши симптомы. У нас в сервисе очень хорошие терапевты, которые могут помочь с расшифровкой анализов и ответить на любые ваши вопросы. Для консультации переходите по ссылке.
источник
Методы санитарно-бактериологического анализа для полевых условий
Water. Methods of sanitary-bacteriological analysis for field conditions
Цели, основные принципы и порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2009 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены»
Сведения о стандарте
1 ПОДГОТОВЛЕН Обществом с ограниченной ответственностью «Протектор» совместно с Федеральным государственным бюджетным учреждением «Научно-исследовательский институт экологии человека и гигиены окружающей среды им.А.Н.Сысина» Министерства здравоохранения Российской Федерации и Федеральным бюджетным учреждением науки «Ростовский научно-исследовательский институт микробиологии и паразитологии» Роспотребнадзора
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии, Техническим комитетом по стандартизации ТК 343 «Качество воды»
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 20 октября 2014 г. N 71 П)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97
Сокращенное наименование национального органа по стандартизации
Минэкономики Республики Армения
Госстандарт Республики Беларусь
4 Приказом Федерального агентства по техническому регулированию и метрологии от 11 ноября 2014 г. N 1537 межгосударственный стандарт ГОСТ 24849-2014 введен в действие в качестве национального стандарта Российской Федерации с 1 января 2016 г.
5 ВЗАМЕН ГОСТ 24849-81
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
Настоящий стандарт распространяется на воду, используемую для питьевых и хозяйственно-бытовых целей, воду источников водоснабжения и устанавливает методы санитарно-бактериологического анализа, в том числе ускоренные и сигнальные, по определению содержания колиформных бактерий, бактерий Escherichia coli (далее — Е. coli), бактерий энтерококков и общего числа микроорганизмов (ОМЧ), проводимые в полевых условиях, когда доставка проб воды в стационарную лабораторию невозможна в течение 6 ч после отбора.
Санитарно-бактериологический анализ воды в полевых условиях проводят в передвижной лаборатории или с использованием комплекта оборудования переносной лаборатории. Выбор метода анализа устанавливают в зависимости от цели анализа и оснащенности лаборатории.
Методы настоящего стандарта не применяют для проведения производственного контроля воды централизованных систем питьевого водоснабжения.
Примечание — Персонал, использующий настоящий стандарт, должен иметь подготовку по отбору проб и проведению бактериологических методов исследования воды различного назначения.
В настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ OIML R 76-1-2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 171-81 Дрожжи хлебопекарные прессованные. Технические условия*
_______________
* В Российской Федерации применяют также ГОСТ Р 54731-2011 «Дрожжи хлебопекарные прессованные. Технические условия»
ГОСТ 857-95 Кислота соляная синтетическая техническая. Технические условия
ГОСТ 975-88 Глюкоза кристаллическая гидратная. Технические условия
ГОСТ 1770-74 (ISO 1042-83, ISO 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 1820-2001 Спички. Технические условия
ГОСТ 2761-84 Источники централизованного хозяйственно-питьевого водоснабжения. Гигиенические, технические требования и правила выбора
ГОСТ 4198-75 Реактивы. Калий фосфорнокислый однозамещенный. Технические условия
ГОСТ 4209-77 Реактивы. Магний хлористый 6-водный. Технические условия
ГОСТ 4233-77 Реактивы. Натрий хлористый. Технические условия
ГОСТ 5556-81 Вата медицинская гигроскопическая. Технические условия
ГОСТ 6038-79 Реактивы. D-глюкоза. Технические условия
ГОСТ 6552-80 Реактивы. Кислота ортофосфорная. Технические условия
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 9412-93 Марля медицинская. Общие технические условия
ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
ГОСТ 13805-76 Пептон сухой ферментативный для бактериологических целей. Технические условия
ГОСТ ИСО/МЭК 17025-2009 Общие требования к компетентности испытательных и калибровочных лабораторий
ГОСТ 17206-96 Агар микробиологический. Технические условия
ГОСТ 17299-78 Спирт этиловый технический. Технические условия
ГОСТ 18300-87 Спирт этиловый ректификованный технический. Технические условия
ГОСТ 21241-89 Пинцеты медицинские. Общие технические требования и методы испытаний
ГОСТ 23932-90 Посуда и оборудование лабораторные стеклянные. Общие технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 25706-83 Лупы. Типы, основные параметры. Общие технические требования
ГОСТ 27068-86 Реактивы. Натрий серноватистокислый (натрия тиосульфат) 5-водный. Технические условия
ГОСТ 29227-91 (ISO 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 31861-2012 Вода. Общие требования к отбору проб
ГОСТ 31942-2012 (ISO 19458:2006) Вода. Отбор проб для микробиологического анализа
ГОСТ 31955-2012 (ISO 9308-1:2000) Вода питьевая. Обнаружение и количественный учет Escherichia coli и колиформных бактерий. Часть 1. Метод мембранной фильтрации
Примечание — При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя «Национальные стандарты» за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
В настоящем стандарте применены термины по ГОСТ 30813, а также следующие термины с соответствующими определениями:
3.1 полевые условия: Условия проведения санитарно-бактериологического посева и анализа проб воды вне стационарной лаборатории.
3.2 передвижная лаборатория: Средства (мобильного) передвижения и оснащения, предназначенные для проведения санитарно-бактериологического анализа воды в полевых условиях, монтируемые на специально для этого предназначенных передвижных транспортных средствах (железнодорожный подвижной состав, автомобили, суда), функционирующие при автономном режиме энергообеспечения.
3.3 переносная лаборатория: Комплект оборудования для проведения санитарно-бактериологического анализа воды в полевых условиях, который может перенести человек или группа лиц на значительное расстояние или можно перевезти на любом транспортном средстве, не предназначенном специально для этих целей.
3.4 общее микробное число: Число аэробных и факультативно анаэробных гетеротрофных микроорганизмов, использующих для питания органические вещества, обладающих свойством образовывать колонии на питательном агаре, при температуре (36±2)°С в течение 24 ч, видимые при двукратном увеличении.
3.5 колиформные бактерии: Грамотрицательные, оксидазоотрицательные, не образующие спор палочки, обладающие свойством образовывать колонии в аэробных условиях на селективной дифференциальной лактозной среде с образованием кислоты при температуре (36±2)°С в течение (24±3) ч.
3.6 бактерии семейства Enterobacteriaceae: Грамотрицательные, оксидазоотрицательные, лактозоотрицательные бактерии, обладающие свойством образовывать колонии в аэробных условиях на селективной дифференциальной лактозной среде и способные ферментировать глюкозу с образованием кислоты и газа при (36±2)°С в течение (21±3) ч.
3.7 Esherichia coli: Колиформные бактерии, обладающие свойством ферментировать лактозу при температуре (44,0±1,0)°С в течение 24 ч с образованием кислоты и газа, а также продуцировать индол из триптофана в течение (21±3) ч.
[ГОСТ 30813-2002, статья 65]3.8 энтерококки: Грамположительные, каталазоотрицательные, полиморфные, круглые или овальные с заостренными концами кокки, располагающиеся попарно или в коротких цепочках, обладающие свойством образовывать колонии на питательных средах, содержащих 0,04% азида натрия и 2,3,5 трифенилтетразолиум хлорид (ТТХ), способностью роста на питательной среде, содержащей 6,5% NaCl, и образующие характерные колонии на средах с эскулином.
3.9 ускоренные методы: Методы, позволяющие получить результаты в течение 24 ч.
3.10 сигнальные методы: Методы, позволяющие получить результаты только на основе качественной оценки.
3.11 сливной рост: Рост одной или нескольких колоний подвижных бактерий, распространившийся на всю поверхность питательной среды и не позволяющий точно подсчитать общее количество выросших колоний.
В настоящем стандарте применены следующие сокращения:
ОМЧ — общее число микроорганизмов;
КОЕ — колонии образующие единицы;
СИБ — система индикаторная бумажная;
ТСА — триптон-соевый агар неселективный;
ТЖА — триптон-желчный агар.
4.1 Общие требования к отбору проб — по ГОСТ 31861.
4.3 Если проба воды не может быть исследована в течение 2 ч после отбора, допускается хранить ее в чистых продезинфицированных контейнерах не более 6 ч до начала испытаний при температуре от 2°С до 8°С, предохраняя от замерзания, действия прямых солнечных лучей и перегрева.
4.4 Если пробы воды отбирают после обеззараживания, нейтрализацию остаточного количества дезинфектанта проводят по ГОСТ 31942.
4.5 Документирование процедуры отбора проб отражают в акте отбора проб с указанием всех сведений, приведенных в ГОСТ 31942. При отборе проб воды из источников водоснабжения в акте дополнительно указывают погодные условия и температуру воды.
5.1 Средства комплектования передвижной лаборатории
Весы неавтоматического действия по ГОСТ OIML R 76-1 с пределами допускаемой абсолютной погрешности взвешивания ±0,001 г.
Весы лабораторные механические (аптечные равноплечные) с пределами допускаемой погрешности при полной нагрузке ±10 мг.
Весы лабораторные механические (аптечные равноплечные) с пределами допускаемой погрешности при полной нагрузке ±50 мг.
РН-метр, обеспечивающий измерение водородного показателя рН с пределами допускаемой абсолютной погрешности ±0,1 единиц рН .
Автоматические дозаторы бактериологические или пипетки однократного или многоразового применения 1-1-2-1, 1-1-2-10 по ГОСТ 29227.
Стерилизатор паровой с режимом стерилизации от (105+3)°С до (134+3)°С при рабочем давлении от 19 до 230 кПа .
Стерилизатор суховоздушный, обеспечивающий поддержание температуры 200°С, с пределами абсолютной допускаемой погрешности ±3°С .
Термостат для инкубации посевов, обеспечивающий поддержание температуры 36°С, с пределами абсолютной допускаемой погрешности измерения температуры ±2°С.
Термостат для инкубации посевов, обеспечивающий поддержание температуры 44°С, с пределами абсолютной допускаемой погрешности измерения температуры ±1°С.
Холодильник портативный, например автомобильный, поддерживающий температуру от 1°С до 10°С, или термоконтейнер с емкостями (например, для льда).
Аппарат для мембранной фильтрации под вакуумом с диаметром фильтрующей поверхности 37 или 47 мм.
Примечание — Допускается использовать одноразовые стерильные фильтровальные аппараты.
Устройство электрическое или ручное для создания разрежения.
Фильтры мембранные со средним диаметром пор 0,45 мкм и диаметром диска 35-37 мм или 45-47 мм, стерильные от производителя или простерилизованные и упакованные в лаборатории.
Емкости из нержавеющей стали или эмалированные с крышкой для стерилизации мембранных фильтров методом кипячения .
Лампа ультрафиолетовая с длиной волны 254 нм.
Примечание — При работе с ультрафиолетовой лампой используют защитные очки и перчатки, т.к. ультрафиолетовое облучение вызывает раздражение глаз и кожи.
Лампа бактерицидная.
Лупа по ГОСТ 25706 с увеличением 2 .
Устройство нагревательное для расплавления питательного агара и приготовления питательных сред из сухих препаратов .
Лабораторный пистолет для фламбирования.
Зажигалки или спички по ГОСТ 1820.
Емкости для отбора проб однократного или многократного применения вместимостью 500 см и другое оборудование, необходимое для отбора проб воды, приведенное в ГОСТ 31942.
Пробирки бактериологические одноразового или многоразового использования по ГОСТ 25336.
Штативы для пробирок.
Чашки (Петри) бактериологические одноразовые или стеклянные многократного применения по ГОСТ 23932.
Посуда мерная лабораторная стеклянная 2-го класса точности вместимостью 500 и 1000 см по ГОСТ 1770.
Пробки силиконовые, выдерживающие стерилизацию сухим жаром . Силиконовые колпачки многоразового использования.
Спиртовки стеклянные или металлические с подставкой по ГОСТ 25336.
Пинцеты по ГОСТ 21241.
Петли бактериологические.
Палочки стеклянные.
Ножницы.
Емкости стеклянные или эмалированные для приготовления сред .
Вата хлопчатобумажная гигроскопическая медицинская по ГОСТ 5556.
Марля медицинская по ГОСТ 9412.
Бумага фильтровальная по ГОСТ 12026.
Фломастер-маркер для маркировки посуды.
Контейнеры для хранения стерильной посуды.
Герметичные контейнеры или мешки для сбора и хранения отработанного материала.
Средства защиты (очки для защиты глаз от УФ-излучения, латексные перчатки, маски и шапочки одноразового использования).
Средство дезинфекционное, допущенное к применению в установленном порядке.
Натрий хлористый по ГОСТ 4233 .
D-глюкоза по ГОСТ 6038.
Бриллиантовый зеленый (С Н N О ), с массовой долей основного вещества — не менее 98%.
Магний хлористый 6-водный по ГОСТ 4209.
Калий фосфорнокислый однозамещенный по ГОСТ 4198.
Натрий серноватистокислый по ГОСТ 27068.
Бромтимоловый синий (C H Br О S), с массовой долей основного вещества — не менее 98% .
Натрия азид.
Кислота ортофосфорная по ГОСТ 6552.
Кислота соляная синтетическая техническая по ГОСТ 857.
Спирт этиловый ректификованный 96%-ный по ГОСТ 18300.
Жидкость горючая для спиртовок (например, спирт этиловый технический по ГОСТ 17299).
Агар микробиологический питательный по ГОСТ 17206 (сухой препарат или агар, приготовленный в стационарной лаборатории по приложению А и разлитый в емкости или пробирки).
Растворы для разведений, приготовленные по приложению А.
Вода дистиллированная по ГОСТ 6709.
Полоски индикаторные бумажные для измерения рН .
Системы индикаторные бумажные для проведения оксидазного теста (диски или полоски).
Реактив для индольного теста.
Реактив Ковача.
Полоски реактивные бумажные для определения индола.
L-триптофан (C H N О ), с массовой долей основного вещества — не менее 98% .
2, 3, 5 — Трифенилтетразолиум хлорид (ТТХ), с массовой долей основного вещества — не менее 99,5% .
Гептадецилсульфат натрия (тергитол 7), с массовой долей основного вещества- не менее 98% .
Тетраметил п -фенилендиамин гидрохлорид (CH ) NC H N(CH ) ·2H CI или диметил- п — фенилендиамин дигидрохлорид (С Н N ·2НСl), с массовой долей основного вещества — не менее 99%.
-нафтол (С Н ОН) для приготовления оксидазного реактива при использовании диметил- п -фенилендиамин дигидрохлорида, с массовой долей основного вещества — не менее 98%.
пара -диметиламинобензальдегид ((CH ) NC H CHO), с массовой долей основного вещества — не менее 99,2%.
Экстракт дрожжевой, сухой или приготовленный из хлебопекарных прессованных дрожжей по ГОСТ 171.
Среда Эндо (сухой препарат) или приготовленная по приложению А или другая селективная дифференциальная лактозная среда (например, среда с тергитолом 7 по ГОСТ 31955 или приготовленная по приложению А).
Сухой препарат с индикатором ВР и глюкозой или полужидкая среда, приготовленная по приложению А, или готовые к использованию тест-системы, например СИБ-глюкоза.
Сухой препарат с индикатором ВР и лактозой или полужидкая среда с лактозой и триптофаном, приготовленная по приложению А, или готовые к использованию тест-системы, например СИБ-лактоза.
Энтерококкагар (сухой препарат) или приготовленный по приложению А или другая азидная среда с ТТХ (например, азидная среда Сланеца-Бертли по приложению А).
Пептон сухой ферментативный для бактериологических целей по ГОСТ 13805 .
Триптон — желчный агар (ТЖА).
Триптон — соевый агар неселективный (ТСА).
Готовые питательные среды для определения колиформных бактерий, Е. coli, энтерококков и ОМЧ сигнальными методами, поставляемые на коммерческой основе и снабженные сертификатом, выданным в установленном порядке.
Примечания
1 Допускается использовать оборудование, расходные материалы, реактивы, питательные среды, диагностические препараты и системы идентификации с аналогичными характеристиками, разрешенные к применению для этих целей в установленном порядке.
2 Комплект средств лаборатории формируется исследователем из приведенного перечня в зависимости от выбранного метода анализа.
4 Помещение передвижной лаборатории, в котором проводят посев воды, должно быть оборудовано бактерицидными лампами для соблюдения правил асептики, а также средствами для утилизации и обеззараживания отработанного материала в соответствии с установленными требованиями безопасности проведения работ.
5 При отсутствии автоклава или условий для кипячения отработанного материала лаборатория комплектуется специальными герметичными контейнерами или мешками для сбора и доставки отработанного материала в стационарную лабораторию с целью его последующей инактивации.
6 В случае возникновения нештатных ситуаций обеззараживание отработанного материала проводят с помощью дезинфекционных средств в концентрациях, эффективных по отношению к патогенным микроорганизмам семейства Enterobacteriaceae и разрешенных к использованию в установленном порядке.
5.2 Средства комплектования переносной лаборатории
Дозаторы автоматические или пипетки стерильные одноразового применения объемом 1 и 10 см .
Переносной термостат для инкубации посевов проб воды, обеспечивающий поддержание температуры 36°С. В зависимости от энергообеспечения, имеющегося на месте выполнения анализа, допускается использовать термоконтейнеры с нагревающими элементами.
Установка для мембранной фильтрации с отметкой объема воды 100 см для фильтрования под вакуумом с диаметром фильтрующей поверхности 35-37 или 47-50 мм и с приспособлением для создания разрежения (например, ручной вакуумный насос; шприцевые фильтрующие насадки, позволяющие фильтровать до 2 дм воды и т.п.).
Фильтры мембранные со средним диаметром пор 0,45 мкм и диаметром фильтрующей поверхности 35-37 мм или 47-50 мм стерильные от производителя или подготовленные и простерилизованные в стационарной лаборатории.
Бумага фильтровальная по ГОСТ 12026 стерильная, нарезанная кружочками диаметром немного большим, чем мембранный фильтр, упакованная в стерильную емкость или плотный пакет.
Пробирки бактериологические стерильные одноразового или многоразового применения.
Спиртовки стеклянные или металлические с подставкой по ГОСТ 25336.
Штатив для пробирок.
Лабораторный пистолет или другое оборудование для фламбирования.
Петля бактериологическая.
Лупа по ГОСТ 25706 с увеличением 2 .
Пинцеты по ГОСТ 21241.
Вата хлопчатобумажная гигроскопическая медицинская по ГОСТ 5556.
Емкости для отбора проб многоразового или одноразового использования вместимостью 500 см и другое оборудование, необходимое для отбора проб воды, приведенное в ГОСТ 31942.
Чашки Петри одноразового применения.
Питательный агар, приготовленный по приложению А в стационарной лаборатории, разлитый в емкости (например, пробирки), удобные для быстрого расплавления агара.
Чашки Петри с готовыми дифференциально-диагностическими и селективными питательными средами для определения колиформных бактерий и энтерококков, приготовленные в стационарной лаборатории (приложение А) и помещенные в пенал или специальные пакеты.
Готовые питательные среды для определения колиформных бактерий, Е. coli, энтерококков сигнальными методами, поставляемые на коммерческой основе и снабженные сертификатом, выданным в установленном порядке.
Пробирки с полужидкой средой с индикатором ВР и глюкозой или готовые тест-системы.
Реактивы для оксидазного теста: при работе с тетраметил-п-фенилендиамин гидрохлоридом — сухой препарат, при работе с диметил-п-фенилендиамин дигидрохлоридом — 1%-ные растворы, приготовленные по приложению А, или готовые бумажные индикаторные системы, заменяющие фильтровальную бумагу и реактивы для оксидазного теста.
Реактив Ковача или УФ лампа с длиной волны 254 нм.
Вода дистиллированная стерильная.
Спирт этиловый ректификованный по ГОСТ 18300.
Жидкость горючая для спиртовки по ГОСТ 17299.
Примечания
1 Комплектование лаборатории зависит от выбранного метода анализа.
2 Допускается использовать другое оборудование, расходные материалы, реактивы, питательные среды, диагностические препараты и системы идентификации с аналогичными характеристиками, разрешенные к применению для этих целей в установленном порядке.
3 Рекомендуется использовать переносные лаборатории промышленного производства для проведения бактериологического анализа в полевых условиях.
4 Используют только заранее стерилизованную посуду, расходные материалы, заранее приготовленные и разлитые питательные среды в условиях стационарной лаборатории или приобретенные на коммерческой основе, готовые к употреблению и снабженные сертификатом среды.
5 Посевы воды в полевых условиях проводят между пламенем двух спиртовок с целью обеспечения условий асептики.
5.3 Средства комплектования лаборатории для посева проб воды на месте отбора проб с последующей доставкой в стационарную лабораторию
Дозаторы автоматические или пипетки стерильные одноразового применения вместимостью 1 и 10 см .
Переносной термостат для инкубации посевов, обеспечивающий поддержание температуры 36°С, или термоконтейнер с нагревающими элементами.
Установка для мембранной фильтрации с отметкой объема воды 100 см для фильтрования под вакуумом с диаметром фильтрующей поверхности 35-37 или 47-50 мм и с приспособлением для создания разрежения.
Фильтры мембранные со средним диаметром пор 0,45 мкм и диаметром фильтрующей поверхности 35-37 или 47-50 мм, стерильные от производителя или подготовленные и простерилизованные в стационарной лаборатории.
Емкости для отбора проб многоразового или одноразового использования вместимостью 500 см и другое оборудование, необходимое для отбора проб воды, приведенное в ГОСТ 31942.
Чашки Петри одноразового применения.
Лабораторный пистолет для фламбирования.
Вода дистиллированная стерильная.
Спирт этиловый ректификованный по ГОСТ 18300.
Жидкость горючая для спиртовки.
Спиртовки стеклянные или металлические с подставкой по ГОСТ 25336.
Пинцеты по ГОСТ 21241.
Вата хлопчатобумажная гигроскопическая медицинская по ГОСТ 5556.
Питательный агар, приготовленный по приложению А в стационарной лаборатории, разлитый в емкости (например, пробирки), удобные для быстрого расплавления агара.
Чашки Петри с готовыми питательными средами для определения колиформных бактерий и энтерококков, приготовленные в стационарной лаборатории по приложению А, помещенные в пенал или специальные пакеты, или готовые питательные подложки для определения ОМЧ, колиформных бактерий, Е. coli, или готовые питательные среды в чашках Петри, поставляемые на коммерческой основе и имеющие сертификат, выданный в установленном порядке.
6.1 Подготовка посуды
Для проведения анализа используют стерильную одноразовую посуду (чашки Петри, пипетки, пробирки, мерные емкости, емкости для отбора проб, в том числе с тиосульфатом натрия).
Допускается комплектовать лабораторию стерильной посудой многократного применения, подготовленной в стационарной лаборатории в соответствии с требованиями ГОСТ 31942. Стерилизованная посуда должна иметь маркировку с указанием даты стерилизации для последующего учета срока хранения.
Емкости для отбора проб питьевой воды, обеззараженной хлорированием или другими окислителями, должны быть стерилизованы с тиосульфатом натрия и соответствующим способом маркированы.
При невозможности комплектования передвижной лаборатории стерильными емкостями для отбора проб и посудой для всего объема анализа, допускается проводить в условиях передвижной лаборатории следующие операции:
— мытье, подготовку к стерилизации и стерилизацию лабораторной посуды в суховоздушном стерилизаторе в соответствии с требованиями ГОСТ 31942;
— обеззараживание отработанного материала полученного после санитарно-бактериологического анализа в паровом стерилизаторе при температуре (126±2)°С, или кипячением в течение 30 мин, или дезинфицирующими средствами в соответствии с инструкцией по их применению.
Сведения о проведении стерилизации и обеззараживания в условиях передвижной лаборатории вносят в журнал испытаний.
6.2 Приготовление питательных сред и реактивов
6.2.1 Приготовление питательных сред и реактивов проводят в стационарной лаборатории или полевых условиях в соответствии с требованиями ГОСТ 31955 и приложением А. Питательный агар как основу большинства плотных питательных сред готовят в соответствии с инструкцией производителя (А.1, приложение А).
6.2.2 Питательные среды, которые в соответствии с указанием производителя не требуют стерилизации автоклавированием, а также среды с коротким сроком хранения после розлива в чашки Петри, могут быть приготовлены непосредственно перед анализом. Такие среды готовят в эмалированной или стеклянной емкости или емкости из нержавеющей стали. Допускается использовать заранее приготовленные в стационарной лаборатории навески из сухого препарата и соответствующий объем стерильной дистиллированной воды. Навески сухого препарата при хранении должны быть защищены от воздействия влаги и света.
6.2.3 Сведения о приготовлении сред и реактивов в условиях передвижной лаборатории должны быть внесены в журнал испытаний.
Примечания
1 Подготовленные заранее стерильные емкости, питательные среды, лабораторная посуда, реактивы должны храниться в условиях, предусмотренных для каждого средства, среды и реактива с соблюдением условий стерильности и предельных сроков хранения. При этом емкости и пробирки с готовыми средами должны быть закрыты силиконовыми пробками и защищены колпачками из силикона или жароустойчивой бумаги. Чашки Петри с готовыми средами должны быть помещены в специальные пакеты или завернуты в плотную бумагу, защищающую среду от высыхания и воздействия света.
2 При вскрытии упаковок и емкостей, удалении пробок (крышек) непосредственно перед проведением анализа пробка (крышка) и края емкости не должны касаться посторонних поверхностей.
3 Операции по подготовке и проведению анализа выполняют чистыми и продезинфицированными руками (например, после обработки рук 70%-ным этиловым спиртом или дезинфицирующими салфетками для индивидуального пользования) или в стерильных перчатках.
6.3 Подготовка мембранных фильтров
Подготовку мембранных фильтров проводят в соответствии с рекомендациями производителя. Если производитель поставляет нестерильные фильтры, их стерилизуют до начала анализа. Целесообразно стерилизовать мембранные фильтры в условиях стационарной лаборатории. После стерилизации фильтры высушивают в асептических условиях и упаковывают стерильно в чашки Петри или стерильные пакеты. Срок хранения фильтров, стерилизованных в лаборатории, — 10 сут.
Перед началом проведения анализа стерильные сухие фильтры смачивают в стерильной дистиллированной воде, накладывая стерильным пинцетом отдельно каждый фильтр на поверхность воды, налитой в стерильную чашку Петри.
Допускается проводить стерилизацию мембранных фильтров в условиях передвижной лаборатории.
7.1 Определение колиформных бактерий и Е. coli
7.1.1 Определение колиформных бактерий ускоренным методом с использованием мембранной фильтрации
7.1.1.1 Проведение анализа
При анализе питьевой воды системы централизованного водоснабжения и подземных источников 1-го класса по ГОСТ 2761 анализируют 300 см воды, пропуская этот объем не менее чем через два мембранных фильтра.
При исследовании питьевой воды нецентрализованного водоснабжения и поверхностных источников водоснабжения анализируют не менее 100 см воды, пропуская ее не менее чем через три мембранных фильтра, например пробы воды 1,0, 10 и 100 см .
При фильтровании воды неизвестного качества целесообразно увеличивать количество фильтруемых объемов для получения изолированных колоний (например, выполняя посев по 1 см из 1-го и 2-го десятикратных разведений). При этом объем воды для посева выбран правильно, если на одном — двух мембранных фильтрах выросли изолированные колонии, среди которых не более 30 колоний относятся к числу колиформных бактерий.
Для фильтрования используют стерильные мембранные фильтры, подготовленные по 6.3. Отмеренные объемы воды фильтруют через мембранные фильтры с использованием аппарата для фильтрования и соблюдением процедуры по 6.4.
После фильтрования анализируемой воды мембранные фильтры размещают посевом вверх на одну из селективных дифференциальных питательных сред (например, на фуксин-сульфитную среду Эндо) (А.3, приложение А), разлитых в чашки Петри, добиваясь полного прилегания фильтров к среде без пузырьков воздуха. Вместо среды Эндо допускается использовать лактозный агар с тергитолом 7 (А.4, приложение А).
Примечание — Лактозный агар с тергитолом 7 допускается использовать только при исследовании воды, в которой фоновая посторонняя водная микрофлора не мешает росту изолированных колоний колиформных бактерий на фильтре.
На одну чашку допускается помещать несколько фильтров с условием, чтобы фильтры не соприкасались. Маркировку профильтрованного объема воды наносят под фильтром с наружной стороны дна чашки Петри.
Чашки с посевами помещают в термостат дном вверх и инкубируют при температуре (36±2)°С в течение 18-24 ч.
7.1.1.2 Учет результатов
После окончания инкубации посевов регистрируют в журнале испытаний отсутствие или наличие на мембранных фильтрах колоний микроорганизмов.
Учитывают в качестве лактозоположительных все выросшие на мембранных фильтрах характерные колонии независимо от их размера:
— на среде Эндо — с темно-красной окраской и металлическим блеском или без него, слизистые с красным центром и отпечатком на оборотной стороне фильтра;
— на среде с тергитолом 7 с желто-оранжевой, кирпично-красной окраской, иногда с ржаво-окрашенным центром, образующим желтую окраску в среде под мембраной (ГОСТ 31955).
Для подтверждения принадлежности колоний к колиформным бактериям проводят оксидазный тест одним из способов, указанных в приложении Б, с использованием реактива для оксидазного теста (А.5, приложение А). При этом исследованию подлежат только те мембранные фильтры, на которых выросло не более 30-50 изолированных характерных колоний.
При использовании способа 3 определения оксидазной активности проводят проверку всех (до 10) колоний или выборочно 3-4 колонии разной морфологии.
Если при выборочной проверке колоний каждого типа получают неодинаковые результаты, то число оксидазоотрицательных колоний рассчитывают по формуле (2), 7.1.1.4.
Выборочную проверку колоний не проводят, если оксидазный тест выполняют по способу 1 или 2. Оксидазную активность одновременно всех колоний на фильтре учитывают через 1-4 мин после контакта с реактивом, что исключает субъективную оценку результатов исследования.
Подсчитывают сумму (А) всех колоний лактозоположительных оксидазоотрицательных бактерий, подтвержденных как колиформные бактерии.
Результаты подсчета регистрируют в журнале испытаний.
7.1.1.3 С целью повышения надежности оценки эпидемической безопасности воды при отсутствии роста колиформных бактерий, но наличии роста лактозоотрицательных оксидазоотрицательных колоний разной морфологии — розовых, розовых с центром подтверждают принадлежность бактерий к семейству Enterobacteriaceae по ферментации глюкозы. Для этого на всех фильтрах подсчитывают число указанных колоний каждого типа отдельно и регистрируют в журнале испытаний. Проводят посев двух-трех колоний каждого типа в бактериологические пробирки на полужидкую среду с индикатором ВР и глюкозой (А.6, приложение А).
Пробирки с посевами помещают в термостат и инкубируют при температуре (36,0±2,0)°С в течение 4-5 ч.
По истечении 4-5 ч инкубации посевов проводят учет реакции ферментации глюкозы:
— отсутствие в пробирках кислоты и газа подтверждает отсутствие бактерий, принадлежащих к семейству Enterobacteriaceae;
— образование в пробирках кислоты и газа подтверждает принадлежность бактерий к семейству Enterobacteriaceae.
Если при выборочной проверке реакции ферментации глюкозы, проведенной на колониях каждого типа, получены неодинаковые результаты, то число подтвержденных колоний рассчитывают по формуле (2), 7.1.1.4.
Подсчитывают число колоний лактозоотрицательных, не обладающих оксидазной активностью бактерий и ферментирующих глюкозу с образованием кислоты и газа, что подтверждает их принадлежность к семейству Enterobacteriaceae.
В журнале испытаний регистрируют число бактерий, относящихся к семейству Enterobacteriaceae.
где — общее число колоний, подсчитанных на всех фильтрах, которые подтверждены и зарегистрированы как лактозоположительные оксидазоотрицательные по 7.1.1.2;
— объем воды, пропущенный через все фильтры, на которых проводился учет числа колоний , см .
Если на мембранных фильтрах зарегистрирован рост колоний разного типа (разной морфологии) и при выборочной проверке колоний одного типа получены неодинаковые результаты, то число подтвержденных колоний бактерий этого типа ( ) рассчитывают по формуле:
где — общее число колоний одного конкретного типа, по которому проведен учет;
— число проверенных колоний из общего числа ;
— число колоний, подтвержденных на принадлежность к конкретному виду микроорганизмов.
Результаты учета колоний по каждому типу рассчитывают по формуле (2), суммируют и обрабатывают по 7.1.1.4, формула (1).
При наличии в пробе воды колиформных бактерий результат испытаний выражают числом КОЕ колиформных бактерий в 100 см пробы воды.
При отсутствии в пробе воды колиформных бактерий и бактерий E. coli в протоколе испытаний записывают: «Колиформные бактерии и бактерии E. coli в 100 см пробы воды не обнаружены».
При необходимости получения количественного результата определения в пробе воды оксидазоотрицательных бактерий, ферментирующих глюкозу до кислоты и газа, для которых по 7.1.1.3 установлена принадлежность к семейству Enterobacteriaceae, расчёт проводят по формуле (1) аналогично определению в пробе воды колиформных бактерий.
7.1.1.5 Оформление результатов
Результаты анализа вносят в протокол испытаний, оформленный в соответствии с требованиями ГОСТ ИСО/МЭК 17025. Протокол должен содержать:
— ссылку на настоящий стандарт;
— информацию, необходимую для идентификации пробы анализируемой воды;
— определяемый показатель, используемый метод и результаты анализа;
— любые отклонения, которые могли повлиять на результаты анализа.
7.1.2 Определение бактерий Е. coli
7.1.2.1 Проведение анализа
Для определения Е. coli используют посевы, которые получены на мембранных фильтрах при проведении анализа на определение колиформных бактерий (см. 7.1.1.1 и 7.1.1.2).
Если на мембранном фильтре в течение 24 ч не обнаружен рост колоний или выросли колонии не характерные для лактозоположительных колиформных бактерий, в журнале испытаний регистрируют сведения об отсутствии Е. coli в пробе воды.
При наличии на мембранных фильтрах характерных колоний на среде Эндо или на среде с тергитолом 7 проводят их дальнейшую идентификацию на наличие бактерий Е. coli. Все указанные колонии (но не более 15) засевают в бактериологические пробирки с полужидкой средой с индикатором ВР и лактозой с добавлением триптофана (А.7, приложение А), предварительно нагретой до температуры 43°С-44°С.
В засеянные пробирки под пробку вставляют полоски, пропитанные реактивом (А.8, приложение А), для обнаружения продуцирования индола. Пробирки немедленно помещают в термостат и инкубируют при температуре (44±1)°С в течение 18-20 ч.
По истечении срока инкубации посева в журнале испытаний регистрируют результаты ферментации лактозы и наличие или отсутствие индола. Подтверждением наличия Е. coli является ферментация лактозы с образованием кислоты и газа и ярко малиновый цвет полоски, пропитанной реактивом, указывающий на наличие индола.
7.1.2.3 Оформление результатов — по 7.1.1.5.
Примечание — Метод применяют в передвижной лаборатории при наличии термостата, поддерживающего температуру (44±1)°С.
7.1.4 Определение Е. coli ускоренным методом с использованием среды с желчью
Для определения Е. coli используют две среды — триптон-желчный агар (ТЖА) и триптон-соевый агар (ТСА) (А. 10, приложение А).
Проводят фильтрование отмеренных объемов воды, установленных по 7.1.1.1, через мембранные фильтры, подготовленные по 6.3 с соблюдением требований 6.4.
После фильтрования отмеренных объемов воды мембранные фильтры с посевами накладывают на среду ТСА и инкубируют в термостате при температуре (36,0±2,0)°С в течение 4-5 ч. Затем фильтры переносят на среду ТЖА. Инкубацию посевов продолжают при температуре (44±1)°С в течение 19-20 ч.
После инкубации посевов регистрируют в журнале испытаний наличие или отсутствие на фильтрах роста колоний. При росте на фильтрах изолированных колоний белого, палевого, кремового цвета мембранный фильтр помещают на фильтровальную бумагу, смоченную реактивом для индольного теста (А.11, приложение А) и облучают ультрафиолетовой лампой в течение 10-30 мин в зависимости от скорости окрашивания. Все колонии микроорганизмов красного цвета на мембранном фильтре учитывают как колонии Е. coli и подсчитывают их число.
Обработку результатов проводят по 7.1.1.4 аналогично обработке результатов по определению колиформных бактерий.
Е. coli в пробе воды рассчитывают по формуле (1), 7.1.1.4.
Результат испытаний выражают числом КОЕ бактерий Е. coli в 100 см анализируемой пробы воды.
При отсутствии роста колоний на фильтрах или наличии отрицательной реакции на образование индола (отсутствие изменения цвета колоний) в протоколе испытаний записывают: «Бактерии Е. coli в 100 см пробы воды не обнаружены».
Оформление результатов — по 7.1.1.5.
Примечания
1 Использование коммерческого реактива Ковача на водной основе дает более четкие и быстрые результаты без применения ультрафиолетового облучения.
2 Неравномерное распределение колоний микроорганизмов на фильтре или обильный рост сопутствующих микроорганизмов могут мешать идентификации колоний микроорганизмов с положительной реакцией на образование индола из-за диффузии окраски в прилегающие колонии микроорганизмов.
7.1.5 Определение колиформных бактерий и Е. coli ускоренными методами с использованием готовых питательных сред на подложке
Для ускоренного определения колиформных бактерий и Е. coli применяют готовые питательные подложки, например петрифильмы серии Aqua по методическим указаниям [1] и другие тест-системы, имеющие сертификат и разрешение на применение.
Примечание — Необходимо перед использованием петрифильмов в полевых условиях проверить сопоставимость результатов в сравнении с методами, применяемыми в стационарной лаборатории. В случае получения достоверных различий по критерию Стьюдента более чем в 80% полученные результаты следует отнести к ориентировочным.
7.1.5.2 Учет, обработка и оформление результатов — по 7.1.1.4 и 7.1.1.5.
Примечания
1 Готовые тест-системы используют в полевых условиях при необходимости проведения анализа воды с небольшим микробным загрязнением; их использование при работе в полевых условиях существенно сокращает перечень необходимого оборудования при комплектовании лабораторий.
2 Использование тест-систем сокращает продолжительность анализа за счет исключения этапов подготовки посуды и приготовления питательных сред, стерилизации, розлива, разогрева и хранения питательных сред, упрощает процедуру посева, в ряде случаев исключает процесс идентификации бактерий, способствует защите персонала от вредного микробного воздействия и исключает контаминацию помещения, сокращает трудозатраты при утилизации.
7.1.6 Определение колиформных бактерий и бактерий Е. coli сигнальным методом
Метод не требует фильтрования воды и наличия в комплекте лаборатории чашек с питательными средами. Метод обеспечивает возможность получения только качественной оценки результатов. Для проведения анализа используют навеску соответствующей среды для определения колиформных бактерий или Е. coli в соответствии с прилагаемой инструкцией производителя.
В стерильные емкости наливают 100 см исследуемой воды, вносят навеску сухой среды и тщательно перемешивают до полного растворения. Посевы инкубируют в течение 10-24 ч при температуре 36°С.
Примечание — Допускается при отсутствии в комплекте лаборатории термостата инкубировать посевы при температуре 20°С-25°С в течение 48 ч.
После инкубации посевов проводят учет результатов, при этом считают, что:
— колиформные бактерии и Е. coli отсутствуют, если цвет среды не изменился или отмечено помутнение без изменения цвета среды;
— бактерии обнаружены, если среда приобрела зелено-голубой цвет во всем объеме или верхнем слое. При перемешивании цвет среды не должен измениться.
Для подтверждения наличия Е. coli в емкостях, в которых отмечено изменение цвета среды, вносят 2,5 см реактива Ковача (А.11, приложение А). Красное кольцо на поверхности среды подтверждает образование индола, что свидетельствует о наличии Е. coli в пробе воды. Наличие Е. coli можно подтвердить также по свечению содержимого емкости в УФ-свете при использовании УФ-лампы (при наличии флюорогенного субстрата в составе среды).
Оформление результатов — по 7.1.1.5.
Примечания
1 Представленные методики позволяют в течение 24 ч оценить санитарное состояние водных объектов при использовании минимально необходимого набора лабораторного оборудования, питательных сред и расходных материалов в полевых условиях.
2 Вода в изучаемом объекте, в которой выявлено бактериальное загрязнение с использованием сигнальных методов и результат превышает допустимые нормативы, подлежит дальнейшему анализу по 7.1.1 и 7.1.2 после повторного отбора пробы.
При расследовании нештатных ситуаций эпидемического характера, а также при использовании водоема для питьевого и хозяйственно-бытового водопользования или в качестве поверхностного источника воды для централизованного водоснабжения помимо определения колиформных бактерий и бактерий Е. coli проводят исследование отобранных проб воды на наличие патогенных энтеробактерий (сальмонелл) используя экспедиционный метод посева в магниевую среду накопления по методическим указаниям [2]. Для этого все компоненты магниевой среды в соответствии с прописью А.12, приложения А, вносят в две емкости, содержащие по 500 см исследуемой воды. Каждый компонент тщательно перемешивают до полного растворения и инкубируют в течение 24 ч при температуре (36±2)°С.
После инкубации посевов из емкостей с признаками роста проводят высев на одну из плотных сред: XLD-агар (А.13, приложение А) или хромогенную дифференциально-диагностическую среду Рамбах-агар (А.14, приложение А) или другую разрешенную к применению среду. Посевы инкубируют в течение 24 ч при температуре (36±2)°С.
На дифференциально-селективной среде XLD сальмонеллы образуют колонии красного цвета с черным центром за счёт образования сероводорода (H S).
На среде Рамбах-агар сальмонеллы образуют колонии красного цвета. Колиформные бактерии растут в виде сине-зеленых или сине-фиолетовых колоний. Остальные энтеробактерии и грамотрицательные бактерии, такие как Proteus, Pseudomonas, Shigella вырастают в виде бесцветных или желтоватых колоний.
Дальнейшую идентификацию выросших колоний при необходимости проводят по методическим указаниям [2] в стационарной лаборатории.
7.2 Определение бактерий энтерококков
7.2.1 Определение бактерий энтерококков с использованием мембранной фильтрации
7.2.1 1 Проведение анализа
Фильтруют 100 см пробы воды через мембранные фильтры с соблюдением требований 6.3 и 6.4. После фильтрования фильтры переносят, не переворачивая, на агаризованную плотную азидную среду Сланеца-Бертли (А.15, приложение А) или энтерококкагар (А.16, приложение А) и добиваются полного прилегания его к среде без образования пузырьков воздуха. Чашки с посевами помещают в термостат дном вверх и инкубируют при температуре (36±2)°С в течение 24 ч.
При отсутствии роста колоний инкубацию посевов продолжают до 48 ч.
После инкубации посевов учитывают колонии, характерные для бактерий энтерококков, — выпуклые, с ровными краями, темно-малиновые, розовые, светло-розовые, равномерно окрашенные или с темно-красным не четко оформленным центром и подсчитывают их число.
Очень мелкие (на пределе видимости невооруженным глазом), плоские разных оттенков, ярко-малиновые с четко выраженным малиновым центром и бесцветным ободком колонии не учитывают.
Регистрируют число колоний бактерий энтерококков или их отсутствие в журнале испытаний.
7.2.1.2 При необходимости подтверждают наличие бактерий энтерококков одним из способов, указанных ниже.
Для этого по 2-3 колонии каждого типа пересевают секторами на солевой агар с ТТХ (А.17, приложение А) и инкубируют при температуре (36±2)°С в течение 24 ч. Бактерии энтерококков на указанной среде дают равномерный нежный рост на протяжении всего штриха. Иные бактерии на этой подтверждающей среде не растут или растут на платформе штриха.
При наличии в комплектации лаборатории термостата, обеспечивающего температуру 44°С, мембранный фильтр с выросшими колониями стерильным пинцетом, не переворачивая, переносят на поверхность желчь-эскулин-азидного агара (А.18, приложение А), предварительно нагретого до 44°С, и инкубируют в течение 2 ч. В течение этого времени энтерококки гидролизируют эскулин с образованием характерных продуктов, что проявляется окрашиванием типичных для кишечных энтерококков колоний от коричневого до черного цвета.
7.2.1.4 Оформление результатов — по 7.1.1.5.
7.2.2 Определение бактерий энтерококков ускоренными методами с использованием готовых питательных сред на подложках
Подготовку подложки перед посевом, фильтрование пробы воды, инкубацию посевов проводят по 7.1.5.1.
Идентификацию бактерий энтерококков среди выросших колоний проводят по морфологии, цвету колоний в соответствии с технической документацией производителя в зависимости от используемой питательной среды.
Обработка и оформление результатов по 7.1.1.4 и 7.1.1.5.
7.2.3 Определение бактерий энтерококков сигнальным методом
Анализ проводят по 7.1.6, применяя среду для определения бактерий энтерококков в соответствии с прилагаемой инструкцией производителя. Навеску среды вносят в 100 см исследуемой воды и тщательно перемешивают до полного растворения. Посевы инкубируют в течение 18-24 ч при температуре 36°С.
Примечание — Производитель среды допускает возможность инкубировать посевы при температуре 20°С-25°С в течение 48 ч.
После инкубации посевов проводят учет результатов, при этом считают, что:
— бактерии энтерококков отсутствуют, если цвет среды не изменился или отмечено помутнение среды без изменения цвета;
— бактерии энтерококков обнаружены, если среда приобрела цвет, описанный в инструкции производителя во всем объеме или верхнем слое. При перемешивании цвет среды не должен изменяться.
Оформление результатов по 7.1.1.5.
7.3 Определение общего числа микроорганизмов
7.3.1 Определение ОМЧ методом заливки питательным агаром
7.3.1.1 Проведение анализа.
При анализе питьевой воды, прошедшей обеззараживание, или воды подземных источников в каждую из двух чашек Петри вносят по 1 см пробы без разведения.
При анализе проб воды нецентрализованного водоснабжения, поверхностного водоема или воды неизвестного уровня микробного загрязнения из каждой пробы делают посев по 1 см воды без разведения и по 1 см из 1-го и 2-го десятикратных разведений (но не менее двух объемов с разным содержанием исходной анализируемой воды), выбранных с таким расчетом, чтобы на чашках Петри выросло от 20 до 300 колоний. При этом ориентируются на результаты предыдущих исследований и санитарную обстановку в месте отбора пробы.
Разведения готовят с использованием любого из растворов, указанных в А.2 приложения А.
Посев воды проводят после тщательного перемешивания пробы. При посеве вносят по 1 см воды из пробы или соответствующих разведений в стерильные чашки Петри, слегка приоткрывая крышку. Сразу же после внесения воды в каждую чашку Петри наливают небольшое количество (5-6 см на одну чашку Петри диаметром 90 мм) расплавленного и остуженного до температуры 45°С-48°С питательного агара (А.1, приложение А) предварительно фламбируя край емкости, в которой он находился. После внесения агара содержимое чашки Петри быстро перемешивают, равномерно распределяя его по дну чашки, избегая образования пузырьков воздуха, попадания агара на края и крышку чашки и помещают на горизонтальную поверхность.
Посев и заливку посевов питательным агаром проводят между пламенем двух спиртовок с целью обеспечения условий асептики.
Не допускается применять посев разведений, приготовленных заранее.
После застывания агара чашки Петри с посевами помещают вверх дном в термостат и инкубируют в термостате при температуре (36±2)°С в течение (24±4) ч.
После инкубации посевов чашки с посевами извлекают из термостата, подсчитывают число всех выросших на чашках колоний микроорганизмов ( N ), видимых при двукратном увеличении, и регистрируют в журнале испытаний. Подсчет проводят только на тех чашках, на которых выросло от 20 до 300 колоний.
Результат допускается представлять на основании подсчета колоний на одной чашке, если на другой ползучий рост колоний распространился на всю поверхность чашки или число колоний превышает 300.
Если на всех чашках имеет место рост расплывчатых колоний, который не распространился на всю поверхность чашки, подсчитывают колонии на секторе с изолированным ростом колоний с последующим пересчетом на всю площадь чашки.
Если на чашке выросло более 300 изолированных колоний и анализ нельзя повторить, подсчитывают колонии на двух секторах, выбранных на участках чашки с максимальным и минимальным ростом, и пересчитывают на всю площадь чашки.
В этих случаях в протоколе испытаний записывают: «Число КОЕ микроорганизмов в 1 см пробы воды ориентировочное».
Если подсчет колоний на чашках невозможен за счет сплошного роста изолированных колоний, в журнале испытаний записывают: «Сплошной рост». Если на всех засеянных чашках рост расплывчатых колоний бактерий распространился на всю поверхность чашки, то в журнале испытаний делают запись: «Сливной рост».
Если ни на одной из засеянных чашек не выросло ни одной колонии, в протоколе испытаний записывают: «КОЕ микроорганизмов в 1 см пробы воды не обнаружено».
Примечание — Если рост колоний на чашках с посевами через 24 ч не обнаружен, то продолжают инкубацию посевов до 48 ч.
где — суммарное число колоний, подсчитанных на чашках и зарегистрированных по 7.3.1.1.
— общий объем исходной анализируемой воды, использованный для посева на чашки Петри, на которых велся учет, в том числе включающий объемы исходной анализируемой воды, использованной при разведении (7.3.1.1), см .
Результат округляют до двух значащих цифр и выражают числом КОЕ микроорганизмов в 1 см пробы воды.
7.3.1.3 Оформление результатов — по 7.1.1.5
7.3.2 Определение ОМЧ ускоренными методами с использованием готовых к употреблению питательных подложек
Подложку с питательной средой готовят к анализу в соответствии с технической документацией производителя и соблюдением правил стерильности.
Для определения ОМЧ анализируемую воду объемом 1 см вносят на поверхность подложки (в центр при использовании петрифильма и аккуратно опускают верхнюю пленку). Посевы инкубируют при температуре 36°С в течение 18-24 ч.
Подсчет колоний микроорганизмов на питательной подложке проводят по 7.3.1.1.
Число КОЕ микроорганизмов в 1 см анализируемой пробы воды рассчитывают по 7.3.1.2.
Оформление результатов — по 7.1.1.5.
8 Проведение посева проб воды на месте отбора проб с последующей доставкой в стационарную лабораторию
8.1 Проведение посева
Посев проб воды на месте отбора для определения колиформных бактерий, Е. coli, энтерококков и ОМЧ проводят по 7.1-7.3.
Посевы помещают в переносной термостат или термоконтейнер с температурой внутри камеры не ниже 30°С и доставляют для дальнейшего анализа в стационарную лабораторию в течение 24 ч.
В стационарной лаборатории посевы переносят в термостат при температуре (36±2)°С. Через 24 ч инкубации посевов проводят учет выросших колоний. При отсутствии роста колоний общая продолжительность инкубации посевов должна составлять 48 ч.
8.2 Подсчет и идентификацию обнаруженных микроорганизмов в посеве проб воды, учет, обработку и оформление результатов проводят в стационарной лаборатории по методам, установленным в [2]-[4].
8.3 Доставка посевов проб воды в стационарную лабораторию должна сопровождаться передачей акта отбора проб воды и документа, включающего информацию о процедуре посева: условия посева (температуру и влажность воздуха), дату и время посева, фамилию, имя и отчество лица, проводившего отбор и посев проб воды.
А.1 Приготовление питательного агара
Питательный агар готовят в стеклянной емкости из сухого препарата в соответствии с инструкцией производителя.
Емкости с готовым питательным агаром должны быть закрыты силиконовыми или ватными пробками, а сверху защищены колпачками из бумаги, пластика или фольги.
Питательный агар допускается хранить не более 1 мес при температуре не ниже 2°С и не выше 23°С.
А.2 Приготовление растворов для разведений
А.2.1 Приготовление солевого (физиологического) раствора
8,5 г хлорида натрия растворяют в 1000 см дистиллированной воды. Значение рН раствора должно быть равно 7,0±0,1. Значение рН раствора контролируют с использованием рН-метра. Раствор разливают в термостойкие стеклянные емкости и стерилизуют при температуре (120±2)°С в течение 15 мин. После стерилизации при необходимости корректируют рН раствора: значение рН раствора должно быть 7,0±0,1.
Срок хранения раствора при температуре не ниже 2°С и не выше 23°С — не более 1 мес.
А.2.2 Приготовление пептонного раствора
1 г пептона растворяют при кипячении в 1000 см дистиллированной воды. Значение рН должно быть равно 7,0±0,1. Значение рН раствора контролируют с использованием рН-метра. Раствор разливают в стеклянные емкости и стерилизуют при температуре (120±2)°С в течение 20 мин. После стерилизации при необходимости корректируют рН раствора: значение рН раствора должно быть 7,0 ±0,1.
Срок хранения раствора при температуре не ниже 2°С и не выше 23°С — не более 1 мес.
А.2.3 Приготовление пептонно-солевого раствора
8,5 г хлористого натрия и 1 г пептона растворяют при кипячении в 1000 см дистиллированной воды. Значение рН должно быть равно 7,0±0,1. Значение рН раствора контролируют с использованием рН-метра. Раствор разливают в стеклянные емкости и стерилизуют при температуре (120±2)°С в течение 20 мин. После стерилизации при необходимости корректируют рН раствора: значение рН раствора должно быть 7,0 ±0,1.
Срок хранения раствора при температуре не ниже 2°С и не выше 23°С — не более 1 мес.
А.3 Приготовление среды Эндо
Среду Эндо готовят из сухого препарата по способу, указанному производителем.
Приготовленную и охлажденную до температуры 60°С-70°С среду Эндо после тщательного перемешивания разливают в стерильные чашки Петри.
Среда, готовая к употреблению, не должна содержать следов влаги на поверхности.
Срок хранения чашек Петри со средой Эндо в стерильных светоизолирующих упаковках (например, пеналах или обернутыми плотной стерильной бумагой) при температуре 4°С-10°С — не более 7 сут.
А.4 Приготовление среды с тергитолом 7
Приготовление среды с тергитолом 7 проводят по ГОСТ 31955 (В1, приложение В) или из готового препарата по способу, указанному производителем. Готовую среду в чашках Петри хранят в защищенном от света месте при (5±3)°С не более 10 сут.
А.5 Приготовление реактивов для оксидазного теста
Реактивы для оксидазного теста готовят по одному из вариантов:
Вариант 1:
тетраметил- п -фенилендиамин гидрохлорид — 0,1 г;
дистиллированная вода — 10 см .
Реактив нестабилен и его необходимо готовить непосредственно перед испытаниями и сразу же использовать. Хранить реактив не допускается.
Вариант 2:
1%-ный спиртовой раствор -нафтола (раствор N 1).
1%-ный водный раствор диметил- п -фенилендиамина дигидрохлорида (раствор N 2).
Срок хранения растворов в емкостях из темного стекла с притертыми пробками составляет: не более 1 мес — раствора N 1; не более 7 сут — раствора N 2.
Перед использованием к 2,5 частям раствора N 1 добавляют 7,5 частей раствора N 2.
Примечания
1 Реактивы являются канцерогенными. Работу по приготовлению реактивов следует выполнять, используя маску и защитные перчатки, избегая контакта реактива с кожей.
2 Для постановки оксидазного теста допускается использовать готовые тест-системы.
А.6 Приготовление полужидкой среды с индикатором ВР и глюкозой
Полужидкую среду с глюкозой по ГОСТ 975 готовят из сухого препарата в соответствии с инструкцией производителя.
Приготовленную среду разливают в небольшие бактериологические пробирки, закрывают силиконовыми или ватными пробками, обернутыми фольгой, и стерилизуют при температуре 112°С в течение 10-12 мин.
Срок хранения приготовленной полужидкой среды при температуре 22°С-25°С — не более 20 сут.
А.8 Приготовление реактивных полосок для определения образования индола
Из фильтровальной бумаги нарезают полоски такого размера, чтобы полоска подходила для размещения под пробку бактериологической пробирки с готовой полужидкой средой с лактозой и триптофаном (см. А.7) и не касалась поверхности среды.
Готовят реактив следующим образом: в стерильную стеклянную колбу вместимостью 100 см вносят 50 см 96%-ного этилового спирта, добавляют до растворения 4 г пара -диметиламинобензальдегида, затем прибавляют 50 см ортофосфорной кислоты (очищенной концентрированной).
Нарезанные полоски из фильтровальной бумаги на 1/3 их длины опускают в колбу с реактивом и выдерживают не более 1 мин для полного смачивания реактивом указанного участка полоски. Затем полоски высушивают и упаковывают в стерильные емкости из темного стекла с притертой пробкой или плотные пакеты из черной бумаги.
Срок хранения высушенных реактивных полосок в темном месте — не более 40 сут.
Цвет обработанного участка поверхности готовой к применению реактивной полоски должен быть желтым.
Примечание — Чувствительность реактивных полосок увеличится, если этиловый спирт заменить на амиловый или изоамиловый.
А.9 Приготовление хромокульт колиформ агара для ускоренного одновременного определения Е. coli и колиформных бактерий в одном посеве
Хромокульт колиформ агар (далее — агар) готовят из сухого препарата в соответствии с инструкцией производителя.
Навеску агара помещают в стекляную или эмалированную емкость с дистиллированной водой и нагревают на кипящей водяной бане, периодически помешивая, до полного растворения препарата в течение 35 мин. Не допускается автоклавировать и перегревать.
Готовую среду охлаждают до 45°С-50°С и разливают в чашки Петри.
Срок хранения питательной среды при температуре 2°С-8°С в защищенном от света месте — не более 21 сут.
Для предотвращения от высыхания чашки со средой рекомендуется поместить в пластиковые мешки.
Готовая среда должна быть желтоватого цвета.
А.10 Приготовление сред для ускоренного определения Е. coli
А.10.1 Приготовление триптон-желчного агара (ТЖА)
Приготовление среды ТЖА проводят по ГОСТ 31955 (В.1, приложение В) или из готового препарата в соответствии с инструкцией производителя. Приготовленную среду охлаждают до температуры (50±5)°С и разливают в чашки Петри. Срок хранения — не более 10 сут в защищенном от света месте при температуре (5±3)°С.
А.10.2 Приготовление неселективного триптон-соевого агара (ТСА)
Приготовление среды ТСА проводят по ГОСТ 31955 (В.1, приложение В) или из готового препарата в соответствии с инструкцией производителя. Приготовленную среду охлаждают до температуры (50±5)°С и разливают в чашки Петри. Срок хранения — не более 10 сут в защищенном от света месте при температуре (5±3)°С.
А.11 Приготовление реактива Ковача для индольного теста для ускоренного определения Е. coli
Реактив готовят в стационарной лаборатории по ГОСТ 31955.
Состав:
пара -диметиламинобензальдегид — 0,5 г;
соляная кислота молярной концентрации 1 моль/дм — 100 см .
Реактив готовят путем растворения лара-диметиламинобензальдегида в соляной кислоте.
Срок хранения реактива — в защищенном от света месте при герметично закрытой капельнице — 1 год; после вскрытия капельницы и частичного использования — 2 мес.
Готовый раствор должен быть светло-желтого цвета; если цвет становится коричневато-желтым, реактив не используют.
А.12 Магниевая среда накопления в экспедиционной модификации
Состав:
источник