
ВИЧ (вирус иммунодефицита человека) — заболевание поражающее иммунную систему человека, вирус в течение долгого времени не проявляет себя и развивается бессимптомно, а между тем поздняя диагностика значительно понижает эффективность терапии. Последние стадии болезни ВИЧ-инфекциями приводят к развитию СПИДа – синдрома приобретенного иммунодефицита, при котором иммунная система вообще утрачивает способность справляться даже с самыми простыми болезнями. В среднем продолжительность жизни после заражения вирусом иммунодефицита составляет порядка 10-ти лет. Примерно такой же срок может длиться латентный или бессимптомный период этого заболевания.
Заражение ВИЧ-инфекцией может происходить тремя путями:
- при контактах с физиологическими выделениями больного человека (спермой, влагалищных выделениях) вследствие их попадания в кровь здорового человека; достаточно соприкосновения с небольшими повреждениями слизистых оболочек, например, при половом контакте;
- непосредственно через кровь при использовании медицинских инструментов, на которых остались следы крови больного человека, или при переливании крови;
- от матери к ребенку, как во время беременности, так и во время родов; в этом случае грудное вскармливание также приводит к инфицированию.
При этом пот, слюна, слезы, моча или фекалии больного ВИЧ-инфекцией человека не представляют угрозы для окружающих. Анализы на ВИЧ-инфекции построены на обнаружении и исследовании антител, вырабатывающихся в организме в качестве отклика на вирус иммунодефицита.
Симптомами, указывающими на наличие в организме вируса иммунодефицита, являются: регулярное обильное потоотделение по ночам, множественное увеличение лимфатических узлов, длительное расстройство пищеварения, лихорадочные состояния без видимых причин, резкая потеря веса. На фоне протекания наличия ВИЧ-инфекций в организме могут развиваться следующие заболевания:
- пневмоциститная пневмония – особый вид воспаления легких, вызванный возбудителем пневмоцистой; наличие данного заболевания характерно для больных СПИДом;
- криптококковый менингит – воспаление коры спинного и головного мозга, вызываемое обитающими в почве и испражнениях птиц грибками;
- герпес, поражающий кожные покровы и органы больного;
- кандидоз – грибковая инфекция, развивающаяся на половых органах и в полости рта;
- туберкулез;
- саркома Капоши – злокачественное новообразование на стенках кровеносных сосудов или внутренних органов;
- лимфома – опухоль, строящаяся из белых кровяных клеток и способная распространять метастазы по всему организму.
В группу сильнейшего риска заболевания вирусом иммунодефицита попадают люди, практикующие беспорядочные и незащищенные половые связи, а также наркоманы, выполняющие внутривенные инъекции.
ВИЧ-инфекции диагностируются на основе анализов крови. Характерной особенностью наличия вируса иммунодефицита является массовая гибель особого вида белых кровяных телец крови – так называемых CD4-лимфоцитов. Количество уничтоженных вирусом клеток прямо пропорционально масштабам ослабления иммунной системы больного. В нашей стране анализы крови на ВИЧ-инфекции входят в обязательный план подготовки к операциям и ведения беременности. Вопреки распространенным заблуждениям, анализ мочи не может показать ВИЧ-инфекции. Он используется как дополнительный критерий для оценки общего состояния организма при подозрении на ВИЧ.
Лабораторная диагностика при определении ВИЧ-инфекций выполняет важнейшую роль. Она включает в себя следующие этапы:
- Иммуноферментный анализ или ИФА, суть которого состоит в определении антител к вирусу иммунодефицита в организме. Несмотря на снижение защитных свойств организма, в нем вырабатываются некоторые количества антител к ВИЧ-инфекциям, и наличие этих антител прямо подтверждает предполагаемый диагноз.
- Установить наличие антител к вирусу иммунодефицита можно также методом иммуноблоттинга. Этот метод является более точным, чем ИФА, и поэтому часто используется в качестве дополнительной проверки полученных результатов.
- На ранних стадиях заболевания особенно эффективен анализ крови методом полиразмерной цепной реакции или ПЦР. В ходе этого исследования выявляется ДНК возбудителя.
- Обязательно выполняется анализ на определение количества CD4-лимфоцитов. Темпы уменьшения количества CD4-лимфоцитов в крови иллюстрируют динамику снижения иммунитета.
- При выполнении теста на вирусную нагрузку оценивается количество единиц вируса в крови.
Если диагноз подтвержден, назначаются исследования для оценки общего состояния организма: проверяется эффективность работы почек и печени. Для этого потребуется сдать анализ мочи при ВИЧ-инфицировании. Перед тем, как сдавать анализ мочи при ВИЧ, позаботьтесь о том, чтобы результаты этого исследования были корректными. Поскольку в результатах анализ мочи при ВИЧ, прежде всего, нужно отследить воспалительные процессы, проявляющиеся в повышении уровня лейкоцитов, появлении бактерий и слизи, обеспечьте непосредственно перед процедурой чистоту половых органов.
Кроме того, чтобы анализ мочи при ВИЧ мог показать истинное положение вещей и чтобы не усугублять ситуацию, собирайте только среднюю порцию мочи, а первую и последнюю – сливайте. Если в анализе мочи при ВИЧ обнаружится избыточное количество солей, то вполне вероятно врач назначит дополнительную микроскопию солевого осадка для определения специфики работы почек. Показательными факторами в результатах анализа мочи при ВИЧ являются мочевина и креатинин в сыворотке. Они являются итоговыми продуктами белкового обмена, которые должны выводиться из организма с помощью почек. Если почки работают плохо, концентрация этих веществ в результатах анализа мочи при ВИЧ повышена.
Для оценки функционирования печени исследуют количество печеночных ферментов — аланинаминотрансферазы (АЛТ) в крови. При заболеваниях печени количество этих ферментов в крови повышается.
Таким образом, ВИЧ и анализ мочи в диагностическом смысле никак не связаны друг с другом, и анализ мочи не может показать наличие этого заболевания.
В соответствии с пунктом 2 статьи №8 ФЗ РФ № 38-ФЗ от 30 марта 1995 г. (Федеральный закон «О предупреждении распространения в Российской Федерации заболевания, вызываемого вирусом иммунодефицита человека (ВИЧ-инфекции)», с изменениями и дополнениями), каждый из нас имеет право на анонимную диагностику, в частности, сдачу анализа на ВИЧ-инфекции. Сам факт обращения за медицинской помощью ни при каких обстоятельствах не подлежит разглашению.
источник
Заболевания органов мочеполовой системы на фоне ВИЧ-инфекции — актуальная проблема современного здравоохранения

В статье отражены результаты ретроспективного анализа оказания урологической помощи 352 ВИЧ-инфицированным больным в ГКУБ № 47 ДЗМ за период 1996–2012 гг. Выполнена оценка динамики поступлений ВИЧ-инфицированных пациентов в урологический стационар, изучен
В настоящее время инфекция, вызванная вирусом иммунодефицита человека (ВИЧ), является одной из наиболее актуальных проблем здравоохранения. Достаточно отметить, что в результате инфекционного процесса, обусловленного ВИЧ, у больного в среднем через 12 лет после заражения развивается фатальный синдром приобретенного иммунодефицита (СПИД) [1].
На сегодняшний день создалась крайне благоприятная ситуация для распространения этой «медленной» инфекции. В естественных условиях основным сдерживающим фактором распространения «медленных» инфекций являются инфекции «быстрые», жизненный цикл которых успевает завершиться до формирования иммунного ответа. В случае отсутствия адекватного иммунного ответа у заболевшего значительно увеличиваются шансы погибнуть и тем самым прекратить распространение возбудителя «медленной» инфекции. Подавляющее большинство «быстрых» инфекций превосходно лечатся антимикробными средствами, некоторые из них легко предотвращаются вакцинопрофилактикой. Причем при классических инфекционных болезнях достаточно редко возникает проблема антибиотикорезистентности. Из «естественных врагов» ретровирусов, к которым относится и ВИЧ, в настоящее время достойна упоминания только микобактерия туберкулеза. Однако и она неплохо поддается медикаментозной терапии, причем даже в условиях иммуносупрессии и приобретенного иммунодефицита. Все это сочетается со сравнительно малопродуктивными противоэпидемическими мероприятиями. Например, в РФ нет прямого запрета на немедицинское применение наркотических средств, а это один из важнейших путей инфицирования. В результате число ВИЧ-инфицированных больных прогрессивно растет, а сам возбудитель уже давно вышел за пределы групп риска в общую популяцию.
В России ВИЧ-инфекция впервые была выявлена в 1987 году, с 1996 года заболеваемость приняла характер эпидемии. К середине 2003 года в Российской Федерации зарегистрировано более 250 тысяч ВИЧ-инфицированных [2].
По данным В. В. Покровского к 2007 году количество ВИЧ-инфицированных только в Российской Федерации достигло 370 тысяч человек. Около 60% случаев ВИЧ-инфицирования среди россиян приходится на 11 из 86 российских регионов (Иркутская, Саратовская, Калининградская, Ленинградская, Московская, Оренбургская, Самарская, Свердловская и Ульяновская области, Санкт-Петербург и Ханты-Мансийский автономный округ). Количество больных ВИЧ-инфекцией в стране за период с 1987 по 2008 гг. превысило 400 тыс. человек [3].
В последнее время в России ежегодно увеличивается число случаев заражения в результате «незащищенных» половых контактов и случаев распространения ВИЧ от ВИЧ-инфицированной матери к ребенку. Это свидетельствует о том, что эпидемия ВИЧ-инфекции/СПИДа в России начинает затрагивать не только группы высокого риска, но и широкие слои населения. По данным Федерального научно-методического центра СПИД на 01.01.2010 г. в России зарегистрированы 516 167 людей с ВИЧ. По данным, опубликованным ВОЗ/ЮНЭЙДС (2010), реальное количество случаев ВИЧ-инфекции в России приближается к одному миллиону [4].
По данным Федерального научно-методического центра по профилактике и борьбе со СПИДом общее число россиян, инфицированных ВИЧ, зарегистрированных в РФ до 1 ноября 2011 г., составило 636 979 человек. За 10 месяцев 2011 года территориальными центрами по профилактике и борьбе со СПИДом было сообщено о 48 363 новых случаях ВИЧ-инфекции среди граждан Российской Федерации. Ориентировочное число зарегистрированных за 2011 г. новых случаев ВИЧ-инфекции составляет более 62 тыс. [5] и превосходит почти в 2 раза прогнозное значение этого показателя, указанное в 2007 году [6].
На слушаниях 2012 года в Общественной палате Российской Федерации, посвященных мерам по противодействию ВИЧ-инфекции в России и роли отечественных некоммерческих организаций в этой деятельности, отмечалась ошибочность положения о стабилизации эпидемического процесса, так как ежегодный прирост заболевших составляет более 10%, число обследованных снижается, а число выявленных больных растет [3].
Разработки и широкое применение этиотропной терапии привели к значительному повышению выживаемости и улучшению качества жизни ВИЧ-инфицированных пациентов. Продолжительность жизни при условии адекватного подбора антиретровирусных препаратов и постоянного контроля за их эффективностью достигла 20 лет [1]. Однако ВИЧ продолжает быть значимым источником патологических изменений практически во всех системах организма, не исключая и мочеполовую сферу [7].
Несмотря на доказанную корреляцию между высокой частотой новообразований и выраженностью иммунодефицита, обусловленного ВИЧ-инфекцией, основной причиной смерти ВИЧ-инфицированных являются генерализованные инфекционные процессы [8, 9].
Иммунодефицит, обусловленный вирусом иммунодефицита человека, создает предпосылки для развития инфекционно-воспалительных процессов с атипичной клинической картиной и широким спектром возможных возбудителей [7]. Для любого выраженного иммунодефицита характерны микобактериозы, в том числе и туберкулез. Возможны грибковые и вирусные поражения. Что касается микозов и микобактериозов при ВИЧ-инфекции, то эта проблема настолько актуальна, что в настоящее время инфекционистами разработаны четкие критерии начала специфической профилактики и ее методики в зависимости от выраженности иммунодефицита [1].
Одна из первых классификаций ВИЧ-инфекции, рекомендованных ВОЗ (1988), рассматривала 4 стадии болезни. Все классификации более позднего времени, по сути, модернизируют ее, сохраняя основные положения. Эта классификация выделяла стадии: 1) начальная (острая) ВИЧ-инфекция, 2) персистирующая генерализованная лимфаденопатия, 3) СПИД-ассоциированный комплекс — преСПИД, 4) развернутый СПИД.
В Российской Федерации используется классификация ВИЧ-инфекции, предложенная В. И. Покровским. Первоначальный вариант ее был принят в 1989 году, а через 11 лет (2001) была составлена новая версия классификации. Согласно новой классификации, заболевание, обусловленное ВИЧ-инфекцией, последовательно проходит 5 стадий:
Стадия инкубации (стадия 1)
С момента заражения до клинических проявлений острой инфекции и/или выработки антител (в среднем от 3 недель до 3 месяцев).
Стадия первичных проявлений (стадия 2)
2«А» — бессимптомная, когда клинические проявления ВИЧ-инфекции или оппортунистических заболеваний отсутствуют, а ответом на внедрение ВИЧ является выработка антител.
2«Б» — острая ВИЧ-инфекция без вторичных заболеваний (разнообразные клинические проявления, в большинстве своем похожие на симптомы других инфекций).
2«В» — острая ВИЧ-инфекция с вторичными заболеваниями (на фоне временного снижения CD4+ лимфоцитов развиваются вторичные заболевания — ангина, бактериальная пневмония, кандидоз, герпес — как правило, хорошо поддающиеся лечению). Продолжительность клинических проявлений острой ВИЧ-инфекции обычно составляет 2–3 недели.
Стадия латентная (стадия 3)
Медленное прогрессирование иммунодефицита. Единственным клиническим проявлением является увеличение лимфоузлов, которое может и отсутствовать. Длительность латентной стадии от 2–3 до 20 и более лет, в среднем 6–7 лет. Отмечается постепенное снижение уровня CD4+ лимфоцитов.
Стадия вторичных заболеваний (стадия 4)
Продолжается репликация ВИЧ, приводящая к гибели CD4+ лимфоцитов и к развитию на фоне иммунодефицита вторичных (оппортунистических) заболеваний, инфекционных и/или онкологических. Симптомы на этой стадии имеют обратимый характер, то есть могут проходить сами по себе или в результате лечения. В зависимости от тяжести вторичных заболеваний выделяют следующие подстадии:
4«А» стадия — характерны бактериальные, грибковые и вирусные поражения слизистых и кожных покровов, воспалительные заболевания верхних дыхательных путей.
4«Б» — более тяжелые и длительные кожные поражения, саркома Капоши, потеря веса, поражения периферической нервной системы и внутренних органов, но без генерализации.
4«В» — тяжелые, угрожающие жизни оппортунистические заболевания.
Терминальная стадия (стадия 5)
Крайне тяжелый иммунодефицит, прогрессирующие, часто инкурабельные необратимые поражения внутренних органов.
По мнению автора, новая классификация более полно отражает стадии клинического течения ВИЧ-инфекции, поскольку стадии 2«Б» и 2«В» (по классификации 1989 года) отличаются друг от друга лишь выраженностью увеличения лимфатических узлов и не отличаются по прогностическому значению и тактике ведения больных [1].
Остается много спорного, неоднозначно трактуемого и условного в вопросах клинической оценки стадии болезни, определении понятий «СПИД-ассоциируемые заболевания», «СПИД-индикаторные болезни», «Стадия СПИД». Все еще нет устоявшегося во времени и одобренного научным сообществом консенсуса. К примеру, нет единства в определении состояний, расцениваемых как фаза «СПИД» и фаза «Пре-СПИД» или «СПИД-ассоциируемый комплекс».
Всем очевидно, что уровень CD4+ лимфоцитов является важным, ключевым, но не абсолютным критерием при определении стадии заболевания, обусловленного ВИЧ-инфекцией. Однако на этом согласие кончается.
Например, на сегодняшний день Центр по контролю и профилактике заболеваний США (англ. Centers for Disease Control and Prevention, CDC) активно выступает против добавления новых ВИЧ-ассоциированных состояний в определение понятий «СПИД», так как, по мнению специалистов Центра ориентироваться целесообразно на объективный критерий — количество Т-хелперов, а не на клинические критерии, ибо многие из этих состояний могут встречаться у лиц, не инфицированных ВИЧ. А в 1998 году этот же Центр занимал диаметрально противоположную позицию, предлагая расширить список СПИД-ассоциированных заболеваний. «Диагноз СПИДа правомерен, если: у ВИЧ-инфицированного диагностировано минимум одно из 23 СПИД-ассоциированных состояний и уровень СD4+ клеток менее 200/мл» [37]. В настоящее время такой уровень СD4+ клеток является одним из показаний к началу этиотропной антивирусной терапии, то есть это — далеко не терминальный иммунодефицит и далеко не всегда пессимистический прогноз. Значит, все решают клинические проявления?
В связи с резким ростом числа ВИЧ-инфицированных возник вопрос об организации монопрофильной медицинской помощи этой специфической категории больных. Причем эта проблема затрагивает не только врачей-инфекционистов, непосредственно проводящих антиретровирусную терапию, но и специалистов смежных дисциплин. Так, согласно Приказу № 404 Департамента здравоохранения г. Москвы от 28.06.96 «О дополнительных мерах по совершенствованию профилактики ВИЧ-инфекции в г. Москве» специализированную урологическую помощь ВИЧ-инфицированным больным оказывала городская урологическая больница № 47. В связи с ее реорганизацией и сменой профиля функции городского учреждения по оказанию урологической помощи ВИЧ-инфицированным больным с 01.09.2012. переданы ГКБ № 70.
Серьезный интерес к указанной проблеме в урологической среде появился только в 2009–2010 годах, когда популяция ВИЧ-инфицированных выросла настолько, что обращаться за стационарной урологической помощью они стали регулярно, и число их поступлений составило не менее 60–70 в год. Эта цифра свидетельствует о том, что каждый врач клиники в среднем за год пролечивал, в том числе и хирургическими методами, не менее 2 ВИЧ-инфицированных больных. Если раньше поступление ВИЧ-инфицированного было настолько редким явлением, что определение тактики его лечения обычно оценивалось консилиумом смежных специалистов, то в последнее время подобные вопросы решаются на уровне лечащего врача, заведующего отделением и службы клинической фармакологии.
Одновременно стала вероятной и ситуация, когда ВИЧ-инфицированный пациент по витальным показаниям госпитализируется в другую урологическую клинику. Действующее законодательство обязывает специализированные отделения оказывать экстренную урологическую помощь всем больным, не зависимо от наличия сопутствующих заболеваний. Поэтому в современных условиях вопрос о лечении ВИЧ-инфицированного пациента может быть поставлен перед каждым практикующим врачом-урологом.
На сегодняшний день у авторов накоплен достаточно большой клинический материал по проблеме урологических заболеваний на фоне ВИЧ-инфекции, насчитывающий 352 пациента, что позволяет проводить обобщения и делать выводы.
Оказание урологической помощи ВИЧ-инфицированным имеет свои особенности. Если техника выполнения хирургических вмешательств у этой категории больных существенных изменений не претерпевает, то терапевтическая составляющая меняется радикально. Мало кто из практикующих врачей-урологов в состоянии внятно ответить на вопросы, как меняется клиническая картина урологических заболеваний в зависимости от степени выраженности иммунодефицита и как это отражается на медикаментозной терапии, каковы возможные лекарственные взаимодействия между препаратами, направленными на подавление ВИЧ, и средствами, применяемыми для лечения урологических заболеваний, и т. д.
Для практической работы необходимо отметить следующие ключевые моменты, касающиеся ВИЧ-инфицированных пациентов любого профиля (не только урологического):
- ВИЧ-инфицированный вне зависимости от стадии инфекционного процесса и клинических проявлений является больным — носительства ВИЧ не бывает.
- Латентная стадия ВИЧ-инфекции — это не аналог ремиссии: на протяжении этой стадии происходит размножение вируса и постепенное подавление иммунитета до определенного критического уровня, по достижении которого при естественном течении заболевания происходит гибель пациента от инфекционно-воспалительных, реже опухолевых процессов вследствие неадекватного иммунного ответа, что носит название СПИД.
Антиретровирусная терапия существенно замедляет прогрессирование заболевания, но остановить его развитие и добиться излечения пациента она не в состоянии. Препараты антиретровирусной терапии обладают сравнительно высокой токсичностью, чаще печеночной или костномозговой, в разы, а иногда и в десятки раз превосходящей токсичность средств, применяемых в урологии. Заболевания органов мочеполовой системы не являются показанием к отмене антиретровирусной терапии, поэтому актуальной становится проблема лекарственных взаимодействий.
Ввиду сниженной реактивности организма сильно меняется клиническая картина и течение сопутствующих заболеваний. Можно отметить:
- выраженную тенденцию к затяжному течению с малой активностью;
- повышенный риск инфекционно-воспалительных осложнений;
- актуальность редких и атипичных возбудителей, практически не встречающихся у больных с условно нормальным иммунитетом (например, острый пиелонефрит, обусловленный зеленящим стрептококком или гонококком, кандидоз мочевого пузыря, мочеточника и даже почечной лоханки, актиномикоз почки и т. д.);
- низкую информативность общепринятых критериев эффективности терапии (например, ВИЧ-инфицированный может иметь субфебрильную лихорадку, изменения в анализах крови и мочи на протяжении недель и месяцев, и это зачастую никак не связано с его простатитом или пиелонефритом).
ВИЧ-инфицированный вне зависимости от стадии инфекционного процесса и клинических проявлений представляет потенциальную опасность для окружающих, в том числе и для персонала ЛПУ. Опасность эта тем актуальнее, что ВИЧ-инфекция не излечивается, а медикаментозная профилактика не гарантирует предотвращение заражения при травмах, нанесенных загрязненным инструментарием, хотя и существенно снижает его риск.
ВИЧ крайне нестоек во внешней среде, чувствителен ко всем дезинфектантам и, наоборот, феноменально устойчив в биологических жидкостях — крови, лимфе и т. д., что в сочетании с неизлечимостью заболевания, им обусловленного, предъявляет особые требования к дезинфекции и мерам безопасности. При травмах, нанесенных загрязненным инструментарием, наиболее принципиальное требование к профилактическим мероприятиям — кратчайшие сроки их начала. Если риск заражения был признан высоким и принято решение о медикаментозной профилактике, то начинать ее необходимо в течение первых суток с момента возможного контакта с ВИЧ.
Для адекватной монопрофильной помощи ВИЧ-инфицированным клиника должна обладать персоналом, имеющим опыт ведения таких больных, соответственным лекарственным обеспечением (в частности, средствами заместительной иммунной терапии, резервными антибактериальными и противогрибковыми препаратами), а также возможностью экстренной консультации инфекционистом — специалистом по ВИЧ-инфекции. При отсутствии всего вышеперечисленного возможна лишь экстренная помощь, преимущественно небольшого объема. В этой ситуации нецелесообразно браться за оперативные вмешательства большого объема, особенно реконструктивные — даже при безупречной оперативной технике результаты часто неудовлетворительны вследствие высокого риска инфекционно-воспалительных осложнений и их стойкости к медикаментозной терапии.
Изучены статистические данные за 2008–2010 гг., когда наметился резкий рост числа этих больных. За указанный период в ГКУБ № 47 пролечено 153 ВИЧ-инфицированных пациента с урологическими заболеваниями.
Основная причина обращения ВИЧ-инфицированных пациентов за стационарной урологической помощью — острые инфекционно-воспалительные заболевания мочеполовых органов — 59,5% поступлений.
При этом частоты встречаемости острых воспалительных поражений почек и мужских половых органов примерно одинаковы — 26,8% и 32,7% соответственно. Существенное место в структуре урологической заболеваемости ВИЧ-инфицированных занимает мочекаменная болезнь без клинических проявлений острого воспалительного процесса (почечная колика), частота которой составляла 23,5% (рис. 1).
Несмотря на доказанное увеличение частоты новообразований на фоне иммунодефицита, опухоли органов мочеполовой системы, как доброкачественные, так и злокачественные, у ВИЧ-инфицированных встречаются нечасто. На долю аденомы простаты приходится всего 2,6% от общего числа поступивших ВИЧ-инфицированных. Рак мочевого пузыря и простаты на фоне ВИЧ-инфекции представлен единичными наблюдениями. Малая частота новообразований мочеполовых органов может быть объяснена тем, что большинство больных не доживают до этой патологии, погибая от генерализованных инфекционных процессов или хронических интоксикаций (многие пациенты продолжали принимать наркотические средства вплоть до момента госпитализации) [1, 11].
Важным является факт, что 92,2% пациентов были госпитализированы по экстренным показаниям с экстренной урологической патологией. В плановом порядке госпитализировано всего 12 человек (7,8%). Показаниями к плановой госпитализации послужили мочекаменная болезнь, аденома простаты, гидронефроз. Указанные заболевания при определенных условиях (острая задержка мочеиспускания, гематурия) также могут повлечь за собой экстренную госпитализацию.
Учитывая большую социальную значимость и недостаточную изученность целесообразно подробнее остановиться на заболеваниях нижних мочевых путей и мужских половых органов на фоне ВИЧ-инфекции.
С 1996 года по май 2011 года урологическая помощь была оказана 159 ВИЧ-инфицированным пациентам, страдающим заболеваниями нижних мочевых путей и мужских половых органов.
Распределение урологических нозологий в изучаемой группе пациентов имеет принципиальные отличия по сравнению с общей популяцией больных. У ВИЧ-инфицированных доминируют острые инфекционно-воспалительные заболевания органов мошонки, на долю которых приходится 51% поступлений, что в 2,15 раза превышает частоту острого простатита (23,7%). Согласно нашим данным за 2011 год в общей популяции частота «первичного», то есть не связанного с инвазивными вмешательствами, острого простатита в 2,7 раза превышает частоту «первичного» острого эпидидимита и орхоэпидидимита, вместе взятых. Таким образом, можно отметить выявленную склонность ВИЧ-инфицированных к острым инфекционно-воспалительным заболеваниям мошонки.
Также целесообразно обратить внимание на сравнительно небольшой вклад острого цистита в структуру урологической заболеваемости на фоне иммунодефицита, обусловленного ВИЧ.
На рис. 2 отражена динамика числа поступлений ВИЧ-инфицированных больных по наиболее актуальным у этой категории пациентов урологическим нозологиям, которая наглядно демонстрирует ранее отмеченные тенденции. Рост числа ВИЧ-инфицированных лиц, требующих урологической помощи, происходит главным образом за счет острых инфекционно-воспалительных нозологий — пиелонефрита, эпидидимита и эпидидимоорхита, в меньшей степени простатита.
Таким образом, основная проблема лечения урологических больных с сопутствующей ВИЧ-инфекцией — это назначение адекватной эмпирической антимикробной терапии и оказание экстренной хирургической помощи.
На сегодняшний день вопрос взаимосвязи между стадией ВИЧ-инфекции и особенностями течения урологических заболеваний все еще остается дискутабельным и требует дальнейшего изучения. По мнению ведущего отечественного специалиста по проблеме ВИЧ-инфекции В. В. Покровского, «развитие у ВИЧ-инфицированных какого-либо заболевания, даже в тяжелой форме, не означает, что эта болезнь как-то связана с ВИЧ-инфекцией и указывает на нее. Лишь четко определенные клинические формы весьма ограниченной группы заболеваний… являются достоверными признаками снижения иммунитета, вызванного ВИЧ-инфекцией, и то лишь в том случае, если исключены другие факторы, угнетающие иммунную систему» [1]. Эти указанные автором «определенные клинические формы» носят название «Определенно индикаторные для СПИДа болезни». Урологические заболевания в данный список не входят.
Однако для практической работы необходимо знать, что «Клиническая классификация ВИЧ-инфекции», предложенная В. И. Покровским (2001), относит «повторные или стойкие бактериальные поражения внутренних органов без диссеминации» к стадии 4«Б», а при наличии генерализации к 4«В».
Урологических пациентов, находящихся в инкубационном периоде ВИЧ-инфекции и острой фазе заболевания, мы не наблюдали. Основная масса ВИЧ-инфицированных, обращающихся за стационарной урологической помощью, находится в бессимптомной фазе (стадия 3) и стадии вторичных проявлений (4«А» и 4«Б») — 43,9%, 26,7%, 20,2% соответственно. Терминальные пациенты, имеющие диссеминированные микробные или опухолевые поражения, обусловленные тяжелым иммунодефицитом (стадии 4«В» и 5), в поле зрения уролога попадают редко (7,8% и 0,8% от общего числа поступлений ВИЧ-инфицированных соответственно).
Таким образом, не менее 46,9% обратившихся за урологической помощью ВИЧ-инфицированных пациентов имели выраженный, но нетерминальный, нефатальный иммунодефицит (стадии 4«А» и 4«Б»), который оказывал влияние на характер течения урологических заболеваний, особенно инфекционно-воспалительных поражений органов мочеполовой системы.
Эффективность эмпирической антибактериальной терапии неспецифических инфекционно-воспалительных заболеваний органов мочеполовой системы у ВИЧ-инфицированных пациентов
Иммунодефицит, обусловленный ВИЧ, создает предпосылки для развития инфекционно-воспалительных процессов с атипичной клинической картиной и очень широким спектром возможных возбудителей. Свою роль играет и внутривенная наркомания значительной доли пациентов, которая является отдельным фактором риска гематогенных инфекций, в том числе и органов мочеполовой системы. Для любого выраженного иммунодефицита характерны микобактериозы, в том числе и туберкулез, а также грибковые и вирусные поражения [1, 11].
Таким образом, наиболее принципиальным требованием к эмпирической антибактериальной схеме является широкий спектр действия. При этом если больной не принимал антибактериальные препараты в течение длительного времени, не подвергался оперативным вмешательствам и инвазивным методам исследования, то наличие полирезистентной микрофлоры маловероятно.
Вопросы эмпирической терапии инфекционно-воспалительных заболеваний органов мочеполовой системы на фоне ВИЧ-инфекции вплоть до настоящего времени во многом остаются дискутабельными [11–13]. Отсутствие регламентирующей документации, а также общепринятого научным сообществом единого мнения по этому вопросу привело к бесконтрольному применению самых разнообразных антибактериальных средств. В результате сейчас мы имеем данные по практически всем фармакологическим группам антибактериальных препаратов, которые возможно применять для лечения неспецифических инфекционно-воспалительных заболеваний у ВИЧ-инфицированных пациентов.
Был проведен ретроспективный анализ эффективности различных антибактериальных препаратов, назначаемых в эмпирическом режиме, для лечения острого пиелонефрита, острого простатита и острых эпидидимита и эпидидимоорхита на фоне ВИЧ-инфекции.
Критерием включения в анализ был факт установления диагноза одного из вышеуказанных заболеваний у пациента, имеющего документальное подтверждение сопутствующей ВИЧ-инфекции.
Критериями исключения из исследования послужили сопутствующие инфекционно-воспалительные заболевания другой локализации, требующие антибактериальной терапии, а также тяжелые гнойно-деструктивные поражения, являющиеся показаниями к немедленному хирургическому удалению органа.
За период с июня 1996 года по май 2012 года указанным критериям ответили 212 пациентов с пиелонефритом на фоне ВИЧ-инфекции, 28 больных простатитом и 54 мужчины, страдавших острым эпидидимитом или эпидидимоорхитом.
Лекарственное средство считалось эффективным, если на фоне его применения удалось подавить активность инфекционно-воспалительного процесса и достичь излечения (снятия диагноза) в случае острого заболевания или ремиссии в случае хронического заболевания.
При эмпирической антибактериальной терапии пиелонефрита на фоне ВИЧ-инфекции наиболее высокую эффективность продемонстрировали антибактериальные препараты резерва — карбапенемы и антисинегнойные цефалоспорины — 81,8% и 76,5% соответственно (рис. 3). Из нерезервных антибактериальных средств практически одинаковую эффективность показали фторхинолоны (70,7%) и комбинированная схема, включающая неантисинегнойный цефалоспорин III поколения и аминогликозид (69,4%). На монотерапии ингибиторзащищенными аминопенициллинами положительная динамика отмечена только у 61,9% пациентов. Результаты раздельного применения неантисинегнойных цефалоспоринов III поколения и аминогликозидов II–III поколения еще хуже — 47,8% и 41,7% соответственно.
При лечении острого простатита на фоне ВИЧ-инфекции эффективность антибактериальных средств в целом аналогичная — 100% у карбапенемов, 83,3% у антисинегнойных цефалоспоринов, 80% у комбинированной схемы, включающей неантисинегнойный цефалоспорин III поколения и аминогликозид, 71,4% у фторхинолонов, 66,7% у аминогликозидов в режиме монотерапии, 50% у неантисинегнойных цефалоспоринов III поколения и 33,3% у аминогликозидов II–III поколения (рис. 4).
При оценке результатов лечения острых инфекционно-воспалительных заболеваний органов мошонки на фоне ВИЧ-инфекции обращает на себя внимание в целом более низкая эффективность лекарственной терапии, не превышающая 75% даже при стартовом назначении антибиотиков резерва — карбапенемов (рис. 5). Антисинегнойные цефалоспорины практически равноэффективны фторхинолонам и ингибиторзащищенным аминопенициллинам (68,8%, 70%, 66,7% соответственно). Использование антибактериальных средств других групп приводит к положительной динамике в еще меньшем проценте случаев — 45,5% при одновременном применении неантисинегнойных цефалоспоринов III поколения и аминогликозидов, 37,5% и 50% соответственно при раздельном назначении вышеупомянутых антибиотиков.
Анализ полученных результатов лечения неспецифических инфекционно-воспалительных заболеваний органов мочеполовой системы на фоне ВИЧ-инфекции в целом подтверждает ранее выдвинутые предположения о необходимости назначения антибактериальных средств возможно более широкого спектра действия. Наблюдавшиеся единичные неудачи при стартовом применении карбапенемов и антисинегнойных цефалоспоринов по всей вероятности связаны с энтерококковой инфекцией. Вместе с тем широкое применение указанных антибактериальных средств нецелесообразно по эпидемиологическим соображениям, из необходимости предотвращения селекции госпитальных полирезистентных штаммов возбудителей [3]. Неприемлемо низкая эффективность антиграмотрицательных препаратов (неантисинегнойных цефалоспоринов и особенно аминогликозидов) также наводит на мысль о частой грамположительной инфекции.
Из нерезервных препаратов удовлетворительный эффект продемонстрировали фторхинолоны и сочетание неантисинегнойных цефалоспоринов с аминогликозидами. В обоих случаях, несмотря на ярко выраженную антиграмотрицательную направленность, имеется клинически значимая активность в отношении грамположительной флоры — стафилококка у фторхинолонов, стрептококка и в меньшей мере стафилококка у комбинированной схемы, включающей цефалоспорин и аминогликозид (в последнем случае наблюдается эффект синергизма между двумя препаратами) [14].
Отсутствие явных преимуществ фторхинолонов перед бета-лактамами позволяет предположить о незначительном вкладе внутриклеточных возбудителей в структуру экстренной урологической заболеваемости на фоне ВИЧ-инфекции.
Теоретически еще более эффективным сочетанием должно являться одновременное назначение ингибиторзащищенных аминопенициллинов и аминогликозидов, особенно амикацина. Здесь в спектре практически вся негоспитальная флора, как грамположительная, так и грамотрицательная. Однако, на наш взгляд, основная ценность ингибиторзащищенных аминопенициллинов для урологической клиники заключается в их высокой активности в отношении энтерококка, который иногда выступает в роли возбудителя суперинфекции, особенно у тяжелых и осложненных пациентов. Поэтому от широкого применения ингибиторзащищенных аминопенициллинов для лечения инфекционно-воспалительных заболеваний органов мочеполовой системы целесообразно воздержаться.
- Покровский В. В., Юрин О. Г., Беляева В. В. Клиническая диагностика и лечение ВИЧ-инфекции. М.: ГЭОТАР-Медицина, 2000. 489 с.
- Онищенко Г. Г. Эпидемия ВИЧ-инфекции на современном этапе и основные задачи по противодействию ее распространению / Материалы III Рос. научн.-практ. конф. по вопросам ВИЧ-инфекции и парентеральных гепатитов. Суздаль, 2003. С. 2–5.
- Покровский В. В. Современная ситуация по ВИЧ-инфекции в Российской Федерации / Материалы выступления на слушаньях в Общественной палате Российской Федерации 30 марта 2012 г. [Электронный ресурс]. URL: http://www.oprf.ru/files/dok2012/pokrovskiy30032012.pps.
- Абашина В. Л., Хомичук Т. Ф., Гребенькова Л. К., Евдокимова Л. П., Смирнова Н. Р., Семейкина Л. М. Эпидемиологические аспекты заболеваемости вич-инфекцией // Здоровье. Медицинская экология. Наука 1–2 (41–42). 2010. С. 114–116.
- Справка. ВИЧ-инфекция в Российской Федерации в 2011 г. Федеральный научно-методический Центр по профилактике и борьбе со СПИДом, 2011. [Электронный ресурс]. URL: http://www.hivrussia.ru/stat/2011.shtml.
- Краткая характеристика действующей и (или) планируемой бюджетной целевой программы, в части, касающейся отчетного периода: ФЦП «Предупреждение и борьба с социально значимыми заболеваниями (2007–2011 годы)»: Приложение № 4 к Докладу о результатах и основных направлениях деятельности Минздравсоцразвития России на 2008 год и на период до 2010 года. [Электронный ресурс]. URL: http://www.minzdravsoc.ru/ministry/budget.
- Lee L. K., Dinneen M. D., Ahmad S. The urologist and the patient infected with human immunodeficiency virus or with acquired immunodeficiency syndrome // BJU Int. 2001; 88: 500–510.
- Francum B. S., Savdie E. HIV and Renal Disease / Ed. G. Stewart. Managing HIV. 1997. P. 94.
- UNAIDS/WHO. Report of Global HIV/AIDS Epidemics. Geneva, 1994. 53 p.
- Center for Disease Control and Prevention. 1998 guidelines for treatment of sexually transmitted disease // Morbidity Mortality Weekly Report. 1998; 47: 1–116.
- Marin B., Thiebaut R., Bucher H. C. et al. Non-AIDS defining deaths and immunodeficiency in the era of combination antiretroviral therapy // Aids. 2009; 23: 1743.
- Breyer B. N., van Den Eeden S. K., Horberg M. A., Eisenberg M. L., Deng D. Y., Smith J. F., Shindel A. W. HIV Status is An Independent Risk Factor for Reporting Lower Urinary Tract Symptoms // The Journal of Urology. 2011. Vol. 185, 1710–1715.
- Wyatt M. Ch., Morgello S., Katz- Malamed R., Wei C., Klotman M. E., Klotman P. E., Dagati V. D. The spectrum of kidney disease with AIDS in the era of antiretroviral therapy // Kidney International. 2009, 75, 428–434.
- Практическое руководство по антиинфекционной химиотерапии / Под ред. Страчунского Л. С., Белоусова Ю. Б., Козлова С. Н. Смоленск: МАКМАКС, 2007. 464 с.
С. К. Яровой 1 , доктор медицинских наук
М. В. Странадко
ФГБУ НИИ урологии МЗ РФ, Москва
Abstract. The article presents results of multidimentional retrospective analysis of urinological aid provisioning to 352 HIV patients of SCUH No 47 of Health Protection Department of Moscow during the period of 1996-2012. Dynamics of HIV patients going to urinological hospital has been analyzed, distribution of these patients for urinological nosologies and HIV stages have been studied. The article also reviews effectiveness of the main pharmacological groups of antibacterial preparations for treatment of non-specific infectious-inflammatory urogenital system diseases against HIV.
источник
У каждого есть ВИЧ-статус, только у одних он положительный, а у других — отрицательный. Однако знать его необходимо, особенно в российских реалиях, когда в стране эпидемия, и уже более одного процента населения живет с вирусом.
Для диагностики вируса иммунодефицита человека существует несколько видов тестов, причем их классификация сложна лишь на первый взгляд, на самом деле она весьма логична. Главное — помнить, что, несмотря на высокую точность анализов, ни один тест не найдет вирус сразу после заражения.
Скрининговые (поисковые) тесты
Они помогают заподозрить инфекцию, но их результаты надо подтверждать другими анализами. Для скрининга используют тесты либо на антитела, либо на антигены/антитела.
ИФА (иммуноферментый анализ).
Этот метод служит не для обнаружения самого вируса, а антител, которые наша иммунная система вырабатывает для борьбы с ним.
Делают его следующим образом: на очищенные части вируса (антигены), зафиксированные в специальной лунке, наносят кровь. Если в ней есть антитела, то образуются иммунные комплексы антиген/антитело, которые вступают в реакцию с красителем, приводя к изменению цвета. Это оценивается качественно (есть/нет реакции) и/или количественно при помощи дополнительной аппаратуры.
Существует несколько поколений ИФА:
- В первом поколении тестов использовался сам вирус, обработанный ультразвуком, при этом определялись антитела только ВИЧ-1. Анализ обладал невысокой чувствительностью и специфичностью.
- ИФА второго поколения научили определять антитела как к ВИЧ-1, так и к ВИЧ-2. Материалом служили синтезированные белки, аналогичные настоящим антигенам вируса. Впрочем, тесты первого и второго поколения давно не используются.
- Следом появились тесты третьего поколения, которые позволяют диагностировать длительно текущую (хроническую) ВИЧ-инфекцию с чувствительностью и специфичностью около 100 %. Однако при острой ВИЧ-инфекции (когда антител мало или совсем нет) их точность считается недостаточной.
Современный ИФА позволяет обнаружить антитела, появляющиеся в крови с 30-го (цифры согласно клиническим рекомендациям Минздрава) дня инфицирования (по данным Центра контроля и профилактики заболеваний в США CDC — c 23 по 90 день).
За счет своей простоты и дешевизны этот метод используется чаще всего, в том числе на его основе работают экспресс-тесты.
Если такой тест оказался положительным, результат перепроверяется на тест-системе другого производителя, и в случае положительного результата применяется иммуноблот (смотри ниже).
Самое последнее поколение ИФА — четвертое. И оно уже позволяет проводить комбинированный анализ, одновременно проверяя: есть ли в крови белковые «обломки» ВИЧ (антигены), а также антитела.
Примечательно, что антиген р24 появляется в крови уже через 15 дней (по данным CDC — с 18 по 45 день) после инфицирования ВИЧ, поэтому такой вид анализа позволяет диагностировать ВИЧ-инфекцию раньше.
Так, эксперты из CDC считают комбинированные тесты наиболее предпочтительными для массового клинического использования. А российский Минздрав рекомендует его применять в качестве скринингового в большинстве лабораторий страны. Однако после получения положительного результата его также нужно перепроверять иммуноблоттингом.
Существуют два вида вируса ВИЧ — 1 и 2. В мире наиболее распространен ВИЧ-1. Разновидности вируса различаются по генетическому материалу, по-разному взаимодействуют с иммунитетом и отвечают на лечение.
Как следует из названия, они позволяют наверняка убедиться в наличии или отсутствии вируса иммунодефицита у человека. Их минус в сложности и дороговизне.
Иммуноблоттинг помогает проверить результаты скрининговых анализов и уточнить, каким видом вируса инфицирован человек: ВИЧ-1, ВИЧ-2 или обоими. Этот метод обладает высокой точностью, чувствительностью, но дорог и сложен в исполнении. Он является комбинацией ИФА и электрофореза, что позволяет определить антитела к специфическим антигенам ВИЧ-1 (gp160, gp120, gp41). Белки под действием электрического поля располагаются в виде полосок на нитроцеллюлозной мембране.
При положительной реакции антиген/антитело на полосках становится видно потемнение.
ПЦР (полимеразная цепная реакция). Тест способен находить генетический материал ВИЧ (ДНК/РНК), то есть проверяет, есть ли непосредственно вирус в крови. Нуклеиновые кислоты могут обнаруживаться уже на 7-й день после инфицирования (по данным CDC — c 10 по 33 день).
При этом методе в пробирке с помощью различных ферментов многократно дублируется участок ДНК или РНК вируса до таких объемов, что его можно увидеть глазом в виде полосок. Кроме того, ПЦР бывает качественным и количественным. В последнем случае можно отслеживать вирусную нагрузку (концентрацию вируса в крови и других биологических жидкостях) у людей с ВИЧ, оценивая эффект терапии.
А я могу сдать сразу иммуноблот или ПЦР, чтобы узнать свой ВИЧ-статус?
Иммуноблот используют специальные лаборатории центров по борьбе со СПИДом. Пробы крови направляются туда для перепроверки уже положительных первичных скрининговых анализов. Сразу сдать его не получится, даже в платных клиниках.
ПЦР, наоборот, можно сдать в любой момент, но только обратившись в коммерческую лабораторию. В СПИД-центрах его делают также для перепроверки ранее положительного теста. Да, ПЦР позволяет максимально быстро (в течение 7—10 дней после инфицирования) обнаружить ВИЧ, но и у него есть недостатки:
- высокая стоимость;
- может обнаружить только ВИЧ-1;
- в редких случаях выявление низких уровней РНК ВИЧ (например, Как тогда правильно проверяться на ВИЧ?
Согласно рекомендациям Минздрава, первоначальным анализом должен быть скрининговый тест ИФА. Если результат оказывается положительным, то в лаборатории, используя тот же образец крови, делают еще один анализ. Если и он «с плюсом», то тогда уже проводят иммуноблот.
Нужно ли повторно тестироваться, если результат анализа отрицательный?
Универсальной рекомендации, увы, нет. Повторные тесты нужны чтобы застраховаться от попадания в период окна, когда в крови еще нет антител и антигенов ВИЧ, а вирус уже проник в организм.
То же самое и с частотой тестирования — она зависит от разных факторов: количества рисков, приема доконтактной (PrEP) и постконтактной (PEP) профилактики, нахождения в группах риска (инъекционные наркопотребители, секс-работники, мужчины, практикующие секс с мужчинами). Однако эксперты рекомендуют проверяться каждые 6—12 месяцев.
Что может влиять на результат теста на ВИЧ?
Анализ на ВИЧ может дать неправильные результаты в следующих случаях:
- при наличии системных аутоиммунных заболеваний (коллагенозов, васкулитов) и злокачественных опухолей;
- при тестировании в период серологического окна — когда в крови еще не появились антитела к ВИЧ;
- из-за ошибки при проведении теста в лаборатории;
- после вакцинации от гриппа.
У детей, рожденных от ВИЧ-положительных матерей, до восемнадцатимесячного возраста в крови могут сохраняться материнские антитела, что может приводить к ложноположительным результатам.
Кроме того, прием PrEP и PEP могут влиять на точность анализов, так как антиретровирусные препараты уменьшают количество вируса в крови и антител к нему.
В случае с PEP после окончания курса рекомендуется посоветоваться с врачом и подобрать оптимальные сроки проведения анализов. Первый тест обычно проводят через 4—6 недель после контакта с ВИЧ, затем через 3 месяца, при необходимости — через 6 месяцев.
Считается, что крайне важно сдать анализ на ВИЧ перед началом приема PrEP и затем проверяться каждые 3 месяца, уже находясь на PrEP.
На результаты теста не влияют прием пищи и алкоголя или курение. Специальной подготовки перед сдачей анализов на ВИЧ не требуется.
Они позволяют провериться на ВИЧ, не посещая лабораторию или поликлинику. По сути, это тесты ИФА третьего поколения, которые определяют антитела к ВИЧ-1 и ВИЧ-2 в слюне, моче или крови.
Их рекомендуют делать через три месяца после возможного риска инфицирования (чтобы избежать попадания в «окно»). Но считаются достоверными они с 30-го дня предполагаемого заражения (период появления антител).
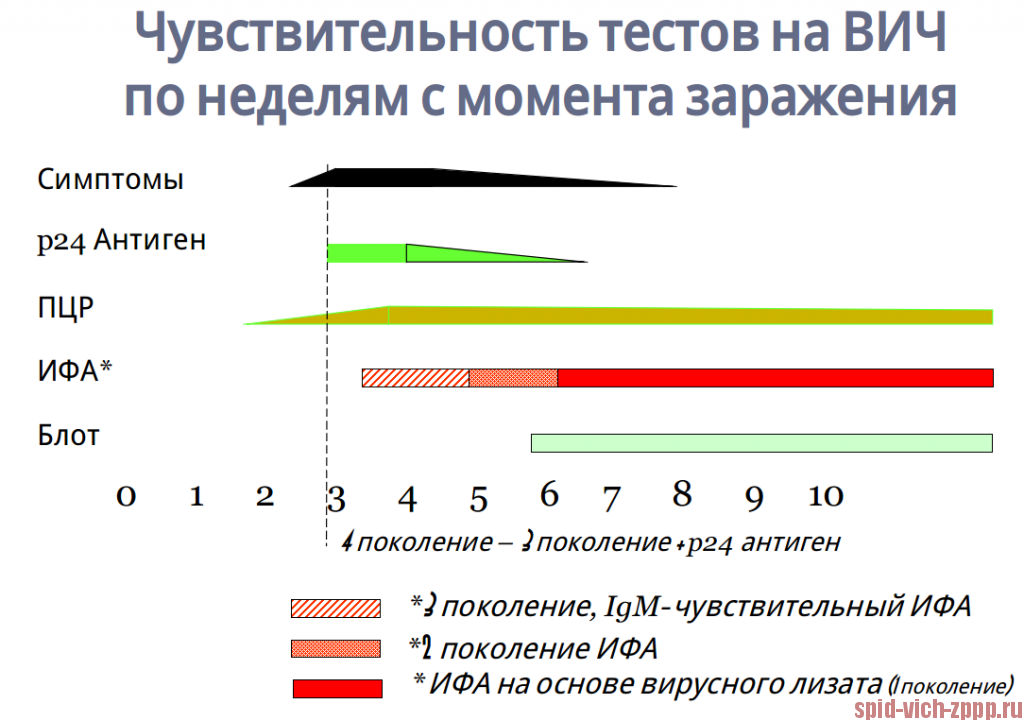
На рисунке показано, как быстро в крови появляются сам вирус (его генетический материал РНК) антитела и антигены, а также какие системы тестирования можно применить.
Точность большинства экспресс-тестов при хронической (длительно текущей) ВИЧ-инфекции достаточно высока (> 99 % чувствительности и специфичности), но все равно чуть ниже лабораторных анализов.
Сегодня среди них наиболее популярны тесты слюны (или околодесневой жидкости) и крови. Их можно либо купить самому, либо получить бесплатно в ВИЧ-сервисных организациях.
Если вы сделали экспресс-тест и он оказался положительным, необходимо его перепроверить более точным методом.
Где я могу сделать тест на ВИЧ анонимно и бесплатно?
Можно пойти в местный СПИД-центр, кабинеты анонимного консультирования или в некоммерческие организации (например, фонд «СПИД.ЦЕНТР»). Анализ на ВИЧ бесплатный и анонимный, прикрепление к поликлинике и регистрация не требуются. После сдачи теста выдается идентификационный номер, по которому можно будет узнать результат.
источник
Ты часто задаёшь себе вопрос: «Мог ли я заразиться ВИЧ?» Это вопрос крутится у тебя в мозгах, отравляет твою жизнь, не даёт покоя. Обычно это усиливается после незащищенного соития, потому что средство защиты могло соскользнуть, разорваться или потому что у тебя был другой риск, такой как травма от укола иглой, контакт с чужой кровью.
Что делать? — Идти и сдавать кровь на ВИЧ!
Тест на ВИЧ может прояснить ситуацию. И если заражение всё таки произошло, то знание об этом приносит огромные преимущества с точки зрения здоровья (психологически это конечно тяжело, но чем раньше узнаешь об этом, тем лучше).
Своевременная терапия от ВИЧ может защитить иммунную систему от вируса. Если инфекция обнаружена поздно, то часто вирус уже успел нанести серьезный вред организму. А этого можно было бы избежать с помощью своевременного обследования и терапии. Тест на ВИЧ также может проводиться анонимно.
Самый точный тест для определения ВИЧ является ИФА 4-го поколения. Тест дает надежный результат уже через 6 недель после последней рискованной ситуации, для 100% уверенности необходимо повторить анализ через 3 месяца после последнего контакта.
Также существуют другие тесты, которые не рекомендуются для скрининга, но могут применятся при определённых ситуациях: домашние тесты (экспресс-тесты), ПЦР.
Экспресс-тесты часто называют домашними тестами или «point-of-care», т.е. их можно использовать в любом месте, «не отходя от кассы». Потому что вместо отправки образца крови в лабораторию можно провести тестирование прямо на месте без специального лабораторного оборудования и сразу отнести результаты врачу для консультирования.
Для большинства экспресс-анализов в местах оказания медицинской помощи требуется крошечный образец крови (из пальца). Другие тесты требуют жидкости ротовой полости (впитывающая прокладка протирается вокруг наружных десен, прилегающих к зубам). Их называют «быстрыми» тестами, потому что результат обычно дается в течение нескольких минут.
Большинство быстрых тестов определяют антитела к ВИЧ. Они не являются частью самого ВИЧ, но вырабатываются организмом человека в ответ на ВИЧ-инфекцию. Через несколько недель после заражения ВИЧ иммунная система распознает некоторые компоненты вируса и начинает вырабатывать антитела к ВИЧ, чтобы повредить, нейтрализовать или убить его (этот период известен как «сероконверсия»). Эти антитела сохраняются на всю жизнь.
Напротив, рекомендуемые лабораторные тесты (ИФА 4-го поколения) также обнаруживают антиген p24, белок, содержащийся в вирусном ядре ВИЧ, который может быть обнаружен раньше, чем антитела. Большинство быстрых тестов, за исключением Alere HIV Combo и Alere Determine HIV-1/2, не могут обнаружить антиген p24.
Одним из отличительных антигенов ВИЧ является вирусный белок, называемый р24, структурный белок, который составляет большую часть вирусного ядра ВИЧ, или «капсид». Высокие уровни p24 присутствуют в сыворотке крови вновь инфицированных людей в течение короткого периода между заражением и сероконверсией, что делает анализ антигена p24 полезным для диагностики первичной ВИЧ-инфекции.
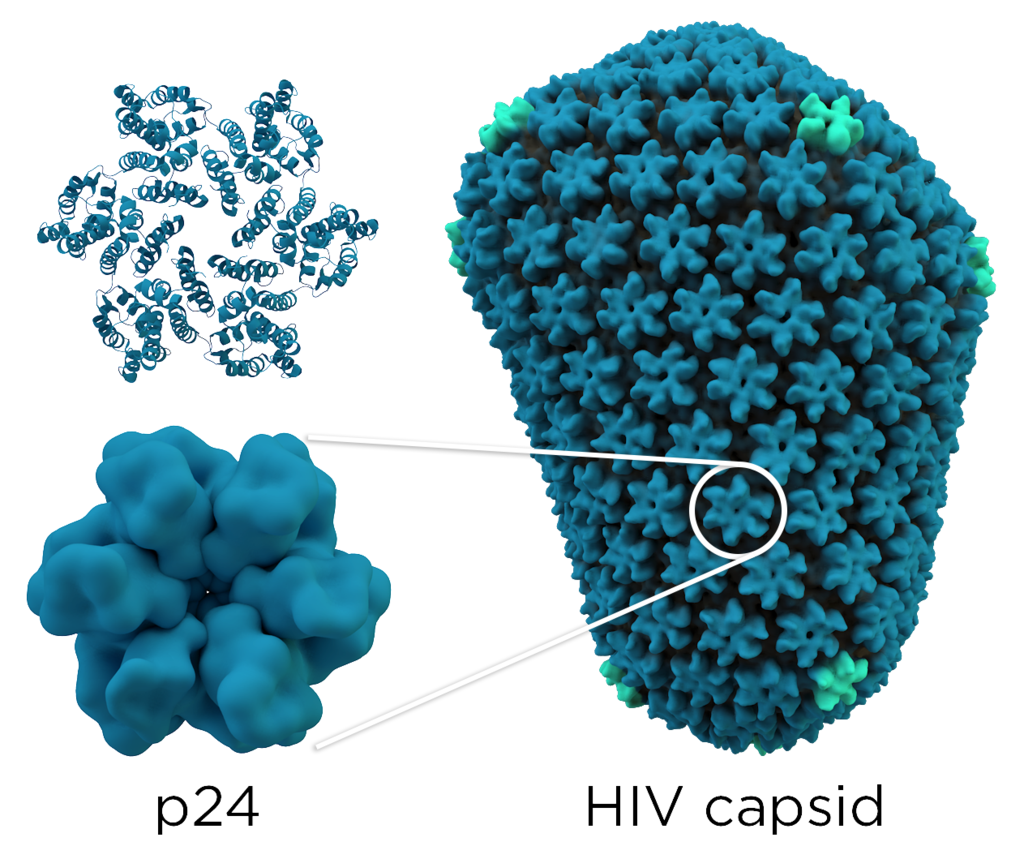
Антитела к р24 продуцируются во время сероконверсии, что делает антиген р24 необнаружимым после сероконверсии в большинстве случаев. Поэтому анализы антигена p24 не являются надежными для диагностики ВИЧ-инфекции в её поздних стадиях.
Тем не менее, ВИЧ-инфекция может быть надежно диагностирована раньше с помощью комбинированных тестов на Антитела/Антигены, а не с помощью тестов, которые определяют только антител. Тесты на Антитела/Антигены четвертого поколения в настоящее время являются стандартным скрининговым анализом в РФ.
Сейчас существуют следующие экспресс-тесты:
- Alere Determine HIV-1/2 Ag/Ab Combo Test (цельная кровь, сыворотка, плазма)
- Clearview HIV 1/2 Ag/Ab Stat-Pak (цельная кровь, сыворотка, плазма)
- Clearview Complete HIV 1/2 (цельная кровь, сыворотка, плазма)
- HomeAccess HIV-1 Test System (капли крови на пластинке, которая отправляется по почте в лабораторию)
- OraQuick In-Home HIV Test (слюна, результат через 20 минут)
Точность испытаний экспресс-тестов не всегда равна точности обычных лабораторных тестов (ИФА), особенно в отношении недавней инфекции. На это есть две основные причины:
- Что ищет тест? В то время как один тест ищет антитела и антиген, другие тесты ищут только антитела. Более того, некоторые могут обнаруживать только антитела к иммуноглобулину G (IgG), но не антитела к иммуноглобулину M (IgM), которые появляются раньше.
- Анализ (образец биоматериала: крови, слюны) взят. Экспресс-тесты проводятся на цельной крови, взятой из пальца. Она имеет более низкую концентрацию антител и р24, чем плазма. Образцы жидкости ротовой полости имеют концентрацию антител, которая еще ниже. (Плазма — это бесцветная жидкая часть крови, отделенная от цельной крови с помощью лабораторного оборудования. Кровь из уколов пальцами получают, покалывая палец ланцетом, тогда как жидкость из полости рта получают, протирая десны.)
В результате период «окна» быстрых тестов, таких как Alere HIV Combo и INSTI HIV-1/HIV-2, может быть на одну-две недели больше, чем для лабораторных тестов ИФА 4-го поколения. Другие быстрые тесты, основанные на более старых технологиях, могут иметь более длительные периоды окна, чем вышеуказанные.
Экспресс-тесты могут выполняться персоналом с низкой лабораторной квалификацией и небольшим опытом. Тем не менее, чтение результатов теста зависит от субъективной интерпретации, и когда результат является пограничным, более квалифицированные и опытные сотрудники
При использовании в популяции с низкой распространенностью ВИЧ, ложноположительные результаты могут создавать очень большие проблемы. Тесты всегда дают небольшое количество ложноположительных результатов, но в условиях, когда очень мало ВИЧ-инфицированных, большинство очевидных положительных результатов на самом деле будут неверными.
Однако по мере увеличения доли людей, проходящих тестирование на ВИЧ, число истинных положительных результатов начинает превосходить число ложных положительных результатов. Это означает, что более целесообразно использовать тесты по месту оказания помощи в группах с высокой распространенностью, например, среди геев и бисексуальных мужчин, чем в общей популяции.
Все тесты на ВИЧ должны иметь реактивные результаты (предварительный положительный результат), подтвержденные дальнейшими тестами. Большинство поставщиков говорят людям, которые проводят тестирование, что отрицательный результат является окончательным, но что реактивный результат просто указывает на необходимость дальнейшего лабораторного тестирования.
В условиях низкой распространенности ВИЧ персонал может не «набить глаз» на достаточном количестве истинно положительных образцов для правильной интерпретации результата в сложных случаях.
Хорошей практикой является повторное чтение результатов анализов вторым сотрудником в сроки, указанные на упаковке. Организации, использующие экспресс-тесты должны поддерживать прочные связи с клинико-диагностическими лабораториеями, которые обеспечат клиническое руководство и проверку качества.
Во многих странах был произведен широкий спектр тестов для оказания медицинской помощи, но лишь немногие из них прошли строгие независимые оценки. Исследования по тестам на ВИЧ публикуются в медицинских журналах лишь изредка. Неофициально, лабораторные специалисты могут знать, какие тесты работают лучше всего.
Важно убедиться, что любой используемый тест имеет маркировку CE. Это должно означать, что тест соответствует европейскому законодательству по охране труда и технике безопасности, хотя это не обязательно означает, что результаты теста оценивались независимо.
Существуют различия в точности разных тестов, причем некоторые старые тесты имеют неоптимальную чувствительность и специфичность. Однако оценки Всемирной организации здравоохранения нескольких экспресс-диагностических тестов, которые либо имеют маркировку СЕ, либо одобрены Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA), показывают, что большинство из них являются чрезвычайно точными. Ключевыми показателями точности являются чувствительность (процент правильно положительных результатов, когда ВИЧ действительно присутствует) и специфичность (процент правильных отрицательных результатов, когда ВИЧ отсутствует).
Следует отметить, что в приведенных ниже данных Всемирной организации здравоохранения тесты проводились с образцами плазмы или сыворотки. Однако тесты менее чувствительны при тестировании цельной крови, взятой из укола пальцем. Кроме того, кровь была взята у людей, которые имели хроническую (не недавнюю) ВИЧ-инфекцию, но тесты менее точны в случаях недавней (острой) инфекции.
OraQuick HIV-1/2 Rapid HIV-1/2 (OraSure), определяет IgG, чувствительность 98.1%, специфичность 100%;
HIV 1/2 STAT-PAK (Chembio), IgG, 99.5%, 100%;
Alere Determine HIV-1/2 (Alere), IgG + IgM, 100%, 98.9%;
Uni-Gold HIV (Trinity), IgG + IgM, 99.8%, 99.9%;
INSTI HIV-1/HIV-2 Antibody Test (bioLytical), IgG + IgM, 100%, 99.7%;
SD BIOLINE HIV-1/2 3.0 (Standard Diagnostics), IgG + IgM, 99.8%, 99.8%;
DPP® HIV 1/2 Assay (Chembio), IgG, 99.8%, 99.8%;
VIKIA HIV 1/2 (bioMérieux), IgG, 99.4%, 99.9%;
Reveal Rapid HIV Antibody Test (MedMira), IgG, 99.8%, 99.9%.
Принимая во внимание, что приведенные выше данные относятся к образцам крови, OraQuick Advance Rapid HIV-1/2 является широко используемым тестом, который также может тестировать образцы пероральной (ротовой полости) жидкости. Несмотря на то, что это неинвазивное и очень удобное для человека тестирование, эффективность при тестировании образцов пероральной жидкости несколько ниже, чем при тестировании образцов крови. Основная причина — в ротовой жидкости меньше антител к ВИЧ, чем в цельной крови, особенно после недавнего инфицирования. В 7 исследованиях, в которых проводилось прямое сравнение эффективности теста, общая чувствительность теста с пероральной жидкостью составила 98,03%, а с цельной кровью 99,68%.
Существует один быстрый тест для экспресс-тестировангия, который определяет и антитела к ВИЧ и антиген p24, аналогично обычным лабораторным тестам на Антитела/Антиген. Alere Determine HIV-1/2 Ag/Ab Combo был впервые представлен в 2009 году, а обновленная версия под названием Alere HIV Combo была запущена в Европе в 2015 году (более старая версия все еще продается в Соединенных Штатах и в некоторых частях мира).
Преследовалась цель создать быстрый тест «4-го поколения», который будет обнаруживать антиген p24 для сокращения периода «окна» подобно обычным лабораторным тестам. Тем не менее, некоторые исследования показали, что, хотя более старая версия этого теста показала хорошие результаты в отношении установленной ВИЧ-инфекции, его способность выявлять недавнюю ВИЧ-инфекцию не соответствовала Ат/Аг лабораторным тестам. Тест был довольно нечувствителен к антигену р24, что делает его лишь незначительно лучше для обнаружения острой (недавней) инфекции, чем тесты, которые определяет только антитела.
Небольшое количество исследований относительно эффективности новой версии теста свидетельствуют, что он лучше работает при острой инфекции, хотя это все еще не дотягивает до эффективности лабораторных тестов антител/антигенов. Чувствительность Alere HIV Combo при острой (свежей) инфекции, по разным оценкам, составляет 28% (в трех африканских странах), 54% (Франция), 65% (Нидерланды) и 88% (Великобритания).
При мета-анализе результатов 18 отдельных исследований, в которых различные экспресс-тесты (включая Determine, OraQuick, UniGold и INSTI) сравнивался с более чувствительным лабораторным тестом. По сравнению с лабораторными тестами 4-го поколения оценочная чувствительность экспресс-тестов составила 94,5% (95% доверительный интервал 87,4-97,7), а специфичность составила 99,6% (99,4-99,7). По сравнению с тестами РНК (вирусная нагрузка) оценочная чувствительность составила 93,7% (95% доверительный интервал 88,7-96,5) и специфичность 98,1% (95% ДИ: 97,9-98,2).
Чувствительность была выше в девяти исследованиях, проведенных в африканских странах, чем в девяти исследованиях, проведенных в Соединенных Штатах и других экономически развитых странах. Вероятно, это зависит от разные группы населения в которых проводился скрининг. В то время как 4,7% из тех, кто дал положительный результат в африканских исследованиях, имели острую (недавнюю) ВИЧ-инфекцию, эта цифра выросла до 13,6% в странах с высоким уровнем дохода.
«Все тесты на ВИЧ должны иметь реактивные результаты (предварительный положительный результат), подтвержденные дальнейшими тестами».
Исследование, проведенное в пяти африканских странах, показало, что результаты испытаний в местах оказания медицинской помощи были неоптимальными. Образцы из некоторых стран с большей вероятностью имели ложноположительные результаты, чем другие, что говорит о том, что тесты должны проходить локальную валидацию, и что некоторые тесты могут быть более точными в отношении некоторых подтипов ВИЧ, чем другие.
Исследователи обнаружили большое количество ложноположительных результатов, тогда как ложноотрицательные результаты были относительно редки. Специфичность теста First Response HIV Card Test 1–2.0, INSTI HIV-1/HIV-2 Antibody Test, Determine HIV-1/2 и Genie Fast HIV 1/2 составляла от 90 до 95%. Полученные данные подтверждают, что диагноз ВИЧ не должен основываться на результатах одного экспресс-теста на ВИЧ. Комбинация тестов на ВИЧ, а точнее алгоритм (последовательность) двух или трех разных тестов, необходима для постановки диагноза ВИЧ. Эти рекомендации прописаны в руководстве по тестированию.
Все тесты на ВИЧ должны иметь реактивные (предварительно положительные) результаты, подтвержденные арбитражными тестами. Особая проблема, с которой сталкиваются работники здравоохранения при проведении быстрых тестов, заключается в том, как сообщить результат теста реагирующему человеку (который может присутствовать при чтении результата) и объяснить, что необходимы дополнительные тесты. Эти проблемы реже встречаются при лабораторных исследованиях — т.к. берётся достаточно большое количество образца крови, чтобы можно было несколько раз перепроверить его и устранить неопределенности в диагнозе.
Период окна — время после заражения и до сероконверсии, в течение которого маркеры инфекции (антиген p24 и антитела) все еще отсутствуют или слишком малы, чтобы их можно было обнаружить. Тесты не могут надежно обнаружить ВИЧ-инфекцию до тех пор, пока не окончится период окна. Все тесты имеют период окна, который варьируется от теста к тесту.
Делани и коллеги оценили периоды времени для нескольких быстрых тестов в исследовании 2017 года. Однако все эти оценки были основаны на тестировании плазмы крови. На практике тесты обычно проводятся на крови полученной путем укола пальца скарификатором, и период окна, вероятно, будет на несколько дней больше.
Тест 4-го поколения Determine HIV-1/2 Ag/Ab Combo имеет средний период окна — 19 дней (межквартильный интервал от 15 до 25 дней). Это указывает на то, что половина всех заражённых будет обнаружена через 15-25 дней после заражения. Девяносто девять процентов ВИЧ-инфицированных будут выявлены в первые 43 дня после заражения.
Межквартильный размах — это разница между 1-м и 3-м квартилями, т.е. между 25-м и 75-м процентилями. В него входят центральные 50% наблюдений в упорядоченном наборе, где 25% наблюдений находятся ниже центральной точки и 25% — выше.
Тест 3-го поколения INSTI HIV-1/HIV-2 имеет средний период окна — 26 дней (межквартильный интервал от 22 до 31 дня). Это указывает на то, что половина всех заражённых будет обнаружена между 22 и 31 днем после заражения. Девяносто девять процентов ВИЧ-инфицированных будут обнаружены в течение 50 дней после заражения.
Было проверено несколько тестов второго поколения, таких как OraQuick Advance Rapid HIV 1/2, Clearview HIV 1/2 STAT-PACK и SURE CHECK HIV 1/2. Средний период окна составил 31 день (межквартильный интервал от 26 до 37 дней). Это указывает на то, что половина всех инфицированных будет обнаружена между 26 и 37 днями после заражения. 99% ВИЧ-инфицированных будут обнаружены в течение 57 дней после заражения. Когда OraQuick Advance Rapid HIV 1/2 используется с образцами ротовой жидкости, периоды окна, вероятно, будут длиннее, чем этот.
Если вы тестируете с помощью быстрого теста в медицинском учреждении, и вы обеспокоены тем, что могли заразиться ВИЧ в течение периода окна экспресс-теста, то вы можете также пройти лабораторный тест 4-го поколения. Для этого требуется образец крови, взятый через иглу из вены на руке, который проверяется в лаборатории с использованием более чувствительного теста. Результаты должны быть доступны через несколько дней.
При некоторых ситуациях экспресс-тесты могут быть малоэффективны. Результаты могут быть неточными:
- В случае свежей ВИЧ-инфекции во время периода окна.
- У людей с диагнозом ВИЧ, которые проходят лечение от ВИЧ-инфекции. Эти тесты не являются надежным способом подтвердить, что у вас все еще есть ВИЧ-инфекция.
- У людей, которые принимают предконтактную профилактику (PrEP) или послеконтактную профилактику (PEP). Если всё же заражение ВИЧ произошло, то у может быть задержка ответа на антитела, продлевающая период окна.
Быстрые тесты на ВИЧ для домашнего использования часто предлагаются через Интернет. Они обычно отправляются из-за границы, потому что в России их не так просто купить в аптеке.
Но домашние тесты не рекомендуются к использованию. Даже небольшие ошибки при использовании теста могут привести к ложноположительным или ложноотрицательным результатам теста. А также в обычном тесте на ВИЧ положительный результат подтверждается вторым тестом до уведомления пострадавшего.
С другой стороны, с помощью быстрых тестов Вы напрямую сталкиваетесь с потенциально ложным результатом при отсутствии консультации со стороны врача. Остаетесь один на один с результатом. Это может быть очень опасно.
Иная ситуация, когда экспресс-тесты используются при анти-СПИД акциях. Там тест проводится экспертами и предлагается консультирование. Если результат теста положительный, для подтверждения крови берется кровь. Результат этого теста можно получить через несколько дней.
Существует три возможных результата теста:
1) Отрицательный (также может быть описан как «нереактивный»). Тест не обнаружил никаких признаков ВИЧ-инфекции. Вероятно, у Вас нет ВИЧ (если вы не проходите тестирование в одной из ситуаций, описанных в разделе выше «В каких ситуаций быстрые тесты могут быть неточными»).
2) Реактивный (часто неправильно описывается производителем как «положительный»). Тестовый тест отреагировал на вещество в Вашей крови. Это не обязательно означает, что Вы инфицированы ВИЧ. Это означает, что Вам нужно пройти больше тестов, чтобы подтвердить результат. Эти дополнительные тесты лучше всего проводить в медицинском учреждении, где есть доступ к самым точным технологиям тестирования на ВИЧ.
3) «Неопределенный», «сомнительный» или «недействительный». Результат теста неясен. Должен быть сделан еще один тест.
Это означает, что тест не обнаружил никаких признаков ВИЧ-инфекции.
Вы можете быть уверены, что у Вас нет ВИЧ, и что Вы ВИЧ-отрицательны, если только Вы не подвергались воздействию ВИЧ совсем недавно, во время периода диагностического окна. Диагностические тесты на ВИЧ могут пропустить заражение, которое произошло за месяц до тестирования.
Его ещё неправильно называют «положительный», но это может быть и ложноположительным результатом. Результат показывает, что тест отреагировал на что-то в вашей крови, и это следует исследовать дальше.
Это не обязательно означает, что Вы ВИЧ-инфицированы. Поскольку могут быть ложные срабатывания, врачи никогда не используют только результат одного теста для постановки диагноза ВИЧ. Если результат является реактивным, результат является только предварительным и должен быть подтвержден серией подтверждающих тестов.
Эти последующие тесты лучше всего проводить у медицинского работника, который имеет доступ к самым точным технологиям тестирования на ВИЧ.
Если Вы прошли тестирование на ВИЧ-инфекцию, Вам могут сказать, что результат «неопределенный», «сомнительный» или «недействительный». Это означает, что результат теста неясен. Нужно сделать ещё один тест.
Неопределенный результат означает, что тест-система показывает слабую положительную реакцию, возможно, из-за неизвестной перекрестной реакции антител, из-за перекрестного загрязнения образцом другого человека или из-за другой технической ошибки. Неопределенные результаты могут также наблюдаться у людей после свежего заражения ВИЧ, поскольку их иммунный ответ все еще развивается.
Если неопределенный результат не воспроизводится в других тестах, это почти наверняка просто ложная положительная реакция. Однако, если более чем один тип теста дает неопределенный результат, необходимо провести повторное тестирование с несколькими типами теста.
Если результаты по-прежнему трудно интерпретировать, новый анализ следует взять примерно через две недели. Если причиной неопределенных результатов была недавняя инфекция, то тесты по прошествии времени должны дать более точный результат.
ПЦР-тест обнаруживает сам вирус, а не наличие антител, как ИФА тест. В большинстве случаев можно обнаружить ВИЧ уже через 15 дней после заражения. Этот тест используется, если есть подозрение на острую ВИЧ-инфекцию. Та же процедура применяется и в терапии ВИЧ для определения вирусной нагрузки.
ПЦР-тесты не подходят в качестве более быстрой альтернативы обычным тестам на антитела к ВИЧ. Этот тест, в частности, до 15 дней от контакта не может надежно исключить, что ВИЧ присутствует в организме, поскольку вирусная пролиферация (умножение) в организме варьируется от человека к человеку.
Кроме того, ПЦР-тест может выявлять штамм вируса ВИЧ-1, например, а не штамм вируса ВИЧ-2. Чтобы быть в безопасности, необходимо провести тест на антитела к ВИЧ через три месяца. ПЦР-тест стоит примерно от 1000 до 3000 руб. Пациент сам оплачивает анализ, если только он не проводится как часть лечения ВИЧ-инфекции или если имеется подозрение на острую ВИЧ-инфекцию.

Как часто Вам необходимо проходить тестирование на ВИЧ, лучше обсудить на консультации у врача. Вот несколько примеров рекомендаций по тестированию:
- Вы должны пройти тестирование, если у Вас была ситуация при которой был риск заражения ВИЧ или у Вас есть симптомы, которые могут указывать на наличие ВИЧ-инфекции.
- Также рекомендуется проходить тестирование мужчинам, имеющих половые контакты с мужчинами, по крайней мере, один раз в год на ВИЧ (и другие венерические заболевания).
- Беременным женщинам обязательно должен быть предложен тест на ВИЧ. Если обнаружена инфекция, можно избежать передачу ВИЧ ребенку.
- Тем, кто употребляет наркотики внутривенно, следует уточнить, как часто необходимо сдавать анализы на ВИЧ и гепатит С у своего врача-нарколога.
Любой, кто хочет пройти курс доконтактной профилактики ВИЧ, должен пройти тестирование на ВИЧ перед началом терапии, через 4 недели после начала и затем каждые 3 месяца.
Если у Вас нет ВИЧ, то Вы можете защитить себя от ВИЧ с помощью барьерной защиты.
Сегодня, помимо средств барьерной защиты, существуют также возможности защитить себя от ВИЧ с помощью доконтактной профилактической терапии (ДКП). Для людей, которые часто сталкиваются с риском заражения ВИЧ, ДКП может быть хорошим вариантом защиты.

Если Вы инфицированы ВИЧ, то Вам следует начать принимать лекарства от ВИЧ в ближайшее время согласно предписанию врача. Тогда у Вас есть хорошие шансы на нормальную продолжительность жизни с хорошим качеством жизни.
Кроме того, при эффективной терапии, когда достигается неопределяемая вирусная нагрузка заражение невозможно даже во время соития без барьерной защиты. Терапия от ВИЧ также предотвращает передачу ВИЧ от матери к ребенку.
Есть несколько мест, где можно провериться на ВИЧ:
- В СПИД-центре,
- в медицинском центре,
- в поликлинике.
Если Вы знаете о своей ВИЧ-инфекции, то Вы можете многое сделать для защиты своего здоровья. Предупреждён — вооружён! Своевременное начало лечения ВИЧ может предотвратить переход ВИЧ-инфекции в стадию СПИДа. С другой стороны, слишком позднее начало терапии может стоить Вам нескольких лет Вашей жизни.
Есть веские причины для прохождения теста на ВИЧ. С одной стороны, это даст ясность ситуации. Если ВИЧ-инфекции нет, тогда больше не о чем беспокоиться. Если результаты теста окажутся положительными, инфекцию можно наблюдать, пока не наступит подходящее время для начала лечения ВИЧ.
Лечение ВИЧ значительно уменьшает количество вирусов в организме, тем самым защищая иммунную систему от ВИЧ. Это создает лучшие условия, которые позволяют жить с ВИЧ в течение длительного времени, без перехода ВИЧ-инфекции в СПИД. Кроме того, это снижает вероятность передачи ВИЧ Вашему партнеру.
К сожалению, многие люди все еще узнают о своей ВИЧ-инфекции слишком поздно, а некоторые только тогда, когда их доставляют в больницу с опасными для жизни заболеваниями. Этого можно избежать с помощью раннего теста на ВИЧ!
Даже если ВИЧ-инфекция потенциально существует достаточно давно, ее все же стоит проверить. Терапия ВИЧ часто может стабилизировать иммунную систему даже на более поздних стадиях заболевания.
Вы должны пройти тестирование, если существует реальный риск заражения. Обычно это тот случай, когда у Вас был незащищенное соитие (анальный или вагинальный половой акт без барьерной защиты) с партнером, который мог быть ВИЧ-положительным. Существует также высокий риск заражения при совместном использовании игл, шприцев.
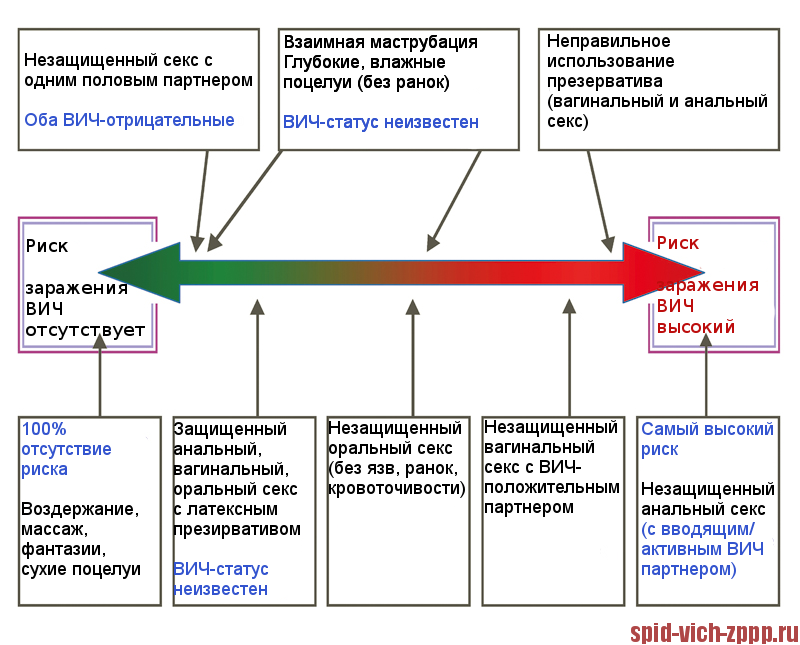
Те, кто хотел бы исключить возможную ВИЧ-инфекцию, должны пройти тестирование, по крайней мере, через шесть недель после последней ситуации риска. Только в этом случае тест на ВИЧ может надежно исключить наличие ВИЧ-инфекции.
Экспресс-тест требует больше времени: экспресс-тест выявляет не сам вирус ВИЧ в крови, а антитела, которые иммунная система вырабатывает для борьбы с вирусом. Для некоторых людей эти антитела формируются и становятся обнаруживаемыми в срок до трех месяцев.
Таким образом, «отрицательный» результат теста вскоре после риска заражения не обязательно означает, что человек не заражен ВИЧ. Это только указывает на то, что в крови до сих пор нет антител и/или антигенов.
Консультация может определить, действительно ли существует риск заражения или вы беспокоитесь излишне. Консультирование также может определить, наступило ли подходящее время для прохождения теста. Дискуссия может заполнить пробелы в ваших знаниях о рисках заражения и способах защиты.
Тест не доказывает наличие самого вируса, а скорее наличие антител. Для выработки этих антител организму требуется до шести недель. Если вы хотите быть уверены, что Вы не инфицированы, Вам следует пройти тестирование через три месяца после последней возможной рискованной ситуации. До этого тест не может с 100% уверенностью показать, что Вы не заражены.

Наиболее точным и надежным и обычно используемым диагностическим тестом на ВИЧ является лабораторный тест, который может обнаружить как антитела к ВИЧ, так и антиген p24. Их называют комбинированными или тестами 4-го поколения , потому что они обнаруживают обе субстанции. Это тесты «четвертого поколения» с более продвинутыми технологиями, чем у предыдущих поколений.
Антитела к ВИЧ вырабатываются организмом человека в ответ на внедрение ВИЧ. Через несколько недель после заражения ВИЧ, иммунная система распознает некоторые компоненты вируса и начинает генерировать антитела к ВИЧ, чтобы повредить, нейтрализовать или убить его (этот период известен как «сероконверсия»). Эти антитела сохраняются на всю жизнь.
Антиген ВИЧ, известный как p24, является структурным белком, который составляет большую часть вирусного ядра ВИЧ. Высокие уровни р24 присутствуют в крови в течение короткого периода между ВИЧ-инфекцией и сероконверсией, прежде чем исчезнуть. Поскольку антиген p24 обычно обнаруживается за несколько дней до появления антител к ВИЧ, тест, который может обнаружить p24, имеет более короткий период окна, чем тест, который обнаруживает только антитела (3-го поколения и ниже).
Комбинированные тесты четвертого поколения обычно проводятся на плазме или сыворотке (два компонента крови, отделенные от цельной крови с использованием лабораторного оборудования). Образец крови берется через иглу из вены в руке. Образцы нескольких людей анализируются одновременно, машинным способом в лаборатории.
Как и любой скрининг-тест, реактивный результат (предварительный положительный результат) должен быть подтвержден подтверждающими тестами.
Эти тесты также могут называться тестами «четвертого поколения» или ELISA (иммуноферментный анализ). Лабораторные тест-системы первого и второго поколений больше не используются. Лабораторный тест третьего поколения обнаруживает только антитела и больше не рекомендуется для использования, но всё же используется, например в Украине, Республике Беларусь.
Тесты этого типа включают в себя: Abbott Architect HIV Ag/Ab combo, ADVIA Centaur HIV Ag/Ab Combo, Genscreen ULTRA HIV Ag-Ab, VIDAS HIV panel and Vitros HIV combo. В названиях продуктов «Ag/Ab» указывает на то, что тест ищет как антиген, так и антитело.
Некоторые тесты также могут быть описаны как пятое поколение — Bio-Rad BioPlex 2200 HIV Ag/Ab и Elecsys HIV Duo. Они обнаруживают одни и те же биомаркеры, но также могут различать образцы, положительные на антиген p24 и антитела, а также на ВИЧ-1 и ВИЧ-2.
Период окна — это время сразу после заражения, в течение которого тесты не всегда могут обнаружить антитела или антиген p24 и поэтому могут давать ложноотрицательный результат. Трудно сказать точно, как долго длится период окна для каждого теста, так как существуют различия между людьми, и это трудная тема для исследования (недавно инфицированным людям нужно было бы точно знать, когда они подверглись воздействию ВИЧ, а затем многократно сдавать кровь в течение следующих дней и недель).
Тем не менее, по оценкам, средний период окна для тестов четвертого поколения составляет 18 дней, причем 50% всех заражений обнаруживается между 13 и 24 днями после заражения. Хотя иногда этот период будет немного дольше, 99% ВИЧ-инфицированных будут обнаружены в течение 44 дней после заражения.
Поэтому, например в британских руководствах говорится, что лабораторный тест на антитела/антигены обнаруживает подавляющее большинство людей, инфицированных ВИЧ через 4 недели после рискованного контакта.
Лабораторные тест-системы четвертого поколения чрезвычайно точные.
Ключевыми показателями точности являются:
- чувствительность (процент правильных положительных результатов, когда ВИЧ действительно присутствует);
- специфичность (процент правильно отрицательных результатов, когда ВИЧ отсутствует).
С точки зрения чувствительности, обзор материалов Центра по контролю и профилактике заболеваний (CDC) выявил четыре исследования двух разных анализов, с чувствительностью всегда выше 99,7% для установленной инфекции.
Оценка Агентства по охране здоровья показала, что девять из десяти тестов, которые они оценивали, имели чувствительность 100%, в то время как французская оценка показала, что десять из двенадцати тестов имели чувствительность 100%. Самая низкая чувствительность составила 99,8%.
Аналогичные результаты были найдены для специфичности. Оба теста, проверенные CDC, имели специфичность 99,5% или выше; все тесты в оценке Агентства по охране здоровья имели специфичность 99,7% или выше, и французское исследование показало, что все тесты, произведенные после 2000 года, имели специфичность 99,8% или выше.
Как и любой скрининг-тест, реактивный результат (предварительный положительный результат) должен быть подтвержден подтверждающими тестами. Лаборатория должна повторно протестировать образец с помощью другого анализа, прежде чем сообщать предварительные результаты. Затем следует взять и протестировать новый образец (повторный забор), чтобы исключить техническую ошибку (например, перепутывание образцов двух пациентов).
Результаты анализов должны быть доступны в загруженных клиниках и в неотложных случаях в течение дня или двух, но других пациентов могут попросить подождать дольше. Основная задержка в получении результатов связана с тем, что образцы анализируются партиями, и может потребоваться несколько дней для того, чтобы собрать достаточно образцов для анализа. Фактический процесс проведения теста обычно занимает несколько часов.
Британская ассоциация по ВИЧ говорит, что результаты теста обычно должны быть доступны врачу, который назначил тест в течение пяти дней, и человеку, тестирующему в течение десяти дней.
Тесты четвертого поколения чрезвычайно чувствительны и специфичны. Они более надежны в выявлении ранней инфекции, чем экспресс-тесты. Их целесообразно использовать, когда немедленное предоставление результатов не требуется, и когда люди могут вернуться за своими результатами. Поскольку тестирование осуществляется центральной лабораторией, легче внедрить программы контроля качества.
Лабораторный тест обычно занимает от трех до пяти дней. Если этот тест возвращает положительный результат, то в это же время проводится подтверждающий тест с использованием другого метода. Это гарантирует, что результат теста не является ложноположительным, как это может случиться в редких случаях. Только тогда это будет считаться положительным результатом теста.
Экспресс-тесты дают результат за 30 минут. Однако они не сокращают время ожидания до 90 дней. Одна из проблем, связанных с использованием быстрых тестов, заключается в том, что, если результат положительный, требуется еще три-пять дней, чтобы еще один тест был выполнен, чтобы подтвердить результат, прежде чем результат можно будет считать достоверным. Если бы первоначальный положительный результат был ложным, то Вы бы бесполезно переживали в течение этого времени.
Комплекты для домашнего тестирования дороги и часто ненадежны. Правильное использование их также требует высокой квалификации. Следовательно, неправильное использование приводит к большому количеству ошибок и ложных результатов. Домашние тесты также могут давать ложноположительный результат, поэтому еще раз требуется подтверждающий тест.
Результат теста показывает, были ли вы заражены ВИЧ шесть недель назад или нет. Если это так, то антитела против вируса будут произведены за это время, что может определить тест. Если эти антитела присутствуют, вы определенно инфицированы ВИЧ. Отрицательный результат, однако, не означает, что вы точно не заражены. Если в то же время был какой-либо риск заражения, тест может еще не определить инфекцию. Необходим еще один тест — через шесть недель после последнего риска.
При обычном тесте на ВИЧ кровь забирают и отправляют в лабораторию. Через несколько дней вам сообщают о результатах один на один, лично.
Тест выявляет не сам вирус ВИЧ, а антитела, которые вырабатывает собственная защитная система организма в ответ на ВИЧ-инфекцию.
Если тест обнаруживает антитела в крови, то присутствует ВИЧ-инфекция. Говоря с медицинской точки зрения, тест «положительный».
Если тест не обнаруживает каких-либо антител, то он считается «отрицательным». Либо инфекция отсутствует, либо инфекция является слишком недавней, и организм еще не может генерировать антитела.
Положительный результат теста обычно вызывает вопросы и вызывает страх у большинства людей. Разговор с опытным врачом и консультация в организации, оказывающей услуги в сфере СПИДа, могут быть очень полезными.
Kosack CS et al. Towards more accurate HIV testing in sub-Saharan Africa: a multi-site evaluation of HIV RDTs and risk factors for false positives. Journal of the International AIDS Society 20:21345, 2017.
источник
