Дисметаболические нефропатии – группа заболеваний, которые характеризуются поражением почек вследствие нарушения обмена веществ.
В зависимости от причины развития выделяют первичные и вторичные дисметаболические нефропатии.
Первичные являются наследственно обусловленными заболеваниями, характеризуются прогрессирующим течением, ранним развитием мочекаменной болезни и хронической почечной недостаточности.
Вторичные дисметаболические нефропатии могут быть связаны с повышенным поступлением определенных веществ в организм, нарушением их обмена в связи с поражением других органов и систем (например желудочно-кишечного тракта), лекарственной терапией и др.
Подавляющее большинство дисметаболических нефропатий связаны с нарушением обмена кальция (от 70 до 90%), около 85–90% из них – с избытком солей щавелевой кислоты, оксалатов (в виде оксалата кальция), остальные с избытком фосфатов (фосфаты кальция – 3–10%) или являются смешанными – оксалатно/фосфатно-уратными.
Первичные дисметаболические нефропатии встречаются редко.
Она наиболее часто встречается в детском возрасте. Ее возникновение может быть связано с нарушением как обмена кальция, так и обмена оксалатов (солей щавелевой кислоты).
Оксалаты попадают в организм с пищей или синтезируются самим организмом.
Причины образования оксалатов:
- Повышенное поступление оксалатов с пищей
- Заболевания кишечника – болезнь Крона, язвенный колит, кишечные анастомозы
- Повышенная выработка оксалатов организмом.
Это многофакторное заболевание. По данным различных авторов, доля наследственности в развитии оксалатной нефропатии составляет до 70–75%. Помимо генетических, большую роль играют внешние факторы: питание, стресс, экологическая нагрузка и др.
Первые проявления болезни могут развиться в любом возрасте, даже в период новорожденности.
Чаще всего они выявляются в 5–7 лет в виде обнаружения кристаллов оксалатов, небольшим содержанием белка, лейкоцитов и эритроцитов в общем анализе мочи. Характерно повышение удельной плотности мочи.
Общее развитие детей с оксалатной нефропатией, как правило, не страдает; но для них характерны аллергии, ожирение, вегетативно-сосудистая дистония со склонностью к понижению артериального давления (гипотонии), головными болями.
Заболевание обостряется в период полового созревания в возрасте 10–14 лет, что, по-видимому, связано с гормональной перестройкой.
Прогрессирование оксалатной нефропатии может привести к формированию мочекаменной болезни, развитию воспаления почек при наслоении бактериальной инфекции.
Фосфатная нефропатия встречается при заболеваниях, сопровождающихся нарушением фосфорного и кальциевого обмена. Основная причина фосфатурии – хроническая инфекция мочевой системы.
Часто фосфатно-кальциевая нефропатия сопровождает оксалатно-кальциевую, но при этом выражена в меньшей степени.
Нарушения обмена мочевой кислоты (уратная нефропатия)
За сутки в организме образуется 570–1000 мг мочевой кислоты, одна треть количества которой секретируется в кишечник и разрушается там бактериями.
Остальные две трети фильтруются в почках, большая часть всасывается обратно, и только 6–12% от профильтровавшегося количества выделяется с мочой.
Первичные уратные нефропатии обусловлены наследственными нарушениями обмена мочевой кислоты.
Вторичные возникают как осложнения других заболеваний (эритремии, миеломной болезни, хронической гемолитической анемии и др.), являются следствием применения некоторых препаратов (тиазидовых диуретиков, цитостатиков, салицилатов, циклоспорина А и др.) или нарушения функции канальцев почек и физико-химических свойств мочи (при воспалении почек, например).
Кристаллы уратов откладываются в ткани почек – это приводит к развитию воспаления и снижению почечных функций.
Первые признаки заболевания могут выявляться в раннем возрасте, хотя в большинстве случаев наблюдается длительное скрытое течение процесса.
А в общем анализе мочи обнаруживают ураты, небольшое количество белка и эритроцитов. При наличии большого количества уратов моча приобретает кирпичный цвет.
Цистин является продуктом обмена аминокислоты метионина.Можно выделить две основные причины повышения концентрации цистина в моче:
- избыточное накопление цистина в клетках почки
- нарушение обратного всасывания цистина в почечных канальцах.
Накопление цистина в клетках происходит в результате генетического дефекта фермента цистинредуктазы. Это нарушение обмена носит системный характер и называется цистинозом.
Внутриклеточное и внеклеточное накопление кристаллов цистина выявляется не только в канальцах и интерстиции почки, но и в печени, селезенке, лимфоузлах, костном мозге, клетках периферической крови, нервной и мышечной ткани, других органах.
Нарушение обратного всасывания цистина в канальцах почек наблюдается вследствие генетически обусловленного дефекта транспорта через клеточную стенку для аминокислот – цистина, аргинина, лизина и орнитина.
По мере прогрессирования заболевания определяются признаки мочекаменной болезни, а при присоединении инфекции – воспаление почек.
Лабораторно-инструментальная диагностика дисметаболической нефропатии основывается на
- выявлении кристаллов солей в общем анализе мочи,
- повышении концентрации тех или иных солей в биохимическом исследовании мочи,
- исследовании антикристаллообразующей способности мочи (АКОСМ),
- проведении тестов на кальцифилаксию и перекиси в моче,
- УЗИ почек.
Выявление кристаллов солей только в общих анализах мочи не является основанием для постановки диагноза дисметаболической нефропатии. Следует иметь в виду, что выделение кристаллов с мочой у детей часто бывает преходящим и оказывается не связанным с нарушением обмена веществ.
Для подтверждения диагноза дисметаболической нефропатии при выявлении кристаллов солей в общем анализе мочи проводится биохимическое исследование мочи.
Тест на кальцифилаксию позволяет выявить нарушения клеточного обмена кальция. Тест на перекиси в моче отражает активность процессов перекисного окисления клеточных мембран.
Изменения, выявляемые при УЗИ почек, как правило, мало специфичны. Возможно выявление в почке микрокамешков или включений.
Лечение любой дисметаболической нефропатии можно свести к четырем основным принципам:
- нормализация образа жизни;
- правильный питьевой режим;
- диета;
- специфические методы терапии.
Прием большого количества жидкости является универсальным способом лечения любой дисметаболической нефропатии, так как способствует уменьшению концентрации растворимых веществ в моче.
Одной из целей лечения является увеличение ночного объема мочеиспускания, что достигается приемом жидкости перед сном. Предпочтение следует отдавать простой или минеральной воде.
Диета позволяет в значительной степени снизить солевую нагрузку на почки.
Специфическая терапия должна быть направлена на предупреждение кристаллообразования, выведение солей, нормализацию обменных процессов.
- При лечении больных с оксалатной нефропатией назначается картофельно-капустная диета, при которой снижается поступление оксалатов с пищей и нагрузка на почки.
- Необходимо исключить холодец, крепкие мясные бульоны, щавель, шпинат, клюкву, свеклу, морковь, какао, шоколад.
- Рекомендуется ввести в рацион курагу, чернослив, груши.
- Из минеральных вод используются такие, как славяновская и смирновская, по 3–5 мл/кг/сут. в 3 приема курсом 1 месяц 2–3 раза в год.
Лекарственная терапия включает мембранотропные препараты и антиоксиданты. Лечение должно быть длительным.
- Пиридоксин (витамин В6) назначается в дозе 1–3 мг/кг/сут. в течение 1 месяца ежеквартально.
- Витамин В6 оказывает мембраностабилизирующее действие за счет участия в обмене жиров в качестве антиоксиданта и обмене аминокислот. Целесообразно также назначение препарата магне В6 из расчета 5–10 мг/кг/сут. курсом в течение 2 месяцев 3 раза в год.
- Мембраностабилизирующее действие оказывает витамин А, который нормализует взаимодействие белков и липидов мембраны клетки. Суточная доза витамина А 1000 МЕ на год жизни ребенка, курсом – 1 месяц ежеквартально.
- Токоферола ацетат (витамин Е) является мощным антиоксидантом, который поступает в организм извне и вырабатывается самим организмом. Необходимо помнить, что избыточное введение витамина Е с пищей может тормозить его внутреннюю продукцию по механизму отрицательной обратной связи. Витамин Е укрепляет белково-липидные связи клеточных мембран. Назначается с витамином А в дозе 1–1,5 мг/кг массы в сутки.
В качестве мембраностабилизаторов используются димефосфон и ксидифон.
Димефосфон применяется в дозе 1 мл 15% раствора на каждые 5 кг веса, 3 приема в сутки. Курс – 1 месяц, 3 раза в год.
Ксидифон предупреждает отложение нерастворимых солей кальция. Назначается в дозе 10 мг/кг/сут. 2% раствора в 3 приема. Курс – 1 месяц, 2 раза в год.
Высокую эффективность имеет цистон, особенно при кристаллурии. Цистон назначается в дозе 1–2 таблетки 2–3 раза в день курсом от 3 до 6 месяцев.
Помимо этого, назначается окись магния, особенно при повышенном содержании оксалатов, в дозе 0,15–0,2 г/сут.
- При лечении уратной нефропатии диета предусматривает исключение богатых пуриновыми основаниями продуктов (печени, почек, мясных бульонов, гороха, фасоли, орехов, какао и др.).
- Преимущество должно отдаваться продуктам молочного и растительного происхождения.
- Важным условием успешной терапии является достаточное употребление жидкости – от 1 до 2 л в сутки. Предпочтение следует отдавать слабощелочным и слабоминерализованным водам, отварам трав (хвощ полевой, укроп, лист березы, брусничный лист, клевер, спорыш и др.), отвару овса.
Для поддержания оптимальной кислотности мочи можно использовать цитратные смеси (уралит-У, блемарен, магурлит, солимок и др.).
При уратной нефропатии важно уменьшить концентрацию мочевой кислоты. Для этого используются средства, снижающие синтез мочевой кислоты – аллопуринол, никотинамид.
Применение в педиатрии аллопуринола ограничено из-за возможных осложнений со стороны кожи, печени, крови.
Под строгим контролем аллопуринол назначают в дозе 0,2–0,3 г/сут. в 2–3 приема в течение 2–3 недель, затем доза снижается. Длительность общего курса – до 6 месяцев.
Никотинамид является более слабым препаратом, чем аллопуринол, но лучше переносится; назначается в дозе 0,005–0,025 г 2–3 раза в сутки по 1–2 месяца повторными курсами.
Мочевую кислоту выводят также оротовая кислота, цистон, этамид, цистенал, фитолизин и др.
Лечение при фосфатной нефропатии должно быть направлено на подкисление мочи (минеральные воды – нарзан, арзни, дзау-суар и др.; препараты – цистенал, аскорбиновая кислота, метионин).
Назначается диета с ограничением продуктов, богатых фосфором (сыр, печень, икра, курица, бобовые, шоколад и др.).
Лечение цистиноза и цистинурии включает диету, высокожидкостный режим и медикаментозную терапию, направленную на подщелачивание мочи и повышение растворимости цистина.
Цель диетотерапии – предотвратить избыточное поступление в организм ребенка предшественника цистина – метионина и других серосодержащих кислот.
Для этого также исключают (или резко ограничивают) из рациона питания ребенка богатые метионином и серосодержащими аминокислотами продукты – творог, рыбу, яйца, мясо и др.
Поскольку метионин необходим организму ребенка для роста, длительное применение строгой диеты невозможно, поэтому через 4 недели от начала диетотерапии рацион ребенка расширяется и приближается к обычному, но характеризуется строгим исключением рыбы, творога и яиц.
Количество жидкости должно быть не менее 2 л/сут., особенно важно принимать жидкость перед сном.
Для подщелачивания мочи используется цитратная смесь, растворы гидрокарбоната натрия, блемарен, щелочные минеральные воды.
Для повышения растворимости цистина и предупреждения кристаллизации назначается пеницилламин. Он обладает некоторой токсичностью, поэтому в начале терапии назначаются невысокие дозы препарата – 10 мг/кг/сут. в 4–5 приемов, далее доза увеличивается в течение недели до 30 мг/кг/сут., а при цистинозе – до 50 мг/кг/сут.
Лечение пеницилламином должно проводиться под контролем содержания цистина в лейкоцитах и/или цианиднитропруссидного теста (проба на цистин в моче, где концентрация цистина должна составлять до 150–200 мг/л). При достижении этих показателей доза пеницилламина снижается до 10–12 мг/кг/сут.
Лечение пеницилламином проводится длительно, годами. Поскольку пеницилламин инактивирует пиридоксин, параллельно назначается витамин В6 (пиридоксин) в дозе 1–3 мг/кг/сут. в течение 2–3 месяцев с повторными курсами.
Для стабилизации мембран почечных канальцев назначаются витамин А (6600 МЕ/сут) и витамин Е (токоферол, 1 капля на 1 год жизни 5% раствора в сутки) в течение 4–5 недель с повторными курсами.
Имеются данные о положительном эффекте применения вместо пеницилламина менее токсичного его аналога – купренила в уменьшенной дозе в сочетании с ксидифоном и другими мембраностабилизаторами.
Антибактериальная терапия показана при присоединении инфекции.
При цистинозе успешно используется трансплантация почки, которая проводится до развития терминальной стадии хронической почечной недостаточности. Трансплантация почки позволяет значительно увеличить срок жизни больных – до 15–19 лет, однако отложение кристаллов цистина наблюдается и в трансплантате, что в конечном итоге приводит к поражению и пересаженной почки.
Прогноз при дисметаболической нефропатии в целом благоприятен.
В большинстве случаев при соответствующем режиме, диете и лекарственной терапии удается добиться стойкой нормализации соответствующих показателей в моче.
В отсутствие лечения или при его неэффективности наиболее естественным исходом дисметаболической нефропатии является мочекаменная болезнь и воспаление почек.
Самым частым осложнением дисметаболической нефропатии является развитие инфекции мочевой системы, в первую очередь пиелонефрита.
Важно! Все материалы носят справочный характер и ни в коей мере не являются альтернативой очной консультации специалиста.
Этот сайт использует cookie-файлы для идентификации посетителей сайта: Google analytics, Yandex metrika, Google Adsense. Если для вас это неприемлемо, пожалуйста, откройте эту страницу в анонимном режиме.
источник
Нарушение обменных процессов в организме человека может вызвать самые различные патологии внутренних органов. Например, неправильное функционирование почек, то есть дисметаболическую нефропатию. Довольно часто ее еще называют обменной. Своевременная диагностика (как по внешним признакам, так и на основе лабораторных анализов) и лечение позволяют не только нормализовать работу почек, но и избежать возможных осложнений. Специалисты, учитывая особенности болезни, назначают медикаментозное лечение и специальный рацион питания (диету).
К обменной нефропатии относят заболевания почек, обусловленные нарушением обмена веществ (метаболизма) и накоплением в организме солей (щавелевой, мочевой или фосфатной) или аминокислот. Такой недуг может быть:
- врожденным (первичным), связанным с генетическими нарушениями (передающимися по наследству) или патологическим протеканием беременности;
- приобретенным (вторичным), обусловленным увеличенным поступлением определенных веществ в организм, сопутствующими болезнями других органов (или длительным применением лекарственным препаратов для их лечения).
В зависимости от того, с проблемами выведения каких солей из организма связана дисметаболическая нефропатия, ее подразделяют на четыре основные разновидности:
- оскалатную, вызванную нарушением обмена кальция и оксалатов (солей щавелевой кислоты);
- уратную, которая возникает при откладывании в почках кристаллов мочевой кислоты;
- фосфатную, возникающую при нарушении обмена солей различных фосфатных кислот;
- цистиновую, которая вызвана кристаллами аминокислоты метионина.
Универсального медицинского препарата для лечения вышеперечисленных видов нефропатии нет, так как они связаны с нарушением обмена различных веществ.
Вторичная дисметаболическая нефропатия может быть вызвана сопутствующими заболеваниями: сахарным диабетом, пиелонефритом, хроническим панкреатитом, эритремией, дискинезией желчевыводящих путей, инфекциями мочеполовых путей, миеломой, гемолитической анемией, болезнями желудочно-кишечного тракта или центральной нервной системы.
Она также может проявиться на фоне дефицита магния или калия, переизбытка витамина D, нарушения рациона питания, ухудшения окружающей экологической обстановки, частых эмоциональных стрессов.
Отсутствие явных симптомов дисметаболической нефропатии на ранних стадиях довольно часто осложняет диагностику этого недуга. Проведение регулярного анализа мочи (особенно после перенесенного заболевания) поможет приступить к лечению этой болезни заблаговременно. Это также позволит избежать осложнений, которые зачастую вызывает нефропатия.
Внешними признаками дисметаболической нефропатии, при появлении которых следует обратиться в медицинское учреждение и пройти соответствующее обследование, являются:
- болезненные ощущения в суставах, животе или пояснице;
- обильное потоотделение;
- нарушение регулярности мочеиспускания;
- сухость кожных покровов;
- отеки конечностей;
- пониженное артериальное давление;
- ухудшение аппетита;
- частые головные боли;
- помутнение мочи и появление в ней хлопьев или взвесей;
При проявлении признаков ненормального функционирования почек следует обратиться к врачу и пройти полное диагностическое обследование. Исследование мочи в лабораторных условиях является основным методом диагностики на наличие нефропатии. Общий и биохимический анализы позволяют:
- выявить кристаллы солей в моче;
- определить их концентрацию (в растворенном виде);
- обнаружить присутствие патогенных микроорганизмов, способствующих образованию кристаллов;
- измерить плотность мочи.
С помощью проведения специального исследования АКОС (антикристаллообразующая способность) врачи определяют, насколько эффективно соли растворяются в моче и выводятся вместе с ней из организма.
Для определения размера почек, состояния их стенок, наличия патологических изменений или посторонних включений (песка и камней) применяют инструментальные методы обследования:
- УЗИ, основанное на различной способности внутренних органов (в зависимости от их плотности) отражать ультразвуковые волны;
Совокупность вышеописанных мер позволяет специалисту наиболее точно поставить диагноз (определить разновидность обменной нефропатии) и назначить наиболее эффективное лечение.
Лечение дисметаболической нефропатии (независимо от ее разновидности) включает в себя целый комплекс мероприятий:
- постановку точного диагноза на основе проведенных необходимых медицинских обследований;
- прием лекарственных препаратов, прописанных специалистом;
- специфическую терапию (лечебную физкультуру);
- диету, способствующую уменьшению солевой нагрузки;
- нормирование потребления жидкости (воды);
- изменение образа жизни.
Важно! Ни в коем случае нельзя прерывать предписанное курсовое лечение даже при нормализации анализов мочи!
Лечить дисметаболическую нефропатию медикаментозными средствами можно только под наблюдением специалиста и исключительно предписанными препаратами.
В зависимости от разновидности нефропатию лечат:
- оксалатную: «Димефосфоном», «Ксидифоном», «Уростоном», солями калия и магния, курсовыми приемами витаминов В6, А, Е;
- уратную: «Никотинамидом», «Аллопуринолом», «Цистоном», «Цистеналом», «Этамидом», «Фитолизином», «Канефроном»;
- фосфатную: «Ксидифоном», «Димефосфоном», «Алопроном», витамином D3;
- цистиновую: раствором гидрокарбоната натрия, «Купренилом», «Пеницилламином», «Блемареном», витамином А.
При лечении дисметаболической нефропатии диета имеет очень важное терапевтическое значение. С помощью нее можно в значительной степени снизить солевую нагрузку на почки. Рекомендованное меню определяет специалист в соответствии с формой нефропатии.
При оксалатной дисметаболической нефропатии следует воздержаться от употребления крепких мясных бульонов, холодца, щавеля, шпината, клюквы, свеклы, моркови, какао и шоколада. Предпочтение следует отдавать блюдам, приготовленным из капусты и картофеля, салатам с отварным мясом, кашам и супам. В качестве десерта рекомендуют ягоды, груши, персики, яблоки, абрикосы, бананы, курага и чернослив.
Для больных с уратной разновидностью нефропатии диета строится обычно на молочных и растительных продуктах. Основными блюдами являются молочные супы и каши (с добавлением сливочного масла), овощные салаты с растительным маслом. Необходимо ограничить употребление мяса (и продуктов, приготовленных на его основе), фасоли, гороха, орехов и какао. Также следует отказаться от слив, крыжовника, клюквы и кислых сортов яблок.
Диета при фосфатной нефропатии подразумевает ограничение в употреблении в пищу сыра, печени, курицы, бобов, шоколада, сладкой выпечки, икры рыб и сливочного масла. Ежедневный рацион строится на любых мясных блюдах, кашах на воде (с добавлением растительного масла). Арбузы, клюквенный морс и некрепкий чай рекомендованы в качестве завершения приема пищи.
При цистиновой нефропатии из рациона исключают яйца, сыр, творог и рыбу.
Естественно, вышеописанные рекомендации носят общий информационный характер. Конкретные продукты (а также их количество) может установить только специалист, учитывая возраст и вес пациента, а также степень выявленной обменной патологии почек.
Как ни странно, но самым эффективным и универсальным средством при лечении обменных нарушений функционирования почек является вода. Именно она способствует снижению концентрации растворенных в моче солей.
В зависимости от степени патологических изменений почек и индивидуальных физиологических характеристик пациента лечащий врач назначает как общее суточное количество необходимой жидкости, так и режим (то есть расписание) ее потребления. В любом случае рекомендованный объем воды будет значительно больше, чем для здорового человека.
Для некоторых разновидностей нефропатии врачи могут рекомендовать курсовой прием лечебных минеральных вод (например, при оксалатной – «Славяновскую» или «Смирновскую»).
К лечению дисметаболической нефропатии народными средствами необходимо относиться весьма осторожно. Общепринятое утверждение о том, что лечение различными отварами трав и растений не может принести вреда, ошибочно. Тот факт, что многие составляющие народных рецептов, на первый взгляд, не принесут вреда здоровому человеку, еще не говорит о том, что они полезны больному. В любом случае, прежде чем приступать к фитотерапии, обязательно проконсультируйтесь со своим лечащим врачом.
Для информации приводим наиболее простые и эффективные (по утверждению народных целителей) рецепты для лечения обменной нефропатии:
- Одну столовую ложку тщательно измельченных листьев лопуха, брусники и зверобоя (приблизительно в равных частях) заливаем двумя стаканами кипятка и оставляем настаиваться в течение 12-14 часов. Профильтрованный лечебный состав принимаем по 3 столовые ложки перед едой.
- Толчем семена укропа и смешиваем их (в пропорции 1:1:1) с измельченными листьями брусники и земляники. 20-30 г смеси заливаем 400-450 мл горячей кипяченой воды и настаиваем (около 12 ч). 2 столовые ложки настойки принимаем за 30-40 мин до приема пищи.
У детей болезнь довольно часто протекает без явно выраженных симптомов, а выявляется случайно при очередной сдаче анализов (например, при поступлении в детский сад, школу, после перенесенного респираторного заболевания и так далее). Протекая незаметно, она может привести к хронической почечной недостаточности.
Основными внешними признаками дисметаболической нефропатии у детей являются: слабость, вялость, повышенная утомляемость, ухудшение аппетита, тени под глазами, отеки век или конечностей (например, ребенок может пожаловаться на то, что ему резко стала мала недавно купленная обувь), нерегулярность мочеиспускания, боли в животе, внезапное повышение температуры.
На заметку! Для того чтобы вовремя «забить тревогу» и обратиться к врачу, родителям следует следить за частотой мочеиспускания своего ребенка. В зависимости от возраста средние показатели: до года – 15 раз; в возрасте 2-3 лет – 10 раз; для дошкольников – 7-8 раз; у школьников – 5-7 раз.
Диагностика выявления дисметаболической нефропатии у детей ничем не отличается от проведения соответствующего лабораторного исследования у взрослых. Опытный врач-педиатр может назначить дополнительные исследования при превышении в общем анализе мочи ребенка белка, лейкоцитов, эритроцитов, солей и бактерий. Как правило, дети сдают такой анализ достаточно часто (при поступлении в ясли, детский сад, школу и так далее). Это позволяет установить наличие болезни почек на ранней стадии и приступить к ее своевременному лечению и, как следствие, избежать серьезных осложнений.
Специалисты подбирают медицинские препараты и диетический рацион питания при лечении дисметаболической нефропатии у детей в строгом соответствии с возрастом ребенка и индивидуальными особенностями развития.
Важно! Самолечением детей заниматься нельзя ни в коем случае. Только профессионал сможет правильно диагностировать болезнь и назначить эффективное лечение.
источник
Дисметаболическая нефропатия — выпадение осадка солей в моче у людей с нарушением обмена веществ и с вторичными изменениям в работе почек. У детей дисметаболическая нефропатия чаще вызвана наследственными патологиями обменных процессов, отягощенным нефрологическим /урологическим анамнезом или неблагоприятными факторами внешней среды.
Заболевание развивается в любом возрасте (нередко — в грудничковом) и не зависит от пола.
Выделяют первичную нефропатию, которая обуславливается наследственностью и встречается редко, и вторичную (приобретенную).
Наиболее часто дисметаболическая нефропатия развивается из-за нарушений кальциевого обмена и переизбытка щавелевой кислоты, что способствует образованию фосфатурии, уратурии или оксалурии.
Патология чаще диагностируется у детей.
Общие факторы риска, способствующие кристаллурии:
• проживание в неблагополучных регионах с плохой водой;
• однообразное питание с камнеообразующими веществами;
• сопутствующая патология: гиперпаратиреоз, почечный канальцевый ацидоз, саркоидоз, гипертиреоз, заболевания ЖКТ;
• опреация по поводу резекции подвздошной кишки;
• синдром мальабсорбции;
• авитаминоз;
• прием некоторых препаратов: витамин Д, С, кальций, сульфаниламиды, цитостатики, гормоны;
• длительная обездвиженность;
• чрезмерные постоянные физические нагрузки, повышающие уровень молочной кислоты;
• лучевая и химиотерапия в анамнезе;
• глистные инвазии;
• пороки развития мочевой системы: стриктуры, рефлюксы, уретероцеле, подковообразная почка и пр.
• хронический инфекционно-воспалительный процесс в мочеполовой системе.
Причина – нарушение обмена кальция и оксалатов. Появлению оксалатов в моче провоцирует следующее:
• погрешность в диете: большое количество продуктов с высоким содержанием щавелевой кислоты, витамина С;
• заболевания желудочно-кишечного тракта,
• авитаминоз А;
• длительный стресс;
• факторы окружающей среды;
• наследственная предрасположенность;
• отравление солями тяжелых металлов;
• прием некоторых лекарственных препаратов;
• изменения гормонального фона;
• сахарный диабет;
• нарушение синтеза паратиреоидного гормона;
• пищевая аллергия;
• неадекватный питьевой режим.
Общее развитие ребенка при оксалурии не страдает, но в ряде случаев патологии сопутствуют ожирение, аллергические реакции, головные боли.
Прогрессирование заболевания усугубляют изменения гормонального фона в период пубертата. Длительно существующая оксалурия у детей ведет к нефроуролитиазу, присоединению вторичной инфекции и острому воспалительному процессу органов мочевыделительной системы.
Заподозрить проблему можно по изменению мочи, в общем анализе периодически выявляются оксалаты. Суточная экскреция их с мочой повышена.
Важно! К оксалатной нефропатии у ребенка приводит переизбыток в рационе питания лактозы, сахарозы, витамина С, оксалатсодержащих продуктов.
Есть данные, что аномальное протекание беременности у матери с нарушением маточно-плацентарного кровообращения способствует появлению оксалурии у ребенка.
Причина — нарушение фосфорного-кальциевого обмена на фоне хронического воспаления в почках.
• неправильное питание,
• сахарный диабет;
• рахит;
• отягощенный урологический или нефрологический анамнез.
У детей периодическая фосфатурия в моче может быть не связана с серьезной патологией, после коррекции рациона питания ситуация иногда разрешается самостоятельно. Моча при фосфатурии с беловатым оттенком, иногда напоминает молоко, характерно появление осадка.
Уратная нефропатия развивается из-за накопления мочевой кислоты. Кристаллы ее оседают в тканях почки, что приводит к нарушению функциональной способности почек. Моча при этом приобретает яркий кирпичный оттенок.
В появлении уратурии рассматривается наследственный фактор, питание с большим количеством мяса, шоколада, насыщенных бульонов и консервированных продуктов. Выпадение уратов может наблюдаться при гемолитической анемии, эритремии, миеломной болезни, хроническом пиелонефрите. Прием цитостатиков, салициллатов, мочегонных препаратов также способствует развитию патологии. Одним из осложнений уратного солевого диатеза является подагрический артрит.
Изначально каких-либо проявлений патологии нет. У детей данный вид нефропатии может сопровождать чрезмерная раздражительность, плаксивость. Позднее изменяется внешний вид суставов, нарушается их функция, появляются кожные высыпания по типу дерматита, что связано с накоплением уратов в тканях.
Это форма нефропатии у детей связана с генетическими нарушениями. Отмечается избыточное накопление цистина (продукт обмена метионина) и связанное с этим нарушение реабсорбции в почечных канальцах.
Патология активно прогрессирует, что приводит к присоединению мочекаменной болезни, вторичного пиелонефрита, а со временем – к хронической почечной недостаточности в терминальной стадии.
Цистинурию несколько корректирует диета, но прогноз при дисметаболической нефропатии с цистинурией серьезный. Показана трансплантация донорского органа, причем почку пересаживают в детском возрасте. Со временем болезнь поражает и трансплантат, поэтому прогноз для жизни серьезный.
Выпадение в осадок оксалатов, уратов, фосфатов.
Для установления диагноза может быть полезным ультразвуковое исследование почек, мочевого пузыря.
Изменений при УЗ-диагностике в почках у детей может и не быть, у взрослых пациентов присутствуют множественные солевые включения, микролиты. Кроме этого, назначают ряд специфических и неспецифических анализов, одни из которых подтверждают диагноз дисметаболической нефропатии, другие позволяют выявить сопутствующую патологию:
• исследование общего и биохимического анализа мочи;
• биохимия крови: мочевина, креатинин, мочевая кислота, сахар, кальций и пр.
• посев на флору и чувствительность к антибиотикам;
• проба Нечипоренко,
• исследование антикристаллобразующих свойств мочи (АКОСМ);
• тестирование мочи на кальцифилаксию и перекиси;
• проба на цистин в моче.
Дополнительно могут быть назначены исследования: экскреторная урография, сцинтиграфия, ретроградная уретеро – и пиелография, компьютерная и магнитно-резонансная томография. Данная инструментальная диагностика проводится для уточнения причины, и чаще применяется при нефроуролитиазе.
Нарушение обмена веществ с повышенным образованием солей сопровождается повышенной нагрузкой на почки.
Токсическое действие неполных метаболитов вызывает повреждение почечных канальцев и постепенную утрату функциональной способности почек.
При выпадении в осадок кристаллов начинаются процессы камнеобразования.
Избыточное отложение солей в почках часто является причиной туболо-интерстициального нефрита.
При сахарном диабете, подагре часто появляются соли в моче у взрослых, у детей.
Среди всех случаев патологии превалирующей является оксалатная дисметаболическая нефропатия (35%), в 33% диагностируется уратная нефропатия, в 16% — фосфатная и в 13, 5 % обнаруживаются смешанные соли.
Патология не имеет каких-либо специфических симптомов, но для некоторых пациентов типичны боли в животе, расстройства мочеиспускания (рези, чувство неполного опорожнения мочевого пузыря, мочеиспускание по каплям, ургентные позывы в туалет), периодические тянущие боли в поясничной области.
Выход солевой пробки может сопровождаться почечной коликой: боли в пояснице, по ходу мочеточника, тошнота, рвота, дизурические расстройства. У некоторых пациентов появляются жалобы на отеки, повышение артериального давления (у детей чаще регистрируется гипотония).
Для мочи пациента характерен насыщенный цвет, могут визуализироваться солевые включения. Суточный диурез при этом может быть уменьшен, полиурия присоединяется, как симптом почечной недостаточности.
Признаки дисметаболической нефропатии в моче:
• изменение цвета;
• повышение плотности;
• осадок;
• эритроциты;
• белок;
• соли.
Большое количество бактерий и лейкоцитов свидетельствует о присоединившемся воспалении.
Подход к лечению комплексный, включает в себя следующие правила:
• нормализация питьевого режима;
• отказ от вредных привычек;
• правильное питание, корректирующее конкретное обменное нарушение;
• специфическую терапию.
Увеличение поступающей жидкости способствует снижению концентрации растворенных веществ в моче и учащает ночное мочеиспускание. Рекомендовано пить минеральную или чистую воду. Снижение нагрузки на почки можно добиться с помощью соответствующей диеты.
Рекомендовано исключить следующее:
• щавель;
• какао;
• холодец;
• шоколад;
• морковь;
• шпинат;
• мясной бульон;
• свеклу.
Рекомендовано добавить в рацион питания картофель, курагу, капусту, чернослив, груши.
Минеральные воды: Славяновская, Смирновская; длительность курса 30 дней, через 3 месяца повторить, по 3–5 мл/кг/сут. в 3 приема на голодный желудок.
Дополнительно принимают витамин В6, Е, А, препараты магния, Цистон.
Мембраностабилизаторы: Димефосфон, Ксидифон.
При уратурии предпочтительнее молочно-растительная диета. Ограничивают следующее:
• мясо;
• жиры;
• копчености и маринады;
• фасоль; орехи;
• какао;
• ливер и субпродукты;
• щавель, зеленые яблоки, шпинат;
• горох и пр.
Питание при уратах должно быть преимущественно молочно-растительным.
Важно пить до 2 литров слабощелочной жидкости, полезны растительные диуретики (отвары трав) на основе хвоща полевого, семян укропа, овса, толокнянки, березового листа.
Можно пить слабоминерализованную воду.
Под контролем биохимических лабораторных показателей назначают Алопуринол, Никотинамид, Фитолизин, Цистон, Цистенал, цитратные смеси: Магурлит, Уралит-У, Блемарен и пр.
Важно! В педиатрической практике Алопуринол не используют из-за выраженных побочных эффектов со стороны печени, крови и кожного покрова.
Отметим, что Никотинамид обладает более слабым действием, но переносится лучше Алопуринола.
Ограничивают потребление продуктов, содержащих большое количество фосфора: сыра, шоколада, икры, яиц, курицы, бобовых, молока и молочные продукты и пр. Шоколад, майонез, кулинарный жир, выпечка также не полезны при фосфатурии. Бульоны только нежирные и второй варки, маринады, копчености, соленья исключаются полностью.
• картофель,
• баклажаны;
• помидоры;
• шпинат;
• хрен;
• картофель;
• капуста брюссельская;
• морковь;
• лук.
Можно включить в питание каши на воде (рис и гречка), макароны, сладкие фрукты и цитрусовые, нежирные сорта мяса, курицы и рыбы (2-3 раза в неделю), шиповниковый отвар, клюква, брусника.
Препараты: Цистинал, витамин С, Метионин.
Нарзан способствует уменьшению фосфатурии. Повышенный питьевой режим до 2-2,5 литров.
• брусничный лист,
• фитонефрол;
• толокнянка и пр.
Отметим, что фосфатурия у детей встречается редко.
Рекомендовано резко ограничить потребление белковой пищи: мяса, сыра, яиц, творога, рыбы, грибов. Строгой диеты следует придерживаться 1-1.5 месяца, потом постепенно меню расширяют, полностью метионин, нужный для развития и роста, исключить нельзя. Уделяют внимание усилению водной нагрузки, пить воду нужно преимущественно в вечерние часы.
Минеральная вода предпочтительнее щелочная.
Дополнительно назначают Пеницилламин, Купренил, Блемарен, цитратную смесь.
Пенициламин обладает способностью инактивировать пиридоксин, поэтому обосновано назначение витамина В6.
В качестве стабилизаторов мембран используют витамины А и Е.
Хорошо помогают клизмы с бикарбонатом натрия (пищевой содой), для ребенка ½ столовой ложки на 500 мл воды, для взрослого 1 столовая ложка на 1 литр воды, 2 раза в неделю.
Суточное потребление жидкости для ребенка от 2 лет – 1,5 литра, старше 10лет – 2-2,5 литра, как и взрослым. Обязательно помимо бульонов, компотов и супов в рационе должна быть чистая вода. Грудной ребенок, находящийся на естественном вскармливании, также нуждается в обычной воде.
Большое количество жидкости способствует растворению солей и выведению их из организма.
Сладкие восстановленные соки, лимонад лучше заменить несладкими компотами и отварами трав с противовоспалительными и мочегонными свойствами.
Вне обострения пиелонефрита рекомендовано санаторно-курортное лечение с употреблением воды из минерального источника, что повышает ее целебные свойства.
Дисметаболическую нефропатию часто рассматривают как предшественницу мочекаменной болезни.
Аномалии развития, приведшие к кристаллурии, требуют рассмотрения вопроса о хирургической коррекции, не дожидаясь камнеобразования и хронического рецидивирующего пиелонефрита.
Большинство случаев нефропатии на фоне нарушения обмена веществ поддаются коррекции с помощью диетотерапии и консервативного лечения.
Группа здоровья при неосложненных обменных нефропатиях у детей – чаще вторая или третья, но следует учитывать и другие заболевания, которые могут быть у ребенка.
Обменная нефропатия у взрослых также бывает врожденной или приобретенной. Необходимо отметить, что диагноз не устанавливается на основании периодической кристаллуриии в моче, он должен быть подтвержден прочими лабораторными и инструментальными методами обследования.
Из питания рекомендовано исключить алкоголь, особенно красное вино, отказаться от вредных привычек.
Жидкости нужно принимать около 2-2,5 литров в сутки.
Стоит избегать ситуаций, связанных с повышенным потоотделением: посещение сауны, прогулки по жаре, чрезмерные физические нагрузки.
Факторы риска, проявления, клинические рекомендации, диагностика, диетотерапия при дисметаболической нефропатии у взрослых сходна с таковой у детей.
источник
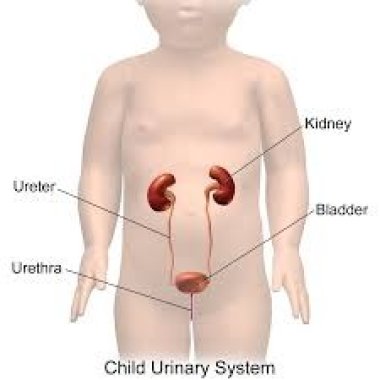
Дисметаболические нефропатии (кристаллурии) являются одними из наиболее часто встречаемых нарушений в практике педиатра и детского нефролога и носят преимущественно вторичный мультифакториальный характер. Наиболее часто у детей встречаются оксалатно-кальц
Dysmetabolic nephropathies (crystalluria) are among the most common disorders in pediatrician and pediatric nephrologist practice and are primarily secondary multifactorial. Most often in children, there are oxalate-calcium, urate and phosphate-calcium crystallurias. In their treatment, dietary correction is used; strengthened water and drinking regime; the use of energy-resistant drugs that improve the function of the mitochondria of the tubular epithelium; remedies which reduce the formation of a certain type of crystal. Complex therapy of dysmetabolic nephropathies allows to avoid possible complications.
Диcметаболические нефропатии (ДН) — гетерогенная группа заболеваний с различной этиологией и патогенезом, которые характеризуются поражением тубулоинтерстициального аппарата почек вследствие нарушения обмена веществ [1, 2, 9].
Проблема ДН является достаточно актуальной в педиатрии и детской нефрологии. Это обусловлено высокой частотой ДН в популяции, а также возможностью их прогрессирования вплоть до развития мочекаменной болезни и/или тубулоинтерстициального нефрита. В структуре заболеваемости мочевыделительной системы у детей ДН составляет от 27% до 64%, а в повседневной практике врача-педиатра синдром обменных нарушений в моче встречается практически у каждого третьего больного [8]. Параллельно отмечается увеличение частоты мочекаменной болезни (МКБ) в популяции в целом, которая в возрастной группе 65–69 лет у мужчин достигает 8,8%, у женщин — 5,6%, а в более молодом возрасте — 3,7% у мужчин и 2,8% у женщин [11]. Одной из причин повсеместного роста частоты МКБ является реализация во взрослом возрасте обменных нарушений, возникших в детстве. По данным эпидемиологического исследования, проведенного V. Romero (2010), частота уролитиаза в таких странах, как США, Италия, Германия, Испания, Япония, за последние 20 лет удвоилась, а в последние годы наблюдается наиболее драматический рост этого показателя [14].
В зависимости от причины выделяют первичные и вторичные ДН. Первичные ДН развиваются в рамках системных наследственно-обусловленных нарушений обмена, характеризуются прогрессирующим течением, ранним развитием уролитиаза и хронической почечной недостаточности. К ним относятся первичная наследственная гипероксалурия (оксалоз), синдром Леша–Нихана, цистиноз, цистинурия и некоторые другие заболевания. Первичные дефекты обмена встречаются достаточно редко, поэтому в данной статье в основном речь пойдет о вторичных ДН.
Вторичные ДН представляют собой вторичные тубулярные синдромы, иначе называемые дисметаболическими расстройствами (диатезами) с кристаллуриями, которые могут быть полигенно-наследуемыми или мультифакториальными. Тубулопатии с кристаллуриями, развивающиеся вследствие генетической предрасположенности, М. С. Игнатовой и Ю. Е. Вельтищевым (1992) были объединены термином «дисметаболические диатезы и нефропатии». Однако причиной вторичных ДН может быть также повышенное поступление определенных веществ в организм, нарушение их метаболизма в связи с поражением других органов и систем (например, желудочно-кишечного тракта), лекарственной терапией, нестабильностью цитомембран канальцев, дегидратацией и др. [1, 2, 8, 9, 11, 14].
В зависимости от типа нарушений обмена при дисметаболических диатезах выделяют оксалатный (щавелевокислый), уратный (мочекислый), цистиновый и другие диатезы.
Любые ДН, вне зависимости от причины, характеризуются мочевым синдромом в виде кристаллурии. В большинстве случаев именно первичная нестабильность мембран канальцевого эпителия является одной из причин кристаллурии. Вследствие генетической предрасположенности или токсического и гипоксического воздействия нарушаются процессы перекисного окисления липидов с образованием свободных радикалов, токсических форм кислорода, что приводит к накоплению вторичных токсических продуктов перекисного окисления липидов, в частности, малонового диальдегида. Параллельно активации процессов перекисного окисления липидов отмечается снижение активности ферментов антиоксидантных защитных систем, в том числе супероксиддисмутазы, активность которой может снижаться до четырех раз. Активное течение свободно-радикальных реакций на мембранах клеток в условиях снижения антиоксидантной защиты приводит к канальцевой мембранопатии, клеточной деструкции, вторичной кристаллурии.
Течение мембранопатологических процессов с развитием иммунного воспаления, циркуляторных нарушений может привести к формированию метаболического тубулоинтерстициального нефрита, представляющего собой острое или хроническое неспецифическое, абактериальное, недеструктивное воспаление интерстициальной ткани почек, сопровождающееся вовлечением в патологический процесс канальцев, кровеносных и лимфатических сосудов почечной стромы.
Персистирующая кристаллурия также может приводить к отложению кристаллов в ткани почки, а также к их адгезии, «слипанию» друг с другом, что служит основой формирования камня и развитию МКБ [12].
Наиболее часто в основе кристаллурии и МКБ лежат нарушения обмена кальция, щавелевой кислоты (оксалатов), мочевой кислоты (уратов), фосфатов, цистина и др. Подавляющее большинство кристаллурий и выявляемых камней связано с кальцием (от 70 до 90%), около 85–90% из них — с оксалатами (в виде оксалата кальция), остальные с фосфатами (фосфаты кальция — 3–10%) или являются смешанными — оксалатно-(фосфатно)-уратными. Уратная кристаллурия и литиаз составляют около 5%, цистиновая — до 3%. В 5–15% выявляются трипельфосфаты — фосфатные кристаллы, содержащие ион аммония, магний и кальций.
На кристаллообразование влияют три основных фактора: 1) перенасыщение канальцевой жидкости сверх пределов ее стабильности; 2) снижение активности ингибиторов перенасыщения; 3) активаторы преципитации.
Для образования кристалла необходимо наличие ионной пары — аниона и катиона (например, иона кальция и иона оксалата). Перенасыщение мочи различными видами ионов в конечном итоге приводит к их преципитации в виде кристаллов, к последующему их росту, кульминацией чего является образование камня [5, 6].
Кроме степени насыщения на растворимость ионов влияет ионная сила, способность к комплексообразованию, рН мочи и скорость ее тока. рН мочи также является важным фактором растворимости. Например, при кислых значениях рН мочевая кислота практически не диссоциирует и легко преципитирует; тогда как фосфатные соли (фосфат кальция), наоборот, малорастворимы при щелочных значениях рН мочи. Нарушение тока мочи также будет способствовать выпадению кристаллов, свидетельством чему является повторное образование камней в условиях частичной обструкции на фоне аномалий развития.
Довольно часто при перенасыщении мочи не выявляется кристаллурии. По всей видимости, это связано с действием ингибиторов перенасыщения — веществ, которые повышают способность мочи удерживать кристаллоиды в растворенном состоянии. Важными ингибиторами образования фосфатно-кальциевых кристаллов и камней являются пирофосфаты, цитрат, магний и низкомолекулярные вещества, а оксалатно-кальциевых — пирофосфаты и высокомолекулярные вещества.
Важными активаторами кристаллообразования является инфекция мочевой системы и рН мочи. Так, трипельфосфаты образуются только вследствие действия уреазоактивной флоры и являются свидетельством инфекции мочевой системы. Стойкое изменение рН мочи вследствие тех или иных заболеваний также может провоцировать кристаллообразование и рост камней. Например, при некоторых заболеваниях желудочно-кишечного тракта (ЖКТ) рН мочи постоянно сдвинут в кислую сторону, что приводит к образованию мочекислых камней из-за снижения растворимости мочевой кислоты в кислой среде [5, 6, 12].
Следует отметить, что понятия «дисметаболическая нефропатия» и «кристаллурия» не являются синонимами. Кристаллурия может носить транзиторный характер, выявляясь, например, на фоне интеркуррентных заболеваний, таких как респираторные вирусные инфекции. Дисметаболическая нефропатия, в свою очередь, не всегда сопровождается кристаллурией (например, после курса терапии и/или на фоне соблюдения диеты).
Одной из наиболее распространенных кристаллурий в детском возрасте к настоящему времени остается оксалатно-кальциевая кристаллурия.
У большинства больных с оксалатно-кальциевой кристаллурией нет выраженного нарушения метаболизма оксалатов или повышения их экскреции с мочой, но выявляется гиперкальциурия. Однако кристаллы оксалата кальция могут образовываться и при нормальном уровне кальция в моче, вследствие повышения содержания оксалатов. Таким образом, патогенез оксалатно-кальциевой кристаллурии может быть связан как с нарушением обмена кальция, так и с нарушением обмена оксалатов. Так как все оксалатные кристаллы содержат кальций, термины «оксалатная нефропатия» и «оксалатно-кальциевая нефропатия» употребляются как синонимы.
Оксалаты являются конечным метаболическим продуктом в организме, поэтому все они должны экскретироваться. Оксалаты попадают в организм экзогенно с пищей и всасываются в кишечнике или образуются эндогенно. Оксалаты полностью фильтруются в клубочках, затем реабсорбируются и секретируются в канальцах. Даже при небольшом повышении количества оксалатов в моче вследствие их высокой ионной силы высока вероятность выпадения кристаллов оксалата кальция, которые практически нерастворимы.
Гипероксалурические состояния возникают при увеличении всасывания оксалатов в кишечнике либо при повышении их эндогенного образования (табл.).
Избыточное всасывание оксалата в кишечнике при питании продуктами, содержащими большие количества щавелевой кислоты (ревень, шпинат, шоколад, крепкий чай, избыток аскорбиновой кислоты и др.) может возникать при увеличенном потреблении с пищей предшественников оксалата, таких как аскорбиновая кислота и этиленгликоль, либо при авитаминозе В6, что означает недостаточность пиридоксина, то есть коэнзима, участвующего в превращении глиоксилата в глицин. Приобретенной гипероксалурии способствуют нарушения функции желудочно-кишечного тракта, сопровождающиеся усиленным всасыванием оксалата. Они возникают при региональном энтерите, синдроме слепой кишки, хроническом панкреатите, хроническом гастрите, неотропическом спру, а также после панкреоэктомии или резекции части кишки. Этот тип гипероксалурии возникает при хирургических вмешательствах, связанных с созданием желудочно-кишечного обхода, когда при интактной толстой кишке создаются условия для движения пищи в обход дистального отдела тонкой кишки и наблюдается избыточное всасывание оксалатов, поступивших с пищей. У таких пациентов развивается стеаторея и затем гипероксалурия. Эти нарушения обусловлены повышением содержания в содержимом толстой кишки жирных кислот. Следует отметить, что жирные и желчные кислоты увеличивают проницаемость толстой кишки для органических веществ, подобных оксалату [7]. Одним из важных факторов нормального обмена оксалатов в кишечнике является Oxalobacter formigenes (O. formigenes), который относится к обычным представителям кишечной микрофлоры и обеспечивает утилизацию около 40–45% оксалатов в полости кишечника. При стойком нарушении кишечного биоценоза число O. formigenes снижается и соответственно увеличивается количество всасываемого оксалата. В целом следует отметить, что роль нарушений ЖКТ в развитии оксалатно-кальциевой кристаллурии настолько велика, что обнаружение оксалатной нефропатии требует обязательной консультации гастроэнтеролога и соответствующего обследования [13, 15].
В генезе гипероксалурий играет важную роль нарушение почечных цитомембран. Причины мембранопатий разнообразны. Лабильность фосфолипидного слоя цитомембран может приводить к кальцифилаксии — нарушению гомеостаза внутриклеточного кальция, приводящего к патологической кальцификации. Нестабильность цитомембран может быть результатом повышенной активности процессов перекисного окисления липидов, как вследствие окислительного стресса, так и снижения факторов антиоксидантной защиты. Все это будет приводить к ускоренному метаболизму мембранных фосфолипидов, вследствие активации фосфолипаз, и высвобождению компонентов липидной оболочки — фосфатидилэтаноламина, фосфатидилсерина, которые через этаноламин и серин будут метаболизироваться в оксалат [3, 5, 6].
Первые симптомы заболевания могут проявиться в любом возрасте, однако чаще отмечаются у детей 5–7 лет в виде лабораторных изменений. Клинически, как правило, данное заболевание себя никак не проявляет. Ввиду отсутствия специфических признаков самочувствие детей, как и общее состояние, чаще всего не страдают. Как правило, это дети, склонные к аллергическим реакциям, к ожирению, дети с синдромом вегетативной дистонии по симпатико-тоническому типу [16]. Иногда отмечаются жалобы на дизурические явления, особенно при присоединении инфекции мочевой системы.
Что касается лабораторных изменений, то мочевой синдром представлен оксалатно-кальциевой или фосфатно-кальциевой кристаллурией, гематурией разной степени выраженности, незначительной протеинурией, абактериальной лейкоцитурией. Также отмечено снижение антикристаллообразующей способности мочи, выявляется фосфолипидурия и повышение фосфолипазной активности мочи. Характерна гиперстенурия.
Морфологически выявляется деструкция апикальных поверхностей эпителия канальцев почек, лимфогистиоцитарная инфильтрация интерстиция. В просветах канальцев и интерстиции обнаруживаются кристаллы оксалата кальция. При прогрессировании заболевания отмечаются явления склероза, вовлечение гломерул.
В случае прогрессирующего течения заболевания, учитывая особенности патогенеза, возможно развитие тубулоинтерстициального нефрита, мочекаменной болезни, рецидивирующего течения пиелонефрита.
Чаще всего фосфатурия встречается при хроническом течении инфекции мочевой системы, что является основной причиной фосфатурии. Особенное значение для этого имеют микроорганизмы с уреазной активностью. Уреаза разлагает мочевину с ощелачиванием мочи, что приводит к перенасыщению мочи фосфатами магния и аммония (струвит). Соединение струвита с углекислым аппатитом в различных количествах приводит к образованию трипельфосфатных кристаллов. Для кристаллизации трипельфосфатов и дальнейшего формирования камней необходима щелочная реакция мочи. Истинная фосфатурия (или первичная) встречается при заболеваниях центральной нервной системы.
Часто фосфатно-кальциевая кристаллурия сопровождает оксалатно-кальциевую, но выражена при этом в меньшей степени. Фосфатурия также может развиваться вследствие нарушения кальциевого обмена при гиперкальциуриях, при этом кристаллы будут представлены в основном фосфатом кальция.
Уратная (подагрическая) нефропатия — патология почек, возникающая вследствие нарушения обмена пуринов или избыточного выведения солей мочевой кислоты почками, приводящая в уратному нефролитиазу или тубулоинтерстициальному нефриту.
Уратные нефропатии в зависимости от происхождения могут быть первичными и вторичными. Первичные уратные нефропатии обусловлены наследственными нарушениями метаболизма мочевой кислоты (подагра, синдром Леша–Нигана). Вторичные возникают как осложнения других заболеваний (эритремии, миеломной болезни, хронической гемолитической анемии, алкоголизма и др.), являются следствием применения некоторых препаратов (тиазидные диуретики, цитостатики, салицилаты, циклоспорин А и др.) или нарушения функции канальцев почек и физико-химических свойств мочи (при пиелонефрите, тубулоинтерстициальном нефрите и др.) [1, 2, 4, 9].
Мочевая кислота (урат) является конечным продуктом обмена пуринов. Следовательно, количество образующейся мочевой кислоты определяется количеством пуринов, поступивших с пищей, эндогенной продукцией и интенсивностью их перехода в мочевую кислоту. Большинство свободных пуриновых оснований утилизируется для ресинтеза пуриновых нуклеотидов.
На кристаллизацию мочевой кислоты влияют рН мочи, суточная экскреция мочевой кислоты и объем мочи. При повышении рН мочи растворимость мочевой кислоты резко возрастает (при изменении рН от 5 до 6 концентрация недиссоциированной формы снижается в 6 раз). В ночное время суток (во время сна) повышается экскреция уратов, снижается количество мочи, а также отсутствует подщелачивание мочи, что усугубляет риск выпадения кристаллов уратов [5, 12].
У больных с уратной нефропатией выявляется дефект почечной экскреции аммония, приводящий к избыточной экскреции титруемых кислот и снижению рН мочи. Причинами экскреции постоянно кислой мочи могут быть заболевания ЖКТ, сопровождающиеся диареей, вследствие дегидратации и/или потери бикарбонатов, а также при илеостоме, лекарственно-индуцированной ацидификации.
Уратурия, как причина, обусловившая поражение почек, выявляется у 14–26% больных. Уратные нефропатии (интерстициальный нефрит на фоне уратурии) представляют собой хронически протекающие заболевания, характеризующиеся умеренной протеинурией, микрогематурией и мочекислой кристаллурией. Результаты обследования детей с уратурией и их родственников выявили обменные нарушения, носящие семейный характер. Очень информативным оказался генеалогический анализ родословных, что позволяет выявлять определенный спектр почечной и внепочечной патологии среди родственников. Так, развитие уратной нефропатии на фоне ожирения, гиперлипидемиии, инсулинрезистентного сахарного диабета рассматривается как клиническое проявление метаболического синдрома, который носит семейный характер. Первые проявления синдрома отмечаются уже в подростковом возрасте. Другая причина развития гиперурикозурии — медикаментозная (диуретики, анальгетики, цитостатики). Экскреция мочевой кислоты с мочой считается превышающей норму при уровне более 1 мг на 1 мл, когда возникает опасность повреждения интерстициальной ткани почек, сосудов и камнеобразования. Что касается клинических проявлений, то при уратной нефропатии могут появиться жалобы на дизурические явления, рецидивирующие боли в животе, боли в поясничной области, в случае уролитиаза (у 5–41%) развивается почечная колика, в тяжелых случаях появляются клинические проявления подагры [4].
Цистин является продуктом метаболизма метионина и представляет собой наименее растворимую из встречаемых в природе аминокислот. Кристаллы цистина выпадают при превышении порога растворимости (более 400 мг/л) и при кислой реакции мочи [1, 2, 5, 9].
Можно выделить две основные причины повышения концентрации цистина в моче: избыточное накопление цистина в клетках почки и нарушение обратного всасывания цистина в почечных канальцах.
Однако наиболее часто кристаллы цистина выявляются при нефропатиях с преимущественным поражением канальцевого аппарата почек (пиелонефрит, тубулоинтерстициальный нефрит), и такая цистинурия носит вторичный характер. Если кристаллы оксалатов, уратов, фосфатов могут появляться эпизодически и при различных колебаниях в диете, то наличие цистина в моче — всегда признак патологии.
Диагноз цистинурии может быть заподозрен у любого пациента при наличии в анамнезе камней в почках, с текущими явлениями уролитиаза, отягощенным семейным анамнезом по мочекаменной болезни и специфическим янтарным окрасом камней.
Постановка диагноза ДН включает в себя комплексную оценку образа жизни ребенка, характер его питания, генеалогический анамнез, результаты лабораторно-инструментальных методов исследования. Скудность клинических проявлений компенсируется характерными лабораторными и инструментальными признаками заболеваний.
Лабораторно-инструментальная диагностика ДН основывается на выявлении кристаллурии в общем анализе мочи, повышении концентрации тех или иных солей в биохимическом исследовании мочи, исследовании антикристаллобразующей способности мочи (АКОСМ) и тестов на кальцифилаксию и перекиси в моче, ультразвуковом исследовании (УЗИ) почек и мочевыводящих путей.
Выявление кристаллов солей только в общих анализах мочи не является основанием для постановки диагноза ДН. Следует иметь в виду, что кристаллурия у детей часто бывает транзиторной и не связанной с патологией обмена и нестабильностью почечных цитомембран. Особенно это касается кристаллурии, выявляемой на высоте лихорадки, после перенесенных инфекций, диареи, а также у детей в периоде новорожденности при развитии «мочекислого инфаркта».
Для подтверждения диагноза ДН при выявлении кристаллурии в общем анализе мочи проводится биохимическое исследование мочи, где следует обратить внимание на концентрацию солей (оксалаты, мочевая кислота, кальций, фосфор и др.) и показатели функции канальцев (глюкоза, титруемая кислотность, аммиак, рН и др.), что позволяет выявить не только повышение экскреции тех или иных веществ, но и оценить условия для кристаллообразования, степень вовлеченности тубулярного аппарата в патологический процесс.
Повышение экскреции солей по данным биохимического исследования мочи при нормальных общих анализах мочи и отсутствии изменений при УЗИ почек также не может в полной мере свидетельствовать о ДН у ребенка, однако позволяет вынести полученные изменения в диагноз, например: гипероксалурия, гиперуратурия и т. д.
При подозрении на ДН отсутствие кристаллурии и повышенной экскреции солей с мочой у ребенка в данный момент не позволяет достоверно исключить этот диагноз. Нормальные показатели в общем и биохимическом анализах мочи могут быть обусловлены, например, правильной диетой и режимом жизни ребенка в данный период, тогда как предпосылки к тем или иным обменным нарушениям сохраняются.
Поэтому важно определить способность мочи растворять различные соли. Для этой цели проводится анализ на АКОСМ к оксалатам кальция, фосфатам кальция и трипельфосфатам, наиболее часто встречаемым при кристаллуриях у детей. В нормальной моче способность растворять эти соли и предотвращать кристаллообразование сохранна за счет наличия ингибиторов кристаллообразования и отсутствия или малой активности активаторов (промоторов) кристаллообразования. При ДН АКОСМ снижена в различной степени за счет повышения концентрации этих солей в растворенном виде и/или нарушения баланса ингибиторов и активаторов.
Тест на кальфилаксию позволят выявить нарушение клеточного гомеостаза кальция, приводящее к патологической кальцификации клеток и тканей. Тест на перекиси в моче отражает активность процессов перекисного окисления липидов цитомембран, повышение уровня перекисей будет являться признаком нестабильности цитомембран.
Ценность методов исследования мочи на АКОСМ, кальцифилаксию и перекиси заключается в возможности доклинического выявления патологии даже при отсутствии каких-либо других лабораторных признаков и в использовании их для контроля эффективности проводимой терапии [3].
Изменения, выявляемые при ультразвуковом исследовании почек, как правило, малоспецифичны и заключаются в очаговом или диффузном повышении эхогенности паренхимы почек за счет отложения кристаллов. Показанием к проведению более углубленного, в частности рентгенологического обследования, является обнаружение в почке при проведении УЗИ микролитов или включений, дающих эффект эхонегативной дорожки.
С учетом особенностей этиопатогенеза комплексное лечение ДН предполагает проведение мероприятий неспецифического (нормализация образа жизни, исключение гиподинамии, повышенный питьевой режим) и специфического характера (диета, коррекция метаболических нарушений медикаментозной терапией).
Нормализация образа жизни, физическое и психическое здоровье являются важным условием для достижения положительного эффекта в терапии ДН. Выраженные и длительные нарушения этих составляющих в конечном счете реализуются в микроциркуляторных отклонениях, ведущих к гипоксии, и/или в непосредственном повреждающем воздействии на клетки. Все это активизирует и/или усугубляет нарушения клеточного обмена, интенсивность перекисного окисления липидов мембран, их нестабильность и т. д.
Прием большого количества жидкости является универсальным способом лечения любой ДН, так как способствует уменьшению концентрации растворимых веществ в моче. Также важно время приема жидкости, особенно в периоды максимальной суточной концентрации мочи, т. е. во время сна. Поэтому одной из целей лечения является никтурия, что достигается приемом жидкости перед сном. Предпочтение следует отдавать простой или минеральной воде, поскольку длительный прием жидкостей, например, подкисляющих мочу или содержащих углеводы, может вызвать увеличение экскреции кальция [5].
Диета позволяет в значительной степени снизить метаболическую нагрузку на тубулярный аппарат.
При лечении больных с оксалатной нефропатией назначается картофельно-капустная диета, при которой снижается поступление оксалатов с пищей и нагрузка на тубулярный аппарат. Применение картофельно-капустной диеты в течение 2–3 недель сопровождается статистически достоверным снижением экскреции оксалатов, что сочетается с улучшением мочевого синдрома. Картофельно-капустная диета назначается на 3 недели с трехнедельными перерывами, во время которых ребенок получает диету № 5 по Певзнеру.
Также необходимо исключить экстрактивные мясные блюда, богатые оксалатами щавель, шпинат, клюкву, свеклу, морковь, какао, шоколад и др. «Подщелачивающий» эффект оказывают курага, чернослив, груши.
Из минеральных вод используются такие, как «Славяновская» и «Смирновская», по 3–5 мл/кг/сут в 3 приема курсом 1 мес 2–3 раза в год.
При лечении уратной нефропатии диета предусматривает исключение богатых пуриновыми основаниями продуктов (печень, почки, мясные бульоны, горох, фасоль, орехи, какао и др.). Преимущество должно отдаваться продуктам молочного и растительного происхождения. Важным условием успешной терапии является достаточное употребление жидкости — от 1 до 2 л в сутки. Предпочтение следует отдавать слабощелочным и слабоминерализованным водам, отварам трав (хвощ полевой, укроп, лист березы, брусничный лист, клевер пашенный, спорыш и др.), отвару овса. Для поддержания рН мочи в пределах 6,2–6,6 можно использовать цитратные смеси (Уралит-У, Блемарен, Магурлит, Солимок и др.), которые обладают значительной буферной емкостью [1, 4, 5, 9, 10].
Специфическая терапия должна быть направлена на предупреждение кристаллообразования, выведение солей, нормализацию обменных и энергетических процессов. Поскольку в большинстве случаев мембранопатия у детей является одним из звеньев патогенеза ДН, основной акцент делается на антиоксидантную и мембраностабилизирующую терапию.
Медикаментозная терапия включает мембранотропные препараты и антиоксиданты [5, 6, 9]. Лечение должно быть длительным и курсовым для достижения пролонгированного эффекта.
Пиридоксин (витамин В6) назначается в дозе 1–3 мг/кг/сут (до 400 мг/сут) в течение 1 мес ежеквартально. Витамин В6 оказывает мембраностабилизирующее действие за счет участия в обмене жиров в качестве антиоксиданта и обмене аминокислот. Целесообразно также назначение препарата Магне В6 из расчета 5–10 мг/кг/сут курсом в течение 2 мес 3 раза в год.
Мембраностабилизирующее действие оказывает витамин А, который встраивается в билипидный слой и нормализует взаимодействие белков и липидов мембраны. Суточная доза витамина А 1000 МЕ на год жизни ребенка, курсом 1 мес ежеквартально.
Токоферола ацетат (витамин Е) является мощным антиоксидантом, который поступает в организм извне и вырабатывается эндогенно. Необходимо помнить, что экзогенное введение витамина Е может тормозить его эндогенную продукцию по механизму отрицательной обратной связи. Витамин Е укрепляет белково-липидные связи клеточных мембран, участвует в процессах акцепции электронов при свободно-радикальных реакциях на мембранах. Назначается с витамином А в дозе 1–1,5 мг/кг массы в сутки.
В качестве мембраностабилизаторов также используются Димефосфон и Ксидифон. Димефосфон восстанавливает связь между окислением и фосфорилированием в клеточном дыхании, разобщенность которого наблюдается при нестабильности митохондриальных мембран, прерывая каскадные процессы перекисного окисления липидов. Применяется в дозе 1 мл 15% раствора на каждые 5 кг веса, 3 приема в сутки. Курс — 1 мес, 3 раза в год.
Ксидифон является комплексообразующим препаратом, который облегчает включение кальция в митохондрии и предупреждает отложение его нерастворимых солей. Назначается в дозе 10 мг/кг/сут 2% раствора в 3 приема. Курс — 1 мес, 2 раза в год.
В лечении детей с оксалатно-кальциевой кристаллурией широко применяется фитотерапия. Из комбинированных фитопрепаратов рекомендуется применение Цистона, Фитолизина и Канефрона. Цистон назначается в дозе 1–2 таблетки 2–3 раза в день курсом от 3 до 6 мес. Канефрон у взрослых применяется в форме драже и капель: по 2 драже 3 раза в день (или по 50 капель 3 раза в день). Для детей доза уменьшается в 2–3 раза в зависимости от возраста: по 11–25 капель или по 1 драже 3 раза в день в течение 6–8 недель [3].
Помимо этого, назначается окись магния, особенно при первичной гипероксалурии, в дозе 0,15–0,2 г/сут. При первичной гипероксалурии следует иметь в виду, что любая терапия является паллиативной. Радикальным методом лечения оксалоза является трансплантация печени, что устраняет дефект отсутствия аланин-глиоксилаттрансферазы и восстанавливает нормальный обмен оксалатов.
При гиперурикемии важно уменьшить концентрацию мочевой кислоты до 6 мг/100 мл и менее. Для этого используются средства, снижающие синтез мочевой кислоты, — ингибиторы ксантиноксидазы. Применение в педиатрии аллопуринола ограничено из-за возможных осложнений — гепатит, эпидермальный некроз, алопеция, лейко- и тромбоцитопения, повышение уровня ксантина в крови. Под строгим контролем аллопуринол назначают в дозе 0,2–0,3 г/сут в 2–3 приема в течение 2–3 нед, затем доза снижается. Длительность общего курса — до 6 мес. Никотинамид является более слабым ингибитором активности ксантиноксидазы, чем аллопуринол, но лучше переносится; назначается в дозе 0,005–0,025 г 2–3 раза в сутки по 1–2 мес повторными курсами. Колхицин снижает транспорт пуриновых оснований и скорость их обмена. Назначается в дозе 0,5–2 мг/сут сроком от 18 мес до нескольких лет.
Урикозурическим эффектом также обладают оротовая кислота, Цистон, Этомид, Цистенал, Фитолизин и др. Калия оротата таблетки назначаются в дозе 10 мг/кг в сут в 2–3 приема в течение 1 мес. Урикозурическим и урикозостатическим действием обладает также бензбромарон, который применяют по 50–100 мг/сут 2–3 раза в сочетании с салуретиками и цитратом натрия [5, 6, 9].
Лечение при фосфатной кристаллурии должно быть направлено на подкисление мочи (минеральные воды: «Нарзан», «Арзни», «Дзау-суар» и др.; препараты: Цистенал, аскорбиновая кислота, метионин). Назначается диета с ограничением продуктов, богатых фосфором (сыр, печень, икра, курица, бобовые, шоколад и др.). При выраженной экскреции фосфата кальция необходимо добиться снижения всасывания фосфора и кальция в кишечнике (например, назначением Альмагеля). Обязательным компонентом лечения при наличии трипельфосфатов является антибактериальная терапия и санация хронической инфекции мочевой системы [9].
Лечение цистиноза и цистинурии включает диету, высокожидкостный режим и медикаментозную терапию, направленную на подщелачивание мочи и повышение растворимости цистина [2, 4–6].
Цель диетотерапии — предотвратить избыточное поступление в организм ребенка предшественника цистина — метионина и других серосодержащих кислот. Для этого также исключают (или резко ограничивают) из рациона питания ребенка богатые метионином и серосодержащими аминокислотами продукты — творог, рыбу, яйца, мясо и др. Поступление метионина при таких диетических мероприятиях сокращается до 0,7 г/сут. Поскольку метионин необходим растущему организму ребенка для пластических процессов, длительное применение строгой диеты невозможно, поэтому через 4 нед от начала диетотерапии рацион ребенка расширяется и приближается к обычному, но характеризуется строгим исключением рыбы, творога и яиц.
Количество жидкости, употребляемой ребенком, должно быть не менее 2 л/сут, особенно важно принимать жидкость перед сном. Для подщелачивания мочи используется цитратная смесь, растворы гидрокарбоната натрия, Блемарен, щелочные минеральные воды. Это позволяет добиться повышения рН мочи до 7,5–8,0. Снижению концентрации цистина и повышению рН мочи будут также способствовать ингибиторы карбоангидразы (Диакарб) и Гипотиазид.
Для повышения растворимости цистина и предупреждения кристаллизации назначается пеницилламин, с целью активации тиолзависимых ферментов. Пеницилламин обладает некоторой токсичностью и антиметаболическим действием на пиридоксин, поэтому в начале терапии назначаются невысокие дозы препарата — 10 мг/кг/сут в 4–5 приемов, далее доза увеличивается в течение недели до 30 мг/кг/сут, а при цистинозе — до 50 мг/кг/сут. Лечение пеницилламином должно проводиться под контролем содержания цистина в лейкоцитах и/или цианиднитропруссидного теста (проба на цистин в моче, где концентрация цистина должна составлять до 150–200 мг/л). При достижении этих показателей доза пеницилламина снижается до 10–12 мг/кг/сут. Лечение пеницилламином проводится длительно, годами. Поскольку пеницилламин инактивирует пиридоксин, параллельно назначается витамин В6 (пиридоксин) в дозе 1–3 мг/кг/сут в течение 2–3 мес с повторными курсами. Для стабилизации мембран почечных канальцев назначаются витамин А (6600 МЕ/сут) и витамин Е (токоферол, 1 капля на 1 год жизни 5% раствора в сутки) в течение 4–5 нед с повторными курсами. Имеются данные о положительном эффекте применения вместо пеницилламина менее токсичного его аналога — Купренила в уменьшенной дозе в сочетании с Ксидифоном и другими мембраностабилизаторами [1, 9].
При цистинозе успешно используется трансплантация почки, которая проводится до развития терминальной стадии хронической почечной недостаточности (ХПН). Трансплантация почки позволяет значительно увеличить срок жизни больных — до 15–19 лет, однако отложение кристаллов цистина наблюдается и в трансплантате с преимущественным поражением интерстиция и мезангиума, что в конечном итоге приводит к развитию интерстициального фиброза и склерозированию в пересаженной почке и ХПН.
При развитии на фоне ДН и МКБ хронического пиелонефрита необходимо включение в комплексную терапию наряду с антибиотиками иммунокорригирующих препаратов, повышающих эффективность антибиотикотерапии, особенно учитывая часто наблюдающуюся у таких больных поливалентную антибиотикорезистентность. С этой целью могут использоваться различные препараты (Уро-Ваксом, Иммунал, Имунофан, левамизол, Ликопид и др.) [6].
Прогноз при вторичной ДН в целом благоприятен. В большинстве случаев при соответствующем режиме, диете и медикаментозной терапии удается добиться стойкой нормализации соответствующих показателей в моче. В отсутствие лечения или при его неэффективности наиболее естественными исходами ДН являются МКБ и тубулоинтерстициальный нефрит.
Диспансерное наблюдение включает в себя ежегодное обследование по плану. При необходимости биохимическое исследование мочи проводят 1 раз в 3–6 месяцев. Основные профилактические мероприятия направлены на сбалансированное питание ребенка и профилактику осложнений (инфекция мочевой системы, мочекаменная болезнь, тубулоинтерстициальный нефрит).
- Вельтищев Ю. В., Игнатова М. С. Наследственные и врожденные болезни почек и мочевыводящих путей. В кн.: Наследственная патология человека / Под ред. Ю. В. Вельтищева, Н. П. Бочкова. М., 1992. Т. 2. С. 3–71.
- Возианов А. Ф., Майданник В. Г., Бидный В. Г., Багдасарова И. В. Основы нефрологии детского возраста. Киев: Книга плюс, 2002. С. 214–225.
- Длин В. В., Османов И. М., Юрьева Э. А. Обменные нефропатии. М.: Оверлей, 2009. 128 с.
- Игнатова М. С. Наследственные и врожденные нефропатии. В кн.: Нефрология / Под ред. И. Е. Тареевой. М.: Медицина, 2000. С. 337–371.
- Малкоч А. В. Дисметаболические нефропатии и мочекаменная болезнь. В кн.: Нефрология детского возраста: Практическое руководство по детским болезням. М.: Медпрактика, 2005. Т. 6. С. 472–516.
- Малкоч А. В., Бельмер С. В. Мочекаменная болезнь у детей // Лечащий Врач. 2005, № 7. [Электронный ресурс: URS https://www.lvrach.ru/2005/07/4532751/, дата обращения: 17.08.2018].
- Малкоч А. В., Бельмер С. В. Нефропатии при целиакии // Лечащий Врач. 2012, № 8. [Электронный ресурс]. URL: https://www.lvrach.ru/2012/08/15435496/ (дата обращения: 17.08.2018).
- Рычкова С. В. Дисметаболические нефропатии в педиатрической практике // Лечащий Врач. 2010, № 8. [Электронный ресурс]. URL: https://www.lvrach.ru/2010/08/15392892/ (дата обращения: 17.08.2018).
- Юрьева Э. А., Длин В. В. Диагностический справочник нефролога. Клиническая и лабораторная диагностика. М.: Изд. «Медпрактика-М», 2007. 352 с.
- Cameron J. S., Moro F., Simmonds H. A. Gout, uric acid andpurine metabolism in paediatric nephrology // Pediatr. Nephrol. 1993; 7: 105–118.
- Indridason O. S., Birgisson S., Edvardsson V. O., Sigvaldason H., Sigfusson N., Palsson R. Epidemiology of kidney stones in Iceland: a population-based study // Scand. J. Urol. Nephrol. 2009. Vol. 40, № 3. P. 215–220.
- Jobs K., Rakowska M., Paturej A. Urolithiasis in the pediatric population — current opinion on epidemiology, patophysiology, diagnostic evaluation and treatment // Dev Period Med. 2018; 22 (2): 201–208.
- John C. Lieske Probiotics for prevention of urinary stones [Электронный ресурс]. URL: http://dx.doi.org/10.21037/atm.2016.11.86 (дата обращения: 17.08.2018).
- Romero V., Akpinar H., Assimos D. G. Kidney Stones: A Global Picture of Prevalence, Incidence, and Associated Risk Factors // Rev Urol. 2010. Vol. 12, № 2–3. P. 86–96.
- Sadaf H., Raza S. I., Hassan S. W. Role of gut microbiota against calcium oxalate. // Microb Pathog. 2017 Aug; 109: 287–291.
- Sakhaee K., Capolongo G., Maalouf N. M., Pasch A., Moe O. W., Poindexter J. et al. Metabolic syndrome and the risk of calcium stones // Nephrol Dial Transplant. 2012. № 8. Р. 3201–3209.
А. В. Малкоч* , 1 , кандидат медицинских наук, профессор
Е. Г. Куликова**
Ю. Б. Юрасова***, доктор медицинских наук, профессор
* ФГБОУ ДПО РМАНПО, Москва
** ГБУЗ МО МОКДЦД, Мытищи
*** ФГБОУ ВО МГУПП, Москва
Дисметаболические нефропатии в практике педиатра/ А. В. Малкоч, Е. Г. Куликова, Ю. Б. Юрасова
Для цитирования: Лечащий врач № 1/2019; Номера страниц в выпуске: 34-39
Теги: диета, водно-питьевой режим, энерготропные препараты
источник