
- подготовка биологического материала для исследования;
- проведение полимеразно-цепной реакции;
- обработка полученных материалов.
ПЦР-диагностика является универсальным и точным методом исследования. В ходе анализа осуществляется копирование конкретного участка нуклеиновой кислоты, соответствующего заданным параметрам, в результате чего подтверждается или опровергается наличие инфекции. Основное преимущество ПЦР по сравнению с другими методами состоит в том, что такое исследование позволяет поставить диагноз даже при небольшой концентрации возбудителей в организме.
Оппортунистические инфекции, выявляемые с помощью ПЦР
- Epstein Barr Virus (EBV);
Под воздействием вируса Эпштейна Барр развивается инфекционный мононуклеоз. Основные его симптомы: лихорадка, воспаление лимфоузлов, миндалин, интоксикация организма. Заразиться им можно воздушно-капельным путем. Диагностика проводится с использованием ПЦР. Кроме того, данный анализ позволяет выявить и ангину, и герпетическую инфекцию, и тонзиллит. В случае трансплантации органов и тканей исследование проводится для определения реактивации вируса. ПЦР обязательно назначается при наличии припухлостей в области лимфатических узлов и других первичных признаков мононуклеоза, а также ВИЧ-инфицированным.
Анализ, осуществляемый на основе венозной или капиллярной крови, позволяет определить наличие и количество вируса Эпштейна Барр в организме. После проведения ПЦР может быть получен отрицательный результат, который свидетельствует либо об отсутствии инфекции в организме, либо низком содержании вируса, или положительный, подтверждающий вирусоносительство или инфицирование.
- Cytomegalovirus (CMV);
Вызывает развитие цитомегаловирусной инфекции, которая диагностируется посредством ПЦР. В качестве биологического материала для анализа берется урогенитальный или ректальный мазок, эякулят, утренняя моча. Для точности результатов пациентам следует соблюдать некоторые правила. Женщинам предоставлять биологический материал необходимо до менструации или после ее окончания, а мужчинам не следует ходить в туалет за 3 часа до сдачи мочи или мазка.
Цитомегаловирусная инфекция передается половым путем, во время поцелуя. Заражение происходит и при контакте с мочой или слюной больного человека. В большинстве случаев инфекция проходит бессимптомно. В тяжелой форме она протекает у пациентов с ослабленным иммунитетом, у детей и ВИЧ-инфицированных. Новорожденным ПЦР назначается, если до его рождения у матери была обнаружена цитомегаловирусная инфекция. Анализ проводится при наличии симптомов мононуклеоза, при иммунодефиците, во время беременности. Отрицательный результат подтверждает отсутствие вируса в организме, положительный свидетельствует о его наличии, причем ПЦР в таком случае в дальнейшем проводится повторно для получения информации об эффективности лечения.
- Human Herpes Virus 6 (HHV-6).
Этот вирус провоцирует развитие герпес-вирусной инфекции 6-го типа. Ее диагностика осуществляется с помощью ПЦР на основе венозной крови. Заражение инфекцией происходит воздушно капельным путем, при контакте с кровью или слюной больного. ПЦР обязательно проводится у детей для диагностики заболеваний, основные симптомы которых – это высокая температура и сыпь, у пациентов, страдающих гемобластозами, больных после трансплантации тканей и органов. Целесообразно также проводить данный анализ у ВИЧ-инфицированных.
По результатам ПЦР можно выявить наличие HHV-6 в организме, определить, активно или пассивно протекает инфекция, диагностировать герпетические инфекции. Данный вирус, оставаясь в пределах одних клеток, способен поражать другие. Это часто становится причиной ложноотрицательного результата.
ПЦР – точный метод диагностики при оппортунистических инфекциях. При соблюдении всех условий проведения анализа и чистоты используемого биологического материала он позволяет выявить заболевание, а в дальнейшем определить эффективность борьбы с вирусом.
источник
Опубликовано в журнале:
«Практика педиатра», февраль 2011, с. 10-15
Ю.А. Копанев, детский гастроэнтеролог-инфекционист, ФГУН Московский НИИ эпидемиологии и микробиологии им. Г.Н. Габричевского Роспотребнадзора, канд. мед. наук
Хронические инфекционные болезни у детей встречаются ненамного реже острых инфекционных состояний, а термин «оппортунистические инфекции» перестал быть сугубо специальным для инфекционистов и гинекологов. Теперь с этой проблемой сталкиваются все врачи, в том числе педиатры.
Современные методы диагностики, в частности определение антител в крови методом ИФА и определение ДНК возбудителя методом ПЦР, продемонстрировали, что инфицированность людей оппортунистическими инфекциями достигает 90–99%.
Что такое оппортунистические инфекции
Так обозначаются распространенные хронические инфекционные заболевания, вызываемые условно патогенными микроорганизмами разных типов (вирусы, бактерии, простейшие, внутриклеточные микробы), поражающими преимущественно слизистые оболочки и лимфатическую систему, передающимися разными путями и имеющими ряд закономерностей.
Главная особенность всех хронических инфекций – возможность существования в активной и «спящей» (латентной) форме, а также «айсберговый» тип существования (рис. 1). Большинство микроорганизмов присутствует в организме в неактивной форме, как подводная невидимая часть айсберга. Для организма такие неактивные микроорганизмы не представляют угрозы, клинической картины не вызывают, иммунная система на них практически не реагирует, и, самое главное, на неактивные формы не действуют этиотропные препараты (антибиотики, противовирусные и другие средства). Активных микробов меньше, они уязвимы для лекарств, вызывают клинические проявления, на них вырабатываются антитела (врачи начинают «видеть» хроническую инфекцию, как надводную часть айсберга). Соотношение активных и неактивных форм зависит от состояния иммунной системы. В случае адекватной работы иммунной системы хроническая инфекция может быть полностью подавлена, т.е. практически все микроорганизмы будут находиться в неактивной форме, а человек не только будет физически здоров, но и антитела на данную инфекцию будут на низком уровне (в пределах нормы).
 |
При ослаблении иммунитета происходит активизация значительных количеств оппортунистических микробов, соотношение «спящих» и активных смещается в сторону последних, нарастает клиническая картина. В этот момент лечение будет максимально эффективным. Знание этих особенностей оппортунистических инфекций помогает выбрать правильную и эффективную лечебную тактику.
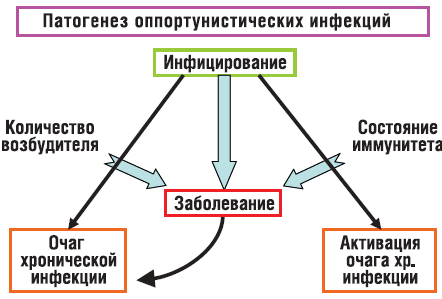
Формирование очагов хронических (оппортунистических) инфекций происходит так, как изображено на рисунке 2. Инфицирование становится заболеванием, если нарушается баланс между количеством возбудителя, попавшего в организм, и состоянием иммунной системы. При ослабленном иммунитете даже небольшое количество микроба может создать проблемы, а большое количество микроорганизмов вызовет заболевание и при неослабленном иммунитете. Некоторые микроорганизмы могут вызвать острое заболевание, а потом перейти в хроническую форму; например, это характерно для вируса Эпштейн Барр – возбудителя инфекционного мононуклеоза. Другие возбудители могут формировать хроническое заболевание без стадии острой болезни, например лямблии (острая форма лямблиоза встречается очень редко). Активизация хронической инфекции может произойти на фоне инфицирования любым другим микробом, тогда к клиническим проявлениям, характерным для этого микроорганизма, присоединяются клинические проявления, характерные для хронического очага. Например, ребенок заболевает ОРВИ, через несколько дней присоединяются симптомы кишечных нарушений. Это может быть активизацией очага хронической инфекции в ЖКТ, спровоцированной ОРВИ.
Эпидемиология
Для оппортунистических инфекций характерны всевозможные пути заражения:
- воздушно капельный (хламидии, легочные микоплазмы); передаваться могут как активные, так и неактивные формы, если человек является не только носителем, но и выделителем микроба в окружающую среду (большинство людей являются носителями, примерно 15% – выделители);
- фекально оральный (хламидии – Ch. psittaci, лямблии); хламидийная инфекция характерна для птиц, животных. Экскременты перемешиваются с землей, загрязняют руки и продукты, при попадании загрязненных и инфицированных элементов в кишечник там может сформироваться очаг хронической инфекции;
- половой (урогенитальный хламидиоз, оппортунистические инфекции); вертикальный (трансплацентарно, во время родов); за счет того, что хронические инфекции существуют в виде активных и неактивных форм (рис. 1), возможен такой способ передачи инфекции от матери плоду: у беременной женщины существует оппортунистическая инфекция в латентной форме, клинических проявлений нет, антитела в крови – в пределах нормы или не выявляются. Происходит вертикальная передача инфекции плоду (передаются неактивные формы), у родившегося ребенка в какой-то момент происходит активизация инфекции;
- трансмиссивный (через кровь и насе комых).
 |
Закономерности влияния на организм
Любой очаг хронической инфекции может вызвать следующие нарушения в организме:
- нарушение функции той системы, где локализуется данный очаг. Очаги хронической инфекции ЖКТ приводят к функциональным нарушениям: дисбактериозу кишечника, диспанкреатизму, дискинезии кишечника и желчевыводящих путей и т.п. Инфекции, тропные к лимфатической системе, вызывают лимфа денопатии. Инфекции дыхательных путей – различные респираторные дисфункции, хронический кашель, хронические заболевания верхних дыхательных путей. Если локализация инфекции мочеполовая система – гинекологические и урологические болезни, а также инфекции мочевыводящих путей;
- ослабление иммунной системы – это не дает возможности организму справиться с очагом хронической инфекции, приводит к появлению новых очагов, а также к частым ОРВИ у детей (часто болеющие дети) и другим проявлениям иммунной дисфункции;
- сенсибилизация с последующим формированием аллергических болезней. Очаги хронической инфекции ЖКТ могут быть одной из главных причин развития атопического дерматита и рецидивирующей крапивницы. Хронические инфекции дыхательной системы способствуют развитию бронхиальной астмы, поллиноза;
- хроническая интоксикация. Продукты жизнедеятельности микроорганизмов и пара зитов могут быть причиной неврологических нарушений, в том числе судорожного синдро ма, бруксизма (скрипение зубами), а также на рушений сна, аппетита, эмоциональной ла бильности, капризности, раздражительности, агрессивности;
- нарушения обмена веществ.
Эти симптомокомплексы менее выражены, когда хроническая инфекция находится в состоянии неактивности, и манифестируют во время активизации очага хронической инфекции. Если очагов хронической инфекции несколько и количество активных форм велико, симптомов становится больше, патологические состояния протекают в подострой форме волнообразно.
Наличие даже одного направления клинической картины должно наводить педиатра на предположение о поиске хронических (оппортунистических) инфекций.
Принципы диагностики
Выявление инфекционного фактора может идти по двум направлениям.
- Поиск возбудителя (микробиологические методы, посевы и т.п.), его ДНК (метод ПЦР) или продуктов его жизнедеятельности (биохимические методы).
- Выявление иммунной реакции организма на инфекцию (поиск антител методом ИФА и др.). Особенности разных методов диагностики представлены в таблице 1.
| Выявление возбудителя | Выявление антител |
|
|
Для первичной диагностики большинства оппортунистических инфекций лучше применять исследование крови – выявление антител. При этом диагностически значимым является повышение количества антител класса G. Методы ИФА и ПЦР могут дополнять друг друга. Возможна такая ситуация: все исследования показали отсутствие инфекции (т.е. ее нет ни по результатам ИФА, ни методом ПЦР или посевом), но это не означает, что микроба нет в организме, он может быть в «спящей» форме и неактивным. Если женщина перед беременностью или во время нее сдавала анализы и оппортунистические инфекции не были выявлены, а у ребенка выявится, например, хламидиоз, это может означать внутриутробное инфицирование неактивным микробом и активизация его у ребенка уже после рождения.
Трактовка результатов анализов представлена в таблице 2. В двух последних строках – ситуации, не требующие лечения.
| IgG | IgM | IgA | ПЦР | Трактовка |
| ↑ | N | N | ↑ или N | Инфекция есть (или есть иммунная память) |
| ↑ или N | ↑ | N | — | Активная фаза (недавнее первичное инфицирование) |
| ↑ или N | ↑ или N | ↑ | — | Активизация хронической инфекции |
| N | N | N | ↑ | Инфекция неактивна (или убитые микробы) |
| N | N | N | N | Инфекции нет (или нет клинически значимой) |
Повышение антител класса G выше диагностически значимых титров к какой либо хронической инфекции при первичной диагностике должно трактоваться как наличие этой инфекции и требует терапевтических действий: иммунокоррекции или активной этиотропной терапии.
Актуальные в педиатрии хронические инфекции
Бактериальные инфекции, вызванные условно патогенной флорой (УПФ)
Возбудители: гемолизирующая кишечная палочка, золотистый стафилококк, гемолизирующие стрептококки, клебсиеллы, лактозонегативные энтеробактерии и др. Живут на слизистых оболочках и в просвете ЖКТ, дыхательных, мочевыводящих путей.
Диагностика: бактериологические посевы – мазки из ВДП, половых органов, посевы на стерильность, исследования фекалий «на дисбактериоз».
Тактика педиатра: иммунокоррекция, применение фаготерапии, антисептиков. Применение антибиотиков показано в острую фазу (фебрильная температура, выраженность клинических проявлений).
Хламидийная инфекция
Возбудители: Ch. trachomatis, Ch. pneumoniae, Ch. psittaci. Вызывают внутриклеточные инфекции, поражающие слизистые оболочки и лимфатическую систему. Могут поражать все системы, где есть слизистая оболочка: конъюнктива глаза (интранатальное инфицирование); верхние дыхательные пути (ВДП), нижние дыхательные пути (воздушно капельный путь); слизистая ЖКТ (фекально оральный путь); мочеполовая система (половой путь или занос через лимфатическую систему);
Источники заражения:
- Человек, как здоровые носители, так и те, у кого активная форма болезни, при условии локализации на слизистых, сообщающихся с окружающей средой. Считается, что носителями хламидий являются более 90% людей.
- Птицы (попугаи, голуби, воробьи и др.). Хламидии выделяются с птичьим пометом, помет попадает в почву и на продукты питания, заражение человека происходит фекально оральным или воздушно-капельным путем.
- Кошки, мелкий рогатый скот (козы).
Заражение происходит воздушно капельным и фекально оральным путем.
Инфицирование – еще не заболевание. Клинические признаки появляются при ослаблении иммунитета.
Клиническая картина зависит от локализации и активности хламидий:
- конъюнктивит (бывает у новорожденных детей при интранатальном инфицировании);
- хронические рецидивирующие заболевания ВДП (тонзиллит, фарингит), а также острые заболевания (ангина);
- рецидивирующие бронхиты или пневмонии, бронхообструкция, астма;
- хроническая дисфункция ЖКТ, дисбактериоз, не поддающийся лечению;
- атопический дерматит (хламидии, будучи внутриклеточной инфекцией, могут приводить к повреждению гистаминобразующих тучных клеток слизистых оболочек) с торпидным течением без эффекта от лечения;
- острые и рецидивирующие заболевания мочевыводящих путей, вульвиты и другие поражения половой системы.
- у детей диагноз подтверждается методом ИФА по выявлению антител;
- метод ПЦР и другие исследования, направленные на выявление возбудителя, практически не имеют смысла, поскольку локализация инфекции происходит чаще всего в труднодоступных для исследования местах (например, глубоко в бронхах или в слизистой оболочке кишечника);
- мазок из зева на выявление хламидий (методом ПЦР) нужен только для выявления степени эпидемиологической опасности, но не может быть основанием для назначения лечения;
- направление на анализы крови для выявления антител к хламидиям – по клинической картине и при наличии эпидемиологических указаний (при выявлении хламидийной инфекции в близком окружении).
Врачебная тактика при хламидийной инфекции. Применение антибактериальной терапии показано только при наличии признаков активности хламидийной инфекции, иначе не будет эффекта.
Показания для антибактериальной терапии:
- любое острое состояние, требующее назначения антибиотика: ангина, пневмония, острый бронхит, гнойный отит, гнойный тонзиллит, гайморит в стадии обострения;
- ОРЗ с высокой температурой (более 38,0 °С) более 3–5 дней;
- ОРЗ с температурой выше 37,0 °С, если она держится более 7–10 дней подряд;
- бронхообструктивный синдром; приступ бронхиальной астмы (если наличие хламидийной инфекции подтверждено анализами);
- затяжной кашель более 3 недель;
- обострение дерматита (если наличие хламидийной инфекции подтверждено анализами);
- неэффективность лечения аллергических болезней.
Все эти симптомы могут возникнуть при активизации хламидий за счет ослабления иммунной системы. В этот период они становятся максимально уязвимыми, а лечение – максимально эффективным. Нужно только применить правильный антибиотик! При подтвержденной хламидийной инфекции или подозрении на нее в случаях, когда нужен антибиотик, можно применять только те антибиотики, которые действуют на хламидии: макролиды, фторхинолоны, препараты тетрациклинового ряда. У детей используются толь ко макролиды! Применение «неправильного» антибиотика (пенициллинового ряда или цефалоспоринов) при хламидийной инфекции приведет не только к упущенной возможности значительно сократить количество хламидий в период их максимальной уязвимости, но и усилит их, позволив распространиться на соседние участки слизистых оболочек. Это в итоге приводит к аллергизации и астматизации (к этому же приводит и несвоевременное применение антибиотика).
Примерная схема лечения в острый период хламидийной инфекции:
- Свечи Виферон и/или КИПферон для укрепления иммунной системы и повышения эффективности антибиотика, 10 дней.
- Антибиотик – макролид (кларитромицин, рокситромицин, мидекамицин, джозамицин, спирамицин), курс 10 дней.
Вне периода активности применяются общеукрепляющие средства и иммунокоррекция.
Микоплазменная инфекция
Возбудители: М. pneumoniae, М. hominis. Вызывают внутриклеточные инфекции, поражающие слизистые оболочки. Излюбленная локализация: дыхательные пути (как верхние, так и нижние) и мочеполовая система (МПС).
Источники заражения: человек – как здоровые носители, так и те, у кого активная форма при условии локализации на слизистых, сообщающихся с окружающей средой. Считается, что носителями микоплазм являются более 90% людей.
Клиническая картина – заболевания дыхательных путей и МПС. До 30% бронхиальной астмы ассоциировано с наличием микоплазменной инфекции, удачное лечение которой может избавить человека от заболевания или существенно улучшить его течение.
Диагностика и лечебная тактика при микоплазменной инфекции не отличаются от таковой при хламидийной инфекции.
Вирусные хронические инфекции Возбудители: вирус Эпштейн Барр (ВЭБ), вирусы простого герпеса 1 го, 2 го, 6 го типов (ВПГ), цитомегаловирусы (ЦМВ) и др.
Для ВЭБ характерны как острое заболевание (инфекционный мононуклеоз), так и хроническое течение по типу оппортунистической инфекции. Для ВПГ 6 го типа характерны острые состояния по клинической картине, напоминающие инфекционный мононуклеоз.
При хроническом течении данные заболевания полностью подчиняются «правилам» оппортунистических инфекций: «айсберговый» тип, активизация при любом другом инфицировании. Характерно поражение лимфоузлов: при активизации ВЭБ или ВПГ 6-го типа развиваются лимфаденопатии той или иной степени тяжести (вплоть до гнойных лимфаденитов). ОРЗ осложняются увеличением лимфоузлов, в редких случаях рецидив инфекционного мононуклеоза; активизация ВПГ 1 го, 2 го типов приводит к появлению типичных везикулярных высыпаний на коже или слизистых.
Диагностика. Исследование крови на антитела (ИФА), диагностически значимым критерием является повышение уровня IgG; возможно также выявление методом ПЦР со слизистых зева.
Лечебная тактика. При выявленном носительстве ВЭБ в период протекания ОРЗ нужно проводить противовирусную терапию (Арбидол, Виферон, Изопринозин) в сочетании с иммунокоррекцией; лечебные мероприятия наиболее эффективны в период обострения.
- Хронические инфекционные заболевания вызывают разнообразные синдромы: нарушение функции пораженной системы, ослабление иммунной системы, сенсибилизацию организма (аллергические болезни), хроническую интоксикацию, нарушения обмена веществ. По этим признакам можно заподозрить хроническую инфекцию и рекомендовать обследование, направленное на ее выявление.
- Ведущим методом диагностики хронических и оппортунистических инфекций является выявление в крови антител класса G выше диагностического титра.
- Для хронических инфекций характерен «айсберговый» тип носительства: небольшое количество активных форм и значительно большее – «спящих», неактивных и неуязвимых для этиотропной терапии.
- Активизация хронических инфекций сопровождается нарастанием клинической картины, появлением новых симптомов дополнительно к симптомам острого заболевания. Активизировать очаг хронической инфекции может любой инфекционный агент, попавший в организм, а также любые факторы, ослабляющие функцию иммунной системы.
- Во время активизации хронические инфекции максимально уязвимы, а этиотропное лечение максимально эффективно. И наоборот, применение этиотропной терапии в неактивный период не дает эффекта.
источник

Некоторые микроорганизмы относятся к условно-патогенным представителям микрофлоры человека. Это означает, что они в небольшом количестве постоянно обитают на слизистых оболочках или коже, но развитие инфекционного заболевания не вызывают, так как иммунная система постоянно их подавляет. Оппортунистические инфекции являются результатом недостаточной активности клеточного (Т-лимфоциты, макрофаги) и гуморального (антитела, интерлейкины) звена иммунной системы (иммунодефицит). Существует несколько основных причин развития иммунодефицита:
- Врожденная (генетическая) функциональная недостаточность иммунитета, связанная с наличием дефектного гена, который отвечает за продукцию антител секреторных иммуноглобулинов ( IgA ) или количество и качество клеток. При этом оппортунистические инфекции развиваются уже в раннем детском возрасте.
- Длительное применение химиотерапии во время лечения онкологического процесса (рак различной локализации, лейкоз) – цитостатики, которые подавляют деление опухолевых клеток, заодно угнетают и иммунную систему.
- Опухолевые заболевания красного костного мозга и лимфоидной ткани, отвечающих за формирование клеток
иммунитета – при этом количество иммунокомпетентных клеток остается таким же или увеличивается, но они практически все являются функционально дефектными.
- Применение иммуносупрессоров – лекарственные средства, которые подавляют иммунитет, их длительное время используют в ситуациях, когда необходимо искусственно снизить иммунитет (аутоиммунные заболевания, ревматизм, ревматоидный артрит, после пересадки органа для предотвращения его иммунного отторжения).
- Длительное лечение антибиотиками (больше месяца), которые вначале приводят к дисбактериозу (нарушение нормальной микрофлоры с преобладанием условно-патогенных микроорганизмов), затем – к непосредственному подавлению активности иммунитета.
- Инфекции иммунной системы – ВИЧ, вирусные гепатиты (особенно вирусный гепатит С), вирус Эпштейна-Барр паразитируют в лимфоцитах, что приводит к снижению их численности и функциональной активности. Иммунитет наибольше повреждается при паразитировании ВИЧ, который приводит к развитию СПИДа (синдром приобретенного иммунодефицита).
В случае комбинированного наличия нескольких причинных факторов, развитие иммунодефицита более выражено, а это в свою очередь приводит к более быстрому и тяжелому течению оппортунистических инфекций.
Оппортунистические инфекции часто вызываются различными микроорганизмами, которые обитают в окружающей среде, человека с ними постоянно контактирует, но функционально активная иммунная система сразу же подавляет их размножение в организме.
Инфекционные заболевания при снижении активности иммунитета могут быть различными, они вызываются представителями патогенной и условно-патогенной флоры только в условиях иммунодефицита и практически никогда не бывают у людей с нормальным иммунитетом. К таким инфекциям относятся:
- Пневмония – воспаление легких вызванное различными неспецифическими бактериями (стафилококки, стрептококки, кишечная палочка). Чаще развивается у курящих людей на фоне интоксикации, оседания вредных веществ в слизистой легких, что усугубляет дефицит иммунитета.
- Пневмоцистная пневмония – вызвана специфическим грибком Pneumocystis carinii. Он обитает в окружающей среде (практически повсюду) и в легких. Эта пневмония на фоне иммунодефицита характеризуется тяжелым течением с частыми летальными исходами.
- Вирус папилломы человека (ВПЧ) – большинство людей заражены этим вирусом, но он находится в ядре клеток в «дремлющем» неактивном состоянии. При снижении иммунитета на коже и слизистых появляются папилломы
или остроконечные кондиломы, количество и размер которых по мере прогрессирования процесса увеличиваются.
- Гистоплазмоз – инфекция, вызванная грибком, который находится в большом количестве в почве. В организм человека он попадает с вдыхаемым воздухом в легкие, где при снижении иммунитета вызывает воспаление. Затем он может распространяться по всему организму с образованием очагов вторичной инфекции.
- Бактериальный процесс, вызванный специфическими микобактериями Mycobacterium avium и Mycobacterium intracellulare, которые обитают в окружающей среде и у человека с нормальным иммунным статусом не вызывают патологического процесса. У лиц с иммунодефицитом эти бактерии могут вызвать очаговый инфекционный процесс в различных органах.
- Криптококковый менингит – поражаются оболочки головного и спинного мозга специфическим грибком, который обитает в почве и попадает в организм с вдыхаемым воздухом.
- Опоясывающий лишай – вирусная инфекция, вызванная герпетическим вирусом Varicella zoster , присутствует в организме большинства людей, но при снижении иммунитета активируется и приводит к появлению сыпи на коже и поражению нервов с развитием интенсивной боли в области их иннервации.
- Простой герпес – вирус также у большинства людей находится в организме в неактивном состоянии, при иммунодефиците часто поражает слизистые оболочки с появлением небольших пузырьков, заполненных жидкостью.
- Криптоспоридиоз – хроническая кишечная инфекция, которая вызывает развитие хронической диареи (понос), эта инфекция часто развивается при СПИДе.
- Кандидоз – процесс, вызванный дрожжеподобными грибками рода Candida , которые обитают в небольшом количестве на слизистых и коже. У женщин часто приводит к развитию молочницы влагалища. Также кандидоз часто развивается в слизистой рта, дыхательных путей, на коже.
- Токсоплазмомз – заболевание, вызванное простейшими токсоплазмами. В организм человека они попадают из
окружающей среды от кошек (выделяются с калом) и при употреблении полусырого мяса. При выраженном иммунодефиците эти микроорганизмы приводят к поражению головного мозга (токсоплазмоз). Активный инфекционный процесс у беременных является причиной выкидыша или тяжелых пороков развития плода.
- Цитомегаловирусная инфекция (ЦМВ) – при иммунодефиците приводит к поражению различных органов, в частности может спровоцировать слепоту на фоне воспаления сетчатки (ретинит), поражение кишечника и нервной системы.
- Туберкулез – тяжелая бактериальная инфекция, вызванная специфическими палочками туберкулеза. Чаще всего поражает легкие, с постепенным разрушением их тканей и формированием каверн (полости или «дырки» в легких).
При значительном снижении иммунитета, может развиваться сразу несколько видов оппортунистической инфекции. Очень тяжело протекают оппортунистические инфекции при ВИЧ СПИД. Лечение этих заболеваний направлено на уничтожение возбудителей с помощью антибиотиков, противовирусных средств или противогрибковых препаратов. Препарат, его дозировка и курс лечения определяются индивидуально, в зависимости от возбудителя и тяжести течения патологического инфекционного процесса. Профилактика СПИДа и развития таких инфекций, заключается в недопущении попадания вируса в организм, так как в случае инфицирования, процесс остановить уже невозможно, развивается иммунодефицит и оппортунистические инфекции, которые и приводят к летальному исходу.
источник
Оппортунистические инфекции и условно-патогенные микроорганизмы – понятие, причины возникновения, способы передачи. Основные особенности и проявления инфекции, методы исследований. Правила забора и транспортировки материала, порядок осуществления бактериологического анализа. Методы лечения и меры профилактики оппортунистических инфекций
Оппортунистические инфекции и условно-патогенные микроорганизмы – понятие, причины возникновения, способы передачи, основные особенности и проявления инфекции, методы исследований, правила забора и транспортировки материала, порядок осуществления бактериологического анализа, методы лечения и меры профилактики оппортунистических инфекций.
Данные инфекции провоцируются условно-патогенными микроорганизмами (УПМ) – бактериями, грибами, простейшими. По своей природе к УПМ близки также некоторые виды вирусов (вирус герпеса 1 и 2 типа, полиомавирусы, вирусы папилломы человека, аденовирусы, вирус Коксаки и др.).
Существует две формы отношений УПМ с организмом человека:
- симбиоз (нейтрализм, комменсализм);
- конкуренция.
В ходе медицинских исследований и экспериментов выявлено, изучено и описано более 100 видов условно-патогенных микроорганизмов, способных спровоцировать инфекцию. Особая роль среди них принадлежит:
- Staphylococcus;
- Streptococcus;
- Escherichia;
- Enterobacter;
- Klebsiella;
- Haemophilus;
- Vibrio;
- Propioni- bacterium;
- Mycobacterium;
- Mycoplasma;
- Candida;
- Pneumocysta.
Среди условно-патогенных микроорганизмов встречаются разновидности, свободно существующие в различных биоорганических средах – воде, почве, воздухе, пищевых продуктах, органических отходах, растворах медикаментов. Большинство их них – так называемые сапронозы, свободно обитающие в организме человека и при соответствующих условиях провоцирующие у него развитие болезни, однако живая среда не является обязательным условием для сохранения их популяции. Представители этой группы – протей, клебсиелла, псевдомонада, ацинетобактерия и др. Сюда же относятся микроорганизмы, паразитирующие в организмах животных и птиц (сальмонелла).
Большая часть УПМ в норме живет в человеческом организме и состоит с ним в симбиотических отношениях. Условно-патогенная флора конкурирует с ним лишь при ряде условий и факторов, однако это не дает УПМ никаких биологических преимуществ и зачастую приводит к утрате хозяина.
В отличие от болезнетворных микроорганизмов, которые попадают в организм через четко обозначенные входные ворота, условно-патогенные микроорганизмы (УПМ) могут провоцировать инфекцию при попадании любым путем в любые органы и ткани. Для развития оппортунистической инфекции достаточно пассивного заноса возбудителя во внутреннюю среду организма и недостатка элиминирующих элементов иммунной системы.
Условно-патогенная флора, размножаясь, выделяет в организм эндотоксины и ферменты агрессии, негативно воздействующие на организм. Отрицательный эффект этих веществ связан не только с разрушением структуры клетки, но и с токсическим воздействием продуктов ферментного распада – аминов, сероводорода, мочевины и др.
Источником таких инфекций выступает заболевший человек или носитель. Наиболее опасны в эпидемиологическом отношении работники медицинских учреждений, так как они могут быть носителями внутрибольничных штаммов УПМ (синегнойной палочки и др.). Оппортунистические инфекции также могут передаваться зоонозным путем, то есть от больного животного к человеку. Также в ряде случаев источниками инфекции выступают объекты больничной среды, обильно обсемененные микроорганизмами.
Таким образом, можно выделить три пути распространения оппортунистических инфекций:
- антропонозный (от человека к человеку);
- зоонозный (от животного к человеку);
- сапронозный (от абиотических (неживых) объектов окружающей среды к человеку).
Поскольку условно-патогенным микроорганизмам свойственна крайне низкая степень вирулентности, восприимчивость к ним очень низка у людей с нормальным иммунитетом. Высока степень восприимчивости к УПМ у лица с различными иммунодефицитными состояниями.

Патологические процессы, обусловленные условно-патогенными микроорганизмами – частое явление при онкологических заболеваниях, вирусе иммунодефицита человека, хронических воспалительных процессах, после серьезного оперативного вмешательства, а также при приеме гормональных, цитотоксических и цитостатических средств, антибиотиков. Подвержены риску люди преклонного возраста, младенцы с недостатком массы тела, лица с патологиями сердечно-сосудистой системы, нарушениями обмена веществ и некоторыми другими заболеваниями.
Данные инфекции способны вызывать практически все виды условно-патогенных микроорганизмов. Клинически это гнойно-воспалительные процессы различной локализации и степени тяжести. Они обладают целым рядом специфических особенностей, в числе которых:
- отсутствие строго определенного органного тропизма – один и тот же вид УПМ может вызывать самые разные нозологические формы (бронхит, пневмония, эмпиема, отит, синусит, менингит, остеомиелит, конъюнктивит, инфекция послеоперационной или ожоговой раны и др.);
- один и тот же инфекционный воспалительный процесс может быть спровоцирован любым УПМ;
- клинические проявления напрямую связаны с характером и функцией пораженного органа – например, пиелонефрит, спровоцированный клебсиеллой, псевдомонадой, кишечной палочкой или стафилококком, существенно не различается по своей картине, однако процесс лечения должен осуществляться с учетом свойств конкретного возбудителя и его чувствительности к тому или иному препарату.
- оппортунистические инфекции часто протекают по смешанному типу, то есть провоцируются не одним, а несколькими УПМ;
- склонность переходу в хроническую форму, генерализации и развитию тяжелых септических осложнений;
- сложность лечения, связанная с распространением антибиотико-резистентных штаммов, а также с изменчивостью и гетерогенностью популяций микробов, низкой активностью факторов естественной резистентности и недостаточной способностью организма к формированию эффективного иммунного ответа на антигены УПМ.
- множественность источников инфекции;
- широкое распространение в условиях лечебных и лечебно-профилактических учреждений, обсемененность объектов внешней среды микробами, их способность размножаться и распространяться в больничных условиях.
- избирательность поражения населения (группа риска – люди с выраженным дефицитом иммунитета);
- большое количество путей, факторов и механизмов передачи возбудителя.
Постановка этиологического диагноза заболевания – непростая задача, поэтому важнейшее значение в диагностике инфекций, вызываемых УПМ, имеют лабораторные микробиологические методы исследований.
Методы лабораторной диагностики оппортунистических инфекций крайне важны в процессе точной постановки диагноза инфекций, спровоцированных УПМ, а также при выработке адекватной схемы лечения и профилактике рецидивов заболевания. Специфическая особенность микробиологических исследований при оппортунистических инфекциях – они направлены на выявление не одного, а нескольких микроорганизмов в исследуемом образце.
Является основным методом микробиологической диагностики оппортунистических инфекций. Его использование связано с учетом некоторых нюансов:
- исследуемый материал, как правило, содержит ассоциацию микроорганизмов, в которую входят как непосредственные возбудители заболевания, так и микробы, занесенные из других органов и из внешней среды, а также попавшие в процессе забора и транспортировки образца;
- количество и видовой состав микрофлоры может быть различным у разных пациентов и меняется с течением болезни, особенно при использовании антибиотиков.
Точность и достоверность бактериологического метода зависит не только от правильности забора материала, но и от использования эффективного набора дифференциально-диагностических и селективных питательных сред, использования количественного посева материала, поэтапного определения выделенных культур (семейство, род, вид, в ряде случаев вариант) и выявления свойств, указывающих на патогенность и принадлежность культуры к госпитальным штаммам.

- вид материала зависит от клиники заболевания и должен соответствовать локализации потенциального возбудителя с учетом патогенеза инфекционного процесса;
- количества материала должно быть достаточным для проведения исследования и его повторения в случае необходимости;
- лучшее время для забора материала – начало болезни;
- забор материала должен осуществляться до начала приема антимикробных препаратов или через какое-то время после назначения терапии – это нужно, чтобы антибиотик вывелся из организма;
- материал берется непосредственно из очага инфекции или же исследуется соответствующее отделяемое (гной, желчь, моча и т.д.);
- необходимо избегать контакта материала с нормальной микрофлорой пациента и бактериями из окружающей среды;
- необходимо обеспечить невозможность попадания в исследуемый образец антисептических, антимикробных средств и дезинфектантов, а также исключить контакт с металлами с олигодинамическими свойствами и с ватой, содержащей жирные кислоты.
Следует помнить, что клинический материал при оппортунистических инфекциях представляет определенную опасность для человека, поэтому при его заборе, транспортировке и обработке должны соблюдаться те же меры предосторожности, что и при работе с болезнетворными микроорганизмами.
Правила транспортировка образца:
- доставка материала в лабораторию должна производиться в самые короткие сроки;
- во время транспортировки материал следует защищать от действия холода, тепла, прямых солнечных лучей и механических повреждений;
- после проведения всех необходимых исследований образцы материала подлежат уничтожению, а емкости, в которых они перевозились – дезинфекции.
К клиническому образцу, направляемому на исследование в лабораторию, прилагается сопроводительный лист, в котором отражена важная информация, необходимая для проведения микробиологического анализа – характер образца, дата и время взятия, Ф.И.О. пациента, наименование учреждения или отделения, номер истории болезни, предварительный диагноз, назначенная терапия, подпись врача.
- забор и доставка материала в лабораторию;
- обработка образца с целью концентрации и гомогенизации;
- окрашивание мазков по Граму, использование дополнительные методы окрашивания бактерий (при необходимости);
- разведение материала от 10-1 до 10-6 в теплом 0,5% растворе NaCl с 0,01% желатина, высев 0,1 мл подготовленного материала на чашки Петри с питательной средой (на 3 чашки из каждого разведения).
Наиболее часто используемый набор питательных сред:
- для стафилококков – желточно-солевой агар;
- для энтеробактерий – среда Эндо или эозинметиловый агар;
- для стрептококков – кровяной агар;
- для грибов – среда Сабуро.
Помимо этого, используются среды для контроля стерильности и специальные среды для анаэробных микроорганизмов. Если имеются указания на возможный возбудитель заболевания, должны использоваться более селективные среды.
- определение характера роста на питательных средах;
- подсчет количества колоний каждого типа на чашках с посевом разведений исследуемого материала по формуле Х КОЕ = N * ПД *СР, где N — число колоний, ПД — посевная доза, СР — степень разведения;
- изучение мазков из выросших колоний под микроскопом;
- отсев на среды накоплений колоний различных типов (эта мера сильно повышает достоверность анализа).
- проверка чистоты культуры, идентификация чистых культур;
- исследование выделенных культур на чувствительность к антимикробным препаратам.
- учет результатов тестов, использованных для идентификации;
- оформление заключения (семейство, род, вид обнаруженных культур, обсемененность образца, антибиотикограмма, этиологическая значимость и состав популяций выделенных микроорганизмов, факторы патогенности и др.)
Этиологическая значимость УПМ базируется на двух критериях:
- выделение условно-патогенных микроорганизмов из ликвора или крови пациента;
- критическое число – численность популяции в пораженном органе (рассчитывается на 1 мл исследуемого материала и составляет 105 КОЕ/мл для бактерий, 103-104 – для простейших и грибов).
Если из исследуемого образца выделено несколько видов УПМ, возбудителем заболевания считается доминирующая популяция. Нельзя не учесть также то, что в ходе терапии численность популяции может меняться и снижается при выздоровлении, выходе в ремиссию, при переходе процесса в хроническую форму, при проведении химиотерапии, в присутствии бактерии-конкурента и при некоторых других условиях.
Терапия инфекций, спровоцированных УПМ – сложная задача, требующая комплексного подхода. Лечение включает в себя хирургическое вмешательство, антибиотикотерапию, поддерживающую иммунотерапию.
При оппортунистических инфекциях часто возникают гнойные очаги, требующие вскрытия и санации. Антимикробные средства назначаются только после проведения антибиотикограммы, поскольку многие условно-патогенные микроорганизмы устойчивы к воздействию данных препаратов. Чаще всего предпочтение отдается лекарствам широкого спектра действия.
Помимо назначения антибиотиков лечение оппортунистических инфекций включает в себя иммунотерапию, для которой используются иммунобиологические препараты направленного действия. Поскольку инфекции, вызванные УПМ, развиваются у пациентов со сниженным иммунитетом, им показано проведение иммунокоррекции с использованием препаратов-иммуномодуляторов.
Предупреждение оппортунистических инфекций должно быть направлено на выявление источника заражения, а также на разрыв путей, факторов и механизмов передачи и воздействие на восприимчивый коллектив.
Оппортунистические инфекции зачастую связаны с носителями из числа работников медицинских учреждений, которые нуждаются в выявлении и санации. Для этого необходим ежедневный осмотр медицинского персонала (в особенности – акушерско-гинекологических и хирургических стационаров, родильных домов и детских больниц) на предмет наличия различных гнойно-воспалительных процессов (гнойничковые поражения кожи, катаральные явления в носоглотке и т.д.), а также периодическое исследование медперсонала на носительство. Носителей временно отстраняют от работы и подвергают санации.
В больничных учреждениях необходимо строжайшее соблюдение санитарно-гигиенических норм, правил асептики, антисептики, дезинфекции и стерилизации.
Мероприятия, направленные на выявление возбудителя оппортунистической инфекции, предусматривают выявление и лечение больных. В условиях хирургического стационара чистые и гнойные больные не должны контактировать друг с другом. Для этого в большинстве лечебных учреждений созданы чистые и гнойные хирургические отделения и операционные. Если операционная только одна, то сначала оперируются плановые пациенты из чистого отделения и только после этого – из гнойного отделения. Операционная тщательно дезинфицируется после каждой операции.
источник
ВИЧ-инфекция – инфекционное заболевание, вызываемое вирусом иммунодефицита человека, характеризующееся многолетним течением, клинически связанным с прогрессирующим снижением иммунитета, приводящим на последней стадии заболевания к синдрому приобретенного иммунодефицита (СПИД), для которого характерно развитие тяжелых форм оппортунистических заболеваний.
Диагностика ВИЧ-инфекции включает два этапа: установление собственно факта инфицирования ВИЧ и клиническая диагностика. Установление факта инфицирования осуществляется путем комплексной оценки эпидемиологических данных, результатов клинического обследования и лабораторных исследований. Клиническая диагностика ВИЧ-инфекции проводится после того, как факт инфицирования установлен. Традиционно клиническая диагностика сводится к установлению стадии заболевания и характеристике его течения. За определением стадии неразрывно следует прогнозирование течения заболевания, а также выбор тактики лечения.
Как во время острой стадии, так и на стадии СПИДа, клинические проявления ВИЧ-инфекции неспецифичны и не позволяют однозначно поставить диагноз. Лабораторная диагностика ВИЧ-инфекции включает исследования для постановки диагноза ВИЧ-инфекции, мониторинга течения заболевания и эффективности терапии.
Человек, однажды инфицированный ВИЧ, остается его носителем до конца жизни. В течение многих лет после инфицирования самочувствие зараженных ВИЧ людей остается обычным, очевидных клинических проявлений инфицирования нет и присутствие ВИЧ в организме зараженного человека можно обнаружить только при проведении диагностического лабораторного исследования. В то же время, несмотря на отсутствие заметных симптомов, ВИЧ-инфекция вызывает в организме человека активный патологический процесс, который постепенно истощает защитные механизмы организма человека. По прошествии многих лет у подавляющего большинства инфицированных людей наблюдается клинически выраженное ослабление иммунной системы организма, и, по устоявшейся терминологии, развивается «СПИД» – синдром приобретенного иммунодефицита. Этот синдром проявляется в развитии угрожающих для жизни больного инфекционных заболеваний, чаще всего вызванных малоопасными для здоровых людей условнопатогенными микроорганизмами, или появлением онкологических заболеваний (эти нозологические формы определяют как «оппортунистические заболевания»). Больной с диагнозом СПИДа при отсутствии специального лечения, направленного на подавление репликации ВИЧ, умирает от оппортунистических заболеваний в среднем в течение одного года. Оппортунистические и вторичные инфекции выступают основной причиной летальных исходов у больных на поздних стадиях ВИЧ-инфекции.
Оппортунистические инфекции могут иметь протозойную, грибковую, бактериальную и вирусную природу. Среди простейших на первое место по значению среди «оппортунистов» может быть отнесена токсоплазма: церебральный токсоплазмоз является главной причиной поражения ЦНС при ВИЧ-инфекции.
Среди грибов лидирующее место сохраняют пневмоцисты, поскольку пневмоцистная пневмония остается самым характерным серьезным проявлением ВИЧ-инфекции по своей частоте и летальности, а также самым частым оппортунистическим поражением легких на поздних стадиях болезни. Повсеместно распространены грибы рода Candida, которые у больных ВИЧ-инфекцией могут вызвать тяжелое поражение любого органа. К наиболее важным «оппортунистам» относятся также широко распространенные Cryptococcus neoformans. В последние годы все большее значение в качестве оппортунистических возбудителей приобретают аспергиллы. Поражения, вызванные ими, чаще обнаруживают при аутопсии, однако описаны и тяжелые клинически выраженные варианты поражения внутренних органов. К эндемичным оппортунистическим микозам относят гистоплазмоз, бластомикоз и паракокцидиоидомикоз, а также зигомикоз (мукормикоз), которые могут вызывать тяжелые поражения внутренних органов или генерализацию процесса с высокой летальностью. Эндемичные микозы связаны с определенной географической зоной, однако некоторые из них уже описаны среди больных ВИЧинфекцией в странах Восточной Европы как завозные случаи, и нельзя исключить возможность их завоза в Россию.
Оппортунистические паразитозы и микозы становятся все более распространенными; появляются новые для человека паразитозы (микроспоридиоз); в качестве оппортунистических агентов более часто выявляют патогенных возбудителей (токсоплазмы, аспергиллы, криптококки); ряд этих возбудителей может передаваться при оказании медицинской помощи: например, пневмоцисты (распространение которых и раньше было актуальным в проблеме внутрибольничных инфекций), а также токсоплазмы и висцеральный лейшманиоз, которые могут передаваться при переливании крови, трансплантации костного мозга и других органов. Кроме этого, токсоплазмоз и лейшманиоз, а также стронгилоидоз приводят к тяжелому поражению клеточного иммунитета, в основном к снижению уровня CD4+ Т-лимфоцитов; таким образом, при этих заболеваниях на фоне ВИЧ-инфекции происходит еще большее усугубление иммунодефицита, что способствует массивной диссеминации возбудителей в организме больного с развитием тяжелого течения заболевания.
Из бактериальных инфекций наибольшее значение в настоящее время имеет туберкулез, который на поздних стадиях ВИЧ-инфекции приобретает все черты тяжелого вторичного заболевания. Туберкулез — основная причина смерти больных ВИЧ-инфекцией: на поздних стадиях ВИЧ-инфекции от туберкулеза умирает более 50% больных. Причиной бактериальных пневмоний чаще всего бывает Streptococcus pneumoniae, реже регистрируют пневмонии, вызванные стафилококками, гемофильной палочкой, клебсиеллами. Увеличивается число больных с атипичным микобактериозом. Чаще стал диагностироваться бациллярный ангиоматоз как проявление бартонеллезной инфекции.
По частоте и значимости среди оппортунистических вирусных инфекций лидирует ЦМВИ. Развиваясь на поздних стадиях ВИЧ-инфекции, цитомегаловирусные поражения периферической и центральной нервной системы, ЖКТ, легких, глаз занимают одно из первых мест среди причин смерти больных. Часто регистрируют поражения, вызванные вирусами простого герпеса 1 и 2 типов, вирусом Varicella zoster, однако среди причин летальных исходов они пока фигурируют редко. Саркома Капоши регистрируется все реже благодаря внедрению в клиническую практику высокоактивной АРВТ. Среди опухолей актуальны различные лимфомы (ходжкинского и неходжкинского типов).
Сроки развития различных оппортунистических заболеваний тесно связаны с глубиной иммунодефицита: большинству из них присуща своя «очередность». Наиболее ранний клинический показатель прогрессирующего иммунодефицита — кандидоз слизистых оболочек. За ним следуют бактериальные пневмонии, туберкулез легких, герпетические поражения, волосатая лейкоплакия, интраэпителиальная неоплазия шейки матки, рак шейки матки. При более глубоком поражении иммунной системы (число CD4-клеток ниже 0,2.109/л) развиваются локализованная саркома Капоши, лимфомы, пневмоцистная пневмония, тяжелые грибковые инфекции (от кандидозного эзофагита до поражения внутренних органов и грибкового сепсиса), внелегочный и генерализованный туберкулез, диссеминированная и хроническая герпетическая инфекция, прогрессирующая многоочаговая лейкоэнцефалопатия. Затем, как правило, при снижении количества CD4-клеток ниже 0,1-0,05.109/л развиваются распространенная/генерализованная саркома Капоши, криптококковый менингит, токсоплазмозный энцефалит, манифестные формы цитомегаловирусной инфекции, атипичные микобактериозы, хронический криптоспоридиоз, микроспоридиоз. Этот уровень снижения иммунитета сопутствует нарастанию истощения, развитию периферической нейропатии, деменции, лимфомы центральной нервной системы, кардиомиопатии, вакуолярной миопатии, прогрессирующего полирадикулоневрита, иммунобластной лимфомы. Кроме того, у 40–60% пациентов различные оппортунистические заболевания проявляются как микст-инфекция, что утяжеляет их течение, затрудняет диагностику и лечение. Некоторые оппортунистические возбудители становятся резистентными к применяемому лечению.
В РФ в последние годы отмечается значительный рост числа больных ВИЧинфекцией, выявляемых на поздних стадиях болезни. Диагноз ВИЧ-инфекции у них устанавливают обычно при госпитализации: эти пациенты доживают до тяжелых проявлений вторичных (оппортунистических) заболеваний, не зная о своем ВИЧ-статусе. Лечение таких больных представляет большие трудности из-за поздней диагностики ВИЧ-инфекции и вторичных поражений, тяжелого характера их течения и частого сочетания нескольких заболеваний на фоне низких параметров иммунитета. В настоящее время основными причинами смерти больных на поздних стадиях ВИЧ-инфекции в России являются туберкулез (66,5%), кандидоз пищевода и внутренних органов (12,0%), манифестная цитомегаловирусная инфекция (3,0%), пневмоцистная пневмония (1,9%), церебральный токсоплазмоз (1,5%), лимфопролиферативные заболевания (0,7%). Значительную часть составляют нерасшифрованные вторичные заболевания (22,4%) и «изнуряющий синдром» (6,8%). Это свидетельствует о трудности клинической диагностики и лабораторного подтверждения различных вторичных поражений у больных ВИЧ-инфекцией, что связано с наличием выраженного иммунодефицита.
Особенности развития и проявления оппортунистических поражений у больных ВИЧ-инфекций определяют требования к применению тестов лабораторной диагностики. Самый распространенный способ диагностики инфекционных болезней – определение специфических АТ (серологическая диагностика) не эффективен при наличии выраженного иммунодефицита. Выявление ДНК/РНК микроорганизма без определения концентрации может свидетельствовать о носительстве и не является однозначным подтверждением активной инфекции. Одна из задач лабораторной диагностики оппортунистических инфекций – разработка методов ПЦР для определения концентрации ДНК/РНК микроорганизма и установление диагностически значимого уровня для выявления манифестной инфекции.
Продолжая использовать наш сайт, вы даете согласие на обработку файлов cookie, пользовательских данных (сведения о местоположении; тип и версия ОС; тип и версия Браузера; тип устройства и разрешение его экрана; источник откуда пришел на сайт пользователь; с какого сайта или по какой рекламе; язык ОС и Браузера; какие страницы открывает и на какие кнопки нажимает пользователь; ip-адрес) в целях функционирования сайта, проведения ретаргетинга и проведения статистических исследований и обзоров. Если вы не хотите, чтобы ваши данные обрабатывались, покиньте сайт.
источник
 иммунитета – при этом количество иммунокомпетентных клеток остается таким же или увеличивается, но они практически все являются функционально дефектными.
иммунитета – при этом количество иммунокомпетентных клеток остается таким же или увеличивается, но они практически все являются функционально дефектными. или остроконечные кондиломы, количество и размер которых по мере прогрессирования процесса увеличиваются.
или остроконечные кондиломы, количество и размер которых по мере прогрессирования процесса увеличиваются. окружающей среды от кошек (выделяются с калом) и при употреблении полусырого мяса. При выраженном иммунодефиците эти микроорганизмы приводят к поражению головного мозга (токсоплазмоз). Активный инфекционный процесс у беременных является причиной выкидыша или тяжелых пороков развития плода.
окружающей среды от кошек (выделяются с калом) и при употреблении полусырого мяса. При выраженном иммунодефиците эти микроорганизмы приводят к поражению головного мозга (токсоплазмоз). Активный инфекционный процесс у беременных является причиной выкидыша или тяжелых пороков развития плода.