Клинико-лабораторная характеристика персистирующих инфекций хламидийной и микоплазменной этиологии у детей
В начале ХХ века ведущая роль принадлежала инфекциям бактериальной природы (скарлатина, дифтерия, коклюш, дизентерия). В структуре заболеваемости у детей преобладают острые инфекции верхних дыхательных путей различной этиологии.
В начале ХХ века ведущая роль принадлежала инфекциям бактериальной природы (скарлатина, дифтерия, коклюш, дизентерия). В структуре заболеваемости у детей преобладают острые инфекции верхних дыхательных путей различной этиологии. Латентные и персистирующие формы инфекций у детей остаются малоизученными. Актуальность изучения перинатальных инфекций обусловлена широкой циркуляцией возбудителей в популяции и высокой частотой передачи их ребенку от матери (В. А. Исаков с соавт., 2006). Наряду с острым течением инфекции, у ребенка может наблюдаться длительная персистенция возбудителя с формированием медленно текущего хронического инфекционного процесса. Атипичность клинических проявлений при внутриутробном заражении плода, трудность лабораторного диагноза и низкий уровень информированности врачей приводят к поздней диагностике внутриутробных инфекций у детей.
Персистирующие и латентные инфекции довольно широко распространены, однако до сих пор их последствия для будущего здоровья детей педиатрами явно недооцениваются. Чаще всего у детей они развиваются при инфицировании внутриклеточными возбудителями (хламидии, микоплазмы). Из инфекций, способных дать персистенцию на длительный срок жизни ребенка, все чаще выявляются вирусы семейства герпес. Персистирующими инфекциями именуют такие формы заболеваний, при которых после перенесенной инфекции не наступает очищения от инфекционного патогена, нередко возбудители инфекции длительно пребывают в латентном («дремлющем») состоянии либо при неблагоприятном состоянии макроорганизма способны реактивироваться с появлением новых клинических доминант.
Хламидийная инфекция. Хламидии вызывают значительно большее число болезней, чем считалось ранее. Доказана роль отдельных представителей семейства хламидий в репродуктивном здоровье женщин и формировании патологии плода и новорожденного. Заражение хламидиями возможно различными путями, в том числе воздушно-капельным, контактным, анте- и интранатальным. Восприимчивость к хламидиям всеобщая. Перенесенная инфекция не обеспечивает пожизненного иммунитета. Основной особенностью хламидий является внутриклеточный паразитизм. Хламидии обладают тропизмом к эпителиальным клеткам конъюнктивы глаз, легких и мочеполовой системы.
При нормальном противоинфекционном иммунитете большинство хламидий уничтожаются фагоцитами хозяина. Однако внутриклеточные патогены обладают способностью блокировать механизмы иммунной защиты, вследствие чего клетки хозяина не только не уничтожают хламидии, но и способствуют их росту и размножению. У матери хламидии колонизируют различные органы плода: конъюнктивы, носоглотку, среднее ухо, дыхательные пути, кишечник, вызывая их поражение. Наиболее тяжелые формы поражения хламидиями связаны с восходящим инфицированием плода. Возможность гематогенного инфицирования хламидиями подтверждается обнаружением во внутрибрюшинных отделах пупочных сосудов лимфогистиоцитарных перифлебитов, реже — периартериитов. При генерализованном инфицировании развиваются комплексные патологические изменения в виде отечно-геморрагического синдрома, синдрома дыхательных расстройств, кровоизлияний в желудочки мозга. Пневмонии хламидийной этиологии у новорожденных детей характеризуются интерстиционально-десквамативным процессом.
Клинически хламидийная инфекция у новорожденных проявляется в виде конъюнктивита, назофарингита, бронхита, пневмонии, гастроэнтерита, проктита, вульвита, уретрита, менингита, миокардита, реактивного артрита. Хламидиоз новорожденных может протекать в острой и хронической форме, возможна персистенция возбудителя. У детей старшего возраста инфицированность хламидиями с высокой частотой выявляется при хронических заболеваниях носоглотки и придаточных пазух носа. У детей с ЛОР-патологией из организованных коллективов хламидийная инфекция выявлялась у 21% пациентов, у больных, находящихся на стационарном лечении в ЛОР-отделении, хламидийная инфекция обнаруживалась в два раза чаще (Т. А. Капустина с соавт., 2007). В последнее время отмечают высокую частоту респираторного хламидиоза у больных бронхиальной астмой (25,9%), особенно при ее тяжелом течении. У детей с рецидивирующими и хроническими бронхитами респираторная хламидийная инфекция обнаруживается чаще, чем при бронхиальной астме, — 35% (Т. В. Спивак, Л. К. Катосова, 2009).
Диагностика. Для лабораторной диагностики у новорожденных используют отделяемые, смывы, мазки-отпечатки, соскобы с участков слизистой оболочки.
Цитологический метод заключается в обнаружении цитоплазматических включений хламидий в эпителиальных клетках препаратов, окрашенных по методу Романовского–Гимзы. Иммунофлюоресцентный метод — окрашивание хламидийных антигенов иммунофлюоресцентными красителями на основе моноклональных антител. Иммунофлюоресцентный метод позволяет выявлять возбудителя в конъюнктивальных, урогенитальных, ректальных и назофаренгеальных образцах.
Иммуноферментный анализ (ИФА): материалом для ИФА является кровь пациента, в которой определяются специфические антитела класса IgG, IgM. При подозрении на хламидийную инфекцию — диагностическое значение имеет обнаружение у ребенка антител класса IgM в титре выше 1:8, а также IgG-антител в титрах выше, чем у его матери (обычно выше 1:64), что свидетельствует об активной инфекции. Лабораторная диагностика базируется на выявлении антител класса IgM, тогда как IgG-антитела свидетельствуют о прошлой инфекции, а при высоких титрах IgA-антител — о реинфекции (А. А. Баранов, 2007). Метод полимеразной цепной реакции (ПЦР) основан на ферментативном размножении специфического участка ДНК (амплификации), носящего экспоненциальный характер за счет многократного повторения циклов ДНК-полимеразной реакции и температурной денатурации двухцепочечных фрагментов ДНК. Выделение ДНК хламидий у новорожденных проводится из крови, мочи и трахеобронхиальных аспиратов. Для повышения достоверности диагностики принято использовать не менее двух методов исследования.
Лечение хламидийной инфекции. Лечение хламидиозов сложное, длительное и не всегда успешное, что связано с присутствием ассоциированных инфекций, резистентностью хламидий к антибиотикам, наличием персистирующих форм и иммунодефицитного состояния больных. Для лечения используются антибиотики группы макролидов. Они относятся к числу тканевых антибиотиков, так как их концентрация в тканях значительно выше сывороточных. Новые макролиды — азитромицин (Сумамед), рокситромицин, отличаются хорошим всасыванием в желудочно-кишечном тракте, а также пролонгированным действием. При хламидийной инфекции у новорожденных проводится лечение эритромицином в течение 14 дней или Сумамедом. Короткие курсы лечения Сумамедом связаны с тем, что препарат сохраняется в бактерицидных концентрациях в очаге воспаления 5–7 дней после приема последней дозы.
Наиболее используемыми остаются 10–14-дневные курсы для лечения острой хламидийной инфекции и ее реинфекции. Перспективным методом лечения является «пульс-терапия» азитромицином. При «пульс-терапии» азитромицин назначается в дозе 10 мг/кг массы тела 1 раз в день по схеме 1–7–14 день или по второй схеме: 10 мг/кг массы тела 1 раз в день 3 дня подряд (4 дня перерыв) в течение 3 недель, что позволяет охватить несколько циклов генераций хламидий. При конъюнктивите новорожденных назначают эритромициновую глазную мазь и капли левомицетина в сочетании с приемом эритромицина внутрь. Низкая иммунологическая резистентность новорожденных с внутриутробным хламидиозом делает необходимым применение иммуномодуляторов. Такими препаратами являются интерфероны. Эффективно применение Виферона-1 в течение 10 дней. Виферон совместим со всеми лекарственными средствами, применяемыми для лечения хламидийной инфекции, при этом его длительное назначение три раза в неделю через день в течение месяца способствует нормализации микрофлоры кишечника. Важное место в лечении хламидийной инфекции должно отводиться применению в возрастных дозировках бифидум- и лактосодержащих пробиотиков.
Микоплазмоз. Этой инфекцией обусловлена значительная часть мертворождений, преждевременных родов и рождения больных детей. Акушерскую и педиатрическую патологию чаще всего вызывают следующие штаммы микоплазм: Mycoplasma pneumoniae, M. hominis, M. urealiticum. Микоплазмы представляют отдельный класс возбудителей Mollicutes, характеризующийся отсутствием ригидной клеточной оболочки, выраженным полиморфизмом, способностью к репродукции. Микоплазмы имеют высокую степень адгезии к клеточной мембране, а также механизм мимикрии под антигенный состав клетки-хозяина, что способствует длительной персистенции и снижению эффективности иммунной защиты и соответственно суперинфекции другими микроорганизмами.
При гистологическом исследовании плаценты выявляются характерные для микоплазменной инфекции изменения децидуальных клеток и периферического трофобласта (В. А. Цинзерлинг, В. Ф. Мельникова, 2002). При микоплазменном поражении последа наиболее отчетливо изменяются сосуды, что свидетельствует о важности гематогенного распространения микоплазм по плаценте.
Диагностические трудности представляют ситуации, когда в анамнезе конкретной беременности у женщины как будто нет типичных нарушений, она не переносила респираторных заболеваний, не было токсикоза, ребенок родился жизнеспособным, с хорошими показателями по шкале Апгар, нормальной массой и длиной тела. В постнатальном анамнезе у детей, если они инфицированы микоплазмами, могут появляться симптомы угнетения ЦНС, возникают респираторные заболевания, отиты, инфекции мочевыводящих путей (пиелонефриты). Поэтому в подобных случаях важно оценивать гистологический анализ плаценты.
Диагностика. Стандартом диагностики микоплазмоза является ИФА с сероконверсией IgG, IgM. Материалом для исследования является кровь ребенка, смывы с задней стенки глотки, наружных половых органов, стенок влагалища, первая порция свежевыпущенной мочи. Для ПЦР-анализа используется кровь ребенка, секрет с задней стенки глотки, мазок со стенок влагалища.
Лечение микоплазменной инфекции у детей практически не отличается от лечения хламидийной инфекции: принципы назначения макролидных антибиотиков, их суточные дозы, режим введения, длительность курса и терапия сопровождения аналогичны описанным выше. Назначение азитромицина тормозит рост M. hominis и M. urealiticum. Рост обеих микоплазм тормозят также левомицетин и особенно тетрациклины (доксициклин), а также ципрофлоксацин, но ввиду побочных эффектов и возрастных ограничений их рекомендуют назначать лишь при микоплазменных менингоэнцефалитах и тяжелых пневмониях (Н. П. Шабалов, 2002).
Под нашим наблюдением находилось 80 детей первых двух лет жизни, у которых было выявлено внутриутробное инфицирование. Преобладали пациенты первого года жизни — 68 детей (85%), старше года было 12 больных (15%). В комплекс обследования детей включались оценка клинико-анамнестических данных, анализа крови, мочи, УЗИ брюшной полости, УЗИ мозга, биохимические печеночные и почечные тесты (по показаниям), ИФА на внутриутробные инфекции, ПЦР-тесты слизи из зева на хламидии, микоплазмы, герпесвирусы, ИФА кала на ротавирусы и бактериологические посевы кала на острые кишечные инфекции.
Беременность и роды у большинства матерей наблюдаемых детей были осложненными. Токсикозы беременности и угроза выкидыша наблюдались у 38,8% и 28% матерей, гипоксия плода в родах и многоводие — соответственно у 38,8% и 16,2%, отслойка плаценты и кесарево сечение — у 17,5%. У 19 беременных женщин (24%) были различные соматические заболевания. У 52 женщин (64,9%) были выявлены инфекции: хламидийная и микоплазменная инфекция (у 35 и 16 беременных соответственно) и у 8,7% — герпесвирусные инфекции.
Заподозрить внутриутробные инфекции у наблюдаемых детей можно было в более ранние сроки их жизни, в первую очередь по высокой степени поражения у них различных органов и систем: ЦНС (54,2%), органов дыхания (48,2%), желудочно-кишечного тракта (96,3%), глаз и слезного канала (39,7%), лимфатического аппарата (4,8%). Однако диагноз хламидийной инфекции в предшествующий период их наблюдения был поставлен только трем детям из 80. Обращало на себя внимание значительное отклонение в клинических анализах крови: анемизация (30,6%), лейкопения с лимфоцитозом (42%), нейтропения (15%), ускорение СОЭ (29,8%), что в совокупности свидетельствовало о наличии воспалительного процесса в организме и выраженном снижении иммунореактивности детей.
При серологических исследованиях и ПЦР-тестировании на внутриутробные инфекции у детей в 100% случаев были обнаружены при помощи ИФА положительные антихламидийные антитела в крови и при ПЦР-тестировании — антигены Chlamydia pneumoniaе или Ch. trachomatis в слизи из носоглотки. ИФА-положительные антитела класса IgM и IgG к Ch. pneumoniaе были выявлены у 88,7% больных, антитела класса IgM и IgG к Ch. trachomatis — у 7,5% пациентов. У 27,5% наблюдаемых детей серологические титры не были диагностически значимыми. Такие пациенты расценивались как больные с латентными формами хламидиоза, они нуждались в симптоматическом лечении и диспансерном наблюдении. Больные с высокими титрами антихламидийных антител и положительным результатом ПЦР-тестов имели признаки активации хламидийной инфекции. У них были заболевания органов дыхания (трахеобронхиты, пневмонии), отиты, конъюнктивиты, дакриоциститы. У 24% детей выявлялись микст-инфекции: хламидиоз с микоплазмозом — у 6 детей и хламидиоз в ассоциации с Candida аlbicans и герпесом — у 13 детей. Необходимо иметь в виду, что хламидийная инфекция, выявляемая в первые недели жизни детей, настолько опасна своими отсроченными осложнениями, что однозначно требует проведения лечения.
Клинический пример 1. Настя К., три месяца, поступила в стационар с диагнозом направления — ОРВИ.
Жалобы: на кашель, насморк, повышение температуры до 38,5 °С, беспокойство, отказ от еды, дисфункцию кишечника.
Анамнез болезни: больна в течение 7 дней, появился кашель, насморк, повысилась температура, изменился стул, стал жидким и водянистым, участился до 6 раз в сутки. В последние два дня перед госпитализацией стала отказываться от еды.
Анамнез жизни: девочка от первой беременности, угроза ее прерывания на сроках в 16, 27 и 38 недель. Мать обследована на внутриутробные инфекции, были выявлены уреаплазмоз и цитомегаловирусная инфекция. Проведено лечение эритромицином. За время беременности перенесла два раза ОРВИ. Роды на 40-й неделе, масса тела 3350 г, длина 50 см. К груди приложена на вторые сутки жизни, в роддоме введен докорм смесью NAN-1. В родильном доме у ребенка диагностировано поражение ЦНС, гипертензионный синдром. При нейросонографии было подозрение на внутрижелудочковое кровоизлияние.
При поступлении в стационар состояние средней тяжести, лихорадка до 39 °С (держалась в течение 6 дней), стул жидкий, учащенный до 6 раз в сутки, водянистый. Аппетит снижен, рвот и срыгиваний не было. При осмотре кожа бледная. Слизистые полости рта сухие. Язык обложен беловатым налетом. Зев рыхлый, зернистый, с выраженной гиперемией. Из носа слизистые выделения, кашель редкий, влажный. Был диагностирован двусторонний средний катаральный отит. Пульс 144 в минуту, удовлетворительного наполнения. Тоны сердца ритмичные, приглушены. Границы сердца не изменены. В легких перкуторно звук с коробочным оттенком, дыхание жесткое, без хрипов. Живот умеренно вздут, перистальтика усилена, печень +2 см ниже реберной дуги, селезенка +0,5 см. Мочеиспускание достаточное.
Анализ крови: гемоглобин 109 г/л; эритроциты — 3,7×1012/л; цветовой показатель — 0,90; лейкоциты — 11,6×109/л; палочкоядерные нейтрофилы — 4%; сегментоядерные — 26%; лимфоциты — 55%; моноциты — 13%; базофилы — 2%; СОЭ — 34 мм/час. Анализ крови на 15 день госпитализации: гемоглобин — 112 г/л; эритроциты — 3,8×1012/л, цветовой показатель — 0,88; лейкоциты — 16,6×109/л; палочкоядерные нейтрофилы — 2%; сегментоядерные — 56%; лимфоциты — 34%; моноциты — 5%; эозинофилы — 2%; базофилы — 1%; СОЭ — 27 мм/час. Анализы мочи, копрограмма и биохимический анализ крови — без отклонения от нормы.
Анализ ликвора от 22.10.2008: количество — 2 мл; белок — 0,25 г/л; сахар — 2,9 ммоль/л; цитоз — 2/3. Посев ликвора — роста флоры нет. Посев крови на микрофлору — стерильный. Посев кала на острую кишечную инфекцию — отрицательный. ИФА кала на ротавирус — положительный. Серологический анализ крови методом ИФА выявил высокий титр антител к Ch. pneumoniae (1:320), антител к Ch. trachomatis не обнаружено. Выявлены также положительные титры антител класса IgG к вирусу цитомегалии и герпесвирусу. Типоспецифические антитела класса IgM к ЦМВ и герпесу — не обнаружены. Оба класса Ig (IgM и IgG) к микоплазме были отрицательные. В слизи с задней стенки глотки методом ПЦР найдены ДНК-Сh. pneumoniae, маркеров ДНК-ЦМВ и ДНК-герпеса методом ПЦР в смыве из носоглотки не было обнаружено. УЗИ органов брюшной полости выявило увеличение размеров печени и селезенки. УЗИ головного мозга обнаружило минимальные резидуальные изменения головного мозга.
На основании данных клинического и лабораторного обследования был установлен диагноз — острый энтероколит, ротавирусной этиологии, средней тяжести. Сопутствующие заболевания: хламидийная инфекция, хламидийный ринофарингит, двусторонний средний катаральный отит. Перинатальная энцефалопатия, гипертензионный синдром, ранний восстановительный период.
Проведенное лечение: дозированное питание смесью NAN-1, пероральная регидратация. Антибактериальные препараты вводились внутримышечно в течение 4 дней цефотаксим и последующих 7 дней — цефазолин (возрастные дозы), затем эритромицин по 50 тыс. ед. 3 раза в день внутрь в течение 8 дней и далее азитромицин 60 мг/сутки (1 день) и далее — по 30 мг в сутки. Антибиотики назначались в сочетании с Вифероном-1 в свечах 2 раза в день и пробиотики внутрь (Бифиформ).
В результате проведенного лечения ротавирусный энтероколит был купирован, стул оформлен, аппетит улучшился, копрограмма нормализовалась. Однако клинические анализы крови в динамике не улучшались, напротив, отмечалось нарастание анемизации (от нормохромии к гипохромии), лейкоцитоз в крови к 15-му дню лечения увеличился с 11,6×109/л до 16,6×109/л, сохранялось ускорение СОЭ 27 мм/час. Все вышеперечисленное в совокупности свидетельствовало об активации хламидийной инфекции на фоне инфицирования ротавирусами. Поэтому курс лечения макролидами был продолжен, эритромицин был заменен на азитромицин и последний препарат назначен по прерывистой схеме. Иммунотропная терапия Вифероном-1 продолжена до 3 месяцев (3 дня в неделю прием препарата, 4 дня перерыв). Диспансерное наблюдение за больной продолжено, состояние ребенка удовлетворительное, гемограмма нормализовалась.
Анализ истории данного пациента показывает отсутствие настороженности у педиатров в отношении внутриутробной инфекции у детей, даже в тех ситуациях, когда у беременной женщины было выявлено инфицирование уреаплазмозом и цитомегаловирусом. Однако после выписки из роддома ни участковый педиатр, ни невролог не провели углубленного обследования ребенка на первом месяце жизни на внутриутробную инфекцию, которая, как правило, в постнатальный период может давать активацию инфекционного процесса у ребенка на ослабленном иммунном фоне при его искусственном вскармливании. У пренатально инфицированных детей легко возникает инвазия ротавирусами, после которых реактивация ожидаема.
Клинический пример 2. Сергей Т., один месяц, поступил в больницу с жалобами на кашель, рвоту после приступа кашля. Кашель появился в последние две недели, сначала был редким, затем участился, в конце кашля небольшое отхождение слизистой мокроты. Учащение стула до 6 раз в сутки. Диагноз направления и приемного покоя больницы — острый гастроэнтерит. Острое респираторное вирусное заболевание (назофарингит).
Анамнез. Ребенок от первой беременности, отягощенной токсикозом в первую половину беременности, нефропатией во вторую ее половину, мать перенесла ОРВИ затяжного характера с длительным кашлем при сроке 12–13 недель. При обследовании беременной в 14 недель была выявлена микоплазменная инфекция. В ИФА крови обнаружены антитела класса IgG в титре 1:200 (серотип M. hominis) и положительный тест методом ПЦР слизи из носоглотки. Лечение было симптоматическим. На 38–39 неделе беременности повторно перенесла ОРВИ. Роды в срок, масса тела при рождении 3600 г, длина 51 см. Оценка по шкале Апгар 8/9 баллов. Через неделю после выписки из роддома у ребенка появились респираторные катаральные явления, рвоты при кашле и дисфункция кишечника.
При осмотре состояние средней тяжести. Кожа чистая, бледноватая. Дыхание через нос, затруднено, выделения из носа слизистые. В зеве гиперемия задней стенки глотки и небных дужек, зернистость слизистой. Тоны сердца приглушенные, частота сердечных сокращений (ЧСС) — 136 в минуту. Дыхание — 46 в минуту. Перкуссия легких — коробочный оттенок звука, дыхание жесткое, без хрипов. Живот мягкий, умеренно вздут, печень +2,0 см ниже реберной дуги. Селезенка +0,5 см. Стул жидкий, водянистый с небольшой примесью зелени, 5 раз в сутки. Мочится достаточно. Неврологический статус без особенностей.
Анализ крови: Hb — 121 г/л; Er — 4,01×1012/л; L — 9,5×109/л; палочкоядерные нейтрофилы — 2%; сегментоядерные — 12%; лимфоциты — 76%; моноциты — 8%; эозинофилы — 2%; СОЭ — 6 мм/час. Анализ мочи — без патологии. Копрограмма — цвет желтый, полужидкий, нейтральный жир +, желчные кислоты ±, мыла ±, слизь +, L — 3–5 в поле зрения. Посев кала на ОКИ и дизентерийную группу отрицательный. Анализ кала методом ИФА на ротавирус — отрицательный. Посев кала на условно-патогенную флору — отрицательный. Реакция Видаля со стафилококковым антигеном — отрицательная. Анализ крови методом ИФА на внутриутробные инфекции: IgM положительная с M. hominis, IgG положительная (в титре 1:200) с тем же серотипом микоплазм. ИФА на антитела к токсоплазмам, цитомегаловирусу, герпесу и хламидиям — отрицательные. ПЦР слизи из носоглотки выявляет антигены M. hominis.
Проведенное лечение. Цефотаксим внутримышечно, курс 5 дней, Бифиформ по 1/2 капсулы 2 раза в день — 2 недели. После получения данных обследования установлен диагноз — респираторный микоплазмоз, пренатального происхождения, активная фаза. Произведена смена антибиотика на азитромицин в сочетании с Вифероном-1 в возрастной дозе (по пролонгированной программе).
Данный клинический пример свидетельствует об активации микоплазменной инфекции у ребенка с возраста двух недель, хотя его инфицирование произошло внутриутробно от матери, перенесшей микоплазмоз во время беременности. Лечение же микоплазмоза у матери было неадекватным, ее заболевание сохраняло свою значимость вплоть до родов, когда она опять перенесла ОРЗ. Полученные результаты обследования на внутриутробные инфекции выявили типоспецифичный IgМ (маркер острого инфекционного процесса) и позволили поставить диагноз микоплазменной инфекции, активная фаза, пренатального происхождения с поражением органов дыхания и функциональными расстройствами органов пищеварения.
- Внутриутробные инфекции у детей первого года жизни наблюдаются чаще, чем диагностируются педиатрами.
- У пациентов с рецидивирующими заболеваниями слизистой глаз, носа, глотки, органов дыхания и пищеварения наиболее часто выявляются хламидиоз и микоплазмоз.
- Для своевременной и достоверной диагностики внутриутробных инфекций следует назначать комплекс исследований с применением серии лабораторных тестов, которые следует проводить в диалектике.
- Исаков В. А., Архипова Е. И., Исаков Д. В. Герпесвирусные инфекции человека: руководство для врачей. С.-Пб, 2006, с. 302.
- Капустина Т. А., Белова Е. В., Манчук В. Т., Кин Т. И. Инфицированность хламидиями у детей с хроническими заболеваниями носоглотки и придаточных пазух носа // Росс. вестник перинатологии и педиатрии. 2007. Т. 52. № 6, с. 65–66.
- Руководство по амбулаторно-поликлинической педиатрии. Под ред. А. А. Баранова. Изд. группа «Гэстар-Медиа», 2007, с. 394–396.
- Спивак Т. В., Катосова Л. К. Роль хламидийной инфекции при бронхиальной астме у детей //Педиатрия. 2009. Т. 87. № 2, с. 19–25.
- Цинзерлинг В. А., Мельникова В. Ф. Перинатальные инфекции. СПб.: Элби- СПб; 2002, с. 52–66.
- Шабалов Н. П., Цвелев Ю. В. Основы перинатологии. М.: «Медпресс-информ», 2002, с. 476–487.
СПБ МАПО, Санкт-Петербург
источник
Менингококковая инфекция — инфекционное заболевание, вызываемое бактерией Neisseria meningitidis.
Существует 12 серогрупп (разновидностей) этой бактерии, из них 6 (A, B, C, W, Y и X) вызывают большинство тяжелых форм менингококковой инфекции. Особенность инфекции в том, что у менингококка, как и у гемофильной палочки типа b и пневмококков, имеется полисахаридная капсула, окружающая бактерию и защищающая ее от атак иммунной системы.
Маленькие дети (в возрасте от 0 до 5 лет) еще, как правило, не имеют сформированного защитного иммунитета против этой инфекции.
Возбудитель менингококковой инфекции передается только от человека к человеку. Инфекция распространяется воздушно-капельным путем и проникает в организм через слизистую носа, полости рта и глотки.
Мельчайшие капли выделений из дыхательных путей, полости рта или носоглотки носителя или больного человека при тесном контакте — поцелуях, чихании, кашле, — попадают на слизистую здорового человека.
Там бактерии могут на некоторое время оставаться и размножаться, не вызывая признаков заболевания и не влияя на самочувствие, вызывая бессимптомное носительство (иногда наблюдаются симптомы насморка [назофарингита]).
По имеющимся данным, считается, что в любой момент времени около 10-20% населения являются носителями менингококков. Но иногда, по не вполне понятным причинам, подавляя защитные силы организма, инфекция проникает через слизистую оболочку в кровь.
Используя питательные вещества, находящиеся в крови, менингококки могут быстро размножаться, вызывая заражение крови (сепсис), и распространяться через кровь в оболочки головного мозга или другие внутренние органы (например, легкие, суставы, сердце, подкожно-жировую клетчатку и др.).
Время между моментом попадания бактерии в организм и до появления первых признаков болезни называется инкубационным периодом. Для менингококковой инфекции он составляет в среднем 4 дня, но может и меняться от 2 до 10 дней.
Под формами заболевания подразумевается то, какой характер носит болезнь, как она протекает, какие органы и системы она поражает. В случаях менингококковой инфекции существуют следующие формы: локализованные, генерализованные и смешанные.
Развиваются в случае, если защитные силы организма справляются с инфекцией, и она не попадает в кровь.
Менингит, менингоэнцефалит, сепсис (заражение крови).
Развиваются, если возбудитель преодолевает местную иммунную защиту на слизистых оболочках носоглотки и попадает в кровь. С током крови бактерии разносятся по организму, проникают в кожу, почки, надпочечники, легкие, ткани сердца, оболочки головного мозга. Размножение и гибель менингококков приводит к выбросу эндотоксина — ядовитого продукта распада бактерий.
Он разрушает стенки сосудов, отчего образуются кровоизлияния, которые выглядят сначала как сыпь (экзантема) — красноватые точки на коже или энантема — такие же высыпания на слизистых полости рта, носоглотки, иногда глаз, а затем принимают типичный вид геморрагической (от темно-красной до черной) сыпи размером от точек до обширных некрозов (отмирания) участков кожи.
Этот же бактериальный токсин приводит к развитию отека мозга и мозговых str-симптомов, кровоизлияниям во внутренние органы.
Сочетание, например, менингита и сепсиса) и редкие формы: развитие воспаления в суставах — полиартрит, в легких — пневмония и т. д.
Протекает без жалоб, длится в среднем 10-15 дней, возбудитель обнаруживается только при лабораторном обследовании.
Симптомы менингококкового острого назофарингита могут напоминать ОРВИ — повышение температуры, слабость, головная боль, сонливость, выделение слизи и небольшая заложенность носа.
Может закончиться выздоровлением, переходом в носительство или стать причиной развития менингита и других тяжелых форм менингококковой инфекции.
В любом случае, даже при минимальных подозрениях или риске заражения менингококком нужно вызывать врача, поскольку самостоятельно определить, действительно ли это менингококковый назофарингит или другая инфекция невозможно: необходимо проведение осмотра и лабораторные анализы.
Развивается быстро, часто на фоне назофарингита. Температура может резко подняться, с ломотой в мышцах, сильной головной болью, помутнением сознания.
В течение 1-2 суток появляется типичная сыпь при менингококковой инфекции — сначала розоватая, затем геморрагическая: неровные высыпания, темно-красного цвета, немного приподнимающиеся над кожей. Как правило, сыпь локализуется на ягодицах, ногах, нижней части туловища.
Элементы сыпи очень разные, от «булавочного укола» и красно-коричневых «звездочек» до больших кровоизлияний, которые в тяжелых случаях приводят к отмиранию тканей — некрозу. Неблагоприятным признаком считается раннее появле ние сыпи на лице.
По некоторым данным в России «50% всех бактериальных менингитов у детей в возрасте до 5 лет» вызывает менингококк.
Начинается менингококковый бактериальный менингит остро, температура может быстро нарастать до высоких цифр, одновременно могут появиться жалобы на боль в спине, шее, резкую головную боль с непереносимостью света, звуков.
Многократно повторяется рвота, облегчения она не приносит. Сознание спутанное, человек сжимается в комочек: лежит на боку, с подтянутыми к животу ногами, типичное описание этого признака — «поза легавой собаки». Общее состояние, как правило, тяжелое или очень тяжелое.
Могут быстро — иногда в первый день, но чаще на 2-3 день после появления признаков болезни, — развиться симптомы, которые говорят о том, что инфекционно-воспалительный процесс затронул оболочки головного мозга, вызывал их раздражение.
Такие симптомы называют менингеальными, к ним относят: ригидность затылочных мышц (невозможно прижать подбородок к груди), симптомы Кернига (врач не может разогнуть у больного ногу в колене), Брудзинского (одновременное сгибание головы и подтягивание ног к животу) и другие. Возможно появление типичной сыпи.
Менингеальная симптоматика может говорить о тяжести заболевания, но самостоятельно, без врача, определить ее не следует: нужна комплексная проверка и опыт в оценке симптомов.
Воспаление затрагивает мозговые оболочки, головной, иногда спинной мозг. Признакисходны с симптомами менингита, также развивается сыпь. При менингоэнцефалите могут появиться геморрагическая экзантема и энантема.
Экзантемой называют разнообразную сыпь на коже, которая может быть при самых разных инфекциях, аллергиях, это общее описание высыпаний. Энантема — это сыпь разного характера, появляющаяся на слизистых оболочках. В самом начале менингоэнцефалита может быть трудно определить тип сыпи.
Она может начинаться как розеола — небольшого, от 1 до 10 мм в диаметре, округлого покраснения, который светлеет при или исчезает при нажатии на него. Затем может переходить в геморрагическую сыпь в виде точек, пятен, звездочек разного размера, не исчезающих при нажатии на них.
Менингококковый сепсис (менигококкцемия) — тяжелая форма заболевания. Состояние больных очень тяжелое: сильная головная боль, рвота, температура может быть как очень высокой — 41° C, так и быть ниже 36,6° C.
Связано это с очень быстрым нарушением работы сосудов, падением артериального давления. Быстро появляется пятнисто-папуле зная сыпь: распространяясь по коже и слизистым, она часто сливается с образованием пузырей с кровянистым содержимым. Смертность при данной форме очень высокая — до 60%.
Поставить точный диагноз можно только после лабораторного исследования: если врач заподозрит менингококковую инфекцию, то он назначает анализ крови, спинномозговой жидкости, отделяемого слизистых и сыпи.
Даже при своевременной и правильной постановке диагноза, правильно назначенном лечении, «высок риск летального исхода. У 10-20% выживших людей бактериальный менингит может приводить к повреждению мозга, потере слуха или трудностям в обучении. В тяжёлых случаях возможна гангрена пальцев кистей, стоп, ушных раковин».
Поэтому при развитии хотя бы одного из симптомов, напоминающих по описанию симптомы менингококковой инфекции, сепсиса и любых других форм, рекомендуется вызвать «скорую помощь».
Предварительный диагноз, а затем его уточнение возможно только после клинического осмотра, с обязательным забором с помощью спинномозговой пункции ликвора — спинномозговой жидкости, а также мазков с поверхности слизистой носоглотки, сыпи.
Согласно данным, «менингококковая инфекция потенциально смертельна, и всегда должна рассматриваться как медицинская чрезвычайная ситуация. Пациента необходимо госпитализировать в больницу».
Лечение зависит от формы заболевания. Госпитализация требуется при любой форме, но если при выявлении бессимптомного носительства менингококковой инфекции и назофарингите могут назначить антибиотики, витаминно-минеральные препараты, то другие формы заболевания требуют экстренного вмешательства и интенсивного лечения.
В зависимости от формы заболевания, особенностей течения, возраста больного и других причин, могут быть назначены антибиотики, возможно, потребуется их комбинация, коррекция дозы.
Также могут потребоваться препараты для снижения температуры, снятия судорог, улучшения циркуляции крови и для дезинтоксикации, поддержания работы сердечно-сосудистой системы, головного мозга, снижения риска возможных осложнений.
Могут потребоваться и другие мероприятия по поддержанию жизненно важных функций, вплоть до вентиляции легких. Чтобы лечение было максимально эффективным «важно идентифицировать серогруппу менингококка и провести тестирование микроорганизма на чувствительность к антибиотикам».
Вызываемая менингококком инфекция одинаково опасна для всех людей, кроме получивших прививку от менингококковой инфекции. По данным ВОЗ (2), 10-20% населения в любой момент считаются бессимптомными носителями менингококковой бактерии N. meningitidis. Выделяют следующие группы повышенного риска по развитию менингококковой инфекции (1) (2) (3):
В отсутствие вакцинации защитный иммунитет против менингококков у детей до 5 лет, как правило, еще не сформирован. Имеет значение и то, что дети часто берут в рот игрушки и предметы окружающей среды, делятся едой друг с другом, пьют из общей посуды. Это повышает риск передачи инфекции, если в коллективе имеется ребенок или взрослый бессимптомный носитель менингококков без признаков заболевания.
Которые часто проводят время в скученных условиях (вечеринки, дискотеки, общежития, казармы). Как указано выше, около 10-20% людей считаются возможными бессимптомными носителями менингококковой инфекции. Чем больше и интенсивнее контакты — тем выше риск заразиться.
По этой же причине в группу риска входят призывники и новобранцы.
Лица, перенесшие удаление селезенки, с ВИЧ-инфекцией, с некоторыми генетическими нарушениями. Это лица с иммунодефицитом — сниженными возможностями организма сопротивляться инфекциям.
При нарушениях слуха и ношении кохлеарного имплантата возможно повреждение внутренних структур уха, снижение местного иммунитета, что может представлять определенный риск заражения.
В страны так называемого «менингитного пояса» в Африке, а также в Саудовскую Аравию для совершения хаджа. Длительный сухой период, ветер, пыль с иссушенной почвы, холодные ночи, распространенность инфекций верхних дыхательных путей снижают защитные возможности слизистой носоглотки.
Низкие показатели социально-экономического развития (кроме ОАЭ и Саудовской Аравии), скученность, перемещение большого числа населения из-за традиционного кочевого образа жизни, а в Саудовской Аравии — из-за паломничества, повышают риск того, что на относительно малых территориях соберется большое количество людей, среди которых могут оказаться и бессимптомные носители менингококковой инфекции, и больные, что может привести к возникновению вспышек инфекции.
Короткий инкубационный период, сложность ранней диагностики, быстрое развитие симптомов, распространенность носительства, особенности детского иммунитета, высокий уровень летальности и инвалидизации, а также высокая распространенность инфекции в некоторых странах мира требуют проведения профилактических мер у детей и отдельных взрослых из групп риска.
При вспышках менингококковой инфекции (ограниченных или при эпидемиях) силами медицинских работников могут проводиться так называемые мероприятия в очаге. К ним относится установление карантина, выявление и изоляция носителей, соблюдение санитарно-эпидемиологического режима, другие мероприятия.
Наиболее эффективной мерой является активная иммунизация, то есть профилактическая прививка. В России она включена в Календарь профилактических прививок по эпидемическим показаниям (4). В нем указано, что вакцинации подлежат «дети и взрослые в очагах менингококковой инфекции, вызванной менингококками серогрупп A или C.
Вакцинация проводится в эндемичных регионах, а также в случае эпидемии, вызванной менингококками серогрупп A или C». Вакцинации подлежат также лица, подлежащие призыву на военную службу.
В перечень вакцин, которые могут использоваться в России для вакцинации от менингококковой инфекции входят:
Менингококковые полисахаридные вакцины:
- моновалентная (против серогруппы A) — полисахаридная сухая;
- четырехвалентная (против серогрупп A, C, Y и W).
Менингококковые конъюгированные вакцины:
- моновалентная (против серогруппы C).
- четырехвалентная (против серогрупп A, C, Y и W). (5) (6)
Согласно позиции Всемирной организации здравоохранения, «конъюгированные вакцины предпочтительнее, чем полисахаридные, поскольку могут формировать популяционный иммунитет, а также обладают более высокой иммуногенностью, особенно у детей младше 2 лет».
источник
Опубликовано в журнале:
«Практика педиатра», февраль 2011, с. 10-15
Ю.А. Копанев, детский гастроэнтеролог-инфекционист, ФГУН Московский НИИ эпидемиологии и микробиологии им. Г.Н. Габричевского Роспотребнадзора, канд. мед. наук
Хронические инфекционные болезни у детей встречаются ненамного реже острых инфекционных состояний, а термин «оппортунистические инфекции» перестал быть сугубо специальным для инфекционистов и гинекологов. Теперь с этой проблемой сталкиваются все врачи, в том числе педиатры.
Современные методы диагностики, в частности определение антител в крови методом ИФА и определение ДНК возбудителя методом ПЦР, продемонстрировали, что инфицированность людей оппортунистическими инфекциями достигает 90–99%.
Что такое оппортунистические инфекции
Так обозначаются распространенные хронические инфекционные заболевания, вызываемые условно патогенными микроорганизмами разных типов (вирусы, бактерии, простейшие, внутриклеточные микробы), поражающими преимущественно слизистые оболочки и лимфатическую систему, передающимися разными путями и имеющими ряд закономерностей.
Главная особенность всех хронических инфекций – возможность существования в активной и «спящей» (латентной) форме, а также «айсберговый» тип существования (рис. 1). Большинство микроорганизмов присутствует в организме в неактивной форме, как подводная невидимая часть айсберга. Для организма такие неактивные микроорганизмы не представляют угрозы, клинической картины не вызывают, иммунная система на них практически не реагирует, и, самое главное, на неактивные формы не действуют этиотропные препараты (антибиотики, противовирусные и другие средства). Активных микробов меньше, они уязвимы для лекарств, вызывают клинические проявления, на них вырабатываются антитела (врачи начинают «видеть» хроническую инфекцию, как надводную часть айсберга). Соотношение активных и неактивных форм зависит от состояния иммунной системы. В случае адекватной работы иммунной системы хроническая инфекция может быть полностью подавлена, т.е. практически все микроорганизмы будут находиться в неактивной форме, а человек не только будет физически здоров, но и антитела на данную инфекцию будут на низком уровне (в пределах нормы).
 |
При ослаблении иммунитета происходит активизация значительных количеств оппортунистических микробов, соотношение «спящих» и активных смещается в сторону последних, нарастает клиническая картина. В этот момент лечение будет максимально эффективным. Знание этих особенностей оппортунистических инфекций помогает выбрать правильную и эффективную лечебную тактику.
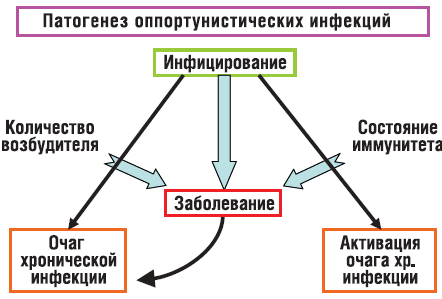
Формирование очагов хронических (оппортунистических) инфекций происходит так, как изображено на рисунке 2. Инфицирование становится заболеванием, если нарушается баланс между количеством возбудителя, попавшего в организм, и состоянием иммунной системы. При ослабленном иммунитете даже небольшое количество микроба может создать проблемы, а большое количество микроорганизмов вызовет заболевание и при неослабленном иммунитете. Некоторые микроорганизмы могут вызвать острое заболевание, а потом перейти в хроническую форму; например, это характерно для вируса Эпштейн Барр – возбудителя инфекционного мононуклеоза. Другие возбудители могут формировать хроническое заболевание без стадии острой болезни, например лямблии (острая форма лямблиоза встречается очень редко). Активизация хронической инфекции может произойти на фоне инфицирования любым другим микробом, тогда к клиническим проявлениям, характерным для этого микроорганизма, присоединяются клинические проявления, характерные для хронического очага. Например, ребенок заболевает ОРВИ, через несколько дней присоединяются симптомы кишечных нарушений. Это может быть активизацией очага хронической инфекции в ЖКТ, спровоцированной ОРВИ.
Эпидемиология
Для оппортунистических инфекций характерны всевозможные пути заражения:
- воздушно капельный (хламидии, легочные микоплазмы); передаваться могут как активные, так и неактивные формы, если человек является не только носителем, но и выделителем микроба в окружающую среду (большинство людей являются носителями, примерно 15% – выделители);
- фекально оральный (хламидии – Ch. psittaci, лямблии); хламидийная инфекция характерна для птиц, животных. Экскременты перемешиваются с землей, загрязняют руки и продукты, при попадании загрязненных и инфицированных элементов в кишечник там может сформироваться очаг хронической инфекции;
- половой (урогенитальный хламидиоз, оппортунистические инфекции); вертикальный (трансплацентарно, во время родов); за счет того, что хронические инфекции существуют в виде активных и неактивных форм (рис. 1), возможен такой способ передачи инфекции от матери плоду: у беременной женщины существует оппортунистическая инфекция в латентной форме, клинических проявлений нет, антитела в крови – в пределах нормы или не выявляются. Происходит вертикальная передача инфекции плоду (передаются неактивные формы), у родившегося ребенка в какой-то момент происходит активизация инфекции;
- трансмиссивный (через кровь и насе комых).
 |
Закономерности влияния на организм
Любой очаг хронической инфекции может вызвать следующие нарушения в организме:
- нарушение функции той системы, где локализуется данный очаг. Очаги хронической инфекции ЖКТ приводят к функциональным нарушениям: дисбактериозу кишечника, диспанкреатизму, дискинезии кишечника и желчевыводящих путей и т.п. Инфекции, тропные к лимфатической системе, вызывают лимфа денопатии. Инфекции дыхательных путей – различные респираторные дисфункции, хронический кашель, хронические заболевания верхних дыхательных путей. Если локализация инфекции мочеполовая система – гинекологические и урологические болезни, а также инфекции мочевыводящих путей;
- ослабление иммунной системы – это не дает возможности организму справиться с очагом хронической инфекции, приводит к появлению новых очагов, а также к частым ОРВИ у детей (часто болеющие дети) и другим проявлениям иммунной дисфункции;
- сенсибилизация с последующим формированием аллергических болезней. Очаги хронической инфекции ЖКТ могут быть одной из главных причин развития атопического дерматита и рецидивирующей крапивницы. Хронические инфекции дыхательной системы способствуют развитию бронхиальной астмы, поллиноза;
- хроническая интоксикация. Продукты жизнедеятельности микроорганизмов и пара зитов могут быть причиной неврологических нарушений, в том числе судорожного синдро ма, бруксизма (скрипение зубами), а также на рушений сна, аппетита, эмоциональной ла бильности, капризности, раздражительности, агрессивности;
- нарушения обмена веществ.
Эти симптомокомплексы менее выражены, когда хроническая инфекция находится в состоянии неактивности, и манифестируют во время активизации очага хронической инфекции. Если очагов хронической инфекции несколько и количество активных форм велико, симптомов становится больше, патологические состояния протекают в подострой форме волнообразно.
Наличие даже одного направления клинической картины должно наводить педиатра на предположение о поиске хронических (оппортунистических) инфекций.
Принципы диагностики
Выявление инфекционного фактора может идти по двум направлениям.
- Поиск возбудителя (микробиологические методы, посевы и т.п.), его ДНК (метод ПЦР) или продуктов его жизнедеятельности (биохимические методы).
- Выявление иммунной реакции организма на инфекцию (поиск антител методом ИФА и др.). Особенности разных методов диагностики представлены в таблице 1.
| Выявление возбудителя | Выявление антител |
|
|
Для первичной диагностики большинства оппортунистических инфекций лучше применять исследование крови – выявление антител. При этом диагностически значимым является повышение количества антител класса G. Методы ИФА и ПЦР могут дополнять друг друга. Возможна такая ситуация: все исследования показали отсутствие инфекции (т.е. ее нет ни по результатам ИФА, ни методом ПЦР или посевом), но это не означает, что микроба нет в организме, он может быть в «спящей» форме и неактивным. Если женщина перед беременностью или во время нее сдавала анализы и оппортунистические инфекции не были выявлены, а у ребенка выявится, например, хламидиоз, это может означать внутриутробное инфицирование неактивным микробом и активизация его у ребенка уже после рождения.
Трактовка результатов анализов представлена в таблице 2. В двух последних строках – ситуации, не требующие лечения.
| IgG | IgM | IgA | ПЦР | Трактовка |
| ↑ | N | N | ↑ или N | Инфекция есть (или есть иммунная память) |
| ↑ или N | ↑ | N | — | Активная фаза (недавнее первичное инфицирование) |
| ↑ или N | ↑ или N | ↑ | — | Активизация хронической инфекции |
| N | N | N | ↑ | Инфекция неактивна (или убитые микробы) |
| N | N | N | N | Инфекции нет (или нет клинически значимой) |
Повышение антител класса G выше диагностически значимых титров к какой либо хронической инфекции при первичной диагностике должно трактоваться как наличие этой инфекции и требует терапевтических действий: иммунокоррекции или активной этиотропной терапии.
Актуальные в педиатрии хронические инфекции
Бактериальные инфекции, вызванные условно патогенной флорой (УПФ)
Возбудители: гемолизирующая кишечная палочка, золотистый стафилококк, гемолизирующие стрептококки, клебсиеллы, лактозонегативные энтеробактерии и др. Живут на слизистых оболочках и в просвете ЖКТ, дыхательных, мочевыводящих путей.
Диагностика: бактериологические посевы – мазки из ВДП, половых органов, посевы на стерильность, исследования фекалий «на дисбактериоз».
Тактика педиатра: иммунокоррекция, применение фаготерапии, антисептиков. Применение антибиотиков показано в острую фазу (фебрильная температура, выраженность клинических проявлений).
Хламидийная инфекция
Возбудители: Ch. trachomatis, Ch. pneumoniae, Ch. psittaci. Вызывают внутриклеточные инфекции, поражающие слизистые оболочки и лимфатическую систему. Могут поражать все системы, где есть слизистая оболочка: конъюнктива глаза (интранатальное инфицирование); верхние дыхательные пути (ВДП), нижние дыхательные пути (воздушно капельный путь); слизистая ЖКТ (фекально оральный путь); мочеполовая система (половой путь или занос через лимфатическую систему);
Источники заражения:
- Человек, как здоровые носители, так и те, у кого активная форма болезни, при условии локализации на слизистых, сообщающихся с окружающей средой. Считается, что носителями хламидий являются более 90% людей.
- Птицы (попугаи, голуби, воробьи и др.). Хламидии выделяются с птичьим пометом, помет попадает в почву и на продукты питания, заражение человека происходит фекально оральным или воздушно-капельным путем.
- Кошки, мелкий рогатый скот (козы).
Заражение происходит воздушно капельным и фекально оральным путем.
Инфицирование – еще не заболевание. Клинические признаки появляются при ослаблении иммунитета.
Клиническая картина зависит от локализации и активности хламидий:
- конъюнктивит (бывает у новорожденных детей при интранатальном инфицировании);
- хронические рецидивирующие заболевания ВДП (тонзиллит, фарингит), а также острые заболевания (ангина);
- рецидивирующие бронхиты или пневмонии, бронхообструкция, астма;
- хроническая дисфункция ЖКТ, дисбактериоз, не поддающийся лечению;
- атопический дерматит (хламидии, будучи внутриклеточной инфекцией, могут приводить к повреждению гистаминобразующих тучных клеток слизистых оболочек) с торпидным течением без эффекта от лечения;
- острые и рецидивирующие заболевания мочевыводящих путей, вульвиты и другие поражения половой системы.
- у детей диагноз подтверждается методом ИФА по выявлению антител;
- метод ПЦР и другие исследования, направленные на выявление возбудителя, практически не имеют смысла, поскольку локализация инфекции происходит чаще всего в труднодоступных для исследования местах (например, глубоко в бронхах или в слизистой оболочке кишечника);
- мазок из зева на выявление хламидий (методом ПЦР) нужен только для выявления степени эпидемиологической опасности, но не может быть основанием для назначения лечения;
- направление на анализы крови для выявления антител к хламидиям – по клинической картине и при наличии эпидемиологических указаний (при выявлении хламидийной инфекции в близком окружении).
Врачебная тактика при хламидийной инфекции. Применение антибактериальной терапии показано только при наличии признаков активности хламидийной инфекции, иначе не будет эффекта.
Показания для антибактериальной терапии:
- любое острое состояние, требующее назначения антибиотика: ангина, пневмония, острый бронхит, гнойный отит, гнойный тонзиллит, гайморит в стадии обострения;
- ОРЗ с высокой температурой (более 38,0 °С) более 3–5 дней;
- ОРЗ с температурой выше 37,0 °С, если она держится более 7–10 дней подряд;
- бронхообструктивный синдром; приступ бронхиальной астмы (если наличие хламидийной инфекции подтверждено анализами);
- затяжной кашель более 3 недель;
- обострение дерматита (если наличие хламидийной инфекции подтверждено анализами);
- неэффективность лечения аллергических болезней.
Все эти симптомы могут возникнуть при активизации хламидий за счет ослабления иммунной системы. В этот период они становятся максимально уязвимыми, а лечение – максимально эффективным. Нужно только применить правильный антибиотик! При подтвержденной хламидийной инфекции или подозрении на нее в случаях, когда нужен антибиотик, можно применять только те антибиотики, которые действуют на хламидии: макролиды, фторхинолоны, препараты тетрациклинового ряда. У детей используются толь ко макролиды! Применение «неправильного» антибиотика (пенициллинового ряда или цефалоспоринов) при хламидийной инфекции приведет не только к упущенной возможности значительно сократить количество хламидий в период их максимальной уязвимости, но и усилит их, позволив распространиться на соседние участки слизистых оболочек. Это в итоге приводит к аллергизации и астматизации (к этому же приводит и несвоевременное применение антибиотика).
Примерная схема лечения в острый период хламидийной инфекции:
- Свечи Виферон и/или КИПферон для укрепления иммунной системы и повышения эффективности антибиотика, 10 дней.
- Антибиотик – макролид (кларитромицин, рокситромицин, мидекамицин, джозамицин, спирамицин), курс 10 дней.
Вне периода активности применяются общеукрепляющие средства и иммунокоррекция.
Микоплазменная инфекция
Возбудители: М. pneumoniae, М. hominis. Вызывают внутриклеточные инфекции, поражающие слизистые оболочки. Излюбленная локализация: дыхательные пути (как верхние, так и нижние) и мочеполовая система (МПС).
Источники заражения: человек – как здоровые носители, так и те, у кого активная форма при условии локализации на слизистых, сообщающихся с окружающей средой. Считается, что носителями микоплазм являются более 90% людей.
Клиническая картина – заболевания дыхательных путей и МПС. До 30% бронхиальной астмы ассоциировано с наличием микоплазменной инфекции, удачное лечение которой может избавить человека от заболевания или существенно улучшить его течение.
Диагностика и лечебная тактика при микоплазменной инфекции не отличаются от таковой при хламидийной инфекции.
Вирусные хронические инфекции Возбудители: вирус Эпштейн Барр (ВЭБ), вирусы простого герпеса 1 го, 2 го, 6 го типов (ВПГ), цитомегаловирусы (ЦМВ) и др.
Для ВЭБ характерны как острое заболевание (инфекционный мононуклеоз), так и хроническое течение по типу оппортунистической инфекции. Для ВПГ 6 го типа характерны острые состояния по клинической картине, напоминающие инфекционный мононуклеоз.
При хроническом течении данные заболевания полностью подчиняются «правилам» оппортунистических инфекций: «айсберговый» тип, активизация при любом другом инфицировании. Характерно поражение лимфоузлов: при активизации ВЭБ или ВПГ 6-го типа развиваются лимфаденопатии той или иной степени тяжести (вплоть до гнойных лимфаденитов). ОРЗ осложняются увеличением лимфоузлов, в редких случаях рецидив инфекционного мононуклеоза; активизация ВПГ 1 го, 2 го типов приводит к появлению типичных везикулярных высыпаний на коже или слизистых.
Диагностика. Исследование крови на антитела (ИФА), диагностически значимым критерием является повышение уровня IgG; возможно также выявление методом ПЦР со слизистых зева.
Лечебная тактика. При выявленном носительстве ВЭБ в период протекания ОРЗ нужно проводить противовирусную терапию (Арбидол, Виферон, Изопринозин) в сочетании с иммунокоррекцией; лечебные мероприятия наиболее эффективны в период обострения.
- Хронические инфекционные заболевания вызывают разнообразные синдромы: нарушение функции пораженной системы, ослабление иммунной системы, сенсибилизацию организма (аллергические болезни), хроническую интоксикацию, нарушения обмена веществ. По этим признакам можно заподозрить хроническую инфекцию и рекомендовать обследование, направленное на ее выявление.
- Ведущим методом диагностики хронических и оппортунистических инфекций является выявление в крови антител класса G выше диагностического титра.
- Для хронических инфекций характерен «айсберговый» тип носительства: небольшое количество активных форм и значительно большее – «спящих», неактивных и неуязвимых для этиотропной терапии.
- Активизация хронических инфекций сопровождается нарастанием клинической картины, появлением новых симптомов дополнительно к симптомам острого заболевания. Активизировать очаг хронической инфекции может любой инфекционный агент, попавший в организм, а также любые факторы, ослабляющие функцию иммунной системы.
- Во время активизации хронические инфекции максимально уязвимы, а этиотропное лечение максимально эффективно. И наоборот, применение этиотропной терапии в неактивный период не дает эффекта.
источник
Детям свойственно в силу более слабого, чем у взрослых иммунитета хуже переносить любые заболевания. Они протекают, как правило, с выраженной симптоматикой с первых дней. Впрочем, есть группа заболеваний, которые протекают чаще бессимптомно, но грозят серьезными последствиями и осложнениями для организма. Скрытые инфекции у ребенка так же сложно диагностировать, как и у взрослого человека. К ним относят все типы герпеса, включая цитомегаловирус, а также папилломы человека и урогенитальные инфекции, которые передаются у взрослых половым путем, а в детский организм попадают еще в утробе матери или в процессе родов.
Существовать скрытые инфекции могут в организме, никак не давая о себе знать долгое время, но в определенных условиях, при снижении защитных сил их возбудители активизируются и размножаются. Вместе с кровью и лимфатической жидкостью болезнетворные микроорганизмы разносятся по всему организму.
Проявляться признаки патологий начинают только при ослаблении иммунитета, в остальных случаях скрытые инфекции протекают без симптомов.
Поскольку заболевание никак себя не проявляет, его достаточно сложно диагностировать. Выявить вирус или болезнетворные бактерии можно только при помощи клинических анализов. Без них невозможно начать лечение, а несвоевременная диагностика часто становиться причиной опасных осложнений и последствий для здоровья.
Один из типов герпеса – цитомегаловирус. Как и другие скрытые инфекции, цитомегаловирусная протекает в латентной форме и поражает ребенка, когда его иммунитет слабеет. Но также проникнуть в организм ребенка возбудитель может еще до рождения, в утробе матери или при родах.
Только у детей с ослабленной иммунной защитой могут проявляться общие симптомы, которые легко спутать с любым другим недугом. Часто цитомегаловирус живет в организме длительное время, не проявляясь, но при благоприятных условиях возбудитель размножается и поражает все органы без исключения.
При активации цитомегаловирус проявляется комплексом общих симптомов:
- повышение температуры тела;
- слабость;
- сонливость;
- вялость;
- увеличение лимфоузлов;
- мышечная слабость;
- увеличение печени и селезенки;
- пожелтение склер;
- снижение аппетита.
Сначала все эти симптомы можно спутать с кишечной инфекцией или простудным заболеванием. У здорового, на первый взгляд, ребенка крайне опасно пускать болезнь на самотек, это может привести к развитию в дальнейшем опасных осложнений. У новорожденных спустя несколько месяцев при скрытой врожденной инфекции начинают проявляться первые расстройства:
- появление судорог;
- аномальное развитие костей черепа;
- расстройства двигательной системы;
- дефицит массы тела.
Со временем становятся заметны нарушения речи, расстройства нервной системы, отставание в умственном развитии, недоразвитость внутренних органов, а у пятой части всех заболевших, стремительно опускается зрение, и наступает слепота.
Заражение ребенка происходит от носителя в любом возрасте. Если инфицирование случилось внутриутробно или в первые часы после появления на свет, речь идет о неонатальном типе герпеса. Симптоматика заболевания может не проявляться длительное время, пока инфекция находится в продромальной стадии, выявить вирус очень сложно.
Латентная форма не менее опасна и требует незамедлительного лечения.
У новорожденных детей заболевание проявляется характерными симптомами практически сразу, у остальных проявления могут меняться и возникать постепенно. Ребенок становится менее подвижным, даже слабая реакция иммунитета на вирус проявляется повышением температуры тела, возникает слабость и общее недомогание. А также для герпеса характерно появление головной боли и воспаление горла. Так себя проявляет и герпесная ангина, которую путают с признаками простуды.
Если диагноз ставят ошибочно и ребенка начинают лечить от респираторного заболевания, упускают драгоценное время и борются не с той болезнью. Иногда вместе с герпесом действительно проявляются различного рода расстройства, и тогда симптоматика становится смазанной, а поставить точный диагноз можно только после лабораторных исследований.
Без лечения вирус герпеса вызывает различные сбои в работе организма. Из самых частых последствий следует выделить такие:
- поражения головного мозга (менингоэнцефалит, энцефалит);
- нарушение зрения, а также конъюнктивит, поражение катаракты, эрозия роговицы и радужной оболочки глаза, сосудов;
- развитие стоматита или гингивита;
- нарушение работы и поражение печени;
- поражение миндалин;
- развитие герпангины;
- детский церебральный паралич.
Вирус герпеса вылечить нельзя, но подавить его активность и предупредить развитие осложнений можно, главное – вовремя диагностировать и начать лечение инфекции у детей.
Заражение папилломавирусом происходит при контактах с инфицированным человеком бытовым путем, а также во время родов и внутриутробно. Попасть в организм человека вирус может при расчесывании и повреждении кондилом (самозаражение).
Длительное время инфекция может не проявляться, но как только иммунитет ребенка слабеет, вирус выходит наружу. Его активность проявляется образованием наростов на кожных покровах, чаще возникающих в подмышечных впадинах, на руках или лице. Этим плоским или нитевидным выростам предшествует покраснение кожи, зуд и жжение. Иногда этих признаков нет, и образование возникает совершенно неожиданно.
Вирус папилломы человека опасен для здоровья и без лечения может привести к серьезным осложнениям. Если наросты возникают на гортани, это может вызвать нарушения дыхательной и голосовой функции. Но хуже всего то, что вирусы папилломы могут спровоцировать злокачественные образования или плоскоклеточный рак.
Выявить скрытые инфекции и подтвердить диагноз, если проявляются признаки заболевания, можно только по результатам клинических анализов. Обнаружить генетический материал вирусов можно в крови, но на сегодняшний день используют несколько методик и для лабораторных исследований берут мазки, соскобы и другие материалы.
Самым информативным и популярным среди лабораторных исследований является анализ ПЦР. Для него подходит кровь, соскоб или любой биологический материал. Тест очень чувствителен к возбудителям, и если будет обнаружен хотя бы фрагмент ДНК патогена, результат будет положительным.
Эту методику серологической диагностики крови применяют чаще других. В процессе исследования в плазме определяют наличие иммуноглобулинов, которые возникают сразу после проникновения инфекции в организм. Этот анализ не только устанавливает тип инфекции, по количеству и характеру антител можно судить о давности заболевания и активности вируса.
Для проведения бак.посева материал забирают, чтобы определить содержащиеся в нем микроорганизмы. Далее, образец помещают на питательную среду, где бактерии размножаются, формируют характерные колонии, по форме и росту которых делаются выводы об их принадлежности к тому или иному виду.
Кроме того, применяют микроскопическую технику. Так изучают мазки, полученные непосредственно от больных, а также берут для изучения фрагменты колоний, выросших на питательной среде.
Впрочем, такие методы не используются для диагностики вирусных инфекций. Эти возбудители способны размножаться только в культуре тканей, а на питательных средах они не растут.
источник


