К группе вирусов герпеса, наряду со всеми известными простым герпесом (простуда на губах), ветрянкой, розеолой или генитальным вариантом вируса, относятся также и некоторые другие. Всего известно 8 типов герпеса, опасных для детей, и 4-й тип – это вирус Эпштейна-Барр (ВЭБ), провокатор мононуклеоза, а при стечении особых обстоятельств – и многих более опасных патологий.
Проблемой именно этого вируса является тот факт, что его попадание в организм не всегда означает инфекцию, но он может крайне негативно влиять на иммунитет ребенка, формируя субклинические иммунодефициты. Кроме того, перенесенный ранее мононуклеоз на 6-12 месяцев после него создает более благоприятные условия для различных респираторных инфекций, что может формировать частые и осложненные ОРВИ. Поэтому важно своевременное и активное выявление ВЭБ-инфекции в любом возрасте.
Чем младше ребенок, тем тяжелее может протекать в его организме ВЭБ-инфекция, особенно она опасна для плода и новорожденного.
Проведение анализов на ВЭБ может быть показано детям и подросткам при подозрении на мононуклеоз или при его исключении, а также беременным женщинам, чтобы исключить внутриутробное поражение плода вирусом. Опасен вирус детям с врожденными и приобретенными иммунодефицитами, младенцам, особенно недоношенным или имеющим аномалии развития.
Также анализы назначают при наличии увеличения лимфоузлов с их воспалением и болезненностью, при наличии атипичной ангины и длительной лихорадки более 38.5 ℃ с симптомами, похожими на грипп или ОРВИ.
Если в анализе крови возникают изменения, которые типичны для мононуклеоза, для подтверждения диагноза или его опровержения проводят более специфичные анализы.
Если говорить об общем анализе крови – это первый из анализов, который может помочь в определении ВЭБ. В нем может наблюдаться увеличение абсолютного количества лимфоцитов, сдвиг лейкоцитарной формулы и понижение количества гемоглобина и эритроцитов. Кроме того, типично повышение уровня тромбоцитов, что грозит повышением свертываемости крови – тромбофилией.
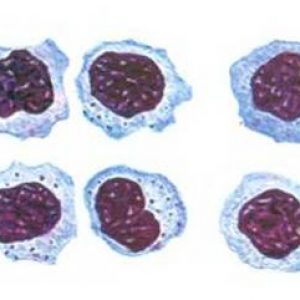
Но самый главный признак ВЭБ – это появление атипичных мононуклеаров (совиный глаз), атипичной формы пораженных лимфоцитов, которые становятся похожими на моноциты.
Дополняет картину изменение в биохимическом анализе крови – выявление аномалий в печеночных ферментах и работе селезенки.
Важнее всего будут иммунологические анализы, которые определяют специфические изменения в иммунитете – изменение концентрации специфических генераций лимфоцитов, а также нарушение количественного соотношения разных классов иммуноглобулинов – дисглобулинемия. В силу того, что вирус обладает иммунодепрессивными свойствами, возникает относительный дефицит иммуноглобулинов памяти (класса G), что подавляет активность иммунной системы против вируса и позволяет вирусу распространяться по телу.
Подобные отклонения типичны как для инфекционного мононуклеоза, так и для некоторых других тяжелых вирусных инфекций, поэтому для подтверждения диагноза необходимо будет ПЦР исследование крови с выявлением ДНК вируса ВЭБ.
Подобные анализы показаны беременным для исключения врожденного мононуклеоза и поражения плода ВЭБ, для новорожденных с признаками иммунодефцита и врожденных патологий, а также для детей с характерными проявлениями ангины, лихорадки и лимфаденоптии.
Самыми основными исследованиями для выявления ВЭБ-инфекции являются определение антител к вирусу методом иммуноферментного анализа или выявление ДНК вируса методом ПЦР.
У детей проводят целый ряд анализов, выполняемых в образце крови. Это важно для определения не только факта заражения, но и стадии болезни. От этого зависит тактика лечения.
ИФА с определением антител к ВЭБ проводится в образце венозной крови ребенка, определяются иммуноглобулины 5 основных видов IgG или IgM к раннему, капсидному либо ядерному антигенам. Для исследования нужна плазма крови, в ней циркулируют антитела. В зависимости от лаборатории, проводится исследование метолом прямой ИФА, непрямой или сендвич-ИФА. Этот метод позволяет не только определить наличие антител к ВЭБ, но и помогает в уточнении стадии болезни.
Разные виды антител (IgG или IgM) синтезируются в разной стадии инфекции, и таким образом те или иные позитивные реакции типичны для разных стадий ВЭБ-инфекции.
Нормативными значениями для ИФА-исследования являются отрицательные результаты всех тестов – они указывают на отсутствие ВЭБ в организме. Но отрицательные результаты могут показать начальную стадию болезни, когда антитела еще не наработались.
Появление антител класса IgМ к раннему антигену можно выявить через 1-2 недели с момента попадания ВЭБ в тело, это острая стадия инфекции. Также они повышаются в период реактивации вируса. Перестают определяться эти иммуноглобулины примерно к концу полугодия с момента заражения. На фоне хронической ВЭБ-инфекции их очень много, при атипичном течении – они не выявляются.
Иммуноглобулины IgG к капсидному антигену также определяются рано, примерно к 3-4 неделе с начала болезни, но максимума их концентрация достигает к двум месяцам болезни.
В острой фазе инфекции в детском возрасте могут не определяться.
При наличии хронической ВЭБ-инфекции, особенно на фоне реактивации вируса, количество этих антител максимально. Они остаются в крови зараженных людей пожизненно, как и сами вирусы, указывая на формирование к инфекции стойкого иммунитета.
Антитела класса IgM к капсидному антигену возникают еще до появления симптомов болезни, особенно много их бывает на протяжении первых 6-ти недель инфекции. Они типичны для острой ВЭБ-инфекции или для активации хронического ее течения. Они постепенно исчезают из крови на протяжении полугода.
Антитела класса IgG к ядерному антигену указывают на прямой контакт с вирусом. Они не определяются в острой фазе болезни, определяясь после выздоровления с периода от 3 до 10 месяцев. В крови они циркулируют до нескольких лет.
Наличие тех или иных вариантов антител говорит о свежести инфекции: только острофазные IgM говорят о первичной и недавней инфекции. Одних только антител в крови для определения острой инфекции или врожденного ВЭБ нередко слишком мало. Тогда для подтверждения диагноза необходимо определить ДНК самого ВЭБ в плазме.
ПЦР-исследование плазмы на определение ВЭБ помогает при первичной инфекции, определяя наличие вируса в плазме. Для реактивации инфекции методика определения не подходит. Нормативные значения – это отрицательная реакция, указывающая на то, что вируса в крови нет. Наличие позитивной реакции в острой стадии болезни говорит о ВЭБ-инфекции.
Если у ребенка имеется бессимптомное носительство ВЭБ или он находится в периоде инкубации острой инфекции, ПЦР отрицательный. Такой же результат будет при отсутствии вируса в организме. В начальных стадиях острой инфекции возможны как отрицательные, так и слабо-положительные результаты.
В стадии разгара, если это острая ВЭБ-инфекция, либо на фоне хронизации процесса, при реактивации вируса, при наличии атипичного течения ВЭБ – ПЦР-реакция дает положительный ответ. Если ребенок переболел несколько лет назад, вирус неактивен и есть к нему иммунитет – ПЦР даст отрицательную реакцию.
Спутать результаты могут вирусы герпеса 5 и 6-го типов, имеющиеся в крови, либо вирус ВИЧ или токсоплазма. Поэтому предварительно проводят анализы, которые исключают у ребенка все эти болезни.
У детей провести анализ на ВЭБ можно в слюне, моче или крови, зачастую проводят именно исследование крови и мочи, так как их легче всего собрать. При этом кровь дает наиболее точную информацию. Для того чтобы результаты были максимально точными и не пришлось повторно брать кровь у малыша, важно правильно подготовиться к исследованию. Все анализы крови берутся утром, до полудня и строго натощак.
Перед исследованием вечером не стоит давать ребенку жирную пищу, утром можно давать только воду. Кровь стоит забирать после 10-15 минутного отдыха, в спокойном состоянии.
За сутки до исследования стоит оградить ребенка от стрессов и тяжелых физических нагрузок, занятий спортом. Важно максимально отменить все принимаемые препараты за два дня до забора крови, если отменять препараты нельзя – важно сообщить названия принимаемых ребенком лекарств врачу-лаборанту. За полчаса до забора крови нужно давать ребенку больше пить кипяченой воды. После забора крови можно вести привычную жизнь.
Парецкая Алена, врач-педиатр, медицинский обозреватель
3,114 просмотров всего, 2 просмотров сегодня
источник
Эпштейн-Барр вирусная инфекция (ЭБВИ) является одной из распространенных заболеваний человека. По данным ВОЗ вирусом Эпштейн-Барр инфицировано около 55-60% детей раннего возраста (до 3х лет), подавляющее большинство взрослого населения планеты (90-98%) имеют антитела к ВЭБ. Заболеваемость в разных странах мира колеблется от 3-5 до 45 случаев на 100 тыс. населения и является довольно высоким показателем. ЭБВИ относится к группе неуправляемых инфекций, при которых нет специфической профилактики (вакцинации), что безусловно влияет на уровень заболеваемости.
Эпштейн-Барр вирусная инфекция – острое или хроническое инфекционное заболевание человека, вызываемое вирусом Эпштейн-Барр из семейства герпетических вирусов (Herpesviridae), обладающим излюбленной особенностью поражения лимфоретикулярной и иммунной систем организма.
Эпштейн-Барр вирус (ВЭБ) – это ДНК-содержащий вирус из Семейства Herpesviridae (гамма-герпесвирусы), является герпесвирусом 4 типа. Впервые выявлен из клеток лимфомы Беркетта около 35-40 лет назад.
Вирус имеет сферическую форму с диаметром до 180 нм. Структура состоит их 4х компонентов: сердцевины, капсида, внутренней и внешней оболочки. Сердцевина включает ДНК, состоящую из 2х нитей, включающих до 80 генов.
Вирусная частица на поверхности содержит также десятки гликопротеинов, необходимых для образования вируснейтрализующих антител. Вирусная частица содержит специфические антигены (белки, необходимые для диагностики):
— капсидный антиген (VCA);
— ранний антиген (ЕА);
— ядерный или нуклеарный антиген (NA или EBNA);
— мембранный антиген (MA).
Значимость, сроки их появления при различных формах ЭБВИ не одинакова и имеет свое специфическое значение.
Вирус Эпштейн-Барр относительно устойчив во внешней среде, быстро погибает при высыхании, воздействии высоких температур, а также действии распространенных дезинфицированных средств. В биологических тканях и жидкостях вирус Эпштейн-Барр способен благоприятно себя чувствовать при попадании в кровь у больного ЭБВИ, клетки головного мозга совершенно здорового человека, клетки при онкологических процессах (лимфома, лейкемия и другие).
Вирус обладает определенным тропизмом (склонностью поражать излюбленные клетки):
1) тропность к клеткам лимфоретикулярной системы (возникает поражение лимфатических узлов любых групп, увеличение печени и селезенки);
2) тропность к клеткам иммунной системы (вирус размножается в В-лимфоцитах, где может сохраняться пожизненно, в силу чего нарушается их функциональное состояние и возникает иммунодефицит); помимо В-лимфоцитов, при ЭБВИ нарушается и клеточное звено иммунитета (макрофаги, NK – натуральные киллеры, нейтрофилы и другие), что ведет к снижению общей сопротивляемости организма к различным вирусным и бактериальным инфекциям;
3) тропность к эпителиальным клеткам верхних дыхательных путей и пищеварительного тракта, в силу чего у детей может возникать респираторный синдром (кашель, одышка, «ложный круп»), диарейный синдром (послабление стула).
Вирус Эпштейн-Барр обладает аллергизирующими свойствами, что проявляется определенными симптомами у больных: 20-25% пациентов имеют аллергическую сыпь, у части больных может развиваться отек Квинке.
Особое внимание обращает на себя такое свойство вируса Эпштейн-Барр, как «пожизненная персистенция в организме». Благодаря инфицированию В-лимфоцитов данные клетки иммунной системы приобретают способность к неограниченной жизнедеятельности (так называемое «клеточное бессмертие»), а также постоянному синтезу гетерофильных антител (или аутоантител, например, антинуклеарные антитела, ревматоидный фактор, холодовые агглютинины). В этих клетках и живет ВЭБ постоянно.
В настоящее время известны 1 и 2 штаммы вируса Эпштейн-Барр, которые не отличаются серологически.
Источник инфекции при ЭБВИ – больной клинически выраженной формой и вирусоноситель. Больной становится заразным в последние дни инкубационного периода, начальный период болезни, разгар заболевания, а также весь период реконвалесценции (до 6 месяцев после выздоровления), причем до 20% переболевших сохраняют способность периодически выделять вирус (то есть остаются носителями).
Механизмы заражения ЭБВИ:
– это аэрогенный (воздушно-капельный путь передачи), при котором заразна слюна и слизь из ротоглотки, которая выделяется при чихании, кашле, разговоре, поцелуе;
— контактный механизм (контактно-бытовой путь передачи), при котором имеет место ослюнение предметов обихода (посуда, игрушки, полотенца и другое), однако в силу нестойкости вируса во внешней среде имеет маловероятное значение;
— допускается трансфузионный механизм заражения (при переливании инфицированной крови и ее препаратов);
— алиментарный механизм (водно-пищевой путь передачи);
— в настоящее время доказан трансплацентарный механизм инфицирования плода с возможностью развития врожденной ЭБВИ.
Восприимчивость к ЭБВИ: дети грудного возраста (до 1 года) болеют Эпштейн-Барр вирусной инфекцией редко благодаря наличию пассивного материнского иммунитета (материнские антитела), наиболее подвержены инфицированию и развитию клинически выраженной формы ЭБВИ – это дети с 2х до 10 лет.
Несмотря на многообразие путей заражения, среди населения имеется хорошая иммунная прослойка (до 50% детей и 85% взрослых): многие инфицируются от носителей без развития симптомов болезни, но с развитием иммунитета. Именно поэтому считается, что для окружения больного ЭБВИ заболевание малозаразно, поскольку многие уже имеют антитела к вирусу Эпштейна-Барр.
Редко в учреждениях закрытого типа (военные части, общежития) все же могут наблюдаться вспышки ЭБВИ, которые малоинтенсивны по выраженности, а также растянуты по времени.
Для ЭБВИ, а в частности наиболее ее частого проявления – мононуклеоза — характерна весеннее-осенняя сезонность.
Иммунитет после перенесенной инфекции формируется прочный, пожизненный. Заболеть повторно острой формой ЭБВИ нельзя. Повторные случаи заболевания связаны с развитием рецидива или хронической формы заболевания и его обострения.
Входные ворота инфекции – слизистая оболочка рото- и носоглотки, где происходит размножение вируса и организация неспецифической (первичной) защиты. На исходы первичного инфицирования влияют: общий иммунитет, сопутствующие заболевания, состояние входных ворот инфекции (есть или отсутствуют хронические заболевания рото- и носоглотки), а также инфицирующая доза и вирулентность возбудителя.
Исходами первичного заражения могут быть:
1) санация (уничтожение вируса во входных воротах);
2) субклиническая (бессимптомная форма);
3) клинически определяемая (манифестная) форма;
4) первично латентная форма (при которой репродукция вируса и выделение его возможны, а клинических симптомов нет).
Далее из входных ворот инфекции вирус проникает в кровь (виремия) – у больного может быть температура и интоксикация. На месте входных ворот формируется «первичный очаг» — катаральная ангина, затруднение носового дыхания. Далее происходит занос вируса в различные ткани и органы с преимущественным поражением печени, селезенки, лимфатических узлов и других. Именно в этот период в крови появляются «атипичные тканевые мононуклеары» на фоне умеренного увеличения лимфоцитов.
Атипичные мононуклеары в крови
Исходами болезни могут быть: выздоровление, хроническая ВЭБ – инфекция, бессимптомное носительство, аутоиммунные болезни (системная красная волчанка, ревматоидный артрит, синдром Шегрена и другие), онкологические заболевания, при онкологических заболеваниях и врожденной ВЭБ-инфекции – возможен летальный исход.
В зависимости от климата преобладают те или иные клинические формы ЭБВИ. В странах с умеренным климатом, к которым относится и Российская Федерация, чаще встречается инфекционный мононуклеоз, причем если нет дефицита иммунитета, то может развиться субклиническая (бессимптомная) форма болезни. Также вирус Эпштейн-Барр может явиться причиной возникновения «синдрома хронической усталости», аутоиммунных заболеваний (ревматические болезни, васкулиты, неспецифический язвенный колит). В странах же с тропическим и субтропическим климатом возможно развитие злокачественных новообразований (лимфосаркома Беркитта, назофарингеальная карцинома и другие), причем нередко с метастазами в различные органы. У ВИЧ-инфицированных пациентов ЭБВИ ассоциирована с возникновением волосатой лейкоплакии языка, лимфомы головного мозга и других проявлений.
В настоящее время клинически доказан факт прямой связи вируса Эпштейн-Барр с развитием острого мононуклеоза, хронической ЭБВИ (или ВЭБ-инфекции), врожденной ВЭБ-инфекции, «синдрома хронической усталости», лимфоидной интерстициальной пневмонии, гепатита, онкологических лимфопролиферативных заболеваний (лимфома Беркитта, Т-клеточная лимфома, назофарингеальная карцинома или НФК, лейомиосаркома, неходжинские лимфомы), ВИЧ-ассоциированных заболеваний («волосатая лейкоплакия», лимфома головного мозга, распространенные новообразования лимфоузлов).
1. Инфекционный мононуклеоз , который проявляется в виде острой формы болезни с цикличностью и специфическими симптомами (лихорадка, катаральная ангина, затруднение носового дыхания, увеличение групп лимфоузлов, печени, селезенки, аллергическая сыпь, специфические изменения в крови). Более подробно – см. в статье «Инфекционный мононуклеоз».
Неблагоприятные в плане развития хронической ВЭБ-инфекции признаки:
— затяжной характер течения инфекции (длительный субфебрилитет – 37-37,5° – до 3-6ти месяцев, сохранение увеличенных лимфатических узлов более 1,5-3х месяцев);
— возникновение рецидивов заболевания с возобновлением симптомов болезни в течение 1,5-3-4х месяцев после возникновения первичной атаки болезни;
— сохранение антител IgM (к EA, VCA антигенам ВЭБ) более 3х месяцев с момента начала заболевания; отсутствие сероконверсии (сероконверсия – исчезновение антител IgM и образование антител IgG в разным антигенам вируса Эпштейн-Барр);
— несвоевременно начатое или полностью отсутствующее специфическое лечение.
2. Хроническая ВЭБ-инфекция формируется не ранее, чем через 6 месяцев после перенесенной острой инфекции, а при отсутствии острого мононуклеоза в анамнезе – через 6 и более месяцев после инфицирования. Нередко латентная форма инфекции при снижении иммунитета переходит в хроническую инфекцию. Хроническая ВЭБ инфекция может протекать в виде: хронической активной ВЭБ-инфекции, гемофагоцитарного синдрома, ассоциированного с ВЭБ, атипичных форм ВЭБ (рецидивирующие бактериальные, грибковые и другие инфекции пищеварительной системы, дыхательных путей, кожи и слизистых оболочек).
Хроническая активная ВЭБ-инфекция характеризуется длительным течением и частыми рецидивами. Больных беспокоит слабость, повышенная утомляемость, чрезмерная потливость, длительная небольшая температура до 37,2-37,5°, кожные высыпания, иногда суставной синдром, боли в мышцах туловища и конечностей, тяжесть в правом подреберье, чувство дискомфорта в области горла, небольшой кашель и заложенность в носу, у некоторых пациентов неврологические расстройства – беспричинные головные боли, нарушения памяти, нарушения сна, частые смены настроения, склонность к депрессиям, больные невнимательны, снижение интеллекта. Нередко пациенты жалуются на увеличение одного или группы лимфоузлов, возможно увеличение внутренних органов (селезенка и печень).
Наряду с такими жалобами при расспросе больного выясняется наличие в последнее время частых простудных инфекций, грибковых заболеваний, присоединение других герпетических болезней (например, простой герпес на губах или половой герпес и другое).
В подтверждение клинических данных будут и лабораторные признаки (изменения крови, иммунного статуса, специфические анализы на антитела).
При выраженном снижении иммунитета при хронической активной ВЭБ-инфекции происходит генерализация процесса и возможно поражение внутренних органов с развитием менингита, энцефалита, полирадикулоневрита, миокардита, гломерулонефрита, пневмонии и других.
Гемофагоцитарный синдром, ассоциированный с ВЭБ проявляется в виде анемии иди панцитопении (снижение состава практически всех элементов крови, связанное с угнетением ростков кроветворения). У больных может наблюдаться лихорадка (волнообразная или перемежающаяся, при которой возможны как резкие, так и постепенные подъемы температура с восстановлением до нормальных величин), увеличение лимфоузлов, печени и селезенки, нарушение функции печени, лабораторные изменения в крови в виде снижение как эритроцитов, так и лейкоцитов и других элементов крови.
Стертые (атипичные) формы ЭБВИ: чаще всего это лихорадка неясного генеза длящаяся месяцами, годами в сопровождении с увеличением лимфоузлов, иногда суставными проявлениями, мышечными болями; другой вариант – это вторичный иммунодефицит с частыми вирусными, бактериальными, грибковыми инфекциями.
3. Врожденная ВЭБ-инфекция возникает при наличии острой формы ЭБВИ или хронической активной ВЭБ-инфекции, возникшей в период беременности матери. Характеризуется возможным поражением внутренних органов ребенка в виде интерстициальной пневмонии, энцефалита, миокардита и другими. Возможны недоношенность, преждевременные роды. В крови рожденного малыша могут циркулировать как материнские антитела к вирусу Эпштейн-Барр (IgG к EBNA, VCA, EA антигенам), так и явное подтверждение внутриутробного инфицирования – собственные антитела ребенка (IgM к EA, IgM к VCA антигенам вируса).
4. « Синдром хронической усталости » характеризуется постоянной усталостью, которая не проходит после продолжительного и полноценного отдыха. Для пациентов с синдромом хронической усталости характерны мышечная слабость, периоды апатии, депрессивные состояния, лабильность настроения, раздражительность, иногда вспышки гнева, агрессии. Пациенты вялые, жалуются на нарушение памяти, снижение интеллекта. Больные плохо спят, причем нарушается как фаза засыпания, так и наблюдается прерывистый сон, возможна бессонница и сонливое состояние в течение дня. Одновременно характерны вегетативные нарушения: дрожание или тремор пальцев рук, потливость, периодически небольшая температура, плохой аппетит, боли в суставах.
В группе риска трудоголики, лица с повышенной физической и умственной работой, лица, находящиеся как в острой стрессовой ситуации, так и в хроническом стрессе.
5. ВИЧ-ассоциированные заболевания
«Волосатая лейкоплакия» языка и слизистой ротовой полости появляется при выраженном
иммунодефиците, связанном чаще с ВИЧ-инфекцией. На боковых поверхностях языка, а также на слизистой оболочке щек, десен появляются белесоватые складки, которые постепенно сливаются, образуя белые бляшки с неоднородной поверхностью, будто покрытые бороздами, образуются трещины, эрозивные поверхности. Как правило, болевых ощущений при данном заболевании нет.
Волосатая лейкоплакия языка
Лимфоидная интерстициальная пневмония является полиэтиологическим заболеванием (имеется связь с пневмоцистами, а также и с ВЭБ) и характеризуется одышкой, малопродуктивным кашлем
на фоне температуры и симптомов интоксикации, а также прогрессирующей потери веса больных. У больного увеличение печени и селезенки, лимфатических узлов, увеличение слюнных желез. При рентгенологическом исследовании двусторонние нижнедолевые интерстииальные очаги воспаления легочной ткани, корни расширены, неструктурны.
6. Онкологические лимфопролиферативные заболевания (лимфома Беркитта, назофарингеальная карцинома – НФК, Т-клеточная лимфома, неходжинская лимфома и другие)
1. Предварительный диагноз всегда выставляется на основании клинико-эпидемиологических данных. Подозрение на ЭБВИ подтверждают клинические лабораторные анализы, в частности общий анализ крови, по которому можно выявить косвенные признаки вирусной активности: лимфомоноцитоз (увеличение лимфоцитов, моноцитов), реже моноцитоз при лимфопении (увеличение моноцитов при снижении лимфоцитов), тромбоцитоз (увеличение тромбоцитов), анемия (снижение эритроцитов и гемоглобина), появление атипичных мононуклеаров в крови.
Атипичные мононуклеары (или вироциты) – это видоизмененные лимфоциты, которые по морфологическим признакам имеют некоторое сходство с моноцитами. Это одноядерные клетки, являются молодыми клетками, появляются в крови с целью борьбы с вирусами. Именно последнее свойство объясняет их появление при ЭБВИ (особенно при острой ее форме). Диагноз инфекционного мононуклеоза считается подтвержденным при наличии атипичных мононуклеаров в крови более 10%, однако их количество может колебаться от 10 до 50 и более %.
Для качественного и количественного определения атипичных мононуклеаров применяется метод концентрации лейкоцитов, который является высокочувствительным методом.
Сроки появления: Атипичные мононуклеары появляются в первые дни болезни, в разгар заболевания их количество бывает максимальным (40-50% и более), у части пациентов их появление фиксируется спустя неделю после начала болезни.
Продолжительность их обнаружения: у большинства пациентов атипичные мононуклеары продолжают выявляться в течение 2-3х недель с момента начала болезни, у части больных – исчезают к началу 2й недели заболевания. У 40% пациентов в крови продолжается обнаружение атипичных мононуклеаров до месяца и более (в этом случае имеет смысл проводить активную профилактику хронизации процесса).
Также на стадии предварительного диагноза проводят биохимическое исследование сыворотки крови, в котором есть признаки поражения печени (небольшое увеличение билирубина, повышение активности ферментов – АЛТ, АСТ, ГГТП, тимоловой пробы).
2. Окончательный диагноз выставляется после специфических лабораторных исследований.
1) Гетерофильный тест – обнаружение гетерофильных антител в сыворотке крови, выявляются у подавляющего большинства больных ЭБВИ. Является дополнительным методом диагностики. Гетерофильные антитела вырабатываются в ответ на заражение ВЭБ – это аутоантитела, которые синтезируются инфицированными В-лимфоцитами. К ним относятся антинуклеарные антитела, ревмофактор, холодовые агглютинины. Они относятся к антителам класса IgM. Появляются в первые 1-2 недели с момента заражения, причем характерно постепенное повышение их в течение первых 3-4х недель, затем постепенно снижение в последующие 2 месяца и сохранение в крови весь период реконвалесценции (3-6 месяцев). Если при наличии симптомов ЭБВИ данный тест отрицательный, то рекомендуется повторить его через 2 недели.
Ложноположительный результат на гетерофильные антитела могут дать такие состояния, как гепатиты, лейкоз, лимфома, употребление наркотических средств. Также положительными антитела данной группы могут быть при: системной красной волчанке, криоглобулинемии, сифилисе.
2) Серологические исследования на антитела к вирусу Эпштейн-Барр методом ИФА (иммуноферментный анализ).
• IgM к VCA (к капсидному антигену) – выявляются в крови в первые дни и недели болезни, максимальны к 3-4й недели заболевания, могут циркулировать до 3х месяцев, а потом их количество снижается до неопределяемой величины и исчезает совсем. Сохранение их более 3х месяцев указывает на затяжное течение болезни. Обнаруживаются у 90-100% больных с острой ЭБВИ.
• IgG к VCA (к капсидному антигену) – появляются в крови спустя 1-2 месяца от начала болезни, затем постепенно снижается и сохраняется на пороговом (низком уровне) пожизненно. Повышение их титра характерно для обострения хронической ЭБВИ.
• IgM к EA (к раннему антигену) – появляется в крови в первую неделю заболевания, сохраняется в течение 2-3х месяцев и исчезает. Обнаруживается у 75-90% больных. Сохранение в высоких титрах длительной время (более 3-4х месяцев) тревожно в плане формирования хронической формы ЭБВИ. Появление их при хронической инфекции служит индикатором реактивации. Нередко могут выявляться при первичном инфицировании у носителей ВЭБ.
• IgG к ЕA (к раннему антигену) – появляются к 3-4й недели заболевания, становятся максимальными на 4-6 недели болезни, изчезают через 3-6 месяцев. Появление высоких титров повторно указывает на активацию хронической инфекции.
• IgG к NA-1 или EBNA (к нуклеарному или ядерному антигену) – являются поздними, поскольку появляются в крови через 1-3 месяца после начала заболевания. Продолжительное время (до 12 мес) из титр достаточно высокий, а затем титр снижается и сохраняется на пороговом (низком) уровне пожизненно. У детей раннего возраста (до 3-4х лет) данные антитела появляются поздно – спустя 4-6 месяцев после инфицирования. Если у человека выраженный иммунодефицит (стадия СПИД при ВИЧ-инфекции, онкологические процессы и другое), то данных антител может и не быть. Реактивация хронической инфекции или рецидив острой ЭБВИ наблюдается при высоких титрах IgG к NA антигену.
Схемы расшифровки результатов
 |
| Рис. 1. Схема комплексной терапии Эпштейна-Барр вирусной инфекции у детей |
В течение нескольких лет для лечения ЭБВИ мы с успехом применяем схему комбинированной этапной этиотропной терапии, в которую входят инозин пранобекс (Изопринозин) и рекомбинантный интерферон α-2β (Виферон) (рис. 1, 2). Инозин пранобекс (Изопринозин) подавляет синтез вирусных белков и тормозит репликацию широкого спектра ДНК- и РНК-содержащих вирусов, в том числе ВЭБ [3]. Препарат обладает иммунокорригирующей активностью — модулирует иммунный ответ по клеточному типу, стимулирует продукцию Ат, цитокинов, ИФН, повышает функциональную активность макрофагов, нейтрофилов и NK-клеток; предохраняет пораженные клетки от поствирусного снижения синтеза белка. Инозин пранобекс (Изопринозин) назначался по 50–100 мг/кг/сут внутрь в 3–4 приема. Проводили три курса лечения по 10 дней с интервалом 10 дней. Рекомбинантный ИФН α-2β (Виферон) тормозит репликацию вирусов за счет активации эндонуклеазы, разрушения вирусной матричной РНК [6]. Препарат модулирует иммунный ответ, способствует дифференцировке В-лимфоцитов, стимулирует выработку цитокинов, повышает функциональную активность макрофагов, нейтрофилов и NK-клеток. Входящие в его состав природные антиоксиданты (витамины Е и С) стабилизируют клеточные мембраны. Препарат назначали по пролонгированной схеме (В. В. Малиновской и соавт., 2006) [6].
Эффективность этиотропной терапии ОЭБВИ оценена в двух группах больных. Пациенты 1-й группы (52 человека) получали инозин пранобекс (Изопринозин) в сочетании с рекомбинантным ИФН α-2β (Вифероном), больные 2-й группы (57 детей) — монотерапию рекомбинантным ИФН α-2β (Вифероном). Клинико-серологические показатели до начала лечения и через 3 мес терапии представлены в табл. 1. У пациентов обеих групп в динамике отмечалось достоверное уменьшение таких симптомов, как генерализованная лимфаденопатия, тонзиллит, аденоидит, гепатомегалия и спленомегалия. Вместе с тем на фоне комбинированной терапии, положительная динамика клинических показателей была более значительной; острые респираторные инфекции (ОРИ) лишь у 19,2% больных 1-й группы и у 40,3% больных 2-й группы (p Рис. 2. Механизмы этиопатогенетического действия комбинации инозина пранобекса (Изопринозина) и рекомбинантного интерферона α-βb (Виферона) при Эпштейна-Барр вирусной инфекции у детей
Комбинированная терапия при ОЭБВИ способствовала модуляции иммунного ответа по клеточному типу (увеличение CD3-, CD4-, CD8-, CD16- и HLA-DRT-лимфоцитов). Снижалась готовность иммунокомпетентных клеток к апоптозу (CD95). Отмечались стимуляция выработки IgA, переключение синтеза Ат с IgM на IgG, снижение содержания ЦИК, улучшались показатели метаболизма нейтрофилов.
Эффективность этиотропной терапии исследована у 60 больных ХЭБВИ. Пациенты 1-й группы (30 детей) получали инозина пранобекс (Изопринозин) и рекомбинантный ИФН α-2β (Виферон), 2-я группа (30 человек) — монотерапию рекомбинантным ИФН α-2β (Вифероном). Независимо от схемы лечения через 3 мес после начала терапии отмечалось достоверное уменьшение частоты генерализованной лимфаденопатии, гипертрофии небных и глоточной миндалин, спленомегалии, интоксикационного, инфекционного и вегето-висцерального синдромов (табл. 2). Комбинация инозина пранобекса (Изопринозина) с рекомбинантным ИФН α-2β (Вифероном) способствовало более существенной динамике клинических показателей. Количество эпизодов ОРИ снизилось с 6–11 (7,9 ± 1,1) до 4–6 (5,2 ± 1,2) в год на фоне монотерапии рекомбинантным ИФН α-2β (Вифероном), и до 2–4 (2,5 ± 1,4) в год на фоне комбинированной терапии (p
Э. Н. Симованьян, доктор медицинских наук, профессор
В. Б. Денисенко, кандидат медицинских наук
Л. Ф. Бовтало, кандидат медицинских наук
А. В. Григорян
Ростовский ГМУ, Ростов-на-Дону
источник