Костная денситометрия у детей или детская денситометрия проводится с целью оценки состояния костной ткани, контроля развития скелета и минерализации кости, определения индивидуального риска переломов, оценки костной массы у детей с переломами и динамического наблюдения за эффективностью проводимой терапии.
Показания для денситометрии у детей определяет врач (эндокринолог, ревматолог, травматолог и т.д.) Наиболее частыми показаниями являются:
- систематический продолжительный прием глюкокортикостероидов,
- хроническая патология, обусловленная нарушением прцессов всасывания, воспалительными заболеваниями кишечника, нервной анорексией, муковисцидозом;
- ревматические болезни;
- хроническая почечная недостаточность (ХПН),
- хроническая обструктивная болезнь легких (ХОБЛ),
- бронхиальная астма, дефицит мышечной массы и маленький скелет,
- дефицит гормона роста,
- первичный или вторичный гипогонадизм,
- продолжительная иммобилизация,
- несовершенный остеогенез и другие наследственные заболевания (синдром Элерса-Данлоса, синдром Марфана и др.)
- переломы в анамнезе: − компрессионные переломы позвонков, − два и более переломов трубчатых костей, − один и более периферических переломов при минимальной нагрузке.
Диагноз «остеопения и остеопороз» у детей не может устанавливаться на основании только денситометрии.
Предпочтительными зонами для денситометрии являются поясничные позвонки и программа «все тело» (для оценки «костной массы» у детей проводится денситометрия поясничного отдела позвоночника, «кортикальной кости» по программе «все тело»).
Заключение «низкая костная минеральная плотность по отношению к хронологическому возрасту» может быть сделано только при Z-критерии ≤ -2.0 SD.
Значения минеральной плотности кости (МПК) для прогноза переломов у детей точно не определено.
Динамику «костной массы» необходимо проводить на одном и том же приборе.
Клинический диагноз «остеопороз» у детей на основании только денситометрических критериев не устанавливается!
Исследование выполняется за относительно короткое время и с минимальными лучевыми нагрузками. Дозы для всех точек сканирования (позвоночник, бедро, предплечье, все тело) незначительны, ниже естественного фонового излучения (в Великобритании, например ,естественное фоновое излучение составляет от 6 до 20 микроЗиверта (мЗ)). Эффективная доза колеблется от 0.4 (мЗ) при сканировании поясничных позвонков до 5.4 (мЗ) при сканировании всего тела. Лучевая нагрузка при рентгенографии грудной клетки — 20 (мЗ), трансатлантический перелет добавляет нам — 40 (мЗ).
Очень важна психологическая подготовка ребенка к исследованию.Соответственно возрасту ребенка ему необходимо рассказать о важности и необходимости исследования, о том как оно будет проводиться и будет ли при этом страшно и больно. Исследование абсолютно безболезнено и, единственное, что требуется от маленького пациента — это неподвижность в течение некоторого времени, с тем чтобы избежать ненужного дополнительного облучения при повторении скана, если он выполнен неправильно.
Подготовка ребенка для денситометрии проходит по тем же основным принципам, что и у взрослых. Необходимо снять любые металлические предметы, которые могут давать артефакты, например одежда с молнией или пряжкой. Для достижения максимального качества скана рекомендуется, чтобы ребенок был в легкой одежде. В процессе сканирования оператор будет информировать ребенка о том, что происходит, когда работает сканер, о шуме который он издает, и сколько времени будет занимать сканирование.
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Для биохимической оценки минеральной плотности кости существуют следующие методы исследований:
- характеристика фосфорно-кальциевого обмена;
- определение биохимических маркёров ремоделирования кости.
При оценке биохимических показателей обязательны рутинные методы исследования — определение содержания кальция (ионизированной фракции) и фосфора крови, суточной экскреции кальция и фосфора с мочой, а также экскреции кальция с мочой натощак по отношению к концентрации креатинина в этой же порции мочи.
Большое количество исследований, посвященных остеопорозу в детском возрасте, доказывает, что чаще всего рутинные биохимические показатели фосфорно-кальциевого обмена не изменены или меняются незначительно и кратковременно даже при выраженном остеопорозе с переломом.
Высокоспецифичные, чувствительные методы диагностики остеопороза — определение уровня паратгормона, кальцитонина, активных метаболитов витамина D в крови. Данные методы имеют строгие показания для их использования и в практической медицине ещё не получили широкого распространения. Паратгормон определяют при подозрении на гиперпаратиреоз (первичный или вторичный) как причину остеопороза; активные метаболиты витамина D — для диагностики генетической остеомаляции витамин D-зависимого рахита.
Для определения состояния костного ремоделирования в крови и моче исследуют высокочувствительные биохимические маркёры костного метаболизма. При патологической ситуации они отражают преобладание нарушенной функции костеообразования или костной резорбции. К маркёрам костеобразования относят общую щелочную фосфатазу (в большей степени её костный изофермент), пропептид человеческого коллагена I типа, остеокальцин. Последний показатель считают наиболее информативным. Маркёры резорбции костной ткани — тартрат-резистентная кислая фосфатаза крови, оксипролин, коллагеновые перекрёстные группы
Биохимические маркёры костного ремоделирования
Показатели активности костеобраэования
Показатели активности резорбции кости
Активность щелочной фосфатазы (кровь): общая щелочная фосфатаза костная щелочная фосфатаза
Коллагеновые перекрёстные группы (cross-links): пиридинолин (моча); дезоксипиридинолин (моча)
Н-концевой телопептид (моча)
Пропептид человеческого коллагена I типа (кровь)
Определение биохимических маркёров костного метаболизма важно не только для характеристики костного обмена, но и для выбора препарата, повышающего минеральную плотность кости, контроля за эффективностью терапии, оптимальной профилактики остеопороза.
Наиболее доступный метод инструментальной диагностики остеопороза — визуальная оценка рентгенограмм костей (при глюкокортикоидном остеопорозе — костей позвоночника).
Характерные рентгенологические признаки снижения минеральной плотности кости:
- повышение «прозрачности», изменение трабекулярного рисунка (исчезновение поперечных трабекул, грубая вертикальная трабекулярная исчерченность);
- истончение и повышенная контрастность замыкательных пластинок;
- снижение высоты тел позвонков, их деформация по типу клиновидных или «рыбьих» (при выраженных формах остеопороза).
Однако при анализе рентгенографических снимков невооружённым глазом практически невозможно количественно оценить минеральную плотность костной ткани. Деминерализация кости может быть выявлена при рентгенографии в случае уменьшения плотности не менее чем на 30%. Рентгенографические исследования имеют большое значение при оценке деформаций и компрессионных изменений позвонков.
Более точны количественные методы оценки костной массы (денситометрия, от английского слова density — «плотность»). Денситометрия позволяет выявить костные потери на ранних стадиях с точностью до 2-5%. Различают ультразвуковые, а также рентгеновские и изотопные методы (моно- и двухэнергетическая денситометрия, моно- и двухфотонная абсорбциометрия, количественная КТ).
Рентгеновские методы костной денситометрии основаны на передаче рентгеновских лучей из наружного источника через кость к детектору. Узкий пучок рентгеновских лучей направляют на измеряемый участок кости. Интенсивность пропущенного через кость пучка регистрируют детекторной системой.
Основные показатели, определяющие минеральную плотность костной ткани:
- минеральное содержание кости, выраженное в граммах минерала в исследуемом участке;
- минеральная плотность кости, которую рассчитывают на диаметр кости и выражают в г/см 2 ;
- Z-критерий, выраженный в процентах от половозрастного норматива и в величинах стандартного отклонения (standard deviation) от сред нетеоретической нормы (SD, или сигма).
Первые 2 критерия — абсолютные показатели плотности кости исследуемого участка, Z-критерий — относительная величина. У детей и подростков используют только этот относительный показатель денситометрии.
У взрослых пациентов помимо Z-критерия рассчитывают Т-критерий, который выражают в процентах от пика костной массы у лиц соответствующих пола и расы в возрасте 40 лет (когда минеральный состав кости считают оптимальным), а также в величинах стандартного отклонения. Этот показатель — основной для оценки степени выраженности деминерализации кости по критериям ВОЗ у взрослых.
Оба критерия (Z- и Т-) выражают в цифрах со знаками (+) или (-). Величину сигмы от -1 до -2,5 трактуют как остеопению, что требует обязательного профилактического лечения и мониторинга, так как существует реальная опасность переломов.
При снижении костной плотности до значений, превышающих стандартное отклонение более чем на 2,5, риск переломов возрастает — состояние трактуют как остеопороз. При наличии перелома (переломов) и изменении Z-критерия, превышающего стандартное отклонение более чем на 2,5 (например, -2,6; -3,1 и так далее) констатируют тяжёлый остеопороз .
Диагностические «инструментальные» категории снижения минеральной плотности костной ткани
От -2,5 или меньше без переломов
От -2,5 или меньше с переломами
Все приборы вычисляют Z- и Т-критерии в процентах и величинах стандартного отклонения от нормативных показателей сигмы.
Согласно более поздним исследованиям МПКТ у детей (2003), были предложены другие денситометрические критерии оценки костной плотности. Констатировать «низкую костную плотность в соответствии с возрастом» или «ниже ожидаемых показателей для возрастной группы» следует при Z-критерии менее -2,0 SD (например, -2,1; -2,6 SD и т.д.).
Монофотонные и моноэнергетические денситометры удобны для скрининговых исследований, контроля лечения, но они могут определять минеральную костную плотность только в периферических отделах скелета (например, в лучевой кости). С помощью данного метода невозможно оценить костную массу в проксимальном отделе бедра, позвонках. Намного шире возможности двухфотонных и двухэнергетических костных денситометров.
Моно- и двухэнергетические (рентгеновские) денситометры обладают преимуществом перед фотонными, так как не требуют замены источника изотопов, обладают большой разрешающей способностью, имеют меньшую лучевую нагрузку.
Количественная КТ позволяет определить и измерить кортикальный и губчатый слои кости, представить истинную костную плотность. Точность метода высокая, однако лучевая нагрузка значительно превышает таковую при вышеописанных методах.
Ультразвуковая костная денситометрия основана на измерении скорости распространения ультразвуковой волны в кости. В основном её используют в качестве скрининг-метода.
Какую же костную область должен выбрать педиатр для наиболее информативного денситометрического исследования? Строгих рекомендаций не существует. Выбор участка измерения зависит от ряда факторов. Потеря костной массы происходит во всех участках скелета, но неравномерно. Целесообразно исследовать те кости, которые имеют больший риск перелома. Чаще рентгеновскую денситометрию проводят в области проксимальных отделов бедренных костей и поясничного отдела позвоночника. Это обусловлено тем, что потери костной массы гетерогенны и между 2 точками определения существуют различия, требующие проведения 2 исследований одновременно.
Поскольку глюкокортикостероидная терапия в большей степени влияет на МПКТ позвоночника, чем бедренной кости или предплечья, для ранней диагностики остеопороза и оценки эффективности его лечения целесообразно применять рентгеновскую двухэнерге-тическую денситометрию поясничных позвонков. Несмотря на использование в клинической практике, денситометрию костей предплечья не считают общепризнанным методом, данные которого достаточны для окончательной постановки диагноза остеопороза.
Денситометрия выявляет наиболее достоверный фактор риска возникновения переломов — сниженную МПКТ. Именно поэтому её определение необходимо включать в перечень инструментальных исследований при подозрении на остеопороз, при этом предпочтительнее использовать двухэнергетическую денситометрию костей позвоночника.
Согласно международным рекомендациям, определение МПКТ (позвоночник, проксимальный отдел бедренной кости) с помощью методов костной денситометрии следует проводить всем взрослым пациентам, которым планируется лечение ГК в дозе более 7,5 мг/сут в течение более 6 мес. Пациентам, не получающим терапию остеопороза, денситометрию следует повторять через каждые 6 мес, а у получающих это лечение — не реже 1 раза в год. Данные рекомендации с некоторыми изменениями можно перенести на детский контингент.
По мере накопления исследовательского материала, посвященного остеопорозу, выяснилось, что возможны ситуации, когда в результате лечения остеопороза происходит увеличение МПКТ, однако частота переломов остаётся такой же высокой. Или наоборот, МПКТ не увеличивается, несмотря на специфическую терапию, при этом частота переломов достоверно уменьшается. Предполагают, что это может быть связано с изменением качества (микроархитектоники) кости, что невозможно протестировать современными методиками. Именно поэтому некоторые авторы называют денситометрию «суррогатным» методом определения фактора риска возникновения переломов, несмотря на специфичность и большую чувствительность этого исследования.
Тем не менее костная денситометрия остаётся наиболее ценным инструментальным методом диагностики остеопороза и профилактики переломов. Наиболее распространена классификация остеопороза ВОЗ, основанная на оценке денситометрического Т-критерия (для детей — Z-критерия).
В программное обеспечение костных денситометров включены нормативные показатели плотности костной ткани различных участков скелета в зависимости от пола и возраста, расы, рассчитанные на основе проведения больших популяционных исследований. На территории России денситометрические программы рассчитаны для обследования детей с 5-летнего возраста. Провести денситометрию у ребёнка моложе 5 лет невозможно, а с 5-летнего возраста допустимо только на аппарате, имеющем данную возрастную программу.
В ряде педиатрических исследований особое внимание было уделено анализу показателей МПКТ с учётом костного возраста и стадии пубертата по Tanner. При последующем пересчёте результатов обследования с учётом вышеуказанных показателей были получены значимые отличия. Это связано с нередким несоответствием биологического и паспортного возраста ребёнка, имеющего остеопороз.
Унифицированных рекомендаций относительно денситометрических исследований у детей не существует.
Показаниями для проведения рентгеновской двухэнергетической абсорбционной денситометрии в детском возрасте могут быть:
- перелом (переломы), возникший при падении с высоты роста без ускорения;
- терапия глюкокортикостероидами препаратами более 2 мес;
- наличие факторов риска развития остеопороза;
- контроль терапии остеопороза (не ранее чем через 1 год от начала лечения).
Дифференциальная диагностика остеопороза у детей не представляет больших трудностей. При наличии клинических симптомов (см. выше) для подтверждения остеопороза необходимы инструментальные методы исследования (денситометрия, в крайнем случае — рентгенография костей позвоночника), в противном случае диагноз подтвердить невозможно. При инструментальном выявлении сниженной МПКТ диагноз остеопороза очевиден, необходимо лишь решить вопрос о том, является ли остеопороз синдромом или основным заболеванием.
У детей раннего возраста остеопороз приходится дифференцировать с остеомаляцией, для которой характерны только деминерализация и размягчение костей без выраженного изменения белкового синтеза в матриксе. Основа остеомаляции — повышенное количество неминерализованной остеоидной ткани.
Классический пример остеомаляции — поражение костной системы при минералодефицитном рахите (в период разгара), гораздо реже — при заболевании из группы генетических остеомаляций. При рахите клинические проявления включают в зависимости от возраста изменение формы черепа (краниотабес, уплощение костей черепа, наличие лобных и теменных бугров), О-образное искривление ног, мышечную гипотонию. Рутинные лабораторные исследования выявляют снижение уровня фосфора (реже кальция), повышение уровня щелочной фосфатазы крови. Для остеопороза подобные биохимические изменения не характерны.
При значительном снижении минеральной плотности костной ткани неясного происхождения большое значение в дифференциальной диагностике имеют биопсия костной ткани, гистологическое и гистоморфометрическое исследования. Однако применение этого метода ограничено (особенно у детей в России) как по причине инвазивности и травматичности, так и из-за недостаточного количества патоморфологических лабораторий со специальным оборудованием для гистоморфометрии.

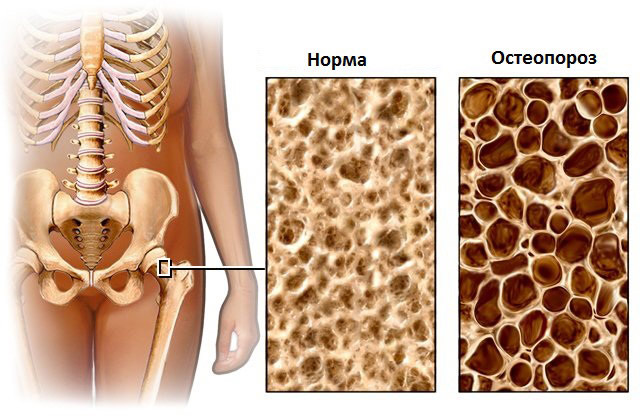
Остеопороз у пожилых людей — заболевание скелета, проявляющееся снижением костной массы и микроструктурным повреждением костной ткани, приводящим к повышению ломкости кости и, вследствие этого, к повышению риска перелома.
источник
Указанная манипуляция на сегодняшний день является наиболее информативным средством выявления остеопороза на ранних его стадиях. Денситометрия считается безопасной процедурой: противопоказаний к ее проведению практически нету, а какие-либо побочные эффекты и осложнения после ее завершения отсутствуют.
Обследованию подлежат наиболее важные участки скелета, благодаря которым можно предугадать развитие негативных состояний в будущем: бедренная кость, предплечье и позвоночный столб.
- Рентгенологический. Для изучения структуры костной ткани применяют два типа рентген-лучей. Благодаря сопоставлению сведений поглощения излучаемой энергии доктор оценивает уровень отклонения от нормы плотности кости. Указанная манипуляция отнимает минимум времени, а доза облучения в 400 раз меньше, нежели при стандартной рентгенографии. К данному виду денситометрии обращаются, когда нужно изучить костную ткань тазобедренного сустава, плеча, предплечья, пояснично-крестцовой зоны позвоночника, либо всего позвоночного столба.
- Ультразвуковой . В силу отсутствия какой-либо лучевой нагрузки указанная методика считается абсолютно безопасной. Ее можно использовать в отношении детей, а также беременных женщин. Однако результативность данной манипуляции более низкая, чем у рентгенологической денситометрии. Ее принцип основан на исчислении скорости, с которой УЗИ-волны распространяются по костным структурам. Плотность кости прямо пропорциональна скорости поглощения лучей костной тканью. При значительных потерях костной массы назначается рентгенологическая денситометрия. С ее помощью возможно получить информацию об эластичности, прочности кортикального слоя, а также толщине отдельных микроструктур.
- Количественная компьютерная томография . Дает возможность получить трехмерную картинку структурной плотности костных элементов. Так как радиационная нагрузка при данной методике весьма существенна, ее на практике применяют очень редко.
В связи со снижением уровня кальция в костях, рассматриваемый метод диагностики назначают людям после достижения ими 50-летнего возраста. Именно в этом возрасте есть большая вероятность появления остеопороза, который, согласно статистическим данным, занимает третье место по смертности.
- Женщины, у которых климакс наступил в раннем возрасте (до 45 лет).
- Ярко-выраженная худоба.
- Наличие остеопороза у ближайших родственников.
- Дефицит кальция и/или витамина Д в ежедневном рационе.
- Малоподвижный образ жизни.
- Табакокурение.
- Сбои в гормональном фоне.
- Злоупотребление алкогольными напитками.
- Лечение кортикостероидами.
- Период вынашивания ребенка (для рентгенологической денситометрии).
- Деформации в пояснично-крестцовой секции позвоночника, которые препятствуют больному в принятии правильного положения тела во время обследования.
- Проведение диагностики с применением бариевого контраста менее чем за неделю до указанной манипуляции.
Рассматриваемый вид обследования не требует специфической подготовки.
- Препараты, содержащие кальций, могут исказить результаты диагностики, поэтому за сутки до денситометрии от них следует полностью отказаться.
- О существовании кардиостимулятора либо металлического имплантата доктора нужно осведомить заблаговременно.
- Врача необходимо проинформировать о проведении в недавнем времени следующих манипуляций:
— Компьютерной томографии.
— Рентгенологическом обследовании.
— Диагностических мероприятий с применением контрастных веществ.
Перед денситометрией пациента просят снять с себя все металлические предметы: цепочки, кольца, очки и т.д. Их наличие может исказить результаты диагностики.
Стационарные
Пациент в этом случае ложится на специальный стол с выпрямленными ногами. Для изучения состояния нижней зоны позвоночника, под ноги пациента устанавливают подставку таким образом, чтобы икры располагались параллельно кушетке.
Источник излучения проходит над пациентом. Рентгеновские лучи попадают на детектор, измеряющий поглощение лучей костной тканью. Полученные данные попадают в компьютер, подвергаются обработке, и результаты денситометрии появляются на мониторе.
Пациент в это время не должен двигаться. В некоторых случаях врач может попросить задержать дыхание на несколько секунд.
Указанная процедура, в среднем, занимает 10-20 минут.
При проведении стандартного обследования рентгенолог изучает структуру шейки бедренной кости, пояснично-крестцовую зону позвоночника, а также лучевую кость.
Моноблочные
Те части тела, которые подлежат обследованию (пальцы, ступни, руки, предплечье) размещают в специальной нише.
На протяжении трех минут можно получить результат.
При ультразвуковой денситометрии можно обследовать лишь мелкие участки кости: фаланги пальцев, пятки, запястья и т.д.
На исследуемую зону доктор предварительно наносит специальный гель, который обеспечивает более легкое скольжение ультразвукового датчика.
Результаты обследования выводятся на монитор.
Расшифровку результатов осуществляет рентгенолог. С полученным заключением пациенту необходимо идти к ревматологу, либо ортопеду.
Обозначает минеральную плотность костной ткани пациента, в сравнении со стандартом плотности ткани у молодых людей.
Данный показатель применяют также для оценивания риска получения перелома кости.
- Если в бланке заключения указана цифра в промежутке между «+2» и «-0,9», это свидетельствует об отсутствии дегенеративных процессов в исследуемом участке.
- При варьировании результатов исследования в пределах от «-1» до «-2,5» доктор диагностирует остеопению.
- Значение указанного показателя ниже «-2,5» — следствие прогрессирования остеопороза с высокой вероятностью получения переломов при малейших травмированиях.
Полученный в ходе исследования результат сравнивают со средним показателем плотности костной массы среди людей идентичной с пациентом возрастной группы, пола и расы. Итогом произведенных расчетов и является указанный Z-балл.
Уменьшение данного критерия свидетельствует о сниженной минеральной плотности костных структур пациента.
Цена денситометрии в клиниках России – куда обращаться, чтобы выполнить обследование плотности костных тканей?
Рассматриваемую диагностику специалисты советуют проходить каждые два года.
- Качества оборудования, на котором проводится денситометрия.
- Авторитета медицинского учреждения.
- Методики осуществления диагностики.
В Москве данный тип обследования можно пройти по 70 адресам.
- Цена в столице стартует от 800 рублей.
- В среднем же, диагностика 1-го отдела позвоночника будет стоить 1200-2500 рублей.
- Если необходимо изучить состояние всего скелета, нужно рассчитывать на минимальную сумму 5000-7000 рублей.

Каждый человек – даже, если он темнокожий — должен ежемесячно проверять свою собственную кожу. Нужно проводить полное обследование кожи каждый месяц перед зеркалом, в уединении, полностью раздеваясь (например, до или после ванны) при ярком естественном солнечном свете или при хорошем … Читать далее → →
Артроскопия (артроскопическая хирургия, артроскопическое исследование, эндоскопия суставов, артроскопия суставов колена и плеч, исследование волоконно-оптического сустава) — это минимально инвазивная процедура, которая используется, чтобы диагностировать и лечить заболевания суставов. Медицинский работник может напрямую просматривать внутреннюю структуру сустава при помощи инструмента, называемого … Читать далее → →
источник
В связи с чем выявление причин остеопении и ее коррекция приобретают особую актуальность в детском возрасте? Каковы причины возникновения остеопении у детей? Минеральная плотность кости (МПК) является одним из важнейших факторов, определяющих ее прочн
В связи с чем выявление причин остеопении и ее коррекция приобретают особую актуальность в детском возрасте?
Каковы причины возникновения остеопении у детей?
Минеральная плотность кости (МПК) является одним из важнейших факторов, определяющих ее прочность.
МПК измеряется несколькими абсолютными показателями:
- BMC — содержание минерала в кости (г);
- BMD — содержание минерала на 1 кв. см сканируемой поверхности (г/кв. см);
- BMD (v); содержание минерала в 1 кв. см костной ткани (г/ куб. см).
В 1994 году рабочей группой ВОЗ было решено диагностировать снижение МПК на основании универсального критерия, выраженного в единицах стандартного отклонения (SD), единого для всех методов костной денситометрии.
Для взрослых это так называемый T-критерий (определяется как отношение фактической костной массы обследуемого к пиковой костной массе молодых здоровых людей того же пола, рассчитанное в процентах и единицах стандартного отклонения).
У детей используется Z-критерий. Показатель Z-score рассматривается как величина стандартного отклонения фактической плотности кости по отношению к соответствующему средневозрастному показателю. Значения Z-score до -1SD рассматриваются как норма, от -1SD до -2,5 SD — как остеопения и более -2,5 SD — как остеопороз.
Снижение минеральной плотности кости клинически идентифицируют как остеопению или остеопороз (ОП).
Терапевты уже давно рассматривают остеопороз как грозную «неинфекционную эпидемию» нового века.
По данным большинства публикаций, ОП страдают от 2 до 16% взрослого населения в мире.
Распространенность остеопороза, тяжесть исходов заболевания, высокая смертность, особенно при переломах бедра, частая потеря способности к самообслуживанию и снижение качества жизни дали основание отнести ОП к числу наиболее значимых в медико-социальном плане болезней человека.
Появление высокоточных и безопасных методов остеоденситометрии позволило в последние годы получить данные о значительной распространенности (около 40%) остеопенического синдрома в детской популяции. Так, среди более чем 400 обследованных в НЦЗД РАМН детей в возрасте от 5 до 18 лет, не имеющих гепатита, тиреотоксикоза, симптомов мальабсорбции и сахарного диабета, снижение МПК выявлено в среднем у 38-43% человек.
Более того, по данным литературы, снижение показателей МПК часто встречается и у новорожденных, особенно у маловесных детей.
Выявляемые в настоящее время структурные и биохимические изменения кости, возрастные особенности минерализации на фоне остеопении, ее причины у детей — все эти вопросы требуют углубленного изучения.
В детском и подростковом возрасте накапливается 86% генетически детерминированной костной массы (пиковой), гарантирующей прочность и устойчивость скелета к воздействию неблагоприятных эндогенных и экзогенных факторов в последующие годы жизни.
В последние годы за рубежом широкое распространение получила гипотеза, согласно которой остеопенический синдром у детей и подростков является одной из причин роста заболеваемости остеопорозом у взрослых.
Появление высокоточных, безопасных и простых в использовании остеоденстометров, достижения современной биохимии в области изучения маркеров костного метаболизма — все это открыло новые возможности для углубленного клинико-эпидемиологического изучения костной минерализации, а также факторов, влияющих на этот процесс у детей.
Несмотря на увеличение числа работ о распространенности ОП в детской популяции, однозначной клинической трактовки причин снижения МПК у детей до настоящего времени нет. По этому вопросу существуют как минимум четыре принципиально отличные точки зрения. Первая — ОП сопровождает естественные процессы роста ребенка; согласно второй — ОП характеризует процесс формирования кости в критические периоды развития; третья гипотеза — ОП свидетельствует об отставании костной массы от возрастных пиковых значений; наконец, согласно четвертой — ОП является симптомом ортопедической патологии.
Для окончательного разрешения этой проблемы, безусловно, потребуется время.
Однако некоторые факты известны уже сегодня.
Высокая активность биологических процессов на фоне линейного роста и дифференцировки костной ткани сопровождается у детей ускоренным ремоделированием (резорбцией и формированием кости), особенно в критические периоды развития, и требует положительного костного баланса для его обеспечения.
Кальций (Са) играет важнейшую роль в формировании прочной и функционально полноценной кости.
До 90-99% всего количества Са в организме человека содержится в костях.
Влияние Са на кости многообразно и уникально по спектру действия. Кальций снижает скорость ремоделирования кости, способствует пролиферации остеобластов (ОБ), активирует внутриклеточную ДНК, участвует в образовании и секреции инсулиноподобного фактора роста-1 (IFG-1), запускает каскад процессов костного моделирования, вовлекает в него кальцитриол, ростовые факторы, оптимизирует фосфорный метаболизм, способствует росту и адекватному обновлению костной ткани.
Ввиду высокой биологической значимости кальция организм длительно адаптируется к его дефициту путем увеличения кишечного всасывания и уменьшения почечной экскреции минерала.
У детей компенсаторные возможности при длительном дефиците кальция ограничены.
Источники кальция, необходимого для развития и роста скелета, на разных этапах онтогенеза отличаются (рис 1). Для плода это преимущественно кальций матери, переходящий через плаценту. В раннем возрасте кальций поступает из грудного молока, смесей для искусственного вскармливания (формулы), продуктов прикорма и частично из препаратов кальция, применяемого в комплексной профилактике и лечении рахита, в более старшем возрасте — с пищей и медикаментами (монопрепараты, витаминно-минеральные комплексы).
На транспорт кальция через плаценту влияют обеспеченность матери кальцием и витамином D, уровень кальция в крови матери и плода, метаболизм кальцийрегулирующих гормонов у беременной женщины, скорость плацентарного кровообращения.
Важно иметь в виду, что интенсивность включения кальция в скелет плода существенно возрастает в последний триместр беременности. В этой связи обеспеченность Са и степень минерализации костей новорожденного зависят от гестационного возраста при рождении. В силу особенностей обмена веществ недоношенный новорожденный задерживает не более 50% поступающего кальция, что также служит предрасположением к более частому развитию остеопении у этой категории детей.
Кальций, содержавшийся в грудном молоке, играет особую роль в формировании здоровых костей, так как хорошо всасывается, стимулирует весь комплекс механизмов, способствующих росту и увеличению костной массы.
Видимо, поэтому содержание его в грудном молоке отличается стабильностью. Есть данные, что потребление кормящей женщиной кальция в количестве 640-2280 мг в день не отражается на составе грудного молока. В то же время известно, что содержание кальция в грудном молоке коррелирует с уровнем обеспеченности минералом в предыдущие беременности. Клинические признаки его дефицита в акушерском анамнезе могут сопровождаться существенным уменьшением концентрации минерала в молоке матери.
У недоношенных детей, рожденных с остеопенией, в первые два месяца идет активация процессов минерализации, что требует строгого контроля за содержанием кальция в питании ребенка, а нередко его дополнительного назначения.
От рождения и до наступления половой зрелости кальций интенсивно усваивается организмом и аккумулируется костью.
В дополнительном назначении кальция нуждаются быстро растущие дети, особенно в период полуростового скачка и в препубертате. На этих этапах развития минерал важен для реализации линейного вытяжения ребенка без ущерба для качества кости, нарастания костной массы, увеличения размеров кости и ее полноценной минерализации.
Участие кальция в формировании и минерализации скелета определяет высокую значимость Ca в профилактике остеопенического синдрома у взрослых и детей.
Доза кальция определяется в соответствии с нормативами, отражающими потребность в минерале у детей разного возраста.
Принимая препараты кальция, надо иметь в виду, что разные его соли содержат неодинаковое число активных форм минерала (см. таблицу).
Кроме того, необходимо учитывать, что на усвоение кальция влияют:
- генетические факторы;
- возраст (у младенцев всасывается 58% Са, в пубертате 34%, у взрослых — 25%);
- пол;
- стадия полового созревания;
- соответствие хронологического возраста паспортному;
- темпы линейного роста;
- двигательная активность;
- число перенесенных инфекционных болезней;
- наличие хронических болезней печени, кишечника, сахарного диабета;
- курение, употребление алкоголя;
- исходная обеспеченность Са, витамином D, цинком, медью, другими микроэлементами, белком, энергией.
Для улучшения всасывания кальция (препаратов кальция) считается целесообразным назначать кальций во время или сразу после приема пищи (это в большей степени касается карбоната кальция; цитрат, лактат и глюконат кальция можно принимать в любое время), запивая его большим количеством воды.
Не рекомендуется одновременно принимать большие дозы препарата, так как малые дозы быстрее всасываются (например, лучше назначать по 500 мг Са два раза в день, чем один раз по 1000 мг).
Для лучшего усвоения кальция чаще всего назначают витамин D, который на 30-50% повышает усвоение Са из кишечника.
Уникальная роль кальция не умаляет значения других минералов (фосфор, магний, цинк, медь, марганец и др.), белка и энергии для формирования, минерализации и роста кости.
Эффективность кальция повышается, если его принимать в сочетании с витаминами Е, А, К, B6 ,C и другими.
В настоящее время имеется большой арсенал фармакологических средств для профилактики и коррекции нарушений минерализации костной ткани. Это соли кальция, препараты витамина D, а также специальные витаминно-минеральные комплексы. Эти медикаменты следует применять, одновременно осуществляя контроль кальций/фосфорного обмена. При значительном снижении МПК (Z score
источник
Остеопороз чрезвычайно распространенное заболевание, характеризующееся снижением плотности костной ткани. В определенной мере, возрастающая частота диагностированных случаев остеопороза, объясняется не столько ухудшением состояния здоровья населения, сколько увеличением продолжительности жизни (заболевание поражает преимущественно людей находящихся в старшей возрастной группе).
Определенную роль в увеличении количества пациентов с повышенной хрупкостью костей, сыграло развитие диагностических возможностей современной медицины. Наиболее информативный метод проведения диагностики остеопороза – денситометрия костей, позволяющая не только определить процент потери костной массы, но и выявить структурные нарушения костной архитектоники.
Кость представляет собой высокоспецифичную ткань, в составе которой содержаться три структурных элемента:
- белковый матрикс, составляющий основную соединительную ткань, удерживающую минеральные вещества в составе кости;
- минеральный компонент, состоящий из кальция и фосфора;
- костные клетки, отвечающие за перестройку костной ткани.
Вопреки сложившемуся мнению, кость не имеет постоянного, единожды сформированного, строения. По сути, она представляет собой живую структуру, основной целью которой является обеспечение оптимального поддержания человеческого тела. В течение жизни, характер нагрузок на несущий аппарат человеческого тела неоднократно меняется, причинами изменений могут служить:
- увеличение массы тела;
- изменение образа жизни (увеличение или уменьшение подвижности);
- увеличение внешних нагрузок (систематическое поднятие тяжестей) и т.д.
Влияние этих факторов заставляет кость постоянно осуществлять внутреннюю перестройку, позволяющую сохранять устойчивость и максимально противодействовать изменяющимся нагрузкам. При этом происходит разрушение костной ткани в месте, не требующем повышенной прочности, и формирование более твердой, в наиболее «нагруженном» участке. Процесс ремоделирования носит постоянный характер, и отвечают за него костные клетки – остеобласты, формирующие новый матрикс и остеокласты – разрушающие его.
Возрастной период до 20-30 лет характеризуется высокой скоростью обменных процессов, в которых под влиянием различных факторов (силовых нагрузок, количества употребленного кальция, гормональных изменений), происходит формирование костей. По достижении максимальной массы костной ткани, процессы потери и восстановления уравновешиваются. Основной причиной остеопороза становится преобладание процессов резорбции (разрушения) над процессами формирования.
Поскольку потеря минеральной плотности костей (МПК) всегда является следствием какого-либо заболевания или состояния, то существуют определенные категории лиц, которым показано обследование на остеопороз.
Так, показаниями к обследованию являются:
- возраст старше 45 лет для женщин и старше 55 для мужчин;
- женщины в период постменопаузы;
- эндокринные нарушения (сахарный диабет, нарушение функции щитовидной железы);
- многократные беременности (более 3) или длительное кормление грудью;
- несколько случаев перелома костей в течение 3–5 лет;
- пациенты, принимающие препараты группы кортикостероидов, а также транквилизаторы и противосудорожные препараты;
- ведение малоподвижного образа жизни (длительный постельный режим, использование инвалидного кресла);
- резкое похудание или постоянный маленький вес;
- наличие родственников с диагнозом остеопороз.
Важно! Недостаточное поступление в организм витамина Д может стать причиной развития остеопороза. Курение и употребление спиртных напитков, являются одной из причин развития остеопороза.
Среди перечня анализов на остеопороз, денситометрия по праву занимает ведущее место, так как позволяет производить количественную оценку состояния костной ткани. Определенную информативность, применимую для оценки интенсивности разрушения костей, имеет анализ мочи на количество выделяемого кальция и гидроксипролина, которые у пациентов с прогрессирующим остеопорозом обычно в большей степени выделяются с мочой, нежели усваиваются организмом.
Кроме того, первоначальный осмотр включает в себя проверку мочи на содержание деоксипиридонолина (ДПИД), выделяющегося с мочой в неизменном виде (несвязанном) в результате замедления или отсутствия обменных процессов в костной ткани.
Поскольку основной целью диагностики остеопороза является выявление категории пациентов, склонных к снижению костной массы, то целесообразно производить комплексную оценку активности остеобластов, определяемую по количеству остеокальцина в сутки, паратгормона, щелочной фосфотазы и деоксипиридонолина.
Таблица . Нормальные показатели биохимических маркеров
Довольно высокую диагностическую ценность имеет выявление концентрации женских и мужских половых гормонов, так как именно эндокринные нарушения зачастую становятся причиной развития остеопороза.
Наиболее применяемым на практике способом обследования костей на остеопороз является денситометрия. Термин «денситометрия» объединяет несколько методов получения изображения, позволяющего выполнить количественную оценку минеральной плотности костей (МПК), обследуемого пациента. Определенные результаты в оценке МПК были достигнуты с помощью обычного рентгеновского снимка.
Однако получить сколько-нибудь значимый количественный результат с его помощью не представляется возможным. Определяющим фактором, исключившим рентгенографию из списков методик, применяемых для диагностики остеопороза, являлся тот факт, что даже при оценке снимка опытным врачом, выявить потерю костной ткани, составляющую менее 40%, не представлялось возможным.
Проведение динамической оценки прогрессии или регрессии заболевания также достаточно затруднительно, из-за низкой чувствительности оборудования. Несмотря на это, рентгенография успешно применяется при необходимости оценки степени деформации костных структур, например, позвонков, так как подобное явление зачастую имеет место при развитии остеопороза.
Наиболее популярными методами рентгеновского исследования МПК принято считать:
- двухэнергетическая рентгеновская абсорбциометрия (DЕХА);
- морфометрическая рентгеновская абсорбциометрия (МRА);
- количественная компьютерная томография (ККТ).
Все рентгенологические методы исследования степени снижения МПК основаны на перемещении ионизирующего излучения из источника, расположенного снаружи, через кость к фиксирующему детектору. При этом узкий пучок рентгеновского излучения направляется на исследуемый объект и конечный результат, то есть интенсивность пропущенного через кость излучения фиксируется компьютерной системой.
Основным принципом метода DЕХА является использование двойного излучения, позволяющего максимально снизить погрешность благодаря регистрации двух вариантов поглощения энергии (в мягких тканях и костях).
Метод МРА является вариантом DЕХА, однако, использование веерного потока излучения позволило повысить качество изображения и сократить время сканирования, и соответственно снизить дозу облучения пациента.
Метод ККТ позволяет получить трехмерное изображение и не только определить МПК, но и получить данные о послойном строении костей, то есть оценить состояние трабекулярного и кортикального слоя. Отрицательной стороной применения ККТ является высокая доза облучения, превышающая DЕХА в 10 раз и зависимость точности показаний от количества костного мозга, процент которого с возрастом увеличивается.
В основе метода ультразвукового денситометрического исследования лежит вычисление скорости перемещения ультразвуковой волны через ткани, имеющие различную плотность. Различие в плотности обследуемой кости обусловливает различия в скорости прохождения ультразвука, то есть более плотная кость (хорошо минерализированная) пропускает ультразвук быстрее, чем менее плотная.
Полученные данные регистрируются датчиком и преобразуются с помощью компьютерного обеспечения в количественные показатели. Характерным свойством ультразвуковой денситометрии является чрезвычайно высокая чувствительность к малейшим изменениям в плотности костей. В связи с этим ее можно применять для диагностики остеопении, когда потеря минеральных веществ не превышает 3–5%.
Несомненными достоинствами методами ультразвуковой компьютерной денситометрии можно считать:
- достаточно высокая информативность;
- отсутствие негативного влияния на организм;
- быстрота проведения процедуры;
- ценовая доступность;
- отсутствие противопоказаний.
Благодаря столь большому перечню положительных сторон, ультразвуковую денситометрию можно применять не только для диагностики остеопении и остеопороза, но и для мониторинга эффективности проводимой терапии. В связи со значительными отклонениями, проявляющимися при обследовании костей, глубоко погруженных в мягкие ткани (проксимальный отдел бедренной кости), денситометрия с помощью ультразвука проводится исключительно на конечностях (лучезапястный сустав, пяточная кость и т.д.).
Техника проведения рентгеновской денситометрии заключается в выполнении комплекса измерений с помощью рентгенограмм в нескольких стандартных точках, наиболее подверженных остеопеническим изменениям:
- поясничный отдел позвоночника;
- шейка бедра;
- лучевая кость.
После выполнения серии снимков, программное обеспечение осуществляет обработку полученных результатов путем сравнения с заложенной в него базой данных. Сравнение при этом осуществляется по двум критериям:
- полученный результат с оптимальным показателем пациентов того же пола (Т-критерий);
- полученный результат со среднестатистическим показателем пациентов аналогичного пола и возраста (Z-критерий).
Наиболее информативным при постановке диагноза является Т-критерий, проверка степени его отклонения от нормальных показателей, имеет существенное диагностическое значение:
- показания выше «-1», говорят о нормальной МПК;
- показания в пределах от «-1» до «-2,5», свидетельствуют об остеопении (начальной стадии остеопороза);
- показания ниже «-2,5», говорят о развитии остеопороза.
Проведение ультразвуковой денситометрии осуществляется путем определения плотности кортикального (внешнего) слоя трубчатых костей. Для этого, с помощью УЗ-датчика ультразвуковую волну пропускают вдоль кости, определяя по скорости ее распространения МПК. За короткий промежуток времени аппарат выполняет тысячи измерений и по результатам рассчитывает Z и Т-критерии. Стандартными проекциями для проведения ультразвуковой компьютерной денситометрии являются:
- фаланга среднего пальца руки;
- лучевая или лучезапястная кость.
В связи с индивидуальными особенностями течения заболевания, очевидных признаков разрушения костной ткани, таких как переломы, может и не быть. Однако своевременно проведенная диагностика, способна существенно снизить риск возникновения такого серьезного осложнения, как перелом шейки бедра.
Несмотря на то что патология не является смертельной, длительное снижение двигательной активности и дорогостоящее лечение (протезирование), которое при тяжелых стадиях остеопороза также невозможно осуществить, часто приводят к летальному исходу.
На сегодняшний день в арсенале врачей имеется большое количество лекарственных препаратов, предназначенных для лечения остеопороза, но в связи с тем, что процесс восстановления является чрезвычайно длительным, оптимально начинать его как можно раньше.
источник
Вторичные остеопатии у детей с наследственными болезнями соединительной ткани и способы их терапевтической коррекции
Новиков П.В., Недашковский О.В., Семячкина А.Н.
Московский НИИ педиатрии и детской хирургии МЗ РФ, Москва
Представлены результаты комплексного обследования 55 детей с наследственными болезнями соединительной ткани — синдромом Марфана, синдромом Элерса-Данлоса и несовершенным остеогенезом. Проведена оценка диагностической значимости показателей, отражающих фосфорно-кальциевый гомеостаз и плотность костной ткани. Установлена высокая частота вторичных остеопатии при всех формах патологии. Разработана комплексная корригирующая терапия выявленных остеопатии с использованием витамина D и его метаболитов.
Наследственная патология занимает значительный удельный вес в структуре детской заболеваемости, младенческой смертности и детской инвалидности [4,5]. В детской популяции 5-5,5 % детей рождаются с наследственными или врожденными болезнями [3].
Многие наследственные болезни нередко сопровождаются тяжелыми нарушениями нервно-психического и физического развития, при этом в патологический процесс часто вовлекается костно-мышечная система с развитием остеопении и остеопороза [9,11,12]. Нарушения опорно-двигательной системы занимают 4-е место в структуре детской инвалидности, в том числе, и в Российской Федерации [7].
Научные исследования последних лет показывают, что истоки многих осложнений метаболических остеопатии у взрослых (боли в конечностях, остеопороз, переломы и др.) лежат в детском возрасте [1,10,13,15].
Одним из наименее изученных вопросов в проблеме метаболических остеопатии является проблема остеопороза [15, 14]. Остеопороз — одно из самых частых заболеваний человека и, по данным ВОЗ, занимает четвертое место после сердечно-сосудистых, онкологических заболеваний и сахарного диабета [10, 12,13]. Огромные затраты общества, связанные с остеопорозом и, прежде всего, с лечением остеопоротических переломов, сделали эту проблему особенно актуальной в течение последних десяти лет [1].
Тем не менее, как показывает анализ научных публикаций, внимание большинства исследователей при изучении наследственной патологии направлено на выявление и исследование главного патогенетического звена заболевания и поиску на этой основе путей коррекции ведущего патологического признака. На этом пути получены несомненные успехи. Однако многие формы наследственных болезней характеризуются полисистемностью поражения ведущих органов и систем, оценка степени тяжести которых остается мало исследованной, а возникающие отклонения длительное время остаются незамеченными и приводят к инвалидизирующим расстройствам. Это приводит к тому, что скрытый первоначально патологический процесс в костной ткани может внезапно проявиться тяжелым остеопорозом, болями при физической нагрузке, развитием костных деформаций и переломами.
Развитие вследствие нарушения обменных процессов так называемых метаболических остеопатии, которые называют «безмолвной эпидемией», приводит к постепенной потере массы костной ткани и они часто диагностируются только после переломов [6,24]. Остеопороз как проявление метаболических остеопатии отличает скудная симптоматика, нередко носящая общий характер: повышенная утомляемость, ноющие боли в крестце, поясничном отделе позвоночника, усиливающиеся при физической нагрузке, чувство тяжести между лопатками, проявление сутулости. По мере прогрессирования остеопороза усиливается болевой синдром. Чаще причиной болей в костях бывают микропереломы трабекул. По мере развития деформаций тел позвонков нарастает мышечная слабость, изменяется осанка, усиливается кифоз. Переломы являются поздним и наиболее ярким проявлением остеопороза, происходят они при минимальной травме [13].
Углубленные исследования, проведенные в последние годы и посвященные более широкому спектру изучения отдельных наследственных аномалий обмена веществ, показали, что поражения костно-мышечной системы могут носить прогрессирующий характер и определять формирование инвалидности ребенка. Клинически они имеют сходство с рахитическими и рахитоподобными изменениями скелета.
Особенностью строения костной ткани у детей являются нормальные процессы образования, резорбции и ремоделирования костной ткани, которые могут нарушаться при многих наследственных болезнях, в частности, при заболеваниях соединительной ткани, связанных с генетически обусловленным дефектом образования аномального коллагена [2]. При этом страдает, главным образом, коллаген первого типа, составляющий основную часть органического матрикса кости. Нарушение формирования коллагеновых волокон (фибрил) приводит к изменению микроархитектуры костной ткани, что негативно сказывается на ее прочности, и формированию вторичного остеопороза.
Несмотря на распространенность наследственных заболеваний соединительной ткани с поражением скелета у лиц молодого возраста и высоким уровнем инва-лидизации при этой патологии, вторичным метаболическим остеопатиям уделяется мало внимания [17].
Среди наследственных болезней соединительной ткани наибольший удельный вес принадлежит синдрому Марфана, синдрому Элерса-Данлоса и несовершенному остеогенезу. Одним из характерных признаков в клинической картине синдрома Марфана, наряду с поражением кожных покровов подкожно-жировой клетчатки, глаз, сердечно-сосудистой системы, органов дыхания и ЦНС, важное место принадлежит системному поражению скелета [8]. Основные изменения скелета при синдроме Марфана (истончение и усиленный рост костей в длину, сколиоз, плоскостопие, воронкообразная или килевидная деформация грудной клетки) обусловлены глубокими нарушениями структур соединительной ткани. L.Kolhermeire et al. при обследовании 14 детей в возрасте от 9 до 17,5 лет с синдромом Марфана обнаружили, используя метод двойной рентгеновской абсорбциометрии костей, снижение плотности костной ткани и явления остеопении у всех исследуемых детей [21]. Показатели плотности бедренной кости были достоверно снижены. Все дети имели рост выше среднего и нормальный вес. В исследованиях также была установлена корреляция между плотностью костной ткани и возрастом, ростом и уровнем полового развития больных детей. Ряд авторов указывает на повышенный риск переломов костей у детей с синдромом Марфана [20].
При синдроме Элерса-Данлоса скелет также вовлекается в патологический процесс. Этот синдром является одним из наиболее распространенных наследственных заболеваний соединительной ткани, его распространенность по данным зарубежных авторов значительно варьирует и составляет от 1 : 560000 до 1:5000 [22]. По классификации 1997 года принято выделять 6 типов синдрома Элерса-Данлоса, которые различаются по распространенности, типу наследования, клиническим проявлениям и биохимическому дефекту [16]. Заболевание является генетически гетерогенным и отличается большим клиническим полиморфизмом. Ряд исследователей обращает внимание на склонность к переломам у пациентов с синдромом Элерса-Данлоса [18]. При этом у больных определялись, наряду со снижением плотности костной ткани, аномалии структуры самой кости.
К группе тяжелых наследственных болезней соединительной ткани, встречающихся в педиатрической практике, относится также несовершенный остеоге-нез. Согласно общепринятой классификации, предложенной Сайлленсом [26], различают 4 генетических варианта заболевания, наследующихся, в большинстве случаев, по доминантному типу и характеризующихся, наряду с голубыми, синими или аспидно-серыми склерами, ранней тугоухостью, развитием костных изменений, поздним закрытием родничков.
Общими и характерными клиническими признаками несовершенного остеогенеза являются частые патологические переломы. При врожденной форме ребенок рождается с деформациями конечностей в результате внутриутробных переломов. При поздней форме переломы появляются позже и в более старшем возрасте. У новорожденных кости черепа могут быть чрезмерно мягкими. Зубы прорезываются поздно, часто имеют янтарную окраску и поражаются кариесом. Чаще всего наблюдаются переломы длинных трубчатых костей и позвоночника, однако не являются исключением переломы и других костей. Количество переломов не зависит от формы несовершенного остеогенеза. Течение заболевания у детей, которые родились с внутриутробными переломами и у которых переломы начались с 3-5 — летнего возраста, может быть легким (редкие переломы) и более тяжелым (частые множественные переломы). Тугоухость у больных с несовершенным остеогенезом обычно возникает в возрасте 20-30 лет.
Анализ научных публикаций показывает, что вопросы терапевтической тактики при метаболических остеопатиях, возникающих при наследственных болезнях соединительной ткани, остаются неразработанными [25]. Так, при синдроме Марфана основные терапевтические подходы направлены на предупреждение прогрессирования сердечно-сосудистых нарушений, в частности — расширения аорты и коррекцию глазной патологии [5], при синдроме Элерса-Данлоса — укрепление сосудистой стенки и профилактику тромбоэмболических осложнений [5]. При несовершенном остеогенезе лечение направлено на предупреждение возникновения переломов и улучшение двигательной активности больных [19]. Малая изученность вторичных остеопатии при данных патологических состояниях обусловлена, вероятно, недостаточной оценкой состояния других органов и систем при конкретной нозологической форме, а также слабой методической оснащенностью многих лечебных учреждений современной диагностической аппаратурой, что не позволяет выявлять отклонения со стороны костной системы на ранних стадиях.
Таким образом, анализ научных публикаций, посвященных проблеме наследственных болезней соединительной ткани показал, что, несмотря на большое число исследований отдельных форм патологии, проблема ранней диагностики, раскрытия патогенетических механизмов и терапевтической коррекции остеопатии при вовлечении в патологический процесс скелета, особенно в детском возрасте, остается практически неразработанной.
Материалы и методы
Учитывая важную роль коллагена в структурной организации костной ткани, нами проведено исследование плотности костной ткани и состояния минерального обмена у 55 больных, страдающих тремя формами наследственных болезней соединительной ткани: у 13 детей с синдромом Марфана в возрасте от 7 до 14 лет, у 34 детей с синдромом Элерса-Данлоса в возрасте от 5 до 14 лет и у 8 детей с несовершенным ос-теогенезом в возрасте от 5 до 11 лет. . В качестве контроля для исследования плотности костной ткани и основных показателей минерального обмена взяты 10 детей соответствующего возраста, не имеющих каких-либо заболеваний.
Обследованные больные имели классические признаки соответствующих заболеваний соединительной ткани. Диагноз базировался на использовании международных критериев. Таким образом, из числа обследованных детей с синдромом Марфана имели проявления метаболической остеопатии 76,9% больных, среди больных синдромом Элерса-Данллоса — 73,5%, больных с несовершенным остеогенезом — 87,5%.
Для оценки состояния минерального обмена использовались следующие методы: определение общего кальция сыворотки крови стандартным колориметрическим методом на анализаторе Labsystems(Финляндия), концентрации ионизированного кальция методом селективной ионометрии на аппарате Easy Lyte Calcium(Medica Corporation USA), исследоваание уровня неорганических фосфатов сыворотки крови и их почечной экскреции по методу Dooze (1979), определение активности щелочной фосфатазы сыворотки крови оптимизированным стандартным методом Schlebusch H., Rick W.(1990). Определение паратгормона, кальцитонина, остеокальцина сыворотки крови с использованием радиоиммунологической системы на основе моноклональных антител фирмы Cis Bio Internatinal (Франция) и мультигамма счетчик (Швеция). Исследование плотности костной ткани (ПКТ) проводилось методом остеоденситометрии с использованием остеоденситометра Hologic — Lunar Achilles (США). Одновременно проводилось исследование структуры костной ткани по данным рентгенографии трубчатых костей. Исследование выполнялось до и после проведенного комплексного лечения . Комплексная терапия метаболических остеопатии включала назначение препаратов витамина D и его метаболитов. Суточная дозировка витамина D составила 10000 ME и не изменялась в зависимости от нозологических форма патологии. Доза метаболитов витамина D (оксидевит) составляла 0,5- 1 мкг в сутки. Дозировка 0,5 мкг назначалась детям при незначительном снижении плотности костной ткани, доза 1 мкг — при выраженной остеопении. Одновременно назначались препараты кальция и фосфора (остеогенон) в возрастной дозировке. Корригирующая терапия назначалась в течение 45 дней. Проведение подобной терапии осуществлялась на фоне базисной терапии, используемой традиционно при той или иной нозологической форме заболевания.
Так, детям с синдромом Марфана комплексная терапия включала широкий спектр медикаментозных препаратов(средства, влияющие на сердечно-сосудистую систему, стимуляторы ЦНС), физио- и санаторно-курортное лечение, при этом назначаются лекарственные вещества, учитывающие выявленные нарушения функционального состояния митохондрий (энерго-тропные препараты, антиоксиданты). Использование в терапии больных с синдромом Марфана р-адреноб-локаторов(обзидан, атенолол) было направлено на уменьшение давления крови на стенку аорты, препятствуя, тем самым, расширению и расслоению последней. Для стимуляции окислительно-восстановительных процессов, повышения активности ферментов цикла Кребса и улучшения обменных процессов в миокарде традиционно проводились 3-4 курса в год лечения рибоксином ( по 0,2 г два раза в день в течение 30 дней).
Дети с синдромом Элерса-Данлоса получали многолетнюю комплексную терапию, направленную на укрепление сосудистой стенки, стимуляцию энергетического обмена, ЦНС, улучшение показателей пере-кисного окисления липидов и антиокислительной активности плазмы. Лечение несовершенного остеоге-неза было направлено на уменьшение частоты переломов, увеличение двигательной активности. Лекарственная терапия этой патологии до настоящего времени разработана недостаточно [27]. Использование препаратов, содержащих флюориды, и монотерапия кальцитонином признаны малоэффективными [23]. Помимо медикаментозного лечения, использовалась физиотерапия, направленная на улучшение мышечного тонуса, стабилизацию суставов, повышение выносливости.
Динамическое исследование показателей фосфор-но-кальциевого обмена и структуры костной ткани проводилось на фоне многолетней традиционной терапии заболеваний. При этом нами использовалась комплексная оценка не только показателей фосфор-но-кальциевого обмена, но и факторов, его регулирующих — содержание паратиреоидного гормона и кальцитонина в сыворотке крови до и после разработанного комплекса медикаментозных средств.
Результаты и обсуждение
Результаты комплексного обследования параметров фосфорно-кальциевого обмена, факторов, его регулирующих, и плотности костной ткани детей всех групп до назначения лечения (исходное состояние) представлены в табл. 1.
Таблица 1
Показатели фосфорно-кальциевого обмена и плотности костной ткани (ПКТ) по данным эхоостеометрии у детей с наследственными заболеваниями соединительной ткани (п=55)
источник