Всем родителям известно, что в крови ребенка присутствуют такие клетки, как эритроциты и лейкоциты, а также тромбоциты. Многие мамы также знают, что лейкоциты представлены разными видами, а определение их уровня в процентах составляет лейкоцитарную формулу.
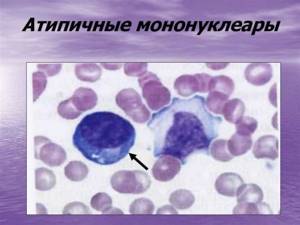
В атипичных мононуклеарах есть одно ядро, которое отличается полиморфизмом и губчатой структурой. Форма таких клеток является круглой или овальной. В зависимости от состава цитоплазмы и размеров эти клетки делят на моноцито- и лимфоцитоподобные.
По мнению многих ученых, атипичные мононуклеары происходят от Т-лимфоцитов. Они вырабатываются в ответ на проникновение вирусов в детский организм или под влиянием других факторов.
Выявление атипичных мононуклеаров в детском возрасте происходит во время проведения клинического анализа крови, включающего лейкограмму. Такие клетки подсчитываются в анализируемом объеме крови, сравниваются с числом всех лейкоцитов и выражаются в процентах. Ребенка направляют на такой анализ:
- Планово, чтобы убедиться в отсутствии скрыто протекающих болезней.
- При наличии жалоб, а также, если врач заподозрил инфекцию на основе осмотра.
- Во время подготовки к операции, а в некоторых случаях – перед вакцинацией.
- При обострении хронических патологий.
- В процессе лечения, чтобы удостовериться в его эффективности либо неэффективности.
Наиболее часто уровень атипичных мононуклеаров повышается при вирусных заболеваниях, например, при ветряной оспе. Повышенный процент вироцитов также выявляют при:
- Опухолевых процессах.
- Аутоиммунных заболеваниях.
- Патологиях крови.
- Отравлениях.
- Длительном приеме некоторых лекарственных средств.
Следует отметить, что в большинстве случаев такие клетки не превышают 10% от всех лейкоцитов. Если же атипичных мононуклеаров в лейкоцитарной формуле анализа крови детей выявляют больше десяти процентов, это является поводом диагностировать у ребенка болезнь под названием «инфекционный мононуклеоз». Поскольку ее причиной является вирус Эпштейна-Барр, такое заболевание также называют ВЭБ-инфекцией.
При такой инфекции атипичные мононуклеары выявляются в крови ребенка всегда. Болезнь чаще диагностируют у детей старше года, а ее инкубационный период может составлять до двух месяцев, а заразиться можно как при прямом контакте с болеющим ребенком, так и воздушно-капельным путем. При данной патологии уровень атипичных мононуклеаров может достигать 50% от всех лейкоцитов, а в некоторых случаях даже бывает выше.
Если анализ крови ребенка показал высокое содержание атипичных мононуклеаров, это является поводом обращения к врачу. Педиатр оценит общее состояние малыша, а также перенесенные болезни, поскольку после недавней вирусной инфекции уровень вироцитов в крови бывает повышенным еще несколько недель.
Подтвердив наличие у ребенка ВЭБ-инфекции, ему назначат симптоматическую терапию, включающую жаропонижающие, общеукрепляющие, антисептические и другие препараты. Специфического лечения, воздействующего на вирус Эпштейна-Барр, не существует.
При поражении печени ребенка переводят на специальную щадящую диету, дополняя ее лекарствами с гепатопротекторным и желчегонным действием. Если присоединилась бактериальная инфекция, показано применение антибиотиков и пробиотиков. При тяжелом течении или осложнениях ребенку могут назначаться гормональные средства, удаление селезенки, трахеостомия или искусственная вентиляция легких.
источник
Оксана Михайловна Драпкина, профессор, доктор медицинских наук:
– Профессор Спичак Татьяна Владимировна.
«Лечение инфекций дыхательных путей, вызванных атипичными возбудителями у детей».
Татьяна Владимировна Спичак, профессор, доктор медицинских наук:
В сегодняшней лекции я хотела бы коснуться ряда вопросов, связанных с атипичными инфекциями. Они по-прежнему продолжают волновать многих практикующих врачей. Ни для кого из нас не секрет, что успех лечения инфекции дыхательных путей в значительной мере определяется достоверностью этиологической диагностики.
С этим вопросом у нас, к сожалению, особенно в амбулаторной практике дело обстоит не очень благополучно. Если говорить о распространенности атипичных инфекций у детей, то литературные источники приводят нам достаточно большой разброс данных.
Мы знаем, что острый бронхит, как правило, обусловлен вирусной этиологией болезни. Что касается атипичных возбудителей, то с. Pneumonia и m. Pnemoniae диагностируют в 4% и 17% случаев.
При внебольничной пневмонии микоплазменная инфекция встречается у детей от 7% до 27%. А инфекция с. Pneumonia в 6% или 32%.
В последнее время большое внимание уделяется ассоциациям пневмококковой и атипичной инфекции, которые по данным наших зарубежных коллег составляют от 8% до 23%. Мы неспроста затрагиваем этот вопрос, потому что (как мы убедились на собственном опыте) ассоциация пневмококковой и микоплазменной инфекции действительно приводит к более тяжелому течению пневмонии по сравнению с монобактериальной этиологией пневмонии.
Всем хорошо известно, что этиологическая структура пневмонии имеет определенную возрастную зависимость, которая распространяется и на атипичные возбудители. По крайней мере, микоплазменную инфекцию чаще диагностируюn у детей 2-4-х лет и подростков.
С. Trachomatis, как правило, диагностируют у детей первого полугодия жизни. С. Pneumonia инфицирует чаще всего детей старше пяти лет. Хламидийная инфекция может произойти в любой последующий период жизни.
Появилось много литературных данных о роли хламидийной инфекции при бронхиальной астме у детей, особенно при ее тяжелом течении. Но если обратить внимание на представленную таблицу, мы видим очень большой разброс данных по частоте встречаемости хламидийной инфекции при бронхиальной астме. Причем зачастую несопоставимых из-за того, что используются разные методы исследований.
Кроме того, я хотела бы обратить внимание не только тех, кто получает из этой лекции просто информацию, но и тех, кто проводит подобные исследования. Очень важно иметь контрольную группу. К сожалению, во многих исследованиях это отсутствует.
Диагностика атипичных инфекций остается достаточно сложной по сегодняшний день. Это связано с тем, что при данных инфекциях отсутствуют специфические клинические и рентгенологические признаки, которые помогли бы нам в этиологической диагностике.
Главным образом это касается респираторно-хламидийной инфекции. Микоплазменную инфекцию мы еще можем как-то заподозрить по клиническим признакам, основываясь на своеобразных крепитирующих мелкопузырчатых влажных хрипах, нередко ассиметричных. По маловыразительной рентгенологической картине, при которой, как правило, мы наблюдаем усиление мелких элементов легочного рисунка. В большинстве случаев отсутствуют типичные легочные инфильтрации.
Основными методами диагностики атипичных инфекций являются лабораторные методы диагностики. Несмотря на большое число существующих методов, которые, казалось бы, должны нам помогать в диагностике этих инфекций, здесь тоже есть определенные проблемы.
Наибольшее распространение получили иммунологические методы исследования. В последнее время все чаще и шире используется полимеразная цепная реакция. Культуральный и морфологический методы используются, главным образом, в научных целях.
Я хотела бы обратить ваше внимание на то, что, несмотря на многообразие методов исследования, чувствительность и специфичность таковы, что ни один из методов не позволяет нам выявлять возбудитель в 100% случаев. Нам приходится пользоваться, как минимум, двумя методами исследования по более достоверной диагностике.
Есть проблема. Все перечисленные методы исследования могут нам давать либо ложноположительные, либо ложноотрицательные результаты. Это вполне естественно чревато либо лечением псевдобольных, либо распространением инфекции у нераспознанных больных.
Иммунологические методы основаны на использовании диагностикумы на основе родо- и видоспецифических антигенов. На выявлении специфических антител в сыворотке крови и секретах инфицированного организма в процессе иммунного ответа не внедрение возбудителей.
Из этих методов рекомендуется в настоящее время пользоваться методом микроиммунофлюоресценции (МИФ) и иммуноферментным анализом (ИФА).
Методы имеют безусловные достоинства. Прежде всего, возможность избежать ложноотрицательных результатов. В ряде случаев определить стадию заболевания. Но серьезным недостатком метода серологической диагностики является ретроспективная диагностика. Антитела класса М появляются лишь на пятый день от начала болезни.
Мы не можем ставить диагноз на основании данных методов исследования в более ранние сроки. Антитела класса М могут самостоятельно исчезнуть через 2-3 месяца, даже не прибегая к лечению. Что касается антител класса А, то они появляются гораздо позже – на 5 – 14 день – и тоже, как правило, исчезают через 2-3 месяца, но уже при условии проведения специальной терапии.
Если этого не происходит, то обнаружение антител класса А в более поздние сроки указывает на хроническую или персистирующую инфекцию.
Самыми последними появляются антитела класса G. На 15 – 20 день. Особенностью этих антител является то, что они могут сохраняться в низких титрах на протяжении ряда лет, отражая так называемую следовую реакцию после перенесенной инфекции.
Что касается диагностики микоплазменной инфекции, то следует обратить внимание на то, что при данной инфекции наблюдается длительная циркуляция АТ класса М. Для данной инфекции характерно большее развитие острых процессов. А реинфицирование отмечается редко.
Для выявления антигена возбудителя используют метод иммунофлюоресцентной микроскопии. К сожалению, этот метод не лишен недостатков, поскольку его чувствительность невысока, специфичность зависит от навыков персонала.
Полимеразная цепная реакция. Как известно, метод относится к молекулярно-биологическим. Основан на выявлении в составе биологического материала фрагментов ДНК или РНК, специфических для вида возбудителя. Этот метод отличает высочайшая чувствительность и специфичность. С помощью данного метода мы можем диагностировать на ранних стадиях болезнь и выявлять минимальное количество возбудителей вне зависимости от его жизнеспособности.
К сожалению, и этот метод не лишен недостатков. Мы имеем возможность получить и ложноположительные результаты в силу такой высокой чувствительности метода. Любая загрязняющая ДНК может дать нам такой результат.
Реакция может быть подавлена биологическим материалом. Это может привести к ложноотрицательному результату.
Показания к назначению лечения при атипичных инфекциях достаточно традиционные. Принято лечить острую инфекцию, реинфекцию и обострение хронической инфекции. Казалось бы, все просто. Но, к сожалению, достаточно непросто в реальной жизни определить стадию болезни и правильно сориентироваться с лечением, руководствуясь не только теми результатами, которые мы получаем на листах бумаги.
При диагностике респираторной хламидийной инфекции многие клиницисты до сих пор используют критерии Грейстона (Grayston G. T.). Они основаны на результатах реакции по определению специфических антител класса М и G. При выявлении специфических антител класса М и высоких титров антител класса G или при четырехкратном увеличении титра антител класса G в парных сыворотках можно говорить об острой инфекции.
При реинфекции хламидийной инфекции антитела класса М отсутствуют. Но наблюдается быстрое, буквально в течение одной-двух недель, появление антител класса G. Или также как при острой инфекции четырехкратное увеличение в парных сыворотках.
Для лечения атипичных инфекций традиционно используются антибактериальные препараты, которые обладают способностью проникать внутрь клеток и воздействовать на атипичные возбудители. Они вам прекрасно известны. Это макролиды, тетрациклины, фторхинолоны и «Рифампицин» («Rifampicin»).
Но поскольку речь идет о лечении детей, то мы предъявляем особые требования к антибактериальным препаратам. Они должны быть не только эффективными, но и максимально безопасными. Наш выбор сводится к макролидным препаратам.
Я не буду останавливаться на классификации макролидов. Она вам прекрасно известна. Хочу еще раз подчеркнуть их уникальные свойства как группы антибактериальных препаратов. Они относятся к числу наиболее безопасных антибиотиков и являются тканевыми антибиотиками, поскольку концентрация в инфицированных тканях во много раз превышает сывороточные.
Фармакодинамика современных макролидов позволяет их назначать 2-3 раза в сутки, что повышает комлпаентность.
Данная группа препаратов обладает уникальным постантибиотическим эффектом. Даже после прекращения введения антибактериального препарата, сохраняясь в инфицированных тканях, препарат продолжает еще обеспечивать терапевтические концентрации в течение еще 5-7 дней.
Говоря о группе макролидов, я хотела обратить ваше внимание на шестнадцатичленный макролидный антибиотик «Джозамицин» («Josamycin»). Он обладает активностью не только в отношении стрептококков, но также и атипичных возбудителей. Этот препарат характеризует стабильную биодоступность при приеме внутрь, не зависящую от приема пищи.
По сравнению с четырнадцатью членами макролидов его характеризует низкая частота лекарственных взаимодействий, хороший профиль безопасности и низкий уровень приобретенной резистентности.
Если говорить о «Джозамицине», выпускаемом в форме диспергируемых таблеток, то эта форма позволяет превратить таблетку в суспензию, что создает определенные удобства для приема препарата ребенком.
В отношении длительности курсового лечения при атипичных инфекциях принято во многих руководствах пользоваться десятидневными курсами лечения макролидными препаратами. Но некоторые руководства предлагают более длительные курсы лечения в течение 2-3 недель. Полагают, что это позволит осуществить профилактику персистирующей или хронической инфекции.
Подобное лечение острых инфекций может вызвать вполне оправданные возражения.
Что касается хронической инфекции (а здесь речь идет о хронической хламидийной инфекции), то приняты более длительные трехнедельные курсы лечения.
Оценка эффективности терапии осуществляется по исчезновению антигенового возбудителя, по снижению или исчезновению титра специфических антител. Я неспроста обращала ваше внимание на особенности динамики антителообразования при атипичных инфекциях. Контрольное исследование следует проводить не ранее, чем через 2-3 месяца.
В заключение я хотела бы привести результаты недавно завершенного нами исследования по определению этиологической структуры внебольничных пневмоний у детей и оценке эффективности рациональной антибиотиковой терапии.
Нами было обследовано 63 ребенка в возрасте от года до 18-ти лет с рентгенологически подтвержденной внебольничной пневмонией. У этих детей проводился комплекс современных методов исследования, направленных на выявление типичной бактериальной флоры. В первую очередь, пневмококка. А также атипичных возбудителей.
Для этих целей мы использовали ПЦР-диагностику. Определили специфические антитела указанных классов методом ИФА.
Из 63-х детей у 57-ми был определен инфекционный патоген, что обеспечило 90,5% выявления этиологически значимого агента.
По совокупности лабораторных методов исследования современная этиологическая структура внебольничной пневмонии у детей по нашим данным выглядит следующим образом. Мы видим, что пневмококк остается лидирующим или весьма значимым типичным бактериальным патогеном при внебольничных пневмониях.
В то же время мы видим, что высока частота и микоплазменных инфекций при пневмонии у детей. Этого нельзя сказать о хламидийных пневмониях, потому что их частота не превышала в наших данных 14%. В каждом седьмом случае мы имели дело со смешанной бактериальной инфекцией при внебольничной пневмонии, обусловленной, главным образом, сочетанием пневмококка и микоплазменной инфекции.
Течение пневмонии было более тяжелым, чем при монопневмококковой инфекции.
Наши наблюдения (несмотря на то, что когда мы уточнили этиологию, группы оказались не такими многочисленными) позволили отметить особенности внебольничных пневмоний, на которые обращают внимание в современных руководствах. По крайней мере, в зарубежных.
Действительно в первые дни маловыразительная клиническая картина. Достаточно редко определяются хрипы и типичная физикальная симптоматика. Но у большинства детей присутствует синдром дыхательных расстройств. Это, в первую очередь, касается пневмококковых пневмоний. В меньшей степени это касается микоплазменной и хламидийной пневмонии.
Синдром дыхательных расстройств, который ведет в число наиболее достоверных диагностических и клинических признаков, в большей степени работает у детей до пяти лет. Дети с микоплазменной и хламидийной пневмонией в нашем наблюдении были школьного возраста.
При лечении внебольничных пневмоний мы поступали также, как поступают все практикующие врачи. Мы назначали антибактериальную терапию эмпирически, в соответствии с принципами рациональной антибиотиковой терапии до получения результатов проведенных нами биологических и других исследований.
Препаратом выбора был, как правило, «Амоксициллин» («Amoxicillin»). А «Джозамицин» мы назначали при подозрении на атипичные инфекции или при аллергии у детей.
В тех случаях, когда мы назначали именно макролидный антибиотик «Джозамицин», мы получили стопроцентную эффективность. В тех случаях, когда мы, не зная этиологию болезни и не предполагая ее по клиническим признакам, назначали препараты пенициллинового ряда, в ряде случаев нам пришлось производить коррекцию с переводом данных больных на макролидный антибиотик для получения терапевтического эффекта. Это не возбраняется, вполне допускается.
В заключение я хотела бы сказать о том, что атипичные инфекции остаются достаточно хорошо распространенными у детей и подростков при инфекциях дыхательных путей. Если мы хотим повысить эффективность и улучшить диагностику атипичных инфекций, то нам надо обращать внимание на микробиологические лаборатории, на то оборудование, на котором они работают, и на приобретение качественных тест-систем.
Естественно, макролидные препараты в педиатрической практике остаются основными препаратами для лечения атипичных пневмоний. «Джозамицин», о котором мы сегодня говорили, является одним из наиболее перспективных для лечения атипичных инфекций у детей.
Мы можем сказать, что макролидные антибиотики являются препаратами выбора при инфекции дыхательных путей и внебольничной пневмонии. В первую очередь, в период сезонных вспышек микоплазменной или хламидийной инфекции. А также у детей, имеющих признаки аллергии на бета-лактамные антибиотики.
источник
Какие назначения необходимы при подозрении на инфекцию нижних дыхательных путей? Какие патогенные факторы играют существенную роль? Как вести больных? Респираторные заболевания являются частой причиной обращения к врачу в Великобритании,
Какие назначения необходимы при подозрении на инфекцию нижних дыхательных путей?
Какие патогенные факторы играют существенную роль?
Как вести больных?
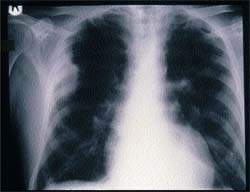 |
Респираторные заболевания являются частой причиной обращения к врачу в Великобритании, причем в большинстве случаев они относятся к инфекционным [1]. Трем четвертям пациентов, обращающихся с признаками острого заболевания нижних дыхательных путей, врач общей практики назначает антибиотики, хотя лишь в немногих случаях удается выделить возбудителя и антибиотики или вообще не влияют, или мало влияют на естественный ход заболевания [2,3].
Назначая антибиотики, врач руководствуется ожиданиями пациента и старается действовать согласно определенной терапевтической стратегии, хотя зачастую, выписывая рецепт, чувствует, что при этом состоянии антибиотики будут неэффективны [4,5].
Причины, по которым пациент первый раз приходит на прием к своему врачу и затем повторно обращается за консультацией, довольно сложны и часто никак не соотносятся с течением болезни. Как правило, они обусловлены обеспокоенностью своим здоровьем или давлением со стороны друзей, семьи и сотрудников.
При необходимости назначить антибиотик для лечения инфекции нижних дыхательных путей обычно выбирают амоксициллин. Пациенты, повторно обращающиеся к врачу, скорее всего, получат другой антибиотик, например эритромицин или новейшее средство из группы макролидов, хинолонов или пероральный цефалоспорин [3,6].
Проведенные нами недавно исследования показали, что повторное обращение пациентов с инфекциями нижних дыхательных путей, уже получивших назначения на первичном приеме, никак не связано с антибиотикотерапией. Только у 4% таких больных сохранялась бактериальная инфекция и ни у одного из них не было устойчивости к амоксициллину [7]. Повторно приходить на прием побуждают пациентов немедицинские факторы, такие как привычка обращаться к врачу.
- Пациент неверно представляет себе естественное течение болезни
- Пациент продолжает беспокоиться по поводу симптомов болезни
- Пациенту нравится ходить на прием к врачу
- По настоянию членов семьи, друзей, сотрудников
- У пациента появились соображения, касающиеся важности симптомов
Редко
- Инфекция хронизируется или к ней присоединяется другая инфекция
- Проявляется серьезное основное заболевание
При повторном обращении по поводу респираторного заболевания врач общей практики прежде всего должен попытаться установить причину такого обращения (табл. 1). Вполне возможно, что оно вызвано необоснованными ожиданиями пациента, и наилучшим средством здесь было бы объяснение нормальных сроков выздоровления от простуды. Или же есть какое-то основное заболевание, не распознанное на первичной консультации, например астма, недолеченное хроническое обструктивное легочное заболевание, рак или бронхоэктазы.
В том случае если врач считает, что причина в продолжающейся инфекции, необходимо определить возможного возбудителя и выбрать соответствующий антибиотик (табл. 2). Ниже мы обсудим некоторые сложные случаи, которые необходимо иметь в виду [8,9]. Однако нужно помнить, что наиболее распространенными возбудителями остаются Streptоcoccus pneumoniae и респираторные вирусы, а сложные случаи составляют скорее исключение, чем правило в ежедневной общей практике.
Пенициллин-резистентный Streptococcus pneumoniae. Хотя число случаев развития лекарственной устойчивости неуклонно возрастает и представляет серьезную проблему для целого ряда европейских стран, в Англии антибиотикорезистентность пока не считается причиной неудачного лечения инфекций дыхательных путей. Нужно убеждать врачей общей практики проводить пневмококковую вакцинацию населения, входящего в группу риска, а антибиотики назначать строго по показаниям и в адекватной дозе.
Амоксициллин-резистентный Haemophilus influenzae. Haemophilus influenza (Hi) является частой бактериальной причиной обострения хронических обструктивых заболеваний легких (ХОЗЛ), а также вызывает персистирующий бронхит у здоровых взрослых людей. Некоторые антибиотики, такие как эритромицин и цефалоспорины первого поколения, недостаточно эффективны в отношении Hi. Наличие b-лактамазы объясняет отсутствие реакции на амоксициллин. Такие штаммы называются амоксициллин-резистентными Hi (АRHi).
Таблица 2. Возможная причина отсутствия цикла терапии острой инфекции нижних отделов дыхательных путей, назначенной на первом приеме*
инфекция
Амоксициллин-резистентный
Haemophilus influenzaе
Распространенные атипичные
инфекции
Mycoplasma pneumoniae
Chlamydia pneumoniae
Moraxella catarrhalis
Пенициллин-резистентный
Streptococcus pneumoniaе
Другие бактериальные возбудители
Иные атипичные инфекции
Chlamydia psittaci
Coxiella burnetti, Legionella pneumophila
Заболеваемость, обусловленная АRHi, растет и составляет сегодня в Великобритании 10-25% общего числа респираторных заболеваний в зависимости от региона. В других странах, таких как Испания, Португалия и некоторые районы Франции, уровень лекарственной устойчивости гораздо выше — это нужно иметь в виду в тех случаях, когда пациент мог заразиться зарубежом.
Об этом возбудителе следует помнить, если у пациента с ХОЗЛ после лечения часто повторяющимися курсами амоксициллина сохраняются симптомы заболевания и гнойная мокрота. В данном случае целесообразным будет недельный курс хинолона или коамоксиклава. От назначения ципрофлоксацина следует воздержаться, если пациент принимает теофиллин.
Moraxella catarrhalis. Некоторым название этого микроорганизма может показаться незнакомым, поскольку раньше его относили к роду Neisseria вида Branhamella.
Это грамотрицательный диплококк, входящий в нормальную микрофлору молодых и пожилых людей. Вслед за Haemophilus influenza и Streptococcus pneumoniae он является третьей по распространенности причиной обострения ХОЗЛ и часто поражает пациентов с тяжелыми хроническими легочными заболеваниями или раком легких.
Обнаружение этого микроорганизма служит показателем тяжести процесса. Сообщалось о недавнем наблюдении 42 случаев пневмонии, вызванной M. catarrhalis, когда около половины пациентов погибло от основного заболевания в течение трех месяцев после обнаружения инфекции.
Важно и то обстоятельство, что практически все штаммы сегодня являются b-лактамазопродуцирующими и соответственно амоксициллинорезистентными. Имеется предположение, что b-лактамаза, продуцируемая M. Catarrhalis, обеспечивает устойчивость к амоксициллину в норме чувствительных респираторных возбудителей, таких как S. pneumoniae и H. influenzae. Проводимая терапия не отличается от той, которая применяется в случаях АРHi (см. выше).
Pseudomonas aeruginosa. Об этом возбудителе нужно помнить в связи с возможностью развития бронхоэктазов и кистозной болезни. Стоит один раз заразиться Pseudomonas aeruginosa, и рецидивы могут следовать один за одним. В настоящее время единственным эффективным пероральным средством является ципрофлоксацин, но к нему быстро развивается устойчивость, и пациентов приходится госпитализировать для проведения внутривенной антибиотикотерапии и физиотерапии.
Другие бактериальные возбудители. Изредка выделяют грамотрицательную кишечную палочку, или Staphylococcus aureus. Эти возбудители чаще связаны с больничными пневмониями, но иногда обнаруживаются у пациентов, недавно выписавшихся из больницы.
- Атипичные инфекции
Под атипичными обычно подразумеваются инфекции, вызываемые Mycoplasma pneumoniae, Chlamydia psittaci, Chlamydia pneumoniae, Coxiella burnetti и Legionella pneumophila. Лихорадка Q, возбудителем которой служит Coxiella burnetti, встречается редко (как правило, в сельской местности), поэтому не будет упоминаться в дальнейшем. Все атипичные инфекции трудно поддаются распознаванию на ранних стадиях; серологические исследования, проведенные как в острый период, так и в период реконвалесценции, редко дают положительный ответ и не представляют клинической ценности.
Ни один из возбудителей атипичных инфекций не поддается воздействию b-лактамных антибиотиков, что объясняет отсутствие эффекта от назначения амоксициллина.
Mycoplasma pneumoniae. Эпидемия, вызванная этим возбудителем, случается каждые три-четыре года, и в такой период может составлять значительную часть всех респираторных заболеваний.
Обычно она охватывает школьников, студентов и людей среднего возраста; маленькие дети и старики страдают редко.
В отличие от бактериальных инфекций, заболевание начинается постепенно, через 10-14 дней после заражения, проявляясь сухим кашлем или выделением скудной чистой мокроты. Общее недомогание и повышение температуры тела обычно умеренные, при исследовании грудной клетки обнаруживаются незначительные изменения. Иногда такие проявления, как сыпь, буллезный мирингит, а также выявление холодовых агглютининов помогают поставить диагноз.
Микоплазменную инфекцию следует заподозрить, если взрослый человек, до этого не жаловавшийся на здоровье, при отсутствии серьезных патологических симптомов и признаков интоксикации не поддается лечению амоксициллином. В этом случае имеет смысл попробовать назначить антибиотик из группы макролидов; альтернативный подход — тетрациклины. Кашель, как правило, медленно поддается лечению.
Хламидии. Большинствo врачей общей практики время от времени сталкиваются со случаями пситаккоза, вызванного длительным контактом с какой-нибудь любимой домашней птичкой. В последние годы установлено, что наиболее распространенным возбудителем инфекций дыхательных путей является Chlamydia pneumoniae, передающаяся от человека к человеку [10]. Эта инфекция проявляется такими же стертыми симптомами, как и микоплазменная, среди которых выделяются кашель и фарингит. Но, в противоположность микоплазменной инфекции, данное заболевание поражает и пожилых людей, часто вследствие реинфекции.
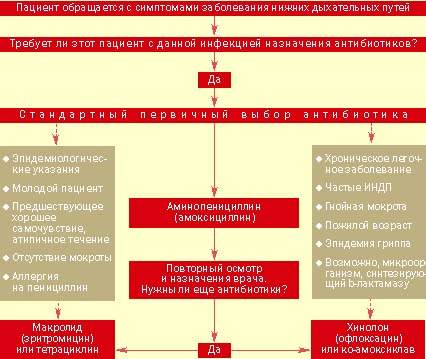 |
| Рисунок 2. Тактика ведения больного с выраженными клиническими показаниями для назначения антибиотиков при остром заболевании нижних дыхательных путей |
В некоторых исследованиях обнаружена связь между Chlamydia pneumoniaе и болезнями коронарных артерий и бронхиальной астмой, возможно обусловленная наличием хламидиального антигена, прикрепляющегося к эндотелию и эпителию. Рекомендуемое лечение — антибиотик из группы макролидов или тетрациклинов.
Legionella pneumophila. Болезнь легионеров все еще находится в центре внимания. Легионелла — редкий возбудитель пневмонии, развивающейся в местах большого скопления людей. Похоже, что легионелла не вызывает такие менее тяжелые заболевания дыхательной системы, как бронхит или инфекции верхних дыхательных путей. Состояние пациентов с болезнью легионеров достаточно тяжелое; обычно им требуется лечение в условиях стационара.
Известна связь этого заболевания с зараженными легионеллами источниками воды, поэтому упоминание пациента о заграничной поездке, пребывании в отеле или больнице, ванне джакузи помогает врачу общей практики правильно поставить диагноз. Нередко встречаются такие осложнения, как дыхательная недостаточность и энцефалит, поэтому все больные, даже в сомнительных случаях, должны быть направлены на госпитальное обследование.
- Практические советы по ведению больных с инфекциями дыхательных путей
Назначение антибиотиков. Подход к ведению больных с острыми инфекциями нижних дыхательных путей представлен на рис. 2. Ключевым моментом является принятие решения о назначении или неназначении антибиотиков. Большинство врачей общей практики считают необходимым применение антибиотиков при серьезных системных нарушениях, постоянном выделении гнойной мокроты, появлении местных признаков поражения легких и отягощенности предшествующими заболеваниями. Если уже решено использовать этот вид лечения, выбор нужного препарата не представляет особого труда.
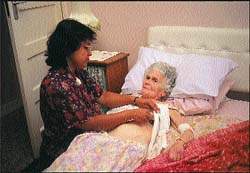 |
| Рисунок 3. Пациентам, входящим в группу риска, необходимо провести пневмококковую вакцинацию |
В большинстве случаев назначается амоксициллин. Согласно последним рекомендациям, доза амоксициллина принята равной 500 мг (а не 250 мг, как было раньше), чтобы снизить частоту развития резистентности пневмококков. Однако эта проблема лучше разрешается путем уменьшения общего количества назначений антибиотиков при инфекциях нижних дыхательных путей.
Врач общей практики не должен рекомендовать больному прием антибиотиков просто потому, что это самый легкий способ, или в случае, когда нет четких клинических показаний для их назначения. Проблемы резистентности возбудителей инфекций дыхательных путей решаются при назначении антибиотиков, обусловленном строгими показаниями. Снабжение пациентов простыми информационными листками значительно снижает необходимость повторных консультаций.
1. Office of Population Censuses and Surveys. Morbidity statistics from general practice: foutrh national study 1992. London: HMSO, 1995 (Series MB5;3).
2. Orr P. H., Scherer K., Macdonald A., Moffatt M. E. Randomosed placebo controlled trials of antibiotics for acute bronchitis: a critical review of the literature. J Fam Pract 1993; 36:507–512.
3. Macfarlane J. T., Holmes W. F., Macfarlane R. M., Lewis S. Contemporary use of antibiotics in 1089 adults presenting with acute lower respiratory tract illness in general practice in the UK: implications for developing managment guidelines. Respiratory Medicine, 1997; 91:427–434.
4. Holmes W. F., Macfarlane J. T., Macfarlane R. M., Lewis S. The influence of antibiotics and other factors on reconsultation for acute lower respiratory tract illness in primary care. Br J Gen Pract (in press).
5. Macfarlane J. T., Holmes W. F., Macfarlane R. M. Acutr lower respiratory tract illness in general practice; a study of the view on 787 patients and their influence on antibiotic prescribing. BMJ, 1997; 315:1211–1214.
6. Macfarlane J. T, Colville A., Guion A., Macfarlane R. M., Rose D. H. Prospective study of aetiology and outcome of adult lower respiratory tract infection in the community. Lancet, 1993; 341:511–514.
7. Macfarlane J., Prewett J., Rose D., Gard P., Guion A., Cunnigham R., Myint S. A prospective, case control study of the aetiology of community acquired lower respiratory tract infections in adult who felt to improve with initial antibiotics. BMJ, 1997; 315:1206–1210.
8. Venkatesan P., Innes J. A. Antibiotic resistance in common acute respiratory pathogenes. Thorax, 1995; 50:481–483.
9. Anon. Lower respiratory tract infections. MeReC Bulletin 1994; 5:5–8.
10. Torres A., ElEbiary M. Relevance of Chlamydia pneumoniae in community acquired respiratory infections. Eur Respir J, 1993; 6:7–8.
11. Macfarlane J. T., Holmes W. F., Macfarlane R. Reducing reconsultations for acute lower respiratory tract illness with an information leaflet. Br J Gen Pract, 1997; 47:710–722.
источник
Инфекционный мононуклеоз или лимфоцитарная ангина, часто развивается у детей и у взрослых, и имеет уникальные особенности в клинической картине и, особенно в общем анализе крови, которые позволяют в типичных случаях ставить правильный диагноз без привлечения дополнительных методов современной диагностики.
Такие симптомы, которые характерны только для одного заболевания, называют патогномоничными.
К ним можно отнести, например, характерные пятна Бельского-Филатова-Коплика на слизистой ротовой полости при заболевании корью, и появление так называемых атипичных мононуклеаров, когда проводится анализ крови при мононуклеозе у детей и у взрослых. О чём идёт речь, и какие изменения характерны для этой инфекции?
Обычно при остром инфекционном заболевании общий анализ крови реагирует неспецифическими изменениями. В случае бактериальных инфекций при наличии хорошего иммунного ответа у ребёнка, да у взрослого, возникает лейкоцитоз, количество лейкоцитов увеличивается свыше 8000, и нередко повышается до 12 — 15 тысяч единиц и более.
Повышается СОЭ, в периферическую кровь из красного костного мозга выходят молодые формы иммунных клеток, которые составляют палочкоядерные лейкоциты, а также более незрелые. При тяжелых инфекциях в крови могут наблюдаться юные лейкоциты и даже миелоциты.
При вирусных инфекциях, к которым относится и инфекционный мононуклеоз, чаще всего в крови может обнаруживаться не лейкоцитоз, а напротив, лейкопения, и увеличение количества лимфоцитов и моноцитов. Но анализ при инфекционном мононуклеозе не ограничивается этими простыми и неспецифическими сдвигами.
В общем анализе крови у ребенка, который берется из пальца или из вены, в разгар заболевания наблюдается характерная клиническая картина.
Во время дебюта, в первую неделю заболевания, у детей анализ крови может показывать общие изменения. Это деликатное общее снижение лейкоцитов, за счёт уменьшения количества нейтрофилов или нейтропении.
В разгар болезни отмечается умеренный лейкоцитоз, и специфические изменения общего анализа крови, к которым относятся выраженный мононуклеоз.
Это уже будет не название заболевания, а феномен клинического исследования.
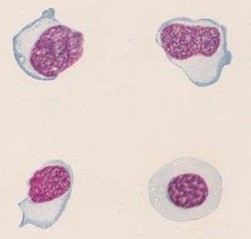
Этот феномен проявляется возникновением в крови своеобразных лейкоцитов, которые называются мононуклеарами, то есть имеют несегментированное, целое ядро. Они бывают самых разных размеров, структуры и формы.
Мононуклеары являются еще более крупными лейкоцитами, чем лимфоциты, которые, имеют наибольшие размеры среди всех лейкоцитов.
У мононуклеаров, несмотря на крупные лимфоцитарные размеры, ядро очень похоже на таковое у моноцитов, при этом у этих клеток широкий поясок цитоплазмы, которая хорошо окрашивается базофильными красителями. 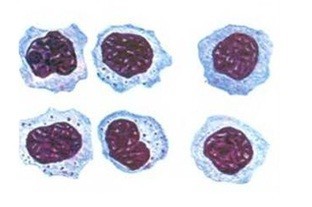
При этом все остальные показатели красной крови — количество эритроцитов, цветовой показатель и уровень гемоглобина не изменены.
Количество тромбоцитов при инфекционном мононуклеозе может резко уменьшаться, включая понижение до 30 тысяч, но быстро приходит в норму. СОЭ при инфекционном мононуклеозе существенно не изменяется.
На иллюстрации ниже приведены атипичные мононуклеары «в интерьере», на фоне эритроцитов, что позволяет сделать вывод об их истинных размерах.
Более подробно о них читайте в статье Атипичные мононуклеары в общем анализе крови.
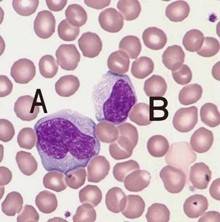
В период выздоровления за счёт повышения мононуклеаров существует феномен гранулоцитопении, или уменьшение количества гранулоцитов, к которым и относятся лидирующие у здорового человека нейтрофилы.
Чем ниже температура у пациентов в период выздоровления, как у взрослых, так и в детском возрасте, тем больше шанс появления в периферической крови повышенного количества эозинофилов, но в невысоких пределах – до 9%.
Помочь поставить диагноз инфекционного мононуклеоза позволяют и другие характерные симптомы, которые видны опытному врачу у постели больного.
Обычно наряду с общим инфекционным началом заболевания, с повышением температуры до фебрильных цифр, с появлением умеренной интоксикации, познабливанием и потливостью обращает на себя внимание значительное увеличение лимфатических узлов задней шейной группы.
Они увеличиваются цепочкой по заднему краю грудино-ключично-сосцевидной мышцы, а также в области сосцевидного отростка височной кости.
Несмотря на значительное увеличение этой группы лимфоузлов, которые могут даже изменить конфигурацию шеи, делая ее толстой, значительной боли обычно не ощущается.
Лишь во время пальпации, а также в случае интенсивного поворота головы дети и взрослые ощущают незначительную боль в шее.
В некоторых случаях лимфоузлы вообще не увеличиваются, или их размер изменяется незначительно, такая клиническая картина часто встречается у взрослых и поэтому может остаться незамеченным.
При этом лимфатические узлы не вызывают покраснения кожи. Никаких симптомов нагноения и локального воспаления обнаружить не удается.
Менее значительно увеличиваются другие группы лимфоузлов, например, поднижнечелюстные и шейные.
Иногда развивается ангина, которая является одной из форм инфекционного мононуклеоза, а также нередко возникают различные изменения в носоглотке, и поэтому пациенты с трудом дышат носом, и предпочитают дышать ртом, хотя при осмотре носовые ходы не забиты слизью, и из носа нет никаких выделений. Опытные врачи называют это состояние «сухим поражением носоглотки».
Общий анализ крови на мононуклеоз у детей и взрослых является одним из самых простых и достоверных способов первичной и достаточно точной постановки диагноза. Но в настоящее время существуют и другие исследования, которые позволяют верифицировать возбудителя, или вирус Эпштейна-Барр с высокой точностью. К ним относятся следующие виды лабораторной диагностики:
- Антитела класса Ig М и G к капсидному антигену вируса Эпштейна-Барр.
Этот иммунологический анализ является основой серологической диагностики инфекционного мононуклеоза. Антитела классов М и G появляются в острую фазу инфекции, и их можно обнаружить практически у всех пациентов с этим заболеванием, вне зависимости от возраста.
После выздоровления иммуноглобулины класса М постепенно исчезают из крови, а иммуноглобулину G циркулируют в крови пожизненно.
Важно помнить, что результаты разового серологического исследования мало что могут сказать для постановки диагноза, и необходимо исследовать оба иммуноглобулина, а также оценивать клиническую картину и расшифровку периферического анализа крови.
- определение ДНК вируса в соскобе эпителиальных клеток ротоглотки, носоглотки, из слюны.
Это исследование позволяет найти геном возбудителя, и проводится методом полимеразной цепной реакции. Известно, что вирус Эпштейна-Барр не только вызывает острый мононуклеоз, который проходит бесследно, но и может быть причиной различных новообразований лимфоидных органов, и даже приводить к онкологическим болезням.
Это анализ показан не только тем пациентам, у которых возникает характерное изменение лимфатических узлов, и появляются атипичные мононуклеары в результатах клинических исследований крови, но и для поиска атипичных форм заболевания, или хронического носительства ВЭБ.
Это может быть острая респираторная инфекция с высокой лихорадкой, состояние резкого ослабления иммунитета при иммуносупрессивной терапии, поиск причин ОРВИ у ВИЧ-инфицированных пациентов и при поиске лимфопролиферативных злокачественных новообразований. Тест на определение ДНК вируса является качественным, и анализ может быть или положительным, что говорит об инфицировании вирусом или отрицательным. В последнем случае, речь может идти как об отсутствии инфекции, так и низкой концентрации вируса.
Но, в любом случае, первым способом лабораторной диагностики мононуклеоза является общий анализ крови. Его информативность в сочетании с характерной клинической картиной типичных случаев позволяет безошибочно поставить диагноз лимфоцитарной ангины, или инфекционного мононуклеоза, как у детей, так и взрослых пациентов.
Такая болезнь, как инфекционный мононуклеоз, нередко встречается в детском возрасте. Она вызывается вирусом группы герпеса, названным в честь обнаруживших его ученых вирусом Эпштейна-Барр. И поэтому вторым названием этого заболевания является ВЭБ-инфекция.
Болезнь передается от заболевшего ребенка здоровому через прямые контакты и воздушно-капельным путем. Ее инкубационный период довольно длительный и может достигать нескольких месяцев, а первыми проявлениями будут лихорадка, боли в горле, увеличение лимфоузлов, слабость и заложенность носа.
Чтобы подтвердить диагноз, следует сдать общий анализ крови, ведь его изменения при мононуклеозе носят специфический характер, то есть позволяют убедиться в присутствии вируса Эпштейна-Барр в детском организме.
Если у ребенка есть такая инфекция, то показатели клинического анализа крови изменятся так:
- Общее число лейкоцитов увеличится (это называют лейкоцитозом).
- Процент моноцитов и лимфоцитов в лейкограмме повысится.
- На первой стадии болезни может выявляться нейтрофилез.
- Будут определяться атипичные мононуклеары. Так называют овальные или круглые одноядерные клетки, напоминающие по строению моноциты и лимфоциты, но имеющие некоторые структурные отличия. В норме такие клетки в анализе крови отсутствуют или могут быть у детей в пределах 0-1%. Их процент повышается при разных вирусных заболеваниях, опухолях и некоторых других патологиях, но при этом составляет менее 10%. Если уровень атипичных мононуклеаров превысил порог в 10%, это подтверждает наличие у ребенка инфекционного мононуклеоза.
- СОЭ будет умеренно повышена.
- Если течение болезни будет не осложненным, число тромбоцитов и эритроцитов останется нормальным. При появлении осложнений будет отмечаться их понижение.
Чтобы уточнить диагноз и определить наличие осложнений ребенка направят на:
- Моноспот-тест. Такой анализ помогает выявить болезнь на ранней стадии и заключается в соединении крови ребенка с особыми реагентами, в результате чего при ВЭБ-инфекции происходит склеивание клеток крови и выпадение их в осадок.
- Анализ на антитела. Такое исследование определить специфические иммуноглобулины, которые вырабатываются в организме ребенка при контакте с вирусом Эпштейна-Барр.
- Биохимическое обследование крови. В таком анализе при поражении печени будут повышены ферменты и уровень билирубина.
Ребенку с инфекционным мононуклеозом проводят несколько анализов крови, поскольку на разных этапах болезни показатели могут отличаться.
К примеру, присутствие в анализе атипичных мононуклеаров может не выявляться в первые недели заболевания.
Кроме того, в процессе лечения педиатру потребуется результат анализа для выявления осложнений, а после острой фазы клинический анализ крови покажет, как идет процесс выздоровления.
Анализ на мононуклеоз — это обобщающее название целого ряда обследований профильного характера. Для диагностики показана сдача ряда анализов крови на инфекционный мононуклеоз, также необходимо проведение ПЦР и ИФА-диагностики. Возможны и иные варианты. Следует разобраться подробнее.
Общий анализ крови у детей и взрослых при мононуклеозе. Кровь из пальца (общий анализ) сдается в первую очередь. Дает комплексную картину воспалительного процесса в организме. В первую очередь увеличивается концентрация лейкоцитов. Это типичный показатель воспаления, но он недостаточно специфичен.
Дополнительно определяется присутствие атипичных мононуклеаров и повышенная скорость оседания эритроцитов. Мононуклеары — это особые B-лимфоциты, защитные клетки крови, которые борются с вирусным возбудителем. В результате столкновения с агентом Эпштейна-Барр наблюдается их трансформация и, соответственно, атипия. Дополнительно определяются показатели нейтрофилов, моноциты и т.д.
Результаты расшифровываются следующим образом. На мононуклеоз указывают такие показатели:
- Скорость оседания эритроцитов варьируется в пределах 30 мм в час.
- Уровень нейтрофилов находится в пределах более 5%.
- Значение лейкоцитов повышено, но незначительно, в пределах 10% от нормы.
- Атипичных мононуклеаров более 12% или около того.
- Концентрация моноцитов составляет свыше 11%.
Эти значения могут указывать также и на цитомегалию, поэтому одного общего анализа крови недостаточно. Более того, такие значения наблюдаются только при остром инфицировании.
Если заражение произошло давно и иммунитет выработал специфические антитела, в большинстве случаев все уровни характерных значений остаются в пределах нормы.
Многое, таким образом, зависит от состояния иммунитета пациента.
В обязательном порядке общее исследование капиллярной крови проводится натощак. Прием пищи изменяет показатели в меньшую сторону и искажает результаты.
- Общий анализ мочи. Моча сдается для оценки состояния почек, поскольку мононуклеоз часто дает осложнения на выделительную систему организма. В структуре исследования определяется белок, соли, лейкоциты. Возможна микрогематурия с повышением показателей эритроцитов.
- Биохимическое исследование венозной крови. Кровь из вены рассматривается в рамках дополнительного лабораторного исследования. Клинические показания включают в себя:
- увеличение показателя щелочной фосфатазы: до 90 единиц на литр и более того;
- повышение количества билирубина;
- увеличение показателей АЛТ и АСТ.
- Агглютинационный тест. Сдавать кровь для подобного обследования необходимо. Оно позволяет выявить гетерофильные антитела во фракциях крови. Тест эффективен при остром инфицировании, когда с момента заражения прошло не более трех месяцев. В противном случае смысла в исследовании нет. Средняя точность составляет 95%. Это обследование является дифференцирующим и дает возможность отделить мононуклеоз от иных заболеваний. Однако можно спутать мононуклеоз с цитомегаловирусной инфекцией, что делает тест недостаточно информативным. В ходе процесса биологическая жидкость смешивается с катализаторами. Дополнительно возможно проведение теста Пауля-Буннеля. Это высокоточный метод, но эффективность его оправдана только в первые две недели с момента заражения.
- ПЦР-диагностика. Дает возможность определить наличие ДНК вируса в структуре крови. Благодаря такому тесту можно узнать, присутствует ли в кровеносном русле вирус Эпштейна-Барр.
- ИФА-исследование. Требует дополнительной расшифровки. Суть анализа заключается в поиске особых антител в структуре биологической жидкости. О наличии вируса Эпштейна-Барр говорят два типа антител: Anti VCM IgM и IgG. Речь идет о специфических иммуноглобулинах против данного штамма. М-иммуноглобулины вырабатываются практически сразу после инфицирования. Обладают крупными размерами и быстро борются с вирусом. Можно сказать, что именно они выступают антителами «быстрого реагирования» и связывают вирусный агент. Другой класс иммуноглобулинов – G-антитела, которые вырабатываются несколько позднее, от двух недель до двух месяцев. Они имеют меньший размер и более плотно связываются с антигенами. Это более эффективные вещества. В зависимости от сочетания двух указанных показателей можно судить, в какое время произошло инфицирование и на каком этапе находится процесс.
- IgM положителен, IgG отрицателен. Речь идет о начале инфицирования. Возможно острое течение процесса.
- IgM положителен, IgG положителен. Инфицирование произошло давно. В данный момент процесс находится в подострой фазе.
- IgM отрицателен, IgG положителен. Процесс инфицирования произошел давно. Организм выработал иммунитет.
- Оба показателя отрицательны. Инфицирование отсутствует, человек не страдает мононуклеозом.
Могут потребоваться серологические исследования, дополнительно проводятся инструментальные тесты, в том числе ультразвуковая диагностика печени, желчного пузыря, почек и мочевыделительных структур, сцинтиграфия, урография. Эти обследования необходимы для выявления изменений со стороны органов и систем.
Исследования на мононуклеоз многочисленны. Конкретные способы диагностики определяются только врачом исходя из состояния пациента. Важно не пропустить момент и назначить адекватное лечение.
Инфекционный мононуклеоз – патология, вызываемая вирусом, который относится к группе герпеса.
Данный вид может длительное время не проявлять себя и присутствовать в организме ребенка, как скрытая инфекция. Мононуклеоз чаще всего диагностируется у детей в осеннее время.
Этот вирус является «одноразовым», после того, как малыш им переболеет, в организме вырабатывается иммунитет, и повторное заражение невозможно.
Заражение происходит воздушно-капельным путем в период обострения у носителя. Также возможна передача в скрытой форме, при переливании крови и при поцелуе.
Не исключены возможности заражения во время поездки в общественном транспорте.
Также заражение подростка школьного возраста может произойти во время занятий, если соседом по парте является одноклассник, у которого поставлен данный диагноз, и у которого болезнь находится в активной форме.
Мононуклеозу подвержены дети, у которых слабый иммунитет, которые в недавнем времени перенесли сильные стрессы или находятся под действием постоянных физических нагрузок. Инкубационный период, после попадания в организм составляет до 50 дней.В зависимости от половой принадлежности вероятность заразиться вирусом в разном возрасте различна:
- Девочки заболевают чаще всего в возрасте от 13 до 16 лет;
- Мальчики – в возрасте от 15 до 18 лет.
При болезни повышается температура до 40 градусов, увеличиваются лимфатические узлы, также присутствуют сильные боли в горле.
Данные симптомы можно спутать с лихорадкой, однако, если среди сопутствующих симптомов есть боли в суставах, головные боли, мышечные боли, воспаление миндалин и затруднение дыхания, можно судить о вирусе.
Болезнь сопровождается набуханием шеи, с увеличением диаметров позвонков до 3 см.
При развитии патологии происходит воспаление лимфотока брыжейки, которое приводит к появлению на коже пятен красного цвета, пигментных пятен и папул. Покраснения на лице наблюдаются до 5 дней, после чего исчезают.
Основными симптомами клинического проявления болезни считаются:
- Беспокойный сон;
- Рвота;
- Понос;
- Боли в средней части живота.
Инфекция также может характеризоваться появлением опухолей в пространстве за брюшиной и опухолей в лимфоузлах. Такие проявления характерны для детей с низким иммунитетом.
С учетом длительного инкубационного периода, самым информативным для диагностики, является исследование крови пациента. Именно это позволит со 100% вероятностью потвердеть или опровергнуть факт наличия болезни в организме.
Стоит также учитывать, что течение происходит волнами: ремиссия-обострение, во время которых симптомы заболевания проявляются различно.
Если не проводить лабораторных исследований и поставить диагноз только по сбору анамнеза и осмотра, существует большая вероятность назначения недейственной терапии, такой как антибактериальная.
Сдать выделения на диагностику болезни можно не только по направлению врача, но и по собственной инициативе, в любом платном клиническом центре в Москве. Для того чтобы установить мононуклеоз, анализ крови нужно брать не только из пальца, но и из вены, для проведения нескольких проверок:
- Биохимические компоненты;
- Общие компоненты;
- На антитела герпеса типа Эпштейна-Барр;
- Моноспот;
- ВИЧ.
Анализ на мононуклеоз необходимо сдавать три раза: первые сдаются с разницей три месяца, последний по истечении трех лет. Повторение прохождения проверок рекомендуется из-за схожести первичных симптомов мононуклеоза и СПИД.
По результатам изучения общего анализа крови можно установить наличие патологии в организме. Определение идет по следующим критериям:
- Лейкоциты (х109г/л) от 13,3;
- Лейкопения (х109г/л) от 4,6;
- Нейтрофилез (%) от 53;
- Нейтропения (%) от 18,2;
- Лимфоцитоз (%) от 62,8;
- Лимфопения (%) от 20,0;
- Моноцитоз (%) от 12;
- Эритропения (х1012г/л) в пределах 3,4 -3,9;
- СОЭ (мм/час) от 21.
На наличие патологии указывает количество атипичных лимфоцитов, которое по сравнению с приемлемыми критерием здорового человека, увеличено в 10 раз.
Наибольшее количество заметно при проведении исследования во время второй недели течения заболевания.
Однако, при возникновении данных клеток врач не может поставить окончательный диагноз, так как атипичные клетки являются в том числе показателями таких болезней, как лейкоз, дифтерия, болезнь Боткина.
Особое внимание при расшифровке необходимо уделить количеству моноцитов, характерным признаком является увеличения этого показателя до десяти.
Если осложнений нет, то в результате исследования норма эритроцитов и тромбоцитов не будет превышена, если же осложнения уже есть, то их уровень будет очень низкий (эритроциты менее 3,0·1012/л; тромбоциты менее 150·109/л). Показатели тромбоцитов и эритроцитов будут увеличены только при условии возникновения осложнений.
При патологии в биохимическом анализе уровень альдолазы повышен, по сравнению с нормой, в 10 раз.Уровень щелочных фосфатов может достигать 150 ед/л.Если в результате инфекции развилась желтуха, то в биохимии, билирубин прямой фракции будет в несколько раз завышен.
Расшифровка анализа на антитела: исследование на антитела дает ответ о наличии вируса Эпштейна-Барр, и его активной или пассивной стадии. Если у ребенка присутствует активная форма, то в результатах будут присутствовать иммуноглобулины IgM. Во время стадии выздоровления в результатах будет видны антитела группы IgG.
Моноспот – тест, направленный на определение вируса, заключающийся в реакции крови с реагентом, который, при наличии заболевания вступает в реакцию с молекулами вируса и выделяет гетерофильные тела, которые можно увидеть. Признаки агглютинации являются явным показателем наличия заболевания в организме.
Однако стоит учитывать, что данный тест подходит только для стадии, которая не перешла в хроническую форму. Во время хронической формы показатели моноспота будут ошибочны.
В разные периоды результаты будут различными, так как вирус находится в различных фазах развития и в разных состояниях. Поэтому для определения стадии необходимо проводить ряд исследований и ставить диагноз, основанный на совокупности результатов, и учитывать результаты минимум двух исследований, сделанных в разные периоды.
Диагностика представляет собой достаточно сложный процесс, в котором нельзя ориентироваться на один или на несколько проб, которые были сданы всего один раз. Для того чтобы полностью вылечиться от этого и получить хороший иммунитет к заболеванию на всю жизнь, необходимо четко следовать инструкциям врача и сдавать все необходимые анализы. Помните: анализы необходимо сдавать минимум три раза!
Болезнь Филатова, иначе инфекционный мононуклеоз, относится к контагиозным инфекционным заболеваниям, спровоцированным герпесвирусами человека: 4-ого типа — вирус Эпштейн-Барр (ВЭБ), либо 5-ого типа – цитомегаловирус (ЦМВ). Наиболее частыми пациентами являются дети с пятилетнего возраста до пубертатного периода.
Группу риска среди взрослых составляют люди со слабым иммунитетом и женщины в перинатальный период. Выраженные клинические признаки болезни определяет специфический анализ крови при мононуклеозе у детей, ОКА (общий клинический анализ) и биохимическое исследование крови.
Герпесовирус Эпштейна-Барр считается главным возбудителем мононуклеоза. Источником заражения является больной человек или носитель вируса. При открытой форме инфицирования заболевание передается воздушно-капельным путем, при скрытой форме – при поцелуях и гемотрансфузии (переливании крови). Выделяют типичное и атипичное течение болезни.
Показанием для назначения ребенку исследований крови является характерная симптоматика:
- ангиноподобное поражение носоглотки (боли при глотании, отек, гиперемия, грязно-серый налет и др.);
- фебрильная (38-39 ℃) и пиретическая (39-40 ℃) температура тела;
- увеличение шейных, поднижнечелюстных, затылочных лимфатических узлов;
- спленомегалия (увеличение селезенки);
- кожные высыпания;
- интоксикационный синдром;
- гепатомегалия (увеличение печени);
- дисания (расстройство сна).
Стадийность патологии определяется, как инкубационный период, фаза проявления острых симптомов, восстановление (реконвалесценция). Атипичный мононуклеоз протекает в латентной форме, со слабо выраженными соматическими симптомами.
Определить заболевание возможно только по результатам лабораторных исследований. Подробная клинико-лабораторная диагностика болезни Филатова необходима для дифференциации инфекции от тонзиллита, ангины, дифтерии, ВИЧ, лимфогранулематоза и др.
Справка! Кроме мононуклеоза, вирус Эпштейна-Барр может стать причиной возникновения онкологических заболеваний лимфоидной ткани, системного гепатита, общей иммунной недостаточности.
Расширенная диагностика при инфекционном мононуклеозе включает:
- визуальный осмотр зева и кожных покровов;
- аускультацию (выслушивание с помощью стетоскопа);
- пальпацию брюшной полости и лимфатических узлов;
- фарингоскопию;
- мазок из зева;
- ОКА крови;
- биохимический анализ крови;
- ИФА (иммуноферментный анализ) крови;
- ИХЛА (иммунохемилюминисцентный анализ);
- моноспот-тест (для острой формы болезни);
- ПЦР (полимеразную цепную реакцию);
- анализ на ВИЧ;
- УЗИ брюшной полости.
Для определения заболевания у ребенка не всегда требуется использование всех методик. К обязательным лабораторным тестам относятся ОКА, биохимия, ИФА (ПЦР, ИХЛА). На первичном приеме, по предъявляемым жалобам назначается общий клинический и биохимический анализ крови.
Если по совокупности результатов исследования и симптоматических проявлений предполагается наличие инфекционного мононуклеоза, пациент направляется на дополнительное обследование.
ОКА проводится по капиллярной крови (из пальца). Общий клинический анализ позволяет выявить нарушения биохимических процессов, характерные для моноцитарной ангины (другое название мононуклеоза). Важное значение в диагностике заболевания имеют показатели лейкограммы, которую составляют белые клетки крови – лейкоциты (в бланке исследования обозначаются WBC).
Они отвечают за защиту организма от бактерий, вирусов, паразитов и аллергенов. Подгруппы лейкоцитов:
- гранулоциты: нейтрофилы — NEU (палочкоядерные и сегментоядерные), эозинофилы – EOS, базофилы – BAS.
- агранулоциты: моноциты – MON и лимфоциты – LYM.
При расшифровке результатов анализа на инфекционный мононуклеоз повышенное внимание уделяется следующим параметрам:
- наличие лейкоцитоза или лейкопении (завышенных или пониженных значений лейкоцитов);
- сдвиг лейкоцитарной формулы (лейкограммы).
- присутствие атипичных мононуклеаров;
- смещение значений моноцитов и лимфоцитов;
- концентрация гемоглобина;
- изменение скорости оседания эритроцитов – красных клеток крови (СОЭ);
- уровень тромбоцитов (кровяных пластинок, отражающих степень свертываемости крови) и эритроцитов.
Маркером болезни Филатова являются атипичные мононуклеары (иначе, вироциты или монолимфоциты) – молодые одноядерные клетки из группы агранулоцитов. В общем анализе здоровой биожидкости (крови) обнаруживается мизерное количество данных клеток, либо они не определяются совсем.
Изменения в составе крови, сопровождающие моноцитарную ангину, обнаруживаются уже в инкубационный период. Острая фаза заболевания характеризуется ярко выраженными отклонениями показателей от нормы.
| Показатели | Норма | Единицы измерения | Отклонения |
| лейкоциты | 4-9 | 109 клеток/л | 15-25 |
| лимфоциты | 19,4-37,4 | % | > 50 |
| нейтрофилы (палочкоядерные/сегментоядерные) | 1,0-6,0 / 40,8-65,0 | % | > 6,0/ 12 |
| атипичные мононуклеары | Читайте также: Воспаление носоглотки: причины, симптомы и лечение, профилактика заболевания С помощью ПЦР в крови обнаруживается вирус и его генетическая структура. Процедура анализа основана на многократном копировании фрагмента РНК (амплификации) в реакторе (амплификаторе). Биологическая жидкость перемещается в реактор, нагревается до расщепления на ДНК и РНК. После этого, добавляются вещества, определяющие пораженные участки в ДНК и РНК. При дифференциации нужного участка вещество присоединяется к молекуле ДНК, вступает с ней в реакцию, и копия вируса, таким образом, достраивается. В ходе цикличных реакций формируются многочисленные копии генной структуры вируса. Моноспот, так же, как ИФА и ИХЛА, базируется на реакции антител. Биологическая жидкость смешивается со специальными реактивами. При наличии инфекции происходит агглютинация (склеивание). Тестирование применяется для диагностики острой фазы мононуклеоза. При хронической форме болезни моноспот-тест диагностической информативности не имеет. Чтобы получить максимально объективную картину заболевания, сдать анализы крови необходимо несколько раз, и в обязательном порядке – после выздоровления. Достоверные результаты обеспечивает соблюдение правил предварительной подготовки к анализам.
Ознакомиться с результатами биохимии и ОКА можно на следующий день. Для выполнения специальных исследований предусмотрен недельный интервал выполнения. Мононуклеоз (моноцитарная ангина, болезнь Филатова) является инфекционным заболеванием, поражающим лимфатические узлы, печень, селезенку. Герпесовирус Эпштейна-Барр передается воздушно-капельным путем, и при поцелуе. Основной процент зараженных пациентов составляют дети от 5 до 13 лет. Диагностическую ценность при выявлении инфекции представляют:
При несвоевременной диагностике и некорректной терапии мононуклеоз у детей провоцирует осложнения, связанные с поражением лимфатической, дыхательной и центральной нервной системы, печени и селезенки (вплоть до разрыва органа). Такая патология, как мононуклеоз, зачастую диагностируется у детей старшего возраста. Излюбленный возраст патологии – 14-18 лет. Мононуклеоз представляет собой инфекцию, развивающуюся из-за проникновения внутрь организма вируса под названием «Эпштейн Барра», который включается в группу герпесвирусов. Когда клетки чужеродного агента начинают размножаться, в организме формируются специфичные антитела. В ходе исследования выявляется их присутствие в сыворотке крови. Какие анализы на мононуклеоз у детей проводятся? Анализ крови на мононуклеоз у детей показан при следующих симптомах:
В 10-15% случаев наблюдается различная по локализации и размерам сыпь на коже. При сдаче анализа крови у детей при инфекционном мононуклеозе смотрят на показатели лейкоцитов, наличие мононуклеаров, изменение уровня гранулоцитов. Те В-клетки (лимфоциты), которые поражены вирусом и которые были подвергнуты бластной трансформации (рост клеток бластов) и называются мононуклеары. Если болезнь у ребёнка только развивается, то эти элементы могут и не выявиться в ходе общего анализа крови. Их появление наблюдается на 2-3 день после инфицирования.
Нормальный тромбоцитарный и лейкоцитарный уровень будет, если мононуклеоз протекает без последствий. При других раскладах численность клеток уменьшается. Биохимический анализ крови в качестве определителя инфекции тоже часто назначается. В результатах исследования сильно увеличивается альдодаза, которая принимает участие в обмене энергией. Нередко можно наблюдать повышение численности щелочной фосфатазы. Если здесь отмечается и превышение прямых билирубиновых показателей, то говорят о развитии желтухи, непрямого – о тяжёлом последствии мононуклеоза – гемолитической аутоиммунной анемии. Анализ на инфекционный мононуклеоз – моноспот – тоже очень эффективное исследование. Проводится с целью выявления у ребёнка гетерофильных антител в кровяной сыворотке. Результативность анализа отмечается в 90% случаев при первичном инфицировании и если начальная симптоматика возникла не позже 2-3 месяцев. При хронически текущей форме болезни у ребёнка моноспот не покажет никаких изменений. В процессе манипуляции кровь соединяется с биологическим катализатором. Если появляется агглютинация – объединение клеток, то выявляются гетерофильные антитела (производимые при заражении). Это подтверждает диагноз «мононуклеоз» у ребёнка и исключает другие заболевания. Если доктор после осмотра подозревает у ребёнка мононуклеоз, то без лабораторных анализов здесь не обойтись. Общий анализ крови и биохимию можно сдать в больнице, поликлинике. В первом случае биологический материал берётся из пальца, во втором – из вены. Результаты будут готовы уже на следующий день. Сдавать анализы важно не на полный желудок, а на пустой и предпочтительнее в утреннее время. За сутки до проведения исследования следует отказаться от жирных блюд. Кроме того, не рекомендуется заниматься тяжёлыми видами спорта. Что касается моноспот-теста, то для его проведения кровь также берётся из вены. Результаты будут готовы через 5 минут. Сдать тест можно бесплатно в больнице (если она оснащена нужным лабораторным оборудованием) либо обратиться в платную клинику. Проходить исследование крови нужно будет несколько раз. Это обусловлено тем, что на первичной стадии развития болезни отмечается незначительное изменение показателей в сыворотке крови. Поэтому может понадобиться вторичное (либо ещё одно) исследование для точного диагностирования заражения. При длительно текущем мононуклеозе педиатр назначит проведение анализа 1 раз в 3 месяца. В общем анализе крови будут наблюдаться такие изменения:
Расшифровка анализа крови при мононуклеозе у детей (биохимия):
Вот перечень анализов, которые могут выявить мононуклеоз у ребёнка:
Врачи иногда рекомендуют сдать мазки. Берётся биологический материал со слизистых тканей миндалин ребёнка. Этому есть объяснение. Поскольку заболевание очень схоже с дифтерией (симптоматикой), то необходимость в исследовании очевидна. Диагностирование у детей мононуклеоза — очень важное мероприятие. Выявить патологию можно при помощи множества исследований. Самыми результативными в данном случае являются показатели крови – общий и биохимический лабораторные анализы. источник |